SKRIPSI
MEMPELAJARI TEKNOLOGI PENGOLAHAN MANISAN SEMI BASAH BUAH TROPIS
Oleh :
MUHAMMAD LUTFI F24104121
2010
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
Judul Skripsi : Mempelajari Teknologi Pengolahan Manisan Semi Basah Buah Tropis
Nama : Muhammad Lutfi
NIM : F24104121
Menyetujui :
Dosen Pembimbing Akademik,
Dr.Ir. Slamet Budijanto, M.Agr
(NIP : 19610502.198603.001)
Mengetahui :
Ketua Departemen ITP,
Dr. Ir. Dahrul Syah, MSc
(NIP : 19650814.199002.001)
Muhammad Lutfi F24104121. Mempelajari Teknologi Pengolahan Manisan Semi Basah Buah Tropis. Dibawah bimbingan Slamet Budijanto (2010).
RINGKASAN
Kerusakan bahan pangan terutama produk hortikultura seperti buah dan sayur di Indonesia terbilang tinggi. Kurang lebih 20 – 40 % buah-buahan mengalami kerusakan setelah panen. Hal ini menunjukkan bahwa diperlukan teknologi yang tepat dalam hal pemanenan dan penanganan pasca-panen agar kehilangan (loss) dapat ditekan serendah mungkin. Salah satu usaha pengawetan buah adalah dengan pengolahan menjadi produk yang memiliki kadar air rendah. Hal ini dapat dilakukan dengan aplikasi panas (pengeringan), penambahan gula, atau gabungan keduanya. Salah satu pengolahan buah yang banyak dilakukan adalah pembuatan manisan. Pada penelitian ini dicoba pembuatan manisan semi basah dari buah belimbing manis, nanas, dan pepaya. Tujuan pembuatan manisan semi basah adalah memformulasi teknologi proses pengolahan manisan semi basah yang dapat diaplikasikan pada industri kecil serta dapat mengurangi kehilangan (loss) buah-buahan pasca-panen.
Penelitian ini terdiri atas tiga tahap penelitian. Tahap pertama meliputi penentuan ketebalan potongan buah terbaik, penentuan konsentrasi dan waktu perendaman dalam larutan kapur, penentuan waktu blansir, dan penentuan kombinasi larutan gula. Seleksi penilaian pada tahap pertama dilakukan oleh 5 orang panelis terbatas. Tahap kedua adalah pengamatan terhadap pengaruh metode pengeringan. Perlakuan yang dilakukan dalam tahap ini adalah jenis, suhu, dan waktu pengeringan. Jenis pengeringan yang dilakukan adalah pengeringan kabinet dengan suhu 50 0C selama 4 jam (a1) dan 6 jam (a2); 60 0C selama 4 jam (b1) dan 6 jam (b2); dan penjemuran dibawah sinar matahari langsung selama 2 hari penjemuran (12 – 15 jam) (c). Seleksi pemilihan sampel paling optimal dilakukan dengan melakukan uji organoleptik oleh 30 orang panelis dengan parameter uji warna, aroma, tekstur, rasa, dan kerenyahan. Produk yang terpilih sebagai yang paling baik kemudian digunakan dalam tahap berikutnya. Tahap ketiga adalah penggunaan bahan dusting untuk menutupi sisa-sisa larutan gula. Perlakuan yang dilakukan adalah jenis bahan dusting yang digunakan. Bahan dusting yang digunakan dalam percobaan adalah campuran tepung gula dan tepung kanji (1 : 1) (A), glukosa kristal (B), dan dekstrin kristal (C). Seleksi pemilihan sampel paling optimal dilakukan dengan melakukan uji organoleptik oleh 30 orang panelis dengan parameter uji warna, aroma, tekstur, rasa, dan kerenyahan. Produk terpilih dari uji organoleptik ini kemudian diuji mutu kimia, fisik, dan mikrobiologinya.
potongan sejajar, perendaman larutan CaCl2 500 ppm 30 menit, blansir 85 0C 1 menit, perendaman larutan gula pasir 40 0brix 12 jam, larutan gula pasir 55 0brix 12 jam, larutan gula batu 70 0brix 12 jam, dan pengeringan suhu 60 0C selama 2 jam menggunakan pengering kabinet, dan bahan dusting glukosa kristal). Sedangkan formula produk manisan pepaya yang paling disukai adalah formulasi B (ukuran 3 cm x 0,5 cm, konsentrasi CaCl2 500 ppm 30 menit, blansir 85 0C 1 menit, perendaman larutan gula pasir 40 0brix 12 jam, larutan gula pasir 55 0brix 12 jam, larutan gula batu 70 0brix 12 jam, pengeringan kabinet suhu 60 0C selama 2 jam, dan bahan dusting glukosa kristal).
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 13 Oktober 1986.
Penulis merupakan anak kedua dari tiga bersaudara dari
pasangan Djeni Hendra dan Nurhayati Syarif. Pendidikan
yang pernah diikuti oleh penulis adalah TK Insan Kamil,
SDN Empang III Bogor, SLTPN 4 Bogor, dan SMAN 4
Bogor. Penulis kemudian melanjutkan pendidikan setelah
diterima di Insitut Pertanian Bogor pada program studi Ilmu dan Teknologi
Pangan melalui jalur SPMB pada tahun 2004.
Semasa kuliah penulis aktif mengikuti kegiatan-kegiatan kemahasiswaan
diantaranya sebagai anggota panitia BAUR 2006, anggota divisi Logistik dan
Transportasi NSPC 2006, dan Kepala Divisi Logistik dan Transportasi NSPC
2007. Penulis juga pernah mengikuti Praktik Lapang di PT. Ciptayasa Putra
KATA PENGANTAR
Segala puji bagi Allah SWT yang telah memberikan karunia-Nya sehingga
penulisan skripsi ini dapat terlaksana dengan baik dan lancar. Skripsi yang
berjudul “Teknologi Pembuatan Manisan Semi Basah Pepaya (Carica papaya),
Belimbing manis (Averrhoa carambola L.), dan Nanas (Ananas comosus (L)
merr)” ini merupakan laporan hasil penelitian yang penulis lakukan sebagai syarat
mendapatkan gelar sarjana di Instutut Pertanian Bogor.
Selama kegiatan penelitian maupun penulisan skripsi ini tentu tak lepas
dari bantuan berbagai pihak. Dalam kesempatan ini penulis mengucapkan terima
kasih sebesar-besarnya kepada :
1. Ibu dan Bapak tercinta, adik dan kakakku atas do’a dan dukungannya.
2. Bapak Dr. Ir. Slamet Budijanto, M.Agr. sebagai dosen pembimbing
akademik atas segala kesabaran, dukungan, arahan, dan bimbingannya.
3. Bapak Dr.Ir.Yadi Haryadi, MSc dan Ibu Dr. Ir. Dede R. Adawiah, M.Si
atas kesediaannya menjadi dosen penguji dan bimbingannya kepada
penulis.
4. Teman seperjuangan satu bimbingan, Yuliana.
5. Mbak Febri, Mbak Iin, Mang Ujang, dan Mang Zaenal. Terimakasih atas
pinjaman ruang dan alat-alat di Technopark.
6. Teman-teman TPG 39, 40, 41, dan 42 yang tidak bisa disebutkan satu
persatu.
7. Semua teknisi dan laboran. Pak Sobirin, Pak Koko, Pak Rojak, Teh Ida,
Bu Rubiyah. Terima kasih atas bantuannya.
8. Pak Aryo dan Pak Leman sebagai supplier pepaya IPB-9.
9. Semua pihak yang telah banyak membantu dalam pelaksanaan penelitian
Dalam penulisan skripsi ini tak lepas dari kekurangan dan kesalahan dan
penulis mohon maaf. Penulis berharap semoga Skripsi ini dapat berguna bagi
semua pihak yang memerlukannya.
Bogor, Juni 2010
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... iii
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... x
I. PENDAHULUAN A. LATAR BELAKANG ... 1
B. TUJUAN PENELITIAN ... 2
C. MANFAAT PENELITIAN ... 2
II. TINJAUAN PUSTAKA A. PEPAYA ... 3
B. BELIMBING MANIS ... 4
C. NANAS ... 6
D. TEKNOLOGI PENGOLAHAN MANISAN SEMI BASAH... 7
E. BAHAN TAMBAHAN PANGAN ... 8
1. Kalsium Klorida (CaCl2) ... 8
2. Asam Sitrat ... 9
3. Potasium Sorbat ... 9
F. GULA ... 11
G. GLUKOSA KRISTAL ... 12
H. DEKSTRIN ... 13
I. PENGERINGAN ... 14
1. Teori Pengeringan ... 14
2. Pengeringan Buah ... 15
3. Metode Pengeringan... 16
III. METODOLOGI PENELITIAN A. BAHAN DAN ALAT ... 20
Halaman
C. METODE PENELITIAN ... 23
1. Tahap Pertama ... 23
2. Tahap Kedua ... 25
3. Tahap Ketiga ... 25
4. Analisis Produk Terpilih ... 26
E. METODE ANALISIS ... 27
1. Kadar Air ... 27
2. Kadar Abu ... 27
3. Kadar Protein ... 27
4. Kadar Lemak ... 28
5. Kadar Karbohidrat ... 29
6. Rendemen ... 29
7. Uji Keasaman (pH) ... 29
8. Uji Kekerasan ... 29
9. Uji Aktifitas Air (aw) ... 29
10. Uji Mikrobiologi ... 30
11. Uji Organoleptik ... 31
IV. HASIL DAN PEMBAHASAN A. TAHAP PERTAMA ... 32
1. Penentuan Ukuran Pemotongan ... 32
2. Penentuan Konsentrasi dan Waktu Perendaman Larutan Kapur 33
3. Penentuan Suhu dan Waktu Blansir ... 34
4. Penentuan kombinasi larutan gula ... 35
B. TAHAP KEDUA ... 37
1. Nilai Warna ... 37
2. Nilai Aroma ... 39
3. Nilai Tekstur ... 40
4. Nilai Rasa ... 42
5. Nilai Kerenyahan ... 43
C. TAHAP KETIGA ... 45
Halaman
2. Nilai Aroma ... 48
3. Nilai Tekstur ... 50
4. Nilai Rasa ... 51
5. Nilai Kerenyahan ... 53
D. ANALISIS PRODUK TERPILIH ... 55
1. Mutu Kimia Manisan Semi Basah ... 55
2. Mutu Fisik Manisan Semi Basah ... 60
3. Mutu Mikrobiologi Manisan Semi Basah ... 63
E. VERIFIKASI PROSES PEMBUATAN MANISAN SEMI BASAH ... 66
1. Pembuatan larutan kapur CaCl2 0,5 % ... 66
2. Pembuatan larutan gula pasir 40 0brix ... 66
3. Pembuatan larutan gula pasir 55 0brix ... 66
4. Pembuatan larutan gula batu 70 0brix ... 67
5. Pembuatan larutan gula batu 70 0brix ... 67
6. Pembuatan manisan semi basah buah nanas ... 69
7. Pembuatan manisan semi basah buah pepaya ... 70
V. KESIMPULAN DAN SARAN A. KESIMPULAN ... 73
B. SARAN ... 74
DAFTAR PUSTAKA ... 75
DAFTAR TABEL
Halaman
Tabel 1. Komposisi kimia pepaya per 100 g ... 4
Tabel 2. Komposisi kimia belimbing manis per 100 g ... 5
Tabel 3. Batas penggunaan potasium sorbat di Indonesia ... 11
Tabel 4. Data uji organoleptik terbatas penentuan ketebalan
potongan ... 32
Tabel 5. Data uji organoleptik terbatas penentuan konsentrasi
dan lama perendaman dalam larutan kapur ... 34
Tabel 6. Data uji organoleptik terbatas penentuan suhu dan
waktu blansir ... 35
Tabel 7. Data uji organoleptik terbatas kombinasi larutan gula ... 36
Tabel 8. Data produk terpilih dari penelitian tahap pertama ... 36
Tabel 9. Komposisi kimia formula manisan semi basah hasil
analisis proksimat (% bb) ... 56
Tabel 10. Aktivitas air (aw) minimum pertumbuhan mikroba pada
bahan pangan ... 62
Tabel 11. Hasil perhitungan koloni manisan semi basah dengan
metode TPC ... 63
DAFTAR GAMBAR
Halaman
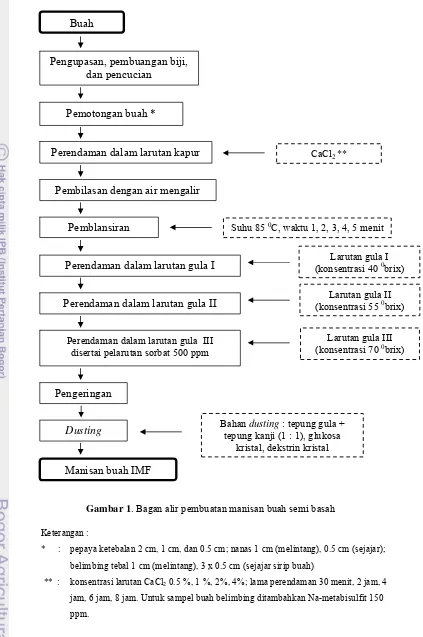
Gambar 1. Bagan alir pembuatan manisan buah semi basah ... 22
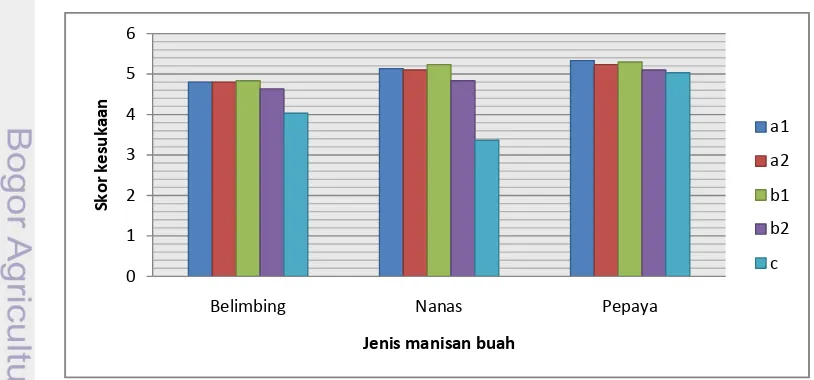
Gambar 2. Histogram pengaruh formulasi pengeringan terhadap skor
rata-rata kesukaan warna manisan ... 38
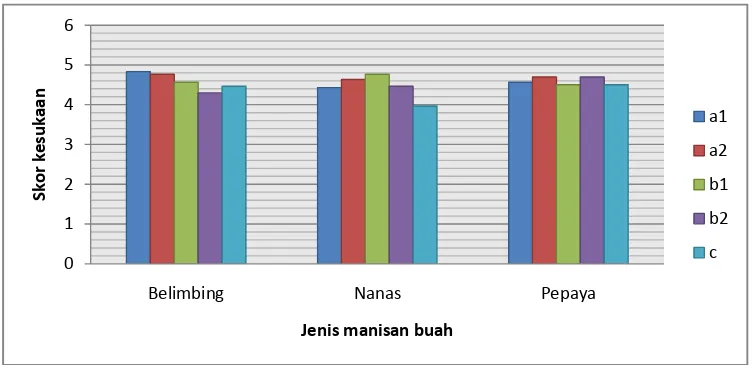
Gambar 3. Histogram pengaruh formulasi pengeringan terhadap skor
rata-rata kesukaan aroma manisan ... 40
Gambar 4. Histogram pengaruh formulasi pengeringan terhadap skor
rata-rata kesukaan tekstur manisan ... 43
Gambar 5. Histogram pengaruh formulasi pengeringan terhadap skor
rata-rata kesukaan rasa manisan ... 43
Gambar 6. Histogram pengaruh formulasi pengeringan terhadap skor
rata-rata kesukaan kerenyahan manisan ... 44
Gambar 7. Histogram pengaruh formulasi dusting terhadap skor
rata-rata kesukaan warna manisan ... 48
Gambar 8. Histogram pengaruh formulasi dusting terhadap skor
rata-rata kesukaan aroma manisan ... 49
Gambar 9. Histogram pengaruh formulasi dusting terhadap skor
rata-rata kesukaan tekstur manisan ... 51
Gambar 10. Histogram pengaruh formulasi dusting terhadap skor
rata-rata kesukaan rasa manisan ... 53
Gambar 11. Histogram pengaruh formulasi dusting terhadap skor
rata-rata kesukaan kerenyahan manisan ... 54
Gambar 12. Bagan alir pembuatan manisan buah belimbing semi
basah ... 68
Gambar 13. Bagan alir pembuatan manisan buah nanas semi basah ... 70
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data jumlah produksi beberapa jenis buah di Indonesia ... 78
Lampiran 2. Form quisioner uji organoleptik ... 78
Lampiran 3. Sidik ragam uji hedonik warna belimbing manis tahap
kedua ... 79
Lampiran 4. Sidik ragam uji hedonik warna nanas tahap kedua ... 79
Lampiran 5. Sidik ragam uji hedonik warna pepaya tahap kedua ... 80
Lampiran 6. Sidik ragam uji hedonik aroma belimbing manis tahap
kedua ... 81
Lampiran 7. Sidik ragam uji hedonik aroma nanas tahap kedua ... 81
Lampiran 8. Sidik ragam uji hedonik aroma pepaya tahap kedua ... 82
Lampiran 9. Sidik ragam uji hedonik tekstur belimbing manis tahap
kedua ... 83
Lampiran 10. Sidik ragam uji hedonik tekstur nanas tahap kedua ... 83
Lampiran 11. Sidik ragam uji hedonik tekstur pepaya tahap kedua ... 84
Lampiran 12. Sidik ragam uji hedonik rasa belimbing manis tahap kedua .. 85
Lampiran 13. Sidik ragam uji hedonik rasa nanas tahap kedua ... 85
Lampiran 14. Sidik ragam uji hedonik rasa pepaya tahap kedua ... 86
Lampiran 15. Sidik ragam uji hedonik kerenyahan belimbing manis tahap
kedua ... 87
Lampiran 16. Sidik ragam uji hedonik kerenyahan nanas tahap kedua ... 87
Lampiran 17. Sidik ragam uji hedonik kerenyahan pepaya tahap kedua ... 88
Lampiran 18. Sidik ragam uji hedonik warna belimbing manis tahap
ketiga ... 89
Lampiran 19. Sidik ragam uji hedonik warna nanas tahap ketiga ... 89
Lampiran 20. Sidik ragam uji hedonik warna pepaya tahap ketiga ... 90
Lampiran 21. Sidik ragam uji hedonik aroma belimbing manis tahap
ketiga ... 91
Lampiran 22. Sidik ragam uji hedonik aroma nanas tahap ketiga ... 91
Halaman
Lampiran 24. Sidik ragam uji hedonik tekstur belimbing manis tahap
ketiga ... 92
Lampiran 25. Sidik ragam uji hedonik tekstur nanas tahap ketiga ... 93
Lampiran 26. Sidik ragam uji hedonik tekstur pepaya tahap ketiga ... 94
Lampiran 27. Sidik ragam uji hedonik rasa belimbing manis tahap ketiga .. 94
Lampiran 28. Sidik ragam uji hedonik rasa nanas tahap ketiga ... 95
Lampiran 29. Sidik ragam uji hedonik rasa pepaya tahap ketiga ... 95
Lampiran 30. Sidik ragam uji hedonik kerenyahan belimbing manis
tahap ketiga ... 96
Lampiran 31. Sidik ragam uji hedonik kerenyahan nanas tahap ketiga ... 97
Lampiran 32. Sidik ragam uji hedonik kerenyahan pepaya tahap ketiga ... 97
Lampiran 33. Data hasil pengujian sampel manisan semi basah
I. PENDAHULUAN
A.LATAR BELAKANG
Komoditas hortikultura merupakan salah satu komoditas hasil
pertanian yang memiliki nilai ekonomi tinggi. Salah satu komoditas
hortikultura yang potensial adalah buah-buahan. Penanganan pra-panen
maupun pasca-panen menjadi hal penting dalam peningkatan produksi
buah-buahan. Kurang lebih 20 – 40 % buah-buahan mengalami kerusakan setelah
panen. Hal ini menunjukkan bahwa diperlukan teknologi yang tepat dalam hal
pemanenan dan penanganan pasca-panen agar kehilangan (loss) dapat ditekan
serendah mungkin.
Sifat mudah rusak pada buah-buahan disebabkan masih
berlangsungnya aktivitas pernapasan dan penguapan setelah panen. Proses
kerusakan semakin dipercepat dengan adanya perubahan fisik, kimia, dan
biokimia akibat aktivitas enzim dan mikroba (Harris, 1989).
Beberapa jenis buah-buahan yang potensial tetapi mudah rusak adalah
pepaya, belimbing, dan nanas. Ketiga buah tersebut sangat potensial untuk
dikembangkan karena sangat digemari dan juga bernilai ekonomi tinggi.
Selain itu, ketiganya juga memiliki rasa yang enak dan aroma yang khas.
Buah-buahan ini adalah salah satu komoditas ekspor non migas yang
potensial (Sosrodihardjo, 1988). Hal ini dapat dilihat dari data Biro Pusat
Statistik pada Lampiran 1.
Kesegaran dan keawetan komoditas buah-buahan dapat dipertahankan
melalui beberapa metode, diantaranya dengan pemberian lapisan lilin, metode
CAS (Control Atmosphere Storage), dan metode MAP (Modified Atmosphere
Packaging). Meskipun dapat memperpanjang umur simpan, metode-metode
ini tetap mengalami kendala dalam aplikasinya, termasuk investasi yang
terlalu mahal.
Produk manisan buah semi basah merupakan salah satu teknologi
alternatif yang dinilai dapat dikembangkan untuk mengatasi hal tersebut.
Pengeringan buah dapat dilakukan dengan alat pengering dan sinar matahari.
Metode pengeringan dan alat pengering yang digunakan berbeda-beda untuk
akan mengalami perubahan warna dan tekstur karena air yang terkandung
dalam buah akan berkurang. Berkurangnya kadar air buah inilah yang
menyebabkan produk akhir lebih tahan lama. Meskipun demikian, produk
akhir yang dihasilkan juga harus mempunyai warna, tekstur, dan penampilan
yang baik atau mendekati penampakan awalnya, serta tidak terkontaminasi
oleh kapang selama masa penyimpanan.
B. TUJUAN PENELITIAN
Penelitian ini bertujuan memformulasi teknologi proses pengolahan
manisan semi basah yang dapat diaplikasikan pada industri kecil serta dapat
mengurangi kehilangan (loss) buah pepaya, belimbing, dan nanas
pasca-panen.
C. MANFAAT PENELITIAN
Tersedianya teknologi pengolahan manisan buah semi basah yang
II. TINJAUAN PUSTAKA A. PEPAYA
Pepaya (Carica papaya) adalah tanaman yang digolongkan ke dalam
Caricaceae. Tanaman pepaya bukan merupakan tanaman asli Indonesia
melainkan berasal dari Amerika Utara dan Amerika Selatan (Arriola et al.
1980). Berbagai sebutan pepaya di Indonesia dikenal seperti Gedang (Sunda,
Bali), Kates (Jawa, Madura, Sasak, Palembang), Kabula (Enggota), Pente
(Aceh), Betik (Karo), dan lain-lain (Rismunandar, 1980).
Pepaya mempunyai daerah penyebaran sangat luas yang meliputi
daerah tropik dan subtropik di seluruh dunia (Arriola et al. 1980). Tanaman
pepaya dapat tumbuh dengan baik di dataran rendah hingga daerah dengan
ketinggian 1000 m di atas permukaan laut. Semakin tinggi tempat tumbuh
pohon pepaya, semakin berkurang rasa manis buahnya. Di Indonesia tanaman
pepaya dapat tumbuh dengan baik di dataran rendah sampai daerah dengan
ketinggian 700 m di atas permukaan laut.
Kulit pepaya bertekstur halus, tipis, dan mudah rusak. Warna pepaya
berkisar antara oranye sampai merah bila matang. Secara tradisional, warna
pepaya digunakan sebagai parameter kematangan buah. Tingkat kematangan
buah pepaya ditunjukkan dengan munculnya warna kuning sampai oranye
pada kulit pepaya.
Pepaya merupakan buah segar dengan kandungan vitamin C tinggi.
Selain itu, buah pepaya juga mengandung vitamin A dan vitamin B kompleks
(Arriola et al. 1980). Buah pepaya matang memiliki nilai gizi lebih tinggi
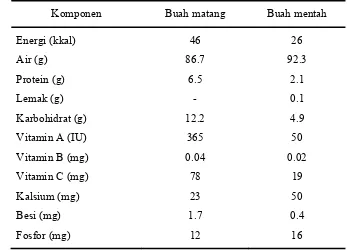
dibandingkan dengan buah pepaya mentah. Hal ini dapat dilihat pada Tabel 1.
Selama proses pematangan, kandungan vitamin C buah pepaya
semakin meningkat. Hal ini merupakan pengecualian dari kebanyakan buah,
karena buah-buahan lain mengalami penurunan kadar vitamin C selama
pematangan. Selama pematangan, terjadi pula peningkatan persentase karoten
Tabel 1. Komposisi kimia pepaya per 100 g
Komponen Buah matang Buah mentah
Energi (kkal) 46 26
Air (g) 86.7 92.3
Protein (g) 6.5 2.1
Lemak (g) - 0.1
Karbohidrat (g) 12.2 4.9
Vitamin A (IU) 365 50
Vitamin B (mg) 0.04 0.02
Vitamin C (mg) 78 19
Kalsium (mg) 23 50
Besi (mg) 1.7 0.4
Fosfor (mg) 12 16
Sumber : Arriola et al. (1980)
Metabolisme dari polisakarida dalam dinding sel menyebabkan kadar
gula buah pepaya meningkat. Total gula yang terkandung dalam 100
grambuah pepaya matang adalah 9 gr. Total gula tersebut dinyatakan sebagai
glukosa (Arriola et al., 1980).
B. BELIMBING MANIS
Tanaman belimbing merupakan tanaman asli Indonesia dan Malaysia
yang menyebar ke Asia Tenggara. Tanaman ini terdiri dari dua jenis yaitu,
belimbing manis (Averrhoa carambola L.) dan belimbing wuluh (Averrhoa
bilimbi L.). meskipun dari keluarga yang sama, kedua jenis belimbing ini
tidak memiliki persamaan baik dari penampakan maupun rasa buahnya.
Belimbing manis memiliki bentuk yang unik dan menarik. Bentuknya seperti
bintang jika dilihat penampang melintangnya dengan ukuran hingga sebesar
gelas. Rasa manisnya bervariasi sesuai dengan jenis atau varietasnya. Semasa
muda buah berwarna hijau muda, dan berubah kuning sampai kemerahan
Buah belimbing manis mempunyai kandungan vitamin dan air yang
tinggi. Belimbing manis bermanfaat sebagai obat, antara lain untuk
menyembuhkan sariawan, batuk rejan, sakit perut, demam dan menurunkan
tekanan darah tinggi. Selain teksturnya yang berserat halus menjadikan
belimbing berkhasiat untuk melancarkan pencernaan. Kandungan zat gizi
buah belimbing dapat dilihat pada Tabel 2.
Tabel 2. Komposisi kimia belimbing manis per 100 g
Komponen Jumlah
Energi (kkal) 36
Air (g) 90
Protein (g) 0.4
Lemak (g) 0.4
Karbohidrat (g) 8.8
Vitamin A (IU) 170
Vitamin B1 (mg) 0.03
Vitamin C (mg) 35
Kalsium (mg) 4
Besi (mg) 1.1
Fosfor (mg) 12
Sumber : Direktorat Gizi Depkes RI (1990).
Ada 13 jenis belimbing unggul di Indonesia. Jenis belimbing unggul
biasanya dicirikan dengan produksi buah per pohon tinggi, ukuran buahnya
besar dengan warna menarik, mengandung banyak air, berserat halus, rasa
buahnya manis dan menyegarkan. Selain itu, tahan terhadap hama penyakit.
Varietas belimbing unggul tersebut antara lain belimbing Demak, Sembiring,
Bangkok, Paris, Dewi, Siwalan, Wulan dan Wijaya.
Kualitas atau mutu buah belimbing ditentukan oleh waktu dan cara
pemetikannya. Pemetikan yang dilakukan pada saat yang tepat akan
menghasilkan buah yang enak dan warna buahnya juga lebih menarik.
menurunkan kualitas buah, dengan rasa yang asam dan sepat, warnanya tidak
menarik, dan jika dibiarkan masak dalam penyimpanan akan menyebabkan
buah keriput dan pucat.
Ciri buah yang siap panen adalah ukurannya besar (maksimal), telah
matang dan warnanya berubah dari hijau menjadi kuning atau merah,
tergantung pada varietasnya. Selain itu ciri buah belimbing siap panen dapat
dilihat dari kulitnya yang mengkilap dan daging pada siripnya (belimbingan)
sudah tampak penuh.
C. NANAS
Menurut Mulyohardjo (1984), tanaman nanas sudah lama dikenal di
Indonesia, namun bukan merupakan tanaman asli Indonesia. Tanaman ini
berasal dari Amerika Selatan dan Hindia Barat. Tanaman nanas merupakan
tanaman berbentuk semak yang mempunyai batang semu dengan tinggi 30 –
50 cm, berdaun tepi panjang dengan tepi berduri atau runcing. Buah nanas
sesungguhnya merupakan buah majemuk. Buah yang tampak merupakan
gabungan buah-buah kecil yang berjumlah 100 – 200 buah yang ditutupi
daun-daun buah kecil. Buah-buah kecil tersebut dihubungkan dengan hati
buah yaitu kelanjutan dari tangkai buah yang berserat. Buah nanas yang biasa
ditanam hanyalah dua jenis, yaitu nanas yang mempunyai mata menonjol dan
rata.
Varietas Ananas comosus yang penting :
1. Spanish (berdaging putih). Jenis ini mempunyai daun yang panjang kecil,
berduri halus sampai kasar, buah bulat bermata pipih dan besar. Jenis ini
cocok untuk dikalengkan atau dikonumsi segar. Contoh : Red spanish,
Sugar loaf, Singapore spanish, Ananas vermelo, dan monte livio.
2. Queen (berdaging kuning). Jenis ini mempunyai daun yang pendek dan
berduri tajam membengkok kebelakang, buah berbentk krucut, mata buah
menonjol, beraroma menarik, dan rasanya manis. Buah nanas Palembang
3. Cayenne. Jenis ini memiliki buah yang berbentuk silindris dengan berat
2.3 – 3.6 kg, penampilan bagus dan bermata datar. Nanas ini baik untuk
dikalengkan atau diawetkan.
D. TEKNOLOGI PENGOLAHAN MANISAN SEMI BASAH
Pembuatan manisan dilakukan melalui beberapa tahap yaitu
pencucian, pemotongan, perendaman dalam larutan garam, perendaman
dalam larutan kapur (CaCl2), blansir, perendaman dalam larutan gula disertai
penambahan potasium sorbat dan asam askorbat, penirisan, dan pengeringan.
Pangan semi basah atau intermediate moisture food (IMF) merupakan
bahan pangan yang mempunyai kadar air antara 10 – 40 % dan aktifitas air
(aw) antara 0.65 – 0.90 (Karel, 1976). Purnomo mendeskripsikan pangan semi
basah sebagai bahan pangan yang memiliki kadar air sekitar 15 – 40 % dan
memiliki aktifitas air antara 0.65 – 0.90. Pada tingkat aw tersebut,
pertumbuhan bakteri dan khamir menjadi tertekan. Pangan semi basah
termasuk pangan yang stabil terhadap pertumbuhan mikroba, tahan disimpan
tanpa memerlukan proses pengawetan yang lain seperti pendinginan,
sterilisasi ataupun pengeringan.
Pangan semi basah merupakan makanan dengan kadar air yang lebih
tinggi dibandingkan dengan makanan kering dan dapat dimakan tanpa
rehidrasi (Taoukis et. Al. 1999). Pangan semi basah mempunyai prinsip
pengolahan dengan menurunkan aw sampai tingkat dimana mikroba patogen
dan pembusuk tidak dapat tumbuh, tetapi kandungan airnya masih cukup
tinggi sehingga dapat dimakan tanpa rehidrasi terlebih dahulu dan cukup
kering hingga stabil dalam penyimpanan (Leisner dan Rodel, 1976).
Karel (1976) menyatakan bahwa cara pengolahan IMF dibedakan atas
tiga cara yaitu cara pencelupan basah, cara pencelupan kering dan cara
pencampuran. Pencampuran secara basah (moist infution) dimana
potongan-potongan bahan dicampur menjadi satu dan dimasukkan dalam larutan
tertentu sehingga menghasilkan produk pada tingkat aw yang diinginkan.
Pencelupan kering (dry infution) dilakukan dengancara mendehidrasi bahan
bertekanan osmose tertentu. Pencampuran (blending), semua bahan dicampur
dan dimasak untuk mengatur kadar air sehingga menghasilkan makanan
dengan aw tertentu.
Berdsarkan klasifikasi teknologi produksi IMF modern tersebut
terdapat dua tipe dasar pengolahan IMF modern, yaitu adsorpsi dan desorpsi.
Pada tipe adsorpsi, bahan pangan dikeringkan sambil dikontrol proses
pembasahan kembali sampai keadaan yang diinginkan sedangkan tipe
desorpsi bahan pangan dimasukkan ke dalam larutan yang mempunyai
tekanan osmotik lebih tinggi, sampai diperoleh keseimbangan pada tingkat
aw yang diinginkan. Proses ini dapat dipercepat dengan menaikkan suhu
(Robson, 1976).
Menuruk Taoukis et. al. (1999), karakteristik produk IMF memiliki
beberapa keunggulan dibandingkan produk kering konvensional atau
makanan dengan kadar air tinggi. Proses pengolahan IMF lebih hemat energi
dibandingkan pengeringan, refrigerasi, pembekuan atau pengalengan.
Teknologi IMF juga menghasilkan produk dengan retensi nutrisi dan kualitas
yang lebih tinggi dibandingkan dengan proses lain seperti pengeringan dan
proses panas. Sifat IMF yang plastis dan mudah dikunyah tanpa ada sensasi
kering menjadikan produk IMF dapat secara langsung dikonsumsi tanpa
penyiapan dan lebih convenience. Sifat plastis yang terdapat pada IMF, juga
memudahkan pengemasan karena dapat dengan mudah dibentuk dengan
ukuran dan bentuk geometris yang diharapkan. Taub dan Singh (1998),
menyatakan bahwa pangan semi basah dapat dikonsumsi tanpa pemasakan
dan dapat dikemas dalam kemasan yang fleksibel.
E. BAHAN TAMBAHAN PANGAN
Bahan tambahan pangan yang dibutuhkan dalam pembuatan manisan
semi basah buah pepaya, nanas, dan belimbing adalah CaCl2, asam sitrat, dan
potasium sorbat.
1. Kalsium Klorida (CaCl2)
Kalsium klorida merupakan kristal putih yang memiliki berat
larut dalam air. Kalsium klorida digunakan dalam produk pangan sebagai
anticaking agent, antimicrobial agent, curing agent, firming agent,
flavour enhancer, humektan, sekuestran, stabilizer, pengental,
pembentuk tekstur, dan lain-lain.
Perendaman dalam air kapur (CaCl2) bertujuan memperkuat
jaringan permukaan buah. Pektin yang terdapat dari buah akan
berinteraksi dengan kalsium yang berasal dari kalsium klorida hingga
membentuk suatu kompleks, yaitu kalsium-pektat. Kompleks inilah yang
akan memperkuat tekstur produk.
2. Asam Sitrat
Asam sitrat (C6H8O7) dengan nama kimia asam β
-3-hidroksi,2-hidroksi-1,2,3-propana trikarboksilik merupakan asidulan yang paling
populer. Asam sitrat berbentuk kristal putih dan tidak berbau. Asam sitrat
memiliki solubilitas dan stabilitas yang baik (Reddish F.G., 1957).
Perendaman buah dalam larutan asam sitrat pada pembuatan
manisan semi basah dilakukan untuk menurunkan pH, memperbaiki
warna, memperbaiki tekstur, dan menambah citarasa. Dengan
menurunnya pH, aktivitas mikroorganisme dapat terhambat.
Asam sitrat berfungsi sebagai chelating agent yaitu dapat
mengikat logam-logam bivalen, seperti Mn, Mg, dan Fe yang sangat
dibutuhkan sebagai katalisator dalam reaksi-reaksi biologis. Oleh karena
itu reaksi-reaksi biologis dapat dihambat dengan penambahan asam sitrat
(Winarno dan Aman, 1981).
3. Potasium Sorbat
Asam sorbat, sodium, dan potasium sorbat efektif dalam
menghambat pertumbuhan kapang dan khamir dalam keju baked goods,
sari buah, buah-buahan, sayuran segar, minuman ringan, pikel,
sauerkraut, daging, dan produk-produk ikan (Rani, 1989). Asam sorbat
dengan rumus kimia C6H8O2 merupakan padatan putih, berbentuk kristal,
dan Busta, 1993). Kelarutan asam sorbat dalam air akan meningkat
dengan meningkatnya suhu (Frazier, 1979). Kelarutan asam sorbat dalam
air menurun dengan semakin tingginya konsentrasi NaCl, sukrosa, dan
glukosa. Potasium sorbat dengan rumus kimia C6H7O2K merupakan
bubuk putih, halus, dan sangat larut dalam air (139.2 g/100 ml) pada suhu
20 0C. Kelarutan dalam alkohol 2.0 g/100 ml pada suhu 20 0C (Sofos dan
Busta, 1993).
Asam sorbat dan garamnya aktif menghambat pertumbuhan
kapang dan khamir tetapi tidak efektif menghambat pertumbuhan bakteri.
Kisaran pH optimumnya lebih besar dari 6.5. Asam sorbat dan garamnya
meningkat aktivitasnya sebagai senyawa antimikroba dengan
menurunnya pH. Dalam keadaan tidak terdisosiasi, asam sorbat dan
garamnya memiliki keaktifan yang paling tinggi dalam menghambat
pertumbuhan mikroba. Asam sorbat 0.1 % pada pH 4.5 dapat
menghambat pertumbuhan fungi yang berfilamen dan khamir. Pada
konsentrasi yang sama pada pH 3.5 pertumbuhan bakteri asam laktat
dapat dihambat (Rani, 1989).
Sifat toksin asam sorbat dan garamnya sangat rendah, sekitar
sepertiga kali asam benzoat (Kirk dan Othmer, 1985). Asam sorbat dan
garamnya tidak mengakibatkan gangguan fisiologis dalam tubuh karena
asam sorbat akan mengalami metabolisme menjadi CO2 dan H2O.
Sebagai bahan pengawet, asam sorbat dan garamnya termasuk ke
dalam kelompok GRAS (Generally Recognized as Safe) (Frazier, 1979).
Di Indonesia pemakaian sorbat diatur dengan peraturan Menteri
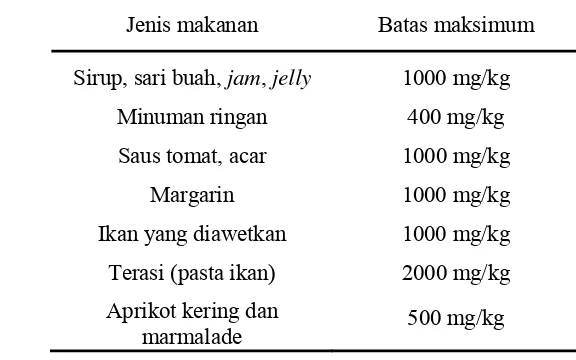
Kesehatan nomor 235/Men.Kes./Per/79. Batas penggunaan sorbat dapat
Tabel 3. Batas penggunaan potasium sorbat di Indonesia
Sumber : Rani (1989)
F. GULA
Gula merupakan senyawa kimia yang termasuk karbohidrat,
mempunyai rasa manis dan larut dalam air, serta mempunyai sifat aktif optis
yang dijadikan ciri khas untuk mengenal setiap gula (Goutara, 1985).
Beberapa macam gula antara lain glukosa, fruktosa, maltosa, sukrosa,
dan laktosa. Setiap gula mempunyai sifat fisik dan kimia yang berbeda-beda
misalnya dalam hal rasa manis, kelarutan dalam air, energi yang dihasilkan,
mudah tidaknya difermentasi oleh mikroba tertentu, daya pembentukan
karamel saat dipanaskan, dan pembentukan kristalnya (Winarno, 1988).
Gula yang digunakan pada penelitian ini adalah sukrosa. Sukrosa
merupakan senyawa oligosakarida dengan nama kimia
-D-glukopiranosida--D-fruktofuranosida. Rumus molekul sukrosa C12H22O11, memiliki berat
molekul 342.30 terdiri atas gugus glukosa dan fruktosa. Titik cair sukrosa
adalah 186C (Kirk dan Othmer, 1985).
Menurut Buckle et al. (1985), apabila gula ditambahkan ke dalam
bahan pangan dalam konsentrasi tinggi minimum 40 % padatan terlarut,
sebagian air yang ada menjadi tidak tersedia untuk pertumbuhan
mikroorganisme dan aktivitas air (aw) bahan pangan akan berkurang. Hal
yang perlu diperhatikan adalah konsentrasi larutan gula yang digunakan untuk
perendaman tidak boleh terlalu tinggi. Minifie dan Chem (1982) menyatakan
Jenis makanan Batas maksimum
Sirup, sari buah, jam, jelly 1000 mg/kg
Minuman ringan 400 mg/kg
Saus tomat, acar 1000 mg/kg
Margarin 1000 mg/kg
Ikan yang diawetkan 1000 mg/kg
Terasi (pasta ikan) 2000 mg/kg
Aprikot kering dan
bahwa jika buah direndam dalam larutan gula panas dengan konsentrasi yang
lebih tinggi dari 75 % akan menyebabkan air keluar dari dinding sel buah
lebih cepat dibandingkan dengan masuknya larutan gula ke dalam buah.
Dengan adanya perbedaan yang besar antara kecepatan keluarnya air dan
masuknya gula menyebabkan struktur sel dan tekstur buah menjadi keras dan
berkerut. Selain itu, proses dehidrasi akan sulit mencapai optimum karena
daerah dengan konsentrasi gula rendah akan terbentuk di sekitar potongan
buah.
Menurut Apriyantono (1985), konsentrasi gula yang dibutuhkan untuk
mencegah pertumbuhan mikroorganisme bervariasi bergantung dari jenis dan
kandungan zat yang terdapat pada bahan makanan, tetapi pada umumnya 70
% gula akan menghentikan pertumbuhan seluruh mikroorganisme dalam
makanan. Larutan gula dengan konsentrasi lebih rendah dari 70 % masih
efektif menghentikan kegiatan mikroorganisme tetapi hanya dalam jangka
waktu yang pendek, kecuali untuk makanan baru atau makanan yang bersifat
asam.
G. GLUKOSA KRISTAL
Glukosa kristal merupakan bahan pemanis berbentuk kristal yang
mengandung gula D-glukosa. Pemanis kristal yang mengandung D-glukosa
mengandung salah satu atau lebih dari tiga bentuk kristal D-glukosa, yaitu α
-D-glukopiranosa monohidrat, anhidrous α-D-glukopiranosa, dan β
-glukopiranosa. Sedangkan menurut Raymond dan Othner (1954), dekstrosa
(D-glukosa, gula jagung, gula pati, dan gula anggur), C6H12O6 BM = 180.16,
merupakan kristal gula putih dengan tingkat kemanisan 70 % sukrosa.
Dalam fasa larutan, dekstrosa terdapat bersama-sama dengan sejumlah
bentuk-bentuk isomer termasuk bentuk α dan β. Pada keadaan kristal, α
-dekstrosa dipisahkan dari larutan aqueous sebagai monohidrat dengan suhu
diatas 50 0C. Diatas 115 0C, β-dekstrosa dipisahkan dalam bentuk anhidrat.
Ketiga bentuk kristal tersebut dihasilkan secara komersial, dan α-monohidrat
Dekstrosa digunakan secara luas dalam industri permen dan roti, pada
pengalengan buah-buahan dan sayuran, minuman dan industri lain yang
memerlukan pemanis dan pewarna karamel (Raymond dan Othner, 1954).
Sedangkan menurut Balagopalan et al. (1988), dekstrosa banyak digunakan
dalam industri makanan sebagai pengembang, pembangkit cita rasa dan
aroma juga berperan dalam pembentukan lapisan warna. Dalam industri
farmasi, dekstrosa juga digunakan sebagai bahan pencampur dalam
pembuatan obat (tablet) dan campuran dalam cairan infus.
H. DEKSTRIN
Dekstrin adalah karbohidrat yang dibentuk selama hidrolisis pati
menajadi gula oleh panas, asam dan atau enzim. Dekstrin dan pati memiliki
rumus umum yang sama, - [Cx(H2O)y)]n - (y = x - 1), dimana unit glukosa
bersatu dengan yang lainnya membentuk rantai (polisakarida) tetapi dekstrin
memiliki ukuran lebih kecil dan kurang kompleks dibandingkan pati.
Dekstrin larut dalam air tetapi dapat diendapkan dengan alkohol. Dekstrin
memiliki sifat seperti pati. Beberapa dekstrin bereaksi dengan iodin
memberikan warna biru dan larut dalam alkohol 25 % (disebut
amilodekstrin), berwarna coklat-kemerahan dan larut dalam alkohol 55 %
(disebut eritrodekstrin) dan tidak membentuk warna dengan iodin serta larut
dalam alkohol 70 % (disebut akhrodekstrin), yang juga diidentifikasi sebagai
desktrosa ekuivalen (DE). DE yang tinggi menunjukkan adanya
depolimerisasi pati yang besar. Maltodekstrin adalah produk dengan DE
rendah.
Dekstrin larut dalam air dingin dalam berbagai derajat tergantung
pada kekuatan hidrolisisnya. Desktrin dapat digunakan untuk berbagai
keperluan. Dektrin dapat dibuat dari berbagai sumber pati seperti tapioka dan
kentang ataupun jagung. Sifat viskositas yang rendah dari dekstrin
menjadikan dekstrin sering dipakai dalam pembuatan jelli sebagai sumber
I. PENGERINGAN 1. Teori Pengeringan
Pengeringan adalah proses pindah panas dan kandungan air secara
simultan. Udara panas yang dibawa oleh media pengering akan
digunakan untuk menguapkan air yang terdapat di dalam bahan. Uap air
yang berasal dari bahan akan dilepaskan dari permukaan bahan ke udara
kering (Pramono, 1993). Dasar proses pengeringan adalah terjadinya
penguapan air ke udara karena perbedaan kandungan uap air antara udara
dengan bahan yang dikeringkan. Tujuan pengeringan adalah mengurangi
kadar air bahan sampai batas dimana perkembangan mikroorganisme
penyebab pembusukan, dan kegiatan enzim didalam bahan pangan
menjadi terhambat atau terhenti sehingga bahan memiliki masa simpan
yang lebih lama (Taib et al. 1988).
Jumlah kandungan air pada bahan akan mempengaruhi daya tahan
bahan tersebut terhadap serangan mikroba, dan biasanya dinyatakan
sebagai water activity (aw). Water activity adalah jumlah air bebas bahan
yang dapat digunakan oleh mikroorganisme untuk pertumbuhannya.
Besarnya nilai aw bahan harus diatur karena mikroba hanya dapat tumbuh
pada kisaran nilai aw tertentu. Bahan yang mempunyai nilai aw di bawah
0.7 biasanya sudah dianggap cukup baik dan tahan dalam penyimpanan.
Berdasarkan proses penguapan air, terdapat tiga macam proses
pengeringan. Pertama, panas diberikan karena kontak langsung dengan
udara panas pada tekanan atmosfer dan uap air. Kedua, vacuum drying,
evaporasi air berlangsung lebih cepat pada tekanan rendah dan panas
diberikan oleh dinding logam secara konduksi dan radiasi. Ketiga, freeze
drying, air diuapkan dari bahan yang membeku dan panas diberikan
secara radiasi dan konduksi.
Air yang diuapkan terdiri dari air bebas dan air terikat. Air bebas
adalah air pada permukaan bahan, sedangkan air terikat adalah air dalam
bahan dan biasanya sulit keluar dibandingkan dengan air bebas. Bila air
permukaan semua diuapkan, terjadi migrasi air dan uap air dari bagian
Pengeringan produk atau hasil pertanian dipengaruhi oleh
beberapa faktor, yaitu suhu, kelembaban udara, dan kecepatan aliran
udara. Ukuran bahan juga mempengaruhi cepat lambatnya pengeringan.
Selain itu jenis alat pengering juga mempengaruhi proses pengeringan.
Menurut Taib et al. (1988), semakin besar perbedaan suhu antara
media pemanas (suhu udara pengering) dengan bahan yang dikeringkan,
semakin cepat pula perpindahan panas ke dalam bahan sehingga
penguapan air dari bahan yang dikeringkan akan lebih banyak dan cepat.
Suhu pengeringan bervariasi untuk setiap bahan yang dikeringkan.
Kelembaban udara (RH) juga mempengaruhi proses pengeringan.
Kelembaban udara berbanding lurus dengan waktu pengeringan.
Semakin tinggi kelembaban udara, proses pengeringan (waktu
pengeringan) akan berlangsung lebih lama. Apabila bahan pangan
dikeringkan dengan menggunakan udara sebagai medium pengering,
maka semakin panas udara tersebut semakin cepat pengeringannya.
Berbeda dengan RH, kecepatan aliran udara berbanding terbalik dengan
waktu pengeringan. Semakin tinggi kecepatan aliran udara, proses
pengeringan akan berjalan lebih cepat.
Pemotongan bahan yang akan dikeringkan akan menjadikan
proses pengeringan berjalan lebih cepat. Hal ini dikarenakan pemotongan
atau pengirisan akan memperluas permukaan bahan sehingga akan lebih
banyak permukaan bahan yang berhubungan dengan udara panas dan
mengurangi jarak gerak panas untuk sampai ke bahan yang akan
dikeringkan.
2. Pengeringan Buah
Teknologi pengeringan bahan pertanian sebenarnya sederhana,
yaitu hanya memberikan tambahan energi dalam bentuk panas ke produk
untuk menurunkan kandungan airnya. Sumber panas dapat diperoleh
secara alami dari panas sinar matahari atau dari sumber panas buatan
pengeringan bahan-bahan pertanian, udara pengering disirkulasikan
secara kontinyu melewati bahan yang dikeringkan (Nuraeni, 2004).
Pada pengeringan buah-buahan sering terjadi perubahan tekstur
yang disebut shrinkage dan case hardening. Shrinkage terjadi akibat
adanya perpindahan massa uap air secara drastis selama pengeringan.
Perpindahan ini menimbulkan tekanan yang kuat pada dinding sel yang
akan menimbulkan kerusakan pada membran sel sehingga kehilangan
permeabilitasnya.
Case hardening adalah suatu keadaan pada bahan yang bagian
permukaannya sangat kering sedangkan pada bagian dalam masih basah.
Kondisi ini terjadi apabila penguapan air pada permukaan bahan jauh
lebih cepat daripada difusi air dari bagian dalam bahan ke luar
permukaan. Lapisan permukaan bahan menjadi keras dan kenyal
sehingga uap air tidak dapat menembusnya walaupun pengeringan
dilanjutkan.
Case hardening umumnya terjadi pada buah-buahan yang banyak
mengandung gula terlarut. Selama pengeringan, air beserta gula-gula
terlarut bergerak dari dalam potongan buah ke permukaan. Air akan
segera menguap sedangkan gula beserta padatan lainnya akan tetap
tertinggal di permukaan, lalu mengering dan mengeras sehingga air
dalam sel atau potongan bahan tidak dapat keluar atau menguap.
Terjadinya case hardening dan shrinkage dapat dicegah dengan cara
menurunkan suhu pada permukaan bahan selama pengeringan (Potter,
1980).
3. Metode Pengeringan
Berdasarkan sumber panas yang digunakan dikenal 2 jenis
metode pengeringan yaitu pengeringan alami dengan sinar matahari dan
pengeringan buatan.
a. Pengeringan alami (penjemuran)
Penjemuran memanfaatkan energi matahari untuk
pengeringan yang termurah tetapi resiko kerusakan akibat cuaca juga
tinggi dan relatif sukar menjaga kondisi pengeringan yang higienis.
Energi panas matahari dialirkan ke bumi dalam bentuk
radiasi surya. Radiasi surya memiliki ciri khas yaitu keberadaannya
yang selalu berubah-ubah. Meskipun hari cerah dan sinar surya
tersedia banyak, besarnya berubah sepanjang hari dengan titik
maksimumnya pada tengah hari. Sinar surya juga bergantung pada
keadaan atmosfer. Besarnya radiasi akan berkurang jika langit
berawan. Selain itu lokasi suatu tempat (perbedaan garis lintang,
ketinggian) dan musim juga berpengaruh terhadap besarnya radiasi
surya.
Pemanfaatan sinar matahari secara langsung merupakan cara
yang umum dan sudah dipakai secara luas sejak lama, misalnya pada
proses pengeringan hasil pertanian. Sebenarnya kondisi tersebut
akan menyebabkan komoditas menyerap uap air dari tanah selama
pengeringan berlangsung.
Panas yang dihasilkan matahari berasal dari proses fusi yang
mengubah 4 ton hidrogen menjadi helium tiap detiknya dan
mengeluarkan panas dengan laju 1024 kWh/detik. Jumlah panas yang
diproduksi matahari yang jatuh ke wilayah Indonesia tersebut
mencapai 9 x 1017 kJ/tahun atau setara dengan 28.35 x 108 MW
energi listrik.
Energi panas matahari dialirkan ke bumi dalam benruk
radiasi yang merupakan gelombang pendek. Ciri khas radiasi surya
adalah sifat keberadaaannya yang selalu berubah-ubah, sehingga
meskipun hari cerah dan sinar surya tersedia banyak, nilainya
sepanjang hari berubah dengan titik maksimum pada tengah hari
karena bertepatan dengan jarak lintasan terpendek sinar surya
menembus atmosfer.
b. Pengeringan buatan
Pada pengering buatan, kondisi saniter mudah dijaga, produk
bergantung pada keadaan cuaca. Akan tetapi, dibutuhkan biaya
bahan bakar dan biaya investasi alat yang lebih besar (Desrosier,
1988). Ada beberapa metode pengeringan buatan, diantaranya
pengeringan kabinet, fluidized bed drier, dan pengeringan vakum.
Menurut Taib et al. (1988), melihat banyaknya pilihan mesin
pengering yang dapat digunakan untuk berbagai jenis produk maka
pemilihan mesin pengering yang optimal didasari pada kapasitas
mesin pengering, sifat fisik bahan umpan basah, spesifikasi hasil
yang diinginkan, operasi pengolahan hulu dan hilir, kadar air bahan
umpan dan hasil pengeringan, kinetika pengeringan, parameter mutu,
aspek keamanan, nilai produk, kebutuhan akan kendali otomatis,
sifat keracunan produk, rasio pengembalian modal, jenis dan biaya
bahan bakar, serta peraturan lingkungan.
Suhu udara pengering yang terkontrol menjamin proses
pengeringan dilakukan secara benar dan energi yang digunakan
efisien, sehingga kualitas bahan kering terjamin. Suhu yang
terkontrol pada kisaran tertentu berpengaruh pada laju perpindahan
panas dari udara pengering ke bahan yang dikeringkan dan laju
penguapan air dari bahan ke udara pengering. Kedua hal ini
berpengaruh pada laju perubahan fisik bahan yang dikeringkan, yaitu
tekstur, warna, dan daya awet. Pengeringan bahan hasil pertanian
yang baik menggunakan aliran udara pengering dengan suhu
berkisar antara 45C sampai 75C. Bila pengeringan dilakukan pada
suhu di bawah 45C maka mikroba dan jamur yang merusak produk
masih hidup, sehingga daya awet produk rendah. Namun
pengeringan pada suhu udara pengering di atas 75C akan
menyebabkan struktur kimiawi dan fisik produk rusak, karena
perpindahan panas dan massa air yang cepat akan berdampak pada
perubahan struktur sel (Nuraeni, 2004).
Aliran udara pengering yang melewati bahan harus dikontrol
polanya, karena udara pengering berfungsi memindahkan panas ke
pengeringan Uap air dari bahan menyebabkan kelembaban udara
pengering meningkat. Hal ini menghambat laju pengeringan. Untuk
menghindari hal tersebut, udara pengering yang telah membawa uap
air harus segera dialirkan ke luar sistem pengeringan dan digantikan
II. METODOLOGI PENELITIAN A. BAHAN DAN ALAT
Bahan utama yang digunakan dalam proses pembuatan manisan semi
basah adalah pepaya, nanas, belimbing manis, garam, CaCl2, air, asam sitrat,
gula, natrium metabisulfat, asam askorbat, dan potasium sorbat.
Alat-alat yang digunakan dalam proses pembuatan manisan semi
basah adalah timbangan digital kasar, baskom, toples, sendok pengaduk,
sendok makan, kompor, panci ukuran besar, pisau, cabinet dryer, termometer,
refraktometer, pH meter, plastik ukuran 5 kg dan 1 kg, mangkok, piring,
sendok-sendok kecil, dan gelas takar ukuran 1000 dan 2000 ml.
Bahan-bahan yang digunakan dalam analisa produk adalah aquades,
K2SO4, HgO, H2SO4, H3BO3, larutan NaOH-Na2S2O3, HCl 0.1 N, NaOH
0.1N, kertas saring, indikator metil merah dan metil biru, heksan, dan etanol.
Alat-alat yang digunakan dalam analisa adalah pipet tetes, pipet
volumetrik 10, 5, dan 2 ml, gelas piala ukuran 100 dan 400 ml, cawan
alumunium, cawan porselen, cawan petri, gelas ukur 10 dan 100 ml,
desikator, alat destilasi, labu kjeldahl, erlenmeyer 100 ml dan 300 ml, neraca
analitik, silica gel, inkubator 30 C, penetrometer, dan tabung reaksi.
B. PEMBUATAN MANISAN SEMI BASAH
Pembuatan manisan semi basah terbagi menjadi beberapa tahap yaitu,
pengupasan kulit, pemotongan disertai perendaman dalam larutan garam,
perendaman dalam larutan kapur CaCl2, pembilasan, pemblansiran,
perendaman dalam larutan gula yang dilakukan sebanyak 3 tahap disertai
penambahan potasium sorbat pada perendaman yang terakhir, penirisan,
pengeringan, pendinginan, dan dusting.
Pembuatan manisan semi basah diawali dengan menyiapkan pepaya
dengan tingkat kemasakan 80 % (mengkal), nanas dengan tingkat kemanisan
80 % (mengkal), dan belimbing dengan tingkat kemanisan 80 % (mengkal).
Ketiga buah tersebut dikupas, dibuang bijinya / mata pada permukaan daging
nanas, dan direndam dalam larutan garam 1 %. Daging buah dipotong dengan
kapur. Selanjutnya potongan daging buah diblansir dengan air panas. Proses
blansir dilakukan untuk menghilangkan sisa-sisa CaCl2 yang tidak terserap
daging buah yang dapat menimbulkan rasa gatal di lidah.
Potongan daging buah direndam dalam larutan gula pertama selama
12 jam pada suhu awal 60 0C dan dibiarkan mendingin selama perendaman.
Perendaman gula kedua dilakukan dengan larutan gula dengan konsentrasi
yang lebih tinggi dari larutan pertama dengan lama perendaman 12 jam dan
suhu awal larutan 60 0C. Kemudian perendaman gula ketiga dilakukan
dengan larutan gula dengan konsentrasi yang lebih tinggi dari larutan kedua
dengan lama perendaman 12 jam dan suhu awal perendaman 60 0C.
Sebelumnya larutan gula terakhir dicampur dengan potasium sorbat 500 ppm.
Setelah itu dilakukan penirisan dan pengeringan menggunakan cabinet dryer.
Gambar 1. Bagan alir pembuatan manisan buah semi basah Keterangan :
* : pepaya ketebalan 2 cm, 1 cm, dan 0.5 cm; nanas 1 cm (melintang), 0.5 cm (sejajar);
belimbing tebal 1 cm (melintang), 3 x 0.5 cm (sejajar sirip buah)
** : konsentrasilarutan CaCl2 0.5 %, 1 %, 2%, 4%; lama perendaman 30 menit, 2 jam, 4
jam, 6 jam, 8 jam. Untuk sampel buah belimbing ditambahkan Na-metabisulfit 150
ppm.
C. METODE PENELITIAN
Buah
Pengupasan, pembuangan biji, dan pencucian
Pemotongan buah *
Perendaman dalam larutan kapur
Pembilasan dengan air mengalir
Pemblansiran
Manisan buah IMF Pengeringan
Perendaman dalam larutan gula III disertai pelarutan sorbat 500 ppm
Perendaman dalam larutan gula II Perendaman dalam larutan gula I
CaCl2 **
Larutan gula I (konsentrasi 40 0brix)
Larutan gula II (konsentrasi 55 0brix)
Larutan gula III (konsentrasi 70 0brix)
Dusting Bahan tepung kanji (1 : 1), glukosa dusting : tepung gula +
kristal, dekstrin kristal
1. Tahap Pertama
Tahap pertama penelitian ini adalah penentuan ukuran
pemotongan, penentuan konsentrasi dan waktu perendaman dalam
larutan kapur, penentuan suhu dan waktu blansir, dan penentuan
kombinasi jenis gula perendaman dalam larutan gula. Seleksi dilakukan
oleh panelis terbatas berjumlah 5 orang. Parameter yang diuji pada
penentuan ukuran pemotongan adalah penampakan dan tekstrur; pada
penentuan konsentrasi dan waktu larutan kapur adalah kerenyahan,
tekstur, dan penampakan; pada penentuan waktu blansir adalah
penampakan warna dan tekstur; dan pada penentuan kombinasi jenis gula
adalah rasa, tekstur, dan penampakan.
a. Penentuan ukuran pemotongan
Pemotongan dilakukan agar diperoleh manisan semi basah
dengan ketebalan yang dapat memberikan tekstur dengan kerutan
paling sedikit. Pemotongan buah dilakukan dengan menggunakan
pisau dapur dengan ketebalan sebagai berikut :
Buah Ketebalan (cm)
Pepaya 2
1
0.5
Nanas 1 (potongan melintang)
0.5 (potongan sejajar)
Belimbing 1 (potongan melintang)
0.5 (potongan sejajar pada sirip buah)
b. Penentuan konsentrasi dan waktu perendaman larutan kapur
Perendaman dalam larutan kapur dilakukan untuk
memperkuat jaringan buah sehingga dapat dihasilkan manisan semi
basah yang memiliki kerenyahan yang baik. Kapur yang digunakan
adalah CaCl2. Konsentrasi larutan kapur yang digunakan pada
percobaan ini adalah 0.5 %, 1 %, 2 %, dan 4 %, dengan lama
c. Penentuan waktu blansir
Proses blansir yang dilakukan pada potongan buah manisan
bertujuan untuk menghentikan kerja enzim-enzim penyebab
pencoklatan, menurunkan jumlah kontaminan mikroba, melemaskan
potongan buah, dan juga untuk menghilangkan sisa-sisa larutan
kapur yang tidak terserap oleh buah. Suhu yang digunakan adalah 85
0C dan waktu blansir yang dilakukan adalah 1, 2, 3, 4, dan 5 menit.
d. Penentuan kombinasi larutan gula
Perendaman potongan buah dalam larutan gula bertujuan
untuk mengeluarkan sebagian air dari dalam buah secara osmosis.
Proses dehidrasi ini berlangsung secara perlahan tergantung kepada
kandungan air buah dan konsentrasi larutan gula yang digunakan.
Proses ini dilakukan secara bertahap, yaitu perendaman dilakukan
sebanyak tiga kali dengan tiap larutan perendaman memiliki
konsentrasi gula yang berbeda.
Perendaman pertama menggunakan konsentrasi larutan gula
sebesar 40 0brix. Perendaman kedua menggunakan larutan gula
dengan konsentrasi gula yang lebih tinggi (55 0brix) dan perendaman
ketiga menggunakan konsentrasi yang lebih tinggi lagi (70 0brix).
Pada percobaan ini digunakan dua jenis gula yang digunakan pada
perendaman yang ketiga yaitu larutan gula pasir dan gula batu.
Kandungan gula pasir (sukrosa) akan berubah menjadi gula
invert (campuran glukosa dan fruktosa) apabila dipanaskan. Gula
invert memiliki sifat tidak mudah mengkristal dan tingkat kemanisan
lebih tinggi dibandingkan sukrosa. Sedangkan kandungan utama
gula batu adalah glukosa yang akan tetap berupa glukosa setelah
dipanaskan dan glukosa lebih mudah mengkristal dibandingkan gula
invert. Selain itu glukosa juga memiliki tingkat kemanisan dibawah
Perendaman ketiga dalam percobaan ini menentukan jenis
gula yang akan terdapat pada permukaan manisan buah, hal ini akan
menentukan karakteristik permukaan dan rasa manisan buah.
2. Tahap Kedua
Tahap kedua penelitian ini adalah mengamati pengaruh metode
pengeringan. Pengeringan manisan buah bertujuan untuk menghilangkan
sebagian besar air didalam potongan buah. Hilangnya air didalam
potongan buah akan membuat manisan buah menjadi lebih tahan
terhadap kontaminasi mikroba dan aktifitas enzim, sehingga akan
meningkatkan umur simpan produk.
Perlakuan pengeringan manisan buah semi basah dilakukan
dengan dua cara, yaitu pengeringan dengan tenaga matahari dan
pengeringan buatan menggunakan pengering kabinet. Pengeringan
dengan tenaga matahari dilakukan dengan penjemuran potongan buah
dibawah sinar matahari secara langsung selama 2 hari pengeringan (12 -
15 jam). Pengeringan potongan buah dengan menggunakan alat
pengering kabinet dilakukan dengan suhu 50 dan 60 0C dengan waktu 2
dan 4 jam.
Uji organoleptik tahap kedua yang meliputi uji kesukaan
(hedonik) terhadap 30 panelis untuk mengetahui tingkat penerimaan
panelis dan mengetahui kekurangan yang terdapat pada produk yang
berhubungan dengan sifat dan mutu sensori. Parameter yang diuji adalah
warna, aroma, tekstur, rasa, dan kerenyahan.
3. Tahap Ketiga
Tahap ketiga penelitian ini adalah aplikasi tepung dusting pada
manisan buah semi basah. Pembuatan manisan semi basah dilakukan
dengan proses pemanasan yang singkat dan suhu yang cukup rendah
dengan tujuan tetap menjaga sebagian kandungan air buah agar
dihasilkan produk yang memiliki tingkat kerenyahan, tekstur, dan rasa
proses pengeringan yang tidak terlalu lama menyebabkan banyaknya sisa
larutan gula di permukaan produk manisan semi basah. Hal ini
mendapatkan perhatian dari panelis dimana permukaan manisan terasa
lengket jika dipegang.
Perlakuan proses panas yang lebih lama atau dengan suhu yang
lebih tinggi dikhawatirkan akan merusak karakteristik produk yang sudah
cukup baik. Karena itu dilakukan perlakuan dusting pada permukaan
manisan buah. Pengaplikasian tepung dusting pada manisan buah akan
menutupi sisa-sisa larutan gula, sehingga manisan buah semi basah
menjadi tidak lengket saat dipegang.
Proses dusting dilakukan dengan menggunakan 3 jenis tepung,
yaitu campuran tepung gula dengan tepung kanji (1 : 1), glukosa kristal,
dan dekstrin kristal. Pemilihan bahan dusting berdasarkan pada rasa
(tingkat kemanisan) bahan tersebut.
Uji organoleptik tahap ketiga meliputi uji kesukaan (hedonik)
terhadap 30 panelis untuk mengetahui tingkat penerimaan panelis.
Parameter yang diuji adalah warna, aroma, tekstur, rasa, dan kerenyahan.
4. Analisis Produk Terpilih
Analisis dilakukan terhadap produk terpilih dari penelitian tahap
ketiga. Analisis yang dilakukan meliputi uji kimia (kadar air, abu,
protein, lemak, dan karbohidrat), uji fisik (rendemen, pH, kekerasan, dan
aw), dan uji mikrobiologi (TPC). Analisis produk bertujuan untuk
memberikan informasi nutrisi, karakteristik fisik produk, dan kandungan
mikroorganisme dalam manisan buah semi basah terpilih yang
D. METODE ANALISIS 1. Kadar Air (AOAC, 1995)
Cawan alumunium dikeringkan dalam oven selama 15 menit dan
didinginkan dalam desikator selama 10 menit dan ditimbang. Sampel
ditimbang kurang lebih sebanyak 2 gramdalam cawan. Cawan beserta isi
dikeringkan dalam oven 100 0C selama 6 jam. Cawan dipindahkan ke
dalam desikator lalu didinginkan dan ditimbang. Cawan beserta isinya
dikeringkan kembali sampai diperoleh berat konstan.
Perhitungan :
Kadar Air (% berat basah) = [W2 - (W3 – W1)] x 100%
W3 - W1
Berat cawan (gr) = W1
Berat sampel (gr) = W2
Berat cawan dan sampel setelah dikeringkan (gr) = W3
2. Kadar Abu (AOAC, 1995)
Cawan disiapkan untuk melakukan pengabuan, kemudian
dikeringkan dalam oven selama 15 menit. Lalu didinginkan dalam
desikator dan ditimbang. Sampel ditimbang sebanyak 3 gramdi dalam
cawan, kemudian dibakar dalam ruang asam sampai tidak mengeluarkan
asap lagi. Kemudian dilakukan pengabuan di dalam tanur listrik pada
suhu 400 – 600 0C selama 4 – 6 jam sampai terbentuk abu berwarna
putih atau memiliki berat yang tetap. Sampel beserta cawan didinginkan
dalam desikator kemudian ditimbang.
Perhitungan :
Kadar abu (%) = Berat abu (g) x 100% Berat sampel kering (g)
3. Kadar Protein Metode Mikro Kjeldahl (Apriyantono et al., 1989)
Sampel sebanyak 100 mg ditimbang dan dimasukkan ke dalam
dan 3.8 + 0.1 ml H2SO4. Batu didih ditambahkan pada labu lalu sampel
didihkan selama 1-1.5 jam sampai cairan menjadi jernih. Labu beserta
sampel didinginkan dengan air dingin. Isi labu dan air bekas
pembilasnya dipindahkan ke dalam alat destilasi. Labu erlenmeyer 125
ml diisi dengan 5 ml larutan H3BO4 dan ditambahkan dengan 4 tetes
indikator, kemudian diletakkan di bawah kondensor dengan ujung
kondensor terendam dalam larutan H3BO4. Larutan NaOH-Na2S2O3
sebanyak 8-10 ml ditambahkan ke dalam alat destilasi dan dilakukan
destilasi sampai didapat destilatnya sebanyak + 15 ml dalam erlenmeyer.
Destilat dalam erlenmeyer tersebut kemudian dititrasi dengan larutan
HCl 0.02 N hingga terjadi perubahan warna hijau menjadi biru.
Perhitungan jumlah nitrogen dilakukan setelah sebelumnya diperoleh
jumlah volume (ml) blanko.
Perhitungan :
Jumlah N (%) = (ml HCl – ml blanko) x NHCl x 14.007 x 100 mg sampel kering
Kadar Protein (%) = jumlah N x faktor konversi (6.25)
4. Kadar Lemak (AOAC, 1995)
Labu lemak disediakan sesuai dengan ukuran alat ekstraksi
soxhlet yang digunakan. Labu dikeringkan dalam oven dengan suhu 105
0
C – 110 0C kemudian didinginkan dalam desikator lalu ditimbang.
Sampel ditimbang sebanyak 5 gramdalam kertas saring dan kemudian
ditutup dengan kapas bebas lemak. Kertas saring beserta isinya
dimasukkan ke dalam ekstraksi soxhlet dan dipasang pada alat
kondensor. Pelarut heksan dituangkan ke dalam labu soxhlet secukupnya.
Refluks dilakukan selama 5 jam sampai pelarut kembali menjadi bening.
Pelarut yang tersisa dalam labu lemak didestilasi kemudian labu
dipanaskan dalam oven pada suhu 105 0C. Setelah dikeringkan sampai
berat tetap dan didinginkan dalam desikator, labu beserta lemak
Perhitungan :
Kadar lemak (%) = Berat lemak (g) x 100% Berat sampel kering (g)
5. Kadar Karbohidrat (By Difference)
Perhitungan :
Kadar Karbohidrat (%) = 100% - % (Protein + Kadar air + Abu +
Lemak)
6. Rendemen
Perhitungan :
Rendemen = Berat akhir produk X 100 %
Berat awal produk
7. Uji Keasaman (pH)
Pengukuran pH produk dilakukan dengan menggunakan alat
pH-meter. Sebelum pengukuran pH-meter dikalibrasi dengan buffer standar
pH 4. Sampel dilumatkan terlebih dulu, elektroda dibilas dengan akuades
kemudian dikeringkan dengan tissue. Batang elektroda dimasukkan
kedalam sampel selama beberapa saat sampai diperoleh pembacaan yang
stabil.
8. Uji Kekerasan
Uji kekerasan dilakukan dengan menggunakan Texture Analyzer.
Sebelum dilakukan uji, alat dikalibrasi. Bahan diuji dengan
menggunakan pisau uji sobek untuk menganalogikan pengujian
kekerasan sampel dengan menggunakan sobekan gigi. Semakin besar
waktu dan gaya yang dibutuhkan untuk menyobek bahan, semakin keras
bahan yang diuji.
9. Uji Aktifitas Air (Aw)
Pengujian Aw produk manisan semi basah dilakukan dengan alat
dimasukkan kedalam wadah uji. Wadah uji ditutup rapat dan alat
dibiarkan untuk mengukur Aw selama kurang lebih 20 menit. Hasil
pengukuran ditunjukkan pada layar display.
10. Uji Mikrobiologi Total Plate Count (Fardiaz, 1992)
Uji mikrobiologi manisan pada penelitian ini dilakukan melalui
uji TPC (Total Plate Count). Uji TPC dilakukan untuk mengetahui
jumlah mikroorganisme yang mungkin tumbuh pada manisan.
Kontaminasi biasanya berasal dari mikroorganisme di seluruh bagian
manisan. Oleh karena itu dalam uji mikrobiologi manisan, pengambilan
contoh dilakukan dengan menggunakan metode penghancuran.
Uji mikrobiologi manisan semi basah dimulai dengan menimbang
sampel sebanyak 10 gr, ditambahkan 90 ml larutan pengencer,
dimasukkan ke dalam plastik stomacher steril, dan distomacher selama 1
menit. Pengenceran dibuat hingga 10-3. Pengenceran yang dilakukan
tergantung mutu sampel yang dianalisis. Semakin rendah mutu sampel,
pengenceran yang diperlukan untuk dapat menghitung jumlah mikroba
semakin tinggi. Sebanyak 0.1 ml sampel yang telah diencerkan
dimasukkan ke dalam masing-masing 2 cawan petri (duplo) yang
selanjutnya dilakukan pemupukan. Pemupukan dilakukan pada
pengenceran 10-2 sampai 10-4. Setelah pemupukan dilakukan, media
dituangkan ke dalam cawan.
Media yang digunakan adalah PCA. PCA dengan pH 7
mengandung tripton, ekstrak khamir, dekstrosa, agar, dan air destilata.
PCA digunakan untuk identifikasi total mikroba, baik kapang, khamir,
maupun bakteri. Selanjutnya inkubasi dilakukan dengan posisi cawan
terbalik pada suhu 30 C selama 2 hari.
Perhitungan:
Pengenceran = pengenceran x pengenceran x jumlah yang awal. selanjutnya ditumbuhkan
11. Uji Organoleptik
Uji organoleptik yang dilakukan adalah uji hedonik. Uji
organoleptik pada peneltian tahap pertama adalah uji organoleptik
terbatas dengan panelis berjumlah 5 orang. Uji di tahap ini dilakukan
pada tiap percobaan dengan parameter uji yang berbeda. Penilaian
dilakukan dengan skala 1 – 5 berupa tanda (+) dimana 1 adalah nilai
untuk paling tidak suka dan 5 untuk sangat suka.
Uji organoleptik produk manisan dari tahap kedua dan ketiga
dilakukan di laboratorium sensori SEAFAST pada 30 orang panelis.
Parameter yang diuji meliputi uji kesukaan terhadap tekstur, kerenyahan
di mulut, aroma, rasa, dan warna. Penilaian dilakukan pada lembar
kuisioner dengan skala nilai 1 – 7 dimana 1 adalah nilai untuk paling
IV. HASIL DAN PEMBAHASAN A. TAHAP PERTAMA
Percobaan yang dilakukan adalah penentuan ukuran pemotongan
buah, penentuan waktu perendaman dan konsentrasi larutan kapur, penentuan
waktu dan suhu proses blansir, dan penentuan kombinasi gula perendaman
dalam larutan gula. Percobaan ini hanya melibatkan panelis terbatas.
Penilaian dilakukan dengan memberikan sejumlah tanda (+) sesuai dengan
tingkat kesukaan panelis terhadap produk tersebut dengan nilai terendah
adalah (+) dan tertinggi (+++++). Produk dengan penilaian terbaik akan
digunakan dalam penelitian tahap selanjutnya.
1. Penentuan ketebalan pemotongan
Ukuran ketebalan buah mempengaruhi lama waktu perendaman
gula dan tingkat penetrasi larutan gula ke dalam daging buah serta lama
pengeringan. Seleksi dilakukan untuk memilih produk dengan jumlah
[image:46.612.129.513.411.480.2]kerutan paling sedikit.
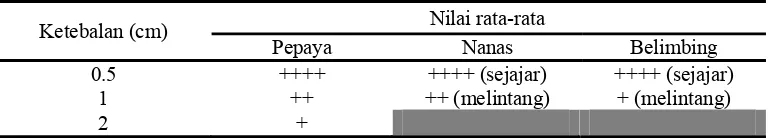
Tabel 4. Data uji organoleptik terbatas penentuan ketebalan potongan
Ketebalan (cm) Nilai rata-rata
Pepaya Nanas Belimbing
0.5 ++++ ++++ (sejajar) ++++ (sejajar)
1 ++ ++ (melintang) + (melintang)
2 +
Ukuran ketebalan yang diujikan pada pembuatan manisan buah
pepaya adalah ukuran 2 cm, 1 cm, dan 0.5 cm. Ukuran ketebalan yang
dipilih sebagai potongan paling baik untuk potongan buah pepaya adalah
0.5 cm. Produk yang dihasilkan memiliki kerutan yang sedikit. Ukuran
ketebalan yang dilakukan pada pembuatan manisan buah nanas adalah 1
cm (potongan melintang), dan 0.5 cm (potongan sejajar). Ukuran
ketebalan potongan buah nanas yang dipilih adalah 0.5 cm potongan
sejajar. Produk yang dihasilkan memiliki kerutan yang paling sedikit.
Ukuran potongan yang dilakukan pada pembuatan manisan buah
belimbing adalah tebal 1 cm (potongan melintang), dan 0.5 (potongan
cm potongan sejajar sirip-sirip buah, produk hasil yang didapat
mengalami kerutan paling sedikit. Data pengujian disajikan pada Tabel 4.
Pemotongan buah secara melintang akan menghasilkan produk
yang sangat sulit disobek (digigit) karena terdapat semacam serat yang
kuat di dalam buah belimbing. Serat tersebut terdapat pada buah dengan
posisi memanjang, sehingga pemotongan melintang akan menyebabkan
serat tersebut ikut terolah di dalam produk.
2. Penentuan konsentrasi dan lama perendaman dalam larutan kapur
Perendaman potongan buah dalam larutan kapur bertujuan untuk
memperkuat jaringan permukaan buah dan memperbaiki tekstur produk.
Kalsium dalam larutan kapur dapat berikatan dengan zat pektat pada
potongan buah membentuk senyawa kalsium-pektat yang kuat. Seleksi
dilakukan untuk memilih produk dengan kerenyahan, tekstur, dan
penampakan produk terbaik.
Perlakuan yang dilakukan pada percobaan ini adalah konsentrasi
larutan kapur yang digunakan dan waktu perendaman. Konsentrasi
larutan kapur adalah 0.5 %, 1 %, 2 %, dan 4 %, dengan lama perendaman
30 menit, 2 jam, 4 jam, 6 jam, dan 8 jam.
Penggunaan larutan kapur dengan konsentrasi yang rendah dan
lama proses perendaman yang singkat cocok diaplikasikan pada manisan
buah semi basah karena produk yang dihasilkan memiliki kerenyahan
yang baik. Proses perendaman kapur paling baik yang dipilih untuk buah
belimbing adalah konsentrasi 0.5 % dengan tambahan campuran
Na-metabisulfat 150 ppm selama 30 menit, penggunaan Na-Na-metabisulfat
pada buah belimbing bertujuan untuk mengurangi tingkat browning.
Konsentrasi dan lama perendaman dalam larutan kapur yang dipilih
untuk buah nanas adalah konsentrasi 0.5 % selama 30 menit, dan untuk
buah pepaya konsentrasi yang dipilih adalah 0.5% selama 30 menit. Data
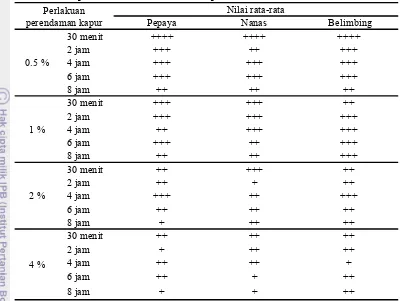
Tabel 5. Data uji organoleptik terbatas penentuan konsentrasi dan lama perendaman dalam larutan kapur
Perlakuan perendaman kapur
Nilai rata-rata
Pepaya Nanas Belimbing
0.5 %
30 menit ++++ ++++ ++++
2 jam +++ ++ +++
4 jam +++ +++ +++
6 jam +++ +++ +++
8 jam ++ ++ ++
1 %
30 menit +++ +++ ++
2 jam +++ +++ +++
4 jam ++ +++ +++
6 jam +++ ++ +++
8 jam ++ ++ +++
2 %
30 menit ++ +++ ++
2 jam ++ + ++
4 jam +++ ++ +++
6 jam ++ ++ ++
8 jam + ++ ++
4 %
30 menit ++ ++ ++
2 jam + ++ ++
4 jam ++ ++ +
6 jam ++ + ++
8 jam + + ++
3. Penentuan waktu blansir
Proses blansir dilakukan dengan tujuan untuk menginaktifkan
enzim-enzim yang masih berkerja setelah buah dipanen, menghilangkan
sebagian kontaminan mikroba, memperbaiki tekstur, dan juga untuk
menghilangkan sisa-sisa larutan kapur yang tidak terserap oleh potongan
buah. Seleksi dilakukan untuk memilih produk dengan warna dan tekstur
terbaik.
Suhu yang digunakan adalah 85 0C dan waktu blansir yang
dilakukan adalah 1, 2, 3, 4, dan 5 menit. Proses blansir yang dilakukan
pada potongan buah menyebabkan permukaan buah menjadi lebih
lembek. Proses pemblansiran yang dipilih sebagai proses paling baikl
untuk buah belimbing adalah suhu blansir 85 0C selama 2 menit.
Perlakuan suhu dan waktu blansir