PENGUJIAN TOTAL COLIFORM DAN FAECAL COLIFORM
PADA AIR BAKU PT TIRTA SUMUT DI LABORATORIUM
PDAM TIRTANADI
TUGAS AKHIR
OLEH:
DIKKY TRI PRATANA H
NIM 102410060
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
KATA PENGANTAR
Syukur Alhamdulillah diucapkan kehadirat Allah SWT, berkat rahmat dan
karunia-Nya penulis dapat menyelesaikan Tugas Akhir ini. Penulis menyadari
bahwa Tugas Akhir ini masih jauh dari sempurna, namun dengan pengetahuan
dan pengalaman yang terbatas akhirnya penulis menyelesaikan Tugas Akhir yang
diberi judul : “Pengujian Total Coliform dan Faecal Coliform pada Air Baku PT
TIRTA Sumut di Laboratorium PDAM TIRTANADI”.
Penulis telah menerima banyak bantuan terutama dari berbagai pihak baik
langsung maupun tidak langsung dalam penyelesaian tugas akhir ini, berkat
bantuan dan dorongan terhadap penulis sehingga tugas akhir ini dapat
terselesaikan. Dalam kesempatan ini penulis mengucapkan terima kasih kepada
pihak-pihak yang antara lain :
1. Bapak Prof. Dr. Sumadio Hadisaputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program
Studi Diploma III Analis Farmasi dan Makanan, Fakultas Farmasi,
Universitas Sumatera Utara.
3. Bapak Dr. Edy Suwarso, S.U., Apt., selaku dosen pembimbing yang telah
memberi petunjuk dan saran dalam menyelesaikan laporan ini.
4. Bapak Agus Karyono Harahap dan Mamak Agustina br Ginting yang
dengan penuh kasih sayang telah mengasuh, mengasihi, mendidik, dan
banyak memberikan dorongan moril maupun materil yang sangat
berpengaruh dalam kehidupan penulis.
5. Seluruh staf pengajar dan pegawai Fakultas Farmasi yang telah banyak
membimbing dan membantu penulis selama melaksankan perkuliahan dan
praktikum di Diploma III Analis Farmasi dan Makanan.
6. Abang saya, Muhammad Syafi’i Zein Harahap dan kakak saya, Rindy
Mita Julianda Harahap.
7. Teman-temanku Astri Ivo Damanik, Clara Arianti, Kholidayani Harahap,
Ramahdani, Tri Wahyuni, Morhan, Istimewa Bako, Rudiansyah,
Arrahman dan Fauzan Lubis. Semoga petualangan kita tidak sampai disini
dan semakin banyak destinasi yang akan kita tuju.
8. Teman-teman seperjuangan yang selalu kompak AFA’10.
Akhir kata penulis mengharapkan semoga Tugas Akhir ini bermanfaat bagi
kemajuan ilmu pengetahuan maupun sebagai bahan perbandingan yang
memerlukannya, dan kiranya Allah SWT senantiasa melimpahkan Rahmat dan
Karunia-Nya kepada kita semua.
Medan, Maret 2013
Penulis
THE TOTAL COLIFORM AND FAECAL COLIFORM
TESTING OF PT TIRTA SUMUT RAW WATER IN
LABORATORY TIRTANADI
ABSTRACT
Raw water is water that is in the form of whole, unprocessed or not having treatment. The water that will be through the stages of the process water treatment companies or institutions, to be circulated in the community. Coliform bacteria and faecal coliform is an indicator of the biological contamination (microbiological parameters) are contaminated with organic and feces. Coliform bacteria are gram-negative bacilli bacteria and not sporulating. Faecal Coliform is normal flora in the human digestive tract. The purpose of testing is to determine the amount of total coliform and faecal coliform in PT TIRTA SUMUT raw water in Medan Tirtanadi Central Laboratory and to determine whether the water meets the requirements stipulated in Government Regulation. 82/PP/I/2001. Samples that were taken from PT TIRTA SUMUT raw water, was tested by the method Most Probable Number (MPN).
The results show that the water is checked Total Coliform 1100000/100 ml. According to Government Regulation No. 82/PP/I/2001, Total Coliform number specified for raw water is 1000/100 ml. Thus, it can be interpreted that the levels of Total Coliform amount of PT Tirta SUMUT raw water are not eligible to be used as clean water and drinking water.
Faecal Coliform test results on the water obtained numbers 20000/100 ml. According to Government Regulation No. 82/PP/I/2001, Faecal Coliform maximum amount specified for the raw water is 100/100 ml. It can be concluded the number of Faecal Coliform in raw water PT Tirta Sumatra does not meet the requirements that have been defined.
PENGUJIAN TOTAL COLIFORM DAN FAECAL COLIFORM
PADA AIR BAKU PT TIRTA SUMUT DI LABORATORIUM
PDAM TIRTANADI
ABSTRAK
Air baku merupakan air yang masih dalam bentuk utuh, yang belum diproses atau belum mengalami pengolahan. Air ini yang nantinya akan melalui tahapan-tahapan proses pada perusahaan atau instansi pengolahan air, untuk diedarkan pada masyarakat. Bakteri Coliform dan Faecal Coliform merupakan indikator biologis terhadap pencemaran air (parameter mikrobiologi) yang terkontaminasi zat organik maupun feses. Bakteri Coliform adalah bakteri basil gram negatif dan tidak berspora. Faecal Coliform merupakan flora normal pada saluran pencernaan manusia. Tujuan pengujian ini adalah untuk mengetahui jumlah Total Coliform dan Faecal Coliform pada air baku PT TIRTA Sumut di Laboratorium Pusat PDAM Tirtanadi Medan serta untuk mengetahui apakah air tersebut memenuhi persyaratan yang telah ditetapkan pada Peraturan Pemerintah No. 82/PP/I/2001. Sampel yg diambil dari air baku PT TIRTA Sumut, diuji dengan metode Angka Paling Mendekati (APM) atau Most Probable Number
(MPN).
Hasil pengujian menunjukkan bahwa air yang diperiksa Total Coliform 1100000/100 ml. Menurut Peraturan Pemerintah No. 82/PP/I/2001, jumlah Total Coliform yang ditetapkan untuk air baku adalah 1000/100 ml. Dengan demikian, dapat diartikan bahwa kadar jumlah Total Coliform dari air baku PT Tirta Sumut tidak memenuhi syarat untuk digunakan sebagai air bersih dan air minum.
Hasil pengujian Faecal Coliform pada air tersebut diperoleh angka 20000/100 ml. Menurut Peraturan Pemerintah No. 82/PP/I/2001, jumlah Faecal Coliform maksimum yang ditetapkan untuk air baku adalah 100/100 ml. Maka dapat diambil kesimpulan jumlah Faecal Coliform pada air baku PT Tirta Sumut tidak memenuhi persyaratan yang sudah ditetapkan.
2.6.2 Analisis Coliform Dengan Metode MPN ... 12
2.6.3 Analisi Coliform Dengan Metode Penyaringan ... 13
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Hasil ... 23
4.2 Pembahasan ... 23
BAB V KESIMPULAN DAN SARAN ... 25
5.1 Kesimpulan ... 25
5.2 Saran ... 25
DAFTAR PUSTAKA ... 26
DAFTAR TABEL
Halaman
Tabel 2.5 Parameter Wajib pada Persyaratan Air Minum ... 11
THE TOTAL COLIFORM AND FAECAL COLIFORM
TESTING OF PT TIRTA SUMUT RAW WATER IN
LABORATORY TIRTANADI
ABSTRACT
Raw water is water that is in the form of whole, unprocessed or not having treatment. The water that will be through the stages of the process water treatment companies or institutions, to be circulated in the community. Coliform bacteria and faecal coliform is an indicator of the biological contamination (microbiological parameters) are contaminated with organic and feces. Coliform bacteria are gram-negative bacilli bacteria and not sporulating. Faecal Coliform is normal flora in the human digestive tract. The purpose of testing is to determine the amount of total coliform and faecal coliform in PT TIRTA SUMUT raw water in Medan Tirtanadi Central Laboratory and to determine whether the water meets the requirements stipulated in Government Regulation. 82/PP/I/2001. Samples that were taken from PT TIRTA SUMUT raw water, was tested by the method Most Probable Number (MPN).
The results show that the water is checked Total Coliform 1100000/100 ml. According to Government Regulation No. 82/PP/I/2001, Total Coliform number specified for raw water is 1000/100 ml. Thus, it can be interpreted that the levels of Total Coliform amount of PT Tirta SUMUT raw water are not eligible to be used as clean water and drinking water.
Faecal Coliform test results on the water obtained numbers 20000/100 ml. According to Government Regulation No. 82/PP/I/2001, Faecal Coliform maximum amount specified for the raw water is 100/100 ml. It can be concluded the number of Faecal Coliform in raw water PT Tirta Sumatra does not meet the requirements that have been defined.
PENGUJIAN TOTAL COLIFORM DAN FAECAL COLIFORM
PADA AIR BAKU PT TIRTA SUMUT DI LABORATORIUM
PDAM TIRTANADI
ABSTRAK
Air baku merupakan air yang masih dalam bentuk utuh, yang belum diproses atau belum mengalami pengolahan. Air ini yang nantinya akan melalui tahapan-tahapan proses pada perusahaan atau instansi pengolahan air, untuk diedarkan pada masyarakat. Bakteri Coliform dan Faecal Coliform merupakan indikator biologis terhadap pencemaran air (parameter mikrobiologi) yang terkontaminasi zat organik maupun feses. Bakteri Coliform adalah bakteri basil gram negatif dan tidak berspora. Faecal Coliform merupakan flora normal pada saluran pencernaan manusia. Tujuan pengujian ini adalah untuk mengetahui jumlah Total Coliform dan Faecal Coliform pada air baku PT TIRTA Sumut di Laboratorium Pusat PDAM Tirtanadi Medan serta untuk mengetahui apakah air tersebut memenuhi persyaratan yang telah ditetapkan pada Peraturan Pemerintah No. 82/PP/I/2001. Sampel yg diambil dari air baku PT TIRTA Sumut, diuji dengan metode Angka Paling Mendekati (APM) atau Most Probable Number
(MPN).
Hasil pengujian menunjukkan bahwa air yang diperiksa Total Coliform 1100000/100 ml. Menurut Peraturan Pemerintah No. 82/PP/I/2001, jumlah Total Coliform yang ditetapkan untuk air baku adalah 1000/100 ml. Dengan demikian, dapat diartikan bahwa kadar jumlah Total Coliform dari air baku PT Tirta Sumut tidak memenuhi syarat untuk digunakan sebagai air bersih dan air minum.
Hasil pengujian Faecal Coliform pada air tersebut diperoleh angka 20000/100 ml. Menurut Peraturan Pemerintah No. 82/PP/I/2001, jumlah Faecal Coliform maksimum yang ditetapkan untuk air baku adalah 100/100 ml. Maka dapat diambil kesimpulan jumlah Faecal Coliform pada air baku PT Tirta Sumut tidak memenuhi persyaratan yang sudah ditetapkan.
BAB I PENDAHULUAN
1.1Latar Belakang
Air merupakan materi esensial di dalam kehidupan. Tidak satupun
makhluk hidup di dunia ini tidak memerlukan dan tidak mengandung air. Sel
hidup, baik tumbuhan, hewan, monera, protista, dan fungi sebagian besar tersusun
atas air. Misalnya pada sel-sel tumbuhan terkandung lebih dari 75% atau di dalam
sel hewan terkandung lebih dari 67% (Waluyo, 2007).
Perairan permukaan, seperti danau, sungai, muara dan lautan merupakan
suatu ekosistem mikrobiologis yang amat rumit. Perairan demikian kurang lebih
rentan terhadap pencemaran berkala oleh mikroorganisme dari air atmosfer, aliran
air pada permukaan tanah dan limbah domestik ataupun industri yang dibuang
kedalamnya. Perairan permukaan amat bervariasi dalam hal kandungan nutrien
yang tersedia bagi mikroba, keadaan fisik, dan ciri-ciri biologinya. Dengan
demikian jelaslah bahwa terdapat perbedaan yang amat besar dalam hal populasi
mikroba yang terdapat di dalamnya (Irianto, 2006).
Untuk menjaga konsumen agar tetap memperoleh air minum yang layak
dikonsumsi sesuai dengan standar kualitas air minum menurut Dep. Kes. R.I dan
WHO, maka pemerintah Indonesia mendirikan Perusahaan Daerah Air Minum
dan seluruh wilayah Indonesia agar terpenuhinya kebutuhan rakyat Indonesia
PDAM Tirtanadi Provinsi Sumatera Utara yang terletak di Jalan
Sisingamangaraja No. 1 Medan, dalam upayanya melayani kebutuhan masyarakat
akan air bersih menggunakan beberapa sumber air yang salah satunya adalah air
baku PT Tirta Sumut. Biasanya air baku berbau dan keruh. Oleh karena itu harus
dilakukan proses pengolahan terlebih dahulu sebelum digunakan sebagai air
bersih.
Mendeteksi mikroorganisme patogen secara spesifik di dalam air
merupakan hal yang sulit, serta membutuhkan waktu dan biaya yang tidak sedikit.
Untuk mendeteksi keberadaan mikroorganisme patogen di dalam air, biasanya
digunakan bakteri Coliform sebagai organisme petunjuk (indicator organism)
(Mulia, 2005).
Mikrobiologi akuatik menjadi makin penting dengan adanya urbanisasi
disertai dengan meningkatnya kebutuhan masyarakat akan air, pentingnya
perairan alamiah sebagai reservoir makanan utama, penyelidikan lepas pantai
untuk mendapatkan minyak dan mineral, didirikannya badan perlindungan
keadaan lingkungan, serta perkembangan-perkembangan lainnya (Irianto, 2006).
1.2 Tujuan dan Manfaat 1.2.1 Tujuan
− Untuk mengetahui APM (Angka Paling Mendekati) Total Coliform
dan Faecal Coliform pada air baku PT TIRTA SUMUT di
− Untuk mengetahui APM (Angka Paling Mendekati) Total Coliform
dan Faecal Coliform pada air baku PT TIRTA SUMUT di
Laboratorium Pusat PDAM Tirtanadi sesuai dengan persyaratan
yang telah ditetapkan pada Peraturan Pemerintah No. 82/2010
tanggal 14 Desember 2001 tentang Persyaratan Kualitas Air Baku.
1.2.2 Manfaat
− Dapat digunakan sebagai informasi kepada masyarakat mengenai
pengujian mikrobiologi pada air baku PT TIRTA SUMUT yang
sesuai dengan persyaratan yang ditetapkan oleh Peraturan
Pemerintah No. 82/2010 tanggal 14 Desember 2001 tentang
Persyaratan Kualitas Air Baku.
− Dapat meningkatkan pengetahuan penulis mengenai kajian tulis
ilmiah yang dilakukan serta menimba pengalaman melakukan
BAB II
TINJAUAN PUSTAKA
2.1 Defenisi Air
Air merupakan suatu sarana utama untuk meningkatkan derajat kesehatan
masyarakat, karena air merupakan salah satu media dari berbagai macam
penularan, terutama penyakit perut. Peningkatan kualitas air minum dengan jalan
mengadakan pengelolaan terhadap air yang akan diperlukan sebagai air minum
dengan mutlak diperlukan terutama apabila air tersebut berasal dari air permukaan
(Sutrisno, 2002).
Air (H2O) di alam tidak pernah dalam keadaan murni. Air murni hanya di
laboratorium dalam bentuk akuades. Air di alam selalu ditambahi dengan factor
X, sehingga rumus kimianya menjadi H2O + X, dimana factor X dapat berbentuk
faktor yang bersifat hidup (biotik) dan faktor yang bersifat tidak hidup (abiotik)
(Waluyo, 2007).
Air merupakan kebutuhan pokok bagi kehidupan manusia di bumi ini.
Sesuai dengan kegunaannya, air dipakai sebagai air minum, air untuk mandi dan
mencuci, air untuk pengairan pertanian, air untuk kolam perikanan, air untuk
sanitasi dan air untuk transportasi baik di sungai maupun di laut. Kegunaan air
seperti tersebut di muka termasuk sebagai kegunaan air secara konvensional
Peraturan Menteri Kesehatan Republik Indonesia No. 16 tahun 2005
tentang pengembangan sistem penyediaan air minum, di dapat pengertian
mengenai:
1. Air baku untuk air minum rumah tangga, yang selanjutnya disebut air baku
adalah air yang dapat berasal dari sumber air permukaan, cekungan air
tanah dan atau air hujan memenuhi baku mutu tertentu sebagai air baku
untuk air minum.
2. Air minum adalah air minum rumah tangga yang melalui proses
pengolahan yang memenuhi syarat kesehatan dan dapat diminum.
3. Air limbah adalah buangan yang berasal dari rumah tangga termasuk tinja
manusia dari lingkungan pemukiman.
4. Penyediaan air minum adalah kegiatan menyediakan air minum untuk
memenuhi kebutuhan masyarakat agar mendapatkan kehidupan yang
sehat, bersih, dan produktif.
5. Sistem penyediaan air minum yang selanjutnya disebut SPAM merupakan
satu kesatuan sistem fisik (teknik) dan nonfisik dari prasarana dan sarana
air minum.
2.2 Sumber-Sumber Air
Menurut Entjang (2000), sumber air di alam dibagi menjadi 2 yaitu:
1. Air dalam tanah (Ground water)
Adalah air yang diperoleh dari pengumpulan air pada lapisan tanah dalam.
mengandung mineral-mineral dalam kadar yang terlalu tinggi. Misalnya:
air sumur dan air dari mata air.
2. Air permukaan (surface water) adalah air yang terdapat pada permukaan
tanah. Air permukaan harus diolah terlebih dahulu sebelum dipergunakan
karena umumnya telah mengalami pengotoran. Misalnya: air sungai, air
rawa, air danau, air kolam, dan air hujan.
2.3 Klasifikasi Air
Menurut Peraturan Pemerintah No. 20 tahun 1990 mengelompokkan
kualitas air menjadi beberapa golongan menurut peruntukannya. Adapun
penggolongan air menurut peruntukannya adalah sebagai berikut :
1. Golongan A, yaitu air yang dapat digunakan sebagai air minum secara
langsung, tanpa pengolahan terlebih dahulu. Contohnya mata air
pegunungan.
2. Golongan B, yaitu air yang dapat digunakan sebagai air baku air minum.
Contohnya air sungai.
3. Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan
dan peternakan. Contohnya air laut.
4. Golongan D, yaitu air yang dapat digunakan untuk keperluan pertanian,
usaha di perkotaan, industri, dan pembangkit listrik tenaga air. Contohnya
2.4 Persyaratan Air Minum 2.4.1 Persyaratan Fisik
Air minum memiliki persyaratan fisik meliputi: air tidak boleh berwarna,
air tidak boleh berasa, air tidak boleh berbau, suhu air hendaknya di bawah sela
udara (sejuk ±250 C), dan air harus jernih (Sutrisno, 2002).
− Warna
Meskipun murni, air dikatakan selalu berwarna, yaitu biru-hijau muda
apabila volume cukup banyak. Sangat penting membedakan antara warna
asli yang disebabkan oleh material-material terlarut dan warna semu yang
diakibatkan zat-zat tersuspensi warna kuning alami pada air berasal dari
pegunungan, yang berasal dari asam-asam organik yang tidak berbahaya
bagi kesehatan dan warna ini dapat diasamkan dengan warna asam tanik
yang terdapat pada air teh.
− Bau dan rasa
Jika air ditemukan berbau, maka penyebab timbulnya harus diperiksa.
Untuk menjamin kualitas air tersebut dapat digunakan sebagai sumber air,
harus dilakukan uji bakteriologis di laboratorium. Jika ditemukan berasa
payau atau asin maka cek hasil laboratorium kandungan klorida (Joko,
2010).
− Suhu
Aktivitas mikroorganisme memerlukan suhu optimum yang berbeda-beda.
Akan tetapi, proses dekomposisi biasanya terjadi pada kondisi udara yang
Pada kisaran suhu ini, setiap peningkatan suhu sebesar 100C akan
meningkatkan proses dekomposisi dan konsumsi oksigen menjadi dua kali
lipat (Effendi, 2003).
− Kekeruhan
Kekeruhan air dapat ditimbulkan oleh adanya bahan-bahan organik dan
anorganik, seperti lumpur dan buangan dari pemukiman tertentu yang
menyebabkan air sungai menjadi keruh (Suriawiria, 2005).
2.4.2 Persyaratan Kimia − pH netral (pH 7)
Derajat keasaman air minum harus netral, tidak boleh bersifat asam
maupun basa. Air yang mempunyai pH rendah (asam) akan terasa asam,
sedangkan air yang mempunyai pH di atas 7 (basa) akan terasa pahit.
Pengukuran pH umumnya dilakukan dengan kertas pH atau pH water
tester. Alat lain yang dapat digunakan adalah pH meter. pH meter selain
sulit diaplikasikan harganya juga relatif mahal (Gufran, 2007).
− Tidak mengandung bahan kimia beracun
Air yang berkualitas baik tidak mengandung bahan kimia beracun seperti
sianida, sulfida, fenolik.
− Tidak mengandung garam atau ion-ion
Air yang berkualitas baik tidak mengandung garam seperti NaCl atau
− Kesadahan rendah
Tingginya kesadahan berhubungan dengan ion-ion yang terlarut di dalam
air terutama Ca2+ dan Mg2+.
− Tidak mengandung bahan organik. Kandungan bahan organik dalam air
dapat terurai menjadi zat-zat yang berbahaya bagi kesehatan.
2.4.3 Persyaratan Mikrobiologi
Air minum tidak boleh mengandung bakteri-bakteri penyakit (patogen)
sama sekali dan tak boleh mengandung bakteri-bakteri golongan Coli melebihi
batas-batas yang telah ditentukan. Bakteri golongan Coli ini berasal dari usus
besar (feaces) dan tanah. Bakteri patogen yang mungkin ada dalam air antara lain
adalah :
− Bakteri penyebab tifus
− Vibrio colera
− Bakteri penyebab disentri
− Shigella sp.
− Bakteri enteris lainnya (penyebab penyakit pada perut)
Air yang mengandung golongan Coli dianggap telah berkontaminasi
(berhubungan) dengan kotoran manusia. Dengan demikian dalam pemeriksaan
bakteriologik, tidak langsung diperiksa apakah air itu mengandung bakteri
2.5 Standar Kualitas Air Minum
Air minum adalah air yang sudah terpenuhi syarat fisik, kimia,
bakteriologi serta level kontaminasi maksimum (LKM) (Maximum Contaminant
Level). Level kontaminasi maksimum meliputi sejumlah zat kimia, kekeruhan dan
bakteri Coliform yang diperkenankan dalam batas-batas aman (Gabriel, 2001).
Air yang digunakan untuk keperluan sehari-hari sebaiknya adalah air yang
memenuhi kriteria sebagai air bersih. Air bersih merupakan air yang dapat
digunakan untuk keperluan sehari-hari yang kualitasnya memenuhi syarat-syarat
kesehatan dan dapat diminum apabila telah dimasak (Waluyo, 2007).
Air minum aman bagi kesehatan apabila memenuhi persyaratan fisika,
mikrobiologis, kimiawi, dan radioaktif yang dimuat dalam paremeter wajib dan
parameter tambahan. Telah ditetapkan bahwa untuk menjaga kualitas air minum
yang dikonsumsi masyarakat dilakukan pengawasan kualitas air minum secara
eksternal dan secara internal. Pengawasan kualitas air minum secara internal pula
merupakan pengawasan yang dilaksanakan oleh penyelenggara air minum untuk
menjamin kualitas air minum yang diproduksi memenuhi syarat sebagaimana
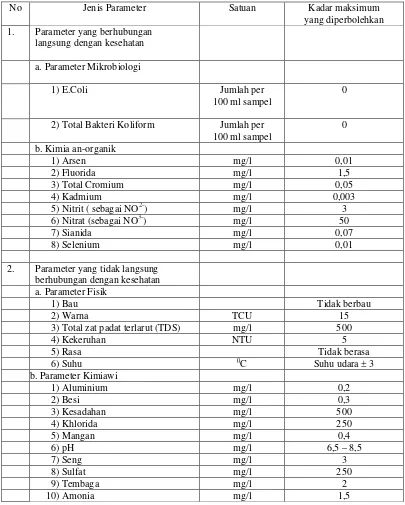
Tabel 2.5 Parameter Wajib pada Persyaratan Kualitas Air Minum
Berdasarkan tabel 2.5, maka didapatkan persyaratan kualitas air minum
sebagai berikut.
No Jenis Parameter Satuan Kadar maksimum yang diperbolehkan 1. Parameter yang berhubungan
langsung dengan kesehatan a. Parameter Mikrobiologi
1) E.Coli Jumlah per 100 ml sampel
0
2) Total Bakteri Koliform Jumlah per 100 ml sampel
2.6 Bakteri Coliform
2.6.1 Pengertian Bakteri Coliform
Kelompok Coliform mencakup semua gram negatif berbentuk batang
yang tidak membentuk spora dan dapat meragikan laktosa dengan pembentukan
asam dan gas pada suhu 37oC dalam waktu kurang dari 48 jam (Buckle, 1985).
Kelompok Coliform mencakup bakteri yang bersifat aerobik dan
anaerobik fakultatif, batang Gram negatif dan tidak membentuk spora. Koliform
menfermentasikan laktosa dengan pembentukan asam dan gas dalam waktu 48
jam pada suhu 35oC. Kelompok Coliform dipilahkan menjadi Coliform asal tinja
(faecal coliform) dan bukan-tinja (misalnya tanah) (Lay, 1994).
2.6.2 Analisis Coliform dengan MPN (Most Probable Number)
Dalam metode MPN (Most Probable Number) unutk uji kualitas
mikrobiologi air dalam praktikum digunakan kelompok Coliform sebagai
indikator. Metode MPN merupakan uji deretan tabung yang menyuburkan
pertumbuhan Coliform sehingga diperoleh nilai untuk menduga jumlah Coliform
dalam sampel yang diuji. Jumlah Coliform ini bukan penghitungan yang tepat
namun merupakan angka yang mendekati jumlah yang sebenarnya. Uji ini diawali
dengan memasukkan 10 ml cairan dari sampel kedalam lauryl tryptose broth. Uji
awal ini disebut uji duga (presumptive test). Tabung yang memperlihatkan
pembentukan gas diuji lebih lanjut dengan uji peneguhan dan bila diperlukan
yang memperlihatkan hasil positif pada uji duga. Kaldu BGLB diinkubasikan
pada suhu 35oC selama 48 jam. Untuk uji Coliform asal tinja dilakukan pada
media E.C yang diinkubasi pada suhu 44,5oC selama 24 jam. Pembentukan gas
dalam tabung menunjukkan hasil positif. Media dan suhu inkubasi menyuburkan
kuman yang diseleksi, baik dalam uji peneguhan maupun uji Coliform
asal-tinja.Uji positif menghasilkan angka indeks, angka ini disesuaikan dengan tabel
MPN untuk menentukan Coliform dalam sampel (Lay, 1994).
2.6.3 Analisis Coliform dengan Metode Penyaringan
Metode penyaringan atau membrane filter (MF) memberikan hasil lebih
cepat dibandingkan dengan metode MPN. Namun demikian, metode sebaiknya
tidak digunakan untuk menentukan jumlah Coliform sampel air yang keruh.
Untuk menentukan dan menghitung Coliform dan Coliform asal-tinja disediakan
media khusus. Coliform menggunakan m-Endo agar, sedangkan Coliform
asal-tinja menggunakan m-Faecal agar (Lay, 1994).
2.7 Faecal Coliform (Escherichia coli)
Escherichia coli dianggap sebagai gram negatif, tidak membentuk spora
yang dapat meragikan laktosa dengan pembentukan asam dan gas pada suhu 37oC
dan 44oC dalam waktu kurang dari 48 jam. Escherichia coli menghasilkan indole
di dalam air pepton yang berisi triptofan dan tidak dapat menggunakan natrium
sitrat saja sebagai satu-satunya sumber karbon . Escherichia coli dapat dipastikan
berasal dari kotoran dan adanya Escherichia coli harus dianggap sebagai petunjuk
BAB III
− Neraca Timbang kapasitas
500 gr
− Tabung Reaksi (single
strength dan double strength)
− Tabung Durham
− Rak tabung reaksi
− Labu takar 100 ml
− Erlenmeyer 1000 ml
− Erlenmeyer 2000 ml
3.1.2 Media/Bahan
− Lactose broth, EC broth,
− BGLB (Brilian Green Lactose
Broth)
− EMBA (Eosin Methylene Blue
Agar)
− Buffer Posfat
− Medium Lauryl Tryptose
− SIM
3.1.3.1. Media Lactose Broth Single Strenght
− Dimasukkan 13 gram lactose broth ke dalam Erlenmeyer
− Ditambahkan monodest sebanyak 1000 ml lalu dihomogenkan
− Dimasukkan ke dalam tabung reaksi ukuran single strength yang telah
berisi tabung durham terbalik sebanyak 10 ml
− Disterilisasikan dengan menggunakan autoklaf selama 20 menit pada suhu
3.1.3.2. Media Lactose Broth Double Strenght
− Dimasukkan 26 gram lactose broth ke dalam erlenmeyer
− Ditambahkan monodest sebanyak 1000 ml lalu dihomogenkan
− Dimasukkan ke dalam tabung reaksi ukuran single strength yang telah
berisi tabung durham terbalik sebanyak 10 ml
− Disterilisasikan dengan menggunakan autoklaf selama 25 menit pada suhu
121°C
3.1.3.3. Media EC Broth
− Dimasukkan 37 gram EC broth ke dalam erlenmeyer
− Ditambahkan monodest sebanyak 1 liter lalu dihomogenkan
− Dimasukkan ke dalam tabung reaksi single strength yang telah berisi
tabung durham terbalik sebanyak 10 ml
− Disterilisasikan dengan menggunakan autoklaf selama 20 menit pada suhu
121°C
3.1.3.4. Media BGLB (Brilian Green Lactose Broth)
− Masukkan 40 gram BGLB ke dalam erlenmeyer
− Ditambahkan monodest sebanyak 1000 ml lalu dihomogenkan
− Dimasukkan ke dalam tabung reaksi single strength yang telah berisi
tabung durham terbalik sebanyak 10 ml.
3.1.3.5. Media EMBA (Eosin Methylene Blue Agar)
− Dimasukkan 36 gram EMBA (Eosin Methylene Blue Agar) ke dalam
Erlenmeyer
− Ditambahkan 1000 ml monodest
− Dimasukkan magnetic stirrer ke dalam larutan EMBA, lalu panaskan di
atas hot plate
− Dimasukkan kedalam botol 250 ml
− Disterilisasikan dengan menggunakan autoklaf selama 20 menit pada suhu
121 °C.
− Dituang ke dalam cawan petri steril sebanyak 10 ml
3.1.3.6. Larutan Buffer Phosphat
− Dipipet 1 ml MgCl2 dan tambahkan 0,25 KH2PO4
− Dimasukkan ke dalam labu ukur 200 ml
− Ditambahkan monodest sampai batas garis pada labu ukur, homogenkan.
− Diatur pH dengan penambahan NaOH 5-10 tetes
− Dimasukkan larutan buffer tersebut ke dalam botol sebanyak 49,5 ml dan
tabung reaksi double strength sebanyak 9 ml.
3.2 Parameter Mikrobiologi 3.2.1 Total Coliform
Metode APM (Angka Paling Mungkin) menggunakan 5 tabung untuk
contoh air, air minum dalam kemasan, dan susu.
3.2.2 Prosedur Kerja Analisa Total Coliform
− Siapkan 4 wadah buffer Phosphat. Masukkan 9 ml buffer ke dalam tabung
single untuk pengenceran pertama dan ke-3, masing-masing satu buah.
Masukkan 49,5 ml buffer kedalam botol untuk pengenceran ke-2 dan ke-4
, masing-masing satu buah.
− Pipet 1 ml dari sampel ke dalam buffer pertama (pengenceran 10-1).
− Pipet 0,5 ml dari pengenceran pertama ke dalam buffer ke-2 yang berisi
49,5 ml buffer (pengenceran 10-2).
− Pipet 1 ml dari pengenceran ke-2 kedalam buffer ke-3 yang berisi 9 ml
buffer (pengenceran 10-3).
− Pipet 0,5 ml dari pengenceran kedua ke dalam buffer ke-4 yang berisi 49,5
ml buffer (pengenceran 10-4).
− Pipet masing-masing 1 ml buffer yang berisi cuplikan kedalam deretan 5
tabung pertama, ke-2 dan ke-tiga yang berisi 9 ml perbenihan yang sama ,
berisi tabung durham tebalik.
− Simpan semua tabung ke dalam inkubator pada suhu 36 ± 1ºC selama
24-48 jam.
masing-dalam inkubator pada suhu 36 ± 1ºC selama 24 jam, kemudian catat
jumlah tabung yang membentuk gas.
− Pindahkan sebanyak 1 sengkelit dari setiap seri tabung yang membentuk
gas pada media Lactose broth ke dalam tabung yang berisi 10 ml Brilliant
Green Lactose Bile broth 2% (BGLB).
− Masukkan semua tabung ke dalam inkubator pada suhu 36 ± 1ºC selama
24-48 jam adanya gas pada tabung BGLB memperkuat adanya bakteri
Coliform dalam contoh.
Catatan : Bila contoh yang dipipet kedalam tabung sebanyak 1 ml dan 0,5 ml
maka APM Coliform per 100 ml dihitung dengan rumus :
Jumlah/100 ml = AngkapadatabelAPMatauMPNxFaktorPengenceranterbesar
Jumlahmlterbesardipipet
3.2.3 Faecal Coliform
Metode APM (Angka Paling Mungkin).
3.2.4 Prosedur Kerja Analisa Faecal Coliform
− Siapkan 4 wadah buffer Phosphat. Masukkan 9 ml buffer ke dalam tabung
single untuk pengenceran pertama dan ke-3, masing-masing satu buah.
Masukkan 49,5 ml buffer kedalam botol untuk pengenceran ke-2 dan ke-4
, masing-masing satu buah.
− Pipet 1 ml dari pengenceran pertama ke dalam buffer ke-2 yang berisi 9
ml buffer (pengenceran 10-2).
− Pipet 1 ml dari pengenceran ke-2 kedalam buffer ke-3 yang berisi 9 ml
buffer (pengenceran 10-3).
− Pipet 1 ml dari pengenceran kedua ke dalam buffer ke-4 yang berisi 9 ml
buffer (pengenceran 10-4).
− Pipet masing-masing 1 ml buffer yang berisi cuplikan kedalam deretan 5
tabung pertama, ke-2 dan ke-tiga yang berisi 9 ml perbenihan yang sama.
− Masukkan 1 sengkelit biakan positif gas pada Lactose broth dari pengujian
Angka Paling Mungkin Faecal Coliform ke dalam tabung yang berisi EC
broth yang didalamnya terdapat tabung durham terbalik.
− Inkubasikan dalam inkubator pada suhu 44-45ºC selama 24-48 jam
− Catat tabung yang didalamnya terbentuk gas (E. coli dianggap positif, jika
didalam tabung terbentuk gas).
Catatan : Bila contoh yang dipipet kedalam tabung sebanyak 1 ml dan 0,5 ml
maka APM Coliform per 100 ml dihitung dengan rumus :
Jumlah/100 ml = AngkapadatabelAPMatauMPNxFaktorPengenceranterbesar
− Lanjutkan penetapan E. coli dengan menginokulasikan biakan yang
membentuk gas ke perbenihan EMB Agar.
− Inkubasi pada suhu 35ºC selam 18-24 jam.
− Hasil positif jika koloni berwarna kilap logam.
− Pilih koloni berwarna kilap logam (EMB)
Lakukan pengujian IMViC (Indol, Merah metil, Voges Proskauer, dan
Sitrat) dari media EMB Agar.
3.2.5 Pengujian IMViC 3.2.5.1 Uji Indol
Dari media EMB Agar, inokulasikan 1 sengkelit biakan ke dalam Media SIM
(Sulfur Indol Motility). Inkubasikan pada suhu 35 ± 1ºC selama 18-24 jam.
Tambahkan 0,2-0,3 ml pereaksi indol ke dalam masing-masing tabung dan kocok
selama 10 menit.
Warna merah tua pada permukaan menunjukkan reaksi indol “positif”,
sedangkan warna jingga menunjukkan reaksi indol “negatif”.
3.2.5.2Uji Merah Metil (Methyl Red)
Dari media EMB Agar, inokulasikan 1 sengkelit biakan ke dalam perbenihan
MR-VP. Inkubasi pada suhu 35ºC selama 48 jam. Dengan menggunakan pipet,
pindahkan 5 ml ke dalam tabung reaksi, tambahkan 5 tetes merah metil dan
kocok. Warna merah menunjukkan reaksi “positif”, sedangkan warna kuning
3.2.5.3Uji VP (Voges Proskauer)
Dari media EMB, inokulasikan 1 sengkelit biakan ke dalam perbenihan
MR-VP. Inkubasi pada suhu 36 ± 1ºC selama 48 jam. Dengan menggunakan pipet,
pindahkan 1 ml suspensi ke dalam tabung reaksi, tambahkan 0,6 ml larutan
alfa-naftol dan 0,2 ml larutan kalium Hidroksida dan kocok. Diamkan selama 2-4 jam.
Warna merah muda hingga merah tua menunjukkan reaksi “positif”, sedangkan
warna tidak berubah menunjukkan reaksi “negatif”.
3.2.5.4Uji Sitrat
Dari media EMB Agar, inokulasikan 1 sengkelit biakan kedalam perbenihan
Simmons Citrate. Inkubasi pada suhu 35ºC selama 48-96 jam. Warna biru
menunjukkan reaksi “positif”, sedangkan warna hijau menunjukkan reaksi
“negatif” (pada perbenihan Simmons Citrat).
Hasil dinyatakan sebagai berikut:
a. Amati terbentuk tidaknya gas dalam tabung durham, jika terbentuk gas,
dengan menunjukkan ke tabel Angka Paling Mungkin (Tabel II), dapat
dinyatakan Angka Paling mungkin E. coli
b. Tegaskan hasil uji dengan reaksi biokimia. Jika reaksi biokimia menunjukkan
uji indol dan merah metil “positif”, dan uji VP serta sitrat “negatif”, dapat
dinyatakan penegasan adanya E.coli
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Berikut ini adalah hasil yang diperoleh dari pengujian kualitas air pada air
baku PT TIRTA SUMUT yang diuji pada tanggal 19 Februari 2013.
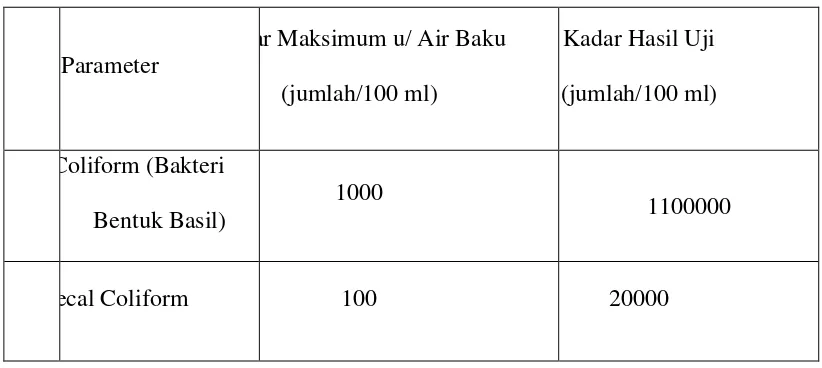
Tabel Hasil Uji
Parameter
ar Maksimum u/ Air Baku
(jumlah/100 ml)
Dari hasil pengujian yang diperoleh dari pengujian air baku PT TIRTA
SUMUT diperoleh 1100000/100 ml Total Coliform dan 20000/100 ml Faecal
Coliform. Menurut Peraturan Pemerintah No. 82 tahun 2010 tanggal 14 Desember
2001, jumlah maksimum Total Coliform maupun Faecal Coliform yang
ditetapkan untuk air baku adalah 1000/100 ml dan 100/100 ml.
Dengan demikian, dapat diartikan bahwa Total Coliform dan Faecal
sebagai air minum dan air bersih karena kadar yang diperoleh melebihi dari kadar
maksimum yang ditetapkan. Kadar Total Coliform dan Faecal Coliform pada air
baku setiap pemeriksaan terdapat perbedaan hasil. Hal ini karena adanya
perbedaan waktu pemeriksaan sampel dan cara pengambilan sampel.
Kontaminasi kotoran dipastikan dengan penemuan organisme yang terjadi
hanya dalam kotoran manusia, tidak pernah bebas di alam. Terdapat beberapa
organisme semacam itu dan di negara ini organisme indikator itu adalah
Escherichia coli. Penemuan Escherichia coli merupakan bukti yang cukup bahwa
air yang diperiksa tidak aman, karena pathogen saluran pencernaan diperkirakan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
− Pengujian air baku PT TIRTA SUMUT di Laboratorium Pusat PDAM
Tirtanadi diperoleh Total Coliform yang diuji dengan metode MPN adalah
1100000/100 ml dan Faecal Coliform yang diuji dengan metode MPN
adalah 20000/100 ml.
− Total Coliform dan Faecal Coliform yang diuji di Laboratorium Pusat
PDAM Tirtanadi Medan tidak memenuhi persyaratan yang telah
ditetapkan pada Peraturan Pemerintah No. 82 tahun 2010 tanggal 14
Desember 2001 tentang Persyaratan Kualitas Air Baku, yaitu melebihi dari
1000/100 ml untuk Total Coliform dan 100 /100 ml untuk Faecal
Coliform.
5.2 Saran
− Perlunya dilakukan pengawasan yang baik terhadap air baku yang
digunakan masyarakat terutama untuk kawasan industri maupun padat
penduduk.
− Diharapkan masyarakat/konsumen dapat lebih memperhatikan lingkungan
DAFTAR PUSTAKA
Buckle, KA., Edwards, R.A., Fleet G.H., dan Wooton M. (1985). Food Science
(Terjemahan dari Bahasa Inggris oleh Purnomo, Hari dan Adiono). (1987).
Ilmu Pangan. Jakarta: Penerbit Universitas Indonesia. Hal. 196-198.
Effendi, H. (2003). Telaah Kualitas Air. Yogyakarta: Kanisius. Hal. 14, 57,174.
Entcang, I. (2000). Ilmu Kesehatan Masyarakat. Bandung: PT. Citra Aditya Bakti. Hal. 77.
Gabriel, J.F. (2001). Fisika Lingkungan. Jakarta: Hipokrates. Hal. 79.
Ghufran, M.H.K.K., dan Andi, B.T. (2007). Pengelolaan Kualitas Air. Jakarta: Rineka Cipta. Hal. 87.
Irianto, K. (2006). Menguak Dunia Mikroorganisme. Bandung: Yrama Widya. Hal.149-151.
Lay, B.W. (1994). Analisis Mikrobiologi di Laboratorium. Jakarta: Raja Grafindo Persada. Hal. 123-126.
Mulia, R.M. (2005). Kesehatan Lingkungan. Yogyakarta: Graha Ilmu. Hal. 48.
Suriawiria, U. (2005). Air Dalam Kehidupan dan Lingkungan yang Sehat. Bandung: Alumni. Hal. 35.
Sutrisno, T. (2002). Teknologi Penyediaan Air Bersih. Jakarta: Rhineka Cipta. Hal. 3, 21-23, 40.
Volk, W.A. (1989). Mikrobiologi Dasar. Jakarta: Erlangga. Hal. 260.
Waluyo, L. (2007). Mikrobiologi Umum. Malang: UMM Press. Hal. 304.
Lampiran 1. Peralatan, Media dan Tes Uji
Peralatan Analisa Mikrobiologi Inkubator 34,80 C
Inkubator 42,50 C Media Lactose Broth Single dan Double Strenght
Lampiran 1. (sambungan)
Tes Pendugaan Positif Tes Penegasan Coliform (BGLB)
Lampiran 2. Tabel Daftar APM Coliform Menggunakan 5 Tabung
Kombinasi JumlahAPM / 100 ml yang Positif Kombinasi JumlahAPM / 100 ml yang Positif
Lampiran 3. Tabel Sifat-sifat bakteri Coliform dengan uji IMViC
Indol Methyl Red
Voges
Proskauer
Sitrat Type
+ + - -
Typical
E. coli
- + - -
Atypical
E. coli
+ + - +
Typical
Intermediate
- + - +
Atypical
Intermediate
- - + +
Typical
Lampiran 6. Perhitungan
Dalam menentukan jumlah Total Coliform dan Faecal Coliform,
menggunakan cara perghitungan yang sama dan mengacu pada tabel APM/MPN ,
yaitu dengan rumus :
Jumlah/100 ml
=
AngkapadatabelAPMatauMPNxFaktorPengenceranterbesar JumlahmlterbesardipipetPada Total Coliform , Tabung BGLB yang positif adalah seri 5-3-1,
sehingga angka yang ditunjukkan 110, jadi perhitungannya adalah :
Jumlah/100 ml
=
AngkapadatabelAPMatauMPNxFaktorPengenceranterbesar Jumlahmlterbesardipipet
=
110x104 1mlJumlah/100 ml = 1100000/100 ml
Pada Faecal Coliform , Tabung E.C.broth yang positif adalah seri 0-0-1,
sehingga angka yang ditunjukkan 2, jadi perhitungannya adalah :
Jumlah/10ml
=
AngkapadatabelAPMatauMPNxFaktorPengenceranterbesarJumlahmlterbesardipipet