ii ABSTRACT
THE STUDY OF THE PHASE TRANSITION ALUMINA PREPARED USING ELECTROCHEMICAL METHOD
BY
LIDIYA PERMATA DEWI
This research was conducted to study the effect of sintering temperatures on the phase transition of alumina prepared using electrochemical method. Preparation of alumina was carried out at different potentials and pHs and constant time of 24 hours. The alumina obtained at optimum condition was subjected to sintering treatment at different temperatures of 400, 800, and 1200 °C. The results obtained indicate that the largest quantity of alumina was produced at pH 4 and potential 22 volt. The results of FTIR showed that the unsintered and those sintered at 400 and 800 °C containing OH groups and Al-O, whereas the samplesintered at 1200 °C only consists of Al-O groups. The results of XRD indicate that the unsintered sample consists of -Al(OH)3 and AlOOH. The composition of the sample was found to change gradually into -Al2O3 and AlOOH after being sintered at temperature of 400 °C, then completely changed into -Al2O3 at temperature of 800 °C, and into α-Al2O3 at 1200 oC. the results of SEM showed that the samples consisted of particles with different sizes and shapes, and the sample subjected to sintering tretament at 1200 °C display more homogeneous surface. Characterization by EDS showed that the samples consist of elements Al and O, supporting the formation of Al2O3. Thermal conductivity measurements indicate that the samples are heat insulators.
i ABSTRAK
STUDY PERUBAHAN FASA ALUMINA YANG DIHASILKAN DENGAN METODE ELEKTROKIMIA
Oleh
LIDIYA PERMATA DEWI
Telah dilakukan penelitian untuk mempelajari pengaruh suhu sintering terhadap perubahan fasa alumina yang dihasilkan dengan metode elektrokimia. Terkait dengan pembuatannya, penelitian ini bertujuan untuk mempelajari pengaruh potensial dan pH, dengan melakukan percobaan pada pH 4 hingga 10, dan potensial 16 hingga 22 volt, dengan waktu 24 jam, untuk mendapatkan kondisi dengan jumlah alumina yang paling optimum. Sampel alumina selanjutnya disintering pada suhu 400, 800, dan 1200 oC. Hasil yang diperoleh mengindikasikan bahwa jumlah alumina yang paling banyak dihasilkan pada pH 4 dan potensial 22 Volt. Hasil FTIR menunjukkan sampel sebelum disintering dan yang disintering pada suhu 400 dan 800 oC mengandung gugus O-H dan Al-O, sedangkan sampel yang disintering pada suhu 1200 oC hanya terdiri dari gugus Al-O. Hasil XRD mengindikasikan bahwa sampel sebelum sintering terdiri dari
-Al(OH)3 dan AlOOH. Komposisi sampel ini berubah secara bertahap menjadi -Al2O3 dan AlOOH setelah disintering pada suhu 400 oC, kemudian menjadi sempurna -Al2O3 setelah disintering pada suhu 800 oC dan menjadi α-Al2O3 setelah disintering pada suhu 1200 oC. Hasil SEM menunjukkan bahwa sampel terdiri dari partikel dengan ukuran dan bentuk yang berbeda, namun semakin homogen setelah sampel disintering pada suhu 1200 oC. karakterisasi dengan EDS menunjukkan bahwa sampel terdiri dari unsur Al dan O, yang mendukung pembentukan Al2O3. Pengukuran konduktivitas termal menunjukkan bahwa sampel merupakan isolator panas.
iii
STUDY PERUBAHAN FASA ALUMINA YANG DIHASILKAN DENGAN METODE ELEKTROKIMIA
Oleh
LIDIYA PERMATA DEWI
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA SAINS
Pada Jurusan Fisika
Fakultas Matematika dan Ilmu Pengetahuan Alam
UNIVERSITAS LAMPUNG BANDAR LAMPUNG
STUDY PERUBAHAN FASA ALUMINA YANG DIHASILKAN DENGAN METODE ELEKTROKIMIA
(Skripsi)
Oleh
Lidiya Permata Dewi 1017041048
JURUSAN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
BANDAR LAMPUNG
xviii
DAFTAR GAMBAR Gambar Halaman 2.1 Struktur kristal mineral korondum alumina... 8
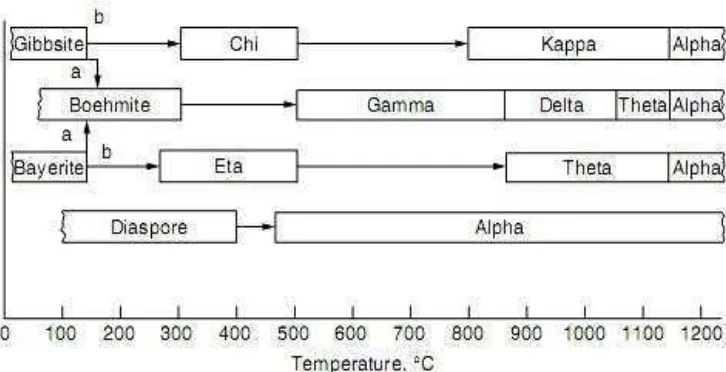
2.2 Grafik transformasi fasa alumina ... 10
2.3 Skema produksi alumina dengan proses Bayer ... 11
2.4 Difraksi dari bidang kristal ... 23
2.5 Skema kerja spektrofotometer FTIR ... 26
2.6 Hasil FTIR nanopartikel alumina dan modifikasi permukaan nanopartikel alumina ... 27
2.7 Skema alat Scanning Electron Microscopy (SEM) ... 29
2.8 Rangkaian alat untuk pengukuran konduktivitas termal ... 34
2.9 Skema representasi tahap sintering dan jenis proses sinter ... 35
3.1 Rangkaian perangkat elektrokimia yang digunakan dalam penelitian ... 38
3.2 Temperature program untuk sintering sampel ... 41
3.3 Rangkaian alat pengukuran konduktivitas termal ... 43
4.1 Proses Elektrokimia: (a) Tahap awal proses elektrokimia, (b). Proses elektrokimia setelah 24 jam... 45
4.2 Alumina basah ... 46
4.3 Alumina kering ... 46
4.4 Hasil elektrolisis alumina: (a) potensial 16 volt, (b) potensial 18 volt, (c) potensial 20 volt, dan (d) potensial 22 volt ... 47
4.5 Hasil analisis FTIR alumina sebelum sintering ... 49
4.6 Hasil karakterisasi FTIR sampel alumina yang disintering: (a) sintering 400 oC, (b) sintering 800 oC, dan (c) sintering 1200 oC ... 51
xviii
xiv DAFTAR ISI
Halaman
ABSTRAK ... i
ABSTRACT ... ii
HALAMAN JUDUL ... iii
HALAMAN PERSETUJUAN ... iv
HALAMAN PENGESAHAN ... v
HALAMAN PERNYATAAN ... vi
RIWAYAT HIDUP ... vii
HALAMAN PERSEMBAHAN ... ix
MOTTO ... x
KATA PENGANTAR ... xi
SANWANCANA ... xii
DAFTAR ISI ... xiv
DAFTAR TABEL ... xvi
DAFTAR GAMBAR ... xvii
I. PENDAHULUAN A. Latar Belakang ... 1
B. Rumusan Masalah ... 5
C. Batasan Masalah... 5
D. Tujuan Penelitian ... 6
E. Manfaat Penelitian ... 6
xv II. TINJAUAN PUSTAKA
A. Alumina ... 8
B. Metode Pembuatan Alumina ... 9
C. Metode Elektrokimia ... 17
D. Karakterisasi Alumina ... 20
E. Sintering... 34
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ... 36
B. Alat dan Bahan ... 36
C. Prosedur Percobaan ... 37
IV. HASIL DAN PEMBAHASAN A. Pengantar ... 43
B. Preparasi Alumina Dengan Metode Elektrokimia ... 43
C. Perlakuan Sintering ... 47
D. Karakterisasi Sampel ... 48
V. KESIMPULAN A. Kesimpulan ... 66
B. Saran ... 67
DAFTAR PUSTAKA ... 68
xvi
DAFTAR TABEL
Tabel Halaman
xi
KATA PENGANTAR
Alhamdulillahirobbil’alamin. Segala puji bagi Allah SWT. yang senantiasa memberikan nikmat iman dan menganugerahkan rahmat, kasih sayang dan ilmu pengetahuan kepada manusia. Sehingga penulis dapat menyelesaikan skripsi yang berjudul “Study Perubahan Fasa Alumina yang Dihasilkan Dengan Metode Elektrokimia”. Skripsi ini disusun sebagai salah satu syarat yang harus ditempuh untuk mendapat gelar Sarjana Sains dari Universitas Lampung.
Penulis menyadari skripsi ini masih banyak kelemahan dan ketidaksempurnaan. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun terhadap kelanjutan dan hasil yang akan dicapai. Semoga skripsi ini bisa bermanfaat bagi kita semua.
Bandar Lampung, November 2014 Penulis,
x MOTO
“Learn from yesterday, live for today, and hope for tomorrow.” (Albert Einstein)
“Manusia yang paling tinggi kedudukanya adalah mereka yang tidak melihat kedudukan dirinya, dan manusia yang paling banyak memiliki kelebihan adalah
mereka yang tidak melihat kelebihan dirinya.” (Imam Syafi’i)
“Jangan kecewa apabila hasil yang diperoleh tidak seperti yang diharapkan, percaya bahwa semuanya adalah kesuksesan, bukan kegagalan.”
(Thomas Alva Edison)
ix
PERSEMBAHAN
Dengan ketulusan dan segala kerendahan hati serta rasa syukur kepada Allah SWT yang telah memberikan kasih sayang dan segala nikmat-Nya,
kupersembahkan karya kecil ini kepada:
Kedua Orangtuaku Tercinta
“Papa dan Mama tersayang yang selalu memberiku cinta, kasih sayang, semangat, pengorbanan dan selalu menyebut namaku dalam setiap bait do’a
yang mereka panjatkan untuk kelancaran dan keberhasilanku”
Adikku Tersayang
“Lingga Agung yang selalu memberiku semangat, dorongan, perhatian, dan kebahagiaan kepadaku sehingga hari-hari yang berat terlewati”
Someone, that I Love
“Dico Primantara yang selalu memberikan semangat, pengertian, perhatian, pengorbanan, cinta dan kasih sayang, sehingga karya kecil ini dapat
terselesaikan dengan lancar”
Serta
vii
RIWAYAT HIDUP
Penulis dilahirkan di Desa Bandar Jaya Kecamatan Terbanggi Besar, Lampung Tengah sebagai anak pertama dari dua bersaudara dari pasangan Bapak Rusli Yusuf dan Ibu Siti Widuri.
Jenjang pendidikan penulis dimulai dari pendidikan sekolah dasar (SD) pada tahun 1998 di SD Negeri 2 Purnama Tunggal, Lampung Tengah dan diselesaikan pada tahun 2004. Tahun 2004 penulis melanjutkan pendidikan ke Sekolah Menengah Pertama (SMP) di SMP Negeri 1 Way Pengubuan, Lampung Tengah yang diselesaikan pada tahun 2007 dan kemudian melanjutkan pendidikan di Sekolah Menengah Atas (SMA) di SMA Negeri 1 Terusan Nunyai, Lampung Tengah dan diselesaikan tahun 2010.
viii
xii
SANWANCANA
Puji syukur penulis panjatkan kehadirat Allah SWT, atas segala rahmat dan karunia-Nya sehingga penulis mampu menyelesaikan skripsi ini. Dengan ketulusan dan kerendahan hati, penulis mengucapkan terima kasih kepada pihak-pihak yang selalu tulus mendukung, membantu, membimbing dan mendoakan dalam menyelesaikan skripsi ini. Penulis ingin mengucapkan terima kasih kepada: 1. Bapak Prof. Drs. Simon Sembiring, Ph.D. sebagai Pembimbing I yang selalu
membimbing dengan tulus, sabar, menerangkan semua materi penelitian dengan detail dan bersedia meluangkan waktunya.
2. Bapak Prof. Drs. Wasinton Simanjuntak, M.Sc., Ph.D. sebagai Pembimbing II yang pengertian dan selalu memberikan pengarahan dan nasehat-nasehat yang membangun.
3. Bapak Drs. Pulung Karo Karo, M.Si. sebagai pembahas yang telah memberikan saran dan kritiknya di dalam memperbaiki skripsi ini.
4. Bapak Drs. Syafriadi sebagai dosen Pembimbing Akademik yang senantiasa memberi nasehat dan wejangan kepada penulis.
5. Ibu Dr. Yanti Yulianti, M.Si. selaku ketua jurusan Fisika FMIPA Unila beserta seluruh dosen dan Karyawan Jurusan Fisika FMIPA Unila.
xii
sayang yang hangat, cinta dan perhatian yang mengalir tiada hentinya adalah motivasi bagiku.
7. Untuk Dico Primantara terima kasih atas doa, semangat keringat dan dukungannya sehingga hari-hari yang berat dapat terlewati.
8. Teman penelitianku Putri dan Anisa yang membantu selama penelitian. 9. Teman-teman seperjuangan ku Fisika 2010 khusus Meta, Irene, Helrita,
Panda, Vera, Devi, Tika, Suci, dan Riza. Serta semua pihak yang tidak bisa saya sebutkan satu persatu. Terima kasih atas semua kenangan terindah dan cerita perjuangan selama di bangku kuliah.
Semoga Allah memberikan balasan yang lebih besar atas semua bantuan kalian. Aamiin Yaa Rabbal ‘Alamiin.
Bandar Lampung, 17 November 2014 Penulis
I. PENDAHULUAN
A.Latar Belakang
Alumina banyak digunakan dalam berbagai aplikasi seperti digunakan sebagai bahan refraktori dan bahan dalam bidang otomotif. Hal ini karena alumina memiliki sifat fisis yang baik antara lain, daya tahan panas yang tinggi, penghambat listrik yang baik, tahan terhadap abrasi, dan daya tahan terhadap korosi yang tinggi (Kagaku et.al., 2007). Karena memiliki aplikasi yang sangat luas, kebutuhan akan alumina terus meningkat, dan diperkirakan pada tahun 2013 kebutuhan alumina di dunia mencapai 280 juta ton (U.S. Geological Survey, 2013).
Di alam, alumina terdapat dalam mineral bauksit yang mengandung alumunium dalam bentuk hidroksida, yakni boehmet ( -AlO(OH)) dan gibsite Al(OH)3, dengan kadar sekitar 30-54%. Sebagai mineral alam, selain aluminium, bauksit juga mengandung berbagai pengotor, misalnya oksida besi, silika, dan mineral lempung. Karena komposisi tersebut, untuk mendapatkan alumina murni, bauksit harus diolah, dan salah satu metode pengolahannya adalah proses Bayer (Amira International, 2001).
dilakukan untuk mengubah oksida aluminium dalam bijih menjadi natrium aluminat {2NaAl (OH)4}, menurut persamaan kimia:
Gibbsite : Al(OH)3 + Na+ + OH-→ Al(OH)4- + Na+
Boehmite : AlO(OH) + Na+ + OH - + H2O → Al(OH)4- + Na+ Al(OH)4- + Na+ + Al(OH)4- + Na+ → 2NaAl (OH)4
Dalam proses di atas, komponen lain dari bauksit tidak ikut larut, sehingga pengotor tersebut dapat dipisahkan dengan penyaringan. Campuran kotoran padat disebut lumpur merah. Awalnya, larutan alkali didinginkan, kemudian gas karbon dioksida dialirkan kedalamnya, untuk mendapatkan endapan aluminium hidroksida berdasarkan reaksi:
2 NaAl (OH)4 + CO2 → 2 Al(OH)3 + Na2CO3 + H2O
Untuk mendapatkan alumina, endapan dipanaskan hingga 980°C (kalsinasi), dimana aluminium hidroksida terurai melepaskan air sesuai dengan reaksi (International Aluminium Institute, 2000):
2 Al(OH)3 → Al2O3 + 3H2O
3
digunakan sebagai penggosok yang sangat lembut dan pelapis permukaan (Van, 2007).
Dewasa ini telah dikembangkan beberapa cara untuk menghasilkan alumina dengan metode yang berbeda dan dikategorikan dalam metode fisika dan metode kimia. Metode fisika meliputi mechanical milling (Wu, 2001), laser ablation (Mamun, et al., 2010), dan flame spray (Tok et al., 2006). Metode kimia meliputi sol–gel processing (Rogajan et al., 2011), solution combustion decomposition (Pathak et al., 2002) dan vapour deposition (Wei et al., 2006). Kebanyakan dari metode fisika di atas berlaku hanya pada material tertentu saja serta ukuran partikel nano tidak dapat dikontrol dengan baik, sehingga metode kimia dianggap lebih baik dalam menghasilkan produk dengan homogenitas yang tinggi, meskipun membutuhkan biaya yang relatif lebih mahal (Halim, 2010).
Berikut ini adalah beberapa contoh dari metode kimia yang sering digunakan untuk menghasilkan alumina. Metode pertama adalah dengan metode sol gel, metode ini didasarkan pada transformasi fase sol yang diperoleh dari alkoksida logam, misalnya Natrium etoksida (CH3CH2ONa), atau organologam, misalnya etilnatrium (C2H5Na). Sol merupakan sistim koloid dimana suatu zat padat tersuspensi dalam zat cair mengandung partikel dalam suspensi dipolimerisasi pada suhu rendah, untuk membentuk gel basah. Pelarut dihilangkan dengan pengeringan gel dilanjutkan dengan perlakuan panas untuk mengubah gel menjadi padatan (Rogajan et al., 2011, Mirjalili, et al., 2011).
4
menghasilkan nanoalumina dari prekursor Alumunium nitrat, yang dilarutkan dalam asam sitrat, sehingga metode ini dikenal juga sebagai proses sitrat (Pathak et al., 2002). Metode ketiga adalah vapour deposition yang merupakan metode untuk menghasilkan nanopartikel menggunakan fasa gas, maka yang paling penting adalah kondensasi gas inert. Prinsip dasar dari proses kondensasi gas inert adalah bagaimana logam diintroduksi dan diuapkan. Pada metode ini digunakan prekursor alumunium pentanedionat yang dilarutkan dalam butanol untuk membentuk larutan dengan konsentrasi tertentu (Wei et al., 2006).
Dalam penelitian ini digagas untuk mempelajari metode elektrokimia sebagai metode alternatif untuk pembuatan alumina langsung dari logam aluminium. Metode ini digagas karena memiliki sejumlah keuntungan dibanding metode konvensional yang dipaparkan di atas. Keuntungan pertama adalah tidak memerlukan senyawa alumunium sebagai bahan baku, sehingga lebih murah dari sudut pandang bahan baku yang diperlukan. Keuntungan lainnya adalah prosesnya yang sangat sederhana, yakni hanya memerlukan perangkat elektrokimia yang sederhana untuk melangsungkan reaksi elektrolisis logam aluminium menghasilkan ion aluminium (Natter et al., 2003). Secara sederhana proses yang berlangsung dapat dirangkum dalam reaksi redoks di bawah ini. Reaksi anodik:
Al → Al3+ + 3 e Reaksi katodik:
H2O + e → H2 + OH
5
Al3+ + 3OH- → Al(OH)3
Al(OH)3 jika dipanaskan akan menghasilkan alumina berdasarkan reaksi: 2 Al(OH)3 → Al2O3 + 3H2O
Secara umum telah diketahui bahwa proses elektrokimia dipengaruhi oleh sejumlah variabel, dua diantaranya adalah potensial dan pH. Atas dasar ini, dalam penelitian ini akan dipelajari pengaruh pH dan potensial terhadap proses elektrokimia yang berlangsung serta kaitannya dengan karaktersitik perubahan fasa alumina yang dihasilkan. Perubahan fasa merupakan sifat khas dari alumina, dimana senyawa ini ditemukan dalam tiga fasa, yakni gamma , beta, dan alfa alumina. Menurut penelitian sebelumnya diketahui bahwa fasa gamma alumina terjadi pada suhu 300 -500°C (Kim, et al., 2005), kemudian mengalami perubahan fasa menjadi beta alumina pada suhu 1000°C (Zyl, et al., 1993). Dari suhu 1000°C terus terjadi perubahan fasa dari beta alumina menjadi fasa alfa alumina yang merupakan fasa yang stabil dan terbentuk secara sempurna pada suhu 1200°C (Rogajan, et al., 2011).
B.Rumusan Masalah
Rumusan masalah pada penelitian ini adalah:
1. Bagaimana pengaruh pH dan potensial dalam pembuatan alumina dengan metode elektrokimia ?
6
C.Batasan Masalah
Dalam penelitian ini masalah yang akan dipelajari dibatasi sebagi berikut: 1. Proses elektrokimia akan dilakukan pada pH 4, 5, 6, 8, 9,dan 10.
2. Proses elektrokimia akan dilakukan pada potensial 16 volt, 18 volt, 20 volt, dan 22 volt.
3. Alumina yang dihasilkan akan disintering pada suhu 400, 800, dan 1200 oC.
D.Tujuan Penelitian
Tujuan dari penelitian ini adalah sebagai berikut :
1. Menghasilkan alumina secara elektrokimia dengan potensial dan pH yang berbeda.
2. Mengkarakterisasai fasa alumina yang disintering pada suhu yang berbeda.
E.Manfaat Penelitian
Hasil penelitian ini diharapkan dapat dikembangkan lebih lanjut sebagai metode pembuatan alumina yang lebih murah dan efisien.
F. Sistematika Penulisan
Sistematika skripsi ini terbagi menjadi lima bab dengan aspek-aspek pemaparan sistematika sebagai berikut:
BAB I PENDAHULUAN
7
BAB II TINJAUAN PUSTAKA
Memaparkan informasi ilmiah tentang alumina, metode pembuatan alumina, metode elektrokimia, karakterisasi alumina dengan FTIR, SEM, XRD, PSA, uji konduktivitas termal, dan sintering.
BAB III METODE PENELITIAN
Berisi pemaparan tentang waktu dan tempat penelitian, alat dan bahan, perangkat elektrokimia untuk percobaan, pembuatan alumina dengan metode elektrokimia, pemisahan alumina, karakterisasi sampel dengan FTIR, SEM, XRD, PSA dan uji konduktivitas termal.
BAB IV HASIL DAN PEMBAHASAN
8
II. TINJAUAN PUSTAKA
A.Alumina
Aluminium oksida (alumina) adalah senyawa kimia dari aluminium dan oksigen, dengan rumus kimia Al2O3. Secara alami, alumina terdiri dari mineral korondum, dan memiiki bentuk kristal seperti ditunjukkan pada Gambar 2.1.
Gambar 2.1. Struktur kristal mineral korondum alumina (Hudson, et. al., 2002).
9
korosi (Mirjalili, et. al., 2011) dan titik lebur yang tinggi, yakni mencapai 2053-2072 oC (Budvari, 2001).
10
Gambar 2.2. Grafik transformasi fasa alumina (Yang, 2003).
B.Metode Pembuatan Alumina
11
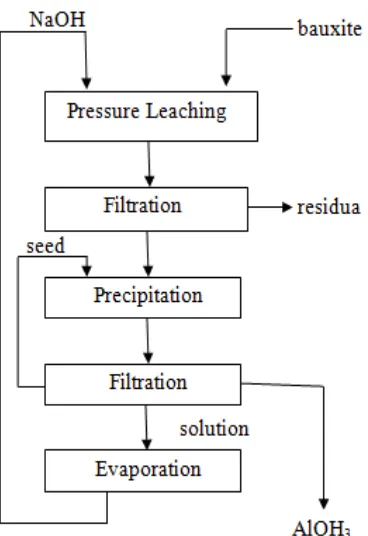
Gambar 2.3. Skema produksi alumina dengan proses Bayer (Ostbo, 2002).
Dalam proses Bayer, bauksit dilebur dengan cara melarutkan bauksit menggunakan larutan natrium hidroksida (NaOH) panas, dengan suhu sekitar 170-180 °C. Hal ini dilakukan untuk mengubah oksida aluminium dalam bijih menjadi natrium aluminat {2NaAl (OH)4}, menurut persamaan kimia:
Gibbsite : Al(OH)3 + Na+ + OH-→ Al(OH)4- + Na+
Boehmite : AlO(OH) + Na+ + OH - + H2O → Al(OH)4- + Na+ Al(OH)4- + Na+ + Al(OH)4- + Na+ → 2NaAl (OH)4
Dalam proses di atas komponen lain dari bauksit tidak ikut terlarut, sehingga pengotor tersebut dapat dipisahkan dengan penyaringan. Campuran kotoran padat disebut lumpur merah. Awalnya, larutan alkali didinginkan, kemudian gas karbon dioksida dialirkan kedalamnya, untuk mendapatkan endapan aluminium hidroksida berdasarkan reaksi:
12
Untuk mendapatkan alumina, endapan dipanaskan hingga 980 °C (kalsinasi), dimana aluminium hidroksida terurai melepaskan air sesuai dengan reaksi (International Aluminium Institute, 2000):
2 Al(OH)3 → Al2O3 + 3H2O
Dewasa ini telah dikembangkan beberapa cara untuk menghasilkan alumina dari bahan baku yang berbeda menggunakan beragam metode. Mirjalili, et al. (2011) mempelajari pembuatan alumina dari bahan baku alumunium isopropoksida (Al P) dan nonahydrate aluminium nitrat (Al N) sebagai template, Sodium bis-2ethylhexyl sulfosuccinate (Na(AOT)) dan Sodium dodecylbenzen sulfonat (SDB S) sebagai surfaktan, mengggunakan metode sol-gel. Proses metode sol gel dalam penelitian ini dimulai dengan menyiapkan larutan dengan cara mencampur 0,5 M alumunium nitrat dengan alumunium isoprokposida secara bertahap hingga nisbah molar aluminium isopropoksida dan aluminium nitrat mencapai 3, lalu campuran diaduk hingga homogen. Larutan yang terbentuk diaduk selama 48 jam, setelah itu ditambahkan Sodium bis-2ethylhexyl sulfosuccinate (Na (AOT)) dan Sodium sulfonat dodecylbenzen (SDB S), kemudian larutan diaduk selama 1jam dan ditambahkan surfaktan. Larutan dipanaskan hingga 60°C dan diaduk terus-menerus selama proses penguapan hingga membentuk gel. Gel kemudian dipanaskan pada 90°C selama 8 jam. Gel kering kemudian dikalsinasi pada suhu kisaran 1000-1200°C, dan digerus menggunakan mortar dan pastel.
13
stabil dari alpha alumina adalah pada suhu 1200 oC. Hasil TGA menunjukkan bahwa terjadi penurunan berat pada suhu dibawah 400 oC sebesar 3-4% dan pada suhu 400-750 oC sebesar 1%. Hasil DSC menunjukkan bahwa fasa gama alumina mulai terbentuk pada suhu 420 oC, fasa alfa alumina mulai terbentuk pada suhu 1035 oC. Hasil FTIR menunjukkan bahwa kedua surfaktan diserap oleh nanoalumina. Hasil SEM menunjukkan bahwa semakin banyak surfaktan yang digunakan, semakin kecil ukuran partikel alumina yang dihasilkan.
14
lagi. Karakterisasi dengan TEM menunjukkan bahwa sampel sebelum kalsinasi memiliki ukuran partikel adalah 10-30 nm, sementara setelah dikalsinansi pada suhu 1100oC ukuran sampel menjadi 50-100 nm. Perubahan ukuran partikel ini mengindikasikan bahwa tiga dan empat butir tumbuh menjadi satu partikel fasa alfa alumina setelah kalsinasi dan bentuk partikelnya menjadi lebih bulat dari sebelum dikalsinasi.
15
sebenarnya bertabrakan dengan target yang berbeda dari jumlah daya laser yang dipancarkan dari sumber karena sinar laser sebelumnya telah mengenai cermin dan udara atau debu. Sampel alumina yang diperoleh dikarakterisasi menggunakan XRD, TEM dan SEM. Hasil karakterisasi dengan XRD dan TEM menunjukkan bahwa yang dihasilkan adalah -Al2O3 dengan ukuran partikel 9,3 nm. Sedangkan hasil SEM menunjukkan bahwa perlakuan sintering mempengaruhi ukuran sampel dan bentuk partikel dari sampel alumina yang dihasilkan, semakin tinggi suhu sintering maka ukuran partikel semakin besar dan bentuknya semakin bulat.
Pathak, et al. (2002) mempelajari pembuatan alumina dengan metode combustion synthesis dengan bahan baku alumunium nitrat dan asam sitrat dengan pH yang berbeda. Proses pembuatan alumina dengan metode ini dimulai dengan membuat larutan induk yang terdiri dari campuran larutan alumunium nitrat dengan asam sitrat, selanjutnya campuran dinetralkan (pH 7) dengan menggunakan amonia. Untuk percobaan, dari larutan induk dibuat larutan dengan pH yang berbeda, yakni 2, 4, 6 dan 10 dengan menambahkan larutan amonia atau larutan asam nitrat. Kemudian larutan yang telah terbentuk dipanaskan sampai kering menggunakan sinar inframerah, yang diarahkan dari bagian atas larutan, hingga diperoleh gel berwarna hitam kering, dan akhirnya berubah menjadi alumina berupa serbuk halus dalam bentuk menyerupai busa.
16
karakterisasi menggunakan XRD diketahui bahwa sampel yang dikalsinasi pada suhu 700 oC membentuk fasa delta dan gamma alumina, dan pada suhu 1200 oC membentuk fasa tunggal alfa alumina. Hasil analisis dengan TGA menunjukkan bahwa puncak endotermik muncul pada suhu 300 oC dan puncak eksotermik muncul pada suhu 470 oC.
Hosseini, et al. (2011) memproduksi gamma alumina (Al2O3) dari kaolin. Bubuk kaolin dikalsinasi pada suhu 800°C selama 2 jam dalam tanur listrik untuk melonggarkan komponen alumina. Lalu, bubuk kaolin dicampurkan dengan larutan H2SO4. Campuran bubuk kaolin dan asam (250 mL) dimasukkan ke dalam labu reaksi 500 mL. Labu reaksi dilengkapi dengan pendingin refluk, dan campuran dicampur dengan pengaduk magnetik selama 18 jam. Suhu pada saat pencampuran berlangsung adalah 70°C. Setelah campuran kaolin dan asam telah tercampur, selanjutnya larutan didinginkan sampai suhu kamar dan disaring untuk menghilangkan residu, yang terdiri dari silika. Larutan tersebut kemudian ditetesi dengan larutan etanol 6,0 mL/menit hingga larutan mencapai 600 mL sambil terus diaduk dengan pengaduk magnetik. Endapan dicuci lagi dengan etanol dan dengan air suling kemudian dikeringkan pada suhu 70 °C selama 10 jam. Endapan dikalsinasi pada 900 °C selama 2 jam dalam tanur listrik.
17
gamma alumina. Hasil analisis dengan SEM menunjukkan bahwa ukuran sampel alumina yang terbentuk adalah 0,5-0,9 m.
Kim, et al. (2005) memproduksi alumina dengan metode hidrolisis dari bahan baku alkil karboksilat yang digunakan sebagai chemical template. Air digunakan sebagai pelarut pada proses hidrolisis dari alumunium alkoksida. Proses dalam pembuatan alumina dengan metode ini diawali melarutkan sumber aluminium dan surfaktan secara terpisah di sec-butil alkohol, setelah itu dua larutan tersebut dicampur. Kemudian air perlahan-lahan ditambahkan tetes demi tetes ke dalam campuran pada tingkat 1 ml/menit hingga menghasilkan endapan putih. Suspensi yang dihasilkan ini kemudian diaduk selama 24 jam. pH larutan reaktan diatur menggunakan larutan HNO3 1M. Hasilnya kemudian dikeringkan pada suhu kamar selama 48 jam. Setelah itu dikalsinasi selama 3 jam pada suhu 450o C. Rasio molar dari campuran reaksi ini adalah 1Al(detik-Buo)3: 0.2C 17H35COOH: 0.04 NaOH: 5 detik-BuOH :4-50 H2O (dalam tepat 1 M HNO3). Alumina disiapkan menggunakan asam stearat sebagai template disebut sebagai MA. Sebagai perbandingan, sampel alumina lainnya disiapkan dengan metode hidrotermal. Prosedur keseluruhan mirip dengan prosedur yang diuraikan di atas, dengan pengecualian non-template yang dibantu sintesis dan persiapan suhu 80°C. Bahan yang dihasilkan ini disebut sebagai HA.
18
menunjukkan titik dimulainya perubahan fasa dari alumunium hidroksida menjadi fasa alumina aktif dan molekul organik dan puncak ketiga menunjukkan asam stearic dan dehydroxylation dari sampel. Hasil karakterisasi dengan TEM menunjukkan bahwa sampel yang dihasilkan berukuran 20nm. Hasil karakterisasi menggunakan XRD menunjukkan bahwa pada suhu 25 oC fasa yang terbentuk adalah fasa bayerite dan boehmite, pada suhu 250-420 oC fasa yang terbentuk fasa gamma alumina dan pada suhu 450 oC yang terbentuk masih fasa gamma alumina.
C. Metode Elektrokimia
19
Metode elekrokimia telah banyak digunakan untuk menghasilkan material yang berukuran nano atau nanomaterial. Secara umum metode ini dikenal sebagai metode elektrosintesis. Teknik atau metode elektrosintesis adalah suatu cara untuk mensintesis atau membuat dan atau memproduksi suatu bahan yang didasarkan pada teknik elektrokimia. Pada metode ini terjadi perubahan unsur atau senyawa kimia menjadi senyawa yang sesuai dengan yang diinginkan. Penggunaan metode ini oleh para peneliti dalam mensintesis bahan didasarkan oleh berbagai keuntungan yang ditawarkan seperti peralatan yang diperlukan sangat sederhana, yakni terdiri dari dua atau tiga batang elektroda yang dihubungkan dengan sumber arus listrik, potensial elektroda dan rapat arusnya dapat diatur sehingga selektivitas dan kecepatan reaksinya dapat ditempatkan pada batas-batas yang diinginkan melalui pengaturan besarnya potensial listrik serta tingkat polusi sangat rendah dan mudah dikontrol. Dari keuntungan yang ditawarkan menyebabkan teknik elektrosintesis lebih menguntungkan dibandingkan metode sintesis secara konvensional, yang sangat dipengaruhi oleh tekanan, suhu, katalis dan konsentrasi (Suwarso, dkk, 2003).
20
sintesis tersebut bebas surfaktan, karena tidak ditambahkan surfaktan pada proses sintesis seperti pada kebanyakan metode sintesis lainnya. Nur, dkk (2013) memproduksi nano Hydroxyapatite menggunakan metode elektrokimia. Bahan yang digunakan adalah Ca2+/EDTA/PO4. Dari metode ini diperoleh nano Hydroxyapatite dengan ukuran 19-143 nm.
Penerapan metode elektrosintesis untuk pembuatan alumina yang digagas dalam penelitian ini didasarkan pada reaksi elektrokimia berikut ini.
Reaksi anodik:
Al → Al3+ + 3e Reaksi katodik:
H2O + e → H2 + OH
-Ion Al3+ yang selanjutnya bereaksi dengan OH- menghasilkan Al(OH)3 sesuai dengan persamaan reaksi;
Al3+ + 3OH- → Al(OH)3
Al(OH)3 jika dipanaskan akan menghasilkan alumina berdasarkan reaksi: 2 Al(OH)3 → Al2O3 + 3H2O
21
elektrokimia yang sederhana untuk melangsungkan reaksi elektrolisis logam aluminium menghasilkan ion aluminium.
Dalam penerapannya, proses elektrokimia diketahui dipengaruhi oleh berbagai faktor, di antaranya adalah pH dan potensial. Sebagai contoh Araoyinbo, et al. (2010) menggunakan metode elektrokimia untuk memproduksi alumina dengan ukuran nano. Potensial yang digunakan selama proses elektrokimia adalah 20V-80V. Dari penelitian tersebut diketahui bahwa besarnya potensial yang digunakan dalam proses elektrokimia mempengaruhi ukuran partikel dan current density alumina yang terbentuk. Pada potensial 20V diperoleh ukuran partikel sebesar 55nm dan rapat arus (current density) 2A/cm2-4A/cm2. Pada potensial 40V
22
D. Karakterisasi Alumina
Seperti telah dijelaskan sebelumnya, alumina ditemukan dalam tiga fasa, dan atas dasar ini, alumina pada umumnya dikaraktersiasi dengan teknik XRD. Di samping fasa, karaktersitik penting lainnya adalah gugus fungsi yang terkandung dalam alumina yang dapat diketahui melalui analisis sampel dengan FTIR, dan morfologi permukaan, yang dapat dievaluasi menggunakan SEM. Salah satu penggunaan alumina adalah sebagai ioslator panas, sehingga konduktivitas panas merupakan sifat alumina yang juga harus ditentukan.
1. Karakterisasi dengan Difraksi Sinar- X (XRD)
23
Hasil penelitiannya membahas permasalahan yang terkait dengan perjalanan gelombang cahaya melalui periodik dan susunan kristalin partikel. Kemudian dari penelitian ini ditarik kesimpulan bahwa sinar elektromagnetik yang jauh lebih pendek dari sinar-x seharusnya akan menyebabkan semacam fenomena difraksi atau interferensi dan bahwa kristal akan memberikan semacam media (James, 2007).
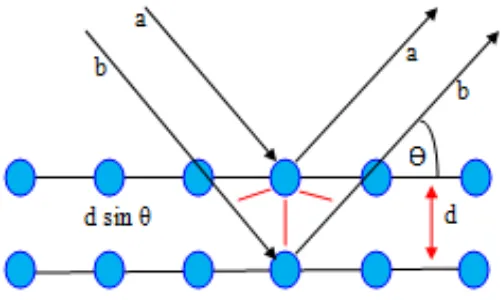
Sinar-x adalah gelombang elektromagnetik dengan panjang gelombang antara 0,5-2,5 A . Sinar-x dihasilkan dari tumbukan elektron berkecepatan tinggi dengan logam sebagai sasarannya. Oleh karena itu, suatu tabung sinar-x harus mempunyai suatu sumber elektron, voltase tinggi, dan logam sasaran (Warren, 1996). Prinsip dasar teknik XRD ditunjukkan dalam Gambar 2.4.
Gambar 2.4. Skema alat XRD (Smallman and Bishop, 2000).
24
struktur kristal dengan teknik sinar x didasarkan pada hukum Bragg, yang secara matematis dinyatakan dengan:
n = 2 d sinθ dengan:
n bilangan bulat 1, 2, 3 ...
adalah panjang gelombang sinar-x d adalah jarak antar bidang
θ adalah sudut difraksi (Scintag, 1λλλ).
Hukum Bragg menyatakan bahwa perbedaan lintasan berkas difrasi sinar-x harus merupakan kelipatan panjang gelombang. Secara umum pada proses difraksi sinar-x, apabila suatu bahan dikenai sinar-x maka intensitas sinar-x yang ditransmisikan lebih kecil dari intensitas sinar datang. Hal ini disebabkan adanya penyerapan oleh bahan dan juga penghamburan oleh atom-atom dalam material tersebut. Berkas sinar yang dihantarkan tersebut ada yang saling menghilangkan karena fasenya berbeda dan ada juga yang saling menguatkan karena fasenya sama. Berkas sinar-x yang saling menguatkan disebut sebagai berkas difraksi. Persyaratan yang harus dipenuhi agar berkas sinar-x yang dihamburkan merupakan berkas difraksi inilah yang kemudian dikenal sebagai Hukum Bragg.
25
karakterisasi dengan XRD diketahui bahwa fasa yang terbentuk adalah fasa α -alumina, setelah mengalami pross sintering pada suhu 1200 oC.
Kim, et al. (2005) memproduksi alumina dengan metode hidrolisis dari bahan baku alkil karboksilat yang digunakan sebagai chemical template. Air digunakan sebagai pelarut pada proses hidrolisis dari alumunium alkoksida. Dari hasil karakterisasi dengan XRD menunjukkan bahwa pada suhu 25 oC fasa yang terbentuk adalah fasa bayerite dan boehmite, pada suhu 250-420 oC fasa yang terbentuk masih fasa gamma alumina dan pada suhu 450 oC yang terbentuk adalah fasa gamma alumina. Atas dasar inilah, maka pada penelitian ini digunakan XRD sebagai alat karakterisasi yang digunakan untuk mempelajari perubahan fasa yang terjadi pada alumina yang terbentuk dari metode elektrokimia.
2. Karakterisasi dengan Fourier Transform Infrared (FTIR)
Seperti lazimnya senyawa kimia, sifat-sifat alumina juga sangat ditentukan oleh sejumlah karakteristiknya. Salah satu sifat mendasar alumina adalah gugus fungsi, yang dapat diketahui melalui analisis sampel dengan Fourier Transform Infrared (FTIR).
26
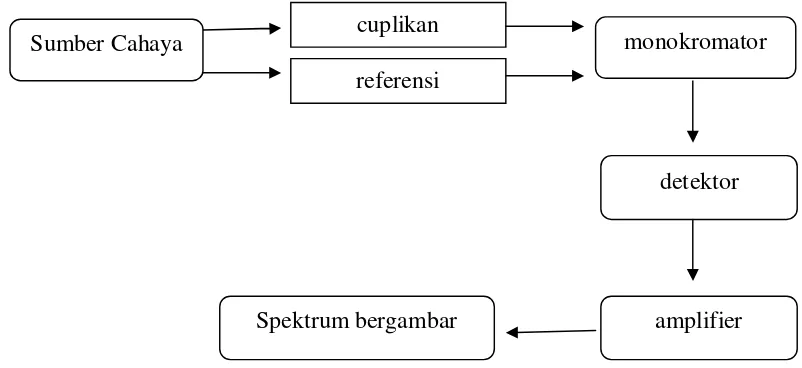
tergantung pada energi ikat dalam suatu gugus fungsi, sehingga akan memberi sinyal pada tingkat atau besaran energi yang berbeda, yang dalam FTIR dinyatakan dalam bentuk bilangan gelombang. Berikut ini merupakan skema kerja FTIR yang ditunjukkan dalam Gambar 2.5.
Gambar 2.5. Skema kerja spektrofotometer FTIR (Khasanah, 2006).
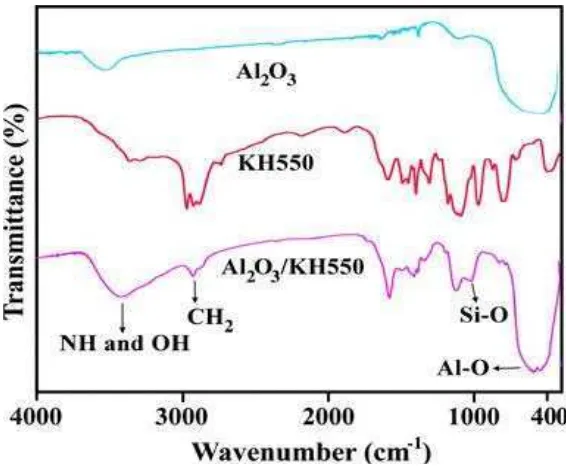
Dengan sifatnya tersebut, FTIR dapat memberikan informasi tentang jenis gugus fungsi dalam sebuah senyawa, termasuk alumina. Pemanfaatan teknik FTIR untuk mempelajari fungsionalitas alumina telah dilaporkan dalam penelitian yang dilakukan oleh Zivar, et al. (2012) yang menyatakan bahwa sampel nanopartikel alumina dan modifikasi permukaan sampel nanopartikel memiliki gugus fungsi seperti yang ditunjukkan dalam Gambar 2.6.
Sumber Cahaya cuplikan
referensi
monokromator
detektor
27
Gambar 2.6. Hasil FTIR nanopartikel alumina dan modifikasi permukaan nanopartikel alumina (Zivar, et al., 2012).
Gambar di atas menunjukkan bahwa sampel nanopartikel alumina terdiri dari gugus fungsi asam amic dan grup karboksil pada bilangan gelombang 2600-3500 cm-1, C-N pada bilangan gelombang 1770 cm-1, C-O pada bilangan gelombang 1720 cm-1, C-N pada bilangan gelombang 1373 cm-1, Al-O-Al pada bilangan gelombang 400-800 cm-1.
3. Karakterisasi dengan Scanning Electron Microscope-Energy dispersive X-Ray Spectrometer (SEM-EDS)
Teori SEM pertama kali dipublikasikan oleh fisikawan Jerman dr. Max Knoll pada tahun 1935, meskipun fisikawan Jerman lainnya Dr. Manfred von Ardenne mengklaim dirinya telah melakukan penelitian suatu fenomena yang kemudian disebut SEM hingga tahun 1937. Mungkin karena itu, tidak satu pun dari keduanya mendapatkan hadiah nobel untuk penemuan itu.
28
mikroskop elektron metode pemindaian (SEM) dengan resolusi hingga 50 nm atau magnifikasi 8.000 kali. Sebagai perbandingan SEM modern sekarang ini mempunyai resolusi hingga 1 nm atau pembesaran 500.000 kali. Mikroskop elektron cara ini memfokuskan sinar elektron (electron beam) di permukaan objek dan mengambil gambarnya dengan mendeteksi elektron yang muncul dari permukaan objek (McMullan, 2006).
Scanning Electron Microscopy (SEM) merupakan salah satu jenis mikroskop elektron yang dapat menggambarkan permukaan sampel. Dalam proses kerjanya alat ini memanfaatkan interaksi elektron berenergi tinggi dengan permukaan sampel. Elektron berenergi tinggi ini dihasilkan dari suatu filamen yang dipanaskan hingga suhu tinggi, dan arus elektron tersebut akan berinteraksi dengan atom di permukaan sampel. Interaksi ini akan menghasilkan pantulan elektron secara inelastis maupun elastis. Pantulan inelastis ini akan menghasilkan sinyal, yakni elektron sekunder. Elektron sekunder memberikan informasi topografi permukaan. Pantulan elastis akan menghasilkan dua sinyal, yakni berupa backscattered electron dan karakteristik sinar X. Elektron Backscattered memberikan informasi mengenai komposisi dari sampel dan informasi permukaan sampel. Karakteristik X-ray radiasi-hasil Mikroanalisis dan distribusi unsur-unsur sampel yang diberikan (Goldstein, et al., 1991).
SEM dilengkapi dengan sistem pencahayaan yang menggunakan energi radiasi elektron yang memiliki daya pisah ℷ = 200✁ sampai dengan 1 Ǻ, sehingga
29
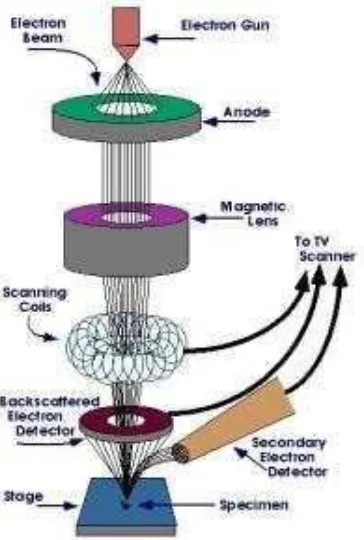
Selain itu SEM juga memiliki daya pisah sekitar 0,5 nm dengan perbesaran maksimum sekitar 500.000 kali (Griffin and Reissen, 1991). Secara umum skema alat Scanning Eelectron Microscopy ditunjukkan pada Gambar 2.7.
Gambar 2.7. Skema alat Scanning Electron Microscopy (SEM) (Griffin and Reissen, 1991).
Prinsip kerja dari alat Scanning Microscopy di atas adalah dengan menembakkan sinar elektron melalui sebuah pistol elektron kemudian sinar elektron tersebut dipercepat dengan anoda. Selanjutnya lensa magnetik memfokuskan elektron menuju ke sampel. Sinar elektron yang terfokus memindai (scan) keseluruhan sampel dengan diarahkan oleh koil pemindai. Ketika elektron mengenai sampel maka sampel akan mengeluarkan elektron baru yang akan diterima oleh detektor dan dikirim ke monitor (CRT) (Wagiyo dan Handayani, 1997).
30
(2007) menggunakan SEM untuk melihat ukuran sampel yang dihasilkan dari metode plasma synthesis. Dari hasil karakterisasi tersebut diketahui bahwa ukuran sampel alumina yang dihasilkan dari metode plasma adalah 10 nm. Hosseini et al. (2011) menggunakan SEM untuk mengetahui ukuran butir dari gamma alumina (Al2O3) yang dihasilkan dengan metode sol gel. Dari hasil karakterisasi menggunakan SEM diketahui bahwa ukurannya adalah 0,5-0,9 m.
Pada umumnya, karakterisasi dengan SEM digabung dengan analisis EDX. EDX didasarkan pada analisis spektral radiasi sinar-X karakteristik yang dipancarkan dari atom sampel pada iradiasi dengan berkas elektron difokuskan dari SEM. Sinar X ditembakkan pada posisi yang ingin kita ketahui komposisinya. Maka setelah ditembakkan pada posisi yang diinginkan akan muncul puncak–puncak tertentu yang mewakili suatu unsur yang terkandung di dalamnya. Dengan EDX dapat dibuat sebuah elemental mapping (pemetaan elemen) dengan memberikan warna berbeda–beda dari masing–masing elemen di permukaan bahan. EDX bisa digunakan untuk menganalisa secara kunatitatif dari persentase masing–masing elemen (Middleton, 1999).
3. Karakterisasi PSA (Particle Size Analyzer)
Ada beberapa cara yang bisa digunakan untuk mengetahui ukuran suatu partikel yaitu:
1. Metode ayakan (Sieve analyses) 2. Laser Diffraction (LAS)
3. Metode sedimentasi
31
5. Analisa gambar (mikrografi) 6. Metode kromatografi
7. Ukuran aerosol submikron dan perhitungan
Sieve analyses (analisis ayakan) dalam dunia farmasi sering kali digunakan dalam bidang mikromeritik, yaitu ilmu yang mempelajari tentang ilmu dan teknologi partikel kecil. Metode yang paling umum digunakan adalah analisa gambar (mikrografi). Metode ini meliputi metode mikroskopi dan metode holografi. Alat yang sering digunakan biasanya SEM, TEM dan AFM. Namun seiring dengan berkembangnya ilmu pengetahuan yang lebih mengarah ke era nanoteknologi, para peneliti mulai menggunakan Laser Ablation Spectroscopy (LAS). Metode ini dinilai lebih akurat bila dibandingkan dengan metode analisa gambar maupun metode ayakan (sieve analyses), terutama untuk sampel-sampel dalam orde nanometer maupun submicron(Lusi, 2011).
Contoh alat yang menggunakan metode LAS adalah particle size analyzer (PSA). Metode LAS bisa dibagi dalam dua metode:
1. Metode basah: metode ini menggunakan media pendispersi untuk mendispersikan material uji.
2. Metode kering: metode ini memanfaatkan udara atau aliran udara untuk melarutkan partikel dan membawanya ke sensing zone. Metode ini baik digunakan untuk ukuran yang kasar, dimana hubungan antarpartikel lemah dan kemungkinan untuk beraglomerasi kecil.
32
ataupun pengukuran partikel dengan metode ayakan dan analisa gambar, terutama untuk sampel-sampel dalam orde nanometer dan submicron yang biasanya memliki kecenderungan aglomerasi yang tinggi. Hal ini dikarenakan partikel didispersikan ke dalam media sehingga partikel tidak saling beraglomerasi (menggumpal). Dengan demikian ukuran partikel yang terukur adalah ukuran dari single particle. Selain itu hasil pengukuran dalam bentuk distribusi, sehingga hasil pengukuran dapat diasumsikan sudah menggambarkan keseluruhan kondisi sampel. Beberapa analisa yang dilakukan, antara lain:
1. Menganalisa ukuran partikel.
2. Menganalisa nilai zeta potensial dari suatu larutan sampel
3. Mengukur tegangan permukaan dari partikel clay bagi industri keramik dan sejenisnya. Dimana hal ini akan berpengaruh pada struktur lapisan clay. Struktur lapisan clay ini sangat berpengaruh pada metode slip casting.
4. Mengetahui zeta potensial coagulant untuk proses coagulasi partikel pengotor bagi industri WTP (Water Treatment Plant)
5. Mengetahui ukuran partikel tegangan permukaan dari densitas pada emulsi yang digunakan pada produk-produk industri beverage (Rusli,2011).
3. Karakterisasi Konduktivitas Termal
33
hubungan dasar untuk proses perpindahan yang diusulkan oleh J.B.J Fourier, yang secara garis besar dapat dijelaskan sebagai berikut:
= ( − )
Keterangan: Q = kalor (J) t = waktu (s)
k = nilai konduktivitas termal (W/m K) A = luas penampang (m2)
T1-T2 = perbedaan suhu (K) l = panjang (m)
Dimana rumusan untuk menghitung kalor (Q) dituliskan dalam persamaan berikut:
= ∆
Sehingga bila dikaitkan dengan rumusan awal, maka rumusan tersebut menjadi:
= ∆
Untuk menentukan nilai konduktivitas termal, maka persamaannya menjadi: k =
∆
34
Aliran Kalor
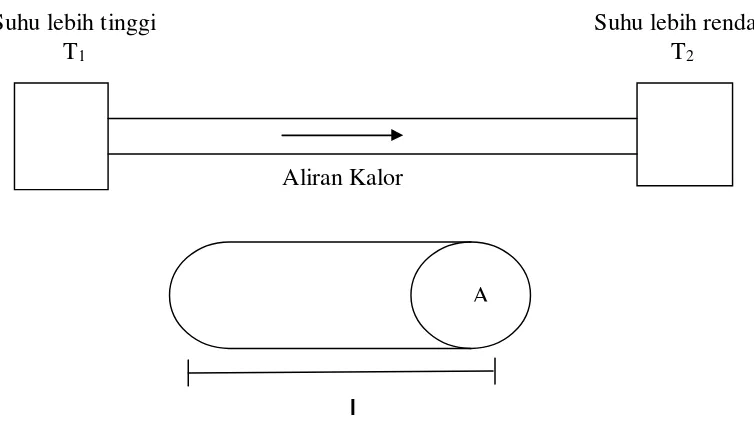
Gambar 2.8. Rangkaian alat untuk pengukuran konduktivitas termal (Setiadi, 2006).
Dari Gambar 2.8 diketahui bahwa, T1 memiliki suhu lebih tinggi dan T2 memiliki suhu yang lebih rendah. Karena adanya perbedaan suhu (T1- T2), maka kalor berpindah dari T1 ke T2. Benda yang dilewati kalor memiliki luas penampang (A) dan panjang (l). Hasil perhitungan nilai konduktivitas termal dari percobaan adalah: diketahui bahwa kalor yang berpindah selama selang waktu tertentu (Q/t) berbanding lurus dengan perbedaan suhu (T1- T2), luas penampang (A), nilai konduktivitas termal (k) dan berbanding terbalik dengan panjang (l) (Setiadi, 2006).
D. Sintering
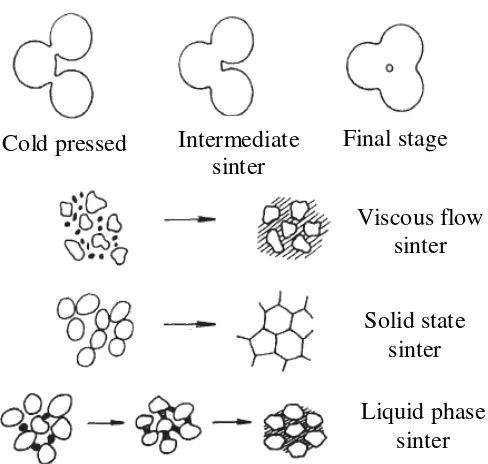
Proses sintering adalah suatu proses pemadatan sekumpulan serbuk pada suhu di bawah titik leburnya sehingga selama proses sintering terjadi pengurangan pori, penyusutan, dan perubahan ukuran butir (William, 1991). Skema representasi dari tahap sintering dan jenis proses sinter ditunjukkan pada Gambar 2.10.
A
l Suhu lebih tinggi
T1
35
Gambar 2.9. Skema representasi tahap sintering dan jenis proses sinter (McClom and Clark, 1998).
Terjadinya pengurangan pori dan pertumbuhan butir selama proses sintering akibat proses difusi diantara butir. Jenis proses difusi akan memberikan efek terhadap perubahan sifat-sifat fisis, yaitu perubahan densitas, pengurangan pori, dan ukuran butir. Umumnya peningkatan densitas, pengurangan pori, dan penyusutan disebabkan karena adanya difusi volume dan difusi batas butir (Randall, 1991).
Benda setelah mengalami proses sintering akan mengalami perubahan mikrostrukturnya sehingga sifat-sifat fisis maupun kemagnetannya akan ikut mengalami perubahan pula. Jelas bahwa suhu sintering memberikan pengaruh yang besar terhadap perubahan sifat fisis maupun sifat magnet. Suhu sintering semakin tinggi maka kerapatan atau kepadatannya akan semakin meningkat akibat adanya proses difusi selama proses sintering sehingga densitasnya cenderung meningkat dengan naiknya suhu sintering (Ristic, 1989).
Cold pressed Intermediate sinter
Final stage
Viscous flow sinter
Solid state sinter Liquid phase
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan dari bulan April 2014 sampai Juli 2014 di beberapa
laboratorium, yaitu Laboratorium Kimia Fisik Jurusan Kimia FMIPA Unila,
Laboratorium Fisika Material Jurusan Fisika FMIPA Unila, Laboratorium Biomassa
Unila.
B. Alat dan Bahan
Peralatan yang digunakan pada penelitian ini antara lain untuk preparasi sampel
adalah perangkat elektrokimia, catu daya, hot plate dengan pengaduk magnetik,
oven, pH universal, spatula, mortar dan pastel, corong pisah, dan peralatan gelas yang
umum digunakan di laboratorium. Untuk karakterisasi sampel, instrumen yang
digunakan adalah Fourier Transform Infrared (FTIR), X-Ray Difraktometer (XRD),
Scanning Electron Microscope-Energy Dispersive X-Ray Spectrometer (SEM-EDS),
PSA (Particle Size Analyzer) dan alat ukur konduktivitas termal sederhana.
Bahan-bahan yang digunakan dalam penelitian ini antara lain adalah akuades, NaOH, HNO3
37
C. Prosedur Percobaan
1. Perangkat Elektrokimia Untuk Percobaan
Perangkat elektrokimia yang digunakan dalam penelitian adalah perangkat yang
dirancang sendiri, dengan rangkaian seperti ditunjukkan dalam Gambar 3.1.
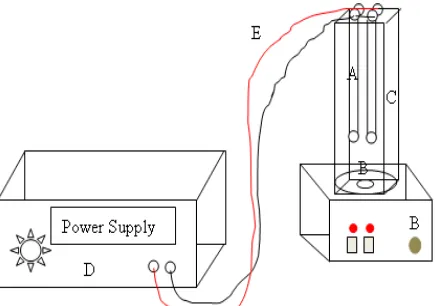
Gambar 3.1 Rangkaian perangkat elektrokimia yang digunakan dalam penelitian.
Secara garis besar, perangkat percobaan terdiri dari reaktor elektrokimia (A) yang
terbuat dari kaca, dengan ukuran 10cm x 10cm x 30cm, reaktor dilengkapi dengan
penutup yang terbuat dari fiber, dan dilengkapi dengan lubang untuk memasukkan
elektroda. Hot plate dengan pengaduk magnetik (B) alat ini digunakan untuk
mengaduk selama proses elektolisis berlangsung. Batang alumunium (C) yang terdiri
dari empat buah batang alumunium yang digunakan sebagai elektroda. Dua batang
alumunium digunakan sebagai katoda dan dua batang sebagai anoda. Elektroda
dihubungkan dengan catu daya (D) yang memiliki besar tegangan 1-22 volt
menggunakan kabel (E), sehingga percobaan dapat dilakukan dengan potensial yang
berbeda.
38
2. Pembuatan Alumina dengan Metode Elektrokimia
Dalam penelitian ini, pembuatan alumina dilakukan dengan pH dan potensial yang
berbeda. Sampel yang digunakan dibuat dengan mengatur pH akuades menggunakan
asam nitrat dan NaOH. Asam nitrat digunakan untuk mengatur pH air menjadi 4, 5,
dan 6, sedangkan NaOH digunakan untuk mengatur pH air menjadi 8, 9, dan 10.
Masing-masing sampel digunakan dalam percobaan elektrokimia dengan potensial
yang berbeda, yakni 16, 18, 20, dan 22 volt.
Dalam pelaksanaanya, sampel disiapkan dengan cara memasukkan akuades sebanyak
2 liter ke dalam gelas beaker, setelah itu pH akuades diatur dengan cara meneteskan
asam nitrat atau NaOH sedikit demi sedikit hingga akuades memilki pH sesuai
dengan yang diinginkan. Setelah akuades telah memiliki pH yang sesuai dengan
yang diinginkan kemudian akuades dimasukkan ke dalam reaktor elektrokimia.
Kemudian reaktor elektrokimia ditutup dengan penutup elektrokimia yang telah
dipasang empat buah batang alumunium. Batang alumunium tersebut kemudian
dihubungkan dengan anoda dan katoda pada catu daya menggunakan kabel
penghubung. Setelah terhubung, maka langkah selanjutnya adalah mengatur
tegangan sesuai dengan yang diinginkan yakni 16, 18, 20, dan 22 volt. Reaksi
elektrolisis berlangsung selama 24 jam.
3. Pemisahan Alumina
Pemisahan sampel alumina yang telah dihasilkan dari proses elektrokimia dilakukan
dengan cara sampel alumina diendapkan selama 24 jam, kemudian sampel yang telah
39
sebelumnya telah diolesi dengan minyak goreng agar sampel alumina tidak
menempel pada dinding corong pisah. Setelah dipisahkan kemudian disaring
kembali menggunakan kertas saring agar kandungan air pada sampel berkurang.
Sampel yang telah disaring diletakkan pada cawan tahan panas dan dioven selama 6
jam dengan suhu 100 oC. Sampel yang telah kering kemudian digerus menggunakan
mortar dan pastel agar sampel halus dan homogen. Kemudian sampel dicetak.
4. Karakterisasi Sampel
a. Karakterisasi dengan FTIR
Karakterisasi ini dilakukan untuk mengetahui gugus fungsi dari alumina yang
diperoleh melalui proses elektrokimia. Dari hasil karakterisasi ini nantinya akan
diperoleh gugus fungsi dari alumina. Karakterisasi ini dilakukan di Laboratorium
Biomassa UNILA.
b. Karakterisasi dengan SEM/EDS
Karakterisasi ini dilakukan untuk melihat karakteristik morfologi permukaan alumina,
sedangkan analisis EDS (Energy Dispersive Spectroscopy) dimaksudkan untuk
mengetahui ketidakhomogenan pada sampel dan menganalisis secara kualitatif dan
kuantitatif jenis unsur yang terkandung dalam alumina. Alumina yang telah digerus
dimasukkan ke dalam alat analisis dan dilakukan pengujiian dengan langkah-langkah
sebagai berikut:
1. Sampel yang akan dianalisis disiapkan dan direkatkan pada specimen holder.
2. Sampel yang telah terpasang pada holder dibersihkan menggunakan hand
40
3. Sampel dimasukkan dalam mesin counting dan diberi lapisan tipis berupa
gold-poladium hingga menghasilkan lapisan dengan ketebalan 200-400Å.
4. Sampel dimasukkan ke dalam specimen chamber.
5. Pengamatan dan pengambilan gambar pada layar SEM dengan mengatur
perbesaran dan spot yang diinginkan.
6. Pemotretan gambar SEM.
c. Karakterisasi dengan XRD
Karakterisasi ini dilakukan untuk mempelajari perubahan fasa alumina yang
dihasilkan sebagai fungsi suhu. Untuk tujuan ini sebelum dikarakterisasi sampel
terlebih dahulu disintering pada suhu yang berbeda yakni 400, 800, dan 1200 oC.
Ketiga suhu sintering tersebut diplih karena dari sumber literatur diketahui bahwa
pada suhu 400 oC alumina terdapat sebagai alumina, pada suhu 800 oC alumina
terdapat sebagai alumina, dan pada suhu 1200 oC alumina terdapat sebagai
alumina. Proses sintering dilakukan dengan temperature program, seperti
ditunjukkan dalam Gambar 3.2.
400 oC (1jam 15menit)
5o/min
50 oC
41
Adapun langkah-langkah dalam analisis ini adalah sebagai berikut :
1. Sampel disiapkan dan diletakkan pada sample holder.
2. Komputer XRD dinyalakan dan parameter pada XRD disesuaikan dengan
kondisi yang diinginkan, meliputi scan mode, rentang sudut, kecepatan scan,
memberikan nama dan nomor file.
3. Kontrol XRD yang berada pada komputer dijalankan.
4. Ditunggu sampai proses analisis (scan) selesai. Setelah proses analisis selesai,
maka diperoleh data berupa grafik dan data puncak-puncaknya.
5. Sampel diambil kembali dari sample holder setelah pengukuran selesai.
d. Karakterisasi dengan PSA
Analisis distribusi partikel (PSA) akan dilakukan dengan metode basah,
menggunakan alat FRITSCH. Analisis ini dilakukan di Laboratorium biomasa.
e. Uji konduktivitas termal
Karakterisasi ini dilakukan untuk mengetahui konduktivitas termal dari alumina yang
dihasilkan dari metode elektrolisis. Untuk tujuan ini sampel alumina sebelumnya
dicetak dengan bentuk batangan dengan ketebalan (ketinggian) 0,5 cm, kemudian
sampel ditimbang untuk mengetahui massanya. Proses pengukuran konduktivitas
42
Gambar 3.3 Rangkaian alat pengukuran konduktivitas termal.
Adapun langkah-langkah dalam pengukuran konduktivitas termal adalah:
1. Menyalakan hotplate, suhu hotplate dibuat hingga mencapai suhu stabil.
2. Meletakkan sampel alumina yang telah dicetak dan ditimbang sebelumnya di atas
hotplate.
3. Sampel dibiarkan di atas hotplate selama 1 menit kemudian suhu pada permukaan
hot plate (posisi 1) dan suhu pada permukaan sampel diukur (posisi 2). Dari
pengukuran ini selisih suhu (dT) dapat dihitung yakni suhu pada posisi1-suhu pada
posisi awal. Pengukuran dilakukan dengan tiga kali pengulangan.
4. Melakukan perhitungan luas permukaan sampel alumina yang telah dicetak.
5. Memasukkan nilai dari masing-masing besaran ke dalam persamaan (3), maka
V.KESIMPULAN DAN SARAN
A.Kesimpulan
Dari penelitian yang telah dilakukan diperoleh kesimpulan sebagai berikut:
1. Metode elektrokimia dapat digunakan untuk menghasilkan alumina langsung dari logam aluminium.
2. Hasil penelitin menunjukkan bahwa jumlah alumina yang diahsilkan dipengaruhi oleh pH dan potensial, dimana alumina yang paling banyak dihasilkan dari percobaan dengan pH 4 dan potensial 22 volt.
3. Dari hasil karakterisasi dengan FTIR diketahui bahwa sampel hasil elektrolisis adalah alumunium hidroksida dan berubah secara bertahap hingga menjadi alumina murni pada suhu 1200 oC.
4. Hasil karakterisasi dengan XRD menunjukkan bahwa suhu sintering sangat mempengaruhi tingkat kristalinitas sampel, dimana secara bertahap -Al(OH)3 yang bersifat kristalin berubah menjadi -Alumina yang bersifat amorph (krsitalinitas rendah), kemudian menjadi α-alumina yang bersifat kristalin setelah disintering pada suhu 1200 oC.
67
6. maka ukuran partikel juga semakin besar, namun ukuran partikel cenderung menurun setelah perlakuan pada suhu 1200 oC disertai dengan perubahan bentuk partikel menjadi lebih bulat.
7. Karakterisasi konduktivitas termal menunjukkan bahwa sampel alumina yang diteliti termasuk isolator panas karena memiliki nilai k < 4,05 W/m oC.
B.Saran
DAFTAR PUSTAKA
Abdullah, M., Khairurrijal, Ahmad, R., Maruly, Liherlinah, dan Sanny, M. 2008. Sintesis Dan Karakterisasi Serbuk α-Al2O3 Skala Submikron dengan Metoda Proses Prekursor. Jurnal Nanosains & Nanoteknologi. Vol. 1, pp. 5-11.
Al-mamun, S. A., Nakajima, R., Zhu, X., Ishigaki, T. 2011. Generation of Alumina Nanoparticles by a Nanosecond Laser-Induced Liquid Plasma in Water. Chemical Science and Technology.Vol. 3, pp. 1-4.
Amira International. 2001. Alumina Technology Roadmap and Nano devices in the United States. Proceedings of the May Workshop, Baltimore, Maryland.and Son, Glasgow and London. pp. 8-9.
Araoyinbo, A.O., Noor, A.F.M., Sreekantan, S., and Aziz, A. 2010. Voltage Effect on Electrochemical Anodization of Aluminum at Ambient Temperature. International Journal of Mechanical and Materials Engineering (IJMME). Vol. 5, No. 1, pp. 53-58.
Arribart, H., and Bernadette, B.V. 2001. The Dibner Institute History of Science and Technology.
Atkins, P.W. 1999. Kimia Fisika Jilid 1 Edisi ke-4. Diterjemahkan oleh Irma I. Kartohadiprojo. Erlangga : Jakarta.
Beitollahi, A., Hosseini, H., and Sapoorlaki, H. 2010. Synthesis and characterization of Al2O3-ZrO2 nanocomposite powder by sucrose process. Journal of Material Science: Material in Electronics. Vol. 21, pp. 130-136.
Basuki, K.T., Muhadi A.W., dan Sudibyo. 2009. Pengaruh pH Dan Tegangan pada Pembuatan Serbuk Itrium dari Konsentrat Itrium Hasil Proses Pasir Senotim Dengan Elektrolisis. Seminar Nasional. Vol. 5, pp. 543-548.
Budavari, S. 2001.(Ed.), The Merck Index: An Encyclopedia of Chemical, Drugs, and Biologicals, Thirteenth Edition, Merck & Co. Inc., USA. pp. 359. Campbell, T., Kalia, R., Nakano, A., Vashishta, P., Ogata, S., and Rodgers, S
.1999. Dynamics of Oxidation of Aluminium Nanoclusters using Variable Charge Molecular-Dynamics Simulations on Parallel Computers. Physical Review Letters .Vol. 82 , No. 24, pp. 4866.
Dieter, Vollath. 2007. Plasma Synthesis of Nanoparticles Dieter KONA. Nano Consulting1. No.25, pp 39-55.
Ghababazade, R., Mirhabibi, A., Pourasad, J., Brown, A., Brydson, A., Amiri, M. J. 2007. Study of the phase composition and stability of explosive synthesis nanosized Al2O3. Journal Surface Science. Vol. 601, pp. 2864.
Halim, Abdul. 2010. Metode Sintesis Nano Partikel Alumina Menggunakan Flame Spray Pyrolysis. pp. 100-140.
Holman, J.P. 1994. Perpindahan Kalor. Jakarta: Erlangga. pp. 12-14.
Hosseini, S.A., Aligholi, N., and Salari, D. 2011. Production of γ-Al2O3 from Kaolin. Open Journal of Physical Chemistry. Vol. 1, pp. 23-27.
Hudson, L. K., Misra, C., Perrotta, Anthony J., Wefers, K., and Williams, F. S. 2002. Aluminum Oxide. Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim.Vol. 10, pp. 557.
James, R.C. 2007. Introduction to X-Ray Powder Diffraction. pp. 1-9.
Jiang Li ,Yubai, P. ,Changshu, X., Qiming, G., Jingkun, G. 2006. Low Temperature Synthesis of Ultrafine α-Al2O3 Powder by a Simple Aqueous Sol–Gel Process. Ceramics International.Vol. 32, No. 5, pp. 587–591.
Kagaku, S., Shinji, F., Yasuaki, T., Hajime, M., Norifumi, A., Yoshiaki, T., Sumitomo. 2007. Synthesis and Properties of Thermostable -Alumina Prepared by Hydrolysis of Phosphide Aluminum. Chemical Co., Ltd. Vol. 1, pp. 1-7.
Kim, Y., Changmook, K., Pil, K., and Jongheop,Y. 2005. Effect of preparation conditions on the phase transformation of mesoporous alumina. Journal of Non-Crystaline Solids. Vol. 351, pp. 550-556.
Knozinger, H., Ratnasamy, and Catal, P.1978. Pulse Electric Current Sintering and Strength of Sintered Alu-mina Using -Alumina Powders Prepared by the Sol-Gel Method. Journal of Science Enggenering. Vol. 17, pp. 31.
Latifah, R., Markus, D., dan Arif, H. 2012. The Influence of Ag in the Film Latex-Extracted of Jatropha of Multifida to the Cristalinity and Conductivity. Jurnal Sains dan Materi Indonesia. Vol. 9, pp. 175-179.
Matori, K.A., Loy, C.W., Manshor, H., Ismayadi, I., and Hafiz, M.Z. 2012. Phase Transformations of α-Alumina Made from Waste Alumunium via a Precipitation Technique. International Journal of Molecular Sciences. Vol. 13, pp. 16812-16821.
McColm, I.C. and Clark, N.J. 1988. High-Performance Ceramics. Blackie. McMullan, D. 2006. Scanning Electron Microscopy. Vol. 17, No. 3, pp. 175. Middleton,W. 1999. Energy-Dispersive. X-Ray Icroanalysis. Noran Instruments
2551 West Beltline Highway. pp. 2-3.
Mirjalili, F., Hasmaliza, M., Luqman, C. 2011. Preparation of Nano Scale α-Al2O3 Powder by the Sol Gel Method. Ceramics Silikaty. Vol. 55, No. 4, pp. 378-383.
Natter, H., and Happelmann, R. 2003. Tailor-Made Nanomaterial Designed by Electrochemical Methods. Electrochemica Acta. Vol. 49, pp. 51-61. Nur, A., Martasari, D.L., Desy, N., Samsudin. A., Arief, W., dan Setyawan, H.
2013. Sintesis Hydroxyapatite Berukuran Nano Dengan metode Elektrokimia yang Dibantu EDTA. Jurnal Teknik Kimia Indonesia.Vol. 11, No. 4.
Okamasa, T., Lee, G., Suzuki, Y., Kasagi, N., and Matsuda, S. 2006. New way to spinnable sols derived from modified aluminium alkoxides. Journal Micromech Microeng. Vol. 16, pp. 198-205.
Orifine, R.L. and Vasconceler, M.R. 2006. Sol Gel Transition and Structural Evolution on Multicomponent Gels Derived from the Alumina Silica System. Journal Sol Gel Science Technology. Vol. 216, pp. 111-115. Pandiangan, T. β006. Analisa Kestabilan Termal Membran -Al2O3 dan Matriks
α-Al2O3 untuk Pemisahan Gas H2. Prosiding PPI-PDIPTN, Pustek Akselerator dan Proses Bahan. Vol. 8, pp. 111-115.
Perry, R.H. 1984. Chemical Engineers Handbook, 6th ed. McGraw-Hill, New York. pp. 23.
Peter, N. 2002. Evolution of Alpha Phase Alumina in Agglomerates upon Addition to Cryolitic Melts. Norwegian University of Science and Technology Department of Materials Technology and Electrochemistry. pp 4-6. Randall. 1991. Engineered Materials Handbook, ed. By Samuel J. Schneider, Jr.
ASM International Handbook Committe, USA. Vol. 4 hal 97-99. Ristic, M.M. 1989. New Development-Sintering. Elsevier Publishing. Netherland.
Vol. 4, pp. 3-7.
Robert, E. 2005. Properties of Materials. New York : Oxford University Press.
Roco, M.C., Bainbridge, and William, S. 2001. Societal Implications of Nanoscience and Nanotechnology, NSET Workshop Report, National Science Foundation, Virginia.
Rogajan, R., Andronescu E., Cristina G., Ştefan, S. 2011. Synthesis And Characterization Of Alumina Nano-Powder Obtained By Sol-Gel Method. VASILE4 U.P.B. Science Bulletin. Vol. 73, Iss. 2.
Satterfield, C. N. Heterogeneous Catalysis in Practice; McGraw-Hill: New York, 1980; Section 4.5.(4) Gates, B. C. Journal ofChemical. 1995, 95, 511. Scintag. 1999. Basic XRD. Vol. 8, pp. 5-8.
Siegel, R. W. (WTEC Panel Chair, Evelyn Hu and Roco, M.C. 1998. R&D Status and Trends in Nanoparticles, Nanostructured Materials, Guozhong Cao, 2004. Nanostructures & Nanomaterials: Synthesis, Properties, & Applications, Imperial College Press. USA
Smallman, R.E and Bishop R.J .2000. Metalurgi Fisika Modern Dan Rekayasa Material, Edisi Keenam (trjmhan Djaprie).Jakarta: Erlangga. pp 221. Smith, R.L., Rohjet, G.S., Perrota, A.J. 2001. Influence of Diaspore Seeding and
Chloride Concentration on the Transformation of Diasporic Precursors to Corundum. Journal American Ceramic Society. Vol. 84, pp. 1896-1902.
The International Aluminium Institute. 2000. Bayer Process Chemistry. New Zealand House: Haymarket. pp. 4-5.
Tijburg, I.I.M., Bruin, H.D., Elberse, P.A., and Geus, J.W. 2000. Sintering Of Pseudo-Boehmite and -Alumina. Journal of Materrial Science. Vol. 26. pp. 5945-5949.
Tikkanen J., Gross K.A., Berndt C.C., Pitkanen V., Keskinen J., Raghu S., Rajala M., and Karthikeyan J. 1997. Characteristics of the liquid flame spray process. Surface Coating Technology. Vol. 90, pp. 210–216.
Tok, A.I.Y., Boey, F.Y.C., and Zhao, X.L. 2006. Novel Synthesis of Al2O3 Nano-Particles by Flame Spray Pyrolysis. Journal of Materials Processing Technology.Vol. 178, pp. 270–273.
Ueda, W., Sadakane, M., and Ogihara, H. 2008. Nano Strusturing of Complex Metal Oxides for Catalytic Oxidation. Catalysis Today. Vol. 132 pp. 2-8.
U.S. Geological Survey. 2013. Mineral Commodity Summaries Bauxites and Alumina.
Utama, J. A. 2009. Spektroskopi Infra Merah. Pelatihan Olimpiade Astronomi. Fakultas Keguruan dan Ilmu Pendidikan. UPI. Bandung. Pp. 1-3.
Van, H.H. 2007. Nano Materials in Nanotechnology Aerospace Applications. pp. 3-4. Educational Note. RTO-EN-AVT-129bis, pp 3. Neuilly-sur-Seine, France: RTO.
Van Zyl , A., Thackeray M.M., and Duncan G.K., Kingon A.I. 1993. The Synthesis of Beta Alumina Hydroxyde And Oxyhydroxide Precursors. Material Reset Bulletin. Vol. 28, No. 2, pp. 145-157.
Vieira, A.C., Rocha, G.A., Souza, S.P., Souza, S.H., and Kiyohara, P.K. 2008. Specific Surface Area and Structure of Alumina from Fribillar Pseudoboehmite. Revista Material. Vol. 13, pp. 329-341.
Vollat, Dieter. 2008. Nanomaterials: An Introduction to Synthesis, Properties, and Application. Environmental Engineering and Mangement Journal. Vol.7, No.6, pp. 865-870.
Warren, E., 1996. X-Ray Diffraction. Addittion-wesley pub: Messach ssetfs. Wei, M., Dan, Z., and Kwang, L.C. 2006. Novel Synthesis of α-Alumina