PENENTUAN KADAR AMMONIA (NH
3TUGAS AKHIR
) PADA AIR BAKU
DAN AIR RESERVOIR WTP MINI KELAMBIR V DI PDAM
TIRTANADI SECARA SPEKTROFOTOMETRI
ANISYA ABDHA
122401061
PROGRAM STUDI D3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENENTUAN KADAR AMMONIA (NH
3TUGAS AKHIR
) PADA AIR BAKU
DAN AIR RESERVOIR WTP MINI KELAMBIR V DI PDAM
TIRTANADI SECARA SPEKTROFOTOMETRI
Diajukan untuk melengkapi tugas dan memenuhi syarat memperoleh Ahli Madya
ANISYA ABDHA 122401061
PROGRAM STUDI D3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Penentuan Kadar Ammonia (NH3
Kategori : Tugas Akhir
) Pada Air Baku Dan Air Reservoir WTP Mini Kelambir V Di PDAM Tirtanadi Secara Spektrofotometri
Nama : Anisya Abdha
Nomor Induk Mahasiswa : 122401061
Program studi : Diploma Tiga (D-3) Kimia
Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Disetujui di Medan, Juni 2015
Program Studi D-3 Kimia FMIPA USU Pembimbing, Ketua,
Dra. Emma Zaidar Nst, M.Si Dr. Rumondang Bulan, MS
NIP. 195509181987012001 NIP. 195408301985032001
Disetujui Oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENENTUAN KADAR AMMONIA (NH3) PADA AIR BAKU DAN
AIR RESERVOIR WTP MINI KELAMBIR V DI PDAM TIRTANADI SECARA SPEKTROFOTOMETRI
TUGAS AKHIR
Saya mengakui bahwa tugas akhir ini adalah hasil karya sendiri. Kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2015
PENGHARGAAN
Segala Puji dan Syukur penulis panjatkan kepada Khadirat Allah SWT, yang tiada hentinya memberikan nikmat amal, insan dan ihsan, serta semangat dan kekuatan sehingga penulis dapat menyelesaikan penyusunan Tugas Akhir ini sesuai dengan yang diharapkan dengan judul Penetapan Kadar Ammonia (NH3
Tugas akhir ini disusun berdasarkan hasil praktek kerja lapangan yang dilaksanakan di PDAM Tirtanadi Provinsi Sumatera Utara pada tanggal 26 Januari sampai 26 Februari 2015. Tugas Akhir ini disusun untuk melengkapi dan memnuhi syarat kelulusan dalam meraih gelar Ahli Madya di Program Studi D-3 Kimia, Departemen Kimia, Fakultas Matematika Dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara. Dalam penyusunan tugas akhir ini penulis banyak menemukan kendala. Namun berkat bantuan, bimbingan dan dukungan dari berbagai pihak, akhirnya penulis dapat mengatasi berbagai kendala tersebut dengan baik.
) Pada Air Baku Dan Air Reservoir WTP Mini Kelambir V Di PDAM Tirtanadi Secara Spektrofotometri.
Maka pada kesempatan ini dengan segala ketulusan dan kerendahan hati, penulis mengucapkan terima kasih kepada :
1. Teristimewa kepada kedua orang tua penulis, Ayahanda Abdul Muin dan Ibunda Khadijah yang telah memberikan bantuan moril dan materil serta doa restu demi kesuksesan penulis.
2. Bapak Dr. Sutarman, M.Sc selaku Dekan FMIPA USU.
3. Ibu Dr. Rumondang Bulan, MS, selaku Ketua Departemen Kimia
FMIPA USU dan dosen pembimbing yang telah memberikan bimbingan dan arahan dalam penulisan Tugas Akhir ini.
4. Ibu Dra. Emma Zaidar Nst, M.Si, selaku Ketua Program Studi D-3 Kimia FMIPA USU.
6. Ibu Siti Zainab S.T, selaku Kepala Bagian Laboratorium PDAM Tirtanadi Provinsi Sumatera Utara yang telah membimbing penulis dalam melaksanakan praktek kerja lapangan.
7. Seluruh staff dan analis Laboratorium PDAM Tirtanadi Provinsi Sumatera Utara.
8. Para staff pengajar dan pegawai Kimia FMIPA USU.
9. Sahabat penulis, Amelia Syahfitri, Sri Wulandari, Ika Puteri K Amanda, Jauharia, Debi Anggreini yang selalu memberikan dukungan dan perhatian.
10.Teman-teman seperjuangan D-3 Kimia stambuk 2012 dan seluruh pihak yang tidak dapat penulis sebutkan satu persatu yang turut andil dalam membantu penulis sehingga selesainya tugas akhir ini.
Medan, Juni 2015
PENENTUAN KADAR AMMONIA (NH3) PADA AIR BAKU DAN AIR RESERVOIR WTP MINI KELAMBIR V DI PDAM TIRTANADI
SECARA SPEKTROFOTOMETRI
ABSTRAK
Penentuan kadar Ammonia (NH3) pada air baku dan air reservoir WTP Mini Kelambir Lima di PDAM Tirtanadi telah dilakukan secara spektrofotometri. Penentuan ini dimaksudkan untuk mengetahui kadar ammonia pada air baku dan air reservoir yang sesuai dengan standar kualitas air. Penentuan kadar ammonia pada air baku dan air reservoir WTP Mini Kelambir Lima dilakukan dengan terlebih dahulu ditambahkan Mineral Stabilizer, Polivynil Alkohol Dispersing Agent dan reagen Nessler. Kadar ammonia diukur pada λ 425 nm dengan menggunakan spektrofotometer DR 2010. Hasil pemeriksaan kadar ammonia pada air baku dan air reservoir adalah 0,573 mg/L pada air baku dan 0,020 pada air reservoir. Kadar ammonia pada air baku telah melebihi ambang batas standart kualitas air berdasarkan Peraturan Pemerintah Republik Indonesia No.82 Tgl 14 Desember 2001 tentang Air Baku Mutu Kelas I yaitu 0,5 mg/L, sehingga air baku WTP Mini Kelambir V harus dilakukan pengolahan lebih lanjut agar dapat dikonsumsi. Sedangkan kadar ammonia pada pada air reservoir masih memenuhi standart Permenkes No. 492/Menkes/Per/IV/2010 Tanggal 19 April 2010 tentang syarat kualitas air minum yaitu 1,5 mg/L sehingga dapat dikonsumsi sebagai air minum.
DETERMINATION OF AMMONIA (NH3
ABSTRACT
) RATE IN RAW WATER AND RESERVOIR WATER OF WTP MINI KELAMBIR V AT PDAM
TIRTANADI BY SPECTROPHOTOMETRY
Determination of Ammonia (NH3
Key Words: Ammonia, Spectrophotometry, Raw water, Reservoir water
) rate in raw water and reservoir water WTP Mini Kelambir V at PDAM Tirtanadi by spectrophotometry has been. Determination is intended to determine levels of ammonia in the raw water and reservoir water are in accordance with the water quality standards. Determination of ammonia in the raw water and reservoir water WTP Mini Kelambir V performed by first added Mineral Stabilizer, Polivynil Alcohol Dispersing Agent
and Nessler reagent. Measuring ammonia rate of λ 425 nm with
DAFTAR ISI
DAFTAR LAMPIRAN xi
BAB 1 PENDAHULUAN 1
1.1. Latar Belakang 1
1.2. Perumusan Masalah 2
1.3. Tujuan 3
1.4. Manfaat 3
1.5. Lokasi Penelitian 3
BAB 2 TINJAUAN PUSTAKA 4
2.5. Pembagian Air Berdasarkan Analisis 10
2.6. Karakteristik Air 11
2.6.1. Karakteristik Fisika Air 11
2.6.2. Karakteristik Kimia Air 12
2.6.3. Karakteristik Biologis Air 16
2.7. Pencemaran Air 17
2.7.1. Indikator Pencemaran Air 18
2.8. Proses Pengolahan Air 20
2.9. Ammonia 20
2.10. Metode Penentuan Ammonia 21
2.10.1. Metode Penentuan Ammonia Dengan Titrasi 24
2.10.2. Metode Penentuan Ammonia Dengan Menggunakan
Elektroda 24
2.10.3. Metode Penentuan Ammonia Dengan Spektrofotometer 24
2.11. Spektrofotometer 25
2.11.1. Komponen Spektrofotometer 26
BAB 3 METODOLOGI PENELITIAN 28
3.1. Alat-alat 28
3.2. Bahan-bahan 28
3.3. Prosedur Penelitian 29
BAB 4 HASIL DAN PEMBAHASAN 31
4.1. Hasil 31
4.1.1. Data Analisa 31
4.2. Perhitungan 31
4.2.1. Penentuan Persamaaan Garis Regresi 31
4.2.2. Penentuan Koefisien Korelasi 32
4.2.3. Grafik Linearitas Parameter Uji Ammonia 33
4.2.4. Perhitungan Konsentrasi Ammonia 33
4.3. Pembahasan 34
BAB 5 KESIMPULAN DAN SARAN 35
5.1. Kesimpulan 35
5.2. Saran 35
DAFTAR PUSTAKA 36
DAFTAR TABEL
halaman
Tabel 4.1. Data Pemeriksaan Penentuan Ammonia 31
Tabel 4.2. Penentuan Persamaan Garis Regresi 31
DAFTAR GAMBAR
halaman
Gambar 2.1. Struktur Molekul Air 4
Gambar 2.2. Reaksi Penguraian Air 8
Gambar 2.3. Reaksi Nitrifikasi Menjadi Nitrit 21
Gambar 2.4. Reaksi Nitrifikasi Menjadi Nitrat 21
Gambar 2.5. Reaksi Amonifikasi 22
Gambar 2.6. Reaksi Kesetimbangan Ammonia Dan Ammonium 23
Gambar 2.7. Skematik Spektrofotometer 27
Gambar 4.1. Grafik Linearitas Parameter Uji Ammonia ( DR 2010) 33
Gambar L.1. Reagen Mineral Stabilizer 38
Gambar L.2. Reagen Polivynil Alcohol Dispersing Agent 38
Gambar L.3. Reagen Nessler 38
DAFTAR LAMPIRAN
halaman
Lampiran 1 Alat dan Bahan yang Diperlukan Dalam Penentuan
Kadar Ammonia 38
Lampiran 2 Peraturan Pemerintah Republik Indonesia No.82
Tanggal 14 Desember 2001 tentang Air Baku Mutu Kelas I 39
PENENTUAN KADAR AMMONIA (NH3) PADA AIR BAKU DAN AIR RESERVOIR WTP MINI KELAMBIR V DI PDAM TIRTANADI
SECARA SPEKTROFOTOMETRI
ABSTRAK
Penentuan kadar Ammonia (NH3) pada air baku dan air reservoir WTP Mini Kelambir Lima di PDAM Tirtanadi telah dilakukan secara spektrofotometri. Penentuan ini dimaksudkan untuk mengetahui kadar ammonia pada air baku dan air reservoir yang sesuai dengan standar kualitas air. Penentuan kadar ammonia pada air baku dan air reservoir WTP Mini Kelambir Lima dilakukan dengan terlebih dahulu ditambahkan Mineral Stabilizer, Polivynil Alkohol Dispersing Agent dan reagen Nessler. Kadar ammonia diukur pada λ 425 nm dengan menggunakan spektrofotometer DR 2010. Hasil pemeriksaan kadar ammonia pada air baku dan air reservoir adalah 0,573 mg/L pada air baku dan 0,020 pada air reservoir. Kadar ammonia pada air baku telah melebihi ambang batas standart kualitas air berdasarkan Peraturan Pemerintah Republik Indonesia No.82 Tgl 14 Desember 2001 tentang Air Baku Mutu Kelas I yaitu 0,5 mg/L, sehingga air baku WTP Mini Kelambir V harus dilakukan pengolahan lebih lanjut agar dapat dikonsumsi. Sedangkan kadar ammonia pada pada air reservoir masih memenuhi standart Permenkes No. 492/Menkes/Per/IV/2010 Tanggal 19 April 2010 tentang syarat kualitas air minum yaitu 1,5 mg/L sehingga dapat dikonsumsi sebagai air minum.
DETERMINATION OF AMMONIA (NH3
ABSTRACT
) RATE IN RAW WATER AND RESERVOIR WATER OF WTP MINI KELAMBIR V AT PDAM
TIRTANADI BY SPECTROPHOTOMETRY
Determination of Ammonia (NH3
Key Words: Ammonia, Spectrophotometry, Raw water, Reservoir water
) rate in raw water and reservoir water WTP Mini Kelambir V at PDAM Tirtanadi by spectrophotometry has been. Determination is intended to determine levels of ammonia in the raw water and reservoir water are in accordance with the water quality standards. Determination of ammonia in the raw water and reservoir water WTP Mini Kelambir V performed by first added Mineral Stabilizer, Polivynil Alcohol Dispersing Agent
and Nessler reagent. Measuring ammonia rate of λ 425 nm with
BAB 1 PENDAHULUAN
1.1. Latar Belakang
Air merupakan zat yang paling penting dalam kehidupan setelah udara. Sekitar
tiga per empat bagian dari tubuh kita terdiri dari air dan tidak seorang pun yang
dapat bertahan hidup lebih dari 4-5 hari tanpa air. Selain itu air juga dipergunakan
untuk memasak, mencuci, mandi dan membersihkan kotoran yang ada disekitar
rumah. Air juga digunakan untuk keperluan industri, pertanian, pemadam
kebakaran, tempat rekreasi, transportasi dan lain-lain (Chandra, 2007).
Air merupakan suatu sarana utama untuk meningkatkan derajat kesehatan
masyarakat, karena air merupakan salah satu media dari berbagai macam
penularan penyakit. Melalui penyediaan air bersih baik dari segi kualitas dan
kuantitasnya di suatu daerah, maka penyebaran penyakit ini dapat ditekan
seminimal mungkin ( Sutrisno, 2004).
Pengelolaan sumber daya air sangat penting, agar dapat dimanfaatkan secara
berkelanjutan dengan tingkat mutu yang di inginkan. Salah satu langkah
pengelolaan yang dilakukan adalah adanya pemantauan dan interpretasi data
kualitas air, mencakup kualitas fisika, kimia, biologi. Namun, sebelum melangkah
pada tahap pengelolaan, diperlukan pemahaman yang baik tentang terminologi,
karakteristik, interkoneksi parameter-parameter kualitas air ( Effendi, 2003 ).
Mengingat air banyak digunakan manusia untuk tujuan bermacam-macam
terhadap lingkungan terutama terhadap air. Salah satu unsur pencemar air adalah
adanya Nitrogen yang berasal dari penggunaan pupuk nitrogen dalam bidang
pertanian serta 78% dari atmosfer yang apabila hujan maka akan terbentuk
ammonia dan ammonium yang terbawa air hujan ke permukaan tanah ( Darmono,
2001).
Ammonia merupakan ion yang terdapat di perairan dalam jumlah sedikit
(Minor Ion ) dan garam-garamnya bersifat mudah larut dalam air ( Effendi, 2003).
Ammonia dalam air akan diubah menjadi nitrat dan nitrit. Jika kandungan
dari Ammonia ini baik nitrat ataupun nitrit melebihi ambang batas maka akan
berbahaya untuk diminum dan juga dapat mengakibatkan wajah membiru bahkan
kematian ( Kristanto, 2004).
Dari penjelasan di atas maka penulis tertarik untuk membuat tugas akhir
dengan judul Penentuan Kadar Ammonia Pada Air Baku Dan Air Reservoir
WTP Mini Kelambir V Di PDAM Tirtanadi Secara Spektrofotometri
sehingga dapat mengetahui kadar Ammonia pada air Baku dan air reservoir WTP
Mini Kelambir V yang sesuai denganPeraturan Pemerintah Republik Indonesia
No.82 Tgl 14 Desember 2001 tentang Air Baku Mutu Kelas I dan Permenkes No.
492/Menkes/Per/IV/2010 Tanggal 19 April 2010 tentang syarat kualitas air
minum.
1.2. Perumusan Masalah
Apakah kadar ammonia pada air baku dan air reservoir WTP Mini Kelambir V
telah memenuhi Peraturan Pemerintah Republik Indonesia No.82 Tgl 14
492/Menkes/Per/IV/2010 Tanggal 19 April 2010 tentang syarat kualitas air
minum.
1.3. Tujuan
Untuk mengetahui kadar ammonia pada air baku dan air reservoir WTP Mini
Kelambir V dengan standar mutu air berdasarkan Peraturan Pemerintah Republik
Indonesia No.82 Tgl 14 Desember 2001 tentang Air Baku Mutu Kelas I dan
Permenkes No. 492/Menkes/Per/IV/2010 Tanggal 19 April 2010 tentang syarat
kualitas air minum.
1.4. Manfaat
Adapun manfaat penulisan tugas akhir ini adalah :
1. Untuk memberikan informasi kepada pembaca tentang hasil penentuan
kadar ammonia pada air baku dan air reservoir WTP Mini Kelambir V
2. Untuk mengetahui kadar ammonia dalam air baku dan air reservoir WTP
Mini Kelambir V telah memenuhi standart kualitas air berdasarkan
Peraturan Pemerintah Republik Indonesia No.82 Tgl 14 Desember 2001
tentang Air Baku Mutu Kelas I dan Permenkes No.
492/Menkes/Per/IV/2010 Tanggal 19 April 2010 tentang syarat kualitas air
minum.
1.5. Lokasi Penelitian
Dalam penyusunan Tugas Akhir ini penulis memperoleh data yang dibutuhkan
mengenai penentuan kadar ammonia pada air baku dan air reservoir WTP Mini
BAB 2
TINJAUAN PUSTAKA
2.1. Air
Air merupakan suatu senyawa yang terdiri dari hidrogen dan oksigen dengan
rumus kimia H2
Chang (2003) mengemukakan bahwa air merupakan pelarut yang sangat
baik untuk berbagai senyawa ionik dan untuk berbagai zat lain yang mampu
membentuk ikatan hidrogen. Untuk memahami tentang air maka perlu mengkaji
struktur elektron molekul H
O ( Dumairy, 1992).
2O. Seperti yang terlihat dibawah ini :
Walaupun banyak senyawa yang mampu membentuk ikatan hidrogen
antarmolekul, perbedaan antara H2O dan molekul polar yang lain seperti NH3
Air merupakan sumber daya alam yang diperlukan untuk hajat hidup orang
banyak, bahkan oleh semua mahluk hidup. Oleh karena itu, sumber daya air harus
dilindungi agar tetap dimanfaatkan dengan baik oleh manusia serta mahluk hidup
yang lain ( Effendi, 2003).
dan
HF adalah bahwa setiap atom oksigen dapat membentuk dua ikatan hidrogen,
sama dengan jumlah pasangan elektron bebas pada atom oksigen. :O:
H H
Air merupakan kebutuhan yang tidak dapat ditinggalkan bagi kehidupan manusia,
karena air diperlukan untuk kebutuhan bermacam-macam kegiatan seperti minum,
pertanian dan industri. Air dapat diminum adalah air yang bebas dari bakteri
berbahaya. Air minum harus bersih dan jernih, tidak berbau dan tidak berwarna
serta tidak mengandung bahan tersuspensi atau kekeruhan. Manusia sejak dahulu
kala sudah menyadari betapa pentingnya air. Secara global tubuh manusia dewasa
mengandung air sebanyak 50-70% dari bobot tubuhnya. Bila tubuh kehilangan air
sebanya 15% dari bobot tubuhnya maka akan mengakibatkan kematian
2.1.1. Air Baku
2.1.1.1 Defenisi Air Baku
Sumber air baku memegang peranan yang sangat penting dalam industri air
minum. Air baku atau raw water merupakan awal dari suatu proses dalam
penyediaan dan pengolahan air bersih. Defenisi air baku adalah “Air yang berasal
dari sumber air pemukaan, cekungan air tanah dan atau air hujan yang memenuhi
ketentuan baku mutu tertentu sebagai air baku untuk air minum”
Sumber air baku bisa berasal dari sungai, danau, sumur air dalam, mata air
dan bisa juga dibuat dengan cara membendung air buangan atau air laut. Evaluasi
dan pemilihan sumber air yang layak harus berdasar dari ketentuan berikut :
1. Kualitas dan kuantitas air yang diperlukan
2. Kondisi iklim
3. Tingkat kesulitan pada pembangunan intake
5. Ketersediaan biaya minimum operasional dan pemeliharaan untuk IPA
6. Kemungkinan terkontaminasinya sumber air pada masa yang akan datang
7. Kemungkinan untuk memperbesar intake pada masa yang akan datang
2.1.1.2. Karakteristik Air Baku
Penyediaan air bersih, selain kuantitasnya, kualitasnya pun harus memenuhi
standar yang berlaku. Dalam hal air bersih, sudah merupakan praktek umum
bahwa dalam menetapkan kualitas dan karakteristik dikaitkan dengan suatu baku
mutu air tertentu (standar kualitas air). Untuk memperoleh gambaran yang nyata
tentang karakteristik air baku, seringkali diperlukan pengukuran sifat-sifat air atau
biasa disebut parameter kualitas air, yang beraneka ragam. Formulasi- formulasi
yang dikemukakan dalam angka-angka standar tentu saja memerlukan penilaian
yang kritis dalam menetapkan sifat-sifat dari tiap parameter kualitas air .
Standar kualitas air adalah baku mutu yang ditetapkan berdasarkan sifat-sifat
fisik, kimia, radioaktif maupun bakteriologis yang menunjukkan persyaratan
kualitas air tersebut. Peraturan Pemerintah Republik Indonesia No. 82 Tahun 2001
Tentang Pengelolaan Kualitas Air Dan Pengendalian Pencemaran Air, air menurut
kegunaannya digolongkan menjadi :
Kelas I : Air yang peruntukannya dapat digunakan untuk air baku air minum atau
peruntukan lain yang mempersyaratkan mutu air yang sama dengan kegunaan
tersebut.
Kelas II : Air yang peruntukannya dapat digunakan untuk prasarana/sarana
pertanaman atau peruntukan lain yang mempersyaratkan mutu air yang sama
dengan kegunaan tersebut.
Kelas III : Air yang peruntukannya dapat digunakan untuk pembudidayaan ikan
air tawar, peternakan, air untuk mengairi pertanaman atau peruntukan lain yang
mempersyaratkan mutu air yang sama dengan kegunaan tersebut
2.1.2. Air Reservoir
Air reservoir adalah air yang telah melalui filter sudah dapat dipakai untuk air
minum. Air tersebut telah bersih dan bebas dari bakteriologis dan ditampung pada
bak reservoir untuk diteruskan pada konsumen ( Sutrisno, 2004).
2.2. Golongan Air
Peraturan pemerintah No. 20 tahun 1990 mengelompokkan kualitas air menjadi
beberapa golongan menurut peruntukannya. Adapun penggolongan air menurut
peruntukannya adalah sebagai berikut :
a) Golungan A, yaitu air yang dapat digunakan sebagai air minum secara
langsung, tanpa pengolahan terlebih dahulu.
b) Golongan B, yaitu air yang dapat digunakan sebagai air baku air minum.
c) Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan dan
peternakan.
d) Golongan D, yaitu air yang dapat digunakan untuk keperluan pertanian, usaha
2.3. Sifat Umum Air
Gabriel (2011) mengemukakan tentang sifat umum air yaitu :
1. Sifat Fisik
c. Massa jenis air (0
3
o
C) 1,00 gr/cm
d. Panas lebur 80 kal/gram
3
e. Titik didih 100o
f. Panas penguapan 540 kal/gram C
g. Temperatur kritis 347 atm
h. Konduktivitas listrik spesifik (25oC) 1x10-17
i. Konstantya dielektrik (25
/ ohm-cm
o
2. Sifat Kimia
C)
Sifat kimia dari air adalah sebagai berikut :
a. air dapat terurai oleh pengaruh arus listrik dengan reaksi dibawah ini :
H2O → H+ + OH
Gambar 2.2. Reaksi Penguraian Air -
b. air merupakan pelarut yang baik
c. air dapat bereaksi dengan asam kuat dan basa kuat
d. air bereaksi dengan berbaga subtansi membentuk senyawa padat dimana
2.4. Sumber - sumber Air
Air yang berada di permukaan bumi ini dapat berasal dari berbagai sumber.
Berdasarkan letak sumbernya, air dapat dibagi menjadi air angkasa (hujan), air
permukaan dan air tanah.
1. Air angkasa (hujan)
Air angkasa atau air hujan merupakan sumber utama air di bumi. Walau pada
saat presipitasi merupakan air yang paling bersih, air tersebut cenderung
mengalami pencemaran ketika berada di atmosfer. Pencemaran yang terjadi
langsung di atmosfer itu dapat disebabkan oleh partikel debu, mikroorganisme
dan gas. Misalnya karbon dioksida, nitrogen dan ammonia.
2. Air permukaan
Air permukaan meliputi badan-badan air semacam sungai, danau, telaga,
waduk, rawa, air terjun dan sumur permukaan. Sebagian besar berasal dari hujan
yang jatuh ke permukaan bumi. Air hujan tersebut kemudian akan mengalami
pencemaran baik oleh tanah, sampah, maupun yang lainnya.
Air permukaan merupakan salah satu sumber penting bahan baku air bersih.
Faktor-faktor yang harus diperhatikan, antara lain :
a. Mutu atau kualitas baku
b. Jumlah atau kuantitasnya
c. Kontinuitasnya
Dibandingkan dengan sumber air yang lain, air permukaan merupakan sumber air
3. Air tanah
Air tanah (ground water) berasal dari air hujan yang jatuh ke permukaan
bumi yang kemudian mengalami perkolasi atau penyerapan kedalam tanah dan
mengalami proses filtrasi secara alamiah. Proses-proses yang telah dialami oleh
air hujan tersebut, didalam perjalanannya kebawah tanah, membuat air tanah
menjadi lebih baik dan lebih murni dibandingkan air permukaan.
Air tanah memiliki beberapa kelebihan dibanding sumber air yang lain. Pertama,
air tanah biasanya terbebas dari kuman penyakitdan tidak perlu mengalami proses
purifikasi atau penjernihan. Persediaan air tanah juga cukup tersedia sepanjang
tahun, saat musim kemarau sekalipun. Sementara itu air tanah juga memiliki
beberapa kerugian atau kelemahan dibanding sumber air lainnya. Air tanah
mengandung zat-zat mineral dalam konsentrai yang tinggi. Konsentrasi yang
tinggi dari zat-zat mineral semacam magnesium, kalsium, dan logam berat seperti
besi dapat mengakibatkan kesadahan air. Akibatnya apabila menggunakan air
sadah untuk mencuci, sabun tidak akan berbusa dan bila diendapkan akan
terbentuk endapan semacam perak. Selain itu untuk menghisap dan mengalirkan
air ke atas permukaan diperlukan pompa (Chandra, 2007).
2.5. Pembagian Air Berdasarkan Analisis
Berdasarkan analisis air maka air digolongkan menjadi 3 (tiga), yaitu:
1. Air kotor/air tercemar
Air yang bercampur dengan satu atau berbagai campuran hasil buangan
disebut air kotor/tercemar.
2. Air bersih
Air yang sudah terpenuhi syarat fisik, kimia, namun bakteriologinya belum
terpenuhi. Air bersih ini diperoleh dari sumur gali, sumur bor, air hujan, air
sumber yang dari mata air.
3. Air minum
Air minum ialah air yang sudah terpenuhi sifat fisik, kimia, maupun
bakteriologi serta level kontaminasi maksimum (LKM). Level kontaminasi
maksimum meliputi kekeruhan, kandungan zat kimia organik atau anorganik,
dan jumlah bakteri coliform ( Gabriel, 2001).
2.6. Karakteristik Air
Air memiliki karakteristik fisika, kimia dan biologis yang sangat mempengaruhi
kualitas air tersebut. Oleh sebab itu, pengolahan air mengacu kepada beberapa
parameter guna memperoleh air yang layak digunakan.
2.6.1. Karateristik Fisika Air
Karakter fisik air ialah karakter pada air yang dapat terlihat langsung melalui fisik
air tanpa harus melakukan pengamatan yang lebih jauh pada air tersebut.
Karakteristik fisik air meliputi:
1. Kekeruhan
Kekeruhan dapat ditimbulkan oleh adanya bahan-bahan anorganik dan organik
yang terkandung dalam air seperti lumpur dan bahan yang dihasilkan oleh
2. Temperatur
Temperatur dalam air merupakan hal penting dalam kaitannya dengan tujuan
penggunaan, pengolahan untuk menghilangkan bahan-bahan pencemar.
3. Warna
Air murni tidak berwarna. Warna didalam air diakibatkan oleh adanya
material yang larut. Air yang mengalir melewati rawa atau tanah yang
mengandung mineral dimungkinkan untuk mengambil warna material
tersebut.
4. Bau dan rasa
Air murni tidak berbau dan berasa. Rasa dalam air biasanya diakibatkan oleh
garam-garam terlarut. Bau dan rasa pada air terjadi karena kehadiran
mikroorganisme, bahan mineral, dan bahan-bahan organik ( Suripin, 2002).
2.6.2. Karakteristik Kimia Air
Karakteristik kimia air meliputi banyaknya senyawa kimia yang terdapat di dalam
air, sebagian diantaranya berasal dari alam secara alamiah dan sebagian lagi
sebagai kontribusi aktivitas makhluk hidup. Karakteristik kimia air meliputi:
1. pH
Pembatasan pH dilakukan karena akan mempengaruhi rasa, korosifitas air,
dan efisiensi klorinasi. Beberapa senyawa asam dan basa lebih toksik dalam
bentuk molekuler, dimana disosiasi senyawa-senyawa tersebut dipengaruhi
2. DO (Dissolved Oxigen)
DO adalah jumlah oksigen terlarut yang berasal dari fotosintesa dan absorbsi
atmosfer/udara. Semakin banyak jumlah DO maka kualitas air semakin baik.
3. BOD (Biological Oxigen Demand)
BOD adalah banyaknya oksigen yang dibutuhkan oleh mikroorganisme untuk
menguraikan bahan-bahan organik (zat pencerna) yang terdapat di dalam air
secara biologi.
4. COD (Chemical Oxigen Demand)
COD adalah banyaknya oksigen yang dibutuhkan untuk mengoksidasi
bahan-bahan organik secara kimia.
5. Kesadahan
Kesadahan air yang tinggi akan mempersulit efektifitas pemakaian sabun,
namun sebaliknya dapat memberikan rasa yang segar. Di dalam pemakaian
untuk industri (air ketel, air pendingin, atau pemanas) adanya kesadahan
dalam air tidaklah dikehendaki. Kesadahan yang tinggi bisa disebabkan oleh
adanya kadar residu terlarut yang tinggi dalam air.
6. Senyawa-senyawa kimia yang bersifat racun didalam air
Zat-zat kimia yang larut dalam air yang dapat mengganggu bahkan
membahayakan bagi kesehatan manusia antara lain :
1. Arsen
Kadar maksimum yang masih diperbolehkan dalam air 0,05 mg/l.
Dikenal sebagai racun, bersifat karsinogenik dengan melalui kontak
2. Barium
Kadar maksimum yang masih diperbolehkan dalam air 1,5 mg/l. Dikenal
sebagai bahan kimia yang bersifat toksis terhadap hati, aliran darah dan
nervous.
3. Cadmium
Kadar maksimum yang masih diperbolehkan dalam air 0,01 mg/l.
Sebagai racun yang akut bagi manusia melalui makanan
4. Chromium
Kadar maksimum yang masih diperbolehkan dalam air 0,05 mg/l.
Bersifat karsinogenik pada pernafasan. Bersifat kumulatif dalam daging
tikus pada kadar mg/l.
5. Lead (timah hitam )
Kadar maksimum yang diperbolehkan dalam air 0,05 mg/l. Dikenal
sebagai racun melalui makanan, air, udara dan menghisap rokok.
6. Merkuri
Kadar maksimum yang diperbolehkan dalam air 0,002 mg/l. Dikenal
sebagai racun pada pekerja dan ikan. Terdapat didalam air kurang dari 1
mg/l. Terdapat di makanan 10-70.
7. Nitrat
Kadar maksimum yang diperbolehkan dalam air minum 10 mg/l. Air
sumur dengan kandungan 15-250 mg/l menyebabkan methemogloinemia
8. Selenium
Kadar maksimum yang masih diperbolehkan dalam air minum 0,01
mg/l. Dikenal sebagai racun yang behubungan dengan pekerjaan. Dan
menyebabkan keracunan pada anak bila lebih dari 3-4 mg/kg makanan
masuk.
9. Silver (perak )
Kadar maksimum yang masih diperbolehkan dalam air minum 0,05 mg/l
menyebabkan penyakit argria, warna kulit yang kelabu kebiru-biruan.
10. Sulfat
Konsentrasi maksimum yang masih diperbolehkan dalam air 250 mg/l.
Menyebabkan laxative apabila kadarnya berupa maksimum dan sodium.
11. Besi
Konsentrasi maksimum yang masih diperbolehkan dalam air 0,3 mg/l.
Besi berguna untuk metabolisme. Nilai ambang rasa 2 mg/l,
menimbulkan warna, menyebabkan timbulnya koloidal yang berwarna
dalam air.
12. Tembaga
Konsentrasi yang masih diperbolehkan dalam air 1 mg/l. Penting untuk
metabolisme. Menyebabkan air mempunyai rasa tertentu. Nilai ambang
rasa 1-5 mg/l.
13. Chlorida
Konsentrasi maksimum yang diperbolehkan dalam air 250 mg/l. Kadar
yang berlebihan menyebabkan air asin rasanya. Rasa asin akan
14. Fluor
Kekurangan fluor di dala air dapat menyebabkan karies gigi, dan
kelebihan fluor menyebabkan penyakit fluoresis. Kadar di dalam air
minum 1-2 mg/l (Sutrisno, 2004).
2.6.3. Karakteristik Biologis Air
Berbagai macam organisme hidup dalam air lebih banyak ditemukan pada air
permukaan daripada air tanah, karena proses penyaringan oleh lapisan tanah.
Jenis-jenis organisme yang terdapat dalam air meliputi organisme mikroskopik
dan makroskopik.
Organisme mikroskopik seperti bakteri dan coliform dapat ditemukan
dalam air. Bakteri yang hidup di perairan umumnya uniseluler, tidak memiliki
klorofil, berkembangbiak dengan pembelahan sel secara transversal atau biner,
sebagian besar (± 80%) berbentuk batang. Secara umum hidupnya saprofitik pada
sisa buangan hewan atau tanaman yang sudah mati, ada juga yang bersifat
parasitik pada hewan dan manusia sehingga dapat menyebabkan penyakit.
Coliform tidak termasuk dalam taksonomi bakteri namun hanya istilah
untuk menyebutkan kelompok mikroorganisme yang berada di air. Pada keadaan
normal, coliform terdapat di air dalam jumlah standar dan dapat diukur, namun
bila terjadi pencemaran air, jumlah coliform akan menjadi sangat banyak dan
dapat melebihi jumlah bakteri patogen lain. Oleh karena itu, coliform dapat
digunakan sebagai indikator pencemaran air. Coliform memproduksi
bermacam-macam racun seperti indol dan skatol yang dapat menimbulkan penyakit bila
Berdasarkan Peraturan Menteri Kesehatan no. 492/MENKES/PER/2010,
coliform tidak boleh terdapat di dalam air minum. Organisme mikroskopik
lainnya seperti; jamur, alga, dan virus juga terdapat di dalam air. Jamur adalah
tanaman yang dapat tumbuh tanpa sinar matahari dan pada waktu tertentu dapat
merajalela pada pipa-pipa air, sehingga menimbulkan rasa dan bau yang tidak
enak. Sementara alga adalah tumbuhan kecil yang hidup di air yang jika dalam
jumlah yang besar dapat mempengaruhi rasa, warna, dan bau pada air.
Pertumbuhan alga yang berlebihan dapat dikontrol dengan penambahan tembaga
sulfat. Dan virus adalah mikrooganisme penyebab infeksi dan ukurannya lebih
kecil dari bakteri. Virus dalam air biasanya dikendalikan dengan klorinasi
dikombinasikan dengan proses penonaktifan virus (Suripin, 2002).
2.7. Pencemaran Air
Pencemaran air didefinisikan sebagai perubahan langsung maupun tidak langsung
terhadap keadaan air dari keadaan yang normal menjadi keadaan air yang
berbahaya atau yang berpotensi menyebabkan penyakit atau gangguan bagi
kehidupan mahluk hidup. Perubahan langsung dan tidak langsung ini dapat berupa
perubahan fisik, kimia,. termal dan biologi. Air alamiah yang terdapat pada
permukaan bumi sangat sulit ditemukan dalam keadaan murni, semuanya
mengandung bahan mineral tertentu dalam konsentrasi yang bervariasi. Namun air
tersebut tidak dikatakan langsung sebagai air tercemar. Kehadiran bahan
pencemar didalam air dalam jumlah yang tidak normal mengakibatkan air
Pencemaran air dapat merupakan masalah, regional maupun lingkungan
global dan sangat berhubungan dengan pencemaran udara serta penggunaan lahan
tanah atau daratan. Pada saat udara yang tercemar jatuh ke bumi bersama dengan
air hujan, maka air tersebut sudah tercemar. Beberapa jenis bahan kimia untuk
pupuk dan pestisida pada lahan pertanian akan terbawa oleh air dan akan
mencemari lokasi bersangkutan. Dengan demikian banyak sekali penyebab
terjadinya pencemaran air ini (Darmono, 2001).
2.7.1. Indikator Pencemar Air
Situmorang (2007) mengemukakan beberapa indikator terhadap pencemaran air
dapat diamati dengan melihat perubahan keadaan air yang meliputi :
1. Perubahan suhu air
Apabila suhu air meningkat maka kelarutan oksigen didalam air juga akan
menurun, akhirnya akan mempengaruhi kehidupan air karena berkurangnya
kadar oksigen yan dibutuhkan oleh mahluk hidup didalam air. Pengaruh
kenaikan suhu ini terhadap kehidupan air dapat dilihat pada kehidupan ikan
sebagai contoh. Apabila suhu didalam air meningkat, maka suhu tubuh ikan
juga akan naik dan mengakibatkan peningkatan laju metabolisme ikan.
Apabila pada peningkatan suhu ini akan menyebabkan penurunan kadar
oksigen, maka daya tahan ikan akan melampaui daya dukung tubuhnya untuk
bertahan hidup dan akhirnya akan mengakibatkan kematian terhadap ikan.
Air dalam keadaan normal memiliki pH 6,0-7,5. Tingkat keasaman air dapat
berubah disebabkan oleh hadirnya senyawa kimia buangan ke dalam air.
Mahluk hidup harus beradaptasi terhadap kadar keasaman, tingkat basa dan
kadar salinitas. Kemudian meningkatnya kadar basa di dalam air biasanya
tidak berasal dari aktivitas manusia secara langsung, akan tetapi berasal dari
pelapukan bahan mineral didalam tanah. Lalu salinitas air juga dapat
meningkat yang disebabkan oleh penambhan pupuk kedalam air pertanian,
kemudian dengan adanya musim kemarau akan meyebabkan kadar garam di
dalam air menjadi meningkat karena proses perubahan konsentrasi.
3. Perubahan warna, bau dan rasa pada air
Air bersih dalam keadaan normal tidak berwarna, tidak berbau dan tidak
berasa. Masuknya limbah kedalam air akan mengakibatkan perubahan warna,
bau dan rasa pada air.
4. Terbentuknya endapan dan koloid
Terbentuknya endapan dan koloid dari bahan terlarut juga merupakan
indikator pencemaran air. Bahan buangan dari industri bila tidak melarut
sempurna didalam air maka akan mengakibatkan terbentuknya koloid dan ada
pula membentuk endapan pada dasar air setelah didiamkan beberapa saat.
5. Mikroorganisme dalam air
Mikroorganisme dapat digunakan sebagai indikator tingkat pencemaran
lingkungan. Kehadiran mikroorganisme seperti bakteri patogen sangat
2.8. Proses Pengolahan Air
Dalam proses pengolahan air ini lazimnya dikenal dengan dua cara yakni :
1. Pengolahan Lengkap atau Complete Treatment Process, yaitu air yang akan
mengalami pengolahan lengkap, baik secara fisik, kimia dan bakteriologis.
a. Pengolahan Fisik, yaitu suatu tingkat pengolahan yang bertujuan untuk
mengurangi atau menghilangkan kotoran-kotoran yang kasar, penyisihan
lumpur dan pasir, serta mengurangi kadar zat-zat organik yang ada didalam
air.
b. Pengolahan kimia, yaitu suatu tingkat pengolahan dengan menggunakan zat-
zat kimia membantu proses pengolahan selanjutnya. Misalnya dengan
pembubuhan kapur dalam proses pelunakan dan sebagainya.
c. Pengolahan bakteriologis, yaitu suatu tingkat pengolahan untuk membunuh
atau memusnahkan bakteri-bakteri yang terkandung didalam air dengan cara
membubuhkan kaporit ( zat desinfektan).
2. Pengolahan sebagian atau Partial Treatment Process
Misalnya dengan diadakan pengolahan kimia atau pengolahan bakteriologis saja.
Pengolahan ini pada lazimnya dilakukan untuk: Mata air bersih dan air dari sumur
yang dalam ( Sutrisno, 2004).
2.9.Ammonia
Ammonium dan ammonia yang merupakan produk penguraian protein yang sudah
dibahas sebelumnya masuk kedalam badan sungai terutama melalui limbah
domestik. Konsentrasinya didalam sungai akan semakin berkurang bila semakin
didalam air. Mikroorganisme tersebut akan mengoksidasi ammonium menjadi
nitrit dan akhirnya menjadi nitrat.
Proses oksidasi ammonium menjadi nitrit dilakukan oleh jenis-jenis bakteri
seperti Nitrosomonas
NH4 + O2 Nitrosomonas NO2 + 2H2
Gambar 2.3. Reaksi Nitrifikasi Menjadi Nitrit O
Selanjutnya nitrit oleh aktivitas bakteri dari kelompok nitrobacter akan dioksidasi
lebih lanjut menjadi nitrat
2NO2 + O2 Nitrobacter 2NO
Gambar 2.4. Reaksi Nitrifikasi Menjadi Nitrat 3
(Jenie, 1993)
Terdapatnya ammonia didalam air erat hubungannya dengan siklus N di
alam ini. Dengan melihat siklus N dapat diketahui bahwa ammonis dapat
terbentuk dari :
d. Dekomposisi bahan-bahan organik yang mengandung N baik yang berasal
dari hewan (misalnya feses) oleh bakteri
e. Hidrolisa urea yang terdapat pada urin hewan
f. Dekomposisi bahan-bahan organik dari tumbuh-tumbuhan yang mati oleh
bakteri.
g. Dari N2 atmosfir, melalui pengubahan menjadi N2 O5 oleh loncatan listrik di
ditanah oleh hujan. Dengan melalui pembentukannya menjadi protein organik
yang terjadi selanjutnya, dan oleh dekomposisi bakteri akhirnya akan terbentuk
ammonia.
h. Dari reduksi NO2
(Sutrisno, 2004)
oleh bakteri
Ammonia (NH3
N organik + O
) dan garam-garamnya bersifat mudah larut dalam air. Ion
ammonium adalah bentuk transisi dari ammonia. Ammonia banyak digunakan
dalam proses produksi urea. Industri bahan kimia ( asam nitrat, ammonium sulfat,
ammonium nitrat dan ammonium sulfat) serta industri bubur kertas dan kertas
(pulp dan paper). Sumber ammonia diperairan adalah pemecahan nitrogen
organik (protein dan urea) dan nitrogen anorganik yang terdapat didalam tanah
dan air, yang berasal dari dekomposisi bahan organik ( tumbuhan dan biota
akuatik yang telah mati) oleh mikroba dan jamur. Proses ini dikenal dengan istilah
amonifikasi, ditunjukkan dalam persamaan reaksi :
2→ NH3-N + O2→ NO2-N + O2 Gambar 2.5. Reaksi Amonifikasi
→ NO3-N
Reduksi nitrat (denitrifikasi) oleh aktivitas mikroba pada kondisi anaerob,
yang merupakan proses yang biasa terjadi pada pengolahan limbah, juga
menghasilkan gas ammonia dan gas-gas lain, misalnya N2O, NO, NO2 dan N2.
Tinja dari biota akuatik yang merupakan limbah aktivitas metabolisme
juga banyak mengeluarkan ammonia. Sumber ammonia yang lain adalah reduksi
gas nitrogen yang berasal dari proses difusi udara atmosfer, limbah industri dan
domestik. Ammonia yang terdapat dalam mineral masuk kebadan air melalui erosi
bentuk gas dan membentuk kesetimbangan dengan gas amonium. Kesetimbangan
antara gas ammonia dan gas ammonium ditunjukkan dalam persamaan reaksi :
NH3 + H2O → NH4+ + OH
Gambar 2.6. Reaksi Kesetimbangan Ammonia dan Ammonium
Selain terdapat dalam bentuk gas, ammonia membentuk kompleks dengan
beberapa ion logam. Ammonia juga dapat terserap ke dalam bahan-bahan
tersuspensi dan koloid sehingga mengendap di dasar perairan. Ammonia di
perairan dapat menghilang melalui proses volatilisasi karena tekanan parsial
ammonia dalam larutan meningkat dengan semakin meningkatnya pH. Hilangnya
ammonia ke atmosfer juga dapat meningkat dengan meningkatnya kecepatan
angin dan suhu.
Ammonia yang terukur di perairan berupa amonia total (NH3 dan NH4+
Ammonia bebas (NH
).
Ammonia bebas tidak dapat terionisasi, sedangkan ammonium dapat terionisasi.
Presentase ammonia bebas meningkat dengan meningkatnya pH di perairan. Pada
pH 7 atau kurang, sebagian ammonia akan mengalami ionisasi. Sebaliknya, pada
pH lebih besar dari 7, ammonia tidak terionisasi yang bersifat toksik terdapat
dalam jumlah yang banyak.
3) yang tidak terionisasi bersifat toksik terhadap organisme akuatik. Toksisitas ammonia terhadap organisme akuatik akan
meningkat jika terjadi penurunan kadar oksigen terlarut, pH dan suhu. Avertebrata
air lebih toleran terhadap toksisitas ammonia daripada ikan.ikan tidak dapat
mengganggu proses pengikatan oksigen oleh darah dan pada akhirnya akan
mengakibatkan sufokasi. Akan tetapi, ammonia bebas ini tidak dapat diukur
secara langsung ( Effendi, 2003).
Kosnsentrasi ammonia yang tinggi pada permukaan air akan menyebabkan
kematian ikan yang terdapat pada perairan tersebut. Keasaman air atau nilai pH
nya sangat mempengaruhi apakah jumlah ammonia yang akan bersifat racun atau
tidak. Pengaruh pH terhadap toksisitas ammonia ditunjukkan dengan keadaan
pada kondisi pH rendah akan bersifat racun bila jumlah ammonia banyak,
sedangkan pada pH tinggi, hanya dengan jumlah ammonia yang rendah pun sudah
akan bersifat racun. Toksisitas ammonia juga tergantung dari jumlah ammonia
yang masuk dalam sel tumbuhan dan hewan ( Jenie, 1993).
2.10. Metode Penentuan Ammonia
2.10.1.Metode Penentuan Ammonia Dengan Titrasi
Pada metode ini dilakukan dengan menggunakan larutan H2SO4 0,2 N
sampai larutan berwarna sama dengan larutan blanko yang terdiri dari air suling
bebas ammonia dan H3BO3, yang volumenya sama dengan sampel.
2.10.2.Metode Penentuan Ammonia Dengan Menggunakan Elektroda
Pada metode ini elektroda yang digunakan untuk menentukan NH3
,
diperlukan elektroda referensi dengan larutan elektrolit yang sesuai selain itu juga
2.10.3.Metode Penentuan Ammonia Dengan Menggunakan Spektrofotometer
Pada metode ini dilakukan dengan cara menyiapkan dua buah sampel agar
teliti, standar dan blanko harus disiapkan secata serempak dan dengan
menggunakan larutan reagen Nessler yang sama. Dengan menggunakan
spektrofotometer, ukurlah panjang gelombang standar pada 400-425 nm terhadap
blanko (Alaerst, 1984).
2.11. Spektrofotometer
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari
spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum
panjang gelombang tertentu dan fotometer adalah adalah alat pengukur intensitas
cahaya yang ditransmisikan atau diabsorpsi. Jadi spektrofotometer digunakan
untuk mengukur energi secara relatif jika energi tersebut ditransmisikan,
direflaksikan atau diemisikan sebagai fungsi dari panjang gelombang. Kelebihan
spektrofotometer dibandingkan dengan fotometer adalah panjang gelombang dari
sinar dengan panjang yang diinginkan diperoleh dengan berbagai filter dari
berbagai warna yang mempunyai spesifikasi melewatkan trayek panjang
gelombang tertentu. (Khopkar, 2003)
Spektrofotometer merupakan instrumen di mana panjang gelombang
diukur dan dipilih sesuai tersebar dari cahaya putih. Membacanya dapat dengan
cara visual atau dengan cara fotolistrik. Spektrofotometri adalah pengukuran
energi radiasi relatif, apakah yang dipancarkan, atau dipantulkan, sebagai fungsi
Mata manusia dapat mendeteksi 10.000 perbedaan gradasi warna. Pada
maksimum spektrofotometer dapat mendeteksi lebih dari 2 juta gradasi warna.
Setiap spektrofotometer terdiri dari instrumen berikut:
1. Sumber cahaya
2. Perangkat untuk mendapatkan cahaya monokromatik
3. Sebuah sel penyerapan untuk sampel dan satu untuk blanko
4. Sarana mengukur perbedaan penyerapan antara sampel dan
(Snell And Cornelia, 1948)
blanko
2.11.1.Komponen Spektrofotometer
Komponen-komponen yang terpenting dari suatu spektrofotometer terdiri dari
sumber spektrum, monokromator, sel pengabsorpsi dan detektor.
1. Sumber, sumber yang biasa digunakan pada spektrofotometri absorpsi
adalah lampu wolfram. Arus cahaya tergantung pada tegangan lampu. Lampu
hidrogen atau lampu deuterium digunakan untuk sumber pada daerah UV.
Kebaikan lampu wolfram adalah energi radiasi yang dibebaskan tidak bervariasi
pada berbagai panjang gelombang.
2. Monokromator, digunakan untuk memperoleh sumber, sinar yang
monokromatis. Alatnya dapat berupa prisma ataupun grating. Untuk mengarahkan
sinar monokromatis yang diinginkan dari hasil penguraian ini dapat digunakan
celah.
3. Sel absorpsi, pada pengukuran di daerah tampak kuvet kaca atau kuvet kaca
corex dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus
smenggunakan sel kuarsa karena gelas tidak tembus cahaya. Umumnya tebal
digunakan. Sel yang biasa digunakan berbentuk persegi tetapi bentuk silinder
dapat juga digunakan.
4. Detektor, peranan detektor penerima adalah memberikan respon terhadap
cahaya pada berbagai panjang gelombang.
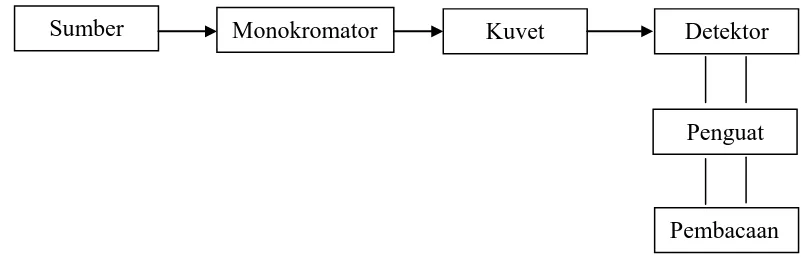
Day dan Underwood (2002) mengemukakan bahwa unsur-unsur
spektrofotometer ditunjukkan secara skematik dalam gambar berikut :
Gambar 2.7. Skematik Spektrofotometer
2.11.2.Cara Kerja Spekrofotometer
Cara kerja spektrofotometer secara singkat adalah : tempatkan larutan
pembanding, misalnya blanko dalam sel pertama sedangkan larutan yang akan
dianalisis pada sel kedua. Kemudian pilih fotosel yang cocok 200 nm – 650 nm
(600-1100) agar daerah λ yang diperlukan dapat terliputi. Dengan ruang fotosel
dalam keadaan tertutup “nol” galvanometer dengan menggunakan tombol
darkcurrent. Pilih yang diinginkan, buka fotosel dan lewatkan berkas cahaya pada
blangko dan “nol” galvanometer didapat dengan memutar tombol sensitivitas.
Dengan menggunakan tombol transmitansi, kemudian atur besarnya pada 100 %.
Lewatkan berkas cahaya pada larutan sampel yang akan dianalisis. Skala
absorbansi menunjukkan absorbansi larutan sampel (Khopkar, 2003).
Sumber Monokromator Kuvet Detektor
Penguat
BAB 3
METODOLOGI PENELITIAN
3.1. Alat-alat
1. Spektrofotometer HACH DR 2010
2. Kuvet 25 ml
3. Beaker gelas 250 ml Iwaki Pyrex
4. Botol sampel
5. Batang pengaduk
6. Pipet volume 1 ml Pyrex
7. Pipet volume 25 ml Pyrex
8. Stoper
3.2. Bahan
- Mineral stabilizer (aq) HACH
- Larutan Nessler (aq) HACH
- Akuades (l)
- Air Baku (aq)
- Air Reservoir (aq)
3.3. Prosedur Penelitian
Prosedur Penentuan Kadar Ammonia Dengan Spektrofotometer
1. Dipastikan analis telah memakai masker dan sarung tangan.
2. Ditekan power pada alat Spektrofotometer DR 2010.
3. Ditekan nomor progam 380 lalu Enter, layar akan menunjukkan Dial nm
to 425
4. Diputar putaran panjang gelombang hingga pada layar menunjukkan 425
nm.
5. Ditekan Enter, layar akan menunjukkan mg/L NH3
6. Dituangkan sampel air yang akan dianalisa kedalam beaker gelas 250 ml. -N Ness.
7. Dipipet 25 ml aquadest dan masukkan kedalam kuvet pertama sebagai
blanko.
8. Dipipet 25 ml sampel air dan masukkan kedalam kuvet kedua sebagai
sampel.
Ditambahkan 3 tetes Mineral Stabilizer kedalam masing-masing kuvet,
tutup dan kocok beberapa saat hingga larutan homogen, tambahkan 3
tetes Polyvinyl Alcohol Dispersing Agent kedalam masing-masin kuvet,
tutup dan kocok hingga homogen.
9. Ditambahkan 1 ml Larutan Nesler kedalam masing-masing kuvet, tutup
dan kocok hingga homogen. Larutan Nesler bersifat racun dan korosif.
Pipet dengan hati-hati. Warna kuning akan terbentuk jika ammonia
terdapat didalam sampel. Larutan Nessler akan berwarna kuning muda
10. Ditekan Shift Timer, 1 menit masa reaksi akan dimulai, setelah waktu
tercapai layar akan akan menampilkan NH3
11. Diletakkan blanko pada dudukan kuvet, tutup. -N Ness.
12. Ditekan Zero, pada layar akan menunjukkan 0,00 mg/l NH3
13. Diletakkan sampel pada dudukan kuvet, kemudian tutup.
-N Ness.
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
Hasil pemeriksaan sampel air WTP Mini Kelambir V yang dilaksanakan di
PDAM Tirtanadi Provinsi Sumatera Utara terdapat pada tabel di bawah ini :
Tabel 4.1. Data Pemeriksaan Penentuan Ammonia
Tanggal Sampel Hasil Pembacaan Hasil
Rata-rata
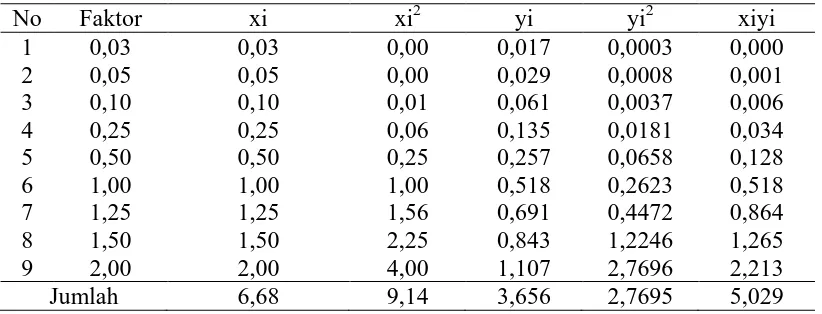
4.2.1. Penentuan Persamaan Garis Regresi
Untuk menentukan persamaan garis regresi dan kurva kalibrasi diturunkan dengan metode least square
Tabel 4.2. Penentuan Persamaan Garis Regresi
Penentuan harga slope (a) dan harga intersept (b) dengan metode least square
Maka persamaan garis regresi yang diperoleh adalah :
y = ax + b
y = 0,5536x -0,00472
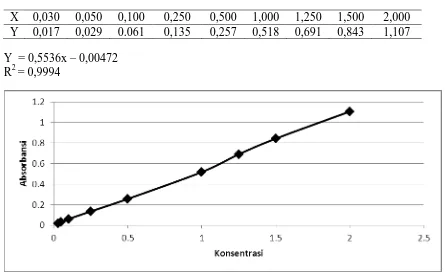
4.2.3. Grafik Linearitas Parameter Uji Ammonia (DR 2010)
Tabel 4.3. Linearitas Parameter Uji Ammonia
X 0,030 0,050 0,100 0,250 0,500 1,000 1,250 1,500 2,000
Y 0,017 0,029 0.061 0,135 0,257 0,518 0,691 0,843 1,107
Y = 0,5536x – 0,00472 R2 = 0,9994
Gambar 4.1. Grafik Linearitas Parameter Uji Ammonia ( DR 2010)
4.2.4. Perhitungan Konsentrasi Ammonia
Dengan menggunakan rumus
y = ax + b
Dimana :
x = konsentrasi
1. Untuk sampel AB 8 y = ax + b
0,573 = 0,5536x – 0,00472 = 1,044
2. Untuk sampel RS 25 y = ax + b
0,020 = 0,5536x – 0,00472 = 0,044
4.3. Pembahasan
Ammonia (NH3
Dari hasil penentuan yang dilakukan terhadap air baku WTP Mini Kelambir
V diperoleh nilai yang tinggi yaitu sebesar 0,573 mg/L, dimana hasil tersebut
melebihi ambang batas yang telah ditetapkan Pemerintah Republik Indonesia
No.82 Tgl 14 Desember 2001 (Baku mutu Kelas I) yaitu sebesar 0,5 mg/L.
Sehingga air baku tersebut harus dilakukan pengolahan lebih lanjut agar dapat
dikonsumsi. Sedangkan hasil penentuan yang dilakukan terhadap pada air
reservoir WTP Mini Kelambir V diperoleh nilai yang rendah yaitu 0,020 mg/L,
dimana hasil tersebut masih dibawah ambang batas yang sesuai persyaratan
kualitas air minum yang ditetapkan oleh Permenkes No.492/Menkes/Per/IV/2010 ) merupakan suatu zat yang menimbulkan bau yang sangat tajam
dan menusuk hidung. Kadar ammonia bebas yang telalu tinggi dapat mengganggu
proses pengikatan oksigen oleh darah dan pada akhirnya akan mengakibatkan
tanggal 19 April 2010 yaitu sebesar 1,5 mg/L. Sehingga dapat dikonsumsi sebagai
air minum.
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Berdasarkan hasil penentuan yang telah dilakukan diperoleh kesimpulan :
1. Kadar ammonia pada air baku WTP Mini Kelambir V adalah 0,573 mg/L.
Hasil tersebut telah melebihi ambang batas Peraturan Pemerintah Republik
Indonesia No.82 Tanggal 14 Desember 2001 (Baku Mutu Kelas I) yaitu
0,5 mg/L, sehingga perlu dilakukan pengolahan lanjutan agar air dapat
dikonsumsi.
2. Kadar ammonia pada pada air reservoir WTP Mini Kelambir V adalah
0,020 mg/L. Hasil tersebut masih jauh dibawah ambang batas Permenkes
No.492/Menkes/Per/IV/2010 Tanggal 19 April 2010 yaitu 1,5 mg/L.
sehingga air tersebut dapat dikonsumsi oleh masyarakat.
5.2. Saran
Diharapkan kepada mahasiswa selanjutnya yang akan melanjutkan penentuan
DAFTAR PUTAKA
Alaerst, G. 1984. Metoda Penelitian Air. Surabaya. Penerbit Usaha Nasional
Chandra,B. 2005. Pengantar Kesehatan Lingkungan. Jakarta. Penerbit Buku Kedokteran EGC
Chang, R. 2003. Kimia Dasar : Konsep-konsep Inti. Jilid 1. Edisi ketiga. Jakarta. Penerbit Erlangga
Darmono. 2001. Lingkungan Hidup Dan Pencemaran. Jakarta. Penerbit Universitas Indonesia.
Day, R.A dan Underwood. 2002. Analisis Kimia Kuantitatif. Jakarta. Penerbit Erlangga
Dumairy. 1992. Ekonomika Sumber Daya Air. Yogyakarta. Peberbit BPFE
Effendi, H. 2003. Telaah Kualitas Air. Yogyakarta. Penerbit Kasinius
Gabriel, J.F. Fisika Lingkungan. Jakarta. Penerbit Hipokrates
Diakses pada tanggal 9 April 2015.
Jenie, B.S dan Winiati P.R. 1993. Penanganan Limbah Industri Pangan. Yogyakarta. Penerbit Kasinius
Khopkar, S. 2003. Konsep Dasar Kimia Analitik. Jakarta. UI Press
Kristanto, P. 2004. Ekologi Industri. Yogyakarta. Penerbit Andi
Situmorang,M. 2007. Kimia Lingkungan. Medan. Penerbit Universitas Negeri Medan
Snell, F And Cornelia. 1948. Colourimetric Mehods Of Analysis. Third Edition. New Jersey. D Van Nostrand Company, Inc
Sutrisno, C.T. et al. 2004. Teknologi Penyediaan Air Bersih. Jakarta. Penerbit Rhineka Cipta
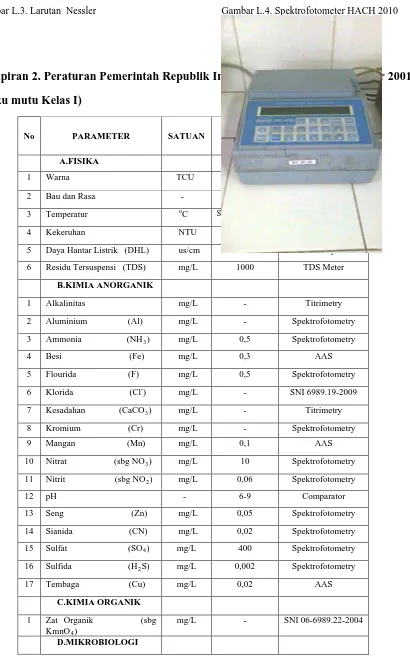
Lampiran 1. Alat Dan Bahan Yang Diperlukan Dalam Penentuan Kadar Ammonia
Gambar L.3. Larutan Nessler Gambar L.4. Spektrofotometer HACH 2010
Lampiran 2. Peraturan Pemerintah Republik Indonesia No.82 Tgl 14 Desember 2001 (Baku mutu Kelas I)
- SNI 06-6989.22-2004
1 Total Coliform Jlh/10mL 1000 SNI 06-4158-1996
2 Faecal Coliform Jlh/10mL 100 SNI 19-3957-1995
Lampiran 3. Permenkes No. 492/Menkes/Per/IV/2010 Tgl. 19 April 2010
1 Total Coliform Jlh/10mL 0 SNI 06-4158-1996