ISOLASI DAN ENKAPSULASI BAKTERI ASAM LAKTAT
(BAL) ASAL AYAM KAMPUNG (
GALLUS DOMESTICUS)
SEBAGAI PENGENDALI
E.COLI
TESIS
Oleh:
NURAINUN HARAHAP
127040002
PROGRAM STUDI ILMU PETERNAKAN
PROGRAM PASCASARJANA FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
ISOLASI DAN ENKAPSULASI BAKTERI ASAM LAKTAT
(BAL) ASAL AYAM KAMPUNG (
GALLUS DOMESTICUS)
SEBAGAI PENGENDALI
E.COLI
TESIS
Oleh:
NURAINUN HARAHAP
127040002
Tesis sebagai salah satu syarat untuk memperoleh gelar Magister Peternakan pada Program Studi Ilmu Peternakan Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI ILMU PETERNAKAN
PROGRAM PASCASARJANA FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
Nama : ISOLASI DAN ENKAPSULASI BAKTERI ASAM LAKTAT
(BAL) ASAL AYAM KAMPUNG (GALLUS DOMESTICUS)
SEBAGAI PENGENDALI E.COLI
Nama : Nurainun Harahap
NIM : 127040002
Program Studi : Peternakan
Menyetujui Komisi Pembimbing
Ketua Anggota
(Dr. Ir. Ma’ruf Tafsin, M.Si ) (Dr. Nevy Diana Hanafi, S.Pt,
M.Si)
An. Ketua Program Studi Dekan Fakultas Pertanian
(Dr. Nevy Diana Hanafi, S.Pt, M.Si) (Prof. Dr. Ir. Darma Bakti, MS)
Tesis ini telah diuji di Medan pada
Tanggal : 21 Januari 2015
PANITIA PENGUJI TESIS
Ketua : Dr. Ir. Ma’ruf Tafsin, M.Si
Anggota : Dr. Nevy Diana Hanafi, S.Pt, M.Si
Penguji : 1. Dr. Ir. Simon P. Ginting, M.Sc
LEMBAR PERNYATAAN
Dengan ini saya menyatakan bahwa segala pernyataan dalam tesis ISOLASI DAN ENKAPSULASI BAKTERI ASAM LAKTAT (BAL) ASAL AYAM KAMPUNG (GALLUS DOMESTICUS) SEBAGAI PENGENDALI E.COLI adalah benar merupakan gagasan dan hasil penelitian saya sendiri dibawah arahan komisi pembimbing. Semua data dan sumber informasi yang digunakan dalam tesis ini telah dinyatakan secara jelas dan dicantumkan dalam daftar pustaka di bagian akhir tesis serta dapat diperiksa kebenarannya. Tesis ini juga belum pernah diajukan untuk memperoleh gelar pada program studi sejenis di perguruan tinggi lain.
Medan, Januari 2015
RINGKASAN
NURAINUN HARAHAP. “Isolasi dan Enkapsulasi Bakteri Asam Laktat (BAL)
Asal Ayam Kampung (Gallus Domesticus) Sebagai Pengendali E.Coli”. Dibimbing oleh
MA’RUF TAFSIN dan NEVY DIANA HANAFI.
BAL dapat menurunkan pertumbuhan bakteri patogen. BAL menghasilkan zat antimikroba sehingga bakteri patogen tidak dapat berkembangbiak. Viabilitas BAL semakin menurun seiring dengan semakin bervariasinya pH yang terdapat pada saluran pencernaan. Untuk mengatasi permasalahan tersebut dapat dilakukan dengan memberikan perlindungan pada sel bakteri melalui proses enkapsulasi. Adapun tujuan penelitian ini adalah untuk mengisolasi dan mengkarakteristik BAL yang diperoleh dari usus ayam kampung, menganalisis pengaruh enkapsulasi pada berbagai kombinasi bahan pengisi terhadap jumlah koloni dan daya hambat BAL, mengetahui viabilitas BAL baik yang dienkapsulasi maupun yang tanpa enkapsulasi serta daya simpan kapsul BAL terhadap kestabilan jumlah koloni selama 4 minggu penyimpanan. Penelitian dilakukan di laboratorium nutrisi pakan ternak Fakultas Pertanian Universitas Sumatera Utara Medan pada bulan April – November 2014.
Penelitian ini dilakukan atas 3 tahap yaitu isolasi dan karakteristik BAL asal ayam kampung dilakukan berdasarkan pewarnaan gram, uji ketahanan BAL terhadap pH, garam empedu, suhu, motilitas dan katalase, pembuatan biopolimer BAL dan perbandingan antara alginat dengan bahan pengisi, daya simpan kapsul BAL dan pembuatan enkapsulasi BAL dalam bentuk kering.
Hasil penelitian pada saluran pencernaan ayam kampung didapat 6 isolat dan yang terbaik adalah isolat yang berasal dari ileum yang menunjukkan karakteristik BAL, tahan terhadap garam empedu, pH, suhu, jumlah koloni serta daya hambat BAL terhadap E.coli. Komposisi bahan enkapsulasi terbaik adalah alginat 5% sedangkan perbandingan alginat dengan bahan pengisi yang tertinggi terhadap alginat-maltodekstrin (2:1) yang menghasilkan rendemen 94% dengan jumlah koloni 9,10 log cfu/g, viabilitas sebesar 92,75% serta efisiensi enkapsulasi sebesar 95,26%. BAL yang terenkapsulasi maupun tanpa enkapsulasi dan lama penyimpanan tidak memberikan pengaruh yang signifikan terhadap viabilitas dan pH sedangkan kestabilan BAL dalam menghambat E.coli selama penyimpanan menunjukkan perbedaan yang nyata bahwa jumlah koloni dan daya hambat BAL yang dienkapsulasi lebih tinggi dibandingkan dengan BAL tanpa enkapsulasi selama 4 minggu penyimpanan. Dapat disimpulakan bahwaisolat yang terbaik dan memenuhi kriteria adalah isolat yang berasal dari ileum dengan konsentrasi biopolimer enkapsulasi BAL yang menunjukkan gel yang baik yaitu pada konsentarsi alginat 5% sedangkan perbandingan konsentrasi alginat dengan bahan pengisi yang terbaik adalah alginat - maltodekstrin (2:1). BAL terenkapsulasi lebih tahan dibandingkan dengan BAL tanpa enkapsulasi selama 4 minggu penyimpanan.
SUMMARY
NURAINUNHARAHAP. "Isolation andEncapsulationof Lactic Acid Bacteria(LAB)
Originof Native Chicken(Gallus domesticus) toControlE. coli". Under supervisedbyMA'RUFTAFSINandNEVYDIANAHANAFI.
LABcan reducethe growth ofpathogenic bacteria.
LABproduceantimicrobialsubstancesthatpathogenicbacteriacan notmultiply.
LABviabilitydecreasedalong with thevariation ofthe pHfound inthe digestivetract. Toovercome these problemscan be doneby providingprotectionin bacterial cellsthroughthe process ofencapsulation. The purposeof thisstudywastoisolateandcharacterizeLABobtainedfromchickenintestine, analyze the effect ofencapsulationonvariouscombinations offillerson the number ofcoloniesandthe inhibition ofLAB,
knowingboththeviability ofencapsulatedLABorwithoutencapsulationandstorabilitycapsuleLABon stabilitynumber ofcoloniesduring the4weeks of storage. The study was conductedinlaboratoryanimal feedscience,Faculty ofAgriculture, University ofSumatera UtaraMedan, inApril-November, 2014.
This study was conductedoverthreestages, namely isolationandcharacteristics of theoriginalLABchicken; LABstability testforpH, bilesalts, temperature; process encapsulation using alginat and various filler (milk skim, maltodekstrin), production biopolymersLAB andcomparisonbetween thealginatewithfillers,
The
LABandstorabilitycapsuleLABencapsulation.
resultsof researchonthe digestivetractchickenobtained6 isolates and isolates from
theileumshowedhighest,resistance tobile salts, pH andinhibitionof LABagainstE.coli.The bestencapsulationmaterial compositionisalginate5% while theratioof alginatewithhighfillerto thealginate-maltodextrin (2:1) whichresulted in94% yieldby the number ofcolonies of9.10log cfu/g,
the viabilityof92.75% andencapsulationefficiencyamounted to95.26%.
LABencapsulatedorwithoutencapsulationand storage timedid nothave a significant influenceon the viabilityandstabilityof pHwhereasLABin inhibitingE. coliduring storageshowed significant differencesthat thenumber ofcoloniesand LAB were encapsulatedmore resistthan theLABwithoutencapsulationfor 4weeks of storage. It is concludedthatisolatesfromthe ileum are potential as candidate probiotics.
BiopolymergelencapsulationLABshowedgoodthatthealginateconcentration of5%, while the ratio ofthe concentration ofalginatewiththebestfillermaterialisalginate-maltodextrin(2:1). LAB wereencapsulated more resist than theLABwithoutencapsulationfor 4weeks of storage.
RIWAYAT HIDUP
Nurainun Harahap, dilahirkan pada tanggal 17 Januari 1987 di Kota Medan
Sumatera Utara. Putri keempat dari empat bersaudara dari keluarga Bapak Aminullah
Harahap dan Ibu Nurbainah Siregar.
Penulis terakhir kalinya menamatkan sekolah menengah umum di SMAN 7 Medan
pada tahun 2005 dan pada tahun yang sama penulis terdaftar sebagai mahasiswa
Departemen Peternakan Fakultas Pertanian Universitas Sumatera Utara dan lulus pada tahun
2010. Pada tahun 2012 penulis diterima di Sekolah Pascasarjana Program Studi Ilmu
Peternakan Fakultas Pertanian Universitas Sumatera Utara.
Selama mengikuti perkuliahan penulis aktif sebagai anggota Himpunan Mahasiswa
Muslim Peternakan (HIMMIP) serta aktif dalam kegiatan seminar-seminar pascasarjana.
Penulis melaksanakan penelitian tesis di Laboratorium Mikrobilogi PeternakanJl.
Prof. A. Sofyan No. 3 Departemen Peternakan Fakultas Pertanian Universitas Sumatera
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan
karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah (tesis) ini. Adapun judul
dari tesis ini adalah “ Isolasi dan Enkapsulasi Bakteri Asam Laktat (BAL) Asal Ayam
Kampung (Gallus Domesticus) sebagai Pengendali E.coli”yang merupakan salah satu syarat
mendapatkan gelar Megister Peternakan di Fakultas Pertanian Universitas Sumatera Utara.
Pada kesempatan ini penulis menghanturkanterima kasih yang sebesar-besarnya
kepada kedua orang tua yang telah membesarkan, memelihara dan mendidik penulis selama
ini. Penulis menyampaikan ucapan terima kasih yang tak terhingga kepada
Dr. Ir. Ma’ruf Tafsin, M.Si dan Dr. Nevy Diana Hanafi, SPt, M.Si selaku ketua dan anggota
komisi pembimbing penulis yang telah membimbing dan memberikan berbagai masukan
berharga kepada penulis dari mulai menetapkan judul, melakukan penelitian, sampai pada
ujian akhir. Ucapan terima kasih kepada Dr. Ir. Simon Ginting, M.Sc dan Dr. Ir. Elisa
Julianti, M.Si selaku dosen penguji yang telah banyak memberikan saran untuk
kesempurnaan tesis ini Ungkapan terima kasih juga disampaikan kepada teman-teman
seperjuangan Pascasarjana Program Studi Peternakan angkatan 2012, teman–teman S1, ibu
Ir. Yunilas, M.Si serta laboran yang telah banyak membantu penulis dalam melakukan
penelitian di Laboratorium.
Penulis menyadari bahwa tesis ini masih mempunyai kekurangan. Oleh karena itu,
penulis mengharapkan saran dan kritik yang bersifat membangun untuk perbaikan
dikemudian hari. Penulis berharap tesis ini dapat bermanfaat bagi penulis dan pembaca.
Medan, Januari 2015
DAFTAR ISI
Teknologi Enkapsulasi ... 8
Bahan Pengkapsul ... 11
Alginat ... 11
Maltodekstrin ... 13
Susu Skim ... 14
Escherichia coli ... 15
Bakteri dalam Saluran Pencernaan ... 17
Penampilan Ayam Broiler terhadap Probiotik ... 18
BAHAN DAN METODE PENELITIAN Lokasi dan Waktu Penelitian ... 19
Metode Penelitian ... 19
Tahap I: Isolasi dan Identifikasi Kualitas BAL Ayam Kampung terhadap Bakteri Uji Bahan dan Alat Penelitian ... 19
Prosedur Penelitian Tahap I Isolasi dan Karakteristik BAL Asal Ayam Kampung ... 20
Karakteristik BAL Berdasarkan Morfologi dan Reaksi Pewarnaan Gram ... 21
Karakteristik BAL Berdasarkan Uji Motilitas ... 21
Karakteristik BAL Berdasarkan Uji Katalase ... 21
Uji Ketahanan BAL terhadap pH, Garam Empedu dan Suhu ... 22
Uji Ketahanan terhadap Keasaman Lambung (pH) ... 22
Uji Ketahanan terhadap Garam Empedu ... 22
Uji Ketahanan terhadap Temperatur/Suhu ... 22
Penentuan Jumlah koloni BAL ... 23
Uji Daya Hambat BAL terhadap Bakteri E.coli ... 23
Isolasi Bakteri Uji E.coli ... 23
Uji Daya Hambat BAL terhadap E.coli ... 24
Tahap II : Pembuatan Kapsul BAL dan Uji Kualitasnya
Bahan dan Alat Penelitian ... 25
Penentuan Total Padatan Bahan Pengkapsul ... 26
Penentuan Perbandingan Natrium Alginat dan Bahan Pengisi Optimum... 27
Viabilitas dan Efisiensi BAL Terenkapsulasi ... 27
Jumlah Populasi BAL Produk Enkapsulasi ... 28
Tahap III : Daya Simpan Kapsul BAL dan Evaluasi Kualitasnya ... 29
Daya Simpan Kapsul BAL dan Uji Kualitasnya ... 29
Pembuatan BAL Enkapsulasi dalam Bentuk Kering ... 31
HASIL DAN PEMBAHASAN Tahap I : Isolasi dan Karakteristik Kualitas BAL Ayam Kampung Terhadap Bakteri Uji Isolasi dan Karakteristik Kualitas BAL Ayam Kampung ... 33
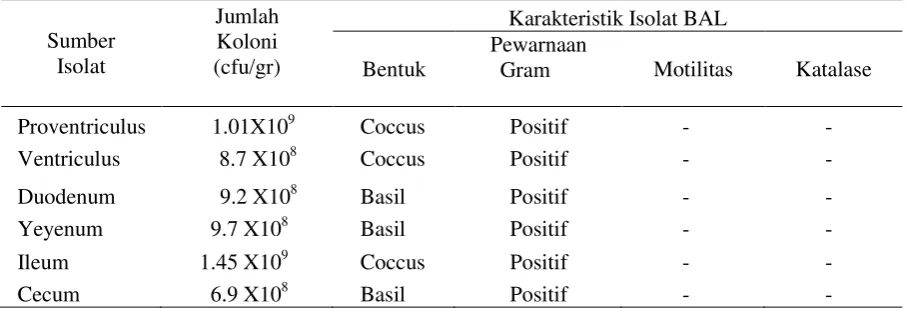
Karakteristik Isolat BAL ... 34
Uji Ketahanan BAL terhadap pH, Garam Empedu dan Suhu ... 36
Uji Daya Hambat BAL terhadap E. coli ... 39
Tahap II : Pembuatan Kapsul BAL dan Uji Kualitasnya Penentuan Konsentrasi Alginat sebagai Bahan Pengkapsul... 41
Perbandingan Natrium-Alginat dan Bahan Pengisi Optimum ... 44
Pengujian Viabilitas dan Efektivitas BAL Terenkapsulasi ... 46
Tahap III : Daya Simpan Kapsul BAL dan Evaluasi Kualitasnya Viabilitas BAL selama Penyimpanan ... 47
Pengaruh Lama Penyimpanan terhadap pH ... 50
Kestabilan BAL dalam Menghambat E.coli selama Penyimpanan ... 51
Pembuatan Beads BAL Terenkapsulasi dalam Bentuk Kering... . 52
KESIMPULAN DAN SARAN ... 54
DAFTAR PUSTAKA ... 55
DAFTAR TABEL
No. Halaman
1. Kelebihan dan kekurangan teknik estruksi dan emulsi ... 10
2. Komposisi natrium alginat ... 12
3. Komposisi maltodekstrin ... 13
4. Komposisi susu skim ... 15
5. Derajat keasaman (pH) di dalam saluran pencernaan ayam ... 17
6. Jumlah koloni BAL, Karakteristik isolat BAL dan uji ketahanan BAL ... 34
7. Uji Ketahanan BAL terhadap pH, Garam Empedu dan Suhu ... 36
8. Luas zona bening dan total asam tertitrasi ... 39
9. Pengaruh konsentrasi Na-alginat terhadap bentuk dan sifat fisik beads ... 41
DAFTAR GAMBAR
No. Halaman
1. Bakteri asam laktat ... 4
2. Mekanisme pertumbuhan BAL... 5
3. Prosedur enkapsulasi dengan metode ekstruksi ... 9
4. Bakteri E.coli... 15
5. Kultur murni isolat ... 33
6. Daya hambat BAL terhadap Eschericia Coli ... 41
7. Alginat dengan konsentrasi 5% ... 42
8. Grafik konsentrasi alginat sebagai bahan pengkapsul terhadap rendemen ... 43
9. Perbandingan alginat-filler terhadap ukuran dan bentuk beads ... 45
10.Viabilitas BAL tanpa dan dengan Enkapsulasi selama penyimpanan 4 minggu ... 48
11.Pengaruh lama penyimpanan terhadap pH ... 50
12.Kestabilan BAL dalam menghambat E.coli ... 51
DAFTAR LAMPIRAN
No. Halaman
1. Skema isolasi bakteri Escherichia coli ... 61
2. Skema isolasi Bakteri Probiotik ... 62
3. Skema pewarnaan gram ... 63
4. Skema kerja uji motilitas ... 64
5. Skema kerja uji ketahanan terhadap keasaman (pH) ... 65
6. Skema kerja uji ketahanan terhadap garam empedu ... 66
7. Skema kerja uji ketahanan terhadap temperatur ... 67
8. Skema kerja uji katalase ... 68
9. Hasil isolasi bakteri uji Escherichia coli dilihat dari mikroskop ... 69
10.Pertumbuhan isolat pada medium MRS broth + Ox bile 5% ... 70
11.Luas zona bening pada saluran pencernaan ayam kampung ... 71
12.Konsentrasi berbagai alginat ... 72
13.Penentuan biopolimer konsentrasi alginat sebagai bahan pengkapsul ... 73
14.Tabel Anova penentuan biopolimer konsentrasi alginat sebagai bahan pengkapsul. 74 15.Uji lanjut Duncan dalam penentuan biopolimer alginat ... 74
16.Pengaruh perbandingan alginat - filler terhadap rendemen beads yang dihasilkan .. 75
17.Tabel Anova pengaruh perbandingan alginat - filler terhadap rendemen beads yang dihasilkan ... 76
18.Uji lanjut Duncan dalam perbandingan alginat - filler terhadap rendemen ... 76
19.Pengaruh perbandingan alginat - fillerterhadap efisiensi dan viabilitas enkapsulasi 77 20.Tabel Anova pengaruh perbandingan alginat - fillerterhadap efisiensi enkapsulasi 77 21.Uji lanjut Duncan perbandingan alginat- fillerterhadap efisiensi enkapsulasi ... 78
23.Uji lanjut Duncan perbandingan alginat- fillerterhadap viabilitas enkapsulasi ... 79
24.Viabilitas dan ketahanan BAL selama masa Pengeringan ... 80
25.Tabel Anova viabilitas dan ketahanan BAL selama masa pengeringan ... 81
26.Uji lanjut t- viabilitas dan ketahanan BAL selama masa pengeringan ... 81
27.Pembuatan beads basah dalam bentuk kering ... 82
28.Viabilitas BAL tanpa dan dengan enkapsulasi selama penyimpanan ... 83
29.Kestabilan BAL selama penyimpanan ... 84
30.Pengaruh lama penyimpanan terhadap kestabilan pH ... 84
RINGKASAN
NURAINUN HARAHAP. “Isolasi dan Enkapsulasi Bakteri Asam Laktat (BAL)
Asal Ayam Kampung (Gallus Domesticus) Sebagai Pengendali E.Coli”. Dibimbing oleh
MA’RUF TAFSIN dan NEVY DIANA HANAFI.
BAL dapat menurunkan pertumbuhan bakteri patogen. BAL menghasilkan zat antimikroba sehingga bakteri patogen tidak dapat berkembangbiak. Viabilitas BAL semakin menurun seiring dengan semakin bervariasinya pH yang terdapat pada saluran pencernaan. Untuk mengatasi permasalahan tersebut dapat dilakukan dengan memberikan perlindungan pada sel bakteri melalui proses enkapsulasi. Adapun tujuan penelitian ini adalah untuk mengisolasi dan mengkarakteristik BAL yang diperoleh dari usus ayam kampung, menganalisis pengaruh enkapsulasi pada berbagai kombinasi bahan pengisi terhadap jumlah koloni dan daya hambat BAL, mengetahui viabilitas BAL baik yang dienkapsulasi maupun yang tanpa enkapsulasi serta daya simpan kapsul BAL terhadap kestabilan jumlah koloni selama 4 minggu penyimpanan. Penelitian dilakukan di laboratorium nutrisi pakan ternak Fakultas Pertanian Universitas Sumatera Utara Medan pada bulan April – November 2014.
Penelitian ini dilakukan atas 3 tahap yaitu isolasi dan karakteristik BAL asal ayam kampung dilakukan berdasarkan pewarnaan gram, uji ketahanan BAL terhadap pH, garam empedu, suhu, motilitas dan katalase, pembuatan biopolimer BAL dan perbandingan antara alginat dengan bahan pengisi, daya simpan kapsul BAL dan pembuatan enkapsulasi BAL dalam bentuk kering.
Hasil penelitian pada saluran pencernaan ayam kampung didapat 6 isolat dan yang terbaik adalah isolat yang berasal dari ileum yang menunjukkan karakteristik BAL, tahan terhadap garam empedu, pH, suhu, jumlah koloni serta daya hambat BAL terhadap E.coli. Komposisi bahan enkapsulasi terbaik adalah alginat 5% sedangkan perbandingan alginat dengan bahan pengisi yang tertinggi terhadap alginat-maltodekstrin (2:1) yang menghasilkan rendemen 94% dengan jumlah koloni 9,10 log cfu/g, viabilitas sebesar 92,75% serta efisiensi enkapsulasi sebesar 95,26%. BAL yang terenkapsulasi maupun tanpa enkapsulasi dan lama penyimpanan tidak memberikan pengaruh yang signifikan terhadap viabilitas dan pH sedangkan kestabilan BAL dalam menghambat E.coli selama penyimpanan menunjukkan perbedaan yang nyata bahwa jumlah koloni dan daya hambat BAL yang dienkapsulasi lebih tinggi dibandingkan dengan BAL tanpa enkapsulasi selama 4 minggu penyimpanan. Dapat disimpulakan bahwaisolat yang terbaik dan memenuhi kriteria adalah isolat yang berasal dari ileum dengan konsentrasi biopolimer enkapsulasi BAL yang menunjukkan gel yang baik yaitu pada konsentarsi alginat 5% sedangkan perbandingan konsentrasi alginat dengan bahan pengisi yang terbaik adalah alginat - maltodekstrin (2:1). BAL terenkapsulasi lebih tahan dibandingkan dengan BAL tanpa enkapsulasi selama 4 minggu penyimpanan.
SUMMARY
NURAINUNHARAHAP. "Isolation andEncapsulationof Lactic Acid Bacteria(LAB)
Originof Native Chicken(Gallus domesticus) toControlE. coli". Under supervisedbyMA'RUFTAFSINandNEVYDIANAHANAFI.
LABcan reducethe growth ofpathogenic bacteria.
LABproduceantimicrobialsubstancesthatpathogenicbacteriacan notmultiply.
LABviabilitydecreasedalong with thevariation ofthe pHfound inthe digestivetract. Toovercome these problemscan be doneby providingprotectionin bacterial cellsthroughthe process ofencapsulation. The purposeof thisstudywastoisolateandcharacterizeLABobtainedfromchickenintestine, analyze the effect ofencapsulationonvariouscombinations offillerson the number ofcoloniesandthe inhibition ofLAB,
knowingboththeviability ofencapsulatedLABorwithoutencapsulationandstorabilitycapsuleLABon stabilitynumber ofcoloniesduring the4weeks of storage. The study was conductedinlaboratoryanimal feedscience,Faculty ofAgriculture, University ofSumatera UtaraMedan, inApril-November, 2014.
This study was conductedoverthreestages, namely isolationandcharacteristics of theoriginalLABchicken; LABstability testforpH, bilesalts, temperature; process encapsulation using alginat and various filler (milk skim, maltodekstrin), production biopolymersLAB andcomparisonbetween thealginatewithfillers,
The
LABandstorabilitycapsuleLABencapsulation.
resultsof researchonthe digestivetractchickenobtained6 isolates and isolates from
theileumshowedhighest,resistance tobile salts, pH andinhibitionof LABagainstE.coli.The bestencapsulationmaterial compositionisalginate5% while theratioof alginatewithhighfillerto thealginate-maltodextrin (2:1) whichresulted in94% yieldby the number ofcolonies of9.10log cfu/g,
the viabilityof92.75% andencapsulationefficiencyamounted to95.26%.
LABencapsulatedorwithoutencapsulationand storage timedid nothave a significant influenceon the viabilityandstabilityof pHwhereasLABin inhibitingE. coliduring storageshowed significant differencesthat thenumber ofcoloniesand LAB were encapsulatedmore resistthan theLABwithoutencapsulationfor 4weeks of storage. It is concludedthatisolatesfromthe ileum are potential as candidate probiotics.
BiopolymergelencapsulationLABshowedgoodthatthealginateconcentration of5%, while the ratio ofthe concentration ofalginatewiththebestfillermaterialisalginate-maltodextrin(2:1). LAB wereencapsulated more resist than theLABwithoutencapsulationfor 4weeks of storage.
PENDAHULUAN
Latar Belakang
Seiring dengan meningkatnya jumlah penduduk, tingkat pendapatan, kesadaran gizi
dan kualitas hidup masyarakat maka kebutuhan daging di Indonesia setiap tahun mengalami
peningkatan. Peningkatan kebutuhan daging ini merangsang para ahli di bidang peternakan
untuk berusaha meningkatkan produktivitas ternak. Salah satu caranya adalah memperbaiki
pakan ternak dengan menggunakan atau menambahkan mikroorganisme seperti probiotik.
Probiotik adalah mikroorganisme hidup yang bila dikonsumsi dapat meningkatkan
kesehatan manusia ataupun ternak dengan cara menyeimbangkan mikroflora dalam saluran
pencernaan jika dikonsumsi dalam jumlah yang cukup. Salah satu kelompok bakteri yang
berperan sebagai probiotik adalah bakteri asam laktat (BAL).
BAL merupakan kelompok bakteri gram-positif yang mampu mengubah karbohidrat
menjadi asam laktat sehingga dapat menurunkan pH (Nettles dan Barefoot, 1993). BAL
hidup disaluran pencernaan ternak. Keberadaan bakteri probiotik tersebut masih sangat
kurang khususnya di usus halus, sehingga penyerapan sari makanan kurang maksimal.
Ternak yang diduga memiliki BAL pada ususnya adalah ayam kampung. BAL dari ayam
kampung lebih menguntungkan karena lebih mudah beradaptasi dengan lingkungannya,
sehingga keseimbangan mikroflora pada sistem pencernaan ternak dengan cepat dapat
dipreroleh. Ayam yang sejak dini sudah memiliki keseimbangan mikroflora yang baik akan
lebih tahan terhadap infeksi bakteri patogen.
BAL dapat menurunkan pertumbuhan bakteri patogen, seperti E.coli karena dalam
usus halus terjadi kompetisi BAL dan E.coli untuk mendapatkan nutrien, dimana BAL dapat
melekat pada sel epitel usus yang kemudian membentuk koloni dan menghasilkan zat anti
menghasilkan asam lemak rantai pendek yang berperan untuk menstimulasi perbanyakan sel
epitel usus, sehingga terjadi peningkatan penyerapan nutrien dalam tubuh dan dapat
mempengaruhi pertambahan bobot badan ayam broiler.
Pemberian BAL tidak dapat diberikan secara langsung pada ternak unggas. Hal ini
dikhawatirkan viabilitasBAL semakin menurun seiring dengan semakin bervariasinya
derajat keasaman (pH) yang terdapat pada saluran pencernaan. Oleh karena itu, perlu adanya
teknologi yang dapat melindungi BAL. Teknologi tersebut adalah teknologi enkapsulasi.
Enkapsulasi adalah suatu teknologi yang digunakan untuk menyalut suatu bahan inti
dengan enkapsulan tertentu (Rizqiati et al. 2009). Teknologi ini berperan dalam melindungi
bahan inti dari lingkungan yang merugikan. Bakteri probiotik merupakan salah satu jenis
komponen bioaktif yang sebaiknya dilindungi kehidupannya agar dapat dimanfaatkan oleh
inangnya.
Studi mengenai isolasi dan enkapsulasi BAL asal ayam kampung sebagai pengendali
E.coli belum pernah dilaporkan. Kajian tesis ini menjadi sangat penting untuk membantu
meningkatkan produktivitas ternak ayam broiler.
Tujuan Penelitian
1. Mengisolasi dan mengkarakteristik BAL yang diperoleh dari usus ayam kampung
2. Menentukan jenis bahan pengkapsul terbaik bagi BAL serta menganalisis pengaruh
enkapsulasi pada berbagai kombinasi bahan pengisi terhadap jumlah koloni dan daya
hambat BAL.
3. Mengetahui viabilitas BAL baik yang dienkapsulasi maupun yang tanpa enkapsulasi
serta daya simpan kapsul BAL terhadap kestabilan jumlah koloni selama 4 minggu
Manfaat Penelitian
1. Memberikan informasi terhadap penelitian selanjutnya tentang pemberian bakteri
probiotik (BAL) dari usus ayam kampung dapat meningkatkan produktivitas ayam
broiler.
2. Memberikan informasi bahwa isolasi BAL dapat diproduksi secara terpadu dari saluran
pencernaan ayam kampung, selanjutnya BAL yang dihasilkan dapat dikapsulasi
TINJAUAN PUSTAKA
Bakteri Asam Laktat (BAL)
Bakteri asam laktat (BAL) merupakan bakteri gram positif yang berbentuk batang atau
bulat, tidak membentuk spora, fermentasi fakultatif anaeorob, tidak mempunyai sitokrom,
tidak memiliki kemampuan untuk mereduksi nitrat dan memanfaatkan laktat, oksidasi
negatif, katalase negatif, motilitas negatif dan kemampuan memfermentasi glukosa menjadi
asam laktat (Carr et al., 2002).
Gambar 1 : Bakteri Asam Laktat
a. Produk Fermentasi BAL dan Manfaatnya sebagai Probiotik
Produk fermentasi BAL salah satunya adalah asam organik. Asam organik ini
dihasilkan selama proses fermentasi terkait spesies organisme, gabungan kultur dan kondisi
pertumbuhan (Lindgren dan Dobrogosz, 1990). Asam organik mampu menurunkan pH dan
berfungsi untuk tidak memutus beberapa ikatan molekul sehingga memiliki kemampuan
aktivitas mikroba. Lebih lanjut Lindgren dan Dobrogosz (1990), melaporkan bahwa
penurunan pH mampu menghasilkan minimum inhibitory concentration (MIC), sehingga
asam laktat dapat menghambat kerja Clostridium tyrobutyricum, E.coli, Enterobacter sp
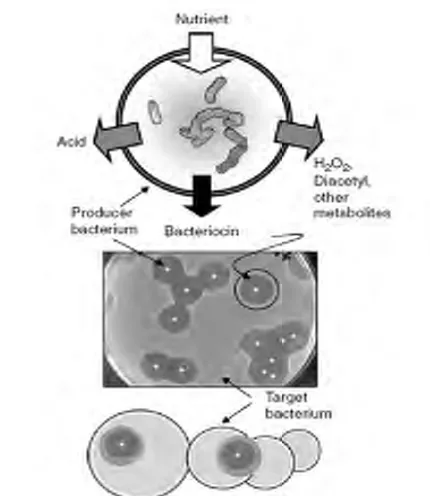
Gambar 2. Produk Fermentasi BAL (Lindgren dan Dobrogosz, 1990)
BAL juga menghasilkan hidrogen peroksida (H2O2) karena adanya oksigen sehingga
terjadi reaksi flavoprotein oksidasi atau nicotinamida adenin hidroxy dinucleotida (NADH)
perioksida. H2O2 berasal dari oxidation sulfhydril disebabkan karena denaturasi dari
sejumlah enzim berasal dari perioksidase membrane lipids sehingga meningkatkan
permeabilitas membran (Kong dan Davidson, 1980). H2O2 juga dapat berfungsi sebagai
prekusor untuk memproduksi bakteri radikal bebas antara lain O2 dan OH yang dapat
merusak DNA (Byczkowski dan Gessner, 1988).
Karbondioksida (CO2) merupakan hasil dari produk fermentasi BAL secara
heterofermentatif. Mekanismenya adalah CO2 bekerja dalam suasana anaerob, selanjutnya
menghambat kerja enzim dekarboksilase dalam membran lipid sehingga tidak mempunyai
fungsi sebagai permeabilitas (Eklund, 1984). CO2 dapat menghambat mikroba pembusuk
Asetildehida diproduksi oleh L.delbruecki sp dan Bulgaricus yang bila direaksikan
dengan threoin aldolase maka treonin tersebut membelah ke dalam asetildehida dan glisin.
Ketiga BAL tersebut tidak dapat merombak asetildehida, hanya terakumulasi dalam produk
pangan dengan konsentrasi sekitar 25 ppm. Asetildehida dengan konsentrasi 10-100 ppm
dapat menghambat pertumbuhan S.aureus, S.typhimurium dan Escherichia coli (Piard dan
Desmazeaud, 1992).
Aktivitas lipolitik dan Lactobacillus dan Lactococci secara signitifikan dapat
menghasilkan beberapa asam lemak dalam proses pengeringan dan fermentasi susu (Rao dan
Reddy, 1984). Aktivitas antimikroba dapat memutuskan ikatan molekul dari asam lemak
bukan anionnya, selain itu menurunkan pH memiliki pengaruh besar terhadap aktivitas
antimikroba (Kabara, 1993).
b. Reaksi Fermentasi Bakteri Asam Laktat (BAL)
Reaksi fermentasi BAL dibagi menjadi 2 bagian yaitu secara homofermentatif dan
heterofermentatif. Reaksi homofermentatif menghasilkan asam laktat, 2 mol ATP dari 1
glukosa/heksosa dalam kondisi normal, tidak menghasilkan CO2 dan menghasilkan
biomassa sel dua kali lebih banyak dari pada BAL heterofermentatif. Sedangkan reaksi
heterofermentatif selain menghasilkan asam laktat juga menghasilkan etanol, CO2, asam
asetat serta 1 mol ATP dari heksosa dan tidak mempunyai enzim aldolase. Untuk lebih
jelasnya reaksi fermentasi BAL dapat dilihat di bawah ini.
Reaksi homofermentatif
1 Heksosa + 2 ADP + 2Pi 2 laktat + 2 ATP
Reaksi Heterofermentatif
1 Heksosa + 1 ADP + Pi laktat + etanol + CO2 + 1 ATP Atau
Menurut Food and Agriculture Organization/World Health Organization
(FAO/WHO) (2001), idealnya strain probiotik seharusnya tidak hanya mampu bertahan
melewati saluran pencernaan tetapi juga memiliki kemampuan untuk berkembang biak
dalam saluran pencernaan, tahan terhadap cairan lambung dan cairan empedu dalam jalur
makanan yang memungkinkan untuk bertahan hidup melintasi saluran pencernaan dan
terkena paparan empedu. Selain itu probiotik juga harus mampu menempel pada sel epitel
usus, mampu membentuk kolonisasi pada saluran pencernaan, mampu menghasilkan zat anti
mikroba (bakteriosin), dan memberikan pengaruh yang menguntungkan inangnya. Syarat
lainnya adalah tidak bersifat patogen dan aman jika dikonsumsi. Strain probiotik juga harus
tahan dan tetap hidup selama proses pengolahan makanan dan penyimpanan, mudah
diaplikasikan pada produk makanan, dan tahan terhadap proses psikokimia pada makanan
(Prado et al., 2008).
Efisiensi penggunaan pakan dapat dilakukan dengan pemberian bahan imbuhan (feed
additive) atau zat pemacu tumbuh (growth promotant). Pencampuran feed additive ini
dimaksudkan untuk meningkatkan daya simpan ransum dan memacu pertumbuhan ternak.
Namun penggunaan feed additif secara terus menerus akan mengakibatkan terdapatnya
produk metabolit berupa residu antibiotik. Oleh karena itu penggunaan feed additive alami
merupakan alternatif untuk mengurangi akumulasi residu feed additive dalam daging. Salah
satu feed additive alami yang mulai digunakan yakni bakteri probiotik (Tensiska, 2008).
Pemberian probiotik pada ternak unggas biasanya diberikan dalam bentuk campuran
ransum atau diberikan melalui air minum, atau dalam bentuk probiotik yang hanya
mengandung satu macam strain mikroba saja atau dalam bentuk campuran terdiri dari
beberapa strain mikroba seperti “probiolac” atau “protexin”. Beberapa keuntungan dari
penggunaan probiotik pada hewan atau ternak antara lain adalah dapat memacu
mencegah terjadinya gangguan pencernaan terutama pada hewan-hewan muda, pengurai
faktor seperti antitripsin (Budiansyah, 2004).
Teknologi Enkapsulasi
Enkapsulasi adalah suatu teknologi dalam proses penyalutan partikel inti dapat
berbentuk cair, padat atau gas dengan suatu bahan pengisi khusus sehingga partikel-partikel
inti tersebut mempunyai sifat fisik dan kimia sesuai yang dikehendaki (Kim dan Morr, 1996). Teknologi ini berperan dalam melindungi bahan inti dari lingkungan yang
merugikan. Bakteri probiotik merupakan salah satu jenis komponen bioaktif yang sebaiknya
dilindungi kehidupannya agar dapat dimanfaatkan oleh inangnya. Manfaat enkapsulasi bagi
probiotik yaitu untuk mempertahankan viabilitas dan melindunginya dari kerusakan akibat
kondisi lingkungan yang tidak menguntungkan (Wu et al. 2000).
Bahan yang umum digunakan sebagai enkapsulan, diantaranya alginat, gum arab, pati,
agar, gelatin, karagenan, albumin dan kasein. Masing-masing bahan tersebut memiliki
karakter tertentu sehingga perlu adanya pertimbangan agar cocok bila digunakan untuk
menyalut suatu bahan inti tertentu. Beberapa peneliti telah melakukan penelitian mengenai
enkapsulasi bakteri probiotik dengan menggunakan enkapsulan tertentu diantaranya
enkapsulasi Bifidobacteria dan Lactobacillus dalam alginat-pati (Sultana et al. 2000), L.
casei dalam alginat-tepung polard dan terigu (Widodo et al. 2003), L.acidophilus dan B.
lactis dengan alginat (Kailasapathy 2006), L. acidophilus, L.helveticus, B. longum dan B.
lactis dalam alginat, gelatin dan pati pada produk yoghurt dengan metode ekstrusi dan
emulsi (Jayalalitha et al. 2011) dan L.plantarum dengan enkapsulan campuran susu skim
dan gum arab (Rizqiati et al. 2009). Dalam hal ini, metode enkapsulasi juga dapat
memperbaiki karakteristik sensori pada produk akhir terutama atribut teksturnya
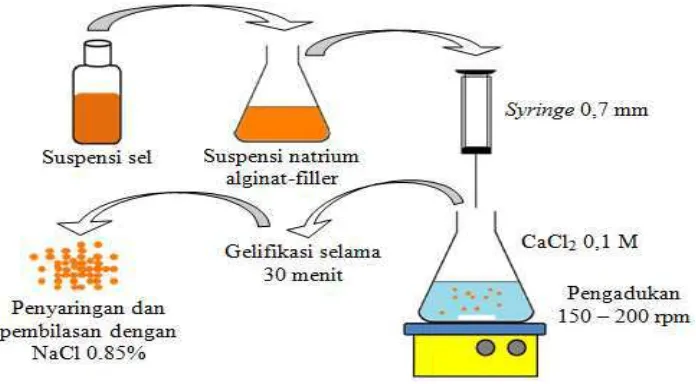
Gambar 3 : Prosedur enkapsulasi dengan metode ekstrusi (Krasaekoopt et al. 2003)
Teknik enkapsulasi probiotik dapat dilakukan dengan dua teknik, yaitu ekstrusi dan
emulsi (Krasaekoopt et al. 2003). Teknik ekstrusi dilakukan dengan cara menambahkan
mikroorganisme probiotik ke dalam larutan hidrokoloid natrium alginat, kemudian
diteteskan ke dalam larutan pengeras (CaCl2) menggunakan syringe sehingga terbentuk
beads. Ukuran dan bentuk beads yang dihasilkan bergantung pada diameter jarum dan jarak
tetes jarum dengan larutan CaCl2.
Berbeda dengan teknik ekstrusi, teknik emulsi dilakukan dengan menyuspensikan
sebagian kecil polimer (alginat) ke dalam minyak nabati seperti minyak kedelai, minyak
bunga matahari, minyak conola, atau minyak jagung, kemudian dihomogenisasi dalam
bentuk emulsi. Emulsi tersebut akan membentuk droplet. Ukuran beads pada metode emulsi
ditentukan oleh ukuran droplet emulsi yang terbentuk. Ukuran droplet emulsi dapat
dikontrol dengan kecepatan pengadukan saat emulsifikasi (Krasaekoopt et al. 2003).
Tabel 1. Kelebihan dan Kekurangan Teknik Ekstrusi dan Emulsi
Ekstrusi Emulsi
Kelayakan teknologi Sulit untuk meningkatkan Mudah untuk meningkatkan skala produksi (scale up) skala produksi (scale up)
Biaya Rendah Tinggi
Kemudahan Mudah Sulit
Ketahanan mikroorganisme 80 – 95% 80 – 95%
Ukuran beads 2 – 5 mm 25 μm – 2 mm
Sumber : Krasaekoopt et al. (2003)
Pada tahap pengeringan bahan pengkapsul berisi sel probiotik untuk mendapatkan sel
terenkapsulasi berbentuk serbuk atau granul dapat dilakukan dengan beberapa teknik, yaitu
freezedrying (Sultana et al. 2000, Capela et al. 2006) dan spray drying (Lian et al. 2003,
Picot dan Lacroix 2004). Enkapsulasi probiotik dengan teknik pengering semprot dan
pengering beku menghasilkan probiotik terenkapsulasi kering dalam bentuk serbuk atau
granul, sedangkan teknik emulsi dan ekstrusi menghasilkan probiotik terenkapsulasi dalam
bentuk jel (hydrocolloid beads) (Krasaekoopt et al. 2003). Namun, penggunaan teknik
freeze drying relatif mahal dan sangat sulit diaplikasikan pada skala industri (Mortazavian et
al. 2007), sedangkan penggunaan teknik spraydrying membutuhkan suhu operasi yang
tinggi sehingga kurang cocok diaplikasikan untuk enkapsulasi probiotik
(Kailasapathy 2002).
Keefektifan dari bahan dan teknik enkapsulasi yang digunakan untuk menghasilkan
probiotik terenkapsulasi dapat dievaluasi dari beberapa parameter kualitatif, diantaranya
viabilitas sel probiotik selama proses enkapsulasi dan pengeringan, pembuatan produk dan
penyimpanan, kelarutan beads dan kemampuan sel untuk keluarserta sifat mikrogeometri
Bahan Pengkapsul
Bahan pengkapsul merupakan bahan yang berfungsi sebagai pengikat suatu materi
serta memperbaiki mutu fisik produk. Enkapsulasi probiotik biasa dilakukan dalam sistem
polimer yang bersifat lembut dan tidak beracun (food grade) (Anal dan Singh 2007).
Polimer yang biasa digunakan dalam proses enkapsulasi bakteri probiotik adalah
polisakarida yang diekstrak dari rumput laut (karagenan dan alginat), tumbuhan (pati dan
turunannya, gum arab), atau bakteri (gellan dan xanthan), dan protein hewan (kasein, whey,
skim, gelatin) (Rokka dan Rantamaki 2010). Keuntungan penggunaan alginat sebagai bahan
pengkapsul adalah tidak toksik, membentuk matriks secara lembut dengan CaCl2 yang dapat
menjerap material sensitif seperti sel bakteri probiotik(Kailasapthy, 2002).
1. Alginat
Alginat merupakan salah satu jenis hidrokoloid yang dihasilkan dari ekstraksi alga
coklat (Sargassum sp., Turbinaria sp., Hormophyta sp., dan Padinasp.). Alginat telah
diaplikasikan secara luas pada produk pangan sebagai penyalut. Bentuk alginat terdiri dari
dua yaitu asam alginat dan garam alginat. Asam alginat merupakan kopolimer liniar yang
tersusun atas asam D-manuronat dan asam L-guluronat. Dalam suatu larutan, alginat
mengadakan interaksi antara kopolimernya dengan kation divalen (garam) seperti kalsium,
sehingga terbentuk gel kalsium alginat. Gel tersebut dipengaruhi oleh jumlah kation divalen
yang dapat berinteraksi dengan alginat (Nussinovitch, 2010).
Penambahan kation divalen (misalnya Ca2+) yang berfungsi sebagai penaut
silangantarmolekul alginat, akan menyebabkan terjadinya gelatinisasi yang akan membentuk
jelmatriks kalsium alginat. Kapsul kalsium alginat sangat berpori yang memungkinkan air
dapatberdifusi keluar masuk matriks (Rokka dan Rantamaki 2010). Penggunaan alginat
sebagai bahan enkapsulasi sering dikombinasikan dengan bahan lainnya, diantaranya dengan
(Widodo et al. 2003) sebagai bahan pengisi, chitosan sebagai coating (Krasaekoopt et al.
2004), dan pektin untuk membentuk kompleks alginat-pektin yang kuat (Castilla et al.
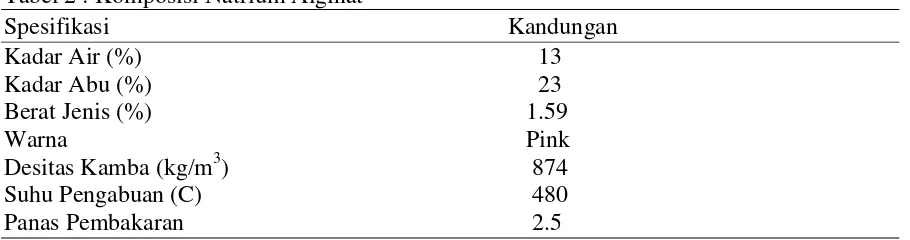
2010). Komposisi bahan natrium alginat dapat dilihat pada Tabel 2.
Tabel 2 : Komposisi Natrium Alginat
Spesifikasi Kandungan
Kadar Air (%) 13
Kadar Abu (%) 23
Berat Jenis (%) 1.59
Warna Pink
Desitas Kamba (kg/m3
Suhu Pengabuan (C) 480
) 874
Panas Pembakaran 2.5
Sumber: Food and Agriculture Organization. (2007)
Beberapa hasil penelitian menyatakan bahwa dengan metode ekstrusi menggunakan
enkapsulan alginat dapat meningkatkan ketahanan probiotik selama penyimpanan pada suhu
rendah (Godward dan Kailasapathy 2003; Krasaekoopt et al. 2006; Kailasapathy 2006;
Purwandhani et al. 2007; Aqilah dan Akhiar 2010). Ketahanan hidup bakteri probiotik
meningkat seiring dengan peningkatan konsentrasi alginat. Mandal et al., (2006)
mengemukakan bahwa L.acidophillus dapat lebih bertahan hidup saat konsentrasi alginatnya
ditingkatkan dari 2% menjadi 5%. Probiotik yang dienkapsulasi dengan alginat juga dapat
bertahan pada kondisi asam dalam saluran pencernaan. Hal ini dibuktikan dengan hasil
penelitian Chavarri et al.(2010) bahwa L. gasseri dan B. bifidum dengan enkapsulasi
alginat-kitosan dapat bertahan selama penyimpanan dingin dan pada kondisi simulasi saluran
pencernaan (pH 2) dan konsentrasi larutan empedu (3%) selama 2 jam. Probiotik masih
2. Maltodekstrin
Menurut FDA (The Food and Drug Administration), Maltodekstrin (C6H12O6) adalah
polimer sakarida yang bergizi, mengandung unit D-Glukose pada ikatan primer α-1,4 dan
memiliki nilai dextrose equivalence (DE) kurang dari 20. Dextrose equivalence (DE)
merupakan sifat utama yang menentukan sifat dari maltodekstrin itu sendiri. DE
maltodekstrin menunjukkan bahwa bahan tersebut mudah untuk dikeringkan, sedangkan
bahan yang memiliki DE lebih besar dari 42 akan sulit untuk dikeringkan dan dipasarkan
hanya dalam bentuk sirup (Kenyon, 1995).
Maltodekstrin merupakan bahan yang sering digunakan dalam pembuatan makanan
yang dikeringkan karena selain bahan pengisi, maltodekstrin memiliki beberapa kelebihan
antara lain tidak manis mudah larut dalam air. Maltodekstrin juga dapat meningkatkan
viskositas, menghambat kristalisasi dan baik untuk kesehatan karena rendah kalori.
Maltodekstrin biasanya digunakan sebagai campuran bahan pangan dan merupakan
pembentuk produk yang baik untuk produk yang sulit kering dan biasanya dijual dalam
bentuk tepung padat berwarna putih (Kuntz,1998). Komposisi maltodekstrin pada Tabel 3.
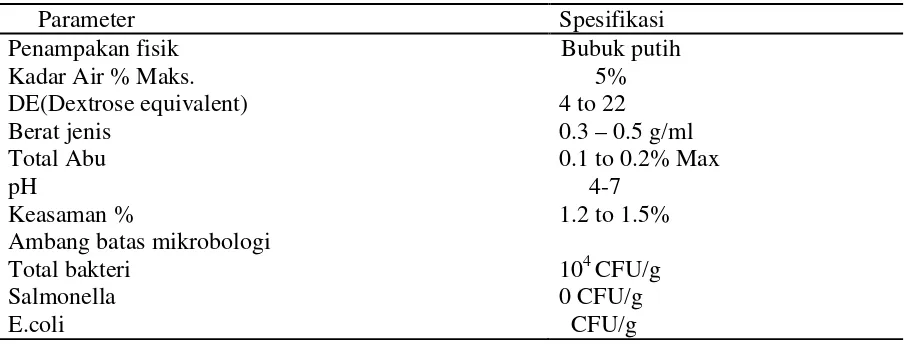
Tabel. 3. Komposisi Maltodekstrin
Parameter Spesifikasi
Penampakan fisik Bubuk putih
Menurut Kenyon dan Anderson (1988), maltodekstrin dan sirup jagung padat
memiliki sifat-sifat fungsional yang berpengaruh terhadap proses enkapsulasi, meliputi
kestabilan emulsi yang rendah yang dikarenakan tidak memiliki sifat lipofilik dan hidrofilik,
sifat pembentukan film, seberapa cepat pembentukan film atau membran pada proses
enkapsulasi flavor akan sangat menentukan kualitas produk akhir higroskopisitas.
3. Susu Skim
Protein merupakan komponen yang sangat penting, baik dari segi nutrisi maupun sifat
fungsionalnya seperti sebagai bahan pengemulsi, pengikat air atau lemak, serta pembentuk
buih atau gel. Selain itu protein juga dapat menghasilkan flavor, memperbaiki penampakan
dengan menghasilkan tekstur yang lebih baik (Buckle et al., 1987). Protein memiliki sifat
fungsional yang baik seperti viskositas, emulsifikasi serta pembentukan film. Dalam
penelitian ini, protein yang digunakan ialah susu skim.
Susu skim adalah bagian susu yang tertinggal setelah krim diambil sebagian
atauseluruhnya. Susu skim mengandung semua komponen gizi dari susu kecuali lemak dan
vitaminyang larut dalam lemak (Buckle et al. 1987). Karena lemaknya telah dipisahkan,
susu skim hanyamengandung 0,5 – 2% lemak (Varnam dan Sutherland 1994).Protein susu
dapatdigolongkan menjadi dua bagian, yaitu kasein dan whey. Kasein merupakan fraksi
protein yangmenggumpal ketika susu diasamkan pada pH 4,6 pada suhu sekitar 300
Susu skim mengandung semua zat makanan dari susu kecuali lemak dan
vitamin-vitamin yang larut dalam lemak. Krim mempunyai berat jenis yang rendah karena banyak
mengandung lemak. Susu skim mempunyai berat jenis yang tinggi karena banyak
mengandung protein. Susu skim adalah susu sapi yang telah diambil lemaknya dan diubah
menjadi bentuk bubuk, mempunyai bentuk seperti granula kecil, dengan warna putih C,
sedangkan fraksi yan tertinggal setelah pengendapan kasein disebut whey. Pada susu sapi
kekuningan. Susu ini banyak mengandung protein dengan kadar air 5% (Saleh, 2004).
Komposisi susu skim dapat dilihat pada Tabel 4.
Tabel 4 : Komposisi Susu Skim
Pada penelitian ini digunakan bakteri indikator E.coli sebagaipengontrol aktivitas
hambat bakteriosin yang memiliki daerah zona penghambatan yang luas.
E.coliadalahbakterigramnegatif,berbentuk batang, tidak tahan asam, hidup dengan cara
aerob dan anaerob, memilikiflagelaperitrikat,berukuran1,1 -
1,5μmx26μm,tersusuntunggalatauberpasangan,bersifatmotilatau nonmotildan
banyakgalurnyayangmemilikikapsuldanmikrokapsul dan sebagian spesiesnya menyebabkan
penyakit pada saluran pencernaan. Beberapagalurnyamerupakanpatogen terhadap manusia
dan hewan.E.colimempunyaitiperespirasi danfermentasidengansuhuoptimum37ºC dan pH
optimum7 (Drasar dan Borrow, 1985).
Pada ayam broiler, infeksi dari bakteri E.coli ini berdampak sangat buruk. Penyakit
ini dapat menyebabkan kematian selama periode pemeliharaan hingga perolehan berat badan
ayam saat panen akan dibawah standar. Bakteri E.coli ini sangat banyak terdapat di usus,
dan akan dikeluarkan dari tubuh dalam jumlah yang sangat besar bersama feses (kotoran).
Bakteri ini dapat bertahan sampai beberapa minggu di dalam feses, dengan kondisi yang
sangat mendukung. Akan tetapi, E.coli tidak tahan pada kondisi asam, kering, dan akan mati
dengan desinfektan (Pierard et al., 1990).
E.coliyang merupakan infeksi bakteri yang paling umum dijumpai pada peternakan
broileryang dikenal dengan penyakit kolibasilosis. Infeksi E.colipada unggas umumnya
bersifat sistemik dan menimbulkan bakteriemia (Costa et al., 2002). Infeksi
E.colimenyebabkan kematian embrio pada telur tetas, infeksi kuning telur, koliseptisemia,
peradangan kantung udara, radang usus, infeksi saluran reproduksi, radang persendian dan
bahkan menyebabkan kematian. Mortalitas dari penyakit ini adalah 10% - 15%. Penularan
kolibasilosis biasanya terjadi secara oral melalui pakan, air minum atau debu yang tercemar
oleh E.coli. Bakteri E.coli juga mampu menyebar melalui peredaran darah sehingga dapat
menyebabkan kerusakan pada berbagai organ sehingga mengganggu pertumbuhan dari ayam
tersebut (Djaafar et al.,1996) hal ini akan menyebabkan kerugian yang cukup besar untuk
peternak broiler. Menurut Fuller (1989) bakteri ini termasuk bakteri enterotoksigenik yang
dapat menyebabkan penyakit diare. Strain bakteri ini memproduksi dua tipe enterotoksin,
Bakteri dalam Saluran Pencernaan
Lebih dari 99% bakteri tinggal di dalam usus besar atau colon dan lebih dari 99%
berupa bakteri anaerob mutlak diantaranya adalah Clostridium, Bacterioides,
Bifidobacterium dan lain-lain. Hanya kurang dari 1% berupa bakteri fakultatif anaerob
seperti E.coli, Enterobacter dan bakteri patogen lainnya. Dengan demikian diperlukan
adanya efek antagonis terhadap bakteri patogen (Surono, 2004).
Lebih lanjut Surono (2004) menyatakan bahwa berbagai rintangan yang harus
dihadapi mikroba dalam saluran pencernaan dari mulut sampai anus. Pada perjalannya
melintasi berbagai sistem pencernaan khususnya yang dijumpai diantaranya enzim lisosom
pada air liur, asam lambung, garam empedu dan senyawa metabolit oleh BAL terutama
asam laktat. Pada usus besar hampir tidak ditemukan lagi hambatan yang cukup berarti
kecuali terjadinya kompetisi terhadap nutrisi. Bakteri probiotik harus mampu bertahan
menghadapi rintangan-rintangan tersebut, agar mencapai usus dalam keadaan hidup dalam
jumlah yang cukup memadai untuk berkembangbiak dalam menyeimbangkan mikrobiota
usus. Untuk mengetahui pH dan waktu transit dapat dilihat pada Tabel 5.
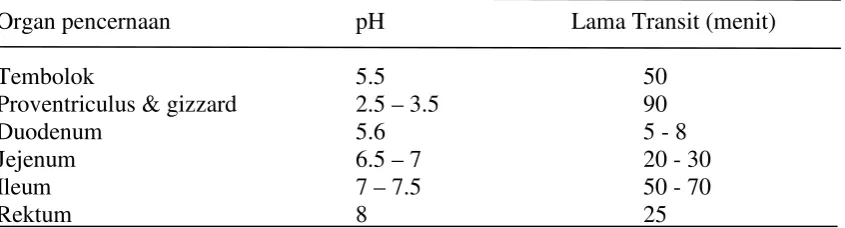
Tabel 5: Derajat Keasaman (pH) di dalam Saluran Pencernaan Ayam
Organ pencernaan pH Lama Transit (menit)
Tembolok 5.5 50
Populasi bakteri semakin kompleks baik jenis dan jumlahnya dengan bertambahnya
umur disepanjang saluran pencernaan. Lambung hanya mengandung bakteri yang tahan
terhadap asam, sebagaimana diketahui bahwa pH atau keasaman lambung sangat rendah
500 jenis bakteri yang jumlahnya trilyunan (1012 - 1014) bakteri dan BAL sekitar 104 - 109
bakteri. Mikroba dalam saluran pencernaan bisa membantu pencernaan makanan bahkan
beberapa jenis menghasilkan beberapa vitamin yang dibutuhkan oleh tubuh, namun
demikian beberapa efek negatif yang secara umum adalah dihasilkan senyawa-senyawa hasil
pembusukan protein, produksi toksin (Surono, 2004).
Penampilan Ayam Broiler terhadap Probiotik
Saat ini telah beredar produk probiotik yang mengandung mikroba lipolitik,
selulolitik, lignolitik, dan mikroba asam lambung. Beberapa penelitian pada broiler
menunjukkan bahwa penambahan probiotik dalam ransum dapat meningkatkan pertambahan
bobot badan, menurunkan konversi pakan dan mortalitas. Penelitian Kim et al., (1988)
menunjukkan bahwa penambahan probiotik yang terdiri dari Lactobacillus sporegenes
ke dalam pakan broiler yang mengandung jagung meningkatkan pertambahan bobot badan.
Probiotik dapat mengubah pergerakan pada populasi mikroba di dalam usus halus
ayam, sehingga keberadaannya dapat meningkatkan fungsi dan kesehatan usus,
memperbaiki mikroflora pada sekum, serta meningkatkan penyerapan zat makanan
(Mountzouris et al., 2010). Probiotik dapat memperbaiki saluran pencernaan dan
meningkatkan kecernaan pakan, yaitu dengan cara menekan bakteri patogen dalam saluran
pencernaan sehingga mendukung perkembangan bakteri yang menguntungkan yang
membantu penyerapan zat-zat makanan (Kompiang et al., 2002).
Beberapa laporan menunjukan bahwa penggunaan probiotik dapat meningkatkan laju
pertumbuhan yang berhubungan dengan manfaat probiotik dapat meningkatkan nafsu makan
dan menghasilkan vitamin serta enzim-enzim pencernaan. Memungkinkan probiotik tersebut
dapat berperan sebagai stimulasi pertumbuhan, sehingga dapat meningkatkan pertambahan
BAHAN DAN METODE PENELITIAN
Lokasi dan Waktu Penelitian
Penelitian dilaksanakan pada bulan April – November 2014. Penelitian dilaksanakan
di Laboratorium Mikrobiologi Nutrisi dan Bahan Pakan Ternak Fakultas Pertanian
Universitas Sumatera Utara Medan. Penelitian ini dilakukan atas 3 tahap yaitu isolasi dan
karakteristik BAL asal ayam kampung, pembuatan kapsul BAL dan uji kualitasnya, daya
simpan kapsul BAL dan pembuatan enkapsulasi BAL dalam bentuk kering.
Metode Penelitian
Tahap I: Isolasi dan Karakteristik BAL Asal Ayam Kampung terhadap Bakteri Uji
Bahan dan Alat Penelitian
Bahan yang digunakan dalam penelitian tahap I ini yaitu isolat bakteri asam laktat
(BAL) yang telah diisolasi dari usus ayam kampung, bakteri indikator Escherichia coli yang
diisolasi dari feses ayam, media yang digunakan adalah medium selektif MRSA (deMan
Rogosa Sharp Agar), deMan Rogosa Sharp Broth (MRSB), Eosin Methylene Blue Agar
(EMBA), Nurient Broth (NB), Nutrient Agar (NA), Muller Hilton Agar (MHA), penicilin, PP
1%, NaOH 0,1N, aquades, NaCl fisiologis 0,85%, kristal violet, iodin, alkohol asam, safranin,
HCl, etanol 70%, CaCO3 1%, reagen H2O2 3%, garam empedu sintetik (Ox bile) 1% dan 5%,
kertas cakram, alkohol 70%, medium SIM (Sulfid Indol Motility), minyak emersi.
Alat yang digunakan dalam penelitian ini adalah autoklaf, laminar flow, jarum ose,
inkubator, cawan petri, tabung reaksi, erlenmeyer, inkubator shaker, sentrifuse, mikropipet,
gelas objek, neraca analitik, desikator, pipet tetes, pH meter, holder milipore dan milipore
0,22 µm, pipet valumetrik, pipet 5 ml, kapas, aluminium foil, kertas saring, pemanas bunsen,
jangka sorong, oven, lemari pendingin, water bath, termometer, gelas ukur, hot plate,
preparat, mikroskop, kertas cakram, pipet pasteur, jangka sorong, scapel (pisau kecil),
Prosedur Penelitian Tahap I
1. Isolasi dan Karakteristik BAL Asal Ayam Kampung
BAL diisolasi dari berbagai segmen pada saluran pencernaan ayam kampung yaitu
pada proventriculus, ventriculus, yeyenum, ileum, usus besar dan cecum. Isolasi dilakukan
dengan mensuspensikan 1 gram dari masing-masing saluran pencernaan ayam kampung
kedalam 100 ml larutan NaCl 0,85% secara aseptis. Kemudian dibuat pengenceran 10-2 –107.
Sebanyak 1 mL hasil pengenceran tadi kemudian diinokulasikan pada medium MRSA
(Man Ragosa Sharpe Agar) yang mengandung CaCO3 1 % kemudian diinkubasikan pada
suhu 370
Setiap koloni yang terbentuk diamati dan diidentifikasi berdasarkan morfologi, reaksi
pengecatan gram, pembentukan gas, pengujian katalase kemudian penamaan taksonomi
dilakukan menggunakan Bergey’s manual of Determinative Bacteriology (Buchanan and
Gibbons, 1974). Masing-masing koloni yang teridentifikasi ditumbuhkan kembali dalam
medium MRSB. Inkubasi pertumbuhan BAL dilakukan pada suhu 37
C selama 48 jam. Koloni yang menunjukkan zona bening disekitar koloni
menunjukkan bahwa koloni tersebut adalah bakteri asam laktat (BAL).
o
Koloni yang terpisah dengan bentuk dan ukuran yang berbeda diambil menggunakan
jarum ose steril dan digoreskan pada MRSA yang telah beku dan diinkubasi pada kondisi
yang sama membentuk goresan kuadran. Penggoresan dilakukan sampai diperoleh koloni
yang seragam. Koloni yang murni dipilih, lalu dilakukan pewarnaan gram dan uji katalase. C selama 48 jam.
2. KarakteristikBAL Berdasarkan Morfologi
Tahap awal pemurnian dimulai dengan memilih koloni tunggal yang tumbuh pada
medium MRSA setelah diinkubasi selama 24 jam. Selanjutnya mengambil koloni tunggal
pada kultur, kemudian diinokulasikan secara goresan pada medium MRSA dan diinkubasi
pada temperatur 370C selama 48 jam. Koloni dari kultur murni selanjutnya diamati
coccobacillus) dan penataan bentuk (tunggal, berpasangan, rantai) dilakukan dengan
pengamatan menggunakan mikroskop (Buchanan and Gibbons, 1974).
3. KarakteristikBAL BerdasarkanReaksi Pewarnaan Gram
Prosedur pewarnaan mengikuti metode (Djide dan Sartini, 2008), dalam Trisna (2012),
biakan bakteri diambil dari stok dan diratakan diatas preparat yang telah dibersihkan
menggunakan etanol 70%. Kemudian difiksasi diatas api bunsen lalu ditetesi dengan zat
warna kristal violet selama 1 menit agar zat warna meresap pada bakteri. Preparat kemudian
dibilas dengan aquades mengalir dan ditetesi dengan larutan iodine kompleks. Kemudian
ditunggu selama 1 menit lalu dibilas dengan aquades mengalir. Preparat dicuci dengan
alkohol asam. Kemudian ditetesi dengan zat warna safranin, lalu ditunggu 30 detik. Setelah
itu dikeringkan dan diperiksa dibawah mikroskop dengan menggunakan minyak imersi.
4. Karakteristik BAL Berdasarkan Uji Motilitas
Sebanyak 1 ose isolat diambil dari stok kemudian diinokulasikan dengan cara ditusuk
pada medium SIM tegak. Selanjutnya diinkubasi pada temperatur 370C selama 48 jam. Hasil
positif (motil) jika terdapat rambatan – rambatan disekitar bekas tusukan jarum pada
medium dan hasil negatif (non motil) bila tidak terdapat rambatan-rambatan disekitar bekas
tusukan jarum ose pada medium.
5. Karakteristik BAL Berdasarkan Uji Katalase
Sebanyak 2 tetes larutan hidrogen peroksida (H2O2) 3% diteteskan pada gelas obyek
bersih, kemudian ditambahkan inokulum BAL. Uji positif ditandai denganterbentuknya
gelembung oksigen dan uji negatif tidak adanya gelembung gas (isolat tidak tumbuh)
6. Uji Ketahanan BAL terhadap Keasaman Lambung (pH), Garam Empedu dan Suhu
a. Uji Ketahanan terhadap Keasaman Lambung (pH)
Menurut Djide dan Wahyuddin (2008), uji ketahanan terhadap asam dilakukan dengan
menggunakan medium MRSB yang ditambahkan dengan HCl 0,1 N untuk mendapatkan pH
2,5 dan 3 (sesuai dengan pH lambung). Sebanyak 1 ose (ose bulat) masing-masing isolat
bakteri yang diambil dari stok kultur kemudian diinokulasikan pada medium MRSB-HCl.
Diinkubasi selama 48 jam pada suhu 370
b. Uji Ketahanan terhadap Garam Empedu
C. Hasil positif apabila terjadi pertumbuhan bakteri
pada medium dan hasil negatif apabila tidak terjadi pertumbuhan bakteri pada medium.
Ketahanan isolat mikroba terhadap garam empedu digunakan untuk mengkaji
kemampuan isolat bertahan pada saluran pencernaan yang terdapat garam empedu pada
permukaan atas usus. Pengujian dilakukan menurut metode Djide dan Wahyuddin (2008).
Metode ini dilakukan dengan menambahkan garam empedu sintetik (oxbile) dengan
konsentrasi 1 % dan 5 % pada medium MRSB. Selanjutnya isolat bakteri diambil dari stok
sebanyak 1 ose kemudian diinokulasikan pada medium MRSB – garam empedu. Diinkubasi
selama 48 jam dengan temperatur 370
c. Uji Ketahanan terhadap Suhu
C. Ketahanan terhadap garam empedu ditentukan
berdasarkan ada tidaknya pertumbuhan bakteri pada medium. Hasil positif jika ditandai
dengan adanya endapan pada dasar tabung dan adanya perubahan media menjadi lebih keruh
dibandingkan sebelum diinkubasi.
Isolat bakteri diambil dari stok sebanyak 1 ose kemudian diinokulasikan pada medium
MRSB. Selanjutnya medium yang telah berisi isolat diinkubasi pada temperatur 150C, 370C,
dan 450C selama 48 jam. Kemudian diamati apakah terjadi petumbuhan bakteri pada
medium. Hasil positif apabila terjadi pertumbuhan bakteri pada medium dan hasil negatif
7. Penentuan Jumlah Koloni BAL
Jumlah koloni BAL dari isolat diukur menggunakan metode Total Plate Count (TPC)
(Fardiaz, 1992). Sebanyak 1 g isolat hasil sentrifugassi dimasukkan ke petri dalam 9 ml
NaCl fisiologis 0.85%, lalu diencerkan sampai pengenceran 7 kali secara serial. Sebanyak
0,1 ml dari pengenceran 6 dan 7 kali ditanam pada cawan petri berisi media MRS agar.
Media agar yang ditanam kemudian diinkubasi pada suhu ruang selama 48 jam. Koloni yang
tumbuh berbentuk bulat miring berwarna agak kekuningan. Kemudian dihitung sebagai
beirikut:
Populasi BAL (cfu/g) = Jumlah koloni X Pengenceran
8. Uji Daya Hambat BAL terhadap Bakteri E.coli
a. Isolasi Bakteri Uji E.coli
Sampel feses segar dimasukkan ke dalam tabung reaksi berisi NaCl fisiologis 10 ml.
Diambil 1 tetes feses yang sudah dihomogenkan dengan larutan NaCl fisiologis. Sebanyak
15 ml media Eosin Methylene Blue (EMB) dimasukkan ke dalam cawan petri untuk
disterilisasi dengan autoklaf pada suhu 1210C selama 15 menit. Setelah sterilisasi media
diambil dari strerilisator untuk selanjutnya didiamkan pada suhu kamar agar media menjadi
padat. Dari pengenceran sampel yang dikehendaki, sebanyak 0,1 ml larutan tersebut
dimasukkan ke dalam cawan petri dengan metode sebar menggunakan gelas bengkok.
Inkubasi dilakukan pada suhu 370C selama 18-24 jam. Setelah akhir inkubasi, koloni yang
tumbuh dan berwarna hijau metalik dengan titik hitam pada bagian tengahnya dihitung
sebagai koloni E. coli. Koloni yang tumbuh dikoleksi dengan cara diinokulasikan pada
b. Uji Daya Hambat BAL terhadap E.coli
Untuk mengetahui bahwa isolat bakteri mempunyai potensi yang bagus sebagai
bakteri BAL maka perlu dilakukan uji daya hambat terhadap bakteri patogen. Bakteri patogen yang digunakan adalah E.coli (bakteri gram negatif).Untuk perlakuan kontrol positif
digunakan kertas cakram yang telah berisi antibiotika amoksilin, karena kloramfenikol
memiliki sensitivitas yang sangat tinggi, dimana pada dosis 30 μg/kertas cakram mampu
menghasilkan diameter zona hambat sebesar 25-31 mm (Fardiaz, 1992).
Langkah awal yang dilakukan adalah menginokulasi 1 ose (ose bulat) isolat dari stok
kultur pada medium MRSA miring dan diinkubasi selama 24 jam pada suhu 37°C. Hal yang
sama dilakukan terhadap bakteri uji (E. coli) yang diinokulasikan pada medium NAmiring
dan diinkubasikan selama 24 jam pada suhu 37°C. Sebanyak 1 ml isolat E. coli
diinokulasikan pada medium NA dengan metode tuang sebanyak 20 ml dan dibiarkan
memadat membentuk ketebalan agar. Campuran dihomogenkan dengan cara cawan petri
digerakkan membentuk angka delapan diatas bidang datar. Sementara itu disiapkan kertas
cakram steril lalu direndam sebanyak 10 μl dalam masing-masing suspensi isolat BAL
selama 10 menit. Kemudian kertas cakram diletakkan di permukaan medium NA yang telah
memadat, lalu diinkubasi selama 48 jam pada suhu 37°C untuk memberikan kesempatan
supernatan beraktivitas terhadap bakteri uji. Zona bening yang terbentuk menunjukkan
adanya hambatan terhadap pertumbuhan bakteri uji oleh supernatan. Diameter zona bening
(mm) diukur dengan jangka sorong sebanyak tiga kali pada posisi yang berbeda dan
9. Pengukuran Total Asam Tertitrasi
Pengukuran total asam tertitrasi dilakukan dengan prinsip titrasi asam basa. Sebanyak
10 ml filtrat dari sampel dimasukkan ke dalam labu erlenmeyer lalu ditambahkan 3 tetes
larutan indikator fenolftalein 1%, selanjutnya dititrasi dengan larutan NaOH 0.1 N hingga
terbentuk warna merah muda. Tepat saat warna merah muda terbentuk, titrasi dihentikan.
Total asam tertitrasi dinyatakan sebagai persen asam laktat. Total asam dapat diperoleh
melalui perhitungan berikut.
% Asam laktat = V NaOH X V NaOH X FP X BM Asam Laktat X 100% Bobot Sampel X 1000
Keterangan: BM asam laktat = 90.08
Tahap II : Pembuatan Kapsul BAL dan Uji Kualitasnya
Tujuan tahap ini adalah menentukan komposisi bahan enkapsulasi (biopolimer) yang
tepat untuk mengenkapsulasi BAL dengan teknik ekstrusi. Enkapsulasi yang digunakan
adalah natrium alginat, maltodeksttri dan skim. Maltodekstrin dan skim digunakan sebagai
bahan pengisi. Tahap ini terdiri atas beberapa kegiatan yaitu: penentuan total padatan bahan
pengkapsul, penentuan perbandingan natrium alginat dengan bahan pengisi optimum serta
pengujian viabilitas, efisiensi dan jumlah populasi BAL terenkapsulasi serta pembuatan
BAL enkapsulasi dalam bentuk kering.
Bahan dan Alat Penelitian
Bahan yang digunakan dalam penelitian penelitian ini adalah BAL, natrium alginat,
CaCl2 0,1M, NaCl 0,85%, alkohol 70%, aquadest, susu skim, maltodekstrin, MRSB, MRSA.
Alat yang digunakan dalam penelitian ini adalah magnetic stirer, syiringe, gelas
ukur, erlenmeyer, jarum ose, cawan petri, neraca analitic, tabung reaksi, kertas saring, pipet
1. Penentuan Total Padatan Bahan Pengkapsul
Kegiatan ini dilakukan untuk menentukan total padatan enkapsulasi optimum.
Enkapsulasi yang digunakan untuk menentukan total padatan optimum adalah natrium
alginat. Pembentukan beads jel kalsium alginat dilakukan dengan metode ekstrusi
(Krasaekoopt et al., 2003). Sebanyak 20 gram `suspensi natrium alginat (1%, 2%, 3%, 4%,
5%, dan 6% b/v) yang telah didinginkan pada suhu ruang diteteskan dalam 60 ml CaCl2
0,1M menggunakan syringe berukuran 0,7 mm dengan jarak tetes 1 cm dan diaduk
menggunakan magnetic stirer dengan kecepatan 150 – 200 rpm. Waktu pengerasan jel dalam
larutan CaCl2 0,1M dilakukan selama 30 menit, kemudian beads disaring secara steril dan
dibilas dengan NaCl 0,85% lalu ditiriskan selama ± 2 menit. Selanjutnya beads ditimbang.
Parameter yang diamati rendemen (yield), bentuk dan ukuran beads:
Rendemen = (massa beads/massa larutan natrium alginat) x 100%
Pada tahap ini, analisis statistik yang digunakan adalah rancangan acak lengkap factor
tunggal (single factor), yaitu konsentrasi biopolimer (natrium alginat). Faktor ini terdiri dari
empat taraf perlakuan, yaitu alginat 1% (A1), alginat 2% (A2), alginat 3% (A3), alginat 4%
(A4), alginat 5% (A5), alginat 6% (A6). Pengulangan dilakukan sebanyak tiga kali. Model
rancangan yang digunakan adalah sebagai berikut :
Yij = µ + Ai + εij
Keterangan:
Yij= Pengamatan pada faktor A taraf ke-i dan ulangan ke-j µ = Rataan umum
Ai = Pengaruh faktor A taraf ke-i εij = Pengaruh galat percobaan
Untuk mengetahui pengaruh antara taraf tersebut dilakukan analisis ragam (analisis
varian) menggunakan tingkat kepercayaan 95% (α=0,05). Jika hasilnya berbeda nyata,
2. Penentuan Perbandingan Natrium Alginat dengan Bahan Pengisi Optimum
Kegiatan ini dilakukan untuk menentukan perbandingan natrium alginat dengan bahan
pengisi optimum pada masing-masing bahan pengisi. Tahap ini diawali dengan menyiapkan
sebanyak 20 gram suspensi bahan pengkapsul yang terdiri atas natrium alginat dan bahan
pengisi dengan perbandingan 1:1, 2:1, 3:1 (b/v) dari masing-masing bahan pengisi.
Pada tahap ini analisis statistik yang digunakan adalah rancangan acak lengkap faktor
tunggal (single factor) yaitu komposisi bahan pengkapsul yang terdiri dari natrium alginat
dan bahan pengisi. Faktor ini terdiri dari 7 taraf perlakuan yaitu natrium alginat tanpa bahan
pengisi (B0), natrium skim 1:1 (B1), natrium skim 2:1 (B2), natrium
alginat-skim 3:1 (B3), natrium alginat-maltodekstrin 1:1 (B4), natrium alginat-maltodekstrin 2:1
(B5), natrium alginat-maltodekstrin 3:1 (B6). Pengulangan dilakukan sebanyak 3 kali.
Dengan model rancangan yang digunakan adalah sebagai berikut:
Yij = µ + Bi + εij
Keterangan:
Yij= Pengamatan pada faktor B taraf ke-i dan ulangan ke-j µ = Rataan umum
Bi = Pengaruh faktor B taraf ke-i εij = Pengaruh galat percobaan
Untuk mengetahui pengaruh antara taraf tersebut dilakukan analisis ragam (analisis
varian) menggunakan tingkat kepercayaan 95% (α=0,05). Jika hasilnya berbeda nyata,
analisis dilakukan dengan uji lanjut Duncan.
a. Pengujian Viabilitas dan Efisiensi BAL Terenkapsulasi
Kegiatan ini dilakukan untuk mengetahui viabilitas dan efisiensi BAL terenkapsulasi.
Komposisi bahan pengkapsul yang digunakan adalah komposisi optimum yang didapat dari
terlebih dahulu diaktivasi dalam 10 ml MRS broth sebanyak 2–3 kali dan diinkubasi pada
suhu 370C selama 24 jam. Suspensi kultur disimpan dalam refrigerator pada suhu 40
Suspensi biopolimer steril yang telah didinginkankemudian ditambahkan suspensi
sel sebanyak 0,1% (Homayouni et al. 2008a) atau denganperbandingan 9:1 (Castilla et al.
2010) lalu dikocok hingga homogen. Suspensi biopolimer-seldimasukan kedalam syringe
steril dan diteteskan kedalam larutan CaCl2 0,1 M steril(perbandingan suspensi
biopolimer-sel dan CaCl2 0,1 M adalah 1:3) dengan jarak tetes 1 cm dandilakukan pengadukan 150 –
200 rpm menggunakan magnetic stirer. Pengerasan jel dilakukanselama 30 menit. Beads
kemudian disaring dan dibilas menggunakan NaCl 0,85% yang telahdisterilisasi. Beads
basah kemudian dimasukan ke dalam wadah atau botol steril. Jumlah selyang terenkapsulasi
di dalam beads dihitung dengan metode yang digunakan Sheu dan Marshal (1993).
C
sebagai kultur stok. Suspensi sel yang akan digunakan untuk enkapsulasi merupakan kultur
berumur 18 jam dalam MRS broth (Homayouni et al., 2008a).
Viabilitas (%) = Log cfu/gram suspensi biopolimer – sel X 100% Log cfu/gram beads basah
Efisiensi enkapsulasi (%) = P X Q X 100% R
Keterangan:
P = Populasi BAL per gram beads (cfu/g beads)
R = Total BAL didalam suspensi biopolimer – sel (cfu)
Q = Massa beads yang dihasilkan dari total suspensi biopolimer – sel yang digunakan (g)
b. Jumlah Populasi BAL Produk Enkapsulasi
Pengujian jumlah koloni BAL didalam kapsul pada masing-masing perlakuan diukur
dengan menggunakan metode Total Plate Count (TPC) menurut Fardiaz (1992). Sebanyak
0,5 g kapsul BAL dimasukkan ke dalam 4,5 ml NaCl fisiologis 0,85% dan divortex untuk
sebanyak 0,1 ml untuk ditanam pada cawan petri berisi media MRS agar. Kultur diinkubasi
pada suhu ruang selama 2 hari. Koloni yang tumbuh kemudian dihitung sebagai berikut:
Populasi BAL (cfu/g) = Jumlah Koloni X Pengenceran
Tahap III : Daya Simpan Kapsul BAL dan Uji Kualitasnya
a. Daya Simpan Kapsul BAL dan Uji Kualitas
Sebanyak 5 g kapsul BAL disimpan dalam 30 kantong plastik steril pada suhu kamar
(270C - 280
Kestabilan BAL dalam menghambat E.coli dihitung berdasarkan daya hambat BAL
yang diperoleh sebelumnya dengan asumsi bahwa daya hambat BAL yang tertinggi (awal)
mempunyai nilai 100%, selanjutnya diperoleh % penurunan kestabilan BAL seiring dengan
semakin menurunnya juga daya hambat yang dihasilkan.
C) dengan kelembaban relatif (75% - 89%) selama 4 minggu. Masing-masing
sampel setiap minggu diambil untuk dianalisis jumlah koloni dan daya hambat BAL
melawan E.coli. Pengujian jumlah koloni BAL didalam kapsul pada masing-masing
perlakuan penyimpanan diukur dengan menggunakan metode Total Plate Count
(TPC)menurut Fardiaz (1992). Kapsul yang berisi BAL dilarutkan terlebih dahulu
menggunakan NaCl sebelum dilakukan penghitungan jumlah koloni BAL. Begitu juga
pengujian terhadap daya hambat E.coli. Jumlah koloni dan daya simpan BAL yang
diperoleh selanjutnya dapat diukur dengan viabilitas dan pH BAL.
Kestabilan BAL menghambat E.coli = Daya hambat BAL terendah X 100%
Daya hambat BAL tertinggi
Pada tahap ini, analisis statistik yang digunakan adalah rancangan acak lengkap