PENGHAMBATAN SERANGAN Sclerotium rolfsii PENYEBAB
REBAH KECAMBAH PADA KEDELAI DENGAN BAKTERI
KITINOLITIK
SKRIPSI
NOVI MALINDA
080805054
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGHAMBATAN SERANGAN Sclerotium rolfsii PENYEBAB REBAH KECAMBAH PADA KEDELAI DENGAN BAKTERI KITINOLITIK
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
NOVI MALINDA 080805054
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ii
PERSETUJUAN
Judul : PENGHAMBATAN SERANGAN Sclerotium rolfsii
PENYEBAB REBAH KECAMBAH PADA KEDELAI DENGAN BAKTERI KITINOLITIK
Kategori : SKRIPSI
Nama : NOVI MALINDA Nomor Induk Mahasiswa : 080805054
Program Studi : SARJANA (S-1) BIOLOGI Departemen : BIOLOGI
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA NIP. 19621211 199803 1 001 NIP. 19640409 199403 1 003
Diketahui/Disetujui oleh
Departemen Biologi FMIPA USU Ketua,
PERNYATAAN
PENGHAMBATAN SERANGAN Sclerotium rolfsii PENYEBAB REBAH KECAMBAH PADA KEDELAI DENGAN BAKTERI KITINOLITIK
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2013
iv
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul
“Penghambatan Serangan Sclerotium rolfsii Penyebab Rebah Kecambah pada
Kedelai dengan Bakteri Kitinolitik” sebagai salah satu syarat untuk mendapatkan
gelar Sarjana Sains (S.Si) pada Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam di Universitas Sumatera Utara.
Ucapan terima kasih penulis sampaikan kedapa Bapak Prof. Dwi Suryanto, M.Sc selaku dosen Pembimbing I dan Bapak Drs. Kiki Nurtjahja, M.Sc selaku dosen Pembimbing II atas bimbingan, arahan, dan dukungannya dalam pembuatan skripsi ini. Penulis juga mengucapkan terima kasih kepada Ibu Dr. It Jamilah, M.Sc dan Ibu Dra. Isnaini Nurwahyuni M.Sc selaku dosen Penguji yang telah memberi banyak saran dan kritik membangun dalam penyempurnaan skripsi ini.
Ucapan terima kasih penulis sampaikan juga kepada Ibu Dra. Isnaini Nurwahyuni, M.Sc selaku dosen Penasehat Akademik, Dr. Nursahara Pasaribu, M.Sc selaku ketua Departemen Biologi FMIPA USU, dan Bapak Drs. Kiki Nurtjahja, M.Sc selaku sekretaris Departemen Biologi FMIPA USU, serta seluruh staf pengajar Departemen Bologi. Penulis berterima kasih juga kepada Ibu Dr. Nunuk Priyani, M.Sc selaku Koordinator Laboratorium Mikrobiologi FMIPA USU, Ibu Nurhasni Muluk, Ibu Roslina Ginting, Bang Erwin selaku pegawai Departemen Biologi FMIPA USU.
Ucapan terima kasih juga penulis sampaikan kepada Bapak Utema Silen, S.P selaku ketua Laboratorium Pengamatan Hama dan Penyakit, Bapak Novit, Bapak Norman, kak Elvi, kak Naima, kak Vivi dan bang Rasyid selaku staf UPT-BPTPH 1 Medan Johor yang telah memberi dukungan dalam menyelesaikan penelitian. Penulis juga mengucapkan terima kasih kepada Bapak Sinulingga dan staf Balai Kesehatan Departemen Kesehatan Medan yang telah menerima penulis untuk praktek kerja lapangan di balai tersebut.
Ungkapan terima kasih penulis sampaikan juga pada kesempatan ini kepada ibunda tercinta Suryati, S.H dan ayahanda tercinta Tasman karena selalu memberikan doa, dukungan, dan kasih sayang yang tak ternilai harganya sehingga penulis dapat menyelesaikan skripsi ini. Ucapan terima kasih penulis sampaikan juga kepada pendamping ibu dan ayah penulis, Bapak Saidin Piliang dan Ibu Jamilah yang telah bersedia memberikan perhatian kepada penulis, serta (Alm) Amrin Usrah yang sudah seperti ayah kandung bagi penulis. Ucapan terima kasih penulis sampaikan juga kepada keluarga besar yang telah memberikan doa dan semangat kepada penulis.
Ucapan terima kasih tak lupa penulis sampaikan kepada BFS crew
skripsi ini (bang Affan, bang Mirza, bang Asril, kak Maika, kak Resti, kak Laura, kak Ria, bang Ncay, Nisa, Erina). Penulis juga mengucapkan terima kasih kepada teman-teman Struggling For The Earth stambuk 2008 (Ira Wulan Dani, Sirma Novita Nasrah, Yuni, Dessy, Sari, Nina, Dame, Yanti, Frans, Jekmal, Albert, Eka, Nanin, Maya, Rildah, Ummi, Riana, Zulfi, Netti, Santi, Ahri, Mela, Igun, Pesta, Asmitra, Indri, Sister, Miduk, Sarah, Oppy, Pinta, Rini, Intan, Inur, Gilang, Ika, Juju, Uya, Tombak, Rani, Destri, Hanna, Rosima, Rohana, Jhon, Ina, Yolanda). Ucapan terima kasih khusus penulis ucapkan kepada sahabat tercinta (Andini Hanif, Arifda Ayu, Dewi Novina, dan Diah Sri Utami), terima kasih atas rasa solidaritas yang telah dibina sampai detik ini. Semoga rantai persahabatan diantara kita tak pernah putus. Terima kasih juga kepada teman-teman baik yang telah membantu penulis dalam menyelesaikan skripsi ini yang penulis tidak dapat tuliskan namanya satu per satu.
Penulis menyadari bahwa skripsi ini jauh dari kesempurnaan, untuk itu penulis meminta maaf sebelumya. Akhir kata penulis mengharapkan semoga tulisan ini bermanfaat bagi kita semua.
Medan, Januari 2013
vi
PENGHAMBATAN SERANGAN Sclerotium rolfsii PENYEBAB REBAH KECAMBAH PADA KEDELAI DENGAN BAKTERI KITINOLITIK
ABSTRAK
Penelitian tentang penghambatan serangan Sclerotium rolfsii penyebab rebah kecambah pada kedelai dengan bakteri kitinolitik telah dilakukan di Laboratorium Pengamatan Hama dan Penyakit UPT-BPTPH 1 dan Laboratorium Mikrobiologi Departemen Biologi, FMIPA USU, Medan. Penelitian ini bertujuan untuk mengetahui potensi bakteri kitinolitik dalam menghambat S. rolfsii. Enam isolat bakteri kitinolitik yang diuji memiliki kemampuan yang bervariasi dalam menghambat pertumbuhan S. rolfsii. Efektivitas tertinggi ditunjukkan oleh Bacillus sp. BK13 dan Enterobacter sp. BK15 dengan zona hambat berturut-turut ialah 3,75 cm dan 3,70 cm. Efektivitas terendah ditunjukkan oleh Enterobackter sp. PB17 yang hanya mampu menghambat sebesar 0,10 cm. Enterobacter cloacae LK08 tidak memiliki kemampuan untuk menghambat S. rolfsii. BK13 dan BK15 menunjukkan pengurangan rebah kecambah pada kedelai. Perendaman benih dalam suspensi bakteri kitinolitik BK13 dan BK15 mampu menurunkan persentase rebah kecambah masing-masing sebesar 44,5% dan 50%.
INHIBITION OF Sclerotium rolfsii CAUSAL OF SOYBEAN DAMPING OFF WITH CHITINOLYTIC BACTERIA
ABSTRACT
A study about the inhibition of Sclerotium rolfsii causal of soybean damping off with chitinolytic bacteria had been done in Laboratory of Observation Pest and Disease UPT-BPTPH 1 and Laboratory of Microbiology, Department of Biology, Faculty of Mathematics and Natural Sciences, University of Sumatera Utara, Medan. The study was aimed to know the ability of chitinolytic bacteria to inhibit S. rolfsii. Six isolates of chitinolytic bacteria showed different ability in inhibiting of S. rolfsii. The most effective isolate was shown by Bacillus sp. BK13 and Enterobacter sp. BK15 with inhibition zone of 3.75 cm and 3.70 cm, respectively. The lowest effective was shown by Enterobacter sp. PB17 with inhibition zone of 0.10 cm. Enterobacter cloacae
LK08 do not have ability to inhibit S. rolfsii. BK13 and BK15 isolates shown to reduce damping off on soybean. The seeds soaked in bacterial suspension of BK13 dan BK15 was able to reduce damping off by 44.4% and 50%, respectively.
viii
2.1 Kitin dan Bakteri Kitinolitik 5 2.2 Jamur Patogen Sclerotium rolfsii 6 2.3 Penyakit Rebah Kecambah pada Kedelai 7 2.4 Pengendalian Hayati oleh Bakteri Kitinolitik 8
BAB 3 BAHAN DAN METODE 10
3.1 Waktu dan Tempat 10
3.2 Alat dan Bahan 10
3.3 Isolasi Sclerotium rolfsii 11 3.4 Uji Antagonis Isolat Bakteri Kitinolitik terhadap
Sclerotium rolfsii 11
3.5 Pengamatan Struktur Hifa Abnormal 12 3.6 Uji Patogenitas Sclerotium rolfsii 13 3.7 Penghambatan Serangan Sclerotium rolfsii pada Benih
Kedelai
13
BAB 4 HASIL DAN PEMBAHASAN 15
4.1 Hasil Isolasi dan Karakteristik Sclerotium rolfsii 15 4.2 Uji Antagonis Isolat Bakteri Kitinolitik terhadap
Sclerotium rolfsii 16
4.5 Penghambatan Serangan Sclerotium rolfsii pada Benih
Kedelai 20
BAB 5 KESIMPULAN DAN SARAN 28
5.1 Kesimpulan 28
5.2 Saran 28
DAFTAR PUSTAKA 29
x
DAFTAR GAMBAR
Halaman
Gambar 2.2.1 Koloni S. rolfsii pada media PDA dan yang menginfeksi
kecambah kedelai 7
Gambar 3.4.1 Metode pengukuran zona hambat bakteri kitinolitik
terhadap koloni jamur 12
Gambar 4.1.1 Hasil isolasi dan karakteristik Sclerotium rolfsii 15
Gambar 4.2.1 Uji antagonis S. rolfsii denganisolat bakteri kitinolitik 16
Gambar 4.3.1 Bentuk hifa abnormal Sclerotium rolfsii setelah uji
antagonis dengan bakteri kotinolitik 19
Gambar 4.4.1 Uji patogenitas Sclerotium rolfsii terhadap benih kedelai 20
Gambar 4.5.1 Persentase rebah kecambah pada kedelai yang
diinokulasikan Sclerotium rolfsii dengan perlakuan
bakteri kitinolitik 21
Gambar 4.5.2 Perbedaan tanaman kedelai umur 4 minggu 23
Gambar 4.5.3 Perbedaan tanaman kedelai yang terserang rebah kecambah
dengan tanaman yang sehat 25
Gambar 4.5.4 Perbedaan tinggi tanaman kedelai yang diinokulasikan
Sclerotium rolfsii dengan perlakuan bakteri kitinolitik 25
Gambar 4.5.5 Perbedaan jumlah daun tanaman kedelai yang
diinokulasikan Sclerotium rolfsii dengan perlakuan
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Isolasi dan Identifikasi Sclerotium rolfsii dan Uji
Antagonis Isolat Bakteri Kitinolitik terhadap Sclerotium
rolfsii 33
Lampiran 2 Pengamatan Struktur Hifa Abnormal, Uji Patogenitas
Sclerotiumrolfsii, dan Reisolasi 34
Lampiran 3 Penghambatan Serangan Sclerotium rolfsii pada Benih
Kedelai dan Pengaruh Pemberian Bakteri Penghasil Kitinase
35
vi
PENGHAMBATAN SERANGAN Sclerotium rolfsii PENYEBAB REBAH KECAMBAH PADA KEDELAI DENGAN BAKTERI KITINOLITIK
ABSTRAK
Penelitian tentang penghambatan serangan Sclerotium rolfsii penyebab rebah kecambah pada kedelai dengan bakteri kitinolitik telah dilakukan di Laboratorium Pengamatan Hama dan Penyakit UPT-BPTPH 1 dan Laboratorium Mikrobiologi Departemen Biologi, FMIPA USU, Medan. Penelitian ini bertujuan untuk mengetahui potensi bakteri kitinolitik dalam menghambat S. rolfsii. Enam isolat bakteri kitinolitik yang diuji memiliki kemampuan yang bervariasi dalam menghambat pertumbuhan S. rolfsii. Efektivitas tertinggi ditunjukkan oleh Bacillus sp. BK13 dan Enterobacter sp. BK15 dengan zona hambat berturut-turut ialah 3,75 cm dan 3,70 cm. Efektivitas terendah ditunjukkan oleh Enterobackter sp. PB17 yang hanya mampu menghambat sebesar 0,10 cm. Enterobacter cloacae LK08 tidak memiliki kemampuan untuk menghambat S. rolfsii. BK13 dan BK15 menunjukkan pengurangan rebah kecambah pada kedelai. Perendaman benih dalam suspensi bakteri kitinolitik BK13 dan BK15 mampu menurunkan persentase rebah kecambah masing-masing sebesar 44,5% dan 50%.
INHIBITION OF Sclerotium rolfsii CAUSAL OF SOYBEAN DAMPING OFF WITH CHITINOLYTIC BACTERIA
ABSTRACT
A study about the inhibition of Sclerotium rolfsii causal of soybean damping off with chitinolytic bacteria had been done in Laboratory of Observation Pest and Disease UPT-BPTPH 1 and Laboratory of Microbiology, Department of Biology, Faculty of Mathematics and Natural Sciences, University of Sumatera Utara, Medan. The study was aimed to know the ability of chitinolytic bacteria to inhibit S. rolfsii. Six isolates of chitinolytic bacteria showed different ability in inhibiting of S. rolfsii. The most effective isolate was shown by Bacillus sp. BK13 and Enterobacter sp. BK15 with inhibition zone of 3.75 cm and 3.70 cm, respectively. The lowest effective was shown by Enterobacter sp. PB17 with inhibition zone of 0.10 cm. Enterobacter cloacae
LK08 do not have ability to inhibit S. rolfsii. BK13 and BK15 isolates shown to reduce damping off on soybean. The seeds soaked in bacterial suspension of BK13 dan BK15 was able to reduce damping off by 44.4% and 50%, respectively.
BAB 1
PENDAHULUAN
1.1Latar Belakang
Kedelai merupakan salah satu tanaman sumber protein yang penting di Indonesia.
Berdasarkan luas panen, kedelai menempati urutan ketiga sebagai tanaman palawija
setelah jagung dan ubi kayu di Indonesia. Menurut Badan Pusat Stastistik atau BPS
(2009), luas panen kedelai sekitar 660.823 ha dengan produksi sekitar 907.031 ton
pada tahun 2010. BPS juga menunjukkan produktivitas kedelai sebesar 13,73 ku/ha
pada tahun 2010. Kedelai (Glycine max L.) mempunyai banyak manfaat sehingga
merupakan tanaman penting bagi masyarakat di Indonesia. Sebagai bahan makanan,
kedelai lebih banyak mengandung protein, lemak dan karbohidrat, sehingga baik
untuk memenuhi kebutuhan gizi masyarakat. Kebutuhan kedelai setiap tahun
meningkat, sedang peningkatan produksi rendah bila dibandingkan dengan
peningkatan kebutuhan yang mencapai 18% tiap tahun (Ratulangi, 2004).
Salah satu kendala yang mempengaruhi produksi kedelai adalah gangguan
penyakit. Penyakit yang umum menyerang adalah rebah semai/rebah kecambah.
Dalam Semangun (1993), penyakit tersebut juga disebut penyakit busuk pangkal
batang atau busuk sclerotium. Penyakit ini disebabkan oleh jamur Sclerotium rolfsii
Sacc. Penyakit rebah kecambah yang disebabkan oleh jamur tersebut merupakan salah
satu penyakit penting pada tanaman kedelai yang dapat menurunkan hasil sampai 75%
bahkan dapat menyebabkan gagal panen (Sudantha, 1997).
Gejala penyakit yang disebabkan oleh S. rolfsii yaitu tumbuhnya miselium
pada benih dan kecambah kedelai. Miselium tersebut berwarna putih seperti benang
dan dengan cepat tumbuh pada permukaan jaringan tanaman. Miselium kemudian
membusuk, sedangkan pada kecambah yang terserang akan layu (Sastrahidayat et al.,
2011). Pengendalian penyakit tersebut umumnya dilakukan secara mekanis yaitu
dengan mencabut tanaman yang terserang dan secara kimiawi dengan menyemprotkan
fungisida. Pengendalian menggunakan fungisida memang efektif tetapi untuk
menghindari dampak negatifnya diperlukan cara pengendalian lain yang ramah
lingkungan (Rahayu, 2008; Hardaningsih, 2011).
Saat ini pengendalian hayati semakin mendapat perhatian dalam perlindungan
tanaman dari serangan organisme pengganggu. Pengendalian hayati adalah cara
pengendalian yang ramah lingkungan dan prospektif dikembangkan untuk mengurangi
penggunaan fungisida kimia yang semakin mahal. Dalam pengendalian hayati
digunakan berbagai mikroorganisme antagonis terhadap patogen, sehingga mampu
berperan sebagai biopestisida. Mikroorganisme antagonis secara alami telah ada di
lingkungan habitat tanaman, sehingga dapat dieksplorasi (Rahayu, 2008).
Bakteri kitinolitik sangat potensial digunakan sebagai pengendalian hayati
terhadap jamur patogen maupun hama, karena kedua organisme ini mempunyai
komponen kitin pada dinding selnya. Umumnya, enzim yang banyak peranannya
adalah yang bertindak sebagai pengurai dinding sel. Salah satu enzim pengurai kitin
adalah kitinase, yang dihasilkan oleh beberapa agen pengendali hayati dan
dikeluarkan ke luar sel (Pal & Gardener, 2006). Enzim ini berperan penting di dalam
pengendalian hayati penyakit tanaman. Penguraian kitin secara enzimatik terlibat di
dalam banyak proses hayati, seperti autolisis, antagonisme, mikoparasitisme,
saprofitisme, morfogenesis, dan nutrisi, dan berperan dalam kerjasama
antar-organisme, termasuk interaksi tanaman-jamur, serangga-jamur, dan jamur-jamur.
Strain agensia pengendali hayati penghasil kitinase merupakan strain yang paling
efektif untuk pengendalian hayati penyakit tanaman, di samping dapat menjadi
patogen serius untuk usaha tani cendawan merang (Soesanto, 2008).
Bakteri kitinolitik ialah bakteri penghasil enzim kitinase yang berperan dalam
mendegradasi kitin menjadi N-asetilglokosamin. Organisme pendegradasi kitin
umumnya berasal dari kelompok mikroorganisme diantaranya adalah dari kelompok
3
Serratia marcescens, Bacillus circulans, Bacillus thuringiensis subsp. pakistani dan
Pseudomonas aeruginosa (Muharni & Widjajanti, 2011). Enzim kitinase yang
dihasilkan oleh mikroorganisme kitinolitik memiliki banyak kegunanaan, karena
mampu mengubah kitin menjadi produk-produk yang berguna untuk bidang pertanian,
farmasi dan medis (Muharni, 2009).
Enzim kitinase dapat diproduksi dari mikroorganisme kitinolitik yang
ditumbuhkan pada media yang mengandung kitin (Pujiyanto & Wijanarka, 2004).
Beberapa laporan menyatakan bahwa aktivitas kitinase dari Aeromonas caviae
efektif digunakan untuk mengontrol serangan jamur patogen Rhizoctonia solani
dan Fusarium oxysporum pada kapas dan Sclerotium rolfsii pada buncis
(Muharni & Widjajanti, 2011 ).
1.2Permasalahan
Pengendalian Sclerotium rolfsii pada kedelai masih dilakukan secara mekanis
dan kimiawi (Rahayu, 2008; Hardaningsih, 2011). Pengendalian secara mekanis dan
kimiawi tersebut memilki kelemahan yaitu dapat merusak lingkungan dengan residu
yang ditinggalkan oleh zat kimia sebagai bahan aktifnya. Pengendalian secara biologi
dengan menggunakan bakteri kitinolitik akan lebih aman dan tidak meninggalkan
residu di dalam tanah. Berdasarkan pentingnya pengendalian hayati terhadap tanaman
yang berpenyakit akibat jamur, perlu dilakukan penelitian untuk mengetahui
kemampuan bakteri kitinolitik dalam mengahambat pertumbuhan jamur patogen
Sclerotium rolfsii penyebab penyakit rebah kecambah pada kedelai.
1.3Tujuan
Penelitian ini bertujuan untuk mengetahui potensi bakteri kitinolitik dalam
menghambat Sclerotium rolfsii penyebab penyakit rebah kecambah pada kecambah
1.4 Hipotesis
Bakteri kitinolitik mampu menghambat pertumbuhan jamur patogen
Sclerotium rolfsii penyebab penyakit rebah kecambah pada kecambah kedelai.
1.5Manfaat
Dengan diketahuinya kemampuan bakteri kitinolitik mengendalikan
BAB 2
TINJAUAN PUSTAKA
2.1 Kitin dan Bakteri Kitinolitik
Kitin adalah polimer kedua terbanyak di alam setelah selulosa. Kitin merupakan
komponen penyusun tubuh serangga, udang, kepiting, cumi-cumi, dan artropoda
lainnya, serta bagian dari dinding sel kebanyakan jamur dan alga. Setiap tahun dari
perairan (laut) dihasilkan sekitar 1011 ton kitin, namun kurang dari 0,1% yang
dimanfaatkan kembali. Kitin memiliki struktur yang mirip selulosa. Selulosa tersusun
atas monomer glukosa, sedangkan kitin tersusun dari monomer N-asetilglukosamin.
Keduanya memiliki kelarutan sangat rendah dalam air serta mengalami biodegradasi
melalui mekanisme yang hampir serupa dengan melibatkan komplek enzim
(Toharisman, 2007).
Berbagai mikroorganisme mensekresi metabolit yang dapat mempengaruhi
aktivitas dan pertumbuhan patogen. Banyak mikroorganisme menghasilkan dan
mengeluarkan enzim litik yang dapat menghidrolisis sebagian besar senyawa polimer
termasuk kitin (Pal & Gardener, 2006). Kitinase ialah enzim yang mendegradasi kitin
menjadi N-asetilglukosamin. Degradasi kitin dapat dilakukan oleh organisme
kitinolitik dengan melibatkan enzim kitinase, seperti dari kelompok bakteri (Muharni,
2009).
Bakteri kitinolitik merupakan kelompok bakteri penghasil kitinase yang dapat
mendegradasi senyawa kitin. Menurut Toharisman (2007), kitinase dari organisme
laut berperan dalam proses daur ulang kitin. Banyak bakteri dan jamur mengeluarkan
kitinase untuk menguraikan kitin menjadi karbon dan nitrogen. Dua senyawa tersebut
penguraian kitin berlangsung terus-menerus sehingga tidak terjadi akumulasi kitin dari
sisa cangkang udang, kepiting, cumi dan organisme laut lainnya.
2.2 Jamur Patogen Sclerotium rolfsii
Menurut Alexopoulos & Mims (1979), Sclerotium rolfsii dapat diklasifikasikan
sebagai berikut :
Kingdom : Mycetaceae
Divisi : Mycota
Kelas : Deuteromycota
Ordo : Mycelia Steril
Famili : Agonomycetaceae
Genus : Sclerotium
Spesies : Sclerotium rolfsii Sacc
Sclerotium rolfsii memproduksi hifa putih kemudian miseliumnya menginfeksi
jaringan tanaman inang yang biasanya setelah 3-4 hari setelah infeksi ketika kondisi
kering. Cabang hifa utama umumnya besar (5-9 µm) dibandingkan pada banyak
kelompok jamur yang biasanya mempunyai diameter hifa 2-4 µm. Sekitar tujuh hari
setelah infeksi, hifa mulai membentuk sklerotia. Sklerotia berdiameter 0,5-2 mm,
tetapi beberapa dapat berdiameter sampai 8-9 mm. Sklerotia dapat bertahan selama
beberapa tahun di dalam tanah, media, atau di tanaman yang terserang. S. rolfsii tidak
memproduksi spora aseksual. Pertumbuhan hifa dan sklerotia terjadi pada suhu
optimum yang berkisar antara 27-35oC seperti yang ditunjukkan pada Gambar 2.2.1.
Pada suhu 27oC di media PDA. Sklerotia terbentuk setelah hari kelima sampai hari
ketujuh (Mullen, 2001).
Menurut Hartati et al., (2008), Sclerotium sp. dapat hidup pada kondisi
lingkungan yang bervariasi. Hal ini disebabkan oleh jamur tersebut mampu tumbuh
7
Gambar. 2.2.1 Koloni Sclerotium rolfsii (a) pada media PDA, (b) menginfeksi
kecambah kedelai. Sumber:
Jamur tular tanah Sclerotium rolfsii menginfeksi lebih kurang 19 tanaman
herba. Jamur ini merupakan suatu patogen yang menyebabkan beberapa gejala
penyakit tanaman di wilayah yang bersuhu panas dan bersuhu dingin termasuk
Amerika Selatan (Edmunds & Gleason, 2003).
2.3Penyakit Rebah Kecambah pada Kedelai
Kebutuhan kedelai semakin meningkat di Indonesia. Oleh karena itu, produksi
kedelai perlu ditingkatkan. Salah satu hambatan dalam upaya meningkatkan produksi
kedelai adalah serangan penyakit tanaman. Salah satu penyakit tanaman yang sering
menyerang kedelai adalah rebah semai/kecambah (damping off). Menurut Djafaruddin
(2008), jamur yang menembus masuk ke akar, tanpa memperlihatkan gejala luar
dengan segera, dan kemudian menyerang dan menyumbat sistem jaringan pembuluh
pengangkutan, hingga menyebabkan gejala layu dan terbatas pada persemaian
dinamakan rebah kecambah. Diantara penyebab damping off pada bibit persemaian
yang paling penting (kadang-kadang pada tanaman yang lebih tua tampak juga, baik
berupa busuk akar atau busuk batang), adalah kelompok jamur yang tergolong kepada
cendawan busuk akar (root rot) dari genera Corticium, Pellicularia, Pythium,
Rhizopus, Phoma, Macrophoma, Phytophthora, Vertillicium, Rhizoctonia, dan
Fusarium, maupun Sclerotium.
Kehilangan hasil kedelai akibat infeksi S. rolfsii diperkirakan mencapai 2.500
ton/tahun di Indonesia. Intensitas kerusakan tanaman kedelai yang terinfeksi patogen
tular tanah seperti S. rolfsii,Fusarium solani, dan Pythium sp. dapat mencapai 35% di
Nusa Tenggara Barat (Sudantha 1997).
Jamur patogen tular tanah memiliki kisaran inang yang luas dan beberapa
diantaranya mempunyai struktur istirahat, sehingga penyakit yang ditimbulkannya
menjadi sulit dikendalikan. S. rolfsii merupakan salah satu jenis jamur patogen tular
tanah yang dapat menyebabkan berbagai jenis penyakit pada lebih dari satu jenis
tanaman (Papuanga, 2008).
Rebah kecambah yang disebabkan oleh S. rolfsii merupakan penyakit penting
tanaman kedelai, terutama pada musim hujan atau pada lahan yang drainasenya buruk.
Infeksi S. rolfsii pada kedelai biasanya mulai terjadi di awal pertumbuhan tanaman
dengan gejala busuk kecambah atau rebah kecambah seperti yang ditunjukkan pada
Gambar 2.2.1. Pada tanaman kedelai berumur lebih dari 2-3 minggu, gejalanya berupa
busuk pangkal batang dan layu, pada bagian terinfeksi terlihat bercak berwarna coklat
pucat dan di bagian tersebut tumbuh miselia jamur berwarna putih (Punja, 1988;
Semangun, 1993).
Gejala serangan mulai tampak pada minggu kedua setelah inokulasi yang
ditandai dengan mulai membusuknya bagian pangkal batang, yaitu pada batas
permukaan tanah, diikuti dengan daun layu secara perlahan-lahan, kemudian
menguning dan mati. Pada tingkat serangan yang lebih lanjut pada bagian pangkal
batang terlihat adanya miselium jamur dan butir-butir sklerotia yang mula-mula
berwarna putih kemudian berubah menjadi coklat (Ratulangi, 2004).
2.4Pengendalian Hayati oleh Bakteri Kitinolitik
Pengendalian S. rolfsii umumnya secara mekanis dengan mencabut dan membuang
tanaman yang sakit. Cara pengendalian tersebut kurang efektif karena patogen masih
mampu bertahan lama di dalam tanah, dengan membentuk organ pembiakan, yaitu
sklerotia. Sklerotia merupakan pemampatan dari himpunan miselium jamur, warnanya
kecoklatan, berbentuk butiran kecil dengan diameter sekitar 1 mm, berkulit keras, dan
9
Pengendalian penyakit tanaman juga dilakukan dengan menggunakan senyawa
kimiawi. Namun demikian, penggunaannya yang berlebihan dan dalam jangka waktu
yang lama dapat berdampak negatif pada kesehatan manusia dan pencemaran
lingkungan. Oleh karena itu, diperlukan upaya penanggulangan alternatif untuk
mengendalikan jamur patogen tanaman misalnya dengan memanfaatkan agen
pengendali hayati yang lebih ramah lingkungan (Papuanga, 2009).
Pemanfaatan mikroorganisme untuk mengendalikan penyakit tanaman
merupakan bidang yang relatif belum lama berkembang. Pengendalian hayati jamur
penyakit tanaman sering menggunakan mikroorganisme seperti jamur dan bakteri
(Suryanto, 2009). Selain bakteri penghasil antibiotik, bakteri kitinolitik juga berperan
dalam pengendalian hama dan penyakit tanaman (Suryanto & Munir, 2006).
Degradasi kitin dapat dilakukan oleh mikroorganisme kitinolitik dengan
melibatkan enzim kitinase. Sebagian besar mikroorganisme ini ialah dari kelompok
bakteri, misalnya Streptomyces, Bacillus, Aeromonas, Serratia, dan Enterobacter.
Beberapa tumbuhan tingkat tinggi juga dilaporkan memiliki aktivitas kitinolitik.
Enzim kitinase yang dihasilkan oleh mikroorganisme kitinolitik memiliki banyak
kegunaan. Adanya enzim kitinase memungkinkan konversi kitin menjadi produk yang
berguna dalam industri pangan, kosmetik, farmasi dan lain-lain. Aplikasi lainnya dari
aktivitas kitinolitik adalah untuk pengendalian jamur patogen secara biologis
(Pujiyanto & Wijanarka, 2004). Bakteri antagonis Serratia marcescens menghasilkan
enzim glukanase dan kitinase. Enzim kitinase yang dilepas oleh bakteri antagonis ini
akan menyebabkan lisis pada ujung hifa. Bagian ujung hifa, sekat dan percabangan,
BAB 3
BAHAN DAN METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan dari bulan Januari 2012 sampai dengan September 2012
bertempat di Laboratorium Pengamatan Hama dan Penyakit, Medan Johor, UPT-Balai
Proteksi Tanaman Pangan dan Hortikultura 1 Medan dan Laboratorium Mikrobiologi
Departemen Biologi FMIPA Universitas Sumatera Utara Medan.
3.2 Alat dan Bahan
Alat yang digunakan dalam penelitian ini adalah: cawan Petri (petridish), tabung
reaksi, rak tabung reaksi, beaker glass, gelas ukur, pipet serologi, karet penghisap,
spatula, jarum ose, autoklaf, oven, mikroskop, jangka sorong nampan berukuran 38 x
30 x 7 cm, Bunsen, Erlenmeyer, inkubator, sprayer, hot plate, vortex, timbangan,
pipet tetes, object glass, cover glass, pinset, gunting, magnetic stirrer, cork borer, dan
botol selai.
Bahan-bahan yang digunakan dalam penelitian ini antara lain: 6 isolat bakteri
kitinase (Bacillus sp. BK13, Enterobacter sp. BK15, Bacillus sp. BK17, Enterobacter
sp. KR05, Enterobacter cloacae LK08, dan Enterobacter sp. PB17) dari laboratorium
Mikrobiologi Departemen Biologi Universitas Sumatera Utara, isolat Sclerotium
rolfsii, media potato dextrose agar (PDA), yeast extract, blank disc (Oxoid) dan
ketokonazol, kloramfenikol, kertas saring, spritus, medium garam minimum kitin
(MGMK) dengan pH 6,8, media glucose yeast broth (GYB), akuades, alkohol 70%,
aluminium foil, kapas, dan benih kedelai yang digunakan ialah varietas Anjasmoro
11
ditumbuhkan dalam media PDA dan diinkubasi pada suhu 28-30°C. Selanjutnya,
biakan isolat S. rolfsii disimpan di dalam kulkas hingga saatnya digunakan.
3.3 Isolasi Sclerotium rolfsii
Bagian tanaman kedelai yang menunjukkan gejala penyakit berupa layu tanaman,
daun menguning dan kering, pada bagian pangkal batang ditumbuhi miselium putih
seperti kapas halus yang disebabkan oleh S. rolfsii dipotong kemudian didesinfeksi
dengan larutan 2% NaClO selama 10 detik, dicuci dengan air steril sebanyak tiga kali
dan ditanam pada media PDA. Setelah miselium tumbuh diinokulasikan kembali pada
media PDA baru untuk mendapatkan biakan murni. Pengamatan untuk
mengidentifikasi dilakukan secara makroskopis dan mikroskopis. (Terlampir pada
Lampiran 1)
3.4 Uji Antagonis Isolat Bakteri Kitinolitik Terhadap Sclerotium rolfsii
Biakan jamur ditumbuhkan di tengah media MGMK ditambah yeast 2% dengan jarak
3,5 cm dari cakram tempat inokulum bakteri. Selanjutnya suspensi bakteri kitinolitik
yang telah dibuat dengan konsentrasi ≈ 108 sel/ml (standart 0,5 McFarland)
diinokulasikan pada cakram dengan diameter 0,6 cm di bagian tepi media sebanyak 10
μl seperti terlihat pada Gambar 3.4.1, dibuat 2 kali pengulangan. Biakan diinkubasi pada suhu 28-30oC. Media MGMK ditambah yeast 2% yang diinokulasi jamur
patogen saja digunakan sebagai kontrol. Akitivitas penghambatan ditentukan
berdasarkan zona hambat yang terbentuk di sekitar koloni. Pengamatan dimulai dari
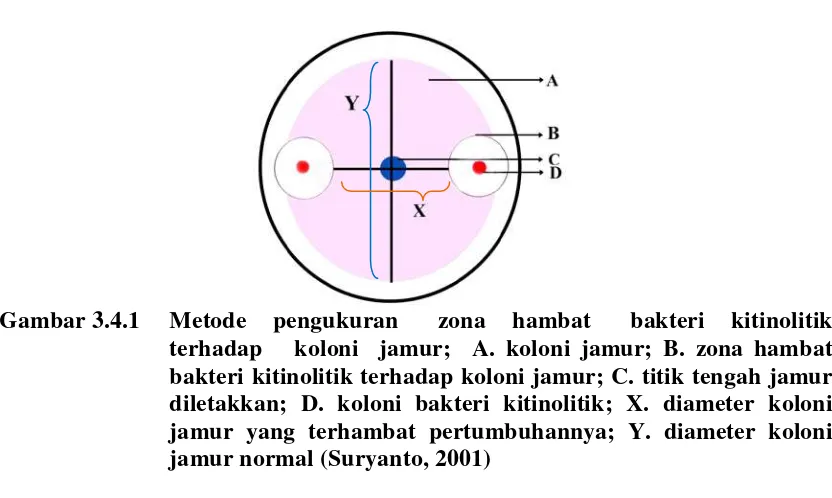
Gambar 3.4.1 Metode pengukuran zona hambat bakteri kitinolitik terhadap koloni jamur; A. koloni jamur; B. zona hambat bakteri kitinolitik terhadap koloni jamur; C. titik tengah jamur diletakkan; D. koloni bakteri kitinolitik; X. diameter koloni jamur yang terhambat pertumbuhannya; Y. diameter koloni jamur normal (Suryanto, 2001)
Pengukuran pertumbuhan Sclerotium rolfsii dilakukan dengan cara mengukur
batas akhir pertumbuhan dari jamur patogen pada sumbu X dan batas akhir
pertumbuhan fungi patogen pada sumbu Y (lihat skema di atas), dilakukan setelah
terjadi penghambatan bakteri kitinase terhadap fungi patogen dengan rumus uji
antagonis Y-X = hasil (Suryanto et al., 2011).
2
3.5 Pengamatan Struktur Hifa Abnormal
Pengamatan secara mikroskopis dilakukan dengan cara mengamati ujung miselium
pada daerah zona hambat jamur patogen. Ujung miselium S. rolfsii yang tumbuh pada
permukaan media PDA dipotong berbentuk block square, kemudian diletakkan pada
object glass. Kemudian, hifa diamati adanya abnormalitas pertumbuhan miselium
jamur patogen, berupa pembengkokan ujung miselium, miselium pecah, miselium
berbelah, miselium bercabang, miselium lisis dan miselium tumbuh kerdil (Lorito et
13
3.6 Uji Patogenitas Sclerotium rolfsii
Biakan S. rolfsii yang telah diremajakan di cawan Petri selama 7 hari diinokulasikan
pada 120 ml media GYB di dalam labu Erlenmeyer 250 ml dan diinkubasi pada suhu
28-30oC selama 10 hari. Sebanyak 120 ml suspensi biakan S. rolfsii dicampur dengan
600 g campuran tanah dan kompos steril (nisbah 3:1) di dalam nampan plastik
berukuran 30 x 38 x 7 cm. Sebanyak 30 benih kedelai ditanam ke dalam tiap nampan
lalu ditutup dengan plastik, dijadikan sebagai kontrol (+). Benih yang ditanam ke
dalam nampan yang tidak dicampur dengan suspensi jamur patogen tersebut
digunakan sebagai kontrol (-). Ulangan dilakukan sebanyak 3 kali pada perlakuan
patogenitas jamur. Peubah yang diamati adalah tanaman yang terserang rebah
kecambah selama masa persemaian 30 hari. Kemudian dihitung persentase jumlah
kecambah yang rebah. Persentase rebah kecambah dihitung dari jumlah kecambah
yang rebah dibagi jumlah seluruh kecambah yang tumbuh (Suryanto et al., 2010).
Reisolasi dilakukan terhadap Sclerotium rolfsii dengan memotong jaringan
pada pangkal batang kecambah yang menunjukkan gejala rebah kecambah. Jaringan
tersebut didesinfeksi dengan larutan 2% NaClO, dicuci dengan air steril sebanyak tiga
kali dan ditanam pada media PDA. Isolat yang diperoleh dibandingkan dengan isolat
sebelum jamur digunakan dalam uji patogenitas. (Terlampir pada Lampiran 2).
3.7 Penghambatan Serangan Sclerotium rolfsii pada Benih Kedelai
Sebanyak 120 ml suspensi biakan S. rolfsii dicampur dengan 600 g campuran tanah
dan kompos steril (nisbah 3:1) dalam nampan plastik berukuran 30 x 38 x 7 cm.
Sebanyak 30 benih kedelai yang telah direndam dalam suspensi bakteri kitinolitik
selama 30 menit ditanam ke dalam tiap nampan lalu ditutup dengan plastik, digunakan
sebagai perlakuan. Benih yang direndam dalam akuades yang tidak diinokulasi bakteri
kitinolitik kemudian ditanam ke dalam nampan digunakan sebagai kontrol (-).
Pemberian bakteri penghasil kitinase dilakukan untuk mengetahui pengaruhnya pada
benih kedelai. Perlakuan ini dilakukan dengan merendam benih dalam suspensi
paling berpotensi. Dua isolat yang telah diremajakan di cawan Petri tersebut
diinokulasikan ke dalam masing-masing tabung reaksi berisi akuades dan dibuat
dengan konsentrasi ≈ 108 sel/ml (standart 0,5 McFarland). Benih kedelai direndam
hingga seluruh benih terendam dalam media selama 30 menit. Sebanyak 30 benih
kedelai ditanam ke dalam tiap nampan lalu ditutup dengan plastik. Parameter yang
diamati adalah tanaman yang terserang rebah kecambah, tinggi tanaman dan jumlah
daun kecambah selama persemaian 30 hari (terlampir pada Lampiran 3). Menurut
Suryanto et al., (2010) Persentase rebah kecambah dihitung dari jumlah kecambah
yang rebah dibagi jumlah seluruh kecambah yang tumbuh, sedangkan pengurangan
persentase rebah kecambah dapat dihitung dengan rumus :
Pengurangan % rebah kecambah =
x 100%
Keterangan : Kontrol (+) = benih yang diinokulasikan S. rolfsii
Kontrol (-) = benih yang tidak diinokulasikan S. rolfsii
[{∑ (Kontrol(+)-∑(Kontrol(-)}-∑kecambah rebah]
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Isolasi dan Karakteristik Sclerotiumrolfsii
Hasil isolasi S. rolfsii dari tanaman kedelai dibiakkan pada media PDA seperti yang
ditunjukkan pada Gambar 4.1.1. Ciri-ciri koloni S. rolfsii pada media PDA secara
makroskopik ialah hifa berwarna putih, tidak membentuk spora, terbentuknya miselia
steril dan sklerotia pada hari ke-5. Sklerotia berwarna putih yang kemudian berubah
warna menjadi coklat muda hingga coklat kehitaman. Sklerotia tersebut dapat
berkecambah kembali. Ciri-ciri secara mikroskopik ialah hifa bersekat dan tidak
ditemukannya konidia. Hasil ini sesuai dengan yang dikemukakan Magenda et al.,
(2011).
Gambar 4.1.1 (a) Isolasi tanaman yang terinfeksi (1. kecambah kedelai, 2. hifa S. rolfsii), (b) biakan murni Sclerotium rolfsii pada media PDA umur 3 hari, dan (c) perkecambahan sklerotia pada media PDA (3. sklerotia coklat)
Menurut Magenda et al, (2011), S. rolfsii yang ditumbuhkan pada media PDA
memiliki miselium berwarna putih seperti kapas. Jamur patogen tular tanah ini
membentuk sklerotia yang dapat bertahan di dalam tanah selama 6-7 tahun. Sklerotia
yang dikultur pada PDA dapat berkecambah. Tipe perkecambahan sklerotia bersifat
4.2 Uji Antagonis Isolat Bakteri Kitinolitik terhadap Sclerotium rolfsii
Hasil uji antagonis 6 isolat bakteri kitinolitik (BK13, BK15, BK17, KR05, LK08,
PB17) terhadap S. rolfsii menunjukkan bahwa ada 5 isolat yang mampu menghambat
pertumbuhan S. rolfsii dengan kemampuan yang bervariasi. Kelima isolat tersebut
diantaranya BK15, BK13, BK17, KR05 dan PB17. Bentuk zona hambat tersebut dapat
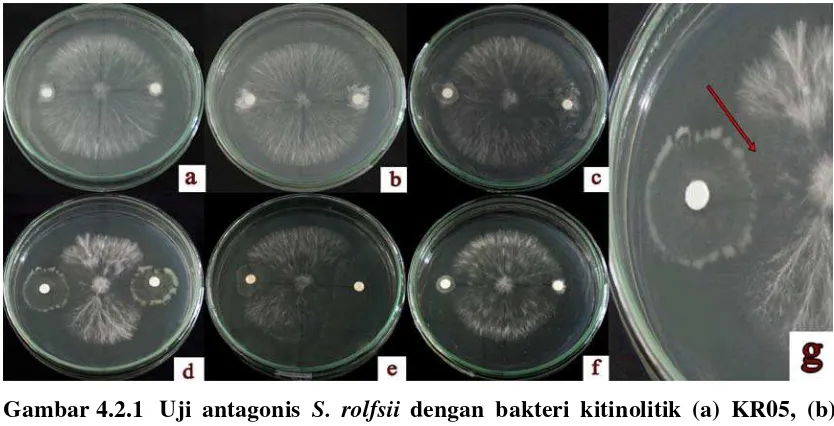
dilihat pada Gambar 4.2.1 di bawah ini:
Gambar 4.2.1 Uji antagonis S. rolfsii dengan bakteri kitinolitik (a) KR05, (b)
LK08, (c) PB17, (d) BK13, (e) BK15, (f) BK17 dan (g) zona hambat
Penghambatan bakteri kitinolitik terhadap pertumbuhan S. rolfsii mulai dapat
diamati pada hari kedua. Hal ini ditandai dengan adanya zona hambat disekitar daerah
tumbuhnya hifa jamur yang menunjukkan adanya aktivitas hidrolisis oleh kitinase
terhadap dinding sel jamur. Zona hambat ada yang terus bertambah dan ada pula yang
semakin berkurang hingga hari ketujuh. Hal ini bisa disebabkan oleh jenis strain
bakteri, jumlah senyawa antimikroba yang dihasilkan, konsentrasi dan kualitas
senyawa antimikroba serta adanya mekanisme penghambatan yang berbeda dari jamur
patogen. Hasil uji antagonis keenam isolat bakteri kitinolitik tersebut dapat dilihat
17
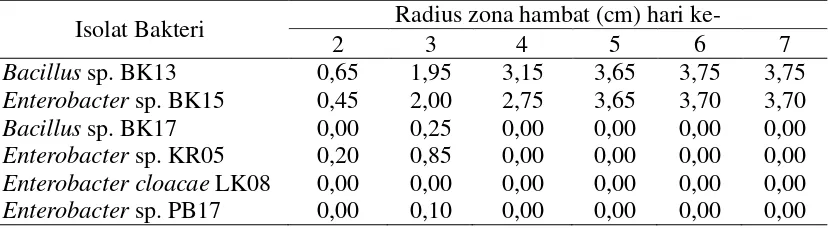
Tabel 4.2.1 Uji Antagonis antara Baketri Kitinolitik denganSclerotium rolfsii
Isolat Bakteri Radius zona hambat (cm) hari ke-
2 3 4 5 6 7
Isolat yang menunjukkan penghambatan paling besar terhadap Sclerotium
rolfsii pada hari ketujuh ialah isolat Bacillus sp. BK13 dengan zona hambat sebesar
3,75 cm dan Enterobacter sp. BK15 dengan zona hambat sebesar 3,70 cm. Isolat
BK17, KR05 dan PB17 hanya mampu menghambat hingga hari ketiga dengan zona
hambat secara berturut-turut yaitu 0,25 cm, 0,85 cm dan 0,1 cm. Setelah hari ketiga,
BK17, KR05 dan PB17 tidak memiliki zona hambat hingga hari ketujuh. Isolat LK08
sama sekali tidak menunjukkan adanya penghambatan terhadap S. rolfsii dari hari
pertama hingga hari ketujuh. Hal ini berbeda dengan penelitian yang dilakukan oleh
Suryanto et al., (2011), dimana Enterobacter cloacae LK08 masih memiliki
kemampuan dalam menghambat Fusarium oxysporum. Hal ini bisa disebabkan karena
beberapa faktor seperti komposisi kitin yang dimiliki oleh setiap jamur tidak sama.
Daya penghambatan terbesar pada pertumbuhan Sclerotiumrolfsii ditunjukkan
oleh bakteri kitinolitik BK13 dan BK15. Menurut Asril (2011), telah diketahui bahwa
BK13 merupakan Bacillus sp. (Gram positif). Sedangkan BK15 merupakan
Enterobacter sp. (Gram negatif). Berdasarkan penelitian Asril (2011), Enterobacter
sp. BK15 dan Bacillus sp. BK13 mampu menghambat pertumbuhan Fusarium
oxysporum dan Ganoderma boninense. Menurut Garderner (2004), beberapa strain
Bacillus juga menghasilkan toksin yang menghambat pertumbuhan atau aktivitas
jamur patogen. Menurut Chernin et al., (1995), sejumlah strain Enterobacter spp.
dapat digunakan sebagai biokontrol jamur patogen tanaman.
Bakteri BK17, KR05, dan PB17 kurang mampu menghambat pertumbuhan
Sclerotiumrolfsii. Ketiga isolat bakteri kitinolitik tersebut hanya mampu menghambat
melewati kertas cakram tempat dimana bakteri kitinolitik ditumbuhkan pada media
agar MGMK + yeast 2%. Hal ini disebabkan oleh spesifikasi yang berbeda dari
seluruh 6 isolat yang diuji, konsentrasi suspensi bakteri yang digunakan serta media
pembuatan suspensi. Dalam penelitian ini, media yang digunakan dalam pembuatan
suspensi ialah akuades steril. Oleh karena itu, beberapa sel bakteri tidak mendapat
nutrisi kemudian mati jika dibiarkan terlalu lama dalam suspensi. Menurut Nasikhah
(2008), kekurangan nutrisi ini disebabkan karena penyimpanan bakteri dilakukan
dalam air steril yang tidak bernutrisi.
4.3 Pengamatan Struktur Hifa Abnormal
Pengamatan mikroskopis untuk melihat hifa abnormal S. rolfsii dilakukan pada hari
ketujuh. Pertumbuhan hifa jamur tersebut yang dihambat oleh bakteri kitinolitik mulai
terlihat pada hari kedua. Hal ini dibuktikan dengan terbentuknya zona hambat oleh
bakteri kitinolitik. Penghambatan yang dilakukan oleh isolat bakteri kitinolitik
mengakibatkan terbentuknya pertumbuhan abnormal pada hifa. Aktivitas antagonis
bakteri kitinolitik menyebabkan hifa S. rolfsii menjadi abnormal seperti yang terlihat
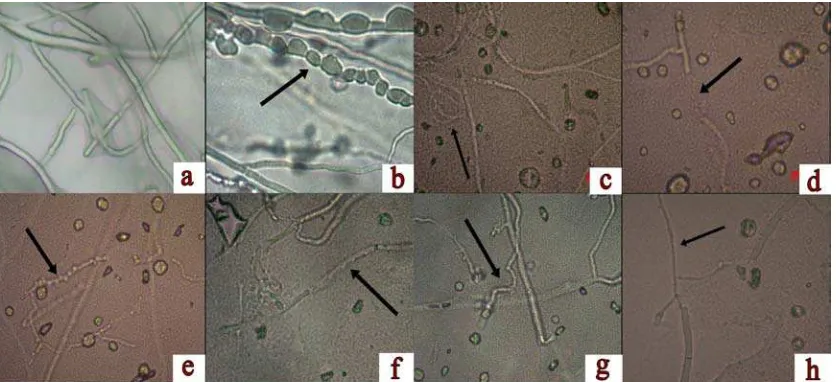
pada Gambar 4.3.1.
Hifa S.rolfsii mengalami berbagai perubahan bentuk hifa. Hal ini dipengaruhi
oleh adanya aktivitas bakteri kitinolitik yang dikultur di kedua sisi dengan jarak 3.5
cm dari tempat jamur di media MGMK + yeast 2%. Abnormalitas hifa jamur patogen
terlihat menggulung, lisis, putus, hifa menggembung, kerdil dan bengkok. Bakteri
tersebut memiliki mekanisme dalam menekan pertumbuhan jamur. Mekanisme
aktivitas antagonis yang diberikan oleh bakteri kitinolitik terhadap jamur patogen
ialah secara hiperparasitik dan enzimatik sehingga mampu digunakan sebagai
pengendalian hayati terhadap jamur patogen tanaman dengan cara mendegradasi
dinding selnya. Menurut Nurhayati (2011), mekanisme penghambatan patogen oleh
agen pengendali hayati dengan cara mengeluarkan metabolit seperti enzim. Kitinase
yang dihasilkan bakteri kitinolitik mengakibatkan terjadinya endolisis atau autolisis
yaitu pecahnya sitoplasma suatu sel sehingga terjadi kerusakan dinding sel. Hal ini
19
Gambar 4.3.1 Bentuk hifa Sclerotium rolfsii setelah uji antagonis dengan bakteri kitinolitik: (a) hifa normal, (b) hifa membengkak dan memendek oleh BK13, (c) hifa menggulung oleh BK15, (d) hifa putus oleh BK15, (e) hifa kerdil oleh BK15, (f) hifa lisis oleh BK15, (g) hifa bengkok oleh BK 15, dan (h) hifa mengecil oleh BK15 (h) (perbesaran 40 x 10)
4.4 Hasil Uji Patogenitas Sclerotiumrolfsii terhadap Kecambah Kedelai
Hasil uji patogenitas menunjukkan bahwa jamur tersebut bersifat patogen terhadap
benih kedelai yang ditanam pada media campuran tanah-kompos (nisbah 3:1) dan
suspensi S. rolfsii. Hal ini terbukti dengan adanya gejala penyakit rebah kecambah
pada kedelai. Gejala penyakit rebah kecambah diawali dengan adanya miselium putih
seperti kapas halus pada permukaan pangkal batang tanaman seperti yang ditunjukkan
pada Gambar 4.4.1. Miselium tersebut menyebabkan busuknya pangkal batang yang
ditandai dengan perubahan warna menjadi coklat pucat pada bagian yang terserang
sehingga menyebabkan kecambah menjadi rebah.
Menurut Sumartini (2012), pada permukaan tanah di sekitar tanaman yang
terserang terdapat miselium putih dan sklerotia. Serangan Sclerotium sp. diawali
dengan infeksi pada bagian akar atau batang yang berbatasan dengan permukaan
tanah. Infeksi pada tanaman tersebut menyebabkan pengangkutan unsur hara dan air
tersumbat sehingga tanaman menjadi layu lalu rebah. Patogen selanjutnya menyebar
Sclerotium rolfsii menyerang sebagian benih yang belum berkecambah dan
sebagian kecambah berumur 5 hari setelah tanam. Hifa jamur tersebut menginfeksi
bagian tanaman dari akar dan pangkal batang. Mekanisme penyerangan ialah hifa S.
rolfsii mensekresikan senyawa enzim ke bagian tanaman yang terinfeksi. Hal ini
mengakibatkan dinding sel terdegradasi. Menurut Papuanga (2009), hifa jamur
tersebut mensekresikan enzim selulolitik dan asam oksalat yang membuat jaringan
menjadi lunak kemudian mati. Hal tersebut mengakibatkan terganggunya jaringan
xilem dalam mengangkut air dan unsur hara. Menurut Abadi (2003), jamur patogen
penyebab layu umumnya berkolonisasi dalam jaringan vaskuler, khususnya pada
xilem.
Gambar 4.4.1 Uji Patogenitas S. rolfsii terhadap benih kedelai: (a) biakan S.
rolfsii umur 7 hari (1. hifa, 2. sklerotia coklat), (b) patogenitas S. rolfsii (3. kecambah kedelai yang terinfeksi, 4. S. rolfsii), (c) reisolasi (5. kecambah, 6. hifa jamur patogen) dan (d) biakan
murni S. rolfsii hasil reisolasi umur 5 hari (7. hifa, 8. sklerotia
putih)
Reisolasi S. rolfsii dilakukan dengan mengisolasi kembali sampel kecambah
kedelai yang terinfeksi miselium dari uji patogenitas pada media PDA seperti yang
terlihat pada Gambar 4.4.1. Hasil reisolasi mendapatkan adanya miselium putih di
sekitar bagian dari kecambah. Miselium jamur tersebut diinokulasi pada media PDA
yang baru untuk mendapatkan biakan murninya dan dibandingkan dengan S. rolfsii
hasil isolasi awal.
4.5 Penghambatan Serangan Sclerotiumrolfsii pada Benih Kedelai
Hasil uji antagonis menunjukkan bahwa 2 isolat yang berpotensial menghambat
21
dilakukan pengujian secara in vivo. Pengamatan persentase rebah kecambah, tinggi
tanaman, dan jumlah daun dilakukan mulai minggu pertama sampai minggu keempat.
Benih kedelai yang ditanam pada media campuran tanah dan kompos yang berisi S.
rolfsii rentan terserang rebah kecambah. Hal ini ditunjukkan oleh kontrol (+). Gambar
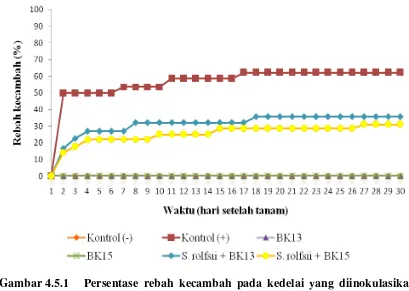
4.5.1 berikut ialah persentase rebah pada tiap perlakuan :
Gambar 4.5.1 Persentase rebah kecambah pada kedelai yang diinokulasikan
Sclerotium rolfsiidengan perlakuan bakteri kitinolitik
Gambar 4.5.1 menunjukkan bahwa serangan S. rolfsii mulai terjadi pada hari
kedua setelah tanam pada benih kedelai yang ditanam dalam nampan berisi campuran
tanah dan suspensi jamur patogen. Penyakit rebah kecambah pada kedelai mengalami
peningkatan dari minggu pertama sampai minggu keempat. Persentase rebah tertinggi
pada kontrol (+) yaitu sebesar 62,07 % dari seluruh benih yang tumbuh. Sebaliknya,
kontrol (-) tidak ditemukan adanya penyakit rebah kecambah.
Menurut Nurhayati (2011), penyakit tanaman dapat terjadi bila adanya
interaksi antara lingkungan, patogen dan tanaman itu sendiri. Patogenitas tinggi terjadi
apabila tanaman yang rentan terinfeksi patogen karena didukung oleh keadaan
lingkungan yang sesuai untuk tumbuhnya patogen. Menurut Sumartini (2012),
lembap. Jenis jamur ini dapat membentuk struktur dorman, yaitu sklerotia pada
permukaan tanah atau pangkal batang. Sklerotia mempunyai kulit tebal dan keras
sehingga tahan terhadap keadaan lingkungan yang tidak menguntungkan, terutama
kekeringan dan suhu tinggi. Masa dorman akan berakhir jika kondisi lingkungan
cocok untuk perkembangannya. Senyawa kimia yang bersifat menguap yang
dihasilkan oleh akar tanaman akan menstimulasi sklerotia untuk segera berkecambah
menjadi hifa yang siap menginfeksi bagian tanaman pada daerah rizosfer (zona
perakaran).
Perendaman benih kedelai dalam suspensi bakteri penghasil kitinase yaitu
Bacillus sp. BK13 dan Enterobakter sp. BK15 kemudian ditanam pada media tanah
yang tidak berisi jamur digunakan untuk mengetahui pengaruh kedua bakteri tersebut
pada benih. Hasil pengamatan menunjukkan, Bacillus sp. BK13 dan Enterobacter sp.
BK15 tidak menyebabkan penyakit rebah kecambah. Hal ini ditunjukkan oleh tidak
adanya nilai persentase rebah selama hari pengamatan.
Perlakuan S. rolfsii + BK13 dan S. rolfsii + BK15 menunjukkan penurunan
persentase rebah secara berturut-turut mencapai 35,72% dan 31,04%. Berdasarkan hal
tersebut, ada beberapa faktor yang menyebabkan persentase rebah kecambah menurun
yaitu pertahanan yang dilakukan oleh tanaman itu sendiri dan pertahanan yang
dilakukan oleh bakteri kitinolitik Bacillus sp. BK13 dan Enterobacter sp. BK15.
Menurut Pudjihartati et al., (2008) pemberian infeksi Sclerotiumrolfsii dapat memicu
tanaman inang mengeluarkan enzim kitinase dan senyawa pertanahan lainnya sebagai
sistem ketahanan terhadap jamur patogen. Faktor selanjutnya ialah kedua bakteri
kitinolitik yang diberikan yaitu Bacillus sp. BK13 dan Enterobacter sp. BK15 mampu
menghambat pertumbuhan jamur patogen S. rolfsii di lapangan. Hal ini terlihat dengan
adanya pengurangan persentase rebah kecambah dibandingkan dengan kontrol (+),
23
Gambar 4.5.2 Perbedaan tanaman kedelai umur 4 minggu (a) kontrol (-), (b) kontrol (+), (c) BK13, (d) BK15, (e) S. rolfsii + BK13, dan (f) S. rolfsii + BK15
Pengurangan persentase rebah tertinggi yaitu Enterobacter sp. BK15 yang
mencapai 50 %. Sedangkan pengurangan persentase rebah terendah yaitu Bacillus sp.
BK13 mencapai 44,5 %. Hal ini sedikit berbeda dengan data yang diperoleh ketika uji
in vitro, dimana Bacillus sp. BK13 menunjukkan daya penghambatan lebih besar
daripada Enterobacter sp. BK15. Perbedaan kecenderungan daya penghambatan
terhadap jamur patogen secara in vitro dan in vivo bisa terjadi karena pengaruh
lingkungan. Pada uji in vitro, kemampuan kedua bakteri tersebut sebagian besar bisa
dipengaruhi oleh ketersedian nutrisi media. Pada uji in vivo, kemampuan kedua
bakteri tersebut dipengaruhi oleh beberapa keadaan lingkungan sekitar seperti suhu,
cahaya matahari, kelembapan, dan media tanam serta patogenitas jamur yang bisa
didukung oleh keadaan lingkungan tersebut.
Menurut Abadi (2003), penyakit tanaman dapat terjadi karena adanya interaksi
antara patogen, tanaman inang dan faktor lingkungan. Namun, dari ketiga faktor
tersebut yang lebih sering berubah adalah faktor lingkungan. Hal ini disebabkan
karena faktor lingkungan dapat mendukung kerentanan tanaman inang saja atau hanya
mendukung kehidupan patogen saja, sehingga dapat mempengaruhi kemampuan agen
pengendali hayati yang digunakan untuk menghambat pertumbuhan jamur patogen di
Namun demikian, kedua bakteri kitinolitik yaitu Bacillus sp. BK13 dan
Enterobacter sp. BK15 telah mampu melindungi sebagian benih kedelai dari serangan
Sclerotium rolfsii selama masa perkecambahan. Berdasarkan sifat dan strain bakteri
kitinolitik yang diuji tersebut mengakibatkan sifat patogenitas jamur terhambat dan
menurun. Menurut Purwantisari et al., (2005), ada bebarapa cara penghambatan
serangan jamur patogen oleh bakteri kitinolitik. Pertama, bakteri menghasilkan
senyawa bioaktif yang dapat mendegradasi komponen struktural jamur. Senyawa
tersebut mendegradasi dinding sel jamur. Kedua, senyawa bioaktif juga
mempengaruhi permeabilitas membran sel jamur sehingga mengganggu transportasi
zat-zat yang diperlukan untuk metabolisme. Hal ini mengakibatkan metabolisme
jamur terganggu. Ketiga, senyawa yang dihasilkan bakteri dapat berfungsi sebagai
inhibitor terhadap suatu enzim yang dihasilkan oleh jamur. Apabila enzim jamur
tersebut berperang penting dalam metabolisme jamur, maka aktivitas enzimatik sel
akan terganggu. Akibatnya akan menekan pertumbuhan jamur. Mekanisme keempat,
yaitu senyawa yang dihasilkan oleh bakteri mampu menekan sintesis protein pada
jamur. Apabila sintesis protein terganggu menyebabkan jamur kekurangan protein
tertentu sehingga menyebabkan pertumbuhan jamur terganggu.
Menurut Gohel et al., (2005), enzim mikolitik (kitinase, protease, dan
glukanase) yang dihasilkan oleh mikroorganisme mampu melisiskan dinding sel jamur
dan berpotensial mengolah limbah kitin dengan menghasilkan kitinase. Oleh karena
itu, beberapa mikroorganisme kitinolitik berpotensial sebagai pengendali patogen
tanaman. Menurut Nalisha et al., (2006), Bacillus sp. menghasilkan senyawa bioaktif
antijamur yang dapat menghambat serangan Sclerotium rolfsii. Salah satu senyawa
yang efektif dihasilkan oleh Bacillus sp. dalam mengendalikan S. rolfsii ialah enzim
kitinase. Menurut Giyanto (2009), Bacillus sp. dapat dikembangkan menjadi pestisida
hayati karena memiliki beberapa sifat yang salah satunya ialah bersifat kitinolitik.
Pertumbuhan tanaman kedelai yang terganggu dapat diamati melalui parameter
seperti tinggi tanaman dan jumlah daun. Menurut Alcivar et al., (2007), tinggi dan
hasil tanaman berkurang bisa terjadi karena penyakit, defesiensi unsur hara, dan
kekurangan air. Gambar 4.5.2 menunjukkan perbedaan tinggi tanaman kedelai yang
25
Gambar 4.5.3 Perbedaan tanaman kedelai antara (a) kontrol (-) dan kontrol (+),
(b) BK13, (c) BK15, (d) S. rolfsii + BK13, dan (e) S. rolfsii + BK15
Pengamatan tinggi tanaman kedelai dilakukan setiap minggu. Pengukuran
tinggi tanaman dilakukan dengan mengukur tanaman mulai dari pangkal batang yaitu
bagian tanaman yang berbatasan dengan tanah sampai dengan ujung batang atau ujung
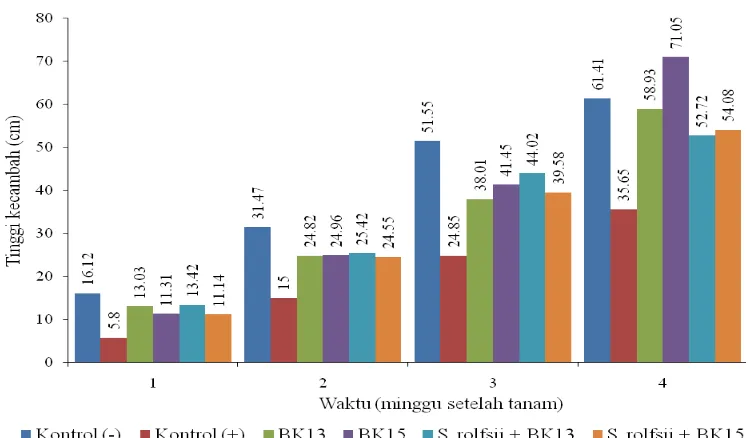
tunas apikal. Gambar 4.5.3 menunjukkan angka tinggi tanaman kedelai.
Gambar 4.5.4 Perbedaan tinggi tanaman kedelai yang diinokulasi Sclerotium rolfsii dengan perlakuan bakteri kitinolitik
Pertambahan tinggi tanaman kedelai meningkat setiap minggunya. Pada
pengamatan minggu pertama kecambah tertinggi ialah pada kontrol (-) yaitu sebesar
diperoleh data tanaman tertinggi ialah pada perlakuan pemberian bakteri kitinoitik
BK15 yaitu sebesar 71,05 cm. Tanaman terendah ialah kontrol (+) yaitu sebesar 35,65
cm. Hal ini disebabkan karena pengaruh besarnya serangan S. rolfsii. Serangan ini
menyebabkan pertumbuhan kecambah kedelai menurun. Hifa jamur patogen tersebut
mengkolonisasi dibagian pangkal batang yang kemudian mengganggu jaringan
pengangkut dalam menyalurkan air dan unsur hara ke bagian-bagian tanaman.
Pada perlakuan benih yang direndam dalam suspensi Bacillus sp. BK13 dan
Enterobacter sp. BK15 saja, tinggi tanaman kedelai berturut-turut ialah 58,93 cm dan
71,05 cm. Hal ini menunjukkan bahwa kedua bakteri tersebut tidak mengganggu
pertumbuhan dan tidak bersifat patogen terhadap benih kedelai yang ditanam selama
hari pengamatan. Menurut Siregar (2011), formulasi pupuk hayati yang berbahan
aktif rizobakteria seperti Bacillus sp. dapat memicu pertumbuhan tinggi kedelai.
Perlakuan benih yang direndam suspensi BK13 dan BK15 lalu diberi serangan S.
rolfsii menunjukkan tanaman kedelai lebih tinggi dari kontrol (+) dengan tinggi
berturut-turut yaitu 52,72 cm dan 54,08 cm. Hal ini bisa terjadi karena adanya
mekanisme pertahanan yang diberikan oleh Bacillus sp. BK13 dan Enterobacter sp.
BK15 dalam melindungi benih dari serangan jamur patogen.
Tanaman kedelai berumur 1-2 minggu yang terserang rebah kecambah akan
menunjukkan beberapa gejala yang salah satunya yaitu membuat daun menjadi kuning
dan mengering. Hal ini disebabkan karena jaringan pengangkut tidak mampu
menyalurkan air dan unsur hara dari akar hingga ke bagian tanaman yang
membutuhkan seperti daun. Jaringan yang berperan dalam melakukan asimilasi berada
di daun. Oleh karena jaringan tersebut tidak mendapat cukup air untuk melakukan
fotosintesis maka pertumbuhan tanaman terhambat. Jika hal ini berlanjut dalam waktu
yang lama mengakibatkan tanaman mengalami kematian. Menurut Ohorella (2011),
daun memegang peranan yang sangat penting bagi poduktivitas suatu tanaman.
Jumlah dan ukuran daun dipengaruhi oleh genotipe dan faktor lingkungan. Faktor
27
Jumlah daun setiap perlakuan tidak berbeda saat pengamatan minggu pertama,
seperti yang ditunjukkan oleh Gambar 4.5.4. Hal ini bisa disebabkan oleh kemampuan
benih untuk tumbuh dengan baik.
Gambar 4.5.5 Perbedaan jumlah daun tanaman kedelai yang diinokulasikan
Sclerotium rolfsii dengan perlakuan bakteri kitinolitik
Gambar 4.5.5 juga menunjukkan perbedaan jumlah daun baru terlihat pada
minggu ketiga hingga minggu keempat. Pada minggu keempat, jumlah daun terendah
ialah pada kontrol (+) yaitu sebanyak 4 helai daun trifoliat. Jumlah daun pada kontrol
(-), Bacillus sp.cBK13, dan Enterobacter sp. BK15 adalah sama yaitu sebanyak 5
helai daun trifoliat. Jumlah daun meningkat pada perlakuan BK13 dan BK15 yang
diinokulasikan Sclerotium rolfsii yaitu berturut-turut sebanyak 6 dan 7 helaian.
Kontrol (+) memiliki jumlah daun paling sedikit karena tanaman terserang
rebah kecambah sehingga pertumbuhan dan perkembangan tanaman menurun. Hal ini
dapat dilihat dari penambahan jumlah daun terhambat yang disebabkan karena air dan
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil penelitian yang dilakukan diperoleh kesimpulan sebagai berikut :
1. Isolat bakteri kitinolitik yang menunjukkan efektivitas tertinggi dalam
menghambat pertumbuhan Sclerotium rolfsii secara in vitro ialah Bacillus sp.
BK13 sebesar 3,75 cm dan Enterobacter sp. BK15 sebesar 3,70 cm.
2. Isolat bakteri kitinolitik yang mampu mengurangi persentase rebah semai yang
disebabkan oleh Sclerotium rolfsii secara in vivo ialah Enterobacter sp. BK15
sebesar 50% dan Bacillus sp. BK13 sebesar 44,5%.
3. Isolat bakteri yang paling berpotensial sebagai agen pengendalian hayati ialah
Enterobacter sp. BK15 dan Bacillus sp. BK13.
5.2 Saran
Perlu dilakukan penelitian lebih lanjut terhadap isolat kitinolitik ini seperti pencarian
media yang lebih cocok untuk pertumbuhannya agar tetap tumbuh lebih baik sehingga
DAFTAR PUSTAKA
Abadi, L. 2003. Ilmu Penyakit Tumbuhan II. Bayumedia Publishing. Malang. hlm: 7, 24, 130.
Agrios, G. N. 2004. Plant Pathology. Fifth Edition. Professor and Chairman Dept. of Plant Pathology University of Florida. Guinesville: Academic Press Inc. hlm: 601.
Alexopoulos, C.J. & Mims, C.W. 1979. Introductory Mycology. Third edition. John Wiley & Sons. New York. hlm: 191-205.
Alcivar, A., Jacobson, J., & Rainho, J. 2007. Genetic Analysis of Soybean Plant Height, Hypocotyl and Internode Lengths. Journal of Agricultural, Food, and Environmental Sciences. 1(1): 1-20.
Asril, M. 2011. Kemampuan Bakteri Tanah dalam Menghambat Pertumbuhan
Ganoderma boninense dan Fusarium oxysporumsecara in vitro dan Uji Penghambatan Penyakit Layu fusarium pada Benih Cabai Merah. Skripsi. FMIPA. USU. Medan.
Badan Pusat Statistik Republik Indonesia. 2009. Tabel Luas Panen-Produktivitas Produksi Tanaman Kedelai Seluruh Provinsi. Tanaman Pangan.
http
Chernin, L., Ismailov, Z., Haran, S., & Chet, I. 1995. Chitinolytic Enterobacter agglomerans Antagonistic to Fungal Plant Pathogens. Journal of Applied and Environmental Microbiology. 61(5): 1720-1726.
Djafaruddin. 2008. Dasar-dasar Pengendalian Penyakit Tanaman. Edisi Pertama. Jakarta: Bumi Aksara. hlm: 43.
Edmunds, B. A., & Gleason, M. L. 2003. Perennation of Sclerotium rolfsii var delphinii in Iowa. Plant Health Progress. Iowa State University.
Garderner, M.B.B. 2004. Ecology of Bacillus and Paenibacillus spp. In Agricultural System. Phytopathology. 94(11): 1252-1258.
Giyanto, Suhendar, A., & Rustam. 2009. Kajian Pembiakan Bakteri Kitinolitik
Formulasinya sebagai Pestisida Hayati (Bio-Pesticide). Prosiding Seminar Hasil-hasil Penelitian IPB. Bogor. hlm: 849-858.
Gohel, V., Singh, A., Vimal, M., Ashwini, P., & Chhatpar, H.S. 2006. Bioprospecting and Antifungal Potential of Chitinolytic Microorganisms. African Journal of Biotechnology. 5(2): 54-72
Hardaningsih, S. 2011. Jenis Penyakit Kedelai dan Efektivitas Jamur Antagonis yang Berasal dari Kalimantan Selatan Terhadap Sclerotium rolfsii di Laboratorium.
Suara Perlindungan Tanaman. 1(3): 23-28.
Hartati, S., Taufik, E., Supriadi., & Karyani, K. 2008. Karakteristik Fisiologis isolat
Sclerotium sp. Asal Tanaman Sambiloto. Jurnal Littri. 14(1): 25-29.
Lorito M.G., Harman E., Hayes C.K., Broadway R.M., Tronsmo S.L, Woo & Di Pietro A. 1993. Chitinolytic Enzymes Produced by Trichoderma harzianum: Antifungal Activity or Purified Endochitinase and Chitobiosidase. Phytopathol
83(3): 302-307.
Magenda, S., Kandao, F., & Umboh, S. 2011. Karakteristik Isolat Jamur Sclerotium rolfsii dari Tanaman Kacang Tanah (Arachis Hypogaea Linn). Jurnal Bioslogos.1(1): 1-7.
Muharni. 2009. Isolasi dan Identifikasi Bakteri penghasil Kitinase dari Sumber Air Panas Danau Ranau Sumatera Utara. Jurnal Penelitian Sains. Edisi Khusus: 73-78.
& Widjajanti, H. 2011. Skrining Bakteri Kitinolitik Antagonis Terhadap Pertumbuhan Jamur Akar Putih (Rigidoporus lignosus) dari Rizosfir Tanaman Karet. Jurnal Penelitian Sains.14(1): 51-56.
Nalisha, I., Muskhazli, M. & Nor Farizan, T. (2006). Production of Bioactive Compounds by Bacillus subtilis Against Sclerotium rolfsii.MalaysianJournal of Microbiology. 2(2): 19-23.
Mullen, J. 2001. Southern Blight, Southern Stem Blight, White Mold. The American Phytopathology Society. Amerika Latin: Auburn University.
31
Nurhayati. 2011. Penggunaan Jamur dan Bakteri dalam Pengendalian Penyakit Tanaman secara Hayati yang Ramah Lingkungan. Prosiding Semirata. UNSRI. Sumatera Selatan.
Ohorella, Z. 2011. Respon Pertumbuhan dan Produksi Tanaman Kedelai pada Sistem Olah Tanah yang Berbeda. Jurnal Agronomika. 1(2): 92-98.
Pal, K. K., & Gardener, B. M. 2006. Biological Control of Plant Pathogens. The Plant Health Instructor. hlm: 1-25.
Papuanga, N. 2009. Aktivitas Penghambatan Senyawa Antimikrob Streptomyces spp. Terhadap Mikroba Patogen Tular Tanah Secara In Vitro dan In Planta. Tesis. ITB. Bogor.
Pudjihartati, E., Siswanto, Ilyas, S., Sudarsono. 2006. Aktivitas Enzim Kitinase pada Kacang Tanah yang Sehat dan yang Terinfeksi Sclerotium rolfsii. Hayati Journal.13(2): 73-78.
Pujiyanto, S. & Wijanarka. 2004. Pemanfaatan Limbah Kulit Udang Sebagai Media Produksi Enzim Kitinase. Laporan Penelitian.
Punja, Z.K. 1988. Sclerotium (Athelia) rolfsii, a Pathogen of Many Plant Species.
Advances in Plant Pathology. 6: 523-535.
Purwantisari, S., Pujiyanto, S., Ferniah R. 2005. Uji Efektivitas Bakteri Kitinolitik sebagai Pengendali Pertumbuhan Kapang Patogen Penyebab Penyakit Utama Tanaman Sayuran dan Potensinya sebagai Bahan Biofungisidaramah Lingkungan. Laporan Penelitian. FMIPA UNDIP. Semarang.
Rahayu, M. 2008. Efikasi Isolat Pseudomonas fluorescens tehadap Penyakit Rebah Semai pada Kedelai. Penelitian Pertanian Tanaman Pangan. 27(8): 179-184.
Ratulangi, M.M. 2004. Control of Sclerotium Wilt Deaseas on Soybean by Soil Solarization. Eugenia 10(1): 1-7.
Sastrahidayat, I. R., Djauhari, S., & Saleh, N. 2011. Biocontrol of Sclerotium rolfsii
(Damping Off Disease) On Soybean Using Streptomyces sp. In Semi Natural Medium and Arbuscular Mycorrhizal Fungi. International Journal of Academic Research. 3(6): 283-288.
Semangun, H. 1993. Penyakit-penyakit Tanaman Pangan di Indonesia. Yogyakarta : Universitas Gadjah Mada. hlm: 128-129, 182-183.
Soesanto, L. 2008. Pengantar Pengendalian Hayati Penyakit Tanaman. Edisi Pertama. Jakarta : PT Raja Gravindo Persada. hlm: 340.
Sudantha, I.M. 1997. Pengendalian Patogen Tular Tanah pada Tanaman Kedelai secara Hayati Menggunakan Bahan Organik dan Trichoderma harzianum. Prosiding Kongres Nasinal XIV dan Seminar Nasional. Perhimpunan Fitopatologi Indonesia. Palembang. hlm: 444.
Sumartini. 2012. Penyakit Tular Tanah (Sclerotium rolfsii dan Rhizoctonia solani) pada Tanaman Kacang-kacangan dan Umbi-umbian serta Cara Pengendaliannya. Jurnal Litbang Pertanian. 31(1): 27-34.
Suryanto, D., Irawati, N., & Munir, E. 2011. Isolation and Characterization of Chitinolytic Bacteria and Their Potential to Inhibit Plant Pathogenic Fungi. Microbiology Indonesia. 5(2): 144-148.
Patonah, S., & Munir, E. 2010. Control of Fusarium Wilt of Chili With Chitinolytic Bacteria. Hayati Journal of Biosciences. 17(1): 5-8.
. 2009. Prospek Keanekaragaman Hayati Mikroba (Microbial Bioprospecting) Sumatera Utara. Pidato Pengukuhan Jabatan Guru Besar Tetap dalam Bidang Mikrobiologi. FMIPA USU. Medan.
& Munir, E. 2006. Potensi Pemanfaatan Isolat Kitinolitik Lokal untuk Pengendalian Hayati Jamur. Prosiding Seminar Hasil-hasil Penelitian. FMIPA USU. Medan.
LAMPIRAN
Lampiran 1
Isolasi dan Identifikasi
Dipotong pada bagian yang terserang Didesinfeksi dengan larutan NaClO 2% Dicuci dengan air steril sebanyak tiga kali Ditanam pada media PDA Diamati dan diidentifikasi
Uji Antagonis Isolat Bakteri Kitinolitik terhadapSclerotiumrolfsii
Diinokulasikan ditengah media MGMK + yeast 2% Diinokulasi sebanyak 10 µl suspensi bakteri 108 sel/ml pada kertas cakram
Diletakkan kertas cakram berdiameter 0,6 cm di tepi media dengan 2 kali ulangan
Diinkubasi pada suhu 28-30oC
Diamati pertumbuhan zona hambat pada hari ke-2 - ke-7 Kecambah Kedelai yang menunjukkan
gejala rebah kecambah
Hasil
Biakan S. rolfsii
Lampiran 2
Pengamatan Struktur Hifa Abnormal (Mikroskopis)
Diambil bagian hifa pathogen yang abnormal Diamati abnormalitas pertumbuhan hifa di bawah mikroskop
Dibandingkan dengan struktur hifa normal
Uji Patogenitas Sclerotiumrolfsii
Diambil sebanyak 120 ml
Dicampur dengan 600 g campuran tanah dan kompos steril (nisbah 3:1) di dalam tiap nampan Ditanam 30 benih tiap nampan
Ditutup nampan dengan plastik
Diamati tanaman yang terserang rebah semai/ kecambah selama 30 hari
Reisolasi
Dipotong pada bagian yang terserang Didesinfeksi dengan larutan NaClO 2% Dicuci dengan air steril sebanyak 3 kali Ditanam pada media PDA
35
Lampiran 3
Penghambatan SeranganSclerotium rolfsiipada Benih Kedelai
Diambil sebanyak 120 ml
Dicampurkan dengan 600 g campuran tanah dan kompos steril (nisbah 3:1) di dalam tiap nampan
Ditanam 30 benih kedelai yang telah direndam ke dalam suspensi bakteri kitinolik pada akuades, benih yang direndam pada akuades yang tidak diinokulasi bakteri kitinolitik dijadikan sebagai kontrol
Ditutup nampan dengan plastik
Diamati tanaman yang terserang rebah semai/kecambah selama 30 hari
Pengaruh Pemberian Bakteri Penghasil Kitinase dan Penyiapan Media Tanam
Dibuat hingga konsentrasi 108 sel/ml dalam akuades
Direndam benih kedelai selama 30 menit, benih yang direndam pada media akuades dijadikan sebagai kontrol
Ditanam ke dalam tiap nampan berisi 600 g campuran tanah dan kompos steril (nisbah 3:1) Ditutup nampan dengan plastik
Diamati pertumbuhan kedelai selama 30 hari
Suspensi Biakan S. rolfsii
Hasil
Suspensi bakteri Kitinolitik
Lampiran 4