TINJAUAN PUSTAKA
Botani Tanaman
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Rosales
Famili : Papilionaceae
Genus : Glycine
Species : Glycine max (L.) Merill
Sistem perakaran kedelai terdiri dari dua macam, yaitu akar tunggang dan akar
sekunder (serabut) yang tumbuh dari akar tunggang. Pertumbuhan batang kedelai
dibedakan menjadi dua tipe, yaitu tipe determinate dan indeterminate. Tanaman kedelai
mempunyai dua bentuk daun yang dominan dengan daun tunggal dan daun bertangkai
tiga (trifoliate leaves) yang tumbuh selepas masa pertumbuhan. Bunga sampai pemasakan biji. Polong kedelai pertama kali terbentuk sekitar 7-10 hari setelah
munculnya bunga pertama (Irwan, 2006).
Syarat Tumbuh Iklim
Kedelai dapat tumbuh baik ditempat yang berhawa panas, ditempat-tempat
terbuka dan bercurah hujan 100 – 400 mm3 per bulan. Kedelai kebanyakan ditanam
didaerah yang terletak kurang dari 400 m diatas permukaan laut dan jarang sekali
ditanam didaerah yang terletak kurang dari 600 m diatas permukaan laut (Sumarno dan
Pada suhu yang lebih tinggi dari 30 0C, fotorespirasi cenderung mengurangi hasil
fotosintesis (Sutedjo dan Kartasapoetra,1987). Rata-rata curah hujan tiap tahun yang
cocok bagi kedelai adalah kurang dari 200 mm dengan jumlah bulan kering 3-6 bulan
dan hari hujan berkisar antara 95-122 hari selama setahun (Irwan, 2006).
Tanah
Tanaman kedelai sebenarnya dapat tumbuh di semua jenis tanah, namun
demikian, untuk mencapai tingkat pertumbuhan dan produktivitas yang optimal, kedelai
harus ditanam pada jenis tanah berstruktur lempung berpasir atau liat berpasir. Faktor
lain yang mempengaruhi keberhasilan pertanaman kedelai yaitu kedalaman olah tanah
yang merupakan media pendukung pertumbuhan akar (Irwan, 2006).
Patogen penyebab penyakit Biologi patogen
Menurut Alexopoulos dan Mims (1979), S. rolfsii dapat diklasifikasikan sebagai berikut :
Kingdom : Mycetaceae
Divisi : Mycopyta
Kelas : Deuteromycetes
Ordo : Mycelia Steril
Famili : Agonomycetaceae
Genus : Sclerotium
Spesies : Sclerotium rolfsii Sacc.
panjang mencapai 350 μm (Semangun 1993). Hifa mempunyai satu atau lebih hubungan
jaringan yang sama. Sel hifa sekunder, tersier, dan seterusnya berukuran lebih kecil dari
sel primer dan mempunyai lebar 1,6–2 μm. Percabangannya membentuk sudut yang
lebih besar dan tidak mempunyai hubungan jaringan yang sama (Sumartini, 2012).
Untuk pemencaran dan untuk mempertahankan diri jamur membentuk sejumlah
sclerotia. Butir-butiran sclerotia mudah sekali lepas dan tersangkut air
(Semangun, 2004). Menurut Rahayu (2008), sklerotia merupakan pemampatan dari
himpunan miselia jamur, warnanya kecoklatan, berbentuk butiran kecil dengan diameter
1 mm, berkulit keras, dan mampu bertahan lama (dorman) di tanah dan residu tanaman.
Pada lapisan dalam sklerotia terdapat gelembung-gelembung yang merupakan
cadangan makanan. Bagian dalam sklerotia yang tua mengandung gula, asam amino,
asam lemak, dan lemak, sedangkan bagian dindingnya mengandung gula, kitin,
laminarin, asam lemak, dan β 1−3 glukosida. Permukaan sklerotium dapat
mengeluarkan eksudat berupa ikatan ion, protein, karbohidrat, enzim
endopoligalakturonase, dan asam oksalat. Asam oksalat yang dihasilkan S. rolfsii
bersifat racun terhadap tanaman (fitotoksik). S. rolfsii juga mengeluarkan L-prolin yang merupakan antibiotik terhadap bakteri tertentu. Selama masa awal pertumbuhannya,
pembentukan asam oksalat meningkat (Sumartini, 2012).
Gejala Serangan
Rebah semai yang disebabkan oleh jamur S. rolfsii merupakan penyakit penting tanaman kedelai, terutama pada musim hujan atau pada lahan yang drainasenya buruk.
Infeksi S. rolfsii pada kedelai biasanya mulai terjadi di awal pertumbuhan tanaman dengan gejala busuk kecambah atau rebah kecambah. Pada tanaman kedelai berumur
bagian terinfeksi terlihat bercak berwarna coklat pucat dan di bagian tersebut tumbuh
miselia (Gambar 1b) (Rahayu, 2008).
Gambar 1.Gejala serangan S. rolfsii di lapangan (a) pangkal batang terinfeksi di selimuti miselia (b) pangkal batang terinfeksi berwarna kecoklatan (c) pertumbuhan sclerotia muda pada tanah di sekitar perakaran terinfeksi.
Sumber : Foto langsung.
S. rolfsii pertama kali menyerang batang, meskipun mungkin menginfeksi beberapa bagian tanaman dibawah kondisi lingkungan yang sesuai termasuk akar, buah,
petiole, daun dan bunga. Tanda pertama infeksi, meskipun tidak terdeteksi adalah coklat
gelap pada batang atau di bawah tanah. Gejala pertama yang mungkin adalah proses
penguningan dan kelayuan pada daun, gejala berikutnya terlihat lapisan putih atau
benang miselium pada jaringan yang terinfeksi dalam tanah (Gambar 1a)
(Fichtner, 2006).
Faktor yang Mempengaruhi Perkembangan Penyakit
Sclerotium rolfsii merupakan salah satu jamur patogen yang dapat menyebabkan beberapa penyakit mematikan pada tanaman seperti busuk batang, layu dan rebah
kecambah. Jamur ini merupakan jamur tular tanah yang dapat bertahan lama dalam
bentuk sklerotia di dalam tanah, pupuk kandang, dan sisa-sisa tanaman sakit. Di
samping itu, jamur tersebut dapat menyebar melalui air irigasi dan benih pada lahan
yang ditanami secara terus menerus dengan tanaman inang dari S. rolfsii tersebut,
sehingga mengakibatkan turunnya produksi tanaman yang akan dipanen
(Magenda et al. 2011).
Perkembangan jamur terjadi lebih cepat pada tanaman yang diperlakukan
dengan sungkup daripada tanpa sungkup, hal ini dikarenakan perbedaan kelembaban.
Pada tanaman yang disungkup, kelembaban mencapai 90%. S. rolfsii dari kacang tanah semakin infektif pada kelembaban tinggi yang menyebabkan tingginya intensitas dan
luas serangan . Sebaliknya, pada kelembaban yang rendah akan memacu S. rolfsii untuk membentuk sklerotia (Gambar 1c) (Sukamto dan Dono, 2013).
Sclerotium rolfsii merupakan salah satu jamur patogen yang dapat menyebabkan beberapa penyakit mematikan pada tanaman seperti busuk batang, layu dan rebah
kecambah. Jamur ini merupakan jamur tular tanah yang dapat bertahan lama dalam
bentuk sklerotia di dalam tanah, pupuk kandang, dan sisa-sisa tanaman sakit. Di
samping itu, jamur tersebut dapat menyebar melalui air irigasi dan benih pada lahan
yang ditanami secara terus menerus dengan tanaman inang dari S. rolfsii tersebut (Magenda et al. 2011).
Pengendalian Penyakit
Pengendalian S. rolfsii selama ini hanya secara mekanis dengan mencabut dan membuang tanaman yang sakit. Cara pengendalian tersebut kurang efektif karena
patogen masih mampu bertahan lama di dalam tanah, dengan membentuk organ
pembiakan, yaitu sklerotia. Sklerotia merupakan pemampatan dari himpunan miselia
jamur, warnanya kecoklatan, berbentuk butiran kecil dengan diameter 1 mm, berkulit
tanaman, dan penggunaan mikroorganisme antagonis dalam upaya pengendalian
penyakit secara hayati (Rahayu, 2008).
Keberhasilan pengendalian hayati sangat dipengaruhi oleh daya antagonis atau
daya hambat yang dimiliki suatu isolat, atau jumlah inokulum yang digunakan, dan cara
aplikasinya (Cook & Baker 1996). Aplikasi P. fluorescens melalui penyelaputan benih (enkapsulasi), sangat sesuai dan praktis untuk pengendalian patogen tular tanah. Masalah yang perlu mendapat perhatian dalam penggunaan P. fluorescens selain daya hambat yang harus tinggi adalah konsentrasi aplikasi yang efektif (Rahayu, 2008).
Enkapsulasi
Enkapsulasi adalah suatu proses pembungkusan suatu bahan atau campuran
beberapa bahan dengan bahan lain. Bahan yang dibungkus atau bahan yang ditangkap
biasanya berupa cairan, walaupun ada juga yang berbentuk partikel padat atau gas yang
disebut sebagai bahan inti atau bahan aktif atau bahan
internal, sedangkan bahan yang berfungsi sebagai pembungkus disebut sebagai dinding
atau bahan pembawa atau membran. Proses enkapsulasi banyak digunakan untuk
mempertahankan flavor, asam, lipida, enzim, mikroorganisme, pemanis buatan, vitamin,
mineral, air, bahan pengembang, warna dan garam (Risch, 1995).
Penggunaan enkapsulasi dalam industri benih sangat efektif karena dapat
memperbaiki penampilan benih, meningkatkan daya simpan, mengurangi risiko tertular
penyakit dari benih di sekitarnya, dan dapat digunakan sebagai pembawa zat aditif,
Alginat
Alginat adalah zat koloidal hidrofilik yang diekstrasi dari ganggang laut
Macrocystis pyrifera dan Ascophyllum nodosum yang bersifat biokompatibel dan biodegradabel terdiri dari β-D manuronat dan α–L guluronat yang dihubungkan dengan
ikatan (1-4) dengan berbagai perbandingan. Alginat yang tersedia secara komersial
adalah dalam bentuk garamnya yaitu natrium alginat. Keunikan natrium alginat yaitu
perubahannya menjadi hidrogel dengan 95% molekul air di dalamnya, yang merupakan
syarat penting untuk penggunaan dalam menjebak senyawa. Ketika natrium alginat
bertemu dengan kation divalent seperti Ca+2 menghasilkan pembentukan gel dimana
residu G dari alginat yang mengikat ion Ca+2 (Wang et al. 2006).
Teknik enkapsulasi ini dikembangkan oleh Redenbaugh et al. (1985) dengan cara membungkus embrio somatik dengan natrium alginat, yaitu sejenis gel yang
diperkaya dengan hara, ZPT, mikroorganisme yang bersifat simbiosis misalnya
Rhizobium dan jamur VAM (Vesicular Arbuscular Mycorhyza) atau komponen lain yang berfungsi dalam perkecambahan. Semakin tinggi konsenterasi alginat yang
digunakan akan mengakibatkan semakin padat kapsul yang terbentuk dan semakin
sempurna membungkus bibit mikro (Warnita dan Suliansyah, 2008).
Tapioka
Tepung tapioka mutlak diperlukan sebagai perekat antar komponen bahan
enkapsulasi dengan benih. Enkapsulasi dapat melindungi benih selama penyimpanan
BiologiTrichodermasp
Menurut Alexopoulos dan Mims (1979), Trichoderma sp. dapat diklasifikasikan sebagai berikut :
Kingdom : Mycetaceae
Divisi : Amastigomycota
Kelas : Denteromycetes
Ordo : Moniliales
Famili : Moniliaceae
Genus : Trichoderma
Spesies : Trichoderma harzianum Trichoderma koningii Trichoderma viridae
Pertumbuhan koloni Trichoderma mula-mula berbentuk anyaman miselium
dengan permukaan yang putih mulus berair dan kemudian berambut banyak karena
terjadinya pembentukan hifa-hifa baru. Selanjutnya koloni Trichoderma akan
berubah warna dan kelihatan hijau pekat sedangkan bagian bawahnya tetap tidak
berwarna. Miselium Trichoderma terdiri dari hifa-hifa yang transparan, berdinding
mulus, bersepta dan bercabang banyak. Hifa ini sering membentuk klamidiospor yang
timbul dalam posisi interseluler. Konidiofor akan muncul pada daerah percabangan
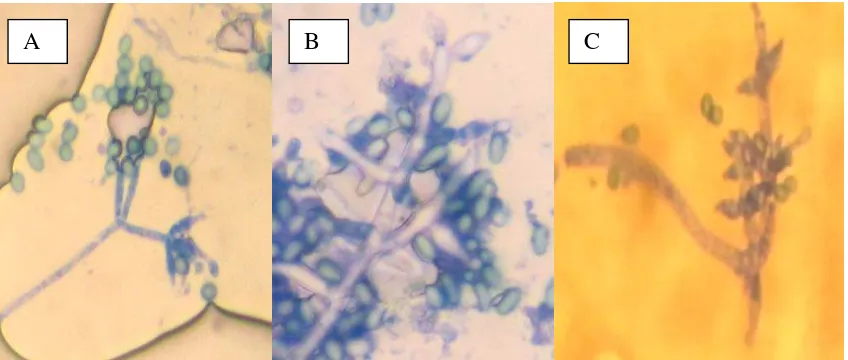
pada miselia. Konidia dapat dihasilkan dari ujung phialides (Gambar 2)
(Hasibuan, 2005).
Trichoderma sp. indigenus mampu memanfaatkan nutrisi, ruang dan tempat tumbuh, serta mampu menghasilkan senyawa antibiosis yang menyebabkan
mikoparasit bagi jamur lain dengan tumbuh mengelilingi miselium patogen dan
menghasilkan enzim dari dinding miselia atau disebut dengan senyawa antibiosis yang
dapat menghambat bahkan membunuh patogen. Trichoderma sp. menghasilkan zat antibiotik lain seperti trichotoxin yang dapat menyebabkan hifa patogen mengalami lisis (Supriati et al. 2008).
Trichoderma mempunyai kemampuan menghasilkan kitinase. Enzim kitinase yang dihasikan oleh Trichoderma sp lebih efektif dibandingkan kitinase yang dihasilkan oleh organisme lain untuk menghambat berbagai fungi patogen tanaman. Kitinase
berperanan penting dalam pengendalian fungi patogen tanaman secara mikoparasitisme
(Umrah et al. 2009).
Gambar 2. Mikroskopis fungi (A) T. viridae (B) T. koningii (C) T. harzianum, Sumber : Foto langsung pada perbesaran 40 x 10.
Trichoderma spp. mempunyai konidia yang berdinding halus koloni mula-mula berwarna hialin, lalu menjadi putih kehijauan, dan selanjutnya hijau tua terutama pada
bagian yang menunjukkan banyak terdapat konidia. Konidiofor dapat bercabang
menyerupai piramida yaitu pada bagian bawah cabang lateral yang berulang-ulang,
sedangkan semakin ke ujung percabangan menjadi bertambah pendek. Phialid tampak C
B
A B
langsing dan panjang terutama pada apeks dari cabang. konidia berbentuk semi bulat hingga
oval pendek (Purwantisari dan Hastuti, 2009).
Koloni jamur T.viridae tumbuh cepat, tiga hari setelah inokulasi menutupi cawan petri (90,00 mm), berwarna putih, setelah terbentuk konidia berubah menjadi
hijau tua. Phialospore bentuk bulat, warna hijau dan diameter 3 – 5 µ. Phialide
terbentuk 2 – 3 pada ujung percabangan konidiofor, dan pada tiap ujung phialide
terbentuk phialospore (Gambar 2a)(Sudantha, 2009).
Koloni T. harzianum tumbuh cepat , tiga hari setelah inokulasi menutupi cawan petri (90,00 mm). Setelah terbentuk konidia koloni berubah menjadi putih kehijauan.
Phialide tumbuh pada setiap ujung percabangan dan pada ujungnya
terdapt phialospore bentuk bulat sampai bulat lonjong, warna hijau pucat, berukuran 2,5 – 3,3 x 2,5 – 2,8µ (Gambar 2c) (Sudantha, 2009).
Secara makroskopis koloni jamur T. koningii pada usia 1-2 hari di awal pertumbuhan berupa miselium putih lembut yang kemudian pada usia 3 hari berubah
menjadi hijau gelap membentuk lingkaran yang beraturan. Pada usia 5 hari koloni
mencapai diameter 8 cm pada media PDA. Pengamatan secara mikroskopis
menunjukkan tipe konidiofor bercabang tidak beraturan. Cabang dengan arah tak
beraturan dan berdinding halus berbintil. Phialide tersusun berpasangan/tunggal dan tak beraturan. Konidia bulat atau lonjong sempit dengan diameter 1 μm dengan warna hijau
(Gambar 2b) (Wirawan et al., 2014).
T. harzianum menghasilkan beberapa antibiotik, di antaranya antibiotik peptaibol yang bekerja secara sinergis dengan enzim ß (1,3) glukanase, senyawa 3- (2 hidroksipropil)-4-(2-heksadienil)-2(5H) furanon karbohidrat, air, oksigen, energi dan
alkil piron (6-n-pentil-2H- piran-2-on atau 6PP) yang mampu mengubah penyebaran
biomassa cendawan dengan kisaran luas. Asam amino bebas seperti asam pembentukan
dinding sel hifa. T. harzianum secara in vitro juga dapat menurunkan patogenitas cendawan patogen (Mukarlina et al. 2010).
Dalam interaksi mikroparasitik Trichoderma sp. menghasilkan enzim-enzim litik pendegradasi dinding sel jamur inang. Endokitinase merupakan enzim yang
mempunyai aktivitas antifugal yang paling tinggi disbanding enzim-enzim yang lain
(Wibowo et al. 2003). Mekanisme pengendalian Trichoderma sp. yang bersifat spesifik target, membentuk koloni dengan cepat dan melindungi akar dari serangan jamur
patogen, mempercepat pertumbuhan tanaman dan meningkatkan hasil produksi
tanaman, menjadi keunggulan lain sebagai agen pengendali hayati. Beberapa
keunggulan Trichoderma sp. yang lain adalah mudah dimonitor dan dapat berkembang biak, sehingga keberadaannya di lingkungan dapat bertahan lama serta aman bagi
lingkungan (Siregar, 2011).
Trichoderma viridae adalah kapang berfilamen yang sangat dikenal sebagai organisme selulolitik dan menghasilkan enzim-enzim selullolitik, termasuk enzim
selobiohidrolase, endoglukanase dan ß-glukosidase. Kelebihan dari Trichoderma viridae selain menghasilkan enzim selulolitik yang lengkap, juga menghasilkan enzim xyloglukanolitik Keberadaan enzim ini akan semakin mempermudah enzim selulolitik
dalam memecah selulosa (Gunam et al. 2011).
Trichoderma koningii merupakan kompetitor yang kuat di daerah rhizosfer pada perakaran dan merupakan jamur antagonis yang sering digunakan dalam pengendalian
pada patogen dengan cara cendawan antagonis membelit hifa cendawan patogen
(Soenartiningsih et al. 2011).
Semua spesies Trichoderma sp. akan tumbuh baik disekitar perakaran tanaman yang sehat, sehingga terjadi simbiosis mutualisme antara jamur antagonis tersebut
dengan tanaman yang dilindunginya.. Mekanisme perlindungan tanaman oleh
Trichoderma sp. tidak hanya melibatkan serangan terhadap patogen pengganggu, tetapi juga melibatkan produksi beberapa metabolit sekunder yang berfungsi meningkatkan
pertumbuhan tanaman dan akar, dan memacu mekanisme pertahanan tanaman itu
sendiri (Agustina et al. 2013).
Trichoderma sp. akan mempertahankan bagian tanah sehingga akan membentuk struktur yang remah. Akar tanaman akan lebih mudah berkembang sehingga penyerapan
terhadap air dan kandungan unsur hara baik makro dan mikro lebih terpenuhi untuk