ARRIN ROSMALA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis yang berjudul Induksi Keragaman pada Stek Pucuk dan Kultur Kalus Handeuleum (Graptophyllum pictum L. Griff) Melalui Iradiasi Sinar Gamma adalah karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk karya apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2011
Arrin Rosmala
Handeuleum (Graptophyllum pictum L. Griff) Trough Gamma Rays Irradiation. Supervised by NURUL KHUMAIDA and DEWI SUKMA.
Handeuleum is medicinal plant that being used by Indonesian people for infection prevention after getting birth, body weight reduction, hemmoroids, abscess, ulcer healing, and prevention of plaque development on teeth. In handeuleum biomass production, Doleschallia bisaltidae attack can reduce its biomass yield up to 70%. That’s the reason to find handeuleum varieties which have better phytochemistry and resistance to pest. Since handeuleum cannot produced seeds, it always propagated vegetatively cause handeuleum has narrow variability. One of the ways improve handeuleum variability is through mutation induction with gamma irradiation which can applied both in vivo and in vitro. This aim of this study is to improve variability of handeuleum trough irradiation gamma rays in vivo (i.e. stem cutting of handeuleum accession Bogor) and in vitro (i.e. callus culture of handeuleum accession Kalimantan and Papua). The results indicate that gamma irradiation caused the diversity toward of cuttings handeuleum Bogor accession and callus culture handeuleum Kalimantan and Papua accession. The GR50 values of irradiation on handeuleum stem cuttings
could be observed on plant height, total number of leaves, leaf length, and leaf weight. Generally irradiation treatment dose 15 Gy, 30 Gy, and 45 Gy have higher value than control (0 Gy) at growth, leaves morphology, leaves anatomy of paradermal, and pigment content (anthochyanine, chlorophyll, and carotenoid) except leaves anatomy of paradermal variable. On the contrary at treatment dose irradiation 60 Gy, 75 Gy, 90 Gy, and 105 Gy on the same variables have lower value than control. Irradiation caused change in phythochemistry content, isozyme pattern (peroxidase (PER); esterase (EST); and acid phosphatase (ACP)), and phenotipic variability. Dose irradiation 45 Gy results the most putative mutant variation. Variability on experiment callus culture of handeuleum accession Kalimantan and Papua seen at callus variance value of relative rate growth, the most value is result by dose 25 Gy.
Handeuleum (Graptophyllum pictum L. Griff) Melalui Iradiasi Sinar Gamma. Dibimbing oleh NURUL KHUMAIDA dan DEWI SUKMA.
Handeuleum merupakan tanaman obat yang daunnya telah lama dimanfaatkan untuk mencegah infeksi setelah melahirkan, mengurangi berat badan, mengobati wasir, bisul, dan borok, serta mencegah pembentukan plak pada gigi. Handeuleum biasanya diperbanyak secara vegetatif karena biji sulit untuk terbentuk sehingga keragaman handeuleum menjadi sempit. Selain itu, handeuleum memiliki kendala dalam produksi biomassa daun yaitu adanya serangan larva Doleschallia bisaltidae yang menyebabkan penurunan hasil hingga 70%. Untuk meningkatkan keragaman, mendapatkan kandidat tanaman dengan kandungan fitokimia tinggi serta tahan hama adalah dengan induksi mutasi menggunakan iradiasi sinar gamma. Iradiasi dapat diterapkan pada tanaman in vivo dan in vitro. Penelitian ini secara umum bertujuan untuk meningkatkan keragaman handeuleum melalui iradiasi sinar gamma secara in vivo (stek pucuk) pada aksesi Bogor dan in vitro (kultur kalus) pada aksesi Kalimantan dan Papua.
Hasil penelitian ini menunjukkan bahwa iradiasi sinar gamma menimbulkan keragaman terhadap stek handeuleum aksesi Bogor dan terhadap kultur kalus handeuleum aksesi Kalimantan dan Papua. Percobaan iradiasi sinar gamma pada stek pucuk handeuleum aksesi Bogor menghasilkan nilai GR50 pada
peubah tinggi tanaman, jumlah daun, panjang daun, dan lebar daun. Umumnya perlakuan iradiasi dosis 15 Gy, 30 Gy, dan 45 Gy memiliki nilai pengamatan lebih besar bila dibandingkan dengan kontrol pada peubah pertumbuhan, morfologi daun, anatomi daun paradermal, dan kandungan pigmen (antosianin, klorofil, dan karotenoid) kecuali peubah irisan anatomi daun transversal. Sebaliknya untuk perlakuan iradiasi dosis 60 Gy, 75 Gy, 90 Gy, dan 105 Gy pada peubah yang sama memiliki nilai yang lebih kecil daripada kontrol. Iradiasi menyebabkan terjadi perubahan kandungan fitokimia, pola pita isozim (peroksidase (PER); esterase (EST); dan asam fosfatase (ACP)), serta menyebabkan keragaman fenotipik.
Variasi mutan putatif paling banyak dihasilkan oleh perlakuan iradiasi dosis 45 Gy. Keragaman akibat iradiasi sinar gamma pada percobaan kultur kalus
handeuleum aksesi Kalimantan dan Papua terlihat pada nilai ragam peubah rentang pertumbuhan kalus, dimana dosis 25 Gy menghasilkan nilai paling besar.
© Hak Cipta Milik IPB, tahun 2011 Hak Cipta Dilindungi Undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan sebagian besar pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
ARRIN ROSMALA
Tesis Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Mayor Agronomi dan Hortikultura
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama : Arrin Rosmala
NRP : A252070081
Disetujui Komisi Pembimbing
Dr. Ir. Nurul Khumaida, M.Si. Ketua
Dr. Dewi Sukma, S.P., M.Si. Anggota
Diketahui
Koordinator Mayor Agronomi dan Hortikultura
Dekan Sekolah Pascasarjana
Dr. Ir. Munif Ghulamahdi, M.S. Dr. Ir. Dahrul Syah, M.Sc. Agr.
rahmat-Nya penulisan tesis ini berhasil diselesaikan. Tesis ini berjudul Induksi Keragaman pada Stek Pucuk dan Kultur Kalus Handeuleum (Graptophyllum pictum L. Griff) Melalui Iradiasi Sinar Gamma.
Terima kasih penulis sampaikan kepada Dr. Ir. Nurul Khumaida, M.Si. dan Dr. Dewi Sukma, S.P., M.Si. atas bimbingannya selama penelitian dan atas sarana penelitian yang diberikan. Penulis juga mengucapkan terima kasih kepada Dr. Muhamad Syukur, SP., M.Si, selaku dosen penguji luar komisi atas masukan dan saran yang diberikan demi kesempurnaan tesis ini. Tidak lupa penulis mengucapkan terima kasih kepada Dr. Ir. Munif Ghulamahdi, M.Si, selaku Ketua Mayor Agronomi dan Hortikultura.
Penghargaan juga penulis sampaikan kepada Ibu Ir. Nova Kristiana dan staf kebun dari BALITTRO, serta Pak Ir. Ahmad Riyadi, M.Si. atas penyediaan bahan tanaman untuk penelitian ini. Kepada Ibu Siti Kholifah, Ibu Juju Juariah, Pak Prayitno, Pak Milin, Pak Joko, Pak Atang, Pak Prasetyo, dan Pak Yudi yang telah banyak membantu selama penelitian. Tidak lupa penulis juga mengucapkan banyak terima kasih kepada Nofia Hardarani, Dwi Rahayu, Dewi Cakrawati, Susi Purwiyanti, Rina Hidayati Pratiwi, Dian Novita, Pienyani Rosawanti, Joan Joulanda Grace Kailola, Aries Kusumawati, Puji Lestari, Richenly Nanlohy, Odit Ferry, Leo Mualim, Syukur Karamang, Tisna Prasetyo, Ahmad Rifqi Fauzi, Pak Nur Arifin, Ibu Atra Romeida, Ibu Kartika Ning Tyas, Lya Nur Yulyaningsih, Mutty Ebtessam, Utami Nurani Putri, Rheka Endalia Meina, Ibu Acih, rekan-rekan mayor AGH 2007 (S-3), PBT 2007 dan 2008, serta kepada teman-teman di Jasminer’s atas persahabatan yang terjalin. Terakhir penulis mengucapkan terima kasih kepada papah, mamah, kakakku Mia Anin Rahmania, adik-adikku: Attin Rachmawati dan Alin Rosliana atas doa, dukungan dan kasih sayang yang tidak pernah berhenti mengalir.
Sebagian dari karya ilmiah ini rencananya akan dimasukkan ke dalam Jurnal Agronomi Indonesia, dan sebagian lagi ke dalam Jurnal Hayati. Semoga Karya Ilmiah ini bermanfaat untuk banyak pihak.
Bogor, Agustus 2011
Halaman
INDUKSI KERAGAMAN PADA STEK PUCUK HANDEULEUM (Graptophyllum pictum L. Griff) AKSESI BOGOR MELALUI IRADIASI SINAR GAMMA
Tinggi Tanaman, Jumlah Daun, Panjang Daun dan Lebar Daun 28 Warna Daun, Tekstur Daun, Warna Batang, Indeks Warna Hijau Relatif Daun ... 33
Kandungan Antosianin, Klorofil Total, dan Karotenoid ... 35
Anatomi Daun ... 39
Gamma ... 58
Simpulan ... 64
Saran ... 65
INDUKSI KERAGAMAN PADA KULTUR KALUS HANDEULEUM (Graptophyllum pictum L. Griff) AKSESI KALIMANTAN DAN PAPUA MELALUI IRADIASI SINAR GAMMA Abstrak ... 67
Pendahuluan ... 68
Tujuan ... 69
Hipotesis ... 70
Metodologi Penelitian ... 70
Waktu dan Tempat ... 70
Analisis Data ... 75
Hasil dan Pembahasan ... 75
Kondisi Umum ... 75
Waktu Inisiasi Kalus, Jumlah dan Persentase Jumlah Eksplan Berkalus dan Bobot Kalus ... 76
Warna dan Tekstur Kalus ... 80
Bobot Kalus Proliferasi ... 83
Iradiasi Sinar Gamma Kalus ... 84
Keragaman Kalus Hendeuleum Akibat Iradiasi Sinar Gamma .. 90
Simpulan ... 91
Saran ... 92
PEMBAHASAN UMUM ... 93
SIMPULAN UMUM DAN SARAN Simpulan ... 99
Saran ... 99
1 Kriteria penilaian kandungan metabolit sekunder secara kualitatif
dengan uji fitokimia ... 20
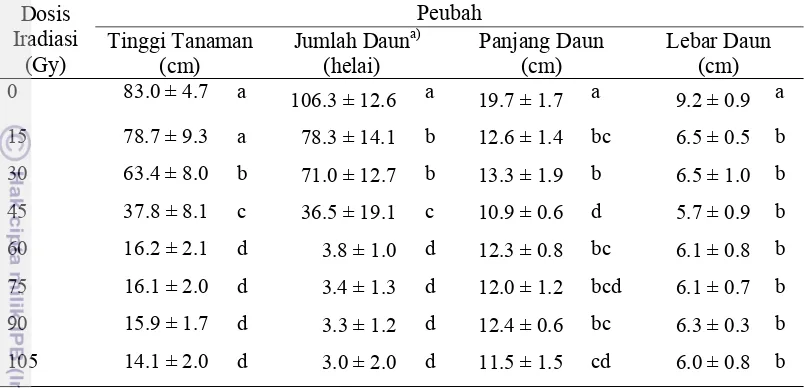
2 Nilai rata-rata tinggi tanaman, jumlah daun, panjang daun, dan lebar daun handeuleum aksesi Bogor pada berbagai perlakuan dosis iradiasi sinar gamma pada 10 MST ... 29
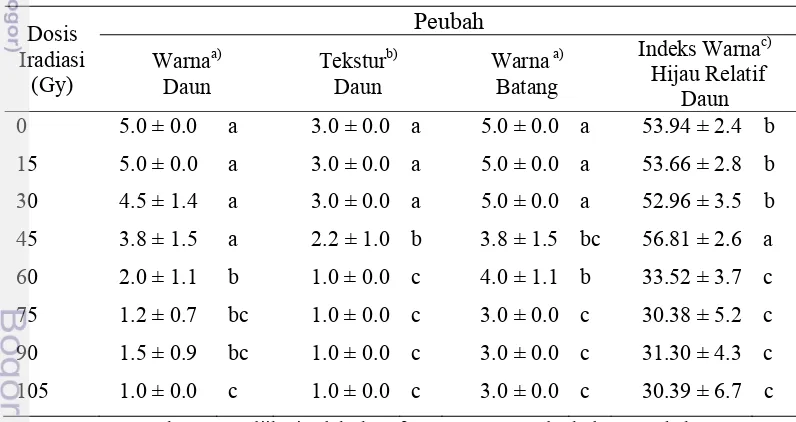
2 Nilai rata-rata warna daun, tekstur daun, warna batang, dan indeks
warna hijau relatif daun handeuleum aksesi Bogor pada berbagai perlakuan dosis iradiasi sinar gamma pada 10 MST ... 33
3 Nilai rata-rata jumlah stomata, jumlah sel epidermis, indeks stomata, dan kerapatan stomata daun handeuleum aksesi Bogor pada berbagai
perlakuan dosis iradiasi sinar gamma pada 10 MST ... 40
4 Nilai rata-rata tebal daun, tebal kutikula, tebal epidermis atas, panjang palisade, tebal bunga karang, dan tebal epidermis bawah daun
handeuleum aksesi Bogor pada berbagai perlakuan dosis iradiasi sinar
gamma pada 10 MST ... 45
5 Korelasi antara karakter pertumbuhan, morfologi, anatomi, dan
pigmen pada tanaman handeuleum aksesi Bogor ... 49
6 Kandungan fitokimia daun handeuleum aksesi Bogor yang diiradiasi
dengan sinar gamma pada 10 MST ... 51
7 Keragaman fenotipik handeuleum aksesi Bogor akibat dosis iradiasi
sinar gamma pada 10 MST ... 59
8 Keragaman regeneran mutan putatif handeuleum hasil perlakuan
dengan iradiasi sinar gamma pada 3 BST ... 62
9 Waktu inisiasi kalus, jumlah eksplan berkalus, persentase jumlah eksplan berkalus, bobot kalus pada tahap induksi kalus handeuleum
aksesi Kalimantan dan Papua ... 78
10 Interaksi antara komposisi media proliferasi dan aksesi terhadap
kalus handeuleum aksesi Kalimantan dan Papua ... 83
11 Interaksi antara aksesi, dosis iradiasi, dan media regenerasi terhadap
Bobot kalus subkultur 1 dan bobot kalus subkultur 2 setelah iradiasi .... 85
1 Kerangka berpikir peningkatan keragaman pada stek pucuk handeuleum aksesi Bogor dan kultur kalus handeuleum aksesi
Kalimantan dan Papua melalui iradiasi sinar gamma ... 4
2 Keragaan handeuleum. Tanaman utuh (kiri) dan bunga (kanan) aksesi
Bogor ... 6
3 Keragaan daun handeuleum aksesi Bogor tanpa dan yang diiradiasi dengan berbagai dosis sinar gamma; ovate (a), obovate (b),
lancoleate (c), kontrol (0 Gy) (d), 15 Gy (e), 30 Gy (f), 45 Gy (g),
60 Gy (h), 75 Gy (i), 90 Gy (j), dan 105 Gy (k) ... 23
4 Keragaan tanaman handeuleum pada berbagai perlakuan iradiasi sinar gamma: kontrol (0 Gy) (a), 15 Gy (b), 30 Gy (c), 45 Gy (d), 60 Gy (e), 75 Gy (f), 90 Gy (g), dan 105 Gy (h). Terlihat bahwa daun pada perlakuan 60 Gy, 75 Gy, 90 Gy, dan 105 Gy memiliki warna
yang berbeda dengan kontrol ... 24
5 Pengaruh dosis iradiasi sinar gamma terhadap GR50 tinggi tanaman
handeuleum aksesi Bogor ... 26
6 Pengaruh dosis iradiasi sinar gamma terhadap GR50 jumlah daun
handeuleum aksesi Bogor ... 26
7 Pengaruh dosis iradiasi sinar gamma terhadap GR50 panjang daun
handeuleum aksesi Bogor ... 27
8 Pengaruh dosis iradiasi sinar gamma terhadap GR50 lebar daun
handeuleum aksesi Bogor ... 27
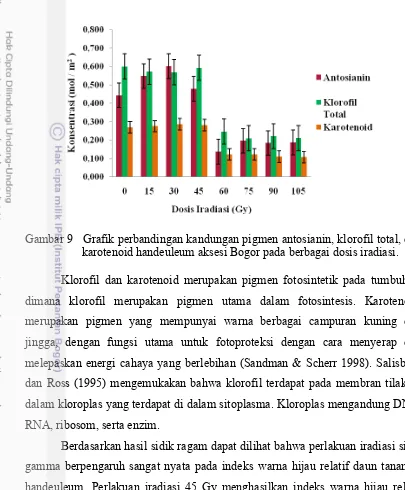
9 Grafik perbandingan kandungan pigmen antosianin, klorofil total, dan
karotenoid handeuleum aksesi Bogor pada berbagai dosis iradiasi ... 36
10 Irisan paradermal daun handeuleum aksesi Bogor (400x): sel
epidermis (a), sel tetangga (b), sel penjaga (c), lubang stomata (d) ... 40
13 Perbandingan struktur anatomi daun handeuleum aksesi Bogor irisan transversal: (a) 0 Gy (kontrol), (b) 15 Gy, (c) 30 Gy, (d) 45 Gy, (e) 60 Gy, (f) 75 Gy, (g) 90 Gy, (h) 105 Gy Semakin tinggi dosis iradiasi, kandungan antosianin semakin berkurang yang berkurang
yang ditunjukkan oleh warna merah ... 47
14 Ilustrasi lintasan metabolik primer pada tanaman (dimodifikasi) menurut Kaufman et al. (1999) ... 50
15 Interpretasi variasi pola pita isozim peroksidase (PER) ... 54
16 Interpretasi variasi pola pita isozim esterase (EST) ... 55
17 Interpretasi variasi pola pita isozim alkohol dehidrogenase (ADH) ... 56
18 Interpretasi pola pita isozim asam fosfatase (ACP) ... 56
19 Interpretasi variasi pola pita isozim enzim malat dehidrogenase (MDH) ... 57
20 Keragaan variasi morfologi handeuluem aksesi Bogor pada berbagai perlakuan iradiasi sinar gamma: Keragaan daun pada dosis 15 Gy (a),30 Gy (b),45 Gy (c); Keragaan tunas pada dosis 0 Gy (d), 45 Gy (e),60 Gy (f); 75 Gy (g); Keragaan warna daun yang umumnya muncul pada penelitian ini: ungu (skoring 5) (h), ungu kehijauan (skoring 3) (i), hijau (skoring 1) (j); Keragaan warna batang yang umumnya muncul pada penelitian ini: ungu (skoring 5) (k), ungu kehijauan (skoring 3) (l), hijau (skoring 1) (m) ... 61
21 Keragaan handeuleum. handeuleum di lapang (a); potongan daun asenik untuk inisiasi kalus pada media perlakuan (b) ... 75
22 Hubungan antara konsentrasi 2.4D dengan bobot kalus dua aksesi handeuleum pada konsentrasi NAA 10 dan 15 µM ... 79
23 Warna kalus pada induksi kalus dari dua aksesi handeuleum: putih (a), putih bening (b), cokelat (c) ... 80
24 Pengaruh kombinasi media terhadap warna kalus dua aksesi handeuleum ... 81
27 Warna kalus handeuleum yang diiradiasi: putih kecokelatan (a),
cokelat keputihan (b), cokelat (c), cokelat kehitaman (d), hitam (e) ... 89
28 Radikal bebas primer (*OH, H*) dan sekunder (H2O2, O2*-) terlibat
pada stres okidatif yang diproduksi oleh IR. eaq- : solvated electron/
elektron terhidrasi ; H2O*: molekul air yang tereksitasi (Esnault et al.
Halaman
1 Analisis fitokimia ... 113
2 Analisis klorofil dan anthosianin ... 114
3 Analisis isozim ... 115
Latar Belakang
Dewasa ini, terdapat kecenderungan pola hidup kembali ke alam (back to
nature), dimana masyarakat lebih memilih untuk menggunakan obat alami yang memiliki harga terjangkau dan dipercaya tidak memiliki efek samping
dibandingkan dengan obat-obatan sintetik. Pramono (2002) mencatat bahwa
terdapat peningkatan tren pasar dunia obat herbal sebesar 13%, dimana nilai
perdagangan tercatat sebesar US$20 milyar pada tahun 2000. Biofarmaka (2002)
menambahkan pada tahun 2001 terjadi peningkatan penjualan menjadi
US$45 milyar. Indonesia sendiri pada tahun 2004 terjadi peningkatan omzet
industri jamu nasional sebesar 15 - 20% (Rp3.2 - 3.5 triliun) dari tahun 2003.
Handeuleum (Graptophyllum pictum L. Griff.) merupakan tanaman obat
yang layak dikembangkan sebagai salah satu tanaman obat unggulan asli
Indonesia. Tanaman ini telah lama dimanfaatkan sebagai obat tradisional untuk
menyembuhkan berbagai macam penyakit. Orang Sunda menggunakannya untuk
mencegah infeksi setelah melahirkan, mengembalikan stamina, menormalkan
kembali ukuran rahim, membersihkan rahim dari darah putih, merangsang
produksi ASI, dan mengurangi berat badan (Bermawie et al. 2006). Kearifan lokal
penggunaan obat ini sebagai obat tradisional juga dilaporkan di Pangalengan Jawa
Barat sebagai obat wasir; di Maluku handeuleum yang dikenal sebagai alifuru
dimanfaatkan sebagai obat bisul, darah tinggi, rematik, dan lain-lain; dan
masyarakat Papua menggunakan handeuleum untuk mengatasi penyakit ulu hati,
diabetes, dan batu ginjal (Khumaida et al. 2008).
Menurut hasil penelitian Wahyuningtyas (2005) ekstrak handeuleum 40%
dapat menghambat pembentukan plak pada gigi. Selain itu, hasil penelitian yang
dilakukan oleh Mu’minah (2007) menunjukkan bahwa ekstrak etanol handeuleum
mampu menurunkan kadar total lipid, kolesterol LDL, dan HDL serum darah
mencit yang diovariektomi bilateral. Penelitian ini merupakan penelitian tahap
awal untuk menyelidiki peranan etanol yang terkandung dalam handeuleum
terhadap kadar hormon estrogen. Estrogen memiliki peran terhadap kondisi
handeuleum dapat dipakai sebagai tanaman obat untuk mengobati wasir,
melancarkan buang air seni, melancarkan haid, dan rematik/encok.
Isnawati dan Soediro (2003) mengemukakan bahwa handeuleum
mengandung antosianin, leukoantosianin, tannin galat, asam protokatekuat,
flavon, dan flavanol. Menurut BPOM (2004), adanya alkohol, pektin, dan asam
formiat pada tanaman ini merupakan bahan kimia yang bermanfaat sebagai obat.
Handeuleum juga mengandung flavonoid 0.4% dan kandungan minyak atsiri
kurang dari 0.4%. Dilaporkan kemudian bahwa vormofoliol merupakan senyawa
yang menjadi identitas tanaman ini.
Hasil uji fitokimia yang dilakukan oleh Khumaida et al. (2008),
menunjukkan bahwa beberapa aksesi handeuleum positif kuat sekali (++++)
mengandung alkaloid, saponin, tanin, flavonoid, triterpenoid, steroid, dan
glikosida. Kandungan flavonoid yang positif kuat sekali menandakan bahwa
tanaman ini dapat dimanfaatkan sebagai sumber vitamin E. Selain itu, kandungan
triterpenoid yang positif kuat sekali diduga dapat digunakan sebagai senyawa
penanda untuk ketahanan tanaman terhadap hama. Pemanfaatan handeuleum
sebagai bahan baku obat telah dilakukan oleh perusahaan jamu berskala nasional,
seperti PT Indo Farma dan PT Sidomuncul, yang memerlukan 1 - 2 ton daun
handeuleum setiap bulannya (PSBI 2008). Menurut Wibowo (2000), PT Fimedco
juga turut memanfaatkan bagian tanaman ini sebagai bahan baku obatnya.
Hasil eksplorasi dan penelitian yang dilakukan oleh Khumaida (2008)
telah mengumpulkan handeuleum sebanyak 38 aksesi dari seluruh Indonesia,
dimana tiga belas aksesi yang diuji memiliki kandungan fitokimia tinggi yang
berguna untuk pengobatan. Saat ini handeuleum belum dibudidayakan secara
khusus, tanaman ini biasanya diperbanyak secara konvensional yaitu dengan cara
distek, karena tidak terbentuk biji pada handeuleum. Perbanyakan secara vegetatif
menghasilkan tanaman yang seragam akan tetapi tingkat keragaman genetiknya
sempit. Selain itu, handeuleum memiliki kendala dalam produksi biomassa daun
yaitu adanya serangan larva Doleschallia bisaltide yang menyebabkan penurunan
hasil hingga 70%. Induksi mutasi dapat diterapkan untuk meningkatkan
keragaman tanaman dan mendapatkan kandidat tanaman yang tahan hama, baik
dilakukan diharapkan dapat meningkatkan keragaman handeuleum dan
memperbesar peluang didapatkannya kandidat-kandidat varian tanaman baru yang
memiliki kandungan fitokimia yang tinggi yang dapat dimanfaatkan untuk
pengembangan obat tradisional Indonesia.
Tujuan
Penelitian ini secara umum bertujuan untuk meningkatkan keragaman
handeuleum melalui iradiasi sinar gamma secara in vivo pada stek pucuk
handeuleum aksesi Bogor dan in vitro pada kultur kalus handeuleum aksesi
Kalimantan dan Papua.
Hipotesis
1. Terdapat keragaman pada stek pucuk handeuleum aksesi Bogor yang diiradiasi
dengan sinar gamma.
2. Terdapat keragaman pada kultur kalus handeuleum aksesi Kalimantan dan
Papua yang diiradiasi dengan sinar gamma.
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi dasar mengenai
peningkatan keragaman handeuleum melalui iradiasi sinar gamma secara in vivo
pada stek pucuk dan secara in vitro pada kultur kalus.
Kerangka Penelitian
Handeuleum adalah tanaman yang banyak dimanfaatkan untuk digunakan
sebagai obat dan sangat berpotensi untuk dikembangkan lebih jauh. Bagian
handeuleum yang banyak dimanfaatkan adalah daunnya. Berdasarkan hasil
penelitian awal yang telah dilakukan, Khumaida et al. (2008) menyatakan bahwa
tanaman ini memiliki keragaman yang sempit, karena hanya dapat diperbanyak
Keterangan: ---- belum didapatkan
Induksi kalus Stek pucuk berakar
Proliferasi
Kalus hasil iradiasi
Inkubasi
Replanting
Pertumbuhan
Identifikasi Keragaman Kandidat varian baru
Iradiasi
Identifikasi Keragaman
Kandidat varian baru Perbanyakan handeuleum dengan stek memiliki tingkat
keragaman genetik sempit.
Peningkatan Keragaman Genetik
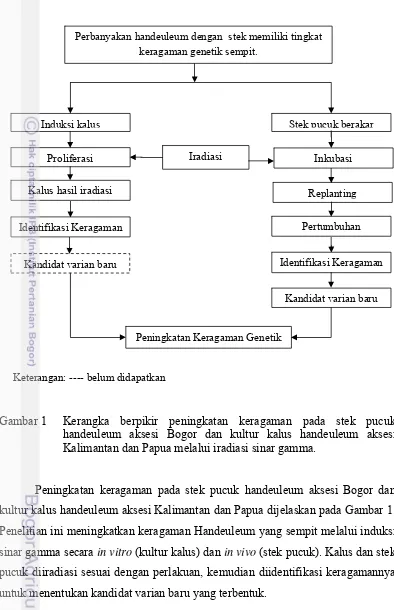
Gambar 1 Kerangka berpikir peningkatan keragaman pada stek pucuk
handeuleum aksesi Bogor dan kultur kalus handeuleum aksesi
Kalimantan dan Papua melalui iradiasi sinar gamma.
Peningkatan keragaman pada stek pucuk handeuleum aksesi Bogor dan
kultur kalus handeuleum aksesi Kalimantan dan Papua dijelaskan pada Gambar 1.
Penelitian ini meningkatkan keragaman Handeuleum yang sempit melalui induksi
sinar gamma secara in vitro (kultur kalus) dan in vivo (stek pucuk). Kalus dan stek
pucuk diiradiasi sesuai dengan perlakuan, kemudian diidentifikasi keragamannya
TINJAUAN PUSTAKA
Taksonomi dan Morfologi
Handeuleum (Graptophyllum pictum L. Griff), merupakan tanaman asli
Papua berbentuk perdu yang tumbuh lurus, tingginya dapat mencapai 1.5 - 8 m.
Handeuleum ditemukan tumbuh di daerah Jawa mulai dari dataran rendah hingga
ketinggian 1 250 m di atas permukaan laut (dpl), sering ditanam sebagai tanaman
hias atau tanaman pagar, dan banyak digunakan sebagai tanda batas di perkebunan
teh. Tanaman ini diperbanyak dengan cara stek (Heyne 1987).
Menurut United States Department of Agriculture (USDA) (2008),
taksonomi handeuleum sebagai berikut:
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Dicotyledonae
Subkelas : Asteridae
Ordo : Scrophulariales
Family : Acanthaceae
Genus : Graptophyllum Nees
Spesies : Graptophyllum pictum (L.) Griff
Menurut Heyne (1987), handeuleum dikenal di luar negeri sebagai
-Caricature plant (Inggris), Gertenschriftblatt (Jerman). Indonesia sendiri
memiliki berbagai macam nama daerah: handeuleum, daun temen-temen (Sunda),
daun putri (Ambon), temen (Bali), kabi-kabi (Ternate) dan dongo-dongo (Tidore).
daerah Madura menyebutnya karoton dan karotong. Daerah Jawa mengenal daun
ini dengan nama demung, tulak, dan wungu. Berdasarkan hasil eksplorasi dan
observasi oleh Khumaida et al. (2008), diketahui bahwa masyarakat di desa
Snaimboy Manokwari-Papua Barat menggunakan handeuleum sebagai obat
tradisional, mereka menyebut handeuleum sebagai brendek, dimanfaatkan untuk
38 aksesi handeuleum yang tersebar di berbagai tempat di Indonesia, dimana 13 di
antaranya memiliki kandungan bioaktif yang tinggi.
Handeuleum memiliki kulit dan daun berlendir, serta baunya kurang enak.
Ciri-ciri batang adalah sebagai berikut: aerial, berkayu, silindris, tegak, warna
ungu kehijauan, bagian dalam solid, permukaan licin, percabangan simpodial
(batang utama tidak tampak jelas), arah cabang miring ke atas. Daunnya tunggal,
tersusun berhadapan (folia oposita), warna ungu tua, panjang 15 - 25 cm, lebar 5 -
11 cm, helaian daun tipis tegar, bentuk bulat telur, ujung runcing, pangkal
meruncing (acuminatus), tepi rata, pertulangan menyirip (pinnate), permukaan
mengkilat (nitidus). Sedangkan bunganya majemuk, muncul dari ujung batang
(terminalis). Buah: kotak sejati (capsula), lonjong, warna ungu kecoklatan, bentuk biji bulat-berwarna putih, dan akarnya tunggang. Keragaan tanaman
handeuleum ditampilkan pada Gambar 2.
Gambar 2 Keragaan handeuleum. Tanaman utuh (kiri) dan bunga (kanan) aksesi Bogor.
Menurut BPPT (2008) handeuleum cocok tumbuh di daerah dataran
rendah sampai ketinggian 1 250 meter di atas permukaan laut. Wibowo (2000)
menambahkan handeuleum mampu tumbuh pada ketinggian di bawah
800 meter dpl, dimana semakin tinggi dataran maka daun handeuleum akan
semakin berwarna ungu yang disebabkan oleh adanya peningkatan senyawa
bahwa handeuleum dapat tumbuh di tempat terbuka, beriklim kering, dan lembab.
Handeuleum umumnya dikembangbiakkan menggunakan stek batang karena buah
dan biji sulit terbentuk (Djazuli & Fathan 2000).
Kandungan Kimia dan Manfaat
Graptophyllum pictum L. Griff telah lama dikenal sebagai tanaman obat, terutama sebagai obat wasir karena bersifat anti inflamasi, sehingga mampu
mengurangi pembengkakan atau peradangan yang disebabkan oleh wasir,
membantu proses melahirkan, serta dapat dipakai sebagai pelembut kulit.
Tanaman ini juga dipakai untuk mengobati bisul, luka-luka, radang, dan
melancarkan datang bulan.
Beberapa pustaka menyebutkan bahwa handeuleum mengandung
metabolit sekunder alkaloid, tanin, saponin, flavonoid, glikosida, dan steroid.
Isnawati dan Soediro (2003) mengemukakan bahwa handeuleum juga
mengandung antosianin, leukoantosianin, tannin galat, asam protokatekuat,
flavon, dan flavanol. Menurut Wahyuningtyas (2005) ekstrak handeuleum 40%
dapat menghambat pembentukan plak pada gigi. Berdasarkan uji klinis pada
kelinci menunjukkan bahwa infus handeuleum dengan kadar 1.56 - 100%
mempunyai efek sebagai laksansia ringan, yaitu dengan menaikkan amplitude
kontraksi otot polos jejunumnya (Sumastuti 2000). Mu’minah (2007) melaporkan
bahwa ekstrak etanol pada daun handeuleum dalam serum darah dapat
menurunkan kadar kolesterol LDL dan total lipid, selain itu juga dapat
menurunkan berat badan mencit yang digunakan pada penelitian.
Kultur Kalus
Menurut Gamborg dan Shyluk (1981), kultur jaringan merupakan
sejumlah teknik untuk menumbuhkan organ, jaringan, dan sel tanaman. Jaringan
dapat dikulturkan secara aseptik dalam medium hara. Kemudahan dalam
melakukan kultur tergantung pada jenis tanaman dan asal jaringan.
Kultur jaringan adalah suatu metode untuk mengisolasi bagian tanaman
seperti protoplasma, sel, sekelompok sel, jaringan, dan organ, serta
Pengatur Tumbuh (ZPT) dalam wadah tertutup yang tembus cahaya agar
bagian-bagian tersebut memperbanyak diri dan beregenerasi kembali menjadi tanaman
lengkap. Teknik kultur jaringan merupakan salah satu metode perbanyakan secara
in vitro. Awalnya teknik kultur jaringan ini dilakukan untuk membuktikan kebenaran teori totipotensi sel, lalu berkembang untuk penelitian di bidang
fisiologi tanaman dan biokimia (Gunawan 1992). Totipotensi didefinisikan
sebagai kemampuan dari sebuah sel untuk tumbuh dan berkembang bila tersedia
lingkungan luar yang sesuai (Mantell et al. 1985).
Menurut George dan Sherrington (1984) ada 2 (dua) kemungkinan
pertumbuhan tanaman secara in vitro yaitu pertumbuhan terorganisasi dan tidak
terorganisasi. Pertumbuhan terorganisasi terjadi pada bagian-bagian tanaman
(organ) seperti titik tumbuh (meristem) pucuk atau akar, daun yang baru/mulai
muncul, kuncup bunga, dan buah-buah kecil yang dikulturkan. Pertumbuhan tidak
terorganisasi jarang terjadi di alam, seringkali terjadi ketika potongan-potongan
tanaman yang dikulturkan secara in vitro. Jaringan-jaringan yang kemudian
terbentuk, kekurangan beberapa struktur khas yang dapat dikenali dan hanya
berisi sejumlah sel berbeda jenis yang ditemukan pada tanaman lengkap yang
selanjutnya disebut kalus. Regenerasi tanaman dapat dilakukan secara langsung
atau melalui dua tahap yaitu media induksi kalus dan media induksi tunas
adventif.
Kultur kalus dapat dihasilkan dari sejumlah besar organ tanaman yang
beragam seperti akar, tunas, dan daun, atau tipe spesifik sel seperti endosperm dan
polen. Untuk inisiasi kalus, secara aseptik eksplan ditransfer ke dalam media semi
solid dan secara halus merendam eksplan ke dalam medium agar sehingga tercipta
suatu kontak yang baik.
Media, jenis, dan konsentrasi ZPT adalah faktor utama dalam
pembentukan kalus. Berdasarkan konsep yang dikemukakan oleh George dan
Sherrington (1984), untuk induksi kalus tanaman dikotil diperlukan auksin dengan
konsentrasi tinggi dan tetap memerlukan sitokinin pada konsentrasi sangat rendah.
Induksi tunas diperlukan sitokinin dengan konsentrasi tinggi dan auksin pada
konsentrasi rendah, ada juga induksi tunas dapat dihasilkan dengan penggunaan
tanaman induk dikulturkan dalam media semi padat yang ditambahkan auksin
dengan konsentrasi yang relatif cukup tinggi, dengan atau tanpa sitokinin. Kalus
yang terbentuk selanjutnya dipindahkan ke media dengan auksin rendah untuk
merangsang pembentukan struktur yang terorganisir. Tunas dan akar akan
terbentuk dari bagian meristemastik, pada bagian permukaan dari kalus.
Faktor genotipe secara keseluruhan mempengaruhi pola pembentukan
organ adventif dari kalus. Kemampuan membentuk tunas dan akar secara terpisah
atau embriogenesis dari kalus berbeda antar famili maupun genus tanaman.
Pembentukan embrio (embriogenesis) dan pengembangan dari embrio pada
umumnya memerlukan taraf auksin yang berbeda. Embrio terbentuk dari sel
meristemastik yang mempunyai isi sitoplasma yang penuh (tanpa vakuola). Hasil
penelitian Sondahl dan Sharp pada tahun 1977 memaparkan bahwa eksplan daun
Coffea arabica ditanam pada medium MS + Kinetin 22 µM (≈ 0.43 mg/L) +
2.4-D 2 µM (≈4.862 mg/L) dapat membentuk kalus dan pada medium MS +
Kinetin 2.5 µM (≈0.538/L) + NAA 0.5 µM (≈0.09 mg/L) dapat membentuk tunas
dan embrio genesis somatik (Ammirato 1982; Tisserat 1985).
Iradiasi Sinar Gamma
Iradiasi ialah pemberian sinar radio aktif pada suatu objek dengan dosis
tertentu selama periode tertentu (Ismachin 2007). Salah satu sifat dari unsur
radioaktif tersebut adalah kemampuannya untuk menghasilkan iradiasi pengion,
yaitu iradiasi dengan energi tinggi yang dapat bereaksi dengan objek yang dikenai
iradiasi dengan cara pengionan. Molekul objek akan mengalami ionisasi dan
tereksitasi. Elektron yang terlepas akibat ionisasi akan ditangkap oleh molekul
lain yang kemudian dapat membentuk radikal bebas yang sangat reaktif.
Pembentukan radikal bebas tersebut akan mempengaruhi air yang merupakan
komponen terbesar di dalam sel atau dalam sistem biologi. Hal tersebut akan
sangat menentukan terhadap kerusakan di dalam sistem biologi.
Briggs dan Constantin (1977) melaporkan bahwa iradiasi elektromagnetik
dapat menimbulkan keragaman genetik, karena pengaruh iradiasi dapat
menimbulkan perubahan struktur gen, struktur kromosom ataupun jumlah
Mutagen fisik yang sering digunakan adalah sinar ultraviolet dan beberapa tipe
radiasi pengion seperti sinar x, sinar gamma, partikel alfa, partikel beta, proton,
dan neutron.
Van Harten (1998) menyatakan bahwa sinar gamma merupakan mutagen
yang paling banyak digunakan, hal ini dikarenakan sinar gamma memiliki panjang
gelombang yang pendek (lebih pendek dari sinar X) sehingga memiliki level
energi tertinggi. Level energi yang tinggi membuat sinar gamma mampu untuk
menembus lebih ke dalam jaringan dibandingan dengan mutagen fisika lainnya,
sehingga frekuensi mutasi yang terjadi menjadi lebih besar. Selain itu, sinar
gamma tidak meninggalkan residu radioaktif seperti yang dihasilkan oleh partikel
alpha dan beta. Lebih jauh van Harten (1998) menjelaskan bahwa sinar gamma
dapat dihasilkan oleh radioisotop 137Cs atau 60Co. Cobalt-60 memiliki dua puncak
spektrum energi radiasi pada 1.33 MeV dan 1.17 MeV, dengan masa paruh5.27
tahun, dan cobalt menjadi hilang terhadap stanium yang stabil. Caesium-137
merupakan mono-energetic dengan puncak energi pada 0.66 MeV.
Menurut Crowder (1997) iradiasi dapat menyebabkan patahnya
kromosom, dan pada dosis yang rendah dapat menyebabkan terjadinya delesi,
semakin tinggi dosis akan menimbulkan duplikasi, inversi, dan translokasi.
Ionisasi dari basa di dalam molekul DNA menyebabkan basa-basa tersebut salah
berpasangan. Tiamin akan berpasangan dengan adenin dalam keadaan normal,
namun apabila tiamin kehilangan satu proton akibat ionisasi maka tiamin akan
berpasangan dengan guanin. Hal demikian akan menimbulkan terjadinya mutasi
gen. Apabila iradiasi pengion memutuskan rantai kromosom pada tempat-tempat
tertentu, maka dapat mengubah struktur kromosom. Apabila kerusakan terjadi
pada benang-benang gelendong (spindle fibre) yang berfungsi menarik kromosom
ke kutub-kutubnya pada fase anafase saat pembelahan mitosis, maka akan
mengubah jumlah kromosom dan menyebabkan euploidi dan aneuploidi. Oleh
karena itu ionisasi dapat menyebabkan terjadinya mutasi kromosom dan aberasi
kromosom.
Mandal et al. (2000) menyatakan pemberian perlakuan iradiasi pada tunas
krisan dengan dosis 1.5 krad, 2.0 krad, dan 2.5 krad telah didapatkan hasil bahwa
dengan perlakuan yang lain dimana 55% daun varigata dan 5% lainnya
mengalami mutasi. Menurut Handayanti et al. (2001), tanaman mini varietas
Romantica meilandina yang diiradiasi 1 krad sampai 10 krad bunga berubah dari
warna pink menjadi warna putih. Eksplan Prince meilandina yang diiradiasi
1 krad sampai 8 krad dari merah tua berubah menjadi merah agak muda.
Pemberian iradiasi sinar gamma dan kolkisin pada kultur in vitro
menyebabkan terjadinya keragaman dalam bentuk dan ukuran daun, serta warna
bunga dari tanaman Crossandra infundibuliformis var Danica (Hewawasam et al.
2004). Penelitian iradiasi sinar gamma pada kultur kalus nodular manggis yang
dilakukan oleh Qosim et al. (2007) mengemukakan bahwa respon daya regenerasi
kalus nodular menurun dan variabel waktu pembentukan tunas meningkat secara
linier seiring dengan meningkatnya dosis iradiasi. Selain itu jaringan bunga
karang dan jumlah berkas pembuluh dari regeneran mutan pada umumnya lebih
tebal dan lebih banyak daripada regeneran kontrol yang tidak mendapat perlakuan
sinar gamma.
Induksi Mutasi In Vivo dan In Vitro
Ibrahim (1999) menyatakan bahwa mutasi adalah perubahan genetik, dan
merupakan sumber pokok dari semua keragaman genetik. Mutasi merupakan
satu-satunya sumber pencipta keragaman pada tanaman yang pada tanaman yang steril
dan tanaman apomiktik obligat. Poespodharsono (1996) menambahkan bahwa
secara molekuler mutasi terjadi karena adanya perubahan urutan (sekuen)
nukelotida DNA kromosom, yang mengakibatkan terjadinya perubahan pada
protein yang dihasilkan.
Van Harten (1998) menyebutkan induksi mutasi sinar gamma dapat
diterapkan pada materi tanaman in vivo dan in vitro. Micke dan Donini (1993)
menyatakan bahwa bagian tanaman yang dapat dimutasi dengan cara diiradiasi
adalah dengan biji dan tepung sari, dan untuk tanaman yang diperbanyak secara
vegetatif bagian yang dapat dimutasi adalah umbi, stek stolon, dan rimpang.
Micke dan Donini (1993) menyebutkan pada tanaman yang diperbanyak secara
vegetatif, mutasi dapat terjadi pada sel-sel somatik, kimera sektoral yang mungkin
dihilangkan. Maluszynski et al. (1995) mengemukakan pada kondisi in vivo sulit untuk mengisolasi mutan dari kimera sektorial dan membutuhkan waktu yang
lama, sedangkan kondisi in vitro mengisolasi mutan dari kimera dapat dilakukan
dengan mudah dan membutuhkan waktu yang cepat. Van Harten (1998)
menambahkan bahwa meski mutan utuh dapat diperoleh secara langsung dari
kalus, akan tetapi kalus memiliki daya regenerasi yang rendah.
Chaudhari (1971) menyatakan bahwa pengaruh iradiasi pada tanaman
yang diperbanyak secara vegetatif ada empat macam, yaitu: (1) perubahan
genetik, (2) pertumbuhan terhambat, (3) perkembangan morfologi yang abnormal,
dan (4) kematian tanaman.
Radiosensitivitas
Menurut van Harten (1998) radiosensitivitas adalah tingkat sensitifitas
tanaman terhadap iradiasi. Radiosensitifitas adalah perhitungan relatif yang
mengindikasikan kuantitas efek iradiasi pada objek yang diiradiasi (tanaman,
bagian tanaman, perbedaan tahap pertumbuhan, tahap meiosis dan mitosis, tahap
bibit muda dengan tanaman dewasa, atau fungsi molekuler yang spesifik). Sel
yang aktif membelah lebih sensitif terhadap iradiasi bila dibandingkan dengan sel
yang tidak aktif membelah. Radiosensitifitas dapat diukur dengan menentukan
dosis iradiasi yang menghasilkan persentase tertentu dari sel yang bertahan hidup.
Kriteria lain untuk mengukur radiosensitifitas adalah jumlah sel yang membelah,
penundaan mitotik, penghambatan pertumbuhan, dan sterilitas dari polen.
Seringkali ditemukan hubungan antara ukuran nukleus (atau ICV = Volume
kromosom interfase) dengan radiosensitifitas, tapi hal ini tidak terdapat pada
mayoritas spesies poliploidi.
Terdapat dua faktor utama yang mempengaruhi radiosensitivitas, yaitu:
(1) faktor lingkungan, seperti oksigen, kandungan air, suhu, dan penyimpanan
paska iradiasi; (2) faktor biologi, seperti volume inti, volume kromosom saat
interfase, dan faktor genetik. Keragaman yang timbul akibat iradiasi mutasi fisik,
sangat tergantung pada tingkat radiosensitivitas.
Secara visual tingkat sensitivitas ini dapat diamati dari respon yang
Reduction 50 (GR50) (Akgun & Tosun 2004). GR50 ialah dosis yang
menyebabkan penurunan pertumbuhan 50% dari populasi yang diiradiasi, pada
umumnya mutasi yang diinginkan berada pada kisaran GR50.
Analisis Isozim
Menurut Taiz dan Zeiger (2002) isozim adalah suatu enzim yang terdiri
dari beberapa molekul aktif yang mempunyai struktur kimia berbeda dan dikode
oleh gen berbeda, akan tetapi mengkatalisis reaksi yang sama. Sastra (1996)
menyatakan bahwa isozim terdiri atas rantai polipeptida, sehingga
memperlihatkan sifat-sifat umum seperti protein. Strukturnya terdiri dari
asam-asam amino yang mengandung gugus karboksil dan gugus amino. Asam amino
akan terionisasi di dalam larutan, dan dapat bersifat asam atau basa (amfoter).
Adanya perbedaan konstanta ionisasi (pK), bila diberi medan listrik akan
menyebabkan asam amino bermigrasi menuju ke kutub yang berlawanan
muatannya.
Keragaman tanaman dapat dilakukan secara morfologi, sitologi, biokimia,
dan molekuler. Analisis morfologi paling umum dilakukan untuk mendeteksi
keragaman, hanya saja analisis ini sangat dipengaruhi oleh lingkungan. Simpson
dan Whiters (1986) menyatakan bahwa protein termasuk isozim merupakan
produk primer ekspresi gen, karenanya keragaman protein atau isozim dapat
dipakai untuk menduga keragaman genetik tanaman atau organisme yang lain.
Molekul-molekul protein atau isozim dapat dipisahkan dengan teknik
elektroforesis, setelah pewarnaan akan tampak pita-pita protein pada gel sehingga
dapat ditelaah perbedaan dan persamaannya. Alel-alel kodominan umumnya
mengontrol pola pita tersebut dan diwariskan sesuai dengan hukum mendel.
Simpson dan Whiters (1986) mengemukakan bahwa sekuen-sekuen asam amino
pada dasarnya ditentukan oleh sekuen nukleotida pada gen, maka analisis genetika
yang berlandaskan isozim dapat digunakan sebagai pendekatan bagi analisis gen
yang mengkodenya.
Menurut Azrai dan Kasim (2003) isozim memiliki kelebihan yaitu bersifat
stabil, hal ini dikarenakan isozim tidak dipengaruhi oleh faktor lingkungan, lebih
dan Weeden (1989) menyebutkan bahwa bagian tanaman yang digunakan untuk
analisis isozim adalah bagian vegetatif tanaman yang masih muda, yang biasanya
mempunyai aktifitas enzim yang tinggi, sehingga akan mudah diamati. Aisyah
(2006) mengemukakan bahwa aktivitas isozim yang dapat diuji pada tanaman
sangat beragam karena masing-masing tanaman memiliki isozim utama.
Peroksidase (PER) dan esterase (EST) banyak dijumpai pada tanaman.
Peroksidase merupakan enzim tanaman yang terlibat dalam sintesis lignin, dan
dijumpai juga pada vakuola tanaman. Boumann dan Klerk (1997) mengingatkan
untuk mempertimbangkan adanya pengaruh fisiologi dan fase perkembangan
tanaman terhadap keberadaan enzim, sehingga disarankan untuk menggunakan
enzim yang bersifat stabil terhadap perubahan fisiologi maupun fase
perkembangan tanaman. Contohnya enzim malat dehidrogenase (MDH), alkohol
dehidrogenase (ADH), asam fosfatase (ACP), fosfoglukoisomerase (PGA), dan
INDUKSI KERAGAMAN PADA STEK PUCUK
HANDEULEUM (
Graptophyllum pictum
L. Griff) AKSESI
BOGOR MELALUI IRADIASI SINAR GAMMA
Abstrak
Salah satu cara untuk meningkatkan keragaman tanaman membiak vegetatif adalah dengan induksi mutasi dengan iradiasi sinar gamma pada stek pucuk. Penelitian ini bertujuan mengetahui pengaruh dosis iradiasi sinar gamma terhadap pertumbuhan, morfologi, anatomi daun, kandungan fitokimia, isozim, serta keragaman fenotipik stek pucuk handeuleum aksesi Bogor. Dosis sinar gamma yang digunakan adalah 0 Gy, 15 Gy, 30 Gy, 45 Gy, 60 Gy, 75 Gy, 90 Gy, dan 105 Gy. Hasil penelitian menunjukkan bahwa iradiasi sinar gamma mempengaruhi semua peubah pertumbuhan, morfologi, anatomi daun handeuleum, mempengaruhi kandungan fitokimia, aktifitas enzimatis, dan keragaman fenotipik pada beberapa perlakuan dosis iradiasi sinar gamma. Iradiasi
sinar gamma menghasilkan GR50 pada peubah tinggi tanaman, jumlah daun,
panjang daun, dan lebar daun. Dosis 15 Gy, 30 Gy, dan 45 Gy menghasilkan klorofil total, antosianin, dan karotenoid yang lebih besar dibandingkan perlakuan lain. Terdapat korelasi yang erat antara jumlah daun dengan panjang daun, lebar daun, dan antosianin; antosianin dengan indeks warna hijau relatif daun dan klorofil total; karotenoid dengan klorofil total; palisade dengan bunga karang. Terdapat perbedaan pola pita enzim peroksidase (PER), esterase (EST), dan asam fosfatase (ACP) bila dibandingkan dengan kontrol menunjukkan adanya perubahan genetik handeuleum yang diiradiasi. Iradiasi sinar gamma menimbulkan keragaman fenotipik pada semua peubah pertumbuhan, morfologi dan anatomi daun handeuleum kecuali pada peubah indeks stomata. Iradiasi sinar gamma dosis 45 Gy menghasilkan variasi dan jumlah mutan putatif yang paling banyak, masing-masing sebesar 9 (sembilan) variasi dan 10 mutan putatif.
Kata kunci: daun ungu, dosis iradiasi, isozim, keragaman fenotipik.
Abstract
One methode way to increase plant variability is to induce mutation by gamma ray irradiation. This research was conducted to study the effect of gamma ray irradiation dose to the growth, morphology, leaves anatomy, phytochemical content, isozymes, and phenotypic variability of handeuleum accession Bogor.
The gamma ray doses used were 0 Gy, 15 Gy, 30 Gy, 45 Gy, 60 Gy, 75 Gy, 90 Gy, and 105 Gy. The results showed that gamma-ray irradiation affected all
variables of plant growth, morphology and anatomy of handeuleum leaves, phytochemical content, enzymatic activity and phenotypic. Gamma irradiation
produced GR50 on plant height, total of leaves, leaves lenght, and leaves width.
chlorophyll; palisade with sponge tissue. There were some differences in enzyme banding pattern of peroxidase (PER), esterase (EST), and acid phosphatase (ACP) indicating changes of irradiated handeuleum. Gamma ray irradiation caused phenotypic variability in all variables of plantgrowth, morphology and anatomy leaves of handeuleum.Gamma irradiation 45 Gy produced number of variation and putative mutant the most, 9 (nine) variation with 10 putative mutant respectively.
Key words: daun ungu, irradiation dose, isozyme, phenotypic variability
Pendahuluan
Perbaikan sifat genetik tanaman dapat dilakukan pemuliaan konvensional
dan induksi mutasi menggunakan mutagen fisika dan kimia. Induksi mutasi
dilakukan guna meningkatkan peluang terjadinya mutasi, dan seringkali
diterapkan pada tanaman yang tidak dapat diperbaiki melalui persilangan.
Menurut van Harten (1998) metode induksi mutasi banyak digunakan karena
memiliki keuntungan dapat merubah satu karakter tanpa merubah seluruh susunan
gen secara signifikan, selain itu kombinasi metode mutasi dengan pembiakan
secara vegetatif dapat menurunkan resiko kehilangan karakter mutan akibat
segregasi.
Handeuleum merupakan tanaman yang belum dibudidayakan secara
khusus dan biasanya diperbanyak secara vegetatif yaitu dengan cara distek, hal ini
dikarenakan handeuleum bijinya tidak berkembang dengan sempurna.
Perbanyakan secara vegetatif menghasilkan tanaman yang seragam akan tetapi
tingkat keragamannya sempit, keragaman pada tanaman dapat dilakukan dengan
induksi mutasi. Menurut Broertjes dan van Harten (1998), sinar gamma sering
digunakan sebagai mutagen untuk induksi mutasi karena merupakan radiasi
elektromagnetik dengan panjang gelombang yang pendek, sehingga dapat
menghasilkan radiasi elektromagnetik dengan tingkat energi yang tinggi. Hal ini
menyebabkan daya tembus ke dalam jaringan sangat dalam, bisa mencapai
beberapa sentimeter dan bersifat merusak jaringan yang dilewatinya.
Sinar gamma bereaksi dengan atom atau molekul untuk memproduksi
radikal bebas dalam sel, contohnya: OH- dan H2O2. Radikal bebas ini dapat
merusak atau memodifikasi komponen yang penting dari sel tanaman (DNA) dan
biokimia, dan fisiologi dari tanaman tergantung dari level iradiasi (Wi et al.
2007).
Khumaida et al. (2008) dalam penelitiannya menyebutkan dari 38 aksesi
tanaman handeuleum yang diteliti menunjukkan karakter morfologi yang tidak
berbeda nyata, sedangkan kandungan fitokimianya (alkaloid, saponin, tanin,
flavonoid, steroid, triterpenoid, dan glikosida) memiliki nilai yang bervariasi.
Sebanyak 13 aksesi yang memiliki kandungan fitokimia yang tinggi, di antaranya
adalah aksesi Bogor, Kalimantan, dan Papua.
Tujuan
Penelitian ini bertujuan mengetahui pengaruh dosis iradiasi sinar gamma
terhadap pertumbuhan, morfologi, anatomi daun, kandungan fitokimia, karakter
isozim, serta keragaman fenotipik stek pucuk handeuleum aksesi Bogor.
Hipotesis
Iradiasi sinar gamma dapat mengakibatkan perubahan terhadap
pertumbuhan, morfologi, anatomi daun, kandungan fitokimia, serta dapat
meningkatkan keragaman stek pucuk handeuleum aksesi Bogor.
Metodologi Penelitian
Waktu dan Tempat
Percobaan dilakukan pada bulan Nopember 2009 hingga Juni 2010.
Aplikasi iradiasi dilakukan di Pusat Aplikasi Teknologi Isotop dan Radiasi
(PATIR) BATAN Pasar Jumat Jakarta. Pengamatan karakter pertumbuhan
tanaman dan morfologi dilakukan di kebun percobaan Cikabayan, University
Farm (UF), IPB. Pengujian fitokimia dilakukan di Balai Penelitian Tanaman Obat dan Aromatik (BALITTRO), Bogor. Analisis kandungan pigmen dilakukan di
Laboratorium Spektrofotometrik, Departemen Agronomi dan Hortikultura IPB,
sedangkan pengamatan karakter anatomi daun dilakukan di Laboratorium
dilakukan di laboratorium Hayati, Pusat Studi Bioteknologi dan Sumberdaya
Hayati IPB.
Metode Percobaan
Rancangan lingkungan yang digunakan adalah Rancangan Acak Lengkap
(RAL), dengan 1 (satu) faktor yaitu dosis iradiasi sinar gamma yang terdiri atas 8
(delapan) taraf yaitu 0 Gy, 15 Gy, 30 Gy, 45 Gy, 60 Gy, 75 Gy, 90 Gy, dan
105 Gy. Setiap perlakuan terdiri dari 10 ulangan, dengan 1 (satu) stek pucuk untuk
setiap ulangan, sehingga secara keseluruhan terdapat 80 stek pucuk.
Model linier RAL adalah sebagai berikut:
Yij = µ + αi + εij
Keterangan:
Yij : Nilai pengamatan perlakuan dosis iradiasi ke-i, dan ulangan ke-j
µ : Rataan umum
αi : Pengaruh perlakuan dosis iradiasi ke-i
εijk : Pengaruh galat percobaan perlakuan dosis iradiasi ke-i ulangan ke-j.
i : 1, 2, 3...8.
j : 1, 2, 3..10.
Persiapan Bahan Tanam
Tanaman yang digunakan berasal dari perbanyakan stek handeuleum
aksesi Bogor yang mempunyai kandungan fitokimia yang tinggi (Khumaida et al.
2008). Stek dengan panjang 3 (tiga) ruas ditanam pada polibag dengan media
tanam menggunakan tanah : kompos dengan perbandingan 2 : 1 (v/v). Stek pucuk
yang sudah berakar dan memiliki daun baru dengan tinggi sekitar 15 cm
digunakan sebagai bahan percobaan yang akan diiradiasi. Stek kemudian dicabut
dengan hati-hati dari media, dibersihkan dari tanah, lalu akarnya dibungkus
dengan aluminium foil. Stek diiradiasi menggunakan sinar gamma dari ionisasi
Cobalt 60, memakai alat irradiator gamma chamber 4000A, tipe Irpasena buatan
Stek yang telah diiradiasi langsung ditanam pada media baru,
ditumbuhkan di bawah kubung kecil selama kurang lebih dua bulan. Stek berumur
dua bulan selanjutnya dipindah tanam ke polibag yang lebih besar berdiameter
15 cm dan dipelihara di lapang dengan naungan paranet 55%. Penyemprotan
pestisida dilakukan untuk menghindari serangan hama dan penyakit. Selama
perawatan tanaman disiram 2 (dua) kali sehari, dan diberi pupuk daun setiap satu
minggu sekali, dan dipupuk dengan NPK sebulan sekali sebanyak 4 g/polibag
dengan perbandingan komposisi N:P:K = 15:15:15.
Pengamatan
Karakter Pertumbuhan Tanaman dan Morfologi
Pengamatan dilakukan pada karakter yang diduga berkaitan dengan
keragaman tanaman yang diinduksi oleh iradiasi sinar gamma, meliputi
1. Tinggi tanaman, diukur mulai dari permukaan media sampai pucuk dengan
menggunakan penggaris.
2. Jumlah daun, dihitung jumlah semua daun yang terdapat pada tanaman.
3. Panjang dan lebar daun, sampel diambil dari daun kedua dari ujung, panjang
daun diukur mulai dari pangkal sampai ujung daun, sedangkan lebar daun
diukur pada area terlebar daun.
4. Indeks warna hijau relatif daun, diamati menggunakan klorofilmeter Minolta
SPAD 502. Sebelum digunakan alat dikalibrasikan terlebih dahulu dengan
standar warna hijau yang telah disertakan pada alat tersebut.
5. Warna daun, warna batang, dan tekstur daun, diukur berdasarkan nilai skoring.
Skoring warna daun dan batang: 5=ungu, 3=ungu kehijauan, 1=hijau. Skoring
tekstur daun: 3=lembut, 1=keras/kaku.
Karakter Anatomi Daun
Pengamatan karakter anatomi daun dilakukan pada irisan transversal dan
paradermal menggunakan metode sediaan utuh menggunakan bahan segar,
meliputi:
1. Jumlah sel epidermis dan stomata, diamati jumlahnya di bawah mikroskop
2. Kerapatan stomata didapat dari perhitungan berikut: Kerapatan stomata =
Σ Stomata / Luas bidang pandang ( mm2).
3. Indeks stomata didapat dari perhitungan berikut: Indeks stomata =
(Σ Stomata / (Σ Stomata + Σ Sel epidermis)) x 100.
4. Tebal daun, tebal kutikula, tebal epidermis atas, panjang palisade, tebal bunga
karang, dan tebal epidermis bawah. Pengamatan dilakukan dengan mikroskop
digital molekuler.
Analisis Kandungan Fitokimia Daun
Analisis dilakukan terhadap kandungan fitokimia daun handeuleum untuk
kandungan alkaloid, saponin, triterpenoid, steroid, flavonoid, tanin, dan glikosida;
serta pada kandungan pigmen seperti klorofil total, karotenoid total, dan
antosianin total.
Tabel 1 Kriteria penilaian kandungan metabolit sekunder secara kualitatif dengan uji fitokimia
Senyawa Dasar Penilaian Penilaian
Alkaloid Jumlah pereaksi 1 tetes
4+
Steroid Perubahan warna biru/hijau 1 tetes
4+
Triterpenoid Perubahan warna merah/ungu Tua
3+
Sedang 2+
Muda 1+
Saponin Pembentukan lapisan busa 3 cm
3+
2 cm 2+
1 cm 1+
Flavonoid Jumlah pereaksi 1 tetes
4+
Tanin Jumlah pereaksi 1 tetes
4+
Analisis kandungan alkaloid, saponin, triterpenoid, steroid, tanin, dan
glikosida dilakukan secara kualitatif (Harborne 2000) dengan data berupa skoring
yang berdasarkan standar laboratorium pengujian Balai Penelitian Tanaman Obat
dan Aromatik (BALITTRO). Kandungan metabolit sekunder dalam sampel
yang terbentuk (Tabel 1). Kegiatan analisis kandungan fitokimia daun dapat
dilihat pada Lampiran 1.
Analisis kandungan pigmen seperti klorofil total, karotenoid total, dan
antosianin total dilakukan dengan metode Sims dan Gamon (2002), menggunakan
alat spektrofotometer yang teknis pelaksanaannya dapat dilihat pada Lampiran 2.
Setiap pigmen diidentifikasi konsentrasinya pada panjang gelombang yang
berbeda-beda, dimana panjang gelombang 663 nm untuk klorofil a, 647 nm untuk
klorofil b, 537 nm untuk antosianin, dan 470 nm untuk karotenoid. Data kemudian
dibaca menggunakan UV spektrofotometer, dan hasilnya dikonversi ke dalam
satuan mol/m2 dengan tahapan perhitungan sebagai berikut:
Antosianin = 0.01373*A537 – 0.00697*A647 – 0.002228*A663
Klorofil a = 0.01373*A663 – 0.000897*A537 – 0.003046*A663
Klorofil b = 0.02405*A647 – 0.004305*A537 – 0.005507*A663
Klorofil total dapat dihitung dengan persamaan berikut:
Klorofil total 7.15*A633 – 18.71*A647
Karotenoid = (A470 – (17.1*(Chl a + Chl b) – 9.479*antosianin))/119.26
Keterangan: A(x) merupakan data hasil pembacaan pada panjang gelombang x.
Konsentrasi pigmen per satuan luas dikonversi menggunakan perhitungan sebagai
berikut:
Pigmen/area = (pigmen*6/1000)/(Luas area daun total dalam m2)
Analisis Isozim
Kegiatan analisis isozim terdiri atas beberapa tahapan, cara penyiapan
bahan untuk analisis bahan dapat dilihat pada Lampiran 3. Interpretasi pola pita
isozim dilakukan dengan cara meletakkan gel di atas plastik bening kemudian
diletakkan di atas lampu pengamatan untuk diambil data dan difoto. Pola pita
isozim yang tampak digambar pada plastik transparan, hasil foto diamati dan
diukur jarak pergerakan pita dari titik awal. Hasil pengukuran jarak pergerakan
ditentukan pola pada Rf (relative electrophoresis mobility) dengan perhitungan
(Sastrosumarjo et al. 2006).
Rf = Jarak pergerakan pita dari tempat awal
Analisis Data
Data pertumbuhan, morfologi dan anatomi daun diuji menggunakan
analisis ragam (uji F) pada taraf nyata (α) 1% dan 5% dengan menggunakan
program SAS. Apabila hasil uji nyata, dilanjutkan dengan uji wilayah berganda
Duncan (Duncan’s Multiple Range Test-DMRT). Nilai Growth Reduction 50
(GR50) didapatkan dengan menggunakan program curve-fit, yaitu suatu program
analisis statistik yang dapat digunakan untuk mencari model persamaan terbaik
terhadap persentase penurunan pertumbuhan dari suatu populasi (Aisyah 2006).
Uji korelasi antar peubah dilakukan berdasarkan persamaan Pearson. Analisis
perbandingan nilai varian antar populasi dengan uji F. Keragaman fenotipik (σ2f)
dihitung menurut Steel dan Torrie (1995): σ2f=∑ X2i–(∑ Xi )2/(n-1). Standar
deviasi ragam fenotipik (Sdσ2f) dihitung menurut Anderson dan Brancot (1952)
dalam Darajat (1987): Sdσ2f = √σ2f. Kriteria penilaian terhadap luas atau sempit
keragaman fenotipik: Apabila σ2f ≥ 2* Sdσ2f Æ keragaman fenotipik luas
Apabila σ2f < 2* Sdσ2f Æ keragaman fenotipik sempit. Keterangan: σ2f = ragam
fenotipik; Xi = nilai rata-rata ke-i; n = jumlah yang diuji; Sdσ2f = standar deviasi
keragaman fenotipik.
Hasil dan Pembahasan
Morfologi Tanaman
Pengamatan terhadap karakter morfologi tanaman dapat mendeteksi
pertumbuhan dari tanaman. Penelitian ini menggunakan karakter pertumbuhan
(tinggi tanaman, jumlah daun, panjang daun, dan lebar daun) dan karakter
morfologi (warna daun, tekstur daun, dan warna batang) sebagai peubah untuk
melihat perubahan pertumbuhan tanaman akibat perlakuan dengan iradiasi sinar
gamma.
Berdasarkan pengamatan terhadap karakter-karakter tersebut di atas
terlihat bahwa terdapat kecenderungan pengelompokkan tanaman hasil iradiasi
berdasarkan dosis iradiasi menjadi dua kelompok. Tanaman yang mendapat dosis
iradiasi 15 Gy, 30 Gy, dan 45 Gy pada umumnya pertumbuhannya normal sama
dengan tananaman kontrol (0 Gy) dengan daun yang berwarna ungu, sedangkan
umumnya pertumbuhannya terhambat, tidak menghasilkan tunas yang baru, dan
daun tetap berwarna hijau.
Gambar 2 Bentuk daun handeuleum pada berbagai dosis iradiasi; (a) ovate, (b) obovate, (c) lancoleate, (d) kotrol (0 Gy), (e) 15 Gy, (f) 30 Gy, (g) 45 Gy, (h) 60 Gy, (i) 75 Gy, (j) 90 Gy, (k) 105 Gy.
Gambar 3 Keragaan daun handeuleum aksesi Bogor tanpa dan yang diiradiasi
dengan berbagai dosis sinar gamma; ovate (a), obovate (b),
lancoleate (c), kontrol (0 Gy) (d), 15 Gy (e), 30 Gy (f), 45 Gy (g), 60 Gy (h), 75 Gy (i), 90 Gy (j), dan 105 Gy (k).
Awal-awal pertumbuhan (3 MST, 4 MST) pada tanaman yang diiradiasi
terbentuk daun-daun baru yang mengalami perubahan baik dari segi bentuk,
(a) (b) (c)
(d) (e) (f) (g)
(h) (i) (j) (k)
warna serta tekstur yang lebih tebal, meskipun bisa dikatakan bahwa respon yang
timbul bersifat individual. Morfologi pada tanaman kontrol pada umumnya adalah
ovate dan sebagian kecil lanceolate. Sedangkan pada tanaman yang diiradiasi
terdapat penambahan bentuk elliptical selain kedua bentuk di atas.
Handeuleum pada stadia awal pertumbuhan umumnya memiliki warna
daun hijau muda dan ketika beranjak dewasa warna daun berubah menjadi
berwarna ungu merah kecoklatan. Tanaman yang diiradiasi sinar gamma dosis
60 Gy, 75 Gy, 90 Gy, dan 105 Gy, warna daunnya tetap hijau sampai daun
tersebut mati. Seterusnya daun-daun baru yang terbentuk kembali normal. Variasi
bentuk dan warna daun terbanyak terdapat pada handeuleum yang diiradiasi sinar
gamma 45 Gy, yaitu sebanyak 9 (sembilan) variasi, dengan jumlah tanaman
mutan putatif yang terbentuk sebanyak 11 tanaman.
Gambar 4 Keragaan tanaman handeuleum pada berbagai perlakuan iradiasi sinar gamma: kontrol (0 Gy) (a), 15 Gy (b), 30 Gy (c), 45 Gy (d), 60 Gy (e), 75 Gy (f), 90 Gy (g), dan 105 Gy (h). Terlihat bahwa daun pada perlakuan 60 Gy, 75 Gy, 90 Gy, dan 105 Gy memiliki warna yang berbeda dengan kontrol.
(h) (g)
(f) (e)
(d) (c)
Bentuk morfologi dan warna daun serta keragaan tanaman pada penelitian
ini disajikan pada Gambar 3 dan 4. Berdasarkan analisis ragam, Fhitung sumber
variasi dosis iradiasi (perlakuan) pada semua peubah yang diamati menunjukkan
berbeda nyata, yang berarti bahwa dosis iradiasi berpengaruh terhadap
peubah-peubah pengamatan.
Hal yang sama dijumpai pada penelitian Datta et al. (2005), dikatakan
bahwa mutasi somatik pada warna bunga dan bentuk floret dideteksi pada
populasi tanaman yang diberi perlakuan dengan sinar gamma. Wi et al. (2007)
menunjukkan bahwa gejala awal tanaman labu yang diiradiasi oleh sinar gamma
tingkat tinggi (1 kGy) adalah daun yang menjadi keriting dan menguning
(data tidak ditunjukkan), keduanya merupakan indikasi dari terjadinya
ketidakseimbangan zat pengatur tumbuh pada tanaman. Penelitian yang dilakukan
Badignnavar dan Murty (2007), menunjukkan bahwa warna daun tanaman kacang
tanah yang diberi iradiasi sinar gamma berubah menjadi hijau dan penampilan
tanaman secara keseluruhan menjadi normal kembali setelah 80 HST. Mutan
selalu tersegregasi ke dalam mutan dan tanaman tetua dengan frekuensi yang lebih
tinggi untuk tipe tanaman tetua bila dibandingkan dengan tanaman mutan.
Menurut Micke dan Donini (1993), kerusakan pada struktur genetik akibat
mutasi dapat berubah normal kembali (diplontic atau haplontic selection), hal ini
dikarenakan sel-sel yang normal pertumbuhannya mengalahkan sel-sel yang
termutasi. Bahkan terkadang terjadi mutasi balik, yaitu mutan yang sudah
terekspresi dapat kembali menjadi fenotip tetuanya pada generasi berikutnya.
Menurut Wi et al. (2007), tanaman memiliki sistem perlindungan alami terhadap
kerusakan oksidatif yaitu salah satunya dengan cara mengaktifkan perlindungan
enzimatik endogen, seperti: peroksidase (POD), superoksida dismutase (SOD),
dan katalase (CAT), yang aktif selama tanaman mengalami luka.
Growth Reduction 50 (GR50)
Sensitivitas iradiasi dapat diketahui dengan Growth Reduction 50 (GR50)
(Akgun & Tosun 2004). Pertumbuhan tanaman kontrol didefinisikan pada GR100,
sedangkan GR50 didefinisikan sebagai penurunan 50% dari pertumbuhan tanaman
tanaman, jumlah daun, panjang daun, dan lebar daun. GR50 dihitung pada akhir
pengamatan, yaitu pada minggu ke-10 setelah tanam.
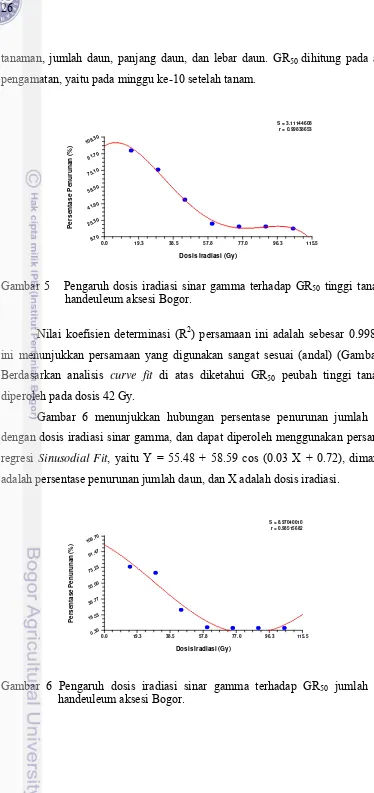
Gambar 5 Pengaruh dosis iradiasi sinar gamma terhadap GR50 tinggi tanaman
handeuleum aksesi Bogor.
Nilai koefisien determinasi (R2) persamaan ini adalah sebesar 0.998, hal
ini menunjukkan persamaan yang digunakan sangat sesuai (andal) (Gambar 5).
Berdasarkan analisis curve fit di atas diketahui GR50 peubah tinggi tanaman
diperoleh pada dosis 42 Gy.
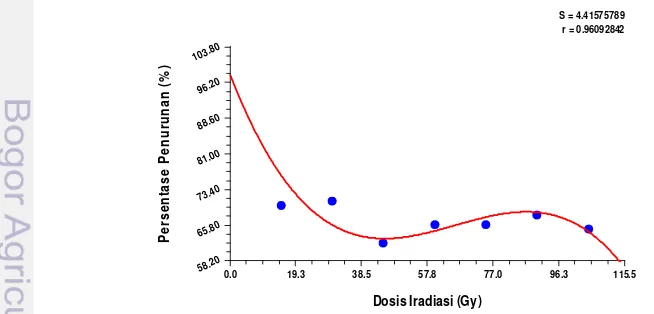
Gambar 6 menunjukkan hubungan persentase penurunan jumlah daun
dengan dosis iradiasi sinar gamma, dan dapat diperoleh menggunakan persamaan
regresi Sinusodial Fit, yaitu Y = 55.48 + 58.59 cos (0.03 X + 0.72), dimana Y
adalah persentase penurunan jumlah daun, dan X adalah dosis iradiasi.
Gambar 6 Pengaruh dosis iradiasi sinar gamma terhadap GR50 jumlah daun
handeuleum aksesi Bogor.
0.0 19.3 38.5 57.8 77.0 96.3 115.5
8.70
0.0 19.3 38.5 57.8 77.0 96.3 115.5
Nilai koefisien determinasi (R) persamaan ini adalah sebesar 0.985, hal ini
menunjukkan persamaan yang digunakan sangat sesuai (andal). Berdasarkan
analisis curve fit di atas diketahui GR50 diperoleh pada dosis iradiasi 33 Gy.
Fungsi matematika yang membantu mengetahui dosis yang
mengakibatkan reduksi panjang daun handeuleum sebesar 50% adalah Polynomial
Fit yang dirumuskan dalam persamaan Y = 96.88 – 2.19 X + 0.04 X2 – 0.0002 X3,
dimana Y adalah persentase penurunan panjang daun, dan X adalah dosis iradiasi.
Gambar 7 Pengaruh dosis iradiasi sinar gamma terhadap GR50 panjang daun
handeuleum aksesi Bogor.
Nilai koefisien determinasi (R2) persamaan ini adalah sebesar 0.942, hal
ini menunjukkan persamaan yang digunakan sangat sesuai (andal) (Gambar 7).
Berdasarkan analisis curve fit di atas diketahui nilai GR50 peubah panjang daun
diperoleh pada dosis 113 Gy.
Gambar 8 Pengaruh dosis iradiasi sinar gamma terhadap GR50 lebar daun
handeuleum aksesi Bogor.
0.0 19.3 38.5 57.8 77.0 96.3 115.5
50.50
0.0 19.3 38.5 57.8 77.0 96.3 115.5
Hubungan persentase penurunan lebar daun dengan dosis iradiasi sinar
gamma dapat menggunakan persamaan Polynomial Fit Y = 97.79 – 1.86 X +
0.03 X2 – 0.0002 X3, dimana Y adalah persentase penurunan jumlah daun, dan X
adalah dosis iradiasi. Nilai koefisien determinasi (R2) persamaan ini adalah
sebesar 0.961, hal ini menunjukkan persamaan yang digunakan sangat sesuai
(andal) (Gambar 8). Berdasarkan analisis curve fit di atas didapat GR50 lebar daun
adalah sebesar 122 Gy.
Menurut Ahnstroem (1977), morfologi tanaman seperti batang tanaman
yang berkayu atau sukulen dapat mempengaruhi tingkat radiosensitivitas, karena
berhubungan dengan ketahanan fisik sel saat menerima iradiasi sinar gamma.
Selain itu, radiosensitivitas juga dipengaruhi oleh faktor genetika dan lingkungan
seperti oksigen, kadar air, penyimpanan paska-iradiasi, dan suhu.
Tinggi Tanaman, Jumlah Daun, Panjang Daun dan Lebar Daun.
Berdasarkan hasil analisis ragam diketahui iradiasi sinar gamma
berpengaruh sangat nyata terhadap peubah tinggi tanaman, jumlah daun, panjang
daun, dan lebar daun (Tabel 2). Peubah ini umumnya nilainya semakin kecil
seiring dengan bertambahnya dosis iradiasi sinar gamma.
Hasil yang disajikan pada Tabel 2 memperlihatkan bahwa tinggi tanaman
paling tinggi diperoleh pada perlakuan kontrol tanpa iradiasi sinar gamma (0 Gy)
yaitu sebesar 83 cm, tidak berbeda nyata dengan perlakuan iradiasi sinar gamma
15 Gy yang menghasilkan tinggi 78.7 cm. Tinggi tanaman paling rendah
diperoleh pada perlakuan 105 Gy sebesar 14.1 cm (tereduksi sebesar 83.0%),
tidak berbeda nyata dengan perlakuan 60 Gy, 75 Gy, dan 90 Gy yang
masing-masing menghasilkan tanaman dengan tinggi berturut-turut sebesar 16.2 cm, 16.1
cm, dan 15.9 cm dimana masing-masing perlakuan mengalami tinggi tanaman
tereduksi secara berturut-turut sebesar 80.5%, 80.6%, dan 80.8%. Dosis iradiasi
sinar gamma yang semakin tinggi menyebabkan tinggi tanaman handeuleum
semakin pendek (Tabel 2). Hal ini menunjukkan bahwa sel-sel meristem pucuk
Tabel 2 Nilai rata-rata tinggi tanaman, jumlah daun, panjang daun, dan lebar daun handeuleum aksesi Bogor pada berbagai perlakuan dosis iradiasi sinar gamma pada 10 MST
Keterangan: Angka yang diikuti oleh huruf yang sama pada kolom peubah yang sama menunjukkan tidak berbeda nyata pada uji Duncan 5%. Nilai ± yang
disajikan adalah standar deviasi. a) Data merupakan hasil transformasi dengan
rumus (√X+0.5)
Penelitian Kon et al. (2007) menyebutkan bahwa semakin tinggi dosis
radiasi sinar gamma yang diberikan, tinggi tanaman long bean semakin tereduksi
bila dibandingkan dengan tanaman kontrol, dimana penurunan paling tinggi
adalah pada dosis 800 Gy, yang merupakan dosis perlakuan paling tinggi.
Menurut Fauza et al. (2005) pada bibit tanaman manggis yang bijinya diberi
perlakuan sinar gamma dosis 0 krad, 1 krad, 2 krad, dan 3 krad, terdapat
kecenderungan terjadi penurunan tinggi bibit tanaman manggis dengan semakin
tingginya dosis iradiasi sinar gamma yang diberikan.
Hasil pada Tabel 2 menunjukkan bahwa tanaman kontrol (0 Gy)
menghasilkan rata-rata jumlah daun paling banyak yaitu sebanyak 106.3 helai,
sedangkan perlakuan iradiasi sinar gamma dosis 105 Gy menghasilkan rata-rata
jumlah daun paling sedikit yaitu sebanyak 3.0 helai, mengalami penurunan
sebesar 97.2%. Hasil ini tidak berbeda nyata dengan perlakuan iradiasi sinar
gamma dosis 60 Gy, 75 Gy, dan 90 Gy yang berturut-turut menghasilkan daun
sebanyak 3.8, 3.4, 3.3 helai. Perlakuan sinar gamma dosis 60 Gy mengalami
penurunan sebesar 96,4%, dosis 75 Gy sebesar 96.8%, sedangkan dosis 90 Gy