BIODEGRADASI ANAEROBIK PADA MAKROALGA
SPESIES
Eucheuma
sp.
FITRIANTI SOFYAN
ILMU DAN TEKNOLOGI KELAUTAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Biodegradasi Anaerobik pada Makroalga Spesies Eucheuma sp. adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada Perguruan Tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, April 2015
Fitrianti Sofyan
NIM C54100042
ABSTRAK
FITRIANTI SOFYAN. Biodegradasi Anaerobik pada Makroalga Spesies
Eucheuma sp. Dibimbing oleh MUJIZAT KAWAROE dan ADRIANI SUNUDDIN.
Produk makroalga Eucheuma sp. yang tersisa dari hasil pemanenan yang memiliki nilai ekonomi terendah, namum dapat dimanfaatkan kembali sebagai alternatif energi terbarukan yaitu biogas. Biogas dihasilkan dari biodegradasi anaerobik Eucheuma sp. dengan bantuan starter yaitu bakteri feses sapi dan menghasilkan dua fraksi utama yaitu biogas dan residu organik (slurry). Penelitian ini bertujuan menganalisis karakteristik slurry dari proses biodegradasi anaerobik makroalga Eucheuma sp. berdasarkan parameter pH, total solid (TS),
volatil solid (VS), soluble chemical oxygen demand (SCOD), SCOD removal dan volume gas yang dihasilkan. Penelitian dilakukan pada bulan Mei-Oktober 2014 di Surfactant and Bioenergy Research Center (SBRC) LPPM-IPB. Uji karakteristik slurry dilakukan terhadap lima perbedaan perlakuan masukan umpan yaitu 0.5 kg COD/m3 hari, 1 kg COD/m3 hari, 1.5 kg COD/m3 hari, 2 kg COD/m3 hari, dan 2.5 kg COD/m3 per 10 hari. Eucheuma sp. sesuai untuk menjadi bahan baku biogas karena memiliki kandungan lignin 0.85%, kadar air 82%, dan rasio C:N 22.99:1. Tahap aklimatisasi starter dan inokulum memiliki pH lingkungan stabil pada nilai 6.9-7.5 dan 6.8-7.3 dengan hasil volume gas rata-rata 1220.5 ml/hari. Proses aklimatisasi biodegradasi anaerobik dilakukan pada suhu 29-31 ˚C dan pH 5-7 dengan menghasilkan volume gas rata-rata tertinggi pada pembebanan 2 kg COD/m3 hari yaitu 4.16 L/hari. Parameter TS, VS, SCOD dan SCOD
removal memiliki masukan yang terdegradasi paling baik pada pembebanan 2.5 kg COD/m3 hari.
ABSTRACT
FITRIANTI SOFYAN. Anaerobic Biodegradation on Macroalgae Spesies
Eucheuma sp. underdirection by MUJIZAT KAWAROE and ADRIANI SUNUDDIN
The residue of macroalgae products Eucheuma sp. from harvesting process which have the lowest economical value, can be reused as the renewable resource of energy (biogas). Biogas is resulted from anaerobic biodegradation of Eucheuma
sp. with cow feces as the starter and was producing two main faction biogas and organic residue (slurry). The objective of this research is to analys of slurry characteristic from anaerobic degradation proccess of Eucheuma sp. observed to pH, total solid (TS), volatil solid (VS), soluble chemical oxygen demand (SCOD) and SCOD removal parameter. This research was conducted on May-October 2014 in Surfactant and Bioenergy Research Center (SBRC) LPPM- IPB. Slurry’s characteristic test of Eucheuma sp. was conducted with five different input feed, there are 0.5 kg COD/m3 day, 1 kg COD/m3 day, 1.5 kg COD/m3 day, 2 kg COD/m3 day, and 2.5 kg COD/m3 day per 10 days. Eucheuma sp. is suitable to be the source material of biogas since it has low lignin content (0.85%), wet (82%) and C:N ratio 22.99:1. pH on system was stable when the starter and inoculum is in acclimatization stage about 6.9-7.5 and 6.8-7.3 with the average of gas volume 1220.5 ml/day. Anaerobic biodegradation process was conducted in the temperature of 29-31 °C and pH 5-7 and resulted in highest average of gas volume 4.16 L/day on input feed 2 kg COD/m3 day. Parameter TS,VS, SCOD and SCOD removal showed that the best degraded loading is on 2.5 kg COD/m3 day.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Ilmu Kelautan
pada
Departemen Ilmu dan Teknologi Kelautan
BIODEGRADASI ANAEROBIK PADA MAKROALGA
SPESIES
Eucheuma
sp.
FITRIANTI SOFYAN
DEPARTEMEN ILMU DAN TEKNOLOGI KELAUTAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB.
PRAKATA
Segala puji dan syukur penulis ucapkan kepada Allah SWT yang telah memberikan segala karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini dengan judul ”Biodegradasi Anaerobik pada Makroalga Spesies Eucheuma sp.”. Skripsi ini dibuat sebagai salah satu syarat kelulusan pada Departemen Ilmu dan Teknologi Kelautan, Institut Pertanian Bogor.
Pada kesempatan ini penulis ingin mengucapkan terima kasih sebesar-besarnya kepada :
1. Dr Ir Mujizat Kawaroe, MSi selaku dosen pembimbing pertama dan Adriani Sunuddin, SPi, MSi selaku pembimbing kedua atas segala bimbingan, arahan dan nasihat kepada penulis dalam proses penelitian dan penyusunan skripsi.
2. Beginer Subhan, Spi, Msi selaku dosen penguji ujian skripsi yang telah memberikan arahan, saran dan nasihat.
3. Dr Ir I Wayan Nurjaya, MSc selaku Ketua Departemen Ilmu dan Teknologi Kelautan dan pembimbing akademik atas saran dan masukannya selama masa studi.
4. Kedua orang tua dan adik atas dukungan doa, perhatian dan kasih sayangnya. 5. Dr Ir Udin Hasanudin MSi selaku dosen ahli bioenergi atas saran dan
masukannya dalam proses penelitian.
6. Wahid Suherfian, Krisye, Tia, Eko, Amelia, dan juga teman-teman di LPPM SBRC-IPB yang telah banyak membantu dalam pengerjaan penelitian. 7. Keluarga ITK 47 yang telah memberikan dukungan, semangat dan
kebersamaannya dalam penyelesaian skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan sehingga segala bentuk kritik dan saran akan dijadikan penulis sebagai bahan evaluasi diri. Semoga skripsi ini bermanfaat.
Bogor, April 2015
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
Latar Belakang 2
Tujuan Penelitian 2
METODE 2
Waktu dan Lokasi Penelitian 2
Prosedur Penelitian 2
Volume Masukan Umpan Eucheuma sp. 4
Peningkatan Volume Masukan Umpan Eucheuma sp. 4 Pegujian Kualitas Umpan dan Komposisi Kimia Eucheuma sp. 6
Biodigester 7
Rancangan Penelitian 8
Analisis Data 9
HASIL DAN PEMBAHASAN 9
Karakteristik Eucheuma sp., Umpan Eucheuma sp., Starter dan Inokulum 9
Aklimatisasi Starter dan Inokulum 11
Peningkatan Volume Masukan Umpan Eucheuma sp. pada Biodigester 13
Suhu 13
Derajat Keasaman (pH) 13
Volume gas 15
Total solids (TS) 16
Volatil solids (VS) 17
Soluble Chemical Oxygen Demand (SCOD) dan SCOD removal 18
SIMPULAN DAN SARAN 19
Simpulan 19
Saran 20
DAFTAR PUSTAKA 20
LAMPIRAN 23
DAFTAR TABEL
1 Metode Analisis komposisi kimia Eucheuma sp. 7
2 Uji proksimat karakterisasi Eucheuma sp. 9
3 Karakteristik umpan Eucheuma sp, starter (bakteri feses sapi), dan
inokulum 10
DAFTAR GAMBAR
1 Prosedur penelitian biodegradasi anaerobik Eucheuma sp. 3 2 Peningkatan volume masukan umpan Eucheuma sp. 5
3 Uji kualitas umpan Eucheuma sp. 6
4 Uji komposisi kimia Eucheuma sp. 6
5 Skema biodigester anaerobik 25 L dan penampung gas sementara 5 L 8 6 Eucheuma sp. basis basah (a) dan basis kering (b) 10 7 Nilai pH aklimatisasi starter (bakteri feses sapi) 12
8 Nilai pH aklimatisasi inokulum 12
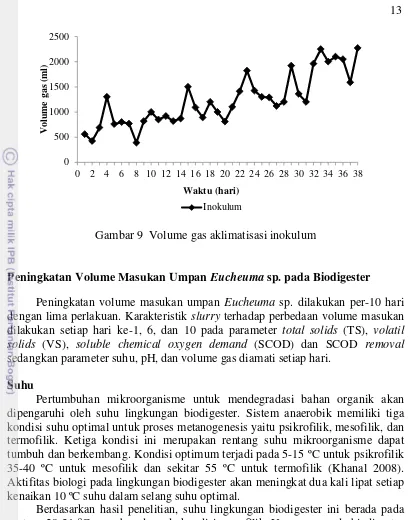
9 Volume gas aklimatisasi inokulum 13
10 Nilai pH per-hari dengan peningkatan volume masukan per-10 hari 14 11 Volume gas per-hari dan kumulatif dengan peningkatan volume
masukan per-10 hari 15
12 Nilai TS slurry dengan peningkatan volume masukan per-10 hari 16 13 Nilai VS slurry dengan peningkatan volume masukan per-10 hari 17 14 Nilai SCOD slurry dengan peningkatan volume masukan per-10 hari 18 15 Nilai SCOD removal slurry dengan peningkatan volume masukan
per-10 hari 19
DAFTAR LAMPIRAN
1 Prosedur analisis kualitas umpan dan komposisi kimia Eucheuma sp. 23
2 Dokumentasi kegiatan 28
PENDAHULUAN
Latar belakang
Kebutuhan terhadap bahan bakar adalah faktor penting yang membantu aktivitas manusia sehar-hari dan salah satunya disediakan oleh gas bumi. Peningkatan populasi dan aktivitas pembangunan telah membuat semakin menurunnya stok bahan baku yang tidak dapat diperbarui termasuk gas bumi. Menurut Pusdatin KESDM (2010) Indonesia hanya memiliki 1.7% dari total cadangan gas bumi dunia (111 triliun kaki kubik), sehingga diperlukan penelitian dalam mengeksplorasi sumber daya laut sebagai bahan baku alternatif energi yang bersifat terbarukan.
Indonesia memiliki potensi yang besar terhadap sumber daya laut, salah satunya adalah makroalga. Makroalga dari kelas alga merah (Rhodophyceae) adalah makroalga yang paling banyak tumbuh di perairan Indonesia (Winarno 1996). Petani rumput laut Indonesia sebagian besar lebih memilih untuk membudidayakan makroalga merah dari jenis Eucheuma sp. karena memiliki nilai jual yang tinggi (Suwaryati 2014). Proses penyortiran setelah panen dilakukan pemisahan produk layak dan tidak layak jual. Produk yang tidak layak ini (potongan kecil/warna tidak baik) akan dimanfaatkan kembali oleh petani itu sendiri untuk berbagai kegunaan. Salah satu pemanfaatan Eucheuma sp. yang tidak layak jual, dapat digunakan sebagai bahan baku energi terbarukan melalui proses biodegradasi anaerobik (Kawaroe et al. 2014). Terdapat beberapa karakteristik fisik yang penting untuk menghasilkan biodegradasi anaerobik yang baik pada biomassa yaitu lignin dan rasio C:N. Lignin merupakan karakteristik dari bahan organik yang tidak dapat terdegradasi sedangkan rasio C:N merupakan perbandingan antara karbon organik dan nitrogen yang akan digunakan pada proses biodegradasi anaerobik. Makroalga memiliki karakteristik yang mudah terdegradasi dengan kandungan lignin terendah dari seluruh biomassa yaitu sekitar 1-7% (Bruton et al. 2009; Bruhn et al. 2011; Chang et al. 2010) dan nilai rasio C:N 20:1 hingga 30:1 yang termasuk dalam kategori baik untuk menjadi bahan baku biogas (Sitompul et al. 2014). Selain itu, umur panen yang relatif singkat dan sistem budidayanya tidak mengganggu aktivitas lahan pertanian membuat
Eucheuma sp. dapat dijadikan sumber energi alternatif terbarukan (Kelly dan Dworanyn 2008).
Biodegradasi anaerobik merupakan proses penguraian bahan organik secara anaerob oleh bakteri. Bakteri yang dapat dimanfaatkan dalam mendegradasi bahan organik ini, terdapat dalam feses ternak. Feses sapi merupakan salah satu feses ternak yang mengandung karbohidrat, lemak dan protein untuk menghasilkan gas metana (Drapcho et al. 2008). Dalam kondisi tersebut, dekomposisi bahan-bahan organik akan menghasilkan dua fraksi utama yaitu gas (biogas) dan residu organik (slurry) (Burke 2001; Taricska et al. 2009). Slurry merupakan umpan atau substrat yang telah terdegradasi. Biogas terdiri dari CH4 (50-80%), CO2 (20-50%)
dan sejumlah gas lainnya seperti H2, CO, N2, O2 dan H2S (Soerawidjaja 2009).
Besarnya persentase masing-masing gas akan dipengaruhi oleh biomassa dan
2
pendekatan yang berkelanjutan yaitu menggabungkan pengolahan limbah dengan memanfaatkan kembali hasil sampingan. Aplikasi luas dari teknologi anaerobik dapat meringankan peningkatan kebutuhan energi yang tidak terkendali dan memiliki batas emisi polutan udara yang beracun, termasuk gas rumah kaca ke atmosfer (Khanal 2008). Masih sedikitnya penelitian mengenai pengolahan
Eucheuma sp. menjadi biogas maka dirasa perlu untuk melakukan penelitian ini. Tujuan Penelitian
Penelitian ini bertujuan menganalisis karakteristik slurry dari proses biodegradasi anaerobik makroalga Eucheuma sp. yang ditinjau dari parameter pH,
total solid (TS), volatil solid (VS), soluble chemical oxygen demand (SCOD), SCOD removal dan volume gas yang dihasilkan.
METODE
Waktu dan Lokasi Penelitian
Penelitian ini dilaksanakan pada bulan Mei – Oktober 2014 di Surfactant and Bioenergy Research Center (SBRC) LPPM-IPB dan Laboratorium
Bioprospecting, Departemen Ilmu dan Teknologi Kelautan, IPB. Prosedur Penelitian
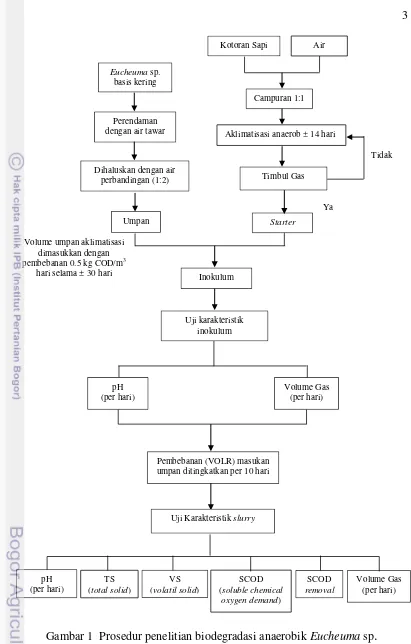
Prosedur penelitian yang dilakukan terdiri atas empat tahapan yaitu, pembuatan umpan, pembuatan dan aklimatisasi starter yang menggunakan feses sapi, aklimatisasi inokulum, dan peningkatan volume masukan umpan. Starter
merupakan penghidup mikroorganisme untuk degradasi bahan organik. Prosedur penelitian yang dilakukan ini terdapat pada skema Gambar 1. Uji karakteristik
slurry yang dilakukan yaitu analisis total solids (TS), volatil solids (VS), soluble chemical oxygen demand (SCOD), SCOD removal, pH, dan volume gas.
3
Gambar 1 Prosedur penelitian biodegradasi anaerobik Eucheuma sp.
Ya
Volume umpan aklimatisasi dimasukkan dengan
pembebanan 0.5 kg COD/m3
hari selama ± 30 hari
Tidak
Kotoran Sapi Air
Campuran 1:1
Aklimatisasi anaerob ± 14 hari
Starter
4
Starter yang telah diaklimatisasi pada biodigester ditambahkan umpan
Eucheuma sp. setiap harinya dengan beban masukan (VOLR) senilai 0.5 kg COD/m3 hari. Pencampuran starter dengan umpan Eucheuma sp. disebut dengan inokulum. Penambahan umpan dilakukan setelah inokulum hasil biodegradasi hari sebelumnya dikeluarkan dengan jumlah yang sama dengan volume masukan umpan Eucheuma sp. Inokulum yang telah dikeluarkan ini disebut slurry dan
slurry selalu dikeluarkan sebelum umpan Eucheuma sp. baru dimasukkan. Slurry
yang telah dikeluarkan, dianalisis karakteristik pH dan volume gas yang dihasilkan. Hal ini terus dilakukan sebagai aklimatisasi inokulum awal pada biodigester selama ± 30 hari. Peningkatan volume masukan umpan Eucheuma sp. akan dilakukan ketika karakteristik pH stabil dan volume gas yang dihasilkan meningkat. Peningkatan volume masukan umpan Eucheuma sp. dilakukan per-10 hari pada beban 0.5 kg COD/m3 hari, 1 kg COD/m3 hari, 1.5 kg COD/m3 hari, 2 kg COD/m3 hari, dan 2.5 kg COD/m3 hari. Slurry yang dikeluarkan setiap harinya dianalisis karakteristik pH dan volume gas yang dihasilkan, sedangkan karakteristik TS, VS, SCOD, dan SCOD removal dilakukan tiga kali dalam setiap periode peningkatan beban masukan umpan Eucheuma sp.
Volume masukan umpan Eucheuma sp.
Beban masukan umpan organik (VOLR) adalah jumlah beban umpan
Eucheuma sp. yang dimasukkan pada penelitian ini. Beban masukan umpan yang digunakan adalah 0.5 kg COD/m3 hari, 1 kg COD/m3 hari, 1.5 kg COD/m3 hari, 2 kg COD/m3 hari, dan 2.5 kg COD/m3 hari. VOLR ini dipengaruhi oleh konsentrasi COD umpan Eucheuma sp. (Ci), laju alir umpan (Q), dan volume
kerja biodigester (V) (Khanal 2008).
VOLR = Ci x Q V
Keterangan :
VOLR = Volumetric organic loading rate (kg COD/m3 hari) = 0.5 ; 1 ;1.5 ; 2 ; 2.5 kg COD/m3 hari
Ci = Konsentrasi COD umpan (kg/m3) = 19.4 kg/m3
Q = Laju alir umpan (m3/hari)
V = Volume kerja biodigester (m3) = 0.025 m3
Laju alir umpan (Q) menunjukkan kemampuan biodigester dalam menerima beban umpan Eucheuma sp. setiap harinya. Laju alir ini merupakan volume umpan Eucheuma sp. yang dimasukkan ke dalam biodigester setiap hari. Volume umpan Eucheuma sp. ini akan berbeda pada setiap VOLR yang digunakan.
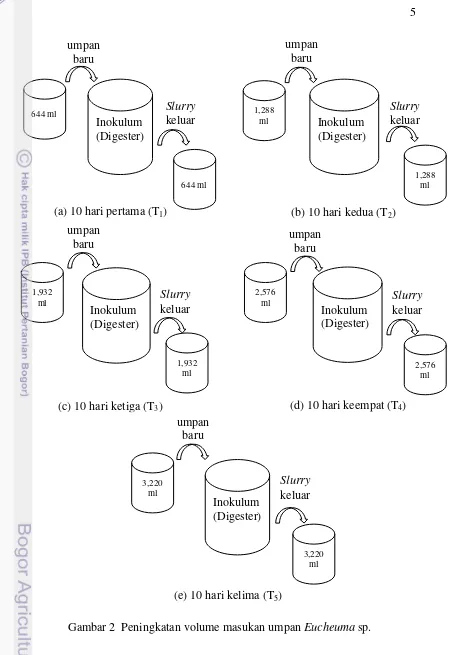
Peningkatan Volume Masukan Umpan Eucheuma sp.
Hasil perhitungan menggunakan persamaan VOLR, volume masukan umpan Eucheuma sp. ditingkatkan dengan nilai 644 ml/hari pada 10 hari pertama (T1), 1,288 ml/hari pada 10 hari kedua (T2), 1,932 ml/hari pada 10 hari ketiga (T3)
, 2,576 ml/hari pada 10 hari keempat (T4), dan 3,220 ml/hari pada 10 hari kelima
(T5). Metode ini dilakukan dengan pemasukan umpan Eucheuma sp. per-hari dan
5
6
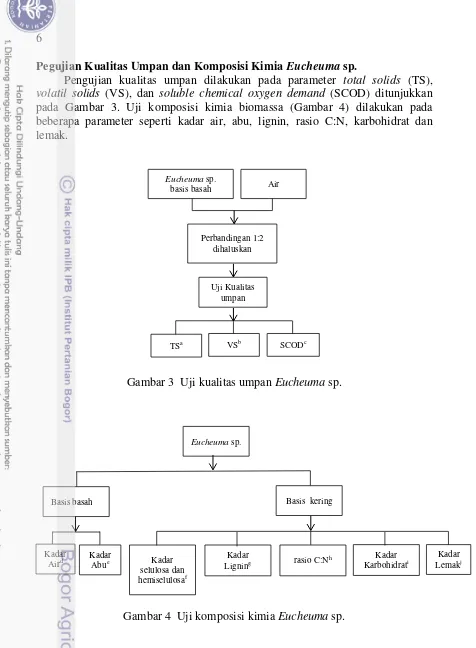
Pegujian Kualitas Umpan dan Komposisi Kimia Eucheuma sp.
Pengujian kualitas umpan dilakukan pada parameter total solids (TS),
volatil solids (VS), dan soluble chemical oxygen demand (SCOD) ditunjukkan pada Gambar 3. Uji komposisi kimia biomassa (Gambar 4) dilakukan pada beberapa parameter seperti kadar air, abu, lignin, rasio C:N, karbohidrat dan lemak.
Gambar 3 Uji kualitas umpan Eucheuma sp.
Gambar 4 Uji komposisi kimia Eucheuma sp.
Uji komposisi kimia Eucheuma sp. dilakukan pada kedua basis yaitu basis basah dan kering. Basis basah digunakan untuk analisa kadar air dan kadar abu, sedangkan basis kering digunakan untuk analisa kadar lignin, rasio C:N, kadar karbohidrat dan kadar lemak. Metode analisis yang digunakan pada pengujian umpan dan biomassa Eucheuma sp. terdapat pada Tabel 1.
Eucheuma sp.
basis basah Air
Perbandingan 1:2 dihaluskan
Uji Kualitas umpan
TSa VSb SCODc
Basis basah
Kadar
Abue
Kadar
Aird
Basis kering
Kadar
Lemakj
rasio C:Nh
Eucheuma sp.
Kadar
Karbohidrati
Kadar
Ligning
Kadar selulosa dan
7 Tabel 1 Metode Analisis komposisi kimia Eucheuma sp.
Parameter Satuan Metode Analisis
Total solids (TS) mg/L APHA 1998*
Volatil solids (VS) mg/L APHA 1998*
Soluble chemical oxygen demand
(SCOD)
Selulosa dan Hemiselulosa % Van Soest, 1991*
Lignin % Van Soest, 1991*
Karbohidrat % SNl 01-2S91-1992
(Luff-Schrool)*
Lemak % Soxhlet*
*Prosedur analisis di Lampiran 1
Biodigester
Biodigester pada penelitian ini dibuat berukuran 25 L dan penampung gas sementara 5 L, dengan skema pada Gambar 5. Bagian-bagian biodigester terdiri atas inlet umpan, kran inlet umpan, pengaduk umpan, outlet gas, biodigester 25 L, dan outlet slurry. Penampung gas sementara terdiri atas bagian inlet air, kran inlet
air, kran inlet dan outlet gas, penampung gas sementara, dan kran outlet air.
Umpan Eucheuma sp. masuk melalui bagian corong inlet umpan dan dengan membuka kran inlet umpan. Kran tersebut berfungsi agar kondisi lingkungan dalam biodigester tetap anaerobik. Umpan akan terdegradasi dalam biodigester oleh bakteri dengan mencampurkan umpan baru dengan inokulum menggunakan pengaduk. Umpan yang terdegradasi (slurry) setiap harinya dibuang melalui kran
outlet umpan. Proses biodegradasi tersebut menghasilkan gas di bagian atas biodigester. Gas akan masuk ke outlet gas yang telah dihubungkan dengan selang menuju penampung gas. Penampung gas (5 L) yang telah terisi air, berfungsi untuk menampung sementara gas hasil degradasi dan menghitung volume gas yang dihasilkan per hari. Air yang terdapat dalam penampung gas akan terdorong keluar melalui outlet air karena tekanan yang disebabkan oleh gas dari biodigester. Volume air yang keluar dari penampung gas akan sesuai dengan volume gas yang dihasilkan. Gas yang telah berpindah pada penampung gas sementara dapat disimpan dalam kantong khusus dengan cara menghubungkan kran outlet gas dengan kantong kemudian air dimasukkan pada penampung gas melalui corong
8
Gambar 5 Skema biodigester anaerobik 25 L dan penampung gas sementara 5 L
Rancangan Penelitian
Rancangan percobaan yang digunakan pada penelitian ini adalah rancangan acak lengkap (RAL) dengan lima perlakuan dan sepuluh kali ulangan. Hipotesis yang diuji pada pengaruh perbedaan volume masukan umpan terhadap karakteristik slurry hasil biodegradasi anaerobik Eucheuma sp. :
H0 = Peningkatan volume masukan umpan Eucheuma sp. tidak berpengaruh
terhadap karakteristik slurry hasil biodegradasi anaerobik
H1 = Peningkatan volume masukan umpan Eucheuma sp. berpengaruh terhadap
karakteristik slurry hasil biodegradasi anaerobik
Pengujian karakteristik (pH, TS, VS, SCOD, SCOD removal, dan volume gas) dari slurry hasil biodegradasi anaerobik Eucheuma sp. Perlakuan pada penelitian yang digunakan ini adalah peningkatan masukan umpan sebesar 644 ml; 1,288 ml; 1,932 ml; 2,576 ml; dan 3,220 ml setiap sepuluh hari. Model rancangannya adalah sebagai berikut :
Keterangan :
Yij = Nilai pengamatan perlakuan ke-i (i= 644 ml; 1,288 ml; 1,932 ml; 2,576
ml; dan 3,220 ml) dan kelompok ulangan ke-j (j= 1,2,3,...dan 10)
9 Analisis Data
Analisis data yang dilakukan pada penelitian ini dianalisis dengan menggunakan analysis of variance (ANOVA) menggunakan program SAS 9.1.3 dengan tingkat kepercayaan 95% dan taraf α 0.05. Hasil uji ANOVA yang berbeda nyata, dapat dilakukan uji lanjut dengan uji Duncan Multiple Range.
HASIL DAN PEMBAHASAN
Karakteristik Eucheuma sp., Umpan Eucheuma sp., Starter dan Inokulum Karakteristik Eucheuma sp. pada Tabel 2 memiliki nilai kadar air 82.04% pada biomassa basis basah pada Gambar 6 (a) dan kadar abu 6.64%. Air merupakan salah satu faktor yang dapat meningkatkan degradasi bahan organik. Hal ini disebabkan mikroorganisme dapat tumbuh subur pada bahan organik yang memiliki kadar air sekitar 90% (Rahman 2007). Menurut Haq dan Soedjono (2009) kelembaban bahan organik 36-99 % akan menaikkan produksi gas 67% sehingga Eucheuma sp. adalah bahan baku yang tepat dalam biodegradasi anaerobik.
Tabel 2 Uji proksimat karakterisasi Eucheuma sp.
Uji Proksimat Kadar Bahan Baku Eucheuma sp.
Kadar Air 82.04%
Kadar Abu 6.64%
Rasio C:N 22.99:1
Kadar lemak 11.89%
Kadar lignin 0.85%
Kadar selulosa 5.79%
Kadar hemiselulosa 1.92%
Kadar karbohidrat 23.39%
Karakteristik perbandingan karbon dan nitrogen (rasio C:N) pada
Eucheuma sp. basis kering (Gambar 6 (b)) yaitu 22.99:1 yang menunjukkan bahwa jumlah karbon lebih banyak dibandingkan dengan nitrogen. Karakteristik ini adalah karakteristik yang tepat dalam pembentukan metana karena nilai rasio C:N yang paling baik adalah 20:1 sampai 30:1 (Sitompul et al. 2012). Karbon bertindak sebagai sumber energi bagi mikroorganisme dan menjadi salah satu penyusun elemen sel pada proses biodegradasi anaerobik. Karbon ini akan direspirasikan 2/3 bagian menjadi CO2 dan yang lainnya dikombinasikan dengan
nitrogen di dalam sel. Karbon yang tidak digunakan di dalam sel protein selanjutnya akan dibebaskan untuk produksi CH4 dan sedikit CO2. Nitrogen dalam
10
amonia (NH3) (Wahyuni 2009). Amonia yang terdapat pada lingkungan
biodigester akan bersifat toksik bagi lingkungan biodigester (Gootas 1956).
Gambar 6 Eucheuma sp. (a) basis basah dan (b) basis kering
Kadar lemak pada Eucheuma sp. diketahui 11.89%. Lipid akan terdegradasi pada tahapan hidrolisis. Tahap ini akan lemak/lipid akan didegradasi oleh bakteri penghidrolisis. Hidrolisis lemak/lipid akan menghasilkan asam lemak rantai panjang dan gliserol. Proses hidrolisis berlangsung sangat lambat dan secara umum merupakan pembatas laju reaksi keseluruhan dari proses degradasi anaerobik (Haandel dan Lubbe 2007; Taherzadeh dan Karimi 2008) dan degradasi lipid memerlukan waktu hingga 3.2 hari (Speece 1996).
Selulosa merupakan polimer yang berasosiasi dengan hemiselulosa dan lignin. Makroalga adalah tanaman yang memiliki selulosa dilapisi oleh lignin. Lignin adalah struktur kompleks yang memiliki fungsi untuk mempertahankan struktur tanaman dalam menahan serangan mikroorganisme dan tekanan oksidasi (Hendriks dan Zeeman 2009). Jika kadar lignin dalam tanaman sedikit, maka selulosa dan hemiselulosa akan mudah terdegradasi (Bayer et al. 1994). Hasil dari pengujian pada basis kering (Gambar 6 (b)) diperoleh bahwa nilai lignin dari
Eucheuma sp. 0.85% yang menunjukkan biomassa ini akan mudah terdegradasi. Menurut Kirk dan Farel (1987), lignin adalah komponen yang paling sulit terdegradasi hingga 110 hari. Nilai kadar selulosa dan hemiselulosa yang akan terdegradasi yaitu 5.79% dan 1.92%. Kadar lignin yang rendah ini akan meningkatkan proses biodegradasi anaerobik. Berlawananan dengan lignin, karbohidrat merupakan unsur yang paling cepat terdegradasi dengan waktu 0.18 hari (Speece 1996). Karbohidrat pada Eucheuma sp. terdegradasi pada tahap hidrolisis menjadi gula sederhana (Kawaroe et al. 2014). Nilai karbohidrat yang terdapat pada Eucheuma sp. yaitu 23.39%.
Kondisi awal umpan Eucheuma sp. yang digunakan, dianalisis untuk mengetahui perubahan terhadap perlakuan aklimatisasi biodegradasi anaerobik. Inokulum yang digunakan merupakan campuran antara umpan Eucheuma sp. dengan starter (bakteri feses sapi) dengan volume masukan pada beban awal 0.5 kg COD/m3 hari (644 ml/hari). Berikut ini merupakan tabel karakteristik umpan
11 Tabel 3 Karakteristik umpan Eucheuma sp, starter (bakteri feses sapi), dan
inokulum
Parameter Karakteristik
Umpan Eucheuma sp. Starter Inokulum
TS (mg/L) 1,179 3,939 4,956
VS (mg/L) 160 240 2,725
SCOD (mg/L) 19,400 13,200 5,222
pH 5.11 7.7 7
Tabel 3 menunjukkan nilai TS pada umpan Eucheuma sp. dan starter
sebesar 1,179 mg/L dan 3,939 mg/L yang menunjukkan jumlah makanan untuk bakteri metanogenik dalam menghasilkan metan yang optimum. Karakteristik parameter VS pada umpan Eucheuma sp. dan starter memiliki nilai sebesar 160 mg/L, 240 mg/L, yang menunjukkan jumlah mikroorganisme. Parameter SCOD memiliki nilai umpan Eucheuma sp. lebih tinggi dibanding inokulum yang digunakan yaitu 19,400 mg/L dan 13,200 mg/L yang menunjukkan umpan
Eucheuma sp. memiliki potensi lebih besar sebagai bahan baku pembentukan biogas (Amelia 2012). Pencampuran umpan Eucheuma sp. dengan starter sebagai bakteri pendegradasi disebut dengan inokulum. Nilai TS inokulum pada Tabel 3 yaitu 4,956 mg/L dan VS yaitu 2,725 mg/L. Nilai ini mengalami peningkatan dari sebelum pencampuran umpan Eucheuma sp. dengan starter yang disebabkan oleh penggabungan bahan organik dari umpan Eucheuma sp. dengan starter.
Tabel 3 menunjukkan nilai pH umpan Eucheuma sp., starter dan inokulum yang digunakan yaitu 5.11, 7.7, dan 7. Umpan Eucheuma sp. memiliki pH yang termasuk asam dan starter memiliki pH yang tepat dalam pembentukan biogas. Nilai pH pada starter adalah kondisi yang optimum dalam pembentukan biogas. Setelah keduanya dibentuk menjadi inokulum, nilai pH pada sistem menjadi 7 yang masih berada pada rentang kondisi optimum untuk pembentukan biogas.
Aklimatisasi Starter dan Inokulum
12
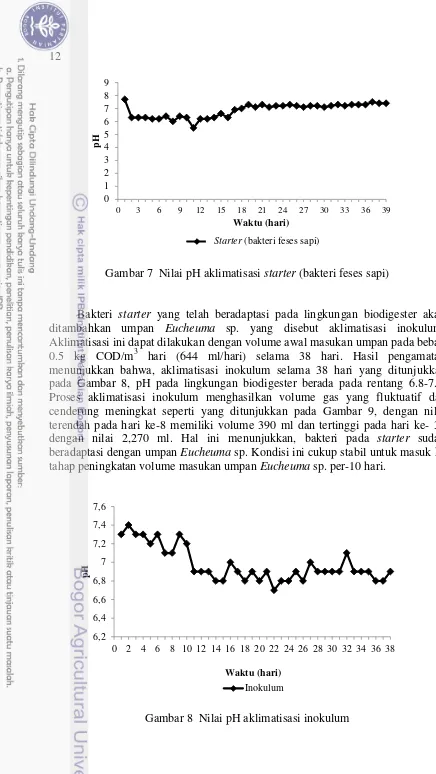
Gambar 7 Nilai pH aklimatisasi starter (bakteri feses sapi)
Bakteri starter yang telah beradaptasi pada lingkungan biodigester akan ditambahkan umpan Eucheuma sp. yang disebut aklimatisasi inokulum. Aklimatisasi ini dapat dilakukan dengan volume awal masukan umpan pada beban 0.5 kg COD/m3 hari (644 ml/hari) selama 38 hari. Hasil pengamatan menunjukkan bahwa, aklimatisasi inokulum selama 38 hari yang ditunjukkan pada Gambar 8, pH pada lingkungan biodigester berada pada rentang 6.8-7.3. Proses aklimatisasi inokulum menghasilkan volume gas yang fluktuatif dan cenderung meningkat seperti yang ditunjukkan pada Gambar 9, dengan nilai terendah pada hari ke-8 memiliki volume 390 ml dan tertinggi pada hari ke- 38 dengan nilai 2,270 ml. Hal ini menunjukkan, bakteri pada starter sudah beradaptasi dengan umpan Eucheuma sp. Kondisi ini cukup stabil untuk masuk ke tahap peningkatan volume masukan umpan Eucheuma sp. per-10 hari.
Gambar 8 Nilai pH aklimatisasi inokulum 6,2
13
Gambar 9 Volume gas aklimatisasi inokulum
Peningkatan Volume Masukan Umpan Eucheuma sp. pada Biodigester
Peningkatan volume masukan umpan Eucheuma sp. dilakukan per-10 hari dengan lima perlakuan. Karakteristik slurry terhadap perbedaan volume masukan dilakukan setiap hari ke-1, 6, dan 10 pada parameter total solids (TS), volatil solids (VS), soluble chemical oxygen demand (SCOD) dan SCOD removal
sedangkan parameter suhu, pH, dan volume gas diamati setiap hari. Suhu
Pertumbuhan mikroorganisme untuk mendegradasi bahan organik akan dipengaruhi oleh suhu lingkungan biodigester. Sistem anaerobik memiliki tiga kondisi suhu optimal untuk proses metanogenesis yaitu psikrofilik, mesofilik, dan termofilik. Ketiga kondisi ini merupakan rentang suhu mikroorganisme dapat tumbuh dan berkembang. Kondisi optimum terjadi pada 5-15 ºC untuk psikrofilik 35-40 ºC untuk mesofilik dan sekitar 55 ºC untuk termofilik (Khanal 2008). Aktifitas biologi pada lingkungan biodigester akan meningkat dua kali lipat setiap kenaikan 10 ºC suhu dalam selang suhu optimal.
Berdasarkan hasil penelitian, suhu lingkungan biodigester ini berada pada rentang 29-31 oC yang berada pada kondisi mesofilik. Umumnya pada biodigester anaerobik skala laboratorium beroperasi pada suhu selang mesofilik. Kerja dari bakteri dapat dimaksimumkan dengan memerlukan kondisi lingkungan biodigester yang konsisten pada suhu yang hangat. Secara umum perlakuan anaerobik ini akan sensitif terhadap perubahan suhu (Khanal 2008).
Derajat Keasaman (pH)
Biodegradasi anaerobik bahan organik akan dipengaruhi oleh kondisi lingkungan dalam biodigester. Lingkungan dengan kadar keasaman yang sesuai biodegradasi anaerobik akan berlangsung secara optimum. Nilai pH pada umpan akan mempengaruhi pertumbuhan bakteri pendegradasi. Bakteri dapat hidup pada rentang nilai pH 6.5-8.5 dengan nilai optimum 7.0-8.0 (Seadi et al. 2008).
14
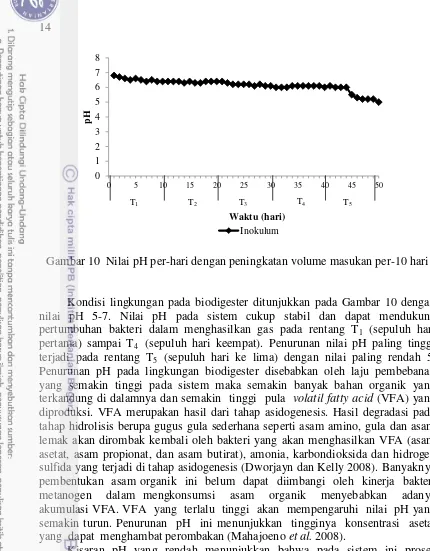
Gambar 10 Nilai pH per-hari dengan peningkatan volume masukan per-10 hari
Kondisi lingkungan pada biodigester ditunjukkan pada Gambar 10 dengan nilai pH 5-7. Nilai pH pada sistem cukup stabil dan dapat mendukung pertumbuhan bakteri dalam menghasilkan gas pada rentang T1 (sepuluh hari
pertama) sampai T4 (sepuluh hari keempat). Penurunan nilai pH paling tinggi
terjadi pada rentang T5 (sepuluh hari ke lima) dengan nilai paling rendah 5.
Penurunan pH pada lingkungan biodigester disebabkan oleh laju pembebanan yang semakin tinggi pada sistem maka semakin banyak bahan organik yang terkandung di dalamnya dan semakin tinggi pula volatil fatty acid (VFA) yang diproduksi. VFA merupakan hasil dari tahap asidogenesis. Hasil degradasi pada tahap hidrolisis berupa gugus gula sederhana seperti asam amino, gula dan asam lemak akan dirombak kembali oleh bakteri yang akan menghasilkan VFA (asam asetat, asam propionat, dan asam butirat), amonia, karbondioksida dan hidrogen sulfida yang terjadi di tahap asidogenesis (Dworjayn dan Kelly 2008). Banyaknya pembentukan asam organik ini belum dapat diimbangi oleh kinerja bakteri metanogen dalam mengkonsumsi asam organik menyebabkan adanya akumulasi VFA. VFA yang terlalu tinggi akan mempengaruhi nilai pH yang semakin turun. Penurunan pH ini menunjukkan tingginya konsentrasi asetat yang dapat menghambat perombakan (Mahajoeno et al. 2008).
Kisaran pH yang rendah menunjukkan bahwa pada sistem ini proses pembentukan asam masih terjadi. Penurunan pH secara tiba-tiba menandakan terjadinya gangguan pada proses fermentasi (Deublein dan Steinhausher 2008). Kondisi pH yang rendah yaitu 5, proses metanogenesis tetap terjadi, namun hanya 25% dari keadaan lingkungan dengan pH netral. Hasil analisis ragam pada Lampiran 3 menunjukkan bahwa perbedaan masukan volume umpan mempengaruhi nilai pH lingkungan biodigester yaitu nilai P-value < 0.0001 lebih kecil dari nilai α=0.5 dan keragaman 74.69%. Uji lanjut Duncan juga menunjukkan perbedaan volume masukan umpan memiliki respon yang berbeda-beda terhadap nilai pH lingkungan biodigester.
15 Volume Gas
Biodegradasi anaerobik pada prosesnya, memiliki tahapan hidrolisis, asidogenesis, asetogenesis, dan metanogenesis (Bastone 2002 Bastone et al. 2006; Gujer dan Zehnder 1983). Pembentukan gas hasil biodegradasi anaerobik ini mengandung metana sebagai komposisi utama untuk dimanfaatkan sebagai energi terbarukan terjadi pada tahapan metanogenesis. Metanogenesis merupakan tahapan terakhir dari seluruh tahapan biodegradasi anaerobik yang akan membentuk hasil dari tahap asetogenesis berupa asetat menjadi metana (CH4) dan
karbondioksida (CO2) (Dworjayn dan Kelly 2008).
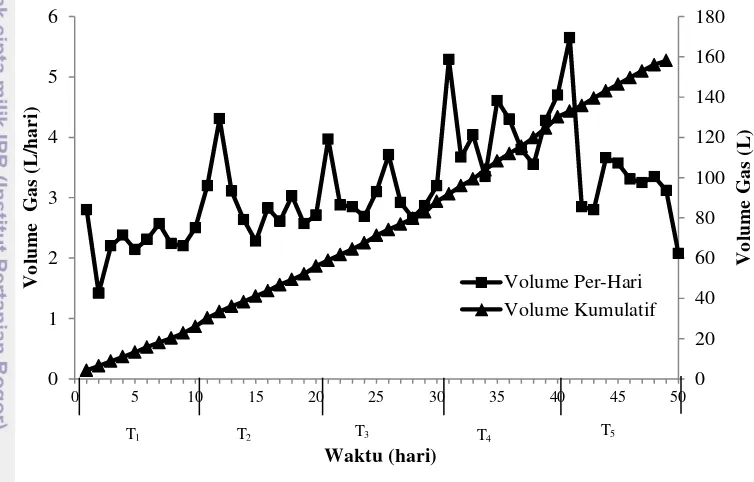
Gambar 11 Volume gas per-hari dan kumulatif dengan peningkatan volume masukan per-10 hari
Volume gas diukur setiap harinya dengan pergantian umpan baru yang dilakukan setiap hari pula. Hasil penelitian menunjukkan pada 5 perlakuan dengan peningkatan volume masukan setiap 10 harinya pada Gambar 11, didapatkan volume gas paling rendah berada pada T1 (sepuluh hari pertama) dengan nilai
rata-rata volume gas 2.27 L/hari hal ini menunjukkan bahwa pada tahap awal, bakteri belum mendegradasi sempurna umpan dan merubahnya menjadi gas, sehingga volume gas pada tahap pembebanan ini cenderung paling rendah. Volume gas tertinggi berada pada T4 (sepuluh hari keempat) dengan rata-rata
volume gas 4.16 L/hari yang menunjukkan bahwa bakteri mendegradasi umpan lebih baik dibandingkan dengan T1 (sepuluh hari pertama). T2 (sepuluh hari
kedua) diperoleh rata-rata volume gas 2.93 L/hari, lalu pada T3 (sepuluh hari
ketiga) volume gas rata-rata mencapai 3.09 L/hari dan pada T5 (sepuluh hari
kelima) volume gas rata-rata yaitu 3.36 L/hari.
Secara akumulasi, volume gas yang diperoleh sampai hari ke-50 percobaan yaitu 158.14 L akan tetapi komposisi gas yang dihasilkan belum diketahui.
16
Volume gas kumulatif yang dihasilkan pada penelitian ini lebih banyak bila dibandingkan dengan penelitian lain menggunakan makroalga Ulva sp. selama 106 hari dengan metode batch dan menghasilkan 153.9 L gas (Krisye et al. 2014). Sesuai dengan hasil analisis ragam pada Lampiran 4 menunjukkan bahwa perbedaan masukan volume umpan mempengaruhi nilai volume gas yang dihasilkan yaitu nilai P-value < 0.0001 lebih kecil dari nilai α=0.5 dan keragaman 53.15%. Uji lanjut Duncan juga menunjukkan perbedaan volume masukan umpan memiliki respon yang berbeda-beda pada volume gas yang dihasilkan.
Total solids (TS)
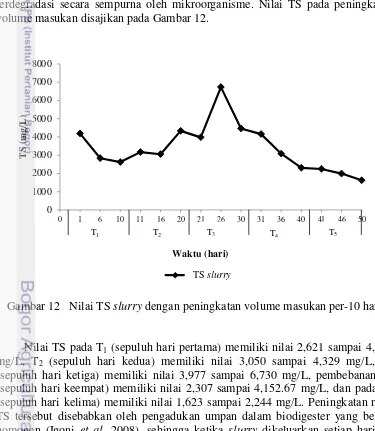
Total solids merupakan jumlah padatan atau bahan organik yang terkandung dalam suatu bahan yang merupakan sumber makanan atau nutrien bagi bakteri metanogenik. Nilai TS yang stabil mampu memacu laju pertumbuhan bakteri metanogenik (Maryanti 2011). Nilai TS diukur pada slurry yang dikeluarkan dari biodigester setiap harinya untuk mengetahui jumlah padatan yang tidak dapat terdegradasi secara sempurna oleh mikroorganisme. Nilai TS pada peningkatan volume masukan disajikan pada Gambar 12.
Gambar 12 Nilai TS slurry dengan peningkatan volume masukan per-10 hari
Nilai TS pada T1 (sepuluh hari pertama) memiliki nilai 2,621 sampai 4,182
mg/L, T2 (sepuluh hari kedua) memiliki nilai 3,050 sampai 4,329 mg/L, T3
(sepuluh hari ketiga) memiliki nilai 3,977 sampai 6,730 mg/L, pembebanan T4
(sepuluh hari keempat) memiliki nilai 2,307 sampai 4,152.67 mg/L, dan pada T5
(sepuluh hari kelima) memiliki nilai 1,623 sampai 2,244 mg/L. Peningkatan nilai TS tersebut disebabkan oleh pengadukan umpan dalam biodigester yang belum homogen (Igoni et al. 2008), sehingga ketika slurry dikeluarkan setiap harinya
17 membuat padatan total akan banyak yang terbawa dan terbuang hingga di tahap akhir pembebanan nilai TS semakin rendah.
Berdasarkan hasil penelitian, nilai TS paling tinggi berada pada T3 (sepuluh
hari ketiga). Sesuai dengan hasil analisis ragam pada Lampiran 5 menunjukkan bahwa perbedaan masukan volume umpan mempengaruhi nilai TS slurry yaitu nilai P-value < 0.0001 lebih kecil dari nilai α=0.5 dan keragaman 60.52%. Uji lanjut Duncan juga menunjukkan perbedaan volume masukan umpan memiliki respon yang berbeda-beda pada nilai TS slurry.
Volatil solids (VS)
Volatil solids (VS) merupakan jumlah bahan organik yang dapat didegradasi melalui reaksi biokimia oleh mikroba anaerobik (Ikbal dan Nugroho 2006). Gambar 13 menunjukkan nilai VS yang diperoleh memiliki fluktuasi yang cukup tinggi. Menurut Hasanudin et al. (2007), semakin tinggi fluktuasi nilai VS maka akan semakin mengganggu kinerja bakteri metan dalam biodigester untuk mendegradasi bahan organik pada Eucheuma sp. yang menghasilkan biogas. Fluktuasi tertinggi terjadi pada T3 yang berlangsung pada hari ke- 21 sampai 26
periode hasil uji dengan nilai 1,561 mg/L sampai 3,157 mg/L.
Gambar 13 Nilai VS slurry dengan peningkatan volume masukan per-10 hari
Nilai VS T1 (sepuluh hari pertama) memiliki nilai VS 722 sampai 909 mg/L,
T2 (sepuluh hari kedua) memiliki nilai VS 867 sampai 1,967 mg/L, T3 (sepuluh
hari ketiga) memiliki nilai VS 1,561 sampai 3,757 mg/L, T4 (sepuluh hari
keempat) memiliki nilai VS 552 sampai 1,970.67 mg/L, dan T5 (sepuluh hari
kelima) memiliki nilai VS 272 sampai 545 mg/L. Nilai VS tertinggi berada pada pembebanan T3 (sepuluh hari ketiga) dan terendah pada T5 (sepuluh hari kelima).
18
Duncan juga menunjukkan perbedaan volume masukan umpan memiliki respon yang berbeda-beda pada nilai VS slurry.
Soluble Chemical Oxygen Demand (SCOD) dan SCOD Removal
Soluble chemical oxygen demand (SCOD) atau kebutuhan oksigen kimia menurut Wardana (2005) merupakan jumlah oksigen yang dibutuhkan agar senyawa organik dalam air dapat teroksidasi melaluli reaksi kimia dalam sampel terlarut. Nilai SCOD pada slurry tidak stabil disetiap pembebanan ditunjukan pada Gambar 14. T1 (sepuluh hari pertama) memiliki nilai SCOD 6,160 sampai
11,760 mg/L, T2 (sepuluh hari kedua) memiliki nilai SCOD 3,264 sampai 14,750
mg/L, T3 (sepuluh hari ketiga) memiliki nilai SCOD 5,933 sampai 16,315 mg/L,
T4 (sepuluh hari keempat) memiliki nilai SCOD 5,549 sampai 14,584 mg/L, dan
pada T5 (sepuluh hari kelima) memiliki nilai SCOD 2,424 sampai 13,843 mg/L.
Gambar 14 Nilai SCOD slurry dengan peningkatan volume masukan per-10 hari
Penurunan nilai SCOD disebabkan oleh pembentukan lapisan mikroorganisme pada inokulum diikuti dengan degradasi senyawa-senyawa organik kompleks yang menghasilkan CH4 dan CO2. Nilai SCOD yang rendah
menunjukkan kandungan senyawa organik pada slurry rendah (Ahmad et al.
2011). Peningkatan nilai SCOD dapat disebabkan oleh bertambahnya kandungan senyawa organik. Selain itu dengan adanya kenaikan nilai SCOD slurry bukan berarti konsumsi senyawa organik oleh mikroorganisme berhenti, namun laju penguraian senyawa organik kompleks menjadi senyawa sederhana lebih cepat dibanding konsumsi umpan oleh mikroorganisme (Budhi et al. 1999)
Nilai persentase SCOD removal merupakan persentase dari penyisihan SCOD umpan dan SCOD slurry. SCOD removal memiliki nilai persentase yang fluktuatif ditunjukkan pada Gambar 15.
19
Gambar 15 Nilai SCOD removal slurry dengan peningkatan volume masukan per-10 hari
Nilai persentase SCOD removal menunjukan bahwa mikroorganisme tidak mampu mendegradasi bahan organik. Hal tersebut diduga adanya senyawa asam fenolik pada umpan dalam biodigester yang menyebabkan mikroorganisme mengalami lisis. Mikroorganisme yang mengalami lisis menyumbangkan beban bahan organik sehingga jumlah bahan organik mengalami peningkatan (Yuliastini
et al. 2014). Hasil analisis ragam pada Lampiran 7 dan 8 menunjukkan bahwa perbedaan masukan volume umpan tidak berpengaruh nyata terhadap nilai SCOD dan SCOD removal dengan nilai P-value < 0.5084 lebih besar dari nilai α=0.5 dan keragaman 6.93%.
SIMPULAN DAN SARAN
Simpulan
Biodegradasi anaerobik makroalga Eucheuma sp. akan semakin baik pada karakteristik TS, VS, SCOD dan SCOD removal dengan perlakuan peningkatan volume masukan umpan. Peningkatan masukan volume umpan akan menurunkan karakteristik volume gas yang dihasilkan dan pH yang tidak baik untuk proses biodegradasi anaerobik.
Saran
Proses pengadukan yang mempengaruhi proses biodegradasi anaerobik ini perlu diperhatikan lebih yaitu dengan kecepatan dan durasi pengadukan yang konstan. Selain itu, untuk diperlukannya analisis komposisi gas yang dihasilkan agar dapat diaplikasikan sebagai energi terbarukan.
0
20
DAFTAR PUSTAKA
Ahmad A, Syarfi, Atikalidia M. 2011. Penyisihan Chemical Oxygen Demand (COD) dan Produksi Biogas Limbah Cair Pabrik Kelapa Sawit dengan Biorekator Hibrid Anaerob Bermedia Cangkang Sawit. Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia dan
Prosiding Seminar Nasional Teknik Kimia “Kejuangan”; 2011 Februari 22; Yogyakarta, Indonesia. Pekanbaru (ID): Universitas Riau. ISSN 1693-4393: 54-61.
Amelia JR. 2012. Rekayasa Proses Aklimatisasi Bioreaktor Akibat Perubahan Substrat dari Thinslop ke Vinnase [Tesis]. Lampung (ID): Universitas Lampung.
[APHA] American Public Health Association. 1998. Standard Method For Examination of Wastewater 20th Edition. American Public Health Association 1015. Fifteenth Street, N.W. Washington DC 2005 – 2605. p 257-258.
Batstone DJ. 2006. Mathematical modelling of anaerobic reactors treating domestic wastewater: Rational criteria for model use. Rev Environ SciBio/technol. 5:57-71.doi: 10.1007_s11157-005-7191-z
Batstone DJ, Keller J, Angelidaki I, Kalyuzhnyi SV, Pavlostathis SG, Rozzi A, Sanders WTM, Siegrist H, Vavilin VA. 2002. Anaerobic Digestion Model No.1 (ADMI), IWA Task Group for mathematical Modelling of Anaerobic Digestion Process. London (UK):IWA Publishing.
Bayer EA, Morag E, Lamed R. 1994. The Cellulosome- A Treasure-Trove for Biotechnology. TIBTECH. 12: 379-386. doi:10.1016/0167-7799(94)90039-6 Briand X, Morand P. 1997. Anaerobic Digestion of Ulva sp. 1. Relationship
Between Ulva sp. Composition and Methanisation. J Appl Phycol. 9: 511-524.doi : 10.1023_a-1007972026328
Bruhn A, Dahl A, Nielsen HB, Nikolaisen L, Markager S, Olesen B, Arias C, Jensen D. 2011 . Bioenergy Potential of Ulva lactuca, Biomass Yield, Methane Production and Combustion. Bioresour Technol. 102: 2595-2604. doi : 10.1016_j.biortech.2010.10.010
Bruton T, Lyons H, Lerat Y, Stanley M, Rasmussen MB. 2009. A Review of The Potential of Marine Algae as a Source of Biofuel in Ireland. Sustainable Energy Ireland Report. p 92.
Budhi YW, Tjandra S, Bimo H. 1999. Peningkatan Biodegradabilitas Limbah Cair Printing Industri Tekstil Secara Anaerob. Bandung (ID). Jurnal ITB.
Burke DA.2001. DairyWaste Anaerobic Digestion Handbook. Olympia (WA): Environtmental Energy Company. p 1-54.
Chang HN, Kim NJ, Kang J, Jeong CM.2010. Biomass-derived Volatile Fatty Acid Platform for Fuels and Chemicals. Biotechnol Bioproc Eng. 15: 1-10. doi : 10.1007/s12257-009-3070-8
Deublein D. Steinhauster A. 2008. Biogas from Waste and Renewable Resources. An Introduction. WILEY- VCH Verlag GmbH & Co. KGaA, Weinheim. Drapcho CM, Nhuan NP, Walker TH. 2008. Biodiesel. In: Drapcho CM, Nhuan
21 Energy Efficiency and Renewable Energy. 2005. US Departement of Energy.
http://www.eere.energy.gov
Gootas HB. 1965. Composting, Sanitary Disposal and Reclamation of Organic Waste, World Health Organization, Geneva. p 13-34.
GujerW, Zehnder AJB. 1983. Conversion processes in aerobic digestion. Water Sci Technol. 15(8-9): 127-167.
Haandel A, Lubbe J. 2007. Handbook Biological Waste Water Treatment. Netherlands (NL): Quist Publishing. p 377-380.
Hasanudin U, Suroso E, Risfaheri, Misgiyarta. 2007. Optimasi Fermentasi Air Limbah Tapioka Sebagai Sumber Biogas [Laporan Hasil Penelitian]. Lampung (ID): Universitas Lampung.
Haq PS, Soedjiono ES. 2009. Potensi lumpur tinja manusia sebagai penghasil biogas. Surabaya (ID): Institut Teknologi Sepuluh September .
Hendriks ATWM, Zeeman G. 2009.Pretreatments to Enhance the Digestibility of Lignocellulose Biomass. Biores Technol. 10 : 10-18. doi : 10.1016_j.biortech.2008.05.027.
Igoni AH, Ayotamuno MJ, Eze CL, Ogaji SOT, Probert SD. 2008. Designs of anaerobic biodigesters for producing biogas from municipal solid-waste.
Applied Energy. 85 (6): 430-438. doi : 10.1016/j.apenergy.2007.07.013. Ikbal dan Nugroho R. 2006: Pengolahan Sludge dengan Proses Biologi
Anaerobik. J Tek Ling. P3TL-BPPT. 7. (1): 80 – 89.
Kawaroe M, Rusmana I, Nurafni. 2014. Production of Bioethanol from Macroalgae Gelidium sp. Using Agarase Enzymes of Marine Bacteria. Int J Environ Bioener. 9(3): 243-251
Kelly MS, Dworjayn S. 2008. The Potential of Marine Biomass for Anaerobic Biogas Production.Marine Estate Research Report, The Crown Estate, England.
Khanal SK. 2008. Anaerobic Biotechnology for Bioenergy Production. Manoa (USA): Blackwell Publishing.
Kirk TK, Farrel RL. 1987. Enzymatic Combustion The Microbial Degradation of Lignin. Ann Rev Microbiology. 41: 465-505.
Krisye, Kawaroe M, Hasanudin U. 2015. Biodegradasi Anaerobik Makroalga
Ulva sp. untuk Menghasilkan Biogas dengan Metode Batch. OLDI, siap terbit.
Mahajoeno E, Lay WB, Sutjahjo HS, Siswanto. 2008. Potensi Limbah Cair Pabrik Minyak Kelapa Sawit untuk Produksi Biogas. Biodiversitas (9):48 –52. Maryanti. 2011. Peningkatan Kinerja Reaktor Biogas Dalam pemngolahan Air
Limbah Industri Bioetanol Berbahan Baku Ubi Kayu [Thesis] . Lampung (ID): Universitas Lampung.
Nurhasanah. 2009. Penentuan Kadar COD (Chemical Oxygen Demand) Pada Limbah Cair Pabrik Kelapa Sawit, Pabrik Karet dan Domestik [Karya Ilmiah]. Medan (ID): Universitas Sumater Utara. p 24-30.
[Pusdatin KESDM] Pusat Data dan Informasi Kementrian Energi dan Sumberdaya Mineral. 2010. Indonesia Energy Outlook 2010. Jakarta [ID]: Pusat Data dan Informasi Kementrian Energi dan Sumberdaya Mineral. Rahman AN. 2007. Pembuatan Biogas Dari Sampah Buah-Buahan Melalui
22
Seadi TA, Rutz D, Prassl H, Kottner M, Finsterwalder T, Volk S, Janssen R. 2008. Biogas. University of Southern Denmark Esbjerg: Denmark.
Sitompul JP, Bayu A, Soerawidjaja TH, Lee HW. 2012. Studies of Biogas Production from Green Seaweeds. Int. J. Environ. Bioener. 3(3): 132-144 Soerawidjaja TH. 2009. Biogas, Teknologi Kemurgi [Modul Kuliah]. Bandung
(ID): Institut Teknologi Bandung. p 1-30.
Speece RE. 1996. Anaerobic Biotechnology. Nashville (USA): Archae Press. Suwaryanti NWE, Susrusa IKB, Rantau IK. 2014. Perbedaan pendapatan usaha
tani rumput laut Eucheuma spinosum dan Eucheuma cottonii di Desa Kutuh Kecamatan Kuta Selatan. E-J Agribisnis dan Agrowisata. 3 (1): 22-31 Taherzadeh MJ, Karimi K. 2008. Pretreatment of lignocellulosic waste to improve
ethanol and biogas production. JMol Sci. 9: 1621- 1651.doi : 10.3390/ijms9091621
Taricska JR, Long DA, Chen P, Hung YT, Zou SW. 2009. Biosolids Treatment Processes. Di dalam: Handbook of Environmental Engineering, Wang LK editor. Volume 6. Totowa (AS): The Humana Press Inc.p 135-176.
Wahyuni. 2009. Biogas. Jakarta (ID): Penebar Swadaya.
Wardana AW. 2005. Dampak Pencemaran Lingkungan. Yogyakarta (ID): Andi. Winarno FG. 1996. Teknologi Pengolahan Rumput Laut. Jakarta (ID): Pustaka
Sinar Harapan. 17 hlm.
23 LAMPIRAN
Lampiran 1 Prosedur analisis umpan dan komposisi kimia Eucheuma sp. a. Total solids (TS) (APHA 1998)
Total solids merupakan jumlah padatan yang terdapat dalam sebuah bahan. Sampel sejumlah 5 ml ditempatkan dalam cawan porselen yang sebelumnya telah ditimbang terlebih dahulu. Sampel tersebut kemudian dipanaskan dalam oven pada suhu 105 ± 3 ˚C selama 1 jam untuk selanjutnya didinginkan dalam eksikator hingga suhu kamar dan ditimbang hingga konstan (± 0.1 mg). Total solids dapat diperoleh dengan persamaan:
Total solids (mg/L) = (�−�)X1000
Volumesampel
Keterangan :
A = Bobot sampel dan cawan setelah dikeringkan (mg)
B = Bobot cawan (mg)
b. Volatil solids (VS) (APHA 1998)
Volatil solids merupakan padatan organik yang dapat dimanfaatkan oleh mikroorganisme untuk berkembang biak. Sampel TS ditempatkan dalam cawan porselen yang sebelumnya telah ditimbang terlebih dahulu. Sampel tersebut dipijarkan pada suhu 500-550 ˚C selama 3 jam untuk selanjutnya didinginkan dalam eksikator hingga suhu kamar dan ditimbang hingga konstan (± 0.1 mg).
Volatil solids dapat diperoleh dengan persamaan:
Volatil solids (mg/L) = �A-B�X 1000
Volume sampel
Keterangan :
A = Bobot sampel dan cawan setelah dipijar (mg)
B = Bobot cawan (mg)
c. Soluble chemical oxygen demand (SCOD) (APHA 1998)
Penentuan nilai SCOD merujuk pada metode titrimetri via oksidator kimia K2Cr2O7 (Nurhasanah 2009). Sebanyak 10 ml sampel umpan diencerkan menjadi
250 ml dengan aquades. 5 ml aliquot, 0.1 g serbuk HgSO4 dan 5 ml larutan
K2Cr2O7 0.25 N dicampurkan ke dalam erlenmeyer 250 ml. Sebanyak 7.5 ml
larutan Ag2SO4-H2SO4 1% ditambahkan ke dalam campuran secara perlahan
melalui dinding tabung sambil diaduk (rendam erlenmeyer dalam air). Campuran direfluks selama 2 jam dan setelah selesai diamkan hingga temperatur kamar. Aquades sebanyak 17.5 ml ditambahkan ke dalam campuran dan juga 3 tetes indikator ferroin. Campuran dititrasi dengan larutan standar ferro amonium sulfat (FAS) 0.05 N hingga titik akhir (warna larutan merah bata). Prosedur yang sama dilakukan untuk larutan blanko. Nilai SCOD ditentukan dengan persamaan:
SCOD (g O2L-1)=�(VFASblanko- VFASsampel) x NFAS x 8000 x fp
Valiquot
�x 10-3
Keterangan :
VFASblanko = Volume larutan FAS untuk titrasi blanko (ml)
VFASsampel = Volume larutan FAS untuk titrasi sampel aliquot (ml)
24
NFAS = Normalitas larutan FAS
Fp = Faktor pengenceran d. Kadar Air
Prinsip pengukuran kadar air ini adalah kehilangan bobot pada pemanasan
105 ˚C dihitung sebagai kadar air yang terdapat pada sampel. Sampel ditimbang ±
5 gram dan dimasukkan ke cawan dengan tutup yang telah diketahui bobotnya. Sampel dikeringkan pada oven dengan suhu 105 ˚C selama 3 jam dan didinginkan dalam eksikator kemudian ditimbang. Tahapan tersebut diulangi hingga memperoleh bobot tetap. Kadar air diperoleh dengan persamaan:
kadar air =w1
w x 100%
Keterangan :
W = Bobot sampel sebelum dikeringkan (g)
W1 = Kehilangan bobot setelah dikeringkan (g)
e. Kadar Abu
Metode pengukuran kadar abu dengan tanur 600 ˚C menggunakan prinsip
pembakaran zat organik pada suhu tersebut dan menyisakan zat anorganik yang tidak dapat terbakar. Sampel yang telah diukur kadar airnya, dibakar dalam tanur
ada suhu 600 ˚C selama 3 jam dan didinginkan dalam eksikator kemudian ditimbang. Kadar abu diperoleh dengan persamaan:
kadar abu =w1-w2
w x 100%
Keterangan:
W1 = Bobot cawan dan sampel setelah diabukan (g) W2 = Bobot cawan kosong (g)
W = Bobot sampel sebelum diabukan (g) f. Selulosa dan Hemiselulosa
Nilai kandungan selulosa dan hemiselulosa dapat diperoleh dari hasil analisa
neutral detergent fiber (NDF) dan acid detergen fiber (ADF). Analisis NDF dilakukan dengan tahapan menimbang sampel sebanyak 1 gram (A) dan dimasukkan kedalam gelas piala 600 ml, lalu ditambahkan 100 ml larutan neutral detergen solution (NDS) dan dipanaskan. Sampel diekstrak selama 60 menit dari mulai mendidih. Sampel disaring menggunakan cawan kaca masir G3 yang telah ditimbang sebelumnya (B). Residu dibilas menggunakan air panas dan aceton kemudian dikeringkan pada oven 105 ºC sampai beratnya stabil. Tahap selanjutnya diangkat dan dinginkan dalam desikator kemudian ditimbang (C). Kadar NDF diperoleh dengan persamaan:
Perhitungan:
% NDF = C-B
A x 100% Keterangan:
A = Bobot sampel yang dianalisis (g)
B = Bobot sampel yang telah disaring (g)
25 Analisis ADF dilakukan dengan prosedur menimbang contoh sebanyak 1 gram (A) dimasukkan kedalam gelas piala 600 ml, lalu ditambahkan 100 ml larutan acid detergen soluble (ADS). Sampel diekstrak selama 60 menit dari mulai mendidih. Sampel disaring menggunakan cawan kaca masir yang telah ditimbang sebelumnya (B). Residu dibilas menggunakan air panas dan aceton kemudian dikeringkan pada oven 105 ºC selama ± 4 jam sampai beratnya stabil kemudian diangkat dan dinginkan dalam desikator. Setelah dingin, cawan dikeluarkan dari desikator dan ditimbang (C). Kadar hemiselulosa dapat diperoleh dari pengurangan NDF dan ADF. Kadar ADF dan hemiselulosa diperoleh dengan persamaan:
% ADF = �−�
� x 100%
Keterangan:
A = Bobot sampel yang dianalisis (g)
B = Bobot sampel yang telah disaring (g)
C = Bobot sampel yang telah dikeringkan (g)
% Hemiselullosa = % NDF - % ADF
Analisa selulosa merupakan lanjutan dari analisa ADF. Sampel analisa ADF yang sudah ditimbang (C) ditambah larutan asam sulfat (H2SO4) 72%
sampai terendam selama 3 jam. Setelah 3 jam, residu dibilas menggunakan air panas dan aceton. Sampel dikeringkan pada oven 105 ºC selama ± 4 jam sampai beratnya stabil, angkat dan dinginkan dalam desikator. Setelah dingin, cawan dikeluarkan dari desikator dan timbang (D). Kadar selulosa diperoleh dengan persamaan:
% Selulosa = �−�
� x 100%
Keterangan:
A = Bobot sampel yang dianalisis (g)
C = Bobot sampel hasil analisis ADF (g)
D = Bobot sampel yang telah dikeringkan (g) g. Lignin (Klasson)
Analisa lignin merupakan kelanjutan dari analisa ADF dan selulosa. Sampel yang sudah dikeringkan (D), selanjutnya dibakar dalam tanur dengan tempratur ± 600 ºC. Angkat dan dinginkan cawan dalam eksikator dan timbang (E). Besarnya kandungan lignin dihitung menggunakan persamaan:
% Lignin = �−�
� x 100%
Keterangan:
A = Bobot sampel yang dianalisis (g)
D = Bobot hasil analisis selulosa (g)
E = Bobot yang telah diabukan (g) h. Rasio C:N
26
dimasukkan ke labu erlenmeyer 250 ml. Campuran diaduk hingga homogen dan ditambahkan 20 ml H2SO4 pekat secara perlahan melalui dinding labu. Campuran
diaduk perlahan dan ditambahkan 200 ml aquades serta 10 ml H3PO4 pekat.
Campuran tersebut ditambahkan 3 tetes indikator difenilamin dan dititrasi dengan larutan FeSO4 0.5 N hingga titik akhir. Prosedur yang sama diulangi untuk
pengujian blanko. Adapun kadar karbon dalam Eucheuma sp. dihitung dengan persamaan :
Kadar C (%)=�
(VFeSO4blanko- VFeSO4sampel) x NFeSO4 x fk
Massa sampel (gram) �x 100%
keterangan :
VFeSO4blanko = Volume larutan FeSO4 untuk titrasi blanko (ml)
VFeSO4sampel = Volume larutan FeSO4 untuk titrasi sampel (ml)
NFeSO4 = Normalitas larutan FeSO4 Fk = Normalitas FeSO4
3 = Bobot ekivalen karbon
1,32 = Faktor koreksi untuk bahan organik
Analisis N total dilakukan dengan metode Kjedahl. Sampel kering
Eucheuma sp. ditimbang 0.5 g dan dimasukkan kedalam labu kjedahl. Kemudian, sampel tersebut ditambahkan 1 g campuran selenium dan 5 ml H2SO4 pekat dan
didestruksi pada suhu 300 ºC selama 1.5 jam dan setelah itu diencerkan dengan 50 ml H2O murni. Hasil destruksi diencerkan sampai ± 100 ml dan ditambahkan 20
ml NaOH 40% lalu disuling. Hasil sulingan ditampung dengan penunjuk asam borat sebanyak 20 ml hingga warna berubah dari jingga menjadi hijau dan volumenya menjadi 50 ml dan dititrasi dengan H2SO4 0.01N sampai titik akhir.
Perhitungan kadar N total Eucheuma sp. diperoleh dengan persamaan : Kadar N(%)=�(VC- Vb) x NH2SO4 x 14 x fk
Massa sampel (gram) �x 100% Keterangan:
VC-Vb = Selisih titar contoh dan blanko (ml) N = Normalitas H2SO4
14 = B.A Nitrogen
Untuk menentukan nilai rasio C:N dari Eucheuma sp. nilai C organik dan nitrogen yang telah diperoleh, dirasiokan.
i. Karbohidrat (SNl 01-2S91-1992)
Kadar karbohidrat ditentukan dengan metode titrasi. Sekitar 5 gr sampel basis kering bersama HCL 3% 200 ml kemudian didihkan selama 3 jam dengan pendingin tegak. Larutan tersebut dibuat menjadi pH netral dengan larutan NaOH 30% (indikator phenolphtalein) dan ditambah sedikit CH3COOH 3% agar suasana
27 H2SO4 25% 25 ml dengan perlahan. Larutan dititrasi dengan larutan tio 0.1 N
(gunakan indikator kanji 0.5%). Perhitungan kadar karbohidrat dapat dilakukan apabila blanko juga telah dianalisis.
Nilai kadar karbohidrat dapat diperoleh dari persamaan:
(Blanko penitar) x Ntio x 10, setara dengan terusi yang tereduksi. Hasil tersebut
dilihat dalam daftar Luff-Schrool untuk mengetahui jumlah (mg) gula yang terkandung untuk sejumlah (ml) tio yang dipergunakan.
kadar glukosa=w1- fp
w x 100%
Keterangan:
w1 = Glukosa yang terkandung dalam (ml) Tiosulfat yang digunakan (daftar
Luff-Schrool)
fp = Faktor pengenceran
w = Bobot sampel yang digunakan (mg)
kadar karbohidrat=0.9 x kadar glukosa
j. Kadar lemak
Metode analisis lemak menggunakan alat soxhlet dengan prinsip ekstraksi lemak dengan pelarut non polar. Sampel yang digunakan 1 sampai 2 gram yang dimasukkan ke dalam selongsong kertas bebas lemak yang dialasi oleh kapas. Sebelum digunakan dalam soxhlet, selongsong dan kapas dikeringkan dalam oven dengan suhu tidak lebih dari 80 ˚C selama kurang lebih satu jam, kemudian selongsong yang telah dimasukkan sampel tersebut dimasukkan dalam alat soxhlet yang telah lengkap dengan labu lemak berisi batu didih yang telah dikeringkan dan diketahui bobotnya. Ekstraksi dilakukan selama kurang lebih 6 jam dengan pelarut heksana. Setelah ekstraksi selama 6 jam, heksana disuling dan
ekstrak lemak dikeringkan dalam oven pada suhu 105 ˚C. Selongsong tersebut
dinginkan dalam eksikator dan timbang. Pengulangan pada pengeringan dilakukan hingga mencapai bobot tetap. Persamaan bobot lemak yang diperoleh, sebagai berikut:
(%)lemak=w2-w1
w x 100%
dimana:
W = Bobot sampel yang digunakan (g)
28
Lampiran 2 Dokumentasi kegiatan
Keterangan :
a: Biodigester 25 L; b: Penampung gas sementara; c: Perendaman Eucheuma sp.; d: Penghalusan Eucheuma sp.; e: Pemasukan umpan Eucheuma sp. ke dalam biodigester; f: Pengeluaran slurry dari biodigester; g: Pengukuran pH slurry
a b
c
d
29
Keterangan:
h: Preparasi slurry untuk analisis karakteristik; i: Preparasi gas hasil biodegradasi anaerobik; j: Cawan untuk analisis TS dan VS; k: Timbangan analitik; l: Tanur untuk analisis VS; m: Oven untuk analisis TS
Lampiran 3 Uji statistik analisis ragam untuk karakteristik pH
Hasil analysis of variance (ANOVA) karakteristik pH pada setiap volume masukan umpan
Sumber keragaman
Derajat Bebas
Jumlah Kuadrat
Kuadrat tengah
F hitung
Nilai P Model 4 5.70920000 1.42730000 33.21 <.0001
Galat 45 1.93400000 0.04297778
Total Koreksi 49 7.64320000
h i
j k
30
Sumber keragaman Derajat Bebas
Type III SS Kuadrat Tengah
Nilai F Nilai P VolumeRumputLaut 4 5.70920000 1.42730000 33.21 <.0001 *Jika hasil Pr > F = < 0.0001 lebih kecil dari α=0.5 maka tolak H0
Uji lanjut Duncan
Pengelompokan Duncan Rata-rata Jumlah Data Volume rumput laut
A 6.54000 10 644
Lampiran 4 Uji statistik analisis ragam untuk karakteristik volume gas
Hasil analysis of variance (ANOVA) karakteristik volume gas pada setiap volume masukan umpan
Sumber keragaman Derajat bebas
Jumlah kuadrat Kuadrat tengah Nilai F Nilai P Model 4 18.79870800 4.69967700 12.76 <.0001
Galat 45 16.56990000 0.36822000
Total Koreksi 49 35.36860800
Sumber Keragaman Derajat Bebas
Type III SS Kuadrat Tengah Nilai F Nilai P VolumeRumputLaut 4 18.79870800 4.69967700 12.76 <.0001 *Jika hasil Pr > F = < 0.0001 lebih kecil dari α=0.5 maka tolak H0
Uji lanjut Duncan
Pengelompokan Duncan Rata-rata Jumlah Data VolumeRumputLaut
31 Lampiran 5 Uji statistik analisis ragam untuk karakteristik total solids (TS)
Hasil analysis of variance (ANOVA) karakteristik TS pada setiap volume masukan umpan
SumberKeragaman Derajat bebas
Jumlah kuadrat Tengah kuadrat Nilai F Nilai P Model 4 44386356.84 11096589.21 17.25 <.0001
Galat 45 28948011.57 643289.15
Total koreksi 49 73334368.40
Sumber keragaman Derajat Bebas
Type III SS Kuadrat tengah Nilai F Nilai p VolumeRumputLaut 4 44386356.84 11096589.21 17.25 <.0001 Uji Duncan
Pengelompokan Duncan Rata-rata Jumlah Data
Lampiran 6 Uji statistik analisis ragam untuk karakteristik volatil solids (VS) Hasil analysis of variance (ANOVA) karakteristik TS pada setiap volume masukan umpan
Sumber keragaman Derajat bebas
Jumlah kuadrat Kuadrat tengah Nilai F Nilai P Model 4 25755864.74 6438966.19 20.50 <.0001
Galat 45 14134646.97 314103.27
Total koreksi 49 9890511.71
Sumber Keragaman Derajat bebas
32
Uji Duncan
Pengelompokan Duncan Rata-rata N VolumeRumputLaut
A 2538.4 10 1932
Lampiran 7 Uji statistik analisis ragam untuk karakteristik soluble chemical oxygen demand (SCOD)
Hasil analysis of variance (ANOVA) karakteristik SCOD pada setiap volume masukan umpan
Sumber keragaman Derajat Bebas
Jumlah kuadrat Tengah kuadrat Nilai F Nilai P
Model 4 63669431.1 15917357.8 0.84 0.5084
Galat 45 854829930.3 18996220.7
Total koreksi 49 918499361.4
Sumber keragaman Derajat Bebas
Type III SS Tengah kuadrat Nilai P Nilai F Volume Rumput Laut 4 63669431.08 15917357.77 0.84 0.5084 *Jika hasil Pr > F = 0.5084 lebih besar dari α=0.5 maka tolak H1
Lampiran 8 Uji statistik analisis ragam untuk karakteristik soluble chemical oxygen demand (SCOD)
Hasil analysis of variance (ANOVA) karakteristik SCOD pada setiap volume masukan umpan
Sumber keragaman Derajat bebas
Jumlah kuadrat Tengah kuadrat Nilai F Nilai P
Model 4 1177.83663 294.45916 0.84 0.5084
Galat 45 15813.71128 351.41581
Total koreksi 49 16991.54790
33
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta 11 April 1992, sebagai anak ke-dua dari 4 bersaudara dari pasangan Yayan Ahmad Sopyan dan Siti Chadijah. Pada tahun 2007-2010 penulis menyelesaikan pendidikan di SMA Negeri 2 Bekasi.
Pada tahun 2010 penulis terdaftar sebagai mahasiswa Ilmu dan Teknologi Kelautan Institut Pertanian Bogor (IPB) melalui jalur USMI (Undangan Seleksi Masuk IPB). Selama menjadi mahasiswa, penulis mendapatkan beasiswa Karya Salemba Empat periode 2011-2014. Penulis juga pernah menjadi asisten praktikum mata kuliah Selam Ilmiah tahun 2012, sertifikasi One Star Scuba Diver (A-1) POSSI tahun 2012, asisten praktikum mata kuliah Ekologi Perairan tahun 2013, praktek kerja lapang di Karimunjawa Jepara bersama WCS (Wildlife Conservation and Society) tahun 2013, asisten praktikum mata kuliah Biologi Laut tahun 2014, dan asisten praktikum mata kuliah Biologi Tumbuhan Laut tahun 2014. Selain bidang akademik, penulis juga aktif dalam Himpunan Mahasiswa Ilmu dan Teknologi Kelautan (HIMITEKA) sebagai Bendahara II tahun 2012 dan Bendahara Umum tahun 2013. Penulis juga pernah mendapatkan pendanaan PKM-K dengan judul “Lampu Hias Kreatif Bebahan Dasar Kertas Daur Ulang Sebagai Media Edukasi Pengenalan Keanekaragaman Hayati di Indonesia” dan PKM-P dengan judul “Identifikasi Sirip Hiu di Tempat Kuliner Melalui Teknik DNA Barcoding Penanda Mitokondria”. Selain itu penulis aktif dalam berbagai perlombaan seni antar Departemen dan bergabung dalam PSM IPB Agriaswara dan anggota perkusi Ilmu dan Teknologi Kelautan “eXplorasi”.
Penulis pernah mengikuti kepanitiaan dari kegiatan konser Agriaswara “Metamorhphosa” tahun 2011 sebagai kepala divisi dana usaha, kegiatan Musyawarah Warga ITK tahun 2011 sebagai kepala divisi dana usaha, kegiatan Fieldtrip Akustik dan Pemetaan tahun 2012 sebagai divisi acara dan kegiatan Pekan Olahraga Perikanan dan Kelautan 2012 sebagai divisi acara.