PEMANFAATAN SPEKTROFOTOMETRI DERIVATIF UNTUK PENETAPAN KADAR CAMPURAN PSEUDOEFEDRIN HIDROKLORIDA DAN TRIPROLIDIN HIDROKLORIDA DALAM
SEDIAAN TABLET
SKRIPSI
OLEH:
RACHMAD ANRES DONGORAN
NIM 071501007
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PEMANFAATAN SPEKTROFOTOMETRI DERIVATIF UNTUK PENETAPAN KADAR CAMPURAN PSEUDOEFEDRIN HIDROKLORIDA DAN TRIPROLIDIN HIDROKLORIDA DALAM
SEDIAAN TABLET
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
RACHMAD ANRES DONGORAN
NIM 071501007
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
PEMANFAATAN SPEKTROFOTOMETRI DERIVATIF UNTUK PENETAPAN KADAR CAMPURAN PSEUDOEFEDRIN HIDROKLORIDA DAN TRIPROLIDIN HIDROKLORIDA DALAM
SEDIAAN TABLET OLEH:
RACHMAD ANRES DONGORAN NIM 071501007
Dipertahankan di Hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: Januari 2011
Pembimbing I, Panitia Penguji,
Dra. Tuty Roida Pardede, M.Si., Apt. Dr. Ginda Haro, M.Sc., Apt. NIP 195401101980032001 NIP 19510816198031002
Pembimbing II, Drs. Chairul Azhar Dalimunthe, M.Sc., Apt. NIP 19490761980021001
Drs. Muchlisyam, M.Si., Apt.
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Kuasa yang telah melimpahkan
berkat-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul
“Pemanfaatan Spektrofotometri Derivatif untuk Penetapan Kadar Campuran
Pseudoefedrin Hidroklorida dan Triprolidin Hidroklorida dalam Sediaan Tablet ”.
Tujuan penelitian ini adalah untuk menetapkan kadar campuran pseudoefedrin
HCl dan triprolidin HCl dengan menggunakan spektrofotometri derivatif dengan
aplikasi zero crossing dalam pelarut HCl 0,1 N. Skripsi ini diajukan sebagai salah
satu syarat guna memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi
Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih yang tiada
terhingga kepada almarhum Ayahanda St. Huala Dongoran, Ibunda Marsaulina
Gultom, Kakak Jernita Dongoran, Kakak Sinna Demak Marholong Dongoran,
Adik Debora Dongoran serta semua keluarga yang tidak dapat disebutkan satu per
satu, yang telah banyak memberikan doa dan dorongan serta bantuan moril dan
materil kepada penulis selama menempuh pendidikan S-1 Farmasi.
Penulis mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Dra.
Tuty Roida Pardede, M.Si., Apt. dan kepada Bapak Drs. Muchlisyam, M.Si., Apt.
selaku dosen pembimbing yang telah banyak memberikan bimbingan dan bantuan
yang sangat berarti mulai dari penelitian hingga selesainya penyusunan skripsi ini.
Pada kesempatan ini penulis juga menyampaikan ucapan terima kasih
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi, Universitas Sumatera Utara.
2. Ibu Dra. Djendakita Purba, M.Si., Apt., selaku Dosen Penasehat Akademik
yang telah memperhatikan dan membimbing penulis selama masa
perkuliahan.
3. Bapak Dr. Ginda Haro, M.Sc., Apt., Bapak Drs. Chairul Azhar
Dalimunthe, M.Sc., Apt., dan Bapak Drs. Maralaut Batubara, M.Phill.,
Apt., selaku dosen penguji yang telah memberikan masukan dan saran
kepada penulis hingga selesainya penulisan skripsi ini.
4. Seluruh Staf Pengajar dan Pegawai Tata Usaha di Fakultas Farmasi, serta
seluruh Asisten di Laboratorium yang telah banyak membimbing penulis
selama perkuliahan dan membantu penulis dalam menyelesaikan
penelitian ini.
5. Abang Edyatur Pane, Amd., Abang Jon Frikson Lumban Gaol, Adek
Kristianto Saputra Simbolon dan Tumiur Gultom.
6. Kelompok kecilku “MISERICORDIAS DOM” (Abang Mangatur
Situmorang, S.Kom., Abang Hardian Leonardo Willy Sitompul, Amd.,
dan Kristian Fransiskus Barus).
7. Sahabat-sahabatku “Rejoicing in Love” ( Santa, Ira, Debi, Alex, Eva,
Novalina, Via, Triwati, Martianus, Vintha, Juwita, Sari, Jimmy, Sandro,
Melati, Cory, Elfrida, Ernal, Hendry, Febri, Wandi, Fanny, Silvana).
8. Teman-teman Farmasi 2007 khususnya konsentrasi Sains dan Teknologi
Farmasi serat semua abang/kakak senior dan adek-adek junior di Fakultas
Penulis menyadari bahwa tulisan ini masih memiliki banyak kekurangan,
oleh karena itu dengan segala kerendahan hati penulis bersedia menerima kritik
dan saran yang membangun pada skripsi ini. Semoga skripsi ini bermanfaat bagi
kita semua.
Medan, Januari 2011
Penulis,
Rachmad Anres Dongoran
PEMANFAATAN SPEKTROFOTOMETRI DERIVATIF UNTUK PENETAPAN KADAR CAMPURAN PSEUDOEFEDRIN HIDROKLORIDA DAN TRIPROLIDIN HIDROKLORIDA DALAM
SEDIAAN TABLET
ABSTRAK
Saat ini banyak beredar sediaan obat dengan lebih dari satu komponen zat
aktif. Salah satu kombinasi yang sering digunakan adalah pseudoefedrin HCl dan
triprolidin HCl yang tersedia dalam bentuk sediaan tablet dan beredar dengan
berbagai merek dagang. Pseudoefedrin HCl adalah salah satu obat
simpatomimetik. Triprolidin HCl adalah obat antihistamin.
Tujuan penelitian ini adalah untuk menetapkan kadar campuran
pseudoefedrin HCl dan triprolidin HCl dengan menggunakan spektrofotometri
derivatif dengan metode zero crossing dalam pelarut HCl 0,1 N. Panjang
gelombang analisis untuk menetapkan kadar campuran pseudoefedrin HCl dan
triprolidin HCl pada spektrum serapan derivat kedua yaitu pada panjang
gelombang 271 nm (zero crossing untk triprolidin HCl) dan pada panjang
gelombang 318 nm (zero crossing untuk pseudoefedrin HCl).
Penentuan linieritas kurva kalibrasi menunjukkan hubungan yang linier
antara absorbansi dengan konsentrasi, untuk pseudoefedrin HCl dengan koefisien
korelasi, r = 0,9999 dan persamaan regresi Y = (9,06X +8,00).10-6; untuk
triprolidin HCl dengan koefisien korelasi, r = 0,9998 dan persamaan regresi Y =
(48,9X – 9,0).10-6 . Batas deteksi (LOD) dan batas kuantitasi (LOQ) untuk
pseudoefedrin HCl berturut-turut adalah 3,16 mcg/ml dan 10,53 mcg/ml
Hasil penetapan kadar campuran pseudoefedrin HCl dan triprolidin HCl
yang dianalisis dalam tablet di pasaran menunjukkan bahwa semua memenuhi
persyaratan sesuai dengan persyaratan yang tertera pada USP (United States
Pharmacopoeia) XXX tahun 2007. Hasil uji validasi yang dilakukan terhadap
tablet Tremenza® (Sanbe) memenuhi persyaratan validasi metode, untuk
pseudoefedrin HCl diperoleh % recovery = 99,90%, simpangan baku relatif
(RSD) = 0,9204% dan untuk triprolidin HCl diperoleh % recovery = 101,14%,
simpangan baku relatif (RSD) = 1,6617 %. Hasil ini menunjukkan
spektrofotometri derivatif metode zero crossing yang digunakan memenuhi
persyaratan akurasi dan presisi.
Kata-kata kunci : pseudoefedrin HCl, triprolidin HCl, spektrofotometri derivatif,
DERIVATIVE SPECTROPHOTOMETRY APPLIED FOR DETERMINATION OF TRIPROLIDINE HYDROCHLORIDE AND PSEUDOEPHEDRINE HYDROCHLORIDE MIXTURE IN TABLETS
ABSTRACT
Nowdays many dosage form of drug which contain more than one active
ingredient. One of combinations which is often used is triprolidine hydrochloride
and pseudoephedrine hydrochloride in tablet form. Pseudoephedrine
hydrochloride is sympathomimetic drug. Triprolidine hydrochloride is
antihistamine drug.
The purpose of this research is to determine pseudoephedrine
hydrochloride and triprolidine hydrochloride mixture using derivative
spectrophotometry with zero crossing method in HCl 0,1 N. Pseudoephedrine hydrochloride and triprolidine hydrochloride mixturing were determined by
measuring the second derivative ratio amplitudes, at 271 nm (zero crossing for triprolidine hydrochloride) and at 318 nm (zero crossing for pseudoephedrine hydrochloride) respectively.
The determination of calibration curve linearity showed a linear
correlation between the absorbtion versus concentration, for pseudoephedrine
hydrochloride with the correlation coefficient, r = 0.9999 and the regression Y =
(9,06X + 8,00). 10-6 , for triprolidine hydrochloride with the correlation
coefficient, r = 0.9998 and the regression Y = (48,9X – 9,0) . Limit of detection
(LOD) and limit of qua ntitation (LOQ) of pseudoephedrine hydrochloride 3,16
mcg/ml and 10,50 mcg/ml. Limit of detection (LOD) and limit of qua ntitation
The result of determination of pseudoephedrine hydrochloride and
triprolidine hydrochloride mixture the requirement of the thirtieth edition United
States Pharmacopoeia 2007. The validation test of tablet Tremenza® showed
pseudophedrine has percent recovery = 99,90 %, relative standard deviation
(RSD) = 0,9204 % and triprolidine hydrochloride has percent recovery = 101,14 %, relative standard deviation (RSD) = 1,6667%. These result showed that
derivative spectrophotometric method fulfilled the requirement of accuracy and
precision.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vii
ABSTRACT ... ix
DAFTAR ISI ... xi
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Bahan ... 5
2.1.1 Pseudoefedrin Hidroklorida ... 5
2.1.2 Triprolidin Hidroklorida ... 6
2.2 Spektrofotometri Infra Merah (IR) ... 7
2.3 Spektrofotometri Ultraviolet ... 8
2.4.1 Pengertian Spektrofotometri Derivatif ... 11
3.5.2.1 Pembuatan Spektrum Serapan Maksimum
Pseudoefedrin HCl ... 20
3.5.2.1 Pembuatan Spektrum Serapan Maksimum Triprolidin HCl ... 20
3.5.4 Pembuatan Spektrum Serapan Derivatif ... 20
3.5.4.1 Pembuatan Spektrum Serapan Derivatif Pseudoefedrin HCl ... 20
3.5.4.2 Pembuatan Spektrum Serapan Derivatif Triprolidin HCl ... 21
3.5.5 Penentuan Zero Crossing ... 21
3.5.6 Penentuan Panjang Gelombang (λ) Analisis ... 21
3.5.7 Pembuatan dan Penentuan Linearitas Kurva Kalibrasi ... 21
3.5.7.1 Pembuatan dan Penentuan Linearitas Kurva Kalibrasi Pseudoefedrin HCl ... 22
3.5.7.2 Pembuatan dan Penentuan Linearitas Kurva Kalibrasi Triprolidin HCl ... 23
3.5.8 Penentuan Kadar pseudoefedrin HCl dan Triprolidin HCl Dalam Sediaan Tablet ... 3.5.9 Uji Validasi ... 24
3.5.9.1 Uji Akurasi ... 24
3.5.9.2 Uji Presisi ... 24
3.5.10 Analisis Data Statistik ... 25
BAB IV HASIL DAN PEMBAHASAN ……… 27
4.1 Uji Identifikasi Menggunakan Spektrofotometer FTIR ... 27
4.2 Pembuatan Kurva Serapan Maksimum ... 29
4.3 Pembuatan Kurva Serapan Biasa ... 30
4.4 Pembuatan Kurva Serapan Derivat Pertama ... 37
4.5 Penentuan Zero Crossing pada Derivat pertama ... 43
4.6 Pembuatan Kurva Serapan Derivat Kedua ... 46
4.7 Penentuan Zero Crossing pada Derivat Kedua ... 53
4.8 Penentuan Panjang Gelombang (λ) Analisis ... 57
4.9 Pembuatan dan Penentuan Linearitas Kurva Kalibrasi ... 68
4.10 Penentuan Kadar Triprolidin HCl dan Pseudoefedrin HCl dalam Sediaan Tablet ……….. 70
4.11 Uji Validasi ………. 71
BAB V KESIMPULAN DAN SARAN ... 74
5.1 Kesimpulan ... 74
5.2 Saran ... 75
DAFTAR PUSTAKA ... 76
DAFTAR TABEL
Halaman
Tabel 1. Data bilangan gelombang (dalam cm-1) pada daerah sidik jari dari pseudoefedrin HCl ... 28
Tabel 2. Data bilangan gelombang hasil identifikasi gugus fungsi dan
ikatan dari pseudoefedrin HCl ... 28
Tabel 3. Data bilangan gelombang (dalam cm-1) pada daerah sidik jari dari
triprolidin HCl ... 29
Tabel 4. Data bilangan gelombang hasil identifikasi gugus fungsi dan
ikatan dari triprolidin HCl ... 29
Tabel 5. Serapan campuran yang di dalamnya terdapat triprolidin HCl 12,5 mcg/ml dengan pseudoefedrin HCl
300 mcg/ml ……… 68
Tabel 6. Data Hasil Perhitungan Kadar Obat Setelah Dilakukan Analisa
Statistik ... ... 70
Tabel 7. Data hasil pengujian perolehan kembali pseudoefedrin HCl dan triprolidin HCl dengan metode penambahan baku standar (standard
DAFTAR GAMBAR
Halaman
Gambar 1. Rumus struktur pseudoefedrin ... 5
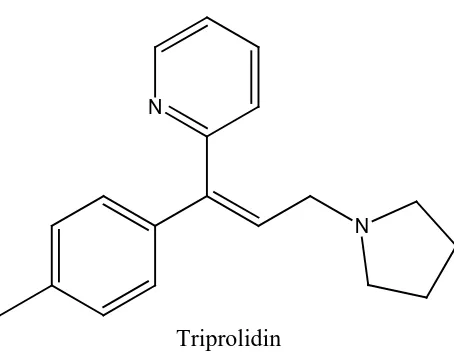
Gambar 2. Rumus struktur triprolidin ... 6
Gambar 3. Kurva serapan derivat pertama sampai derivat keempat ... 12
Gambar 4. Kurva sederhana aplikasi zero crossing (z) ... 13
Gambar 5. Spektrum inframerah pseudoefedrin HCl BPFI ... 27
Gambar 6. Spektrum inframerah triprolidin HCl BPFI ... 28
Gambar 7. Spektrum inframerah triprolidin HCl BPFI ... 30
Gambar 8. Kurva serapan maksimum triprolidin HCl 12,5 mcg/ml ... 30
Gambar 9. Kurva serapan biasa triprolidin HCl 5 mcg/ml ... 31
Gambar 10. Kurva serapan biasa triprolidin HCl 10 mcg/ml ... 31
Gambar 11. Kurva serapan biasa triprolidin HCl 15 mcg/ml ... 32
Gambar 12. Kurva serapan biasa triprolidin HCl 20 mcg/ml ... 32\
Gambar 13. Kurva serapan biasa triprolidin HCl 25 mcg/ml ... 33
Gambar 14. Kurva overlapping serapan biasa triprolidin HCl ... 33
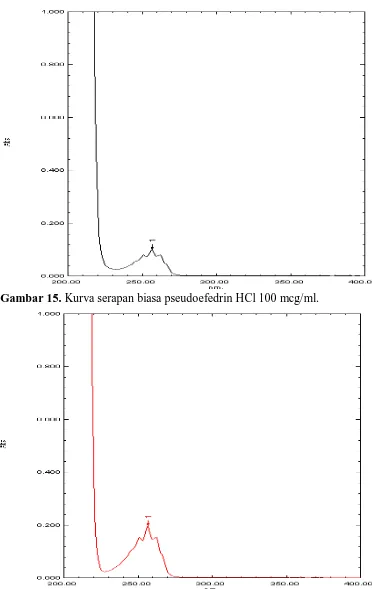
Gambar 15. Kurva serapan biasa pseudoefedrin HCl 100 mcg/ml ... 34
Gambar 16. Kurva serapan biasa pseudoefedrin HCl 200 mcg/ml ... 34
Gambar 17. Kurva serapan biasa pseudoefedrin HCl 300 mcg/ml ... 35
Gambar 18. Kurva serapan biasa pseudoefedrin HCl 400 mcg/ml ... 35
Gambar 19. Kurva serapan biasa pseudoefedrin HCl 500 mcg/ml ... 36
Gambar 20. Kurva overlapping serapan biasa pseudoefedrin HCl ... 36
Gambar 22. Kurva serapan derivat pertama triprolidin HCl 10 mcg/ml ... 38
Gambar 23. Kurva serapan derivatm pertama triprolidin HCl 15 mcg/ml . 38
Gambar 24. Kurva serapan derivat pertama triprolidin HCl 20 mcg/ml. ... 39
Gambar 25. Kurva serapan derivat pertama triprolidin HCl 25 mcg/ml. .. 39
Gambar 26. Kurva overlapping serapan triprolidin HCl derivat pertama .. 40
Gambar 27. Kurva serapan derivat pertama pseudoefedrin HCl 100 mcg/ml ... 40
Gambar 28. Kurva serapan derivat pertama pseudoefedrin HCl 200 mcg/ml. ... 41
Gambar 29. Kurva serapan derivat pertama pseudoefedrin HCl 300 mcg/ml ... 41
Gambar 30. Kurva serapan derivat pertama pseudoefedrin HCl 400 mcg/ml ... 42
Gambar 31. Kurva serapan derivat pertama pseudoefedrin HCl 500 mcg/ml ... 42
Gambar 32. Kurva overlapping serapan pseudoefedrin HCl derivat pertama ... 43
Gambar 39. Kurva serapan derivat kedua triprolidin HCl 10 mcg/ml. ... 47
Gambar 40. Kurva serapan derivat kedua triprolidin HCl 15 mcg/ml ... 48
Gambar 41. Kurva serapan derivat kedua triprolidin HCl 20 mcg/ml ... 48
Gambar 43. Kurva overlapping serapan derivat kedua dari
triprolidin HCl ... 49
Gambar 44. Kurva serapan derivat kedua pseudoefedrin HCl 100 mcg/ml ... 50
Gambar 45. Kurva serapan derivat kedua pseudoefedrin HCl 200 mcg/ml ... 50
Gambar 46. Kurva serapan derivat kedua pseudoefedrin HCl 300 mcg/ml ... 51
Gambar 47. Kurva serapan derivat kedua pseudoefedrin HCl 400 mcg/ml ... 51
Gambar 48. Kurva serapan derivat kedua pseudoefedrin HCl 500 mcg/ml ... 52
Gambar 49. Kurva overlapping serapan derivat kedua dari pseudoefedrin HCl ... 52
Gambar 60. Kurva serapan biasa campuran yang di dalamnya terdapat triprolidin HCl 12,5 mcg/ml dan pseudoefedrin HCl 300 mcg/ml ... 59
Gambar 62. Kurva overlapping serapan biasa triprolidin HCl
12,5 mcg/ml, pseudoefedrin HCl 300 mcg/ml, dan campuran yang di dalamnya terdapat triprolidin HCl 12,5
mcg/ml dan pseudoefedrin HCl 300 mcg/ml ... 60
Gambar 63. Kurva serapan derivat pertama triprolidin HCl 12,5 mcg/ml . 60 Gambar 64. Kurva serapan derivat pertama pseudoefedrin HCl
300 mcg/ml ... 61 Gambar 65. Kurva serapan derivat pertama campuran yang di
dalamnya terdapat triprolidin HCl dan pseudoefedrin HCl
300 mcg/ml ... 61 Gambar 66. Kurva overlapping serapan derivat pertama triprolidin HCl
12,5 mcg/ml dengan pseudoefedrin HCl 300 mcg/ml... 62 Gambar 67. Kurva overlapping serapan derivat pertama dari triprolidin
HCl 12,5 mcg/ml, pseudoefedrin HCl 300 mcg/ml, dan campuran yang di dalamnya terdapat triprolidin HCl 12,5
mcg/ml dan pseudoefedrin HCl 300 mcg/ml ... 62
Gambar 68. Kurva serapan derivat kedua triprolidin HCl 12,5 mcg/ml... 63 Gambar 69. Kurva serapan derivat kedua pseudoefedrin HCl
300 mcg/ml ... 63 Gambar 70. Kurva serapan derivat kedua campuran yang di
dalamnya terdapat triprolidin HCl dan pseudoefedrin HCl
300 mcg/ml ... 64
Gambar 71. Kurva overlapping serapan derivat kedua triprolidin
HCl 12,5 mcg/ml dengan pseudoefedrin HCl 300 mcg/ml ... 64 Gambar 72. Zero crossing dari triprolidin HCl 12,5 mcg/ml pada
λ = 271 nm ... 65 Gambar 73. Zero crossing dari pseudoefedrin HCl 300 mcg/ml pada
λ = 285,21-400 nm ... 65
Gambar 74. Kurva overlapping serapan derivat kedua dari
triprolidin HCl 12,5 mcg/ml, pseudoefedrin HCl 300 mcg/ml, dan campuran yang di dalamnya terdapat triprolidin HCl 12,5 mcg/ml dengan pseudoefedrin HCl
300 mcg/ml ... 66
Gambar 76. Panjang gelombang (λ) analisis untuk triprolidin HCl ... 67
Gambar 77. Kurva kalibrasi pseudoefedrin HCl pada panjang gelombang 271 nm ... 69
Gambar 78. Kurva kalibrasi triprolidin HCl pada panjang gelombang 318 nm ... 69
Gambar 79. Kurva serapan derivat kedua triprolidin HCl 12,5 mcg/ml .... 79
Gambar 80. Kurva serapan derivat kedua pseudoefedrin HCl 300 mcg/ml ... 79
Gambar 81. Kurva serapan campuran yang di dalamnya terdapat pseudoefedrin HCl dan triprolidin HCl masing-masing dengan konsentrasi 300 mcg/ml dan 12,5 mcg/ml ... 80
Gambar 82. Kurva kalibrasi pseudoefedrin HCl pada kurva serapan derivat kedua pada panjang gelombang, λ = 271 nm . 82
Gambar 96. Kurva serapan perolehan kembali 80 %-1 pada
tablet Tremenza® ... 111
Gambar 97. Kurva serapan perolehan kembali 80 %-2 pada tablet Tremenza® ... 111
Gambar 98. Kurva serapan perolehan kembali 80 %-3 pada tablet Tremenza® ... 112
Gambar 99. Kurva serapan perolehan kembali 100 %-1 pada tablet Tremenza® ... 112
Gambar 100. Kurva serapan perolehan kembali 100 %-2 pada tablet Tremenza® ... 113
Gambar 101. Kurva serapan perolehan kembali 100 %-3 pada tablet Tremenza® ... 113
Gambar 102. Kurva serapan perolehan kembali 120 %-1 pada tablet Tremenza® ... 114
Gambar 103. Kurva serapan perolehan kembali 120 %-2 pada tablet Tremenza® ... 114
Gambar 104. Kurva serapan perolehan kembali 120 %-3 pada tablet Tremenza® ... 115
Gambar 105. Spektrofotometer UV (Shimadzu 1800) ... 124
Gambar 106. Sonikator (Branson 1510). ... 124
Gambar 107. Spektrofotometer FTIR (Shimadzu) ... 125
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Bilangan Gelombang Spektrum IR Pseudoefedrin
HCl BPFI ... ... 78
Lampiran 2. Data Bilangan Gelombang Spektrum IR Triprolidin
HCl BPFI ... 79
Lampiran 3. Kurva Serapan Penentuan Panjang Gelombang Analisis ... 80
Lampiran 4. Kurva Kalibrasi Pseudoefedrin HCl dan Triprolidin HCl ... 82
Lampiran 5. Perhitungan Regresi Kalibrasi Pseudoefedrin HCl ... 84
Lampiran 6. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi
(LOQ) Pseudoefedrin HCl ... 86
Lampiran 7. Perhitungan Regresi Kalibrasi Triprolidin HCl ... 87
Lampiran 8. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi
(LOQ) Triprolidin HCl ………. 89
Lampiran 9. Contoh Perhitungan Penetapan Kadar ... 90
Lampiran 10. Kurva Serapan Penetapan Kadar Trifed® ... 92
Lampiran 11. Kurva Serapan Penetapan Kadar Tremenza® ... 95
Lampiran 12. Data Kadar Triprolidin HCl dalam Sediaan Tablet ... 98
Lampiran 13. Data Kadar Pseudoefedrin HCl dalam Sediaan Tablet ... 99
Lampiran 14. Perhitungan Statistik Pseudoefedrin HCl pada Tablet Trifed® 100
Lampiran 15. Perhitungan Statistik Kadar Triprolidin HCl pada Tablet
Trifed®……….. 101
Lampiran 16. Perhitungan Statistik Kadar Pseudoefedrin HCl
pada Tablet Tremenza® ……… 103
Lampiran 17. Perhitungan Statistik Kadar Triprolidin HCl
pada Tablet Tremenza® ……… 105
(% recovery) ... 107
Lampiran 19. Kurva Serapan Tremenza® pada Uji Perolehan Kembali ... 111
Lampiran 20. Data Hasil Persen Perolehan Kembali Pseudoefedrin HCl padaTablet Tremenza® dengan Metode
Penambahan Baku (Standard Addition Method)... 116
Lampiran 21. Data Hasil Persen Perolehan Kembali Triprolidin HCl padaTablet Tremenza® dengan Metode Penambahan
Baku (Standard Addition Method) ... 117
Lampiran 22. Perhitungan Rata-Rata, Standar Deviasi dan Relatif Standar deviasi Perolehan Kembali Pseudoefedrin HCl pada
Tablet Tremenza® ... 118
Lampiran 23. Perhitungan Rata-Rata, Standar Deviasi dan Relatif Standar deviasi Perolehan Kembali Triprolidin HCl pada Tablet
Tremenza®……… 119
Lampiran 24. Daftar Distribusi Nilai t ... .. 120
Lampiran 25. Daftar Spesifikasi Sampel……… 121
Lampiran 26. Sertifikat Bahan Baku Pseudoefedrin HCl dan Triprolidin HCl BPFI……… 122
PEMANFAATAN SPEKTROFOTOMETRI DERIVATIF UNTUK PENETAPAN KADAR CAMPURAN PSEUDOEFEDRIN HIDROKLORIDA DAN TRIPROLIDIN HIDROKLORIDA DALAM
SEDIAAN TABLET
ABSTRAK
Saat ini banyak beredar sediaan obat dengan lebih dari satu komponen zat
aktif. Salah satu kombinasi yang sering digunakan adalah pseudoefedrin HCl dan
triprolidin HCl yang tersedia dalam bentuk sediaan tablet dan beredar dengan
berbagai merek dagang. Pseudoefedrin HCl adalah salah satu obat
simpatomimetik. Triprolidin HCl adalah obat antihistamin.
Tujuan penelitian ini adalah untuk menetapkan kadar campuran
pseudoefedrin HCl dan triprolidin HCl dengan menggunakan spektrofotometri
derivatif dengan metode zero crossing dalam pelarut HCl 0,1 N. Panjang
gelombang analisis untuk menetapkan kadar campuran pseudoefedrin HCl dan
triprolidin HCl pada spektrum serapan derivat kedua yaitu pada panjang
gelombang 271 nm (zero crossing untk triprolidin HCl) dan pada panjang
gelombang 318 nm (zero crossing untuk pseudoefedrin HCl).
Penentuan linieritas kurva kalibrasi menunjukkan hubungan yang linier
antara absorbansi dengan konsentrasi, untuk pseudoefedrin HCl dengan koefisien
korelasi, r = 0,9999 dan persamaan regresi Y = (9,06X +8,00).10-6; untuk
triprolidin HCl dengan koefisien korelasi, r = 0,9998 dan persamaan regresi Y =
(48,9X – 9,0).10-6 . Batas deteksi (LOD) dan batas kuantitasi (LOQ) untuk
pseudoefedrin HCl berturut-turut adalah 3,16 mcg/ml dan 10,53 mcg/ml
Hasil penetapan kadar campuran pseudoefedrin HCl dan triprolidin HCl
yang dianalisis dalam tablet di pasaran menunjukkan bahwa semua memenuhi
persyaratan sesuai dengan persyaratan yang tertera pada USP (United States
Pharmacopoeia) XXX tahun 2007. Hasil uji validasi yang dilakukan terhadap
tablet Tremenza® (Sanbe) memenuhi persyaratan validasi metode, untuk
pseudoefedrin HCl diperoleh % recovery = 99,90%, simpangan baku relatif
(RSD) = 0,9204% dan untuk triprolidin HCl diperoleh % recovery = 101,14%,
simpangan baku relatif (RSD) = 1,6617 %. Hasil ini menunjukkan
spektrofotometri derivatif metode zero crossing yang digunakan memenuhi
persyaratan akurasi dan presisi.
Kata-kata kunci : pseudoefedrin HCl, triprolidin HCl, spektrofotometri derivatif,
DERIVATIVE SPECTROPHOTOMETRY APPLIED FOR DETERMINATION OF TRIPROLIDINE HYDROCHLORIDE AND PSEUDOEPHEDRINE HYDROCHLORIDE MIXTURE IN TABLETS
ABSTRACT
Nowdays many dosage form of drug which contain more than one active
ingredient. One of combinations which is often used is triprolidine hydrochloride
and pseudoephedrine hydrochloride in tablet form. Pseudoephedrine
hydrochloride is sympathomimetic drug. Triprolidine hydrochloride is
antihistamine drug.
The purpose of this research is to determine pseudoephedrine
hydrochloride and triprolidine hydrochloride mixture using derivative
spectrophotometry with zero crossing method in HCl 0,1 N. Pseudoephedrine hydrochloride and triprolidine hydrochloride mixturing were determined by
measuring the second derivative ratio amplitudes, at 271 nm (zero crossing for triprolidine hydrochloride) and at 318 nm (zero crossing for pseudoephedrine hydrochloride) respectively.
The determination of calibration curve linearity showed a linear
correlation between the absorbtion versus concentration, for pseudoephedrine
hydrochloride with the correlation coefficient, r = 0.9999 and the regression Y =
(9,06X + 8,00). 10-6 , for triprolidine hydrochloride with the correlation
coefficient, r = 0.9998 and the regression Y = (48,9X – 9,0) . Limit of detection
(LOD) and limit of qua ntitation (LOQ) of pseudoephedrine hydrochloride 3,16
mcg/ml and 10,50 mcg/ml. Limit of detection (LOD) and limit of qua ntitation
The result of determination of pseudoephedrine hydrochloride and
triprolidine hydrochloride mixture the requirement of the thirtieth edition United
States Pharmacopoeia 2007. The validation test of tablet Tremenza® showed
pseudophedrine has percent recovery = 99,90 %, relative standard deviation
(RSD) = 0,9204 % and triprolidine hydrochloride has percent recovery = 101,14 %, relative standard deviation (RSD) = 1,6667%. These result showed that
derivative spectrophotometric method fulfilled the requirement of accuracy and
precision.
BAB I PENDAHULUAN
1.1Latar Belakang
Saat ini banyak beredar sediaan obat dengan lebih dari satu komponen zat
aktif. Salah satu kombinasi yang sering digunakan adalah pseudoefedrin HCl dan
triprolidin HCl yang tersedia dalam bentuk sediaan tablet dengan berbagai merek
dagang. Pseudoefedrin HCl adalah salah satu obat simpatomimetik dan triprolidin
HCl adalah obat antihistamin (Moffat, 2004).
Bentuk sediaan farmasi seperti tablet harus memenuhi beberapa
persyaratan sesuai dengan standar yang ada pada acuan misalnya pada farmakope.
Salah satu persyaratan tersebut adalah persyaratan kadar. Persyaratan kadar untuk
sediaan tablet campuran pseudoefedrin HCl dan triprolidin HCl menurut USP
(United States Pharmacopoeia) XXX ( 2007 ) yaitu mengandung triprolidin HCl
dan pseudoefedrin HCl tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari
jumlah yang tertera pada etiket.
Triprolidin HCl dapat ditetapkan kadarnya dengan spektrofotometri
ultraviolet pada panjang gelombang maksimum 290 nm ( A 1%, 1 cm dalam
larutan asam = 347a ). Demikian juga dengan pseudoefedrin HCl dapat ditetapkan
kadarnya dengan spektrofotometri ultraviolet pada panjang gelombang maksimum
257 nm (A 1%, 1 cm dalam larutan asam = 11,9a) (Moffat, 2004).
Pada penetapan kadar campuran pseudoefedrin HCl atau triprolidin HCl
secara spektrofotometri ultraviolet yang menjadi kendala adalah terjadinya
senyawa ini dapat larut dalam pelarut yang sama yaitu dalam HCl 0,1 N serta
memiliki serapan maksimum pada panjang gelombang yang berdekatan.
USP XXX (2007) merekomendasikan penggunaan kromatografi cair
kinerja tinggi (KCKT) untuk menetapkan kadar kedua komponen itu sedangkan Sriphong (2009) menganjurkan spektrofotometri derivatif. Hayun (2006) juga melaporkan penggunaan spektrofotometri derivatif pada panjang gelombang zero
crossing untuk penetapan kadar campuran tersebut.
Spektrofotometri derivatif merupakan metode manipulatif terhadap spektra
pada spektrofotometri ultraviolet dan cahaya tampak. Pada spektrofotometri konvensional, spektrum serapan merupakan plot serapan (A) terhadap panjang gelombang (λ). Pada spektrofotometri derivatif, plot A lawan λ, ditransformasikan menjadi plot dA/dλ lawan λ untuk derivatif pertama, dan d2A/ dλ2lawan λ untuk
derivatif kedua, dan seterusnya. Spektrofotometri derivatif dapat digunakan untuk
analisis kuantitatif zat-zat yang spektrumnya tumpang tindih dan/atau spektrumnya mungkin tersembunyi dalam suatu bentuk spektrum besar (Hayun, 2006).
Ada tiga aplikasi spektrofotometri derivatif yang sering digunakan dalam
anlisa kuantitatif antara lain metode zero crossing, metode peak to peak dan
metode multivariate spectrrophotometric calibration (Talsky, 1994).
Pada penelitian ini dilakukan penetapan kadar triprolidin HCl dan pseudoefedrin HCl dalam sediaan tablet secara simultan (tanpa pemisahan terlebih
dahulu) yaitu menggunakan spektrofotometri derivatif dengan aplikasi metode
Untuk memperoleh validitas dari metode ini, maka dilakukan batas deteksi
(limit of detection, LOD), batas kuantitasi (limit of quantitation, LOQ), uji akurasi yang dinyatakan dalam persen perolehan kembali (% recovery) dan uji presisi
yang dinyatakan dalam Relative Standart Deviation (RSD). 1.2 Perumusan Masalah
1. Apakah campuran pseudoefedrin HCl dan triprolidin HCl dalam sediaan
tablet dapat ditetapkan kadarnya secara simultan dengan menggunakan
spektrofotometri derivatif pada panjang gelombang zero crossing dan
apakah metode yang digunakan memenuhi syarat validasi metode ?
2. Apakah kadar campuran pseudoefedrin HCl dan triprolidin HCl dalam
sediaan tablet yang ditetapkan menggunakan spektrofotometri derivatif
pada panjang gelombang zero crossing secara simultan memenuhi
persyaratan USP XXX tahun 2007?
1.3 Hipotesis
1. Campuran pseudoefedrin HCl dan triprolidin HCl dalam sediaan tablet
dapat ditetapkan kadarnya secara simultan dengan menggunakan
spektrofotometri derivatif pada panjang gelombang zero crossing dan
memenuhi syarat validasi metode.
2. Kadar campuran pseudoefedrin HCl dan triprolidin HCl dalam sediaan
tablet yang ditetapkan secara simultan menggunakan spektrofotometri
derivatif pada panjang gelombang zero crossing memenuhi persyaratan
1.4 Tujuan Penelitian
1. Melakukan penetapan kadar campuran pseudoefedrin HCl dan triprolidin
HCl secara simultan dalam sediaan tablet mengunakan spektrofotometri
derivatif pada panjang gelombang zero crossing dan melakukan uji
validasi terhadap metode yang digunakan.
2. Membandingkan hasil yang diperoleh pada penetapan kadar campuran
pseudoefedrin HCl dan triprolidin HCl secara simultan mengunakan
spektrofotometri derivatif pada panjang gelombang zero crossing dengan
persyaratan USP XXX tahun 2007.
1.5 Manfaat Penelitian
Manfaat penelitian adalah untuk memperoleh panjang gelombang zero
crossing analisis dalam menetapkan kadar pseudoefedrin HCl dan triprolidin HCl
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Bahan
2.1.1 Pseudoefedrin Hidroklorida
OH NH
Pseudoefedrin
Gambar 1. Rumus struktur pseudoefedrin
Pseudoefedrin adalah salah satu alkaloid yang diperoleh dari Epedra sp dan
merupakan stereoisomer dari efedrin. Pseudoefedrin HCl mempunyai rumus
molekul = C10H15NO.HCl; BM = 201,70; pemerian : hablur putih atau serbuk
putih, serbuk halus putih atau hampir putih, bau khas lemah; kelarutan: sangat
mudah larut dalam air, mudah larut dalam etanol, agak sukar larut dalam
kloroform; titik lebur : 182,50 – 182,50 ; pKa = 9,8 (Ditjen POM, 1995; Moffat,
2007).
Pseudoefedrin HCl adalah salah satu obat simpatomimetik yang bekerja
dengan cara langsung terhadap reseptor di otot polos dan jantung dan juga secara
tak langsung dapat membebaskan noradrenalin. Penggunaan utamanya adalah
bronkodilatasi kuat (β2), sebagai dekongestan. Efek midriatikum dari obat ini
kurang merangsang dibandingkan dengan adrenalin. Waktu paruh plasmanya
untuk flu. Volume distribusi 3L/Kg. Dosis 3-4 kali sehari 60 mg (Tjay, T.H. dan
Rahardja, K., 2010).
Salah satu analisa kualitatif untuk efedrin dan derivatnya adalah reaksi
Chen-kao. Reaksi ini adalah reaksi dengan CuSO4 dan NaOH menghasilkan
warna ungu. Jika dikocok dengan dengan eter, maka akan terbentuk dua lapisan berwarna. Lapisan eter akan berwarna ungu dan lapisan air akan berwarna biru.
Reaksi ini adalah reaksi pembentukan kompleks antara Cu dengan turunan fenilalkilamin yang mempunyai gugus amino dan gugus hidroksi. Selain
menggunakan eter dapat juga digunakan n-butanol yang akan menghasilkan warna ungu pada lapisan n-butanol dan warna biru pada lapisan air (Roth, et al., 1991).
Pseudoefedrin HCl dapat ditetapkan kadarnya dengan beberapa cara yaitu
spektrofotometri ultraviolet pada panjang gelombang 257 nm (A 1%, 1 cm dalam
larutan asam = 11,9a), kromatografi gas, dan dengan kromatografi cair kinerja
tinggi (Moffat, 2007). Dapat juga ditetapkan kadarnya secara titrasi bebas air
karena mempunyai atom N yang bersifat basa (Cairns, 2008).
2.1.2 Triprolidin Hidroklorida
N
N
Tripprolidin HCl mempunyai rumus molekul = C19H22N2.HCl.H2O; berat molekul
= 332,87; pemerian : serbuk hablur putih, ringan, berbau tidak enak, larutan
bersifat basa terhadap lakmus, melebur pada suhu lebih kurang 115oC; kelarutan
: larut dalam air, dalam etanol dan dalam kloroform, tidak larut dalam eter; pKa =
6,5 (Ditjen POM, 1995; Moffat, 2007).
Triprolidin HCl adalah antihistamin yang bekerja dengan daya kuat.
Bekerja mengurangi efek histamin terhadap tubuh dengan cara menghambat
reseptor histamin. Mula kerjanya cepat dan bertahan lama. Dosis 1-10 mg dan
diberikan pada malam hari berhubung dengan efek sedatifnya (Tjay, T.H. dan
Rahardja, K., 2010). Waktu paruhnya 1,5 sampai 20 jam, tetapi rata-rata 5 jam
(Moffat, 2007).
Triprolidin HCl dapat ditetapkan kadarnya dengan beberapa metode antara
lain dengan spektrofotometri ultraviolet pada panjang gelombang maksimum 290
nm (A 1%, 1 cm dalam larutan asam = 347a), dengan kromatografi cair kinerja
tinggi, dengan densitometri dan dengan kromatografi gas (Moffat, 2007).
Triprolidin juga dapat ditetapkan kadarnya secara titrasi bebas air karena
mempunyai atom N yang bersifat basa (Cairns, 2008).
2.2 Spektrofotometri Infra Merah (IR)
Senyawa kimia yang memiliki ikatan kovalen, baik senyawa organik
maupun senyawa anorganik akan menyerap radiasi elektromagnetik pada
frekuensi yang berbeda pada daerah InfraMerah. Terjadinya absorbsi karena
molekul tereksitasi ke tingkat energi yang lebih tinggi ketika mengabsorbsi radiasi
InfraMerah. Karena setiap ikatan yang berbeda memiliki frekuensi getaran yang
lingkungan yang berbeda, maka tidak ada dua molekul yang berbeda struktur
memiliki spektrum InfraMerah yang sama (Pavia, et al., 1979).
Radiasi elektromagnetik InfraMerah bila dilewatkan pada suatu sampel
maka akan diserap oleh ikatan – ikatan molekul di dalam sampel sehingga
molekul tersebut akan mengalami gerakan vibrasi regangan dan vibrasi
bengkokan. Bentuk vibrasi regangan ini dapat dibagi lagi atas beberapa, yakni:
regangan asimetrik dan regangan simetrik. Bentuk vibrasi bengkokan juga dapat
dibagi atas: guntingan, pelintiran, kibasan, dan goyangan. Vibrasi regangan terjadi
pada bilangan gelombang yang lebih besar (panjang gelombang yang lebih kecil)
sedangkan vibrasi bengkokan terjadi pada bilangan gelombang yang lebih kecil
(panjang gelombang yang lebih besar) (Pavia, et al., 1979; Watson, 2005).
Radiasi elektromagnetik yang diserap merupakan ciri khas dari setiap
ikatan. Spektrum InfraMerah dapat digunakan untuk memeriksa identitas bahan
baku obat yang digunakan dan dapat mengidentifikasi bahan kimia sintetik
sebagai pemeriksaan pendahuluan (Watson, 2005).
2.3 Spektrofotometri Ultraviolet
Jika suatu molekul sederhana dikenakan radiasi elektromagnetik maka
molekul tersebut akan menyerap radiasi elektromagnetik. Interaksi antara molekul
dengan radiasi elektromagnetik ini akan meningkatkan energi dari tingkat dasar ke
tingkat tereksitasi. Apabila pada molekul yang sederhana tadi hanya terjadi
transisi elektronik pada satu macam gugus yang terdapat pada molekul, maka
hanya akan terjadi satu absorpsi yang merupakan pita spektrum. Terjadinya dua
kompleks karena terjadi beberapa transisi sehingga mempunyai lebih dari satu
panjang gelombang (Rohman, 2007).
Gugus fungsi seperti –OH, -O, -NH2, dan –OCH3 yang memberikan
transisi n → π* disebut gugus auksokrom. Gugus ini adalah gugus yang tidak
dapat menyerap radiasi ultraviolet-sinar tampak, tetapi apabila gugus ini terikat
pada gugus kromofor mengakibatkan pergeseran panjang gelombang ke arah yang
lebih besar (pergeseran batokromik) (Rohman, 2007).
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel
yang disinari. Sedangkan menurut Beer, serapan berbanding lurus dengan
konsentrasi. Kedua pernyataan ini dapat dijadikan satu dalam Hukum
Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi
dan ketebalan sel, yang dapat ditulis dengan persamaan :
A= a.b.c (g/liter) atau A= ε. b. c (mol/liter)
Dimana: A = serapan
a = absorptivitas
b = ketebalan sel
c = konsentrasi
ε = absorptivitas molar
Hukum Lambert-Beer menjadi dasar aspek kuantitatif spektrofotometri
dimana konsentrasi dapat dihitung berdasarkan rumus di atas. Absorptivitas
merupakan suatu tetapan dan spesifik untuk setiap molekul pada panjang
gelombang dan pelarut tertentu.
Penggunaan utama spektrofotometri ultraviolet adalah dalam analisis
mengabsorpsi radiasi, akan terjadi pengurangan kekuatan radiasi yang mencapai
detektor. Parameter kekuatan energi radiasi yang diabsorpsi oleh molekul adalah
absorban (A) yang dalam batas konsentrasi tertentu nilainya sebanding dengan
banyaknya molekul yang mengabsorpsi radiasi. Senyawa yang tidak
mengabsorpsi radiasi ultraviolet-sinar tampak dapat juga ditentukan dengan
spektrofotometri ultraviolet-sinar tampak, apabila ada reaksi kimia yang dapat
mengubahnya menjadi kromofor atau dapat disambungkan dengan suatu pereaksi
kromofor .
Spektrofotometer adalah alat untuk mengukur transmitans atau serapan
suatu sampel sebagai fungsi panjang gelombang. Spektrofotometer merupakan
penggabungan dari dua fungsi alat yang terdiri dari spektrometer yang
menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan
fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang
diabsorpsi.
Menurut Day dan Underwood (1998), unsur -unsur terpenting suatu
spektrofotometer adalah sebagai berikut:
1. Sumber-sumber lampu: lampu deuterium digunakan untuk daerah UV
pada panjang gelombang dari 190-350 nm, sementara lampu halogen
kuarsa atau lampu tungsten digunakan untuk daerah visibel pada panjang
gelombang antara 350- 900 nm.
2. Monokromotor: digunakan untuk memperoleh sumber sinar yang
monokromatis. Alatnya dapat berupa prisma untuk mengarahkan sinar
3. Kuvet (sel): digunakan sebagai wadah sampel untuk menaruh cairan ke
dalam berkas cahaya spektrofotometer. Kuvet itu haruslah meneruskan
energi radiasi dalam dearah spektrum yang diinginkan. Pada pengukuran
didaerah tampak, kuvet kaca atau kuvet kaca corex dapat digunakan,
tetapi untuk pengukuran pada daerah ultraviolet kita harus menggunakan
sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Kuvet
tampak dan ultraviolet yang khas mempunyai ketebalan 1 cm, namun
tersedia kuvet dengan ketebalan yang sangat beraneka, mulai dari
ketebalan kurang dari 1 mm sampai 10 cm bahkan lebih.
4. Detektor: Peranan detektor penerima adalah memberikan respon terhadap
cahaya pada berbagai panjang gelombang.
5. Suatu amplifier (penguat) dan rangkaian yang berkaitan yang membuat
isyarat listrik itu dapat dibaca.
6. Sistem pembacaan yang memperlihatkan besarnya isyarat listrik
2.4 Spektrofotometri Derivatif
2.4.1 Pengertian Spektrofotometri Derivatif
Spektofotometri deivatif bersangkutan dengan transformasi spektrum serapan menjadi spektrum derivatif pertama, kedua atau spektrum derivatif
dengan order yang lebih tinggi Spektrum derivat pertama dibuat dengan memplotkan dA/dλ dengan panjang gelombang (Ditjen POM, 1995).
Pada spektrofotometri konvensional, spektrum serapan merupakan plot serapan (A) terhadap panjang gelombang (λ). Pada spektrofotometri derivatif, plot
A lawan λ, ditransformasikan menjadi plot dA/dλ lawan λ untuk derivatif
A = f(λ), order nol
dA/dλ = f ′(λ), order pertama
d2A/dλ2 = f ″(λ), order kedua
dan seterusnya( Moffat, 2007).
Sesuai dengan hukum Lambert-Beer, maka :
Gambar 3. Kurva serapan derivat pertama sampai derivat keempat
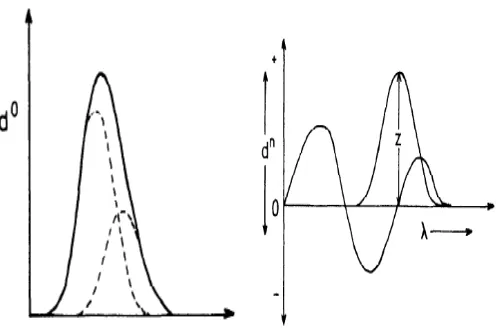
2.4.2 Metode Spektrofotometri Derivatif
Ada tiga metode spektrofotometri derivatif yang sering digunakan dalam
anlisa kuantitatif antara lain metode zero crossing, metode peak to peak dan
metode multivariate spectrrophotometric calibration. Panjang gelombang zero
crossing adalah panjang gelombang dimana senyawa tersebut mempunyai serapan
nol dan menjadi panjang gelombang analisis untuk zat lain dalam campurannya.
Gambar 4. Kurva sederhana aplikasi zero crossing (z)
Panjang gelombang peak to peak ditentukan dari penggabungan spektrum
derivatif larutan baku dan sampel (analit). Dari hasil penggabungan spektrum
derivatif tersebut, dicari daerah panjang gelombang dimana terdapat spektrum
yang saling berimpit satu sama lain secara total (Hayun, 2006).
2.4.3 Penggunaan Spektrofotometri Derivatif
Spektrofotometri derivatif banyak digunakan untuk zat-zat dalam suatu
memiliki serapan maksimum pada panjang gelombang yang berdekatan. Sebagai
contoh penetapan kadar campuran pseuoefedrin HCl, triprolidin HCl dan
dekstrometorfan HBr (Watson, 2007), penetapan kadar efedrin dan zat warna
dalam sediaan sirup (Cairns, 2008), penetapan kadar campuran parasetamol dan
ibuprofen (Hassan, 2008), penetapan kadar campuran parasetamol, kafein dan
salisilamid (Wulandari, 2006), penetapan kadar dekstrometorfan HBr dan
gliserilguaiakolat dalam sediaan tablet dan sirup obat batuk, campuran tetrasiklin dan oksitetrasiklin, penetapan kadar teofilin dan efedrin HCl dalam sediaan tablet,
penetapan kadar campuran vitamin B kompleks (Hayun,2006). Selain dalam bidang farmasi, spektrofotometri derivatif telah diaplikasikan secara luas di dalam analisis lingkungan, klinik, forensik, biomedik, dan industri (Skujins and
Varian, 2006).
2.4.4 Komponen Spektrofotometer Derivatif
Komponen-komponen pada spektrofotometer UV/Vis biasa sama dengan komponen pada spektrofotometer derivatif. Alat spektrofotometer harus dilengkapi dengan peralatan sedemikian rupa untuk dapat menghasilkan spektrum
derivatif (Ditjen POM, 1995). Biasanya spektrofotometer telah mempunyai software untuk mengolah data yang dapat dioperasikan malalui komputer yang
telah terhubung dengan spektrofotometer (Moffat, 2007). 2.5 Validasi Metode Analisis
Validasi metode adalah suatu proses yang menunjukkan bahwa prosedur
analitik telah sesuai dengan penggunaan yang dikehendaki. Validasi merupakan
persyaratan mendasar yang diperlukan untuk menjamin kualitas dan hasil dari
metode menurut USP (United States Pharmacopeia) XXX yaitu
akurasi/kecermatan, presisi/keseksamaan, spesifisitas, batas deteksi, batas
kuantitasi, linieritas, rentang dan kekuatan/ketahanan
2.5.1 Akurasi (Kecermatan)
Akurasi adalah kedekatan antara nilai hasil uji yang diperoleh melalui
metode analitik dengan nilai sebenarnya. Akurasi dinyatakan dalam persen
perolehan kembali (% recovery). Akurasi dapat ditentukan dengan dua metode,
yakni spiked – placebo recovery dan standard addition method. Pada spiked –
placebo recovery atau metode simulasi, analit murni ditambahkan (spiked) ke
dalam campuran bahan pembawa sediaan farmasi, lalu campuran tersebut
dianalisis dan jumlah analit hasil analisis dibandingkan dengan jumlah analit
teoritis yang diharapkan. Jika plasebo tidak memungkinkan untuk disiapkan,
maka sejumlah analit yang telah diketahui konsentrasinya dapat ditambahkan
langsung ke dalam sediaan farmasi. Metode ini dinamakan standard addition
method atau metode penambahan baku. (USP XXX, 2007; Ermer, 2005; Harmita,
2004).
2.5.2 Presisi (Keseksamaan)
Presisi adalah ukuran keterulangan metode analitik, termasuk di antaranya
kemampuan instrumen dalam memberikan hasil analitik yang reprodusibel.
Berdasarkan rekomendasi ICH (the International Conference on the
Harmonisation), karakteristik presisi dilakukan pada 3 tingkatan, yakni
keterulangan (repeatability), presisi antara (intermediate precision) dan
reprodusibilitas (reproducibility). Keterulangan dilakukan dengan cara
yang sama dalam periode waktu singkat. Presisi antara dikerjakan oleh analis
yang berbeda. Sedangkan reprodusibilitas dikerjakan oleh analis yang berbeda dan
di laboratorium yang berbeda (USP XXX, 2007; Épshtein, 2004).
2.5.3 Spesifisitas
Spesifisitas adalah kemampuan untuk mengukur analit yang dituju secara
tepat dan spesifik dengan adanya komponen lain dalam matriks sampel seperti
ketidakmurnian, produk degradatif dan komponen matriks. Secara umum,
spesifisitas dapat ditunjukkan oleh pendekatan secara langsung maupun tidak
langsung. Pendekatan langsung dapat ditunjukkan oleh minimalnya gangguan
oleh senyawa lain terhadap hasil analisis misalnya mendapatkan hasil yang sama
dengan atau tanpa senyawa pengganggu, resolusi kromatografik yang bagus dan
kemurnian puncak (peak purity). Pendekatan tidak langsung adalah lewat
pengamatan karakteristik akurasi dari metode tersebut. Bila akurasi metode telah
dapat diterima (acceptable) dan valid, maka metode tersebut otomatis telah masuk
kriteria sebagai metode yang spesifik (Ermer, 2005).
2.5.4 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah konsentrasi analit terendah dalam sampel yang masih
dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. Sedangkan batas
kuantitasi adalah konsentrasi analit terendah dalam sampel yang dapat ditentukan
dengan presisi dan akurasi yang dapat diterima pada kondisi operasional metode
yang digunakan (USP XXX, 2007).
2.5.5 Linearitas
Linieritas adalah kemampuan suatu metode untuk memperoleh hasil uji
diberikan. Linieritas dapat ditentukan secara langsung dengan pengukuran sampel
(analit) yang ditambahkan baku pada sekurang-kurangnya lima titik konsentrasi
yang mencakup seluruh rentang konsentrasi kerja (Ermer, 2005). Berdasarkan
rekomendasi ICH, linieritas dalam prakteknya diperkirakan pertama kali secara
visual dari penampilan kurva plot luas area / tinggi puncak dengan konsentrasi.
Untuk prosedur analitik, CDER (Center for Drug Evaluation and Research, US
FDA) merekomendasikan bahwa kriteria linieritasnya pada tingkat koefisien
korelasi tidak lebih kecil dari 0,999 (Épshtein, 2004).
2.5.6 Rentang
Rentang adalah konsentrasi terendah dan tertinggi yang mana suatu
metode analitik menunjukkan akurasi, presisi dan linieritas yang cukup (Ermer,
2005). Rentang suatu prosedur dapat divalidasi lewat pembuktian bahwa prosedur
analitik tersebut mampu memberikan presisi, akurasi dan linieritas yang dapat
diterima ketika digunakan untuk menganalisis sampel (USP XXX, 2007; USP
Convention, 2006).
2.5.7 Kekuatan (Ketahanan)
Kekuatan dievaluasi dengan melakukan perubahan parameter dalam
melakukan metode analitik seperti persentase kandungan pelarut organik dalam
fase gerak, pH larutan dapar, waktu pengekstraksian analit, komposisi
BAB III
METODOLOGI PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian ini termasuk jenis penelitian eksperimental dan penelitian ini
dilaksanakan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera
Utara pada bulan Juni 2010 sampai dengan Agustus 2010.
3.2 Alat
Alat – alat yang digunakan dalam penelitian adalah spektrofotometer IR
(Shimadzu), spektrofotometer ultraviolet (UV -1800 Shimadzu) double beam
yang dilengkapi dengan komputer, sonikator (Branson 1510), neraca analitik
(Mettler Toledo), kuvet, lumpang dan alu, alat-alat gelas dan alat-alat lainnya
yang diperlukan dalam penyiapan sampel dan larutan.
3.3 Bahan
Bahan – bahan yang digunakan dalam penelitian adalah HCl 0,1 N
(diencerkan 8,3 ml HCl 37% (v/v) dengan akuades secara kuantitatif dalam labu
tentukur 1 L), akuades (Laboratorium Kimia Farmasi Kuantitatif), triprolidin HCl
baku (BPFI), pseudoefedrin HCl baku (BPFI), tablet merek dagang Tremenza®
(Sanbe) dan Trifed® (Interbat).
3.4 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu tanpa
membandingkan antara satu tempat dengan tempat yang lain, karena sampel
digunakan adalah dua tablet merek dagang yaitu Tremenza® (Sanbe) dan Trifed®
(Interbat).
3.5 Prosedur Penelitian
3.5.1 Uji Identifikasi Baku Pseudoefedrin HCl dan Triprolidin HCl dengan Spektrofotometer IR
Uji identifikasi baku pseudoefedrin HCl dan triprolidin HCl dilakuka n
dengan menggunakan spektrofotometer FTIR, yaitu dengan cara: masing-masing
ditimbang 10 mg, lalu dicampur dengan 100 mg serbuk KBr dalam lumpang,
digerus hingga halus dan homogen, dan dianalisis pada bilangan gelombang
4000-500 cm-1.
3.5.2 Pembuatan Larutan Induk Baku
3.5.2.1 Pembuatan Larutan Induk Baku Triprolidin HCl
Ditimbang 50 mg triprolidin HCl BPFI, dimasukkan ke dalam labu
tentukur 50 ml, ditambahkan HCl 0,1 N, dikocok hingga larut, lalu dicukupkan
sampai garis tanda dengan HCl 0,1 N sehingga diperoleh larutan dengan
konsentrasi 1000 mcg/ml, larutan ini disebut larutan induk baku I (LIB I). Dari
larutan ini dipipet 12,5 ml, dimasukkan ke dalam labu tentukur 50 ml, diencerkan
dengan HCl 0,1 N sampai garis tanda, lalu dikocok sampai homogen sehingga
diperoleh larutan dengan konsentrasi 250 mcg/ml (LIB II).
3.5.2.2 Pembuatan Larutan Induk Baku Pseudoefedrin HCl
Ditimbang 50 mg pseudoefedrin HCl BPFI, dimasukkan ke dalam labu
tentukur 25 ml, ditambahkan HCl 0,1 N, dikocok hingga larut, lalu dicukupkan
sampai garis tanda dengan HCL 0,1 N sehingga diperoleh larutan dengan
konsentrasi 2000 mcg/ml, larutan ini disebut larutan induk baku I (LIB I). Dari
dengan HCl 0,1 N sampai garis tanda, lalu dikocok sampai homogen sehingga
diperoleh larutan dengan konsentrasi 1000 mcg/ml (LIB II).
3.5.3 Pembuatann Spektrum Serapan Maksimum
3.5.3.1 Pembuatan Spektrum Serapan Maksimum Pseudoefedrin HCl
Dipipet 1,85 ml Larutan Induk Baku II (LIB II) pseudoefedrin HCl
(konsentrasi = 1000 mcg/ml), dimasukkan ke dalam labu tentukur 25 ml,
diencerkan dengan HCl 0,1 N hingga garis tanda, lalu dikocok sampai homogen
sehingga diperoleh larutan dengan konsentrasi 370 mcg/ml, kemudian diukur
serapan pada panjang gelombang 200 – 400 nm.
3.5.3.2 Pembuatan Spektrum Serapan Maksimum Triprolidin HCl
Dipipet 1,25 ml Larutan Induk Baku II (LIB II) triprolidin HCl
(konsentrasi = 250 mcg/ml), dimasukkan ke dalam labu tentukur 25 ml,
diencerkan dengan HCl 0,1 N hingga garis tanda, lalu dikocok sampai homogen
sehingga diperoleh larutan dengan konsentrasi 12,5 mcg/ml, kemudian diukur
serapan pada panjang gelombang 200 – 400 nm.
3.5.4. Pembuatan Spektrum Serapan Derivatif
3.5.4.1 Pembuatan Spektrum Serapan Derivatif Pseudoefedrin HCl
Dipipet Larutan Induk Baku II pseudoefedrin HCl (konsentrasi = 1000
mcg/ml) sebanyak 1,25 ml; 2,5 ml; 3,75 ml; 5 ml; dan 6,25 ml. Masing-masing
dimasukkan ke dalam labu tentukur 10 ml, diencerkan dengan HCl 0,1 N hingga
garis tanda. Lalu dikocok sampai homogen sehingga diperoleh larutan dengan
konsentrasi 100; 200; 300; 400; dan 500 mcg/ml. Kemudian dibuat spektrum
serapan biasa (tanpa diderivatkan), spektrum serapan derivat pertama dan derivat
3.5.4.2 Pembuatan Spektrum Serapan derivatif Triprolidin HCl
Dipipet Larutan Induk Baku II triprolidin HCl (250 mcg/ml) sebanyak 0,5 ml; 1
ml; 1,5 ml; 2 ml; dan 2,5 ml. Masing-masing dimasukkan ke dalam labu tentukur
25 ml, diencerkan dengan HCl 0,1 N hingga garis tanda. Lalu dikocok sampai
homogen sehingga diperoleh larutan dengan konsentrasi 5; 10; 15; 20; dan 25
mcg/ml. Kemudian dibuat spektrum serapan biasa (tanpa diderivatkan), spektrum
serapan derivat pertama dan derivat kedua pada panjang gelombang 200-400 nm
dengan ∆λ = 10 nm.
3.5.5 Penentuan Zero Crossing
Penentuan zero crossing diperoleh dengan menumpangtindihkan atau
mengoverlappingkan spektrum serapan pada masing-masing derivat dari berbagai
konsentrasi larutan. Zero Crossing tiap spektrum derivat dari masing-masing zat
ditunjukkan oleh panjang gelombang yang memiliki serapan nol pada berbagai
konsentrasi.
3.5.6 Penentuan Panjang Gelombang (λ) Analisis
Dibuat larutan pseudoefedrin HCl dengan konsentrasi 300 mcg/ml,
triprolidin HCl dengan konsentrasi 12,5 mcg/ml, dan larutan campuran kedua zat itu sehingga di dalamnya terdapat pseudoefedrin HCl dengan konsentrasi 300
mcg/ml dan triprolidin HCl dengan konsentrasi 12,5 mcg/ml. Kemudian dibuat spektrum serapan derivat pertama dari masing-masing larutan zat tunggal dan dari campuran zat. Spektrum serapan derivat pertama dari larutan zat tunggal dan
campuran keduanya ditumpangtindihkan. Demikian juga untuk spektrum serapan derivat kedua. Yang dipilih untuk menjadi panjang gelombang analisis adalah
campurannya hampir sama atau persis sama, karena pada panjang gelombang
tersebut dapat secara selektif mengukur serapan zat tersebut.
3.5.7 Pembuatan dan Penentuan Linieritas Kurva Kalibrasi
3.5.7.1 Pembuatan dan Penentuan Linearitas Kurva Kalibrasi Pseudoefedrin HCl
Dipipet Larutan Induk Baku II pseudoefedrin HCl (konsentrasi = 1000
mcg/ml) sebanyak 1,25 ml; 2,5 ml; 3,75 ml; 5 ml; dan 6,25 ml. Masing-masing
dimasukkan ke dalam labu tentukur 10 ml, diencerkan dengan HCl 0,1 N hingga
garis tanda. Lalu dikocok sampai homogen sehingga diperoleh larutan dengan
konsentrasi 100; 200; 300; 400; dan 500 mcg/ml. Kemudian diukur serapan pada
derivat kedua (∆λ = 10 nm) pada panjang gelombang 271 nm. Kemudian
dilakukan analisis hubungan antara konsentrasi dengan serapan, sehingga
diperoleh persamaan regresi linear y = ax + b, dan berdasarkan nilai serapan pada
panjang gelombang 271 nm, dilakukan pula perhitungan limit deteksi/ limit of
detection (LOD) dan limit kuantitasi/limit of quantitation (LOQ).
Untuk menentukan batas deteksi (LOD) dan batas kuntitasi (LOQ) dapat
digunakan rumus :
LOQ = Batas Kuantitasi
3.5.7.2 Pembuatan dan Penentuan Linearitas Kurva Kalibrasi Triprolidin HCl
Dipipet Larutan Induk Baku II triprolidin HCl (250 mcg/ml) sebanyak 0,5
ml; 1 ml; 1,5 ml; 2 ml; dan 2,5 ml. Masing-masing dimasukkan ke dalam labu
tentukur 25 ml, diencerkan dengan HCl 0,1 N hingga garis tanda. Lalu dikocok
sampai homogen sehingga diperoleh larutan dengan konsentrasi 5; 10; 15; 20; dan
25 mcg/ml. Kemudian diukur serapan pada derivat kedua (∆λ = 10 nm) pada
panjang gelombang 318 nm. Kemudian dilakukan analisis hubungan antara
konsentrasi dengan serapan, sehingga diperoleh persamaan regresi linear y = ax +
b, dan berdasarkan nilai serapan pada panjang gelombang 318 nm, dilakukan pula
perhitungan limit deteksi/ limit of detection (LOD) dan limit kuantitasi/limit of
quantitation (LOQ). Perhitungan menentukan batas deteksi (LOD) dan batas
kuntitasi (LOQ) seperti rumus di atas.
3.5.8 Penentuan Kadar Pseudoefedrin HCl dan Triprolidin HCl dalam
Sediaan Tablet
Dua puluh tablet merek dagang yang mengandung pseudoefedrin HCl 60
mg dan triprolidin HCl 2,5 mg ditimbang, lalu digerus dalam lumpang sampai
halus dan homogen. Kemudian ditimbang seksama sejumlah serbuk setara dengan
50 mg pseudoefedrin HCl . Kemudian dari berat analit yang ditimbang setara 50
mg pseudoefedrin HCl ini dihitung kesetaraan triprolidin HCl yang terkandung di
dalamnya (penimbangan serbuk sebanyak 6 kali pengulangan), dimasukkan ke
dalam labu tentukur 50 ml, ditambahkan HCl 0,1 N sampai garis tanda sambil
dikocok. Larutan kemudian dihomogenkan dengan pengaduk ultrasonik selama 20
menit. Larutan tersebut kemudian disaring, lebih kurang 10 ml filtrat pertama
ml dan dimasukkan ke dalam labu tentukur 10 ml dan diencerkan dengan HCl 0,1
N hingga garis tanda (konsentrasi = 300 mcg/ml untuk pseudoefedrin HCl dan
konsentrasi = 12,5 mcg/ml untuk triprolidin HCl) dan diukur serapannya pada
serapan/derivat kedua pada panjang gelombang 271 nm dan 318 nm.
3.5.9 Uji Validasi 3.5.9.1 Uji Akurasi
Uji akurasi dilakukan dengan metode penambahan baku (Standard
Addition Method), yaitu dengan membuat 3 konsentrasi analit sampel dengan
rentang spesifik 80 %, 100 %, 120 %, dimana masing-masing dilakukan sebanyak
3 kali replikasi. Setiap rentang spesifik mengandung 70 % analit dan 30 % baku
pembanding, kemudian dianalisa dengan perlakuan yang sama seperti pada
penetapan kadar sampel.
Persen perolehan kembali (% recovery) dapat dihitung dengan rumus
sebagai berikut :
% Recovery
Keterangan :
A = konsentrasi sampel yang diperoleh setelah penambahan baku
B = konsentrasi sampel sebelum penambahan bahan baku
C = konsentrasi baku yang ditambahkan
3.5.9.2 Uji Presisi
Uji presisi (keseksamaan) ditentukan dengan parameter RSD (Relative
Standard Deviasi) dengan rumus :
RSD =
Untuk menghitung Standar Deviasi (SD) digunakan rumus :
Keterangan :
RSD = Relative Standard Deviasi
SD = Standard Deviasi
X = Kadar Rata-rata pseudoefedrin HCl atau triprolidin HCl dalam
Sampel
3.5.10 Analisis Data Statistik
Analisis data secara statistik menggunakan uji t. Untuk mengetahui apakah data
diterima atau ditolak digunakan rumus seperti di bawah ini :
t hitung =
Untuk mencari kadar sebenarnya dengan taraf kepercayaan 99% dengan derajat
kebebasan dk= n-1, digunakan rumus :
µ = X± t(1-1/2α)dk x
n SD
Keterangan :
µ = interval kepercayaan
α = tingkat kepercayaaan
dk = derajat kebebasan
SD = standar deviasi
BAB IV
HASIL DAN PEMBAHASAN
4.1 Uji Identifikasi Menggunakan Spektrofotometer FTIR
Pseudoefedrin HCl dan triprolidin HCl BPFI sebelum digunakan sebagai
baku pembanding terlebih dahulu diidentifikasi menggunakan Spektrofotometer
FTIR pada rentang bilangan gelombang 4000 – 500 cm-1. Spektrum IR
pseudoefedrin HCl dapat dilihat pada gambar 5 di bawah ini.
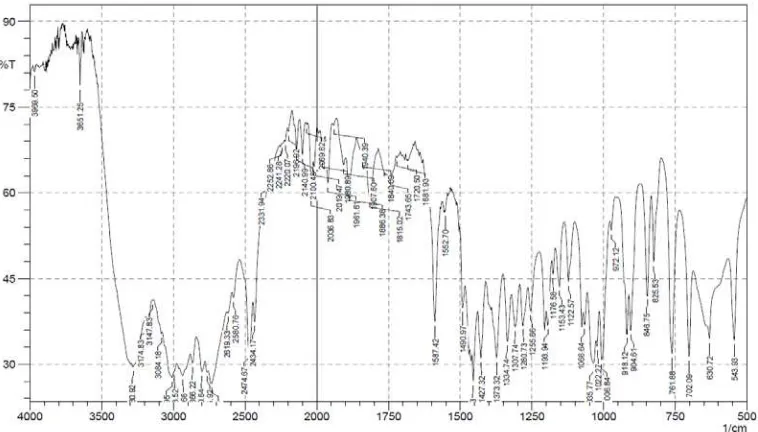
Gambar 5. Spektrum inframerah pseudoefedrin HCl BPFI
Dari hasil penelitian diperoleh bentuk spektrum pseudoefedrin HCl BPFI
hampir sama dengan bentuk spektrum yang terdapat pada literatur dan pada
sertifikat BPFI. Pada daerah sidik jari juga diperoleh bilangan gelombang yang
hampir sama dengan bilangan gelombang pada literatur dan pada data sertifikat
BPFI. Toleransi perbedaan bilangan gelombang yang diijinkan untuk bilangan
Tabel 1. Data bilangan gelombang (dalam cm-1) pada daerah sidik jari dari pseudoefedrin HCl
Data Clarke’s 704 764 1005 1036 1585
Data Penelitian 702,09 761,88 1006,84 1035,77 1587,42 Data BPFI 702,09 761,85 1001,06 1034,20 1585,49
Tabel 2. Data bilangan gelombang hasil identifikasi gugus fungsi dan ikatan dari
pseudoefedrin HCl
Gugus fungsi dan
ikatan Literatur Baku Parasetamol
C−H Aromatis 3020 – 3100 cm-1 3084,18 cm-1 Benzen 1500 dan 1600 cm-1 1552,7 dan 1587,42 cm-1
C=C 1650 cm-1 – 1670 cm-1 1681,93 cm-1
C=N 1030 cm-1 dan 1320 cm-1 1035,77 cm-1 dan 1334,74 cm-1 N-H 3310 cm-1 – 3500 cm-1 3280,92 cm-1
C−H Alifatis 2850 – 2960 cm-1 2866,22 cm-1, 2935,66 cm-1
O−H 3100 cm-1 3147,83 cm-1
C−O 1050 – 1150 cm-1 1066,64 cm-1, 1122,27 cm-1
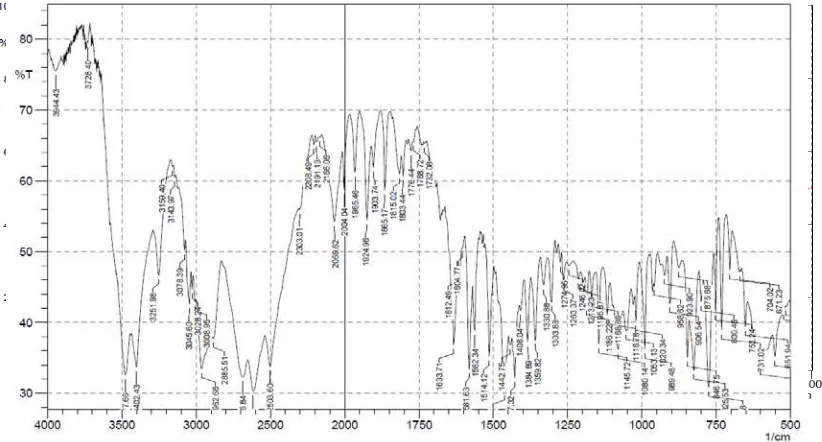
Spektrum IR dari triprolidin HCl BPFI dapat dilihat pada gambar 6 di bawah ini.
Dari hasil penelitian diperoleh bentuk spektrum triprolidin HCl BPFI
hampir sama dengan bentuk spektrum yang terdapat pada literatur dan pada
sertifikat BPFI. Pada daerah sidik jari juga diperoleh bilangan gelombang yang
hampir sama dengan bilangan gelombang pada literatur dan pada data sertifikat
BPFI. Toleransi perbedaan bilangan gelombang yang diijinkan untuk bilangan
gelombang pada daerah sidik jari adalah ± 4 cm-1 (Moffat, 2007).
Tabel 3. Data bilangan gelombang (dalam cm-1) pada daerah sidik jari dari triprolidin HCl
Data Clarke’s 775 825 990 1146 1580
Data Pengukuran 775,38 825,23 989,48 1145,72 1581,63 Data BPFI 775,38 825,33 989,40 1145,72 1581,63
Tabel 4. Data bilangan gelombang hasil identifikasi gugus fungsi dan ikatan dari
triprolidin HCl
Gugus fungsi dan
ikatan Literatur Baku Parasetamol
C−H Aromatis 3020 – 3100 cm-1 3045,60 cm-1, 3078,39 cm-1 Benzen 1500 dan 1600 cm-1 1514,12 dan 1604,77 cm-1
C=C 1650 cm-1 – 1670 cm-1 1633,71 cm-1
C=N 1030 cm-1 dan 1320 cm-1 1020,34 cm-1 dan 1330,88 cm-1 C−H Alifatis 2850 – 2960 cm-1 2885,51 cm-1
Jadi, baku yang diidentifikasi dan digunakan dalam penelitian adalah baku
pseudoefedrin HCl dan triprolidin HCl.
4.2 Pembuatan Kurva Serapan Maksimum
Pembuatan kurva serapan maksimum dilakukan pada panjang gelombang
200-400 nm. Pengukuran dilakukan pada konsentrasi 370 mcg/ml untuk
pseudoefedrin HCl dan pada konsentrasi 12,5 mcg/ml untuk triprolidin HCl.
257 nm untuk pseudoefedrin HCl ( gambar 5) dan pada λ = 290 nm untuk
triprolidin HCl ( gambar 6).
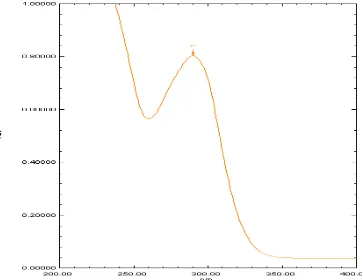
Gambar 7. Kurva serapan maksimum pseudoefedrin HCl 370 mcg/ml.
Gambar 8. Kurva serapan maksimum triprolidin HCl 12,5 mcg/ml.
Kurva serapan biasa dibuat dengan membuat larutan pseudoefedrin HCl
dengan konsentrasi 100; 200; 300; 400; dan 500 mcg/ml dan larutan triprolidin
HCl dengan konsentrasi 5; 10; 15; 20; dan 25 mcg/ml. Dibuat kurva serapan pada
panjang gelombang 200-400 nm. Kurva serapan dari masing-masing zat pada
berbagai konsentrasi tersebut ditumpangtindihkan atau dioverlappingkan. Kurva
serapan biasa untuk triprolidin HCl dapat dilihat pada gambar 9 – gambar 14, dan
kurva serapan biasa pseudoefedrin HCl dapat dilihat pada gambar 15 – gambar
20.
Gambar 9. Kurva serapan biasa triprolidin HCl 5 mcg/ml.
Gambar 11. Kurva serapan biasa triprolidin HCl 15 mcg/ml.
Gambar 13. Kurva serapan biasa triprolidin HCl 25 mcg/ml.
Gambar 15. Kurva serapan biasa pseudoefedrin HCl 100 mcg/ml.
Gambar 17. Kurva serapan biasa pseudoefedrin HCl 300 mcg/ml.
Gambar 19. Kurva serapan biasa pseudoefedrin HCl 500 mcg/ml.
4.4 Pembuatan Kurva Serapan Derivat Pertama
Kurva serapan derivat pertama dibuat dengan terlebih dahulu membuat
kurva serapan biasa dari larutan pseudoefedrin HCl dengan konsentrasi 100; 200;
300; 400; dan 500 mcg/ml dan larutan triprolidin HCl dengan konsentrasi 5; 10;
15; 20; dan 25 mcg/ml pada panjang gelombang 200-400 nm. Kurva serapan biasa
yang telah diperoleh ditransformasikan menjadi kurva serapan derivat pertama
dengan ∆λ = 10 nm. Kurva serapan derivat pertama dari masing-masing zat pada
berbagai konsentrasi tersebut ditumpangtindihkan atau dioverlappingkan. Kurva
serapan derivat pertama untuk triprolidin HCl dapat dilihat pada gambar 21 –
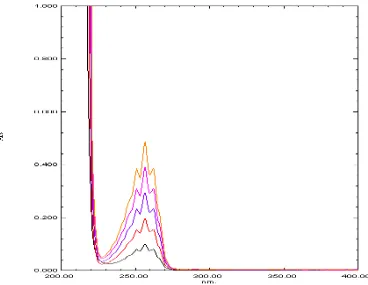
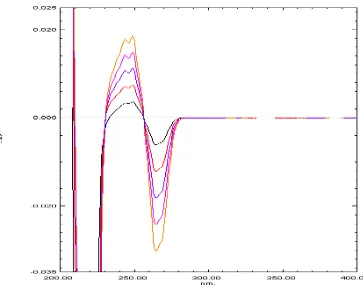
gambar 26, dan kurva serapan derivat pertama pseudoefedrin HCl dapat dilihat
pada gambar 27 – gambar 32.
Gambar 22. Kurva serapan derivat pertama triprolidin HCl 10 mcg/ml.
Gambar 24. Kurva serapan derivat pertama triprolidin HCl 20 mcg/ml.
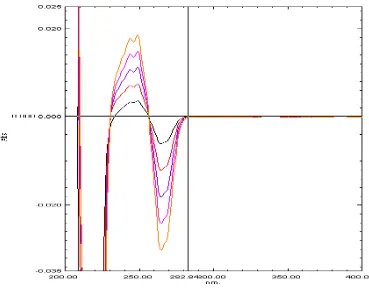
Gambar 26. Kurva overlapping serapan triprolidin HCl derivat pertama.
Gambar 28. Kurva serapan derivat pertama pseudoefedrin HCl 200 mcg/ml.
Gambar 30. Kurva serapan derivat pertama pseudoefedrin HCl 400 mcg/ml.