LAMPIRAN
Lampiran 1. Formula Media Spesifik Bakteri Azospirillum sp (Media Okon)
Nama Bahan Jumlah
Sumber : Danapriatna dan Simarmata (2011) Lampiran 2. Hasil Analisis Awal Tanah
Jenis Analisis Nilai Satuan Kriteria
pH (H2O) tanah 5.71 - Agak masam
C-Organik 1.62 % Rendah
N-Total 0.18 % Rendah
Rasio C/N 9.0 - Rendah
Melampirkan Hasil analisis Laboratorium Riset Teknologi FP USU ( N-total) Lampiran 3. Hasil Analisis C –organik dan N-total (%) sampel kompos
Jenis Analisis A1 A2 A3 A4
C-Organik (%) 3.61 6.53 48.63 36.13
N-Total (%) 0.24 0.29 0.91 0.49
Laboraorium Riset Teknologi FP USU (dilampirkan lembar hasil analisis)
Lampiran 5. Perhitungan Jumlah tanaman, dosis kompos dan perlakuan urea Jumlah Tanaman
1 Ha : 7400 m Juring
Lahan Percobaan : 36 Juring 5 meter Jarak antar Tanaman : 40 cm
Populasi Tanaman Per Juring : 500 cm 40 cm
: 12 bibit per juring Total bibit : 12 bibit x 36 = 432 bibit
Dosis Kompos
Dosis Penggunaan Kompos : 3 ton/ Ha Lahan Percobaan : 36 Juring 5 meter
Jadi, Dosis Kompos yang diaplikasikan : 3000
7400 m Juring
kg = 0,405 kg/ m juring Lebar juring 5 meter, jadi kompos diaplikasikan 0,405 kg x 5 = 2,025 kg/ juring Dalam 1 juring ada 12 bibit, sehingga : 2,025
12 bibit
kg = 150 gram per tanaman Dosis Urea
Dosis Penggunaan Urea : 200 kg/ Ha Lahan Percobaan : 36 Juring 5 meter
Jadi, Dosis Kompos yang diaplikasikan : 200
7400 m Juring
kg = 0,0270 kg/ m juring Lebar juring 5 meter, jadi kompos diaplikasikan 0,0270 kg x 5 = 0,135 kg/ juring Dalam 1 juring ada 12 bibit, sehingga : 0,135
12 bibit
kg = 10 gram per tanaman (U1)
Untuk Perlakuan selanjutnya adalah 75% dan 50 % dari anjuran 75% x 17 gram = 15 gram (U3)
Lampiran 7. Data Tinggi Tanaman 4 MST
Lampiran 8. Tabel Sidik Ragam Tinggi Tanaman 4 MST
Sumber Keragaman db JK KT F.hit F.05 F.01
Lampiran 9. Data Tinggi Tanaman 7 MST
Lampiran 10. Tabel Sidik Ragam Tinggi Tanaman 7 MST Interaksi 6 39,50457222 6,584095 0,790872tn 2,55 3,76
Error 22 183,152 8,325106
Lampiran 11. Data Tinggi Tanaman (cm) 10 MST
Lampiran 12. Tabel Sidik Ragam Tinggi Tanaman 10 MST
Lampiran 13. Data Diameter Batang (cm) 4 MST
Lampiran 14. Tabel Sidik Ragam Diameter Batang (cm) 4 MST
Sumber Keragaman db JK KT F.hit F.05 F.01
Blok 2 0,049718056 0,024859 4,718089* 3,44 5,72 Perlakuan 11 0,219307639 0,019937 3,78393** 2,26 3,18 Azos 2 0,058718056 0,029359 5,572161* 3,44 5,72 Urea 3 0,134457639 0,044819 8,506408** 3,05 4,82 Interaksi 6 0,026131944 0,004355 0,826613tn 2,55 3,76
Error 22 0,116 0,005269
Total 35 0,385
KK = 28.29 %
Keterangan : tn : tidak nyata
* : nyata pada taraf α 5 % ** : nyata pada taraf α 1 %
Lampiran 15. Data Diameter Batang (cm) 7 MST
7 A0U2 0,295 0,37 0,055 0,72 0,24
8 A1U2 0,205 0,325 0,315 0,85 0,28
9 A2U2 0,31 0,335 0,28 0,93 0,31
10 A0U3 0,195 0,22 0,135 0,55 0,18
11 A1U3 0,245 0,205 0,14 0,59 0,20
12 A2U3 0,495 0,285 0,28 1,06 0,35
Total 3,28 3,50 2,46 9,24 3,28
Rataan 0,26
No. Sampel Ulangan Total Rataan
I II III
1 A0U0 0,805 0,94 0,685 2,43 0,81
2 A1U0 0,94 1,02 0,77 2,73 0,91
3 A2U0 1,21 0,99 0,815 3,02 1,01
Lampiran 16. Tabel Sidik Ragam Diameter Batang 7 MST
Lampiran 17. Data Diameter Batang (cm) 10 MST
Lampiran 18. Tabel Sidik Ragam Diameter Batang (cm) 10 MST
Interaksi 6 0,092827778 0,015471 0,565844tn 2,55 3,76
Error 22 0,602 0,027342
Lampiran 19. Data Berat Jumlah Anakan 4 MST
Lampiran 20. Tabel Sidik Ragam(transformasi √(x + 0,5)) Jumlah Anakan 4 MST
Lampiran 21. Jumlah Anakan 7 MST
Lampiran 22. Tabel Sidik Ragam Jumlah Anakan 7 MST Interaksi 6 19,61111111 3,268519 1,700832 tn 2,55
3,76
Lampiran 23. Data Jumlah Anakan 10 MST
Lampiran 24. Tabel Sidik Ragam Jumlah Anakan 10 MST
Sumber Keragaman db JK KT F.hit F.05 F.01
Blok 2 22,05555556 11,02778 4,00275 3,44 5,72 Perlakuan 11 20,88888889 1,89899 0,689276tn 2,26
3,18 Azos 2 0,722222222 0,361111 0,131072 tn 3,44
5,72 Urea 3 9,555555556 3,185185 1,156126 tn 3,05
4,82 Interaksi 6 10,61111111 1,768519 0,641919 tn 2,55
3,76
Error 22 60,611 2,755051
Total 35 103,556
KK = 33.95%
Keterangan : tn : tidak nyata
* : nyata pada taraf α 5 % ** : nyata pada taraf α 1 %
5 A1U1 3 7 5 15,00 5,00
6 A2U1 6 8 3 17,00 5,67
7 A0U2 4 6 3 13,00 4,33
8 A1U2 7 7 5 19,00 6,33
9 A2U2 3 8 4 15,00 5,00
10 A0U3 2 4 5 11,00 3,67
11 A1U3 5 4 4 13,00 4,33
12 A2U3 2 3 7 12,00 4,00
Total 31,00 47,00 70,00 59,00 176,00
Lampiran 25. Data Berat Kering Tajuk (g)
Lampiran 26. Tabel Sidik Ragam (transformasi √(x + 0,5)) Berat Kering Tajuk (g)
Lampiran 27. Data Berat Kering Akar (g)
Lampiran 28. Tabel Sidik Ragam Berat Kering Akar(g)
Sumber Keragaman db JK KT F.hit F.05 F.01
Blok 2 575,7105556 287,8553 6,155719 3,44 5,72 Perlakuan 11 3050,852222 277,3502 5,931071 2,26 3,18 Azos 2 2206,670556 1103,335 23,59457** 3,44 5,72
Urea 3 232,89 77,63 1,6601tn 3,05 4,82
Interaksi 6 611,2916667 101,8819 2,178722tn 2,55 3,76
Lampiran 29. Data pH Tanah
Lampiran 30. Tabel Sidik Ragam pH Tanah
Lampiran 31. Data C-Organik Tanah (%)
Lampiran 32. Tabel Sidik Ragam C-Organik Tanah (%)
Sumber Keragaman db JK KT F.hit F.05 F.01
Blok 2 0,066293735 0,033147 0,875176 3,44 5,72 Perlakuan 11 0,814733607 0,074067 1,955581 2,26 3,18 Azos 2 0,586336463 0,293168 7,740512** 3,44 5,72 Urea 3 0,105414066 0,035138 0,927748tn 3,05 4,82 Interaksi 6 0,122983078 0,020497 0,541186tn 2,55 3,76
Lampiran 33. Data N-Total Tanah (%)
Lampiran 34. Tabel Sidik Ragam N-Total Tanah (%)
Sumber Keragaman db JK KT F.hit F.05 F.01
Blok 2 0,00665 0,003325 1,191045 3,44 5,72
Perlakuan 11 0,024608333 0,002237 0,801357tn 2,26 3,18 Azos 2 0,004816667 0,002408 0,862687tn 3,44 5,72 Urea 3 0,017763889 0,005921 2,121061tn 3,05 4,82 Interaksi 6 0,002027778 0,000338 0,121061tn 2,55 3,76
Lampiran 35. Data Rasio C/N Tanah
Lampiran 36. Tabel Sidik Ragam Rasio C/N tanah
Sumber Keragaman db JK KT F.hit F.05 F.01
Blok 2 6,247634292 3,123817 0,441455 3,44 5,72 Perlakuan 11 92,25770635 8,387064 1,185252tn 2,26 3,18 Azos 2 62,50363079 31,25182 4,416477* 3,44 5,72 Urea 3 24,64698752 8,215663 1,16103tn 3,05 4,82 Interaksi 6 5,107088042 0,851181 0,120288tn 2,55 3,76
Lampiran 37. Data N-Tanaman (%)
Lampiran 38. Tabel Sidik Ragam N-Tanaman (%)
Sumber Keragaman db JK KT F.hit F.05 F.01
Blok 2 1,87625 0,938125 4,872897 3,44 5,72
Perlakuan 11 2,575608333 0,234146 1,216224tn 2,26 3,18 Azos 2 0,755466667 0,377733 1,962058tn 3,44 5,72 Urea 3 0,294986111 0,098329 0,510748tn 3,05 4,82 Interaksi 6 1,525155556 0,254193 1,320351tn 2,55 3,76
Lampiran 39. Data Serapan N (mg/ Tanaman)
Lampiran 40. Tabel Sidik Ragam N-Tanaman (%)
Lampiran 40. Foto Penelitian
A. Penelitian Tahap I ( Isolasi, Inokulasi, Perlakuan kompos, Analisis Kompos)
Kultur murni Agar Miring Azospirillum sp Media okon Cair
Azospirillum pada Media okon Agar Inokulasi Azospirillum pada media okon cair
Inkubasi Kompos yang diaplikasi Analisis kimia kompos
B. Penelitian Tahap II ( Pra Tanam, saat tanam, saat panen)
Persiapan bahan (kompos, urea, dll) Aplikasi Azospirillum cair pada kompos
Pengambilan Data Panen Tanaman dan Tanah
Menghitung BKT dan BKA Kering udara tanah
Dokumentasi Sebelum Panen
A0U0 ( blok II) A0U1 (blok II)
A0U2 (Blok II) A0U3 (Blok II)
A1U2 (Blok II) A1U3 (Blok II)
A2U0 (Blok II) A2U1 (Blok II)
DAFTAR PUSTAKA
Azizah., 2011. Pengaruh tiga Inokulan Bakteri Rhizobium terhadap pembentukan bintil akar tanaman kedelai (Glycine max L.Meriil). Skripsi Universitas Andalas, Padang.
Balai Penelitian Tanaman Pemanis dan Serat, 2013. Pembibitan Tebu. Balai Pesnelitian Tanaman Pemanis dan Serat. Diakses pada 01 Maret 2014 pada http://balittas.litbang.deptan.go.id
Barat, R., 2006. Kecepatan Pengomposan dan Kualitas Kompos Ampas tebu oleh beberapa Aktivator. Skripsi Ilmu Tanah Universitas Sumatera Utara, Medan. Bashan, Y., and G. Holguin. 1997. Azospirilum – plant relationships:
environmental and physiological advances (1990-1996). Can. J. Microbiol. 43: 103- 121.
Damanik, M. M. B., Hasibuan, B.E, Fauzi, Sarifuddin, dan Hanum, H. 2011. Kesuburan Tanah dan Pemupukan. USU Press. Medan.
Danapriatna dan Simarmata., 2011. Viabilitas Pupuk Hayati Penambat Nitrogen (Azotobacter dan Azozpirilum) ekosistem padi sawah pada berbagai formulasi bahan pembawa. Hurnal Agribisnis dan Pengembangan Wilayah 3(1), Sumedang.
Duan Y.H, Zhang Y.L, Ye L.Y, Fan X.R, Xu G.H, Shen Q.R. 2007. Responses of rice cultivars with different nitrogen use efficiency to partial nitrate nutrition. Ann Bot 99: 1153–1160
Dubrovsky, J.G., Esther Pljente, M and Bashan, Y. 1994. Arabidopsis Thaliana As A Model System For The Study Of The Effect Of Inoculation By Azospirillum Brasilense Sp-245 On Root Hair Growth. Soil Bid. Biochem 26(12), pp. 1657-1664.
Eckert, B., Weber, O.B, Kirchhof, G, Halbritter, A, Stoffels, M and Hartmann, A. 2001. Azospirillum doebereinerae sp. nov., a nitrogen-fixing bacterium associated with the C4-grass Miscanthus. International Journal of Systematic and Evolutionary Microbiology 51, 17–26. Great Britain.
Ferreira., Pires, R.R, Rabelo, P.G, Oliveira, R.C, Luz, J.M.Q and Brito, C.H. 2013. Implications of Azospirillum brasilense inoculation and nutrient addition on maize in soils of the Brazilian Cerrado under greenhouse and field conditions. Applied Soil Ecology 72 (2013) 103– 108.
composting without forced aeration––effect of compost pile scale. Bioresource Technology 89 : 109–114.
Gadagi, R.S., Krishnaraj, P.U, Kulkarni, J.H and Tongmin. 2003. The effect of combined Azospirillum inoculationand nitrogen fertilizer on plant growth promotionand yield response of the blanket flower Gaillardia pulchella. Scientia Horticulturae 100(2004):323-332.
Hanafiah, A. S., Sabrina, T dan Guchi, H. 2009. Biologi dan Ekologi Tanah. Buku Pedoman Perkuliahan. Program Studi Agroekoteknologi Fakultas Pertanian USU.
Holguin, G And Bashan, Y. 1996. Nitrogen-Fixation By Azospirillum Brasilense Cd Is Promoted When Co-Cultured With AMangrove Rhizosphere Bacterium (Staphylococcus Sp.). Soil Biol. Biochem 28(12) , pp. 1651-1660.
Hungria, M., Rubens, Campo, J ,Souza , E.M, Fabio and Pedrosa., 2010. Inoculation with selected strains of Azospirillum brasilense and A. lipoferum improves yields of maize and wheat in Brazil. Plant Soil 331:413–425.
Karti, 2005. Penggunaan Azospirillum pada tanah masam dengan Aluminium tinggi terhadap serapan Produksi dan serapan nitrogen rumput Setaria splendida ilan Chloris gayana. Media Peternakan 28(1) : 37-45. Departemen llrnu Nutrisi dan Makanan Ternak Fakutas Petemakan, Institut Pertanian Bogor.
Kim, K., Boruah, H.P.D,Woo Kim, C, Shagol, C.C and Tong-Min Sa., 2010. Isolation and evaluation of inoculation effect of Azospirillum sp. on growth,colonization and nutrient uptake of crops under green house condition. World Congress of Soil Science, Soil Solutions for a Changing World, Brisbane Australia
Larasati, T., Mulyana, N dan Sudrajat, D. 2012. Pembuatan Bahan Pembawa Berbasis Vermikompos UntukInokulan Bakteri Rhizosfer Peningkat PertumbuhanTanaman. Prosiding Pertemuan dan Presentasi Ilmiah - Penelitian Dasar Ilmu Pengetahuan dan Teknologi Nuklir 2012. Pusat Teknologi Akselerator dan Proses Bahan – BATANYogyakarta, 4 Juli 2012. Leovici, H., 2012. Pemanfaatan Blotong Pada Budidaya Tebu (Saccharum Officinarum L.) Di Lahan Kering. Skripsi Budidaya Pertanian Universitas Gajah Mada, Yogyakarta.
Metasari, K., 2011. . Eksplorasi Bakteri Penambat nitrogen non simbiosis dari tanah kawasan mangrove wonorejo Surabaya. Jurnal Biologi Universitas Airlangga, Surabaya.
Musarofah, 2002. Pengelolaan Tanaman tebu (Saccharum officinarum L.) lahan kering di PT gula Putih Mataram, Lampung ; Studi Kasus Kehilangan Fisik Tebu saat tebang angkut. Skripsi Budidaya Pertanian IPB, Bogor.
Nurhayati., 2006. Isolasi dan Seleksi Bakteri Penambat Nitrogen non simbiotik dari lahan kering masam. Skripsi Biologi Universitas Islam Negri Malang. Nurmayulis dan Maryati., 2008. Kandungan Nitrogen dan bobot biji kentang yang
diberi pupuk organik di fermentasi, Azospirillum sp, dan pupuk nitrogen di Cisarua, Lembang. J.Tanah Trop 13(3): 217-224.
Nursoid, Odjijono dan Lestari., 2008. Kemampuan Azozpirilum sp JG3 dalam Menghasilkan Lipase pada medium campuran dedak dan onggok dengan waktu inkubasi berbeda. Jurnal Biologi Universitas Soedirman, Purwokerto. Parto, Y., Syawal, Y dan Achadi, T. 2011. Pengaruh pemberian Urea dan
Aplikasi Herbisida Pra Tumbuh terhadap pertumbuhan bibit karet dan Gulma di pembibitan.Agrovigor 5(2). Fakultas Pertanian, Univ. Sriwijaya. Sumatera Selatan.
Pawirosemadi, M., 1996. Dasar- Dasar Teknologi Budidaya Tebu dan Pengolahan Hasilnya. Universitas Negri Malang Press, Malang.
Pitriana, A., 1999. Pengaruh Azotobacter, Azozpirilum dan Mikroba Pelarut Posfat Terhadap Pertumbuhan Padi IR 64pada dua tingkat pemupukan urea dan SP36. Skripsi Ilmu Tanah IPB, Bogor
Purushothaman, D., Gunasekaran, S and Oblisami, G. 1980. Nitrogen Fixation by Azospirillum in Some Tropical Plants. Proc.Indian Natn. Sci.Acad 46(5), pp. 713-717.
Purwanti, E., 2008. Pengaruh dosis Pupuk Majemuk dan Konsentrasi EM4 terhadap pembentukan bibit stek Tebu (Saccharum officinarum L.). Skripsi Agronomi Universitas Sebelas Maret, Surakarta.
Purwanto, B.H, Utami, Maas, A, Widayati, W.E dan Widowati., 2010. Peningkatan Efisiensi Searapan N Tebu Pada tanah Sawah melalui aplikasi pupuk Urea Humat. Kemajuan Teknik Riset. Universitas Gajah Mada. Lembaga Penelitian dan Pengabdian masyarakat, Yogyakarta.
Rusmana, I dan Hadijaya, D. 1994. Aktivitas Nitrogenasi Azozpirilu sp dan efektivitas Simbiotiknya dengan Jagun. J.Hayati 1(2): 51-54.
Sabrina, T., Hanafi, M.M, Mahmud, T.M.M and Nur Azwady, A.A. 2011. Vermicomposting of Oil Palm Fruit Bunch and Its Potential supplying of Nutrients for Crop Growth.Compost Scince dan Utilization. 19(1) : 61-68. Saraswati, R., 2012. Teknologi pupuk hayati untuk efisiensi pemupukan dan
keberlanjutan sistem produksi pertanian. Penelitian Badan Litbang Pertanian, Bogor.
Setyorini. D, Saraswati, R dan Kosman, E.A. 2006. Pupuk Organik dan Pupuk Hayati. Bab 2. Kompos. Balai Besar Penelitian dan Pengembangan Sumberdaya Lahan Pertanian. Bogor : Jawa Barat.
Stevenson, F.J. 1982. Origin and Distribution of N in Soil. In F.J. Stevenson (ed.) Nitrogen in Argicultural Soils. American Society of Agronomy, Madison, WI.
Sutanto, R. 2002. Pertanian Organik : Menuju Pertanian Alternatif dan Berkelanjutan. Kanisius. Yogyakarta
Widiawati dan Muharam., 2012. Uji Laboratorium Azospirillum sp yang diisolasi dari beberapa ekosistem. J.Horti 22(3): 258-267.
Widawati, Sudiana, Sukara, dan Muharam., 2012. Teknologi Budidaya Tanaman Tomat Melalui Inverted Gardening dan Conventional Gardening Berbasis Pemanfaatan Bakteri Indigenus. J. Hort. 22(3):224-232.
Yulianti, T., 2012. Menggali Potensi endofit Untuk Meningkatkan Kesehatan tanaman Tebu Mendukung Peningkatan Produktifitas gula. Perspektif 11 (2) : 111 – 122,Desember 2012. Balai Penelitian Tanaman Pemanis dan Serat, Malang.
BAHAN DAN METODE PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di lahan pertanaman tebu Kebun Tanjung Jati PTPN II dan Laboratorium Biologi Tanah Fakultas Pertanian USU dengan ketinggian tempat ±25 meter di atas permukaan laut. Penelitian ini dilaksanakan pada Maret hingga Juli 2014.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah isolat bakteri Azospirillum sp. yang diperoleh dari laboratorium Bioteknologi Tanah UNPAD
sebagai bahan yang akan diisolasi., media okon sebagai media untuk menanam dan perbanyakan bakteri, bibit tanaman tebu varietas BZ134 sebagai tanaman yang akan menjadi indikator, pupuk urea sebagai bahan yang diaplikasikan dalam perlakuan, kompos limbah perkebunan tebu sebagai carrier inokulan serta bahan lainnya yang mendukung percobaan.
Metode Penelitian
Penelitian ini dilakukan dalam dua tahap. Tahap I bertujuan untuk mendapatkan carrier kompos dengan rasio C/N yang terbaik dalam menumbuhkan Azospirillum sp. Azospirillum sp. sementara tahap II bertujuan untuk mengetahui
pengaruh Azospirillum sp., urea maupun interaksi terhadap peningkatan serapan N tanaman dan pertumbuhan tebu.
Penelitian Tahap I
Pada penelitian tahap I ini dilaksanakan dengan menguji populasi bakteri Azospirillum pada carrier kompos skala laboratorium dengan 3 taraf kompos ;
A1 : Kompos umur 5 bulan sebanyak 250 g + Azospirillum 15mL A2 : Kompos umur 2 bulan sebanyak 250 g + Azospirillum 15mL A3 : Kompos umur 1 hari sebanyak 250 g + Azospirillum15mL A4 : Kompos umur 3 Minggu sebanyak 250 g + Azospirillum15mL
Dari hasil penelitian tahap I akan didapat kompos dengan rasio C/N berbeda dan hasil terbaik yang ditandai dengan peningkatan populasi bakteri Azospirillum sp. meningkat lebih besar akan digunakan pada penelitian tahap II
Penelitian Tahap II
Penelitian ini menggunakan metode RAK (Rancangan Acak kelompok) dengan dua faktor yaitu :
Faktor 1 : kompos dan Azospirillum
A0 : Tanpa aplikasi kompos dan Azospirillum (perlakuan kontrol)
A1 : Kompos dengan rasio terbaik 150 g/tanaman ( Tanpa bakteri Azospirillum) A2 : Kompos dengan rasio terbaik 150 g/tanaman+ Azospirillum 10 mL
U0: Tanpa aplikasi Urea (perlakuan kontrol) U1: Pupuk Urea 5 g/tanaman
U2: Pupuk Urea 10 g/tanaman U3: Pupuk Urea 15 g/tanaman
Sehingga diperoleh 12 kombinasi perlakuan : A0U0 A1U0 A2U0
A0U1 A1U1 A2U1 A0U2 A1U2 A2U2 A0U3 A1U3 A2U3
Jumlah Ulangan : 3 Ulangan Jumlah Juringan : 36 Juring Panjang Juringan : 5 meter Jarak Antar Juring : 1, 35 meter Jarak Antar Blok : 1,5 meter Jarak Antar Tanaman : 40 centimeter Jumlah Tanaman /Juring : 12 tanaman Jumlah Populasi seluruhnya : 432 tanaman
Luas Lahan : 22 m x 20 m
Model linier Rancangan Acak Kelompok: Yhij = μ +ρh + αi + βj + + βɣij + Σhij
Dimana:
Yhij = Hasil perlakuan ke - hij μ = nilai rataan umum
αi = pengaruh perlakuan kompos berbeda rasio C/N ke-i βj = pengaruh perlakuan dosis urea ke –j
βɣij = pengaruh interaksi antara kompos dan urea ke-ij
Σhij= pengaruh galat percobaan ulangan ke-hperlakuan kompos ke-i dengan dosis
urea ke-j
Jika dari hasil sidik ragam menunjukkan efek pemberian Azospirillum sp pada kompos berbeda rasio C/N dan urea menunjukkan hasil yang nyata, maka dilanjutkan dengan uji beda rataan berdasarkan Uji Jarak Berganda Duncan (DMRT) pada taraf 5%.
Pelaksanaan Penelitian Penelitian Tahap I
Persiapan Bakteri Azospirillum sp
Bakteri dalam bentuk kultur murni diperoleh dari Laboratorium Bioteknologi Tanah Universitas Padjajaran Bandung yang di perbanyak serta di remajakan kembali di laboratorium Biologi Tanah Universitas Sumatera Utara. Adapun jenis bakteri Azospirillum sp yang diperoleh adalah Azospirillum sp. yang merupakan isolat dari rhizosfer pada tanaman jagung.
Persiapan Kompos
Analisis kompos
Kompos yang akan menjadi carrier aplikasi bakteri Azospirillum akan analisis terlebih dahulu dengan beberapa parameter diantarnya C-organik (%) dengan Metode Walkey and Black, N-total ( % ) dengan Metode Kjedahl, Rasio C/N ( Rasio C-Organik dan N-total ), pH (H2
Sterilisasi Kompos
O) dengan Metode Elektrometri perbandingan 1 : 2,5.
Masing-masing kompos selanjutnya dilakukan sterilisasi dengan metode sterilisasi basah menggunakan autoklaf sehingga kompos steril dari organisme lain dan siap untuk diaplikasi bakteri Azospirillum sp.
Inokulasi Azospirillum
Isolat yang telah diperbanyak kemudian diinokulasi pada media okon cair yang telah dibuat sebelumnya, dengan cara menggoreskan isolat yang ada pada media okon cair kemudian di shaker selama 3 hari.
Menghitung Populasi Awal Azospirillum
Setelah diinokulasi yang dibiarkan selama 3 hari, selanjutnya populasi bakteri Azospirillum dihitung dengan metode MPN (Most Probable Number) menggunakan teknik pengenceran.
Aplikasi Azospirillum pada Kompos
Pengamatan Parameter
Setelah diinkubasi selanjutnya diamati parameter yakni populasi bakteri dengan metode MPN (Most Probable Number), pH kompos metode elektrometri 1 : 2,5. Dari hasil perhitungan populasi kompos yang memiliki peningkatan populasi tertinggi akan digunakan pada penelitian tahap II
Penelitian Tahap II Persiapan Tanaman
Bibit tebu yang digunakan merupakan bibit varietas BZ134 dari pembibitan bud chip yang sehat dan telah diseleksi pada semaian yang berumur 2 bulan dengan kriteria sudah memiliki daun lebih dari empat ,bebas penyakit, dan sehat dengan tinggi ±20-30 cm.
Persiapan Lahan
Persiapan lahan dilakukan dengan membuka lahan seluas 22 x 20 m dan membuat juringan dengan lebar 20 meter sebanyak 12 juringan,dimana setiap lebar 5 meter merupakan 1 blok dan jarak antar blok 1,5 meter sehingga setiap bloknya terdiri dari 12 juringan dengan jarak antar juringan 1,35 meter dan kedalaman juringan ±30 cm, membuat parit disekeliling juringan dengan kedalaman ±20 cm dan lebar 30cm serta membuat lubang tanam secara tugal dengan menggunakan tongkat tugal dengan jarak setiap 40 cm dalam juringan. Persiapan Kompos Aplikasi
sebanyak 150 g kemudian diaplikasikan kembali Azospirillum sp. sebanyak 10mL/150g dan dibiarkan selama seminggu
Analisis Awal
Analisa awal dilakukan pada saat sebelum penanaman berupa analisis C-organik (%) dengan Metode Walkey and Black, N-total ( % ) dengan Metode Kjedahl, Rasio C/N ( Rasio C-Organik dan N-total ), pH (H2
Aplikasi Pupuk Dasar
O) dengan Metode Elektrometri perbandingan 1 : 2,5
Pada lubang tanam yang telah dibuat diaplikasikan pupuk dasar yakni Urea dan TSP dengan dosis 100kg/ha dan 150 kg/ha setara dengan 6 g/tanaman dan 9 g/tanaman, dimana pada kombinasi perlakuan yang tidak menggunakan urea tidak diaplikasikan pupuk dasar urea.
Penanaman
Penanaman bibit pada juringan dilakukan dengan memindahkan bibit yang dipilih dari semaian pada lubang tanam yang telah dibuat sebelumnya dengan hati-hati, dimana terlebih dahulu pupuk dasar telah diaplikasikan .
Aplikasi Perlakuan
Pemeliharaan Tanaman
Dilakukan pemeliharaan tanaman dengan menyiangi gulma sekitar area secara manual, kemudian dilakukan penyulaman dengan mengganti tanaman yang mati atau pertumbuhannya abnormal dengan tanaman cadangan serta melakukan penyiraman terhadap tanama pada pagi dan sore hari.
Pemanenan
Pemanenan dilakukan dengan mengambil seluruh bagian tanaman pada sampel tanaman yang telah ditetapkan sebanyak 36 sampel secara acak pada setiap kombinasi perlakuan pada saat 10 MST (Minggu Setelah Tanam).
Pengamatan Parameter
Adapun parameter yang diamati adalah diameter batang, tinggi tanaman, jumlah anakan . Pengambilan data parameter dalam satu kombinasi perlakuan disetiap juringan dipilih 5 dari 12 tanaman secara random sejak awal penanaman yang akan diambil data pada 1 MST sebagai tinggi awal, 4 MST, 7 MST dan 10 MST saat sebelum panen, kemudian dirata-ratakan menjadi perwakilan dalam setiap satu kombinasi perlakuan sehingga diperoleh 36 data untuk 36 kombinasi perlakuan
Tinggi tanaman (cm)
Pengukuran tinggi tanaman dilakukan dari pangkal batang sampai titik tumbuh dengan menggunakan meteran, dilakukaan saat 1 MST (Minggu Setelah Tanam) sebagai data tinggi awal dan 10 MST saat sebelum panen.
Jumlah Anakan
Perhitungan jumlah anakan dilakukan dengan menghitung seluruh jumlah tunas yang tumbuh termasuk tanaman induk, dilakukaan mulai saat 1 MST (Minggu Setelah Tanam) sebagai data jumlah anakan awal dan 10 MST saat sebelum panen sebagai data akhir.
Diameter Batang ( cm)
Diameter batang diukur dengan menggunakan jangka sorong yang diambil setiap minggunya , dilakukaan saat 1 MST (Minggu Setelah Tanam) sebagai data diameter batang awal dan 10 MST sebagai data akhir.
Bobot Kering Tajuk (g)
Pengukuran bobot kering tajuk dilakukan dengan memotong tajuk tanaman dari setiap sampel bibit pada saat 10 MST dan di ovenkan pada suhu 60-700
Bobot Kering Akar (g)
C selama 24 jam selanjutnya ditimbang.
C-Organik Tanah
Pada umur 10 MST , tanah dari setiap sampel tanaman diambil untuk dilakukan analisa kembali berupa analisis C-organik (%) dengan Metode Walkey and Black
N-total ( % )
Pada umur 10 MST , tanah dari setiap sampel tanaman diambil untuk dilakukan analisis berupa analisis N-total yang dilakukan dengan Metode Kjedahl. Rasio C/N
Rasio C/N dapat dihitung dengan perbandingan C-organik dan N-total yang didapat pada setiap sampel tanah
pH H2
pH dapat dihitung dengan Metode Elektrometri perbandingan 1 : 2,5 yakni setiap 10 g sampel tanah pada larutan aquades 25mL.
O
N Tanaman
N tanaman dapat dianalisis dengan mengambil sampel seluruh bagian tanaman pada tanaman tebu berumur 10 MST. Kemudian dianaliss dengan metode destruksi basah.
Serapan N
HASIL DAN PEMBAHASAN
Hasil
Penelitian Tahap 1
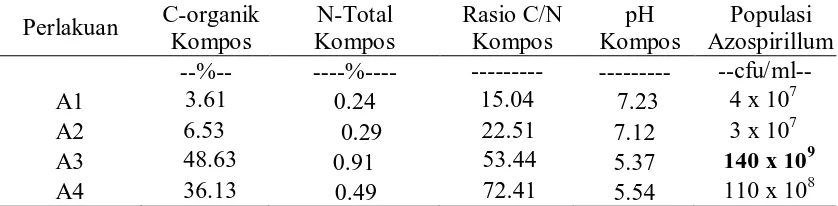
Dari hasil penelitian tahap I di laboratorium dengan tujuan untuk menguji jenis rasio kompos yang terbaik terhadap pertumbuhan bakteri Azospirillum, dimana terdiri dari empat taraf yakni : A1: Kompos umur 5 bulan (5 bulan dibiarkan setelah penggilingan dari bahan mentah saat akan digunakan kompos), A2: kompos umur 2 bulan (2 bulan dibiarkan setelah penggilingan dari bahan mentah saat akan digunakan kompos), kompos A3: kompos umur 1 hari ( 1 hari dibiarkan setelah penggilingan dari bahan mentah saat akan digunakan kompos) dan A4: Kompos umur 3 minggu (3 minggu dibiarkan setelah penggilingan dari bahan mentah saat akan digunakan kompos). Maka telah diperoleh hasil terhadap C-organik kompos, N total kompos, pH kompos dan populasi Azospirillum sp. awal dan setelah aplikasi kompos (Tabel 1)
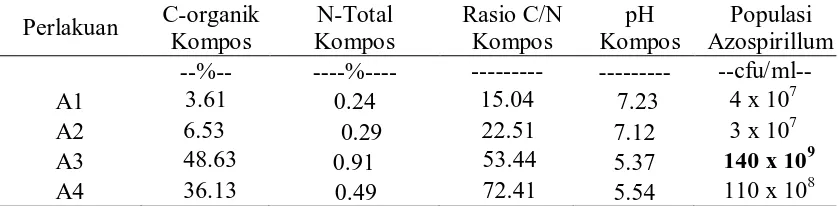
Tabel 1. Sifat kimia dan populasi Azospirillum sp. pada kompos berbeda tingkat kematangan Keterangan : Populasi Azospirillum sp. yang diaplikasikan yaitu 2 x 108
cfu/ml diikuti 110 x 108 cfu/ml, 4 x 107 cfu/ml dan 3 x 107
Penelitian Tahap II
cfu/ml berturut-turut untuk kompos A4, A1 dan A2 (Tabel 1). Kompos A3 memiliki ciri dengan nilai C organik tertinggi yaitu 48.63% diikuti kompos A4 (36.13%), kompos A2 (6.53%) dan A1 (3.61%) dimana pada kompos A3 dan A4 yang memiliki populasi Azospirillum sp terbanyak bersifat masam (pH 5.37 dan 5.54). Sehingga kompos
matang A3 merupakan yang terbaik untuk dilanjutkan pada penelitian tahap II.
Sifat Kimia Tanah
Dari hasil analisis sidik ragam menunjukkan bahwa pemberian Azospirillum pada carrier kompos, berpengaruh sangat nyata terhadap C-organik
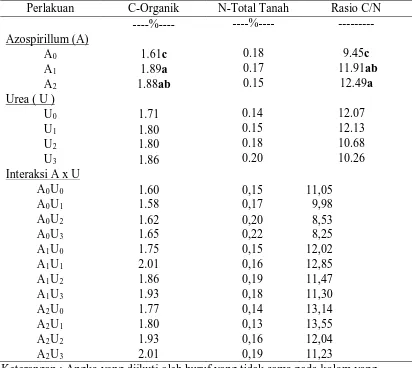
Tabel 2. Sifat kimia tanah C-organik, N-total dan rasio C/N tanah akibat pemberian Azospirillum, urea dan interaksinya
Perlakuan C-Organik N-Total Tanah Rasio C/N ----%---- ----%---- ---
Keterangan : Angka yang diikuti oleh huruf yang tidak sama pada kolom yang sama dan perlakuan yang sama menunjukkan perbedaan nyata pada taraf 5% menurut uji DMRT
Dari Tabel 2 dapat dilihat bahwa pemberian Azospirillum pada carrier kompos meningkatkan C-organik tanah sangat nyata pada A2 (1.88%) daripada tanpa Azospirillum dan kompos A0(1.61%) begitu juga pada pemberian kompos tanpa Azospirillum( A1) yakni 1.89% yang meningkat sangat nyata daripada tanpa Azospirillum dan kompos (A0). Pemberian urea sebanyak 5 g/tanaman (U1), 10
antara Azospirillum dan urea juga meningkatkan C-organik tanah secara tidak nyata daripada perlakuan kontrol (A0U0).
Dari Tabel 2 terlihat juga bahwa kedua faktor serta interaksi tidak berpengaruh nyata pada N-total tanah, namun pemberian Azospirillum carrier kompos berpengaruh nyata dalam meningkatkan pada rasio C/N, rasio C/N A0, A1, A2 berturut-turut (9.45, 11.91, 12.49) . Sedangkan pada pemberian urea tidak berpengaruh nyata, namun C/N cenderung menurun pada U0, U1, U2 dan U3.
Tabel 3. Sifat kimia tanah pH, N-total tanaman dan serapan N tanah akibat pemberian Azospirillum, urea dan interaksinya
Perlakuan pH Tanah N-Tanaman Serapan N
---- ----%---- ----mg/tanaman----
Keterangan : Angka yang diikuti oleh huruf yang tidak sama pada kolom yang sama dan perlakuan yang sama menunjukkan perbedaan nyata pada taraf 5% menurut uji DMRT
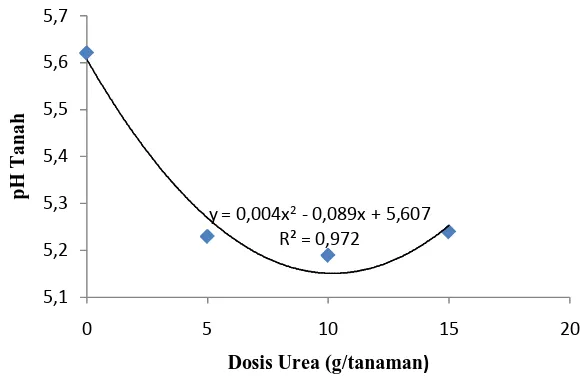
Hubungan antara dosis urea dengan pH tanah ditampilkan dalam bentuk kurva pada Gambar 1. Dengan sidik ragam pada lampiran 29.
Dari Tabel 3 dapat dilihat bahwa pemberian urea dengan berbeda dosis pada perlakuan U1, U2 dan U3 (5, 10 dan 15 g/tanaman) berpengaruh nyata menurunkan pH tanah berturut-turut (5.23, 5.19 dan 5.24) dari pada tanpa pemberian urea (5.62). Sementara aplikasi Azospirillum maupun interaksi antara Azospirillum sp. dan urea tidak memberikan pengaruh yang nyata dalam
perubahan pH tanah.
Dari Tabel 3 dapat dilihat bahwa pada N-tanaman, pemberian Azospirillum carrier kompos, urea serta interaksinya tidak berpengaruh nyata. Sedangkan pada serapan N pemberian Azospirillum sp. carrier kompos berpengaruh nyata dalam meningkatkan serapan N dengan tertinggi pada pada faktor Azospirillum sp. adalah perlakuan A2 (3.81 mg/tanaman), diikuti A1 (2.44 mg/tanaman) sedangkan A0 (1.23 mg/tanaman) dan pada pemberian urea serta interaksinya tidak berpengaruh nyata.
Pertumbuhan dan Produksi Tanaman
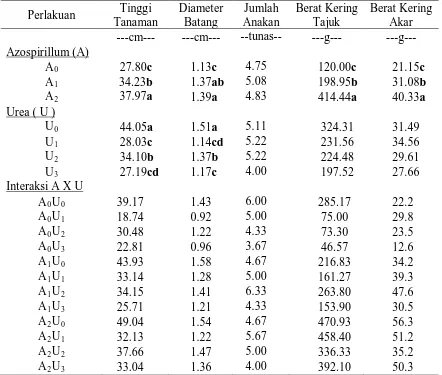
Tabel 4. Pertumbuhan dan produksi tanaman akibat pemberian Azospirillum carrier kompos dan urea serta interaksinya
Perlakuan Tinggi
Hubungan dosis urea dengan tinggi tanaman dan diameter batang ditampilkan dalam bentuk kurva pada Gambar 2 dan 3 dengan sidik ragam pada lampiran 11 dan 17.
Gambar2. Hubungan peningkatan dosis urea terhadap tinggi tanaman 10 MST
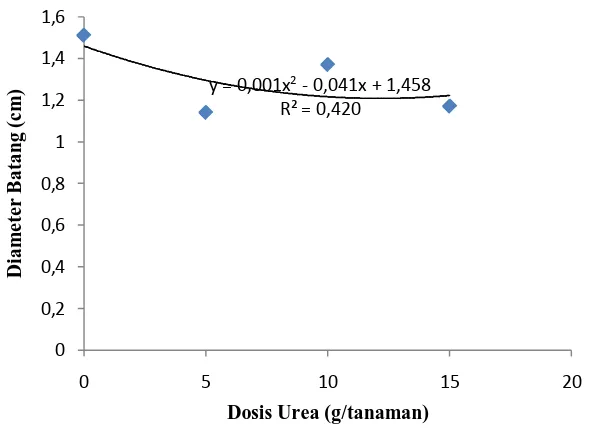
Gambar3. Hubungan peningkatan dosis urea untuk diameter batang 10 MST
Demikian juga pada diameter batang dengan pemberian Azospirillum sp. pada carrier kompos berpengaruh nyata dalam meningkatkan diameter batang, diameter batang tertinggi pada A2 (1.39 cm), A1(1.37 cm) dan A0 (1.13cm), sedangkan pada peningkatan dosis urea menekan pertumbuhan diameter batang dibandingkan perlakuan tanpa urea U0 (1.51 cm), U2 (1.47 cm), U3(1.17 cm) dan terendah pada U1(1.14 cm).
Pada parameter jumlah anakan tidak berpengaruh nyata pada 10 MST seperti yang dapat dilihat pada Tabel 4 tersebut. Namun pada data 4 MST berpengaruh nyata pada faktor Azospirillum sp. carrier kompos dalam meningkatkan jumlah anakan dan urea dalam mengurangi jumlah anakan (Lampiran 21).
Pemberian Azospirillum sp. pada carrier kompos mampu meningkatkan berat kering tajuk pada tanaman tebu sangat nyata dibanding A0 (120 g), A1(198.95 g) dan tertinggi pada A2(414.44 g), sedangkan pada pemberian urea tidak berbeda nyata antar perlakuannya dimana terjadinya penurunan berat dibanding tanpa urea U0. Begitu juga pada berat kering akar yang berbeda sangat nyata dalam meningkatkan pada faktor pemberian Azospirillum sp. pada carrier kompos dibanding A0(21.15 g), A1(30.08 g) dan tertinggi A2(40.33 g) sedangkan pada faktor urea tidak berbeda nyata, menyebabkan penurunan berat dibanding tanpa urea U0.
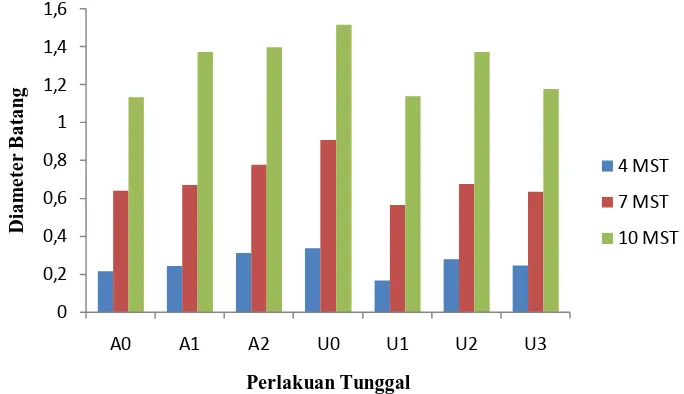
Gambar 4. Laju pertumbuhan Tinggi Tanaman 4 MST, 7 MST dan 10 MST pada perlakuan Tunggal.
Pada Gambar 4 laju pertumbuhan tinggi tanaman tertinggi pada perlakuan tunggal U0 (tanpa diberikan urea) diikuti dengan A2 (kompos + Azospirillum sp.), A1 (Kompos tanpa Azospirillum sp.), U2 (dosis urea 10g/tanaman), U1 (urea 5
g/tanaman), A0 (tanpa kompos Azospirillum sp.) dan terendah pada U3 (15 g/tanaman).
Pada Gambar 5 laju pertumbuhan diameter batang tertinggi pada perlakuan tunggal U0 (tanpa diberikan urea) diikuti dengan A2 (kompos + Azospirillum sp.), A1 (Kompos tanpa Azospirillum sp.), U2 (dosis urea 10 g/tanaman), U3 (urea 15 g/tanaman), U1 (5 g/tanaman) dan terendah pada A0 (tanpa kompos dan Azospirillum sp.)
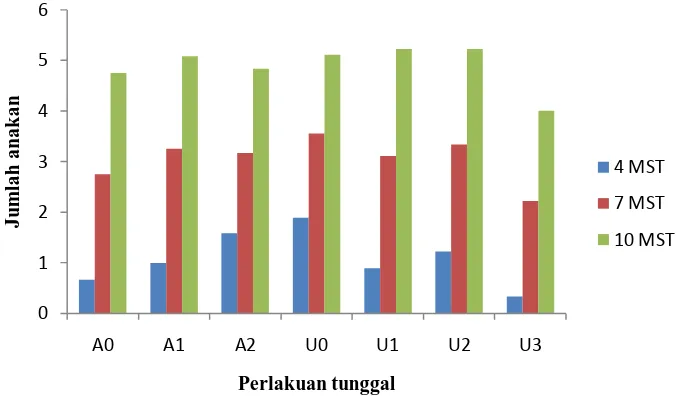
Gambar 6. Laju pertumbuhan Jumlah anakan 4 MST, 7 MST dan 10 MST pada perlakuan Tunggal
Pada Gambar 6 laju pertumbuhan diameter batang tertinggi pada perlakuan U1 (5g/tanaman) diikuti U2 (dosis urea 10 g/tanaman), U0 (tanpa urea), A1 (Kompos tanpa Azospirillum sp.), A2 (kompos + Azospirillum sp.), A0 ( tanpa kompos dan Azospirillum sp )dan terendah pada U3 (15 g/tanaman).
Pembahasan Penelitian Tahap I
Dari hasil penelitian pada tahap I dalam menentukan kompos rasio terbaik yang digunakan sebagai carrier dapat dilihat pada Tabel 1. bahwa kompos A3 merupakan kompos yang dapat mendukung pertumbuhan Azospirillum dengan
terendah pada A1( 3.61%), begitu juga pada N-total kompos tertinggi pada kompos A3 (0.91%), A4 (0.49%) , A2 (0.29%) dan A1 (0.24%). dengan demikian diperoleh rasio C/N dari masing-masing kompos dengan rasio tertinggi pada A4(72.41), A3(53.44), A2(22.51) dan terendah A1(15.04). Hal ini disebabkan bahwa tingkat kematangan kompos yang dianalisis berbeda yakni matang dan mentah dimana A1 merupakan limbah tebu yang telah dibiarkan setelah penggilingan selama 5 bulan (saat akan dianalisis), A2 dibiarkan setelah penggilingan selama 2 bulan (saat akan dianalisis), A3 yang baru saja digiling dan dibiarkan 1 hari (saat akan dianalisis) dan A4 dibiarkan 3 minggu setelah penggilingan (saat akan dianalisis). Kompos dari limbah tersebut dapat digunakan sebagai carrier pada inokulan yang membutuhkan energi terutama karbon seperti Azospirillum sp.
Dari Tabel 1 dapat dilihat bahwa pada umumnya kompos yang memiliki pH tinggi yakni 7.23 (A1) dan 7.12 (A2) sedangkan kompos yang berumur muda memiliki pH 5.37 (A3) dan 5.54 (A4) . Kompos memiliki pH rendah disebabkan masih terjadinya proses fermentasi dari limbah yang baru digiling sehingga masam. Namun, demikian pertumbuhan Azospirillum sp meningkat pada kompos A3 dan A4 karena pada kondisi pH diatas 7 pertumbuhan Azospirillum sp
terhambat, sementara pada pH 5.5-7 aktifitas nitrogenase dapat terjadi (Hanafiah et al., 2009)
Penelitian Tahap II
cfu/ml). Hal ini disebabkan tingginya carbon dan nitrogen pada kompos A3 dan senyawa-senyawa pada limbah tebu masih banyak karena masih mentahnya limbah dibandingkan kompos yang lain sehingga Azospirillum dapat memperoleh sumber energi yang banyak dan berkembang. Azospirillum sp. tumbuh baik pada pada kultur yang bersumber C dan energi berasal dari malate, succinat, laktat maupun pyruvat (Hanafiah et al., 2009)
Sifat Kimia
Pada Tabel 2. hasil penelitian tahap II dapat dilihat bahwa faktor Azospirillum berpengaruh nyata dalam meningkatkan C-organik pada tanah
dibanding kontrol A0 (1.613%), dimana C-organik tertinggi pada perlakuan A1( Kompos tanpa Azospirillum) yaitu 1.889% yang berbeda sangat sedikit
dengan A2 (Azospirillum + Kompos) yakni 1,878%. Sedangkan kombinasi tidak berpengaruh nyata, dimana terlihat bahwa C-organik tertinggi pada perlakuan A2U3 dan A1U1 yaitu 2.01% dan terendah pada A0U1 (1.58%).Hal ini disebabkan carrier yang digunakan adalah kompos limbah tebu dengan C-organik kompos yang tinggi yakni 48,63% sehingga C-organik tanah yang diberikan kompos ini dapat meningkat dibanding kontrol dan digunakan oleh mikroba tanah untuk merombak bahan organik yang ada ditanah serta dalam proses metabolisme terutama pada Azospirillum. seperti pada penelitian Zulkarnain et al., (2012) menyatakan bahwa pemberian kompos dapat meningkatkan C-organik tanah, semakin banyak kompos yang diberikan C-organik tanah akan semakin meningkat.
kombinasi perlakuan diperoleh N-total tertinggi adalah pada A0U3 (0.22%) dan terendah pada A2U1 (0.13%). terlihat bahwa N-total tertinggi pada kombinasi perlakuan yang menggunakan urea 15 g/tanaman tanpa pemberian kompos dan Azospirillum sedangkan yang terendah pada kombinasi perlakuan kompos +
Azospirillum dan Urea 5 g/tanaman, dimana pemberian urea dengan dosis yang
tinggi dapat meningkatkan N-total tanah sedangkan pemberian Azospirillum carrier kompos pada penelitian ini cenderung menurunkan N-total tanah. Hal ini disebabkan bahwa carrier kompos yang digunakan merupakan kompos yang masih mentah sehingga masih adanya perombakan yang dilakukan oleh mikroorganisme tanah dan membutuhkan nitrogen untuk kelangsungan jasad renik, begitu juga pada Azospirillum. Pada proses dekomposisi bahan organik terutama yang mengandung kadar nitrogen rendah, nitrogen tersebut digunakan untuk menyusun jaringan-jaringan jasad renik (Damanik et al., 2011). Azospirillum dapat mengunakan NH4+, NO3-, N2
2). Sutanto (2002) menyatakan Nisbah karbon dan nitrogen (nisbah C/N) sangat penting untuk memasok hara yang dibutuhkan mikroorganisme selama proses pengomposan berlangsung. Karbon diperlukan mikroorganisme sebagai sumber energi dan nitrogen untuk membentuk protein.
Dari hasil penelitian pada Tabel 3 terlihat faktor urea berpengaruh nyata dalam menurunkan pH tanah dari setiap perlakuan dibandingkan perlakuan kontrol U0 (5.62) dan menurun pada U1(5.234), U2(5.19) dan U3(5.24) penurunan dapat dilihat. Hal ini disebabkan adanya ion H+
CO(NH
yang dihasilkan pada oksidasi enzimatik (nitrifikasi) sehingga menyebabkan pH menurun. Mukhlis et al., (2011) mengatakan bahwa pemberian urea pada tanah berpH kurang dari 6.3,
amonium hilang melalui volatilisasi dan terdekomposisi sebagai berikut :
2)2 + 2H+ + 2H2O → 2NH4+ + H2CO
Dikonsumsi 2 H+ untuk setiap molekul urea, sehingga reaksi ini cenderung menaikkan pH diawal, tetapi ion amonium diubah menjadi nitrat dengan membebaskan empat ion H+ sehingga pH akan menurun lebih besar, scara keseluruhan urea akan mengasamkan tanah.
3
Dari Tabel 3 hasil menunjukkan bahwa pada faktor Azospirillum sp. dan urea serta interaksinya tidak berpengaruh nyata untuk N tanaman. Dapat dilihat pada kombinasi perlakuan N tanaman tertinggi adalah A0U1 yaitu 1.77% dan terendah pada A2U1 0.84% . Pada hasil penelitian Nurmayulis dan Maryati (2008) bahwa N tanaman pada kentang meningkat dengan diberikannya inokulan Azospirillum. N tanaman meningkat karena aktivitas Azospirillum membentuk
pada hasil penelitian ini yang menunjukkan N-tanaman pada perlakuan yang diberi Azospirillum rendah adalah karea N tersedia pada tanah yang rendah pula (berbanding lurus antara N-tanah dan N-tanaman).
Pada Tabel 3 diketahui faktor Azospirillum sp. memberikan pengaruh nyata dalam meningkatkan serapan N sedangkan pada faktor urea serta interaksi tidak berpengaruh nyata dalam meningkatkan serapan N secara statistik. Pada faktor Azospirillum serapan N tertinggi adalah pada A2 (3.81 mg/tanaman) dibanding A1 (2.43 mg/tanaman) dan A0 (1.229 mg/tanaman) sedangkan pada kombinasi perlakuan dapat dilihat tertinggi pada A2U0 (4.09 mg/tanaman) dan terendah pada A0U3 (0.72 mg/tanaman). serapan N ini sangat dipengaruhi oleh berat kering tajuk dari masing-masing perlakuan. Berdasarkan hasil baik kombinasi maupun faktor Azospirillum, bahwa yang diberikan Azospirillum carrier kompos (A2) memiliki serapan N yang lebih tinggi dari perlakuan lainnya. Pada hasil penelitian Pitriana (1999) juga telah menununjukkan bahwa pemberian inokulan Azospirillum memberikan hasil serapan N sebesar 187.96- 288.58% sedangkan dengan pupuk NP sebesar 150.98-189%. Pemberian Azospirillum dapat meningkatkan serapan N pada tanaman cabe merah, tomat dan padi sebesar 12.0- 26.7% (Kim et al., 2010).
Pertumbuhan dan Produksi Tanaman
Dari hasil penelitian pada Tabel 4 faktor Azospirillum sp. berpengaruh sangat nyata dalam meningkatkan tinggi tanaman dan berpengaruh sangat nyata dalam menurunkan pada faktor urea. Pada faktor Azospirillum sp.tinggi tanaman tertinggi pada perlakuan A2 yakni 37.97cm, dengan A1 (34.23 cm) dan A0 (27.80
U1 (28.03 cm), U2 (34.10 cm) dan U3 (27.19 cm). Pada perlakuan kombinasi tidak berpengaruh nyata, dimana tanaman tertinggi pada perlakuan kombinasi A2U0 yakni 49.04 cm dan terendah pada A0U1 (18.74 cm). Demikian juga pada parameter diameter batang masing-masing faktor berpengaruh sangat nyata. Pada faktor Azospirillum berpengaruh sangat nyata dalam meningkatkan dimana tertinggi A2 (1.39 cm), kemudian A1 (1.37 cm) dan terendah A0 (1.13 cm), sedangkan pada faktor urea sangat nyata dalam menurunkan diameter batang dibanding U0 (1.51 cm), dimana terendah pada U1 (1.14 cm), U3 (1.17 cm) dan U2 (1.14 cm). Pada kombinasi perlakuan tidak berpengaruh nyata dengan diameter tertinggi adalah A1U0 (1.58 cm) dan terendah A0U1 (0.92 cm). Untuk pertumbuhan dari tinggi tanaman dan diameter batang pada 4, 7 sampai 10 MST dapat dilihat (Gambar 4 dan 5) dengan data pertumbuhan tinggi tanaman 4, 7 dan 10 MST (Lampiran 7, 9 dan 11) dan data pertumbuhan diameter batang 4,7 dan 10 MST ( Lampiran 13, 15 dan 17).
Pada faktor Azospirillum sp memperlihatkan bahwa adanya peningkatan terhadap tinggi tanaman dan diameter batang. Hal ini disebabkan bahan organik yang digunakan sebagai carrier dapat menyediakan unsur hara yang optimal untuk pertumbuhan tanaman, mampu mempertahankan jalannya siklus hara dan dapat mengikat/mengadsorpsi kation dan anion serta sebagai sumber energi karbon dan mineral untuk mikrobia (Hanafiah et al., 2009). Dengan demikian pada perlakuan Azospirillum yang diberikan dapat berkembang lebih aktif sehingga mampu
keuntungan, karena adanya suplai amonium dalam jumlah tidak berlebihan secara terus menerus, dan adanya hormon tumbuh seperti auksin, IAA dan giberelin.
Pada penelitian ini peningkatan dosis urea yang diberikan menurunkan tinggi tanaman serta diameter batang tanaman tebu nyata secara statistik. Pada hasil penelitian lain juga memperlihatkan penurunan yakni Parto et al., (2011) yang meneliti pengaruh pemberian urea terhadap pertumbuhan karet menunjukkan bahwa pemberian urea menurunkan diameter batang tanpa urea 1.46 cm menurun menjadi 1.41 cm dengan dosis 2 g/tanaman dan pada dosis 4 g/tanaman menjadi 1.37 cm. Pada Tabel 4 jumlah anakan tidak berpengaruh nyata, namun jumlah anakan terbanyak pada pemberian urea 10 g/tanaman (5.22 tunas). Ganguan pertumbuhan tanaman tebu akibat penambahan dosis pupuk urea kemungkinan disebabkan terganggunya keseimbangan hara dalam tanah. Hal ini bertentanga dengan pernyataan Pawirosemadi (1996) dimana pemberian nitrogen pada tanaman tebu akan meningkatkan populasi batang tebu, peningkatan pupuk nitrogen akan selalu meningkatkan jumlah tunas hingga tercapai suatu optimum, dan penambahan nitrogen berikutnya tidak akan memberikan pengaruh lagi.
bahan organik dan Azospirillum yang diberikan dalam memberikan hara yang seimbang yang berpengaruh meningkatkan bobot tajuk dan akar. Hal ini sejalan dengan Bashan dan Holguin (1997) inokulasi campuran Azospirillum sp. dengan mikroorganisme yang menguntungkan memungkinkan terjadinya keseimbangan nutrisi untuk meningkatkan kandungan hara N, P, dan hara lainnya pada tanaman.
Pada faktor urea untuk parameter berat kering tajuk dan berat kering akar tidak berpengaruh nyata namun relatif menurunkan bobot. Hal ini sejalan dengan tinggi tanaman dan diameter batang, pendugaan yang sama bahwa adanya ketidak seimbangan hara dan pertumbuhan terhambat sehingga mempengaruhi pada produksi. Nurmayulis dan Maryati (2008) mengatakan bahwa dengan pemberian pupuk N, selain digunakan untuk kebutuhan tanaman, dekomposisi bahan organik juga sangat ditentukan oleh ketersediaan N tanah, terutama N-NO3 - yang
KESIMPULAN
Kesimpulan1. Perkembangan populasi Azospirillum sp. terbanyak pada kompos A3 (kompos umur 1 hari) dengan rasio C/N kompos 53 yakni sebesar 140 x 109 2. Perlakuan tunggal pemberian Azospirillum sp. carrier kompos berpengaruh
nyata dalam meningkatkan Tinggi tanaman, diameter batang, berat kering tajuk, berat kering akar tanaman tebu, C-organik, Rasio C/N dan serapan N.
.
3. Pemberian Azospirillum sp tidak berpengaruh nyata secara statistik dalam meningkatkan pH, N-total tanah, jumlah anakan tanaman tebu dan kadar N tanaman.
4. Perlakuan tunggal pemberian urea tidak berpengaruh nyata dalam meningkatkan N-total tanah, N tanaman, serapan N, berat kering tajuk, berat kering akar, C-organik, rasio C/N, jumlah anakan namun berpengaruh nyata dalam menurunkan tinggi tanaman, diameter batang serta pH tanah secara statistik.
5. Interaksi dari urea dan bakteri tidak berpengaruh nyata pada semua parameter yang diukur
Saran
TINJAUAN PUSTAKA
Nitrogen (N)
Nitrogen adalah unsur hara utama yang dibutuhkan oleh tanaman dalam jumlah cukup banyak, unsur ini penting artinya dalam pembentukan klorofil daun, sintesa protein dan lain-lain. Sebagian besar nitrogen dalam tanah berasal dari bahan organik tanah, karena itu jika kandungan bahan organik di dalam tanah rendah biasanya diikuti oleh rendahnya kandungan nitrogen ( Purwanti, 2008).
Nitrogen (N) merupakan unsur hara yang paling penting. Kebutuhan tanaman akan N lebih tinggi dibandingkan dengan unsur hara lainnya, selain itu N merupakan faktor pembatas bagi produktivitas tanaman. Kekurangan N akan menyebabkan tumbuhan tidak tumbuh secara optimum, sedangkan kelebihan N selain menghambat pertumbuhan tanaman juga akan menimbulkan pencemaran terhadap lingkungan (Duan et al., 2007).
Nitrogen diserap oleh tanaman dengan kuantitas terbanyak dibandingkan dengan unsur lain yang didapatkan dari tanah. Sumber nitrogen di dalam tanah adalah dari fiksasi oleh mikroorganisme, air irigasi dan hujan, absorpsi amoniak, perombakan bahan organik, dan pemupukan. Nitrogen di dalam tanah mempunyai dua bentuk utama, yaitu nitrogen organik dan nitrogen anorganik berupa amonium (NH4), amoniak (NH3), nitrit (NO2), dan nitrat ( NO3) (Stevenson, 1982).
Nitrogen diserap tanaman dalam bentuk NO3 dan NH4.
Pupuk Urea [CO(NH
Nitrogen dalam bentuk anorganik dijumpai dalam bentuk ion-ion yang berada di dalam larutan tanah, yang berada di kompleks adsorpsi, atau dalam bentuk ion amonium yang terfiksasi pada kisi mineral liat ( Hanafiah et al., 2009). Pemberian nitrogen pada tanaman tebu akan meningkatkan populasi batang tebu, peningkatan pupuk nitrogen akan selalu meningkatkan jumlah tunas hingga tercapai suatu optimum, sehingga penambahan nitrogen berikutnya tidak akan memberikan pengaruh lagi (Pawirosemadi, 1996).
2)2
Pupuk Urea adalah pupuk kimia yang mengandung Nitrogen (N) berkadar tinggi. Unsur Nitrogen merupakan zat hara yang sangat diperlukan tanaman. Pupuk Urea berbentuk butir-butir kristal berwarna putih, dengan rumus kimia CO(NH
]
2)2, merupakan pupuk yang mudah larut dalam air dan sifatnya sangat
mudah menghisap air (higroskopis), karena itu sebaiknya disimpan di tempat kering dan tertutup rapat. Pupuk Urea mengandung unsur hara N sebesar 46%
dengan pengertian setiap 100 kg Urea mengandung 46 kg Nitrogen (Damanik et al ., 2011). Beberapa tuntutan yang bersifat menekan sebagai
kenyataan bahwa efisiensi serapan kembali (recovery efficiency) pupuk N jarang melebihi 50% ( Mukhlis et al., 2011).
Pemberian urea pada tanah berpH kurang dari 6.3, amonium hilang melalui volatilisasi dan terdekomposisi sebagai berikut :
CO(NH2)2 + 2H+ + 2H2O → 2NH4+ + H2CO
Dikonsumsi 2 H
3
+
untuk setiap molekul urea, sehingga reaksi ini cenderung menaikkan pH diawal, tetapi ion amonium diubah menjadi nitrat dengan membebaskan empat ion H+
Biologi Azospirillum sp
sehingga pH akan menurun lebih besar, scara keseluruhan urea akan mengasamkan tanah ( Mukhlis et al., 2011).
Azospirillum sp. merupakan bakteri tanah penambat nitrogen
nonsimbiotik. Bakteri ini hidup bebas di dalam tanah, yang berada disekitar atau dekat dengan perakaran (Nurosid et al., 2008). Azospirillum mempunyai ciri berupa sel yang berbentuk setengah spiral yang padat dan bergetar dengan sebuah flagel polar, sehingga bergerak secara berputar. Pertumbuhan genus Azospirillum pada media semi padat dicirikan dengan pembentukan pellicle berwarna putih di permukaan media dengan diameter 2-4 mm. Koloni berbentuk irregular berwarna putih dan berukuran besar (Nurhayati, 2006). Spesies Azospirillum berbentuk polimorf, motil, dan termasuk gram negatif (Pitriana, 1999).
meningkatkan kesuburan tanah melalui penyediaan P dan fiksasi N2. Bakteri
pemfiksasi N2
Azospirillum sp. dikenal juga sebagai mikroorganisme diazotrof yang
simbiotik, artinya Azospirillum sp. mampu menambat N
seperti Azospirillum, Enterobactercloacae, Alcaligenes,
Acetobacter diazotrophicus, Herbaspirillum seropedicae, Ideonella dechlorantans
(Yulianti, 2012).
2 dan mengadakan
asosiasi yang erat dengan tanaman inang tertentu. Azospirillum sp. mampu tumbuh pada tanaman tebu dan membentuk seperti kapsul yang mampu menambat N2
Spesies dari Azospirillum yang dikenal adalah A. brasilense, A. lipoferum dan A. amazone. Keduanya adalah bakteri gram negatif, memiliki sel berbentuk
batang, diameter 1 ηm, sangat motile dan memiliki flagellum panjang dan polar
untuk dapat berenang dan kadang-kadang peritrichous flagella untuk berkumpul dipermukaan. Sel dari Azospirillum berubah bentuk dan ukuran tergantung pada umur kultur, dan memproduksi cysts (Hanafiah et al., 2009).
(Berg et al., 1980 ; Rusmana dan Hadijaya, 1994).
Pertumbuhan Bakteri Azospirillum sp.
Azospirillum dapat tumbuh pada glukosa, fruktosa, serta pada garam dan
mana pada tanaman ini bakteri berkembang dengan baik (Okon et al., 1976 ; Purushotman et al.,1980).
Beberapa spesies hidup bebas dalam tanah atau berasosiasi dengan akar tanaman rumput-rumputan, sayur-sayuran dan legum. Penambatan nitrogen maksimum terjadi pada pH 6-7 (Pitriana, 1999). Azospirillum tumbuh baik pada kultur yang bersumber C dan energi berasal dari malate, succinat, laktat maupun pyruvat (Hanafiah et al., 2009). Azospirillum sp terdapat di tanah sekitar akar, permukaan akar dan didalam akar, asosiasi antara Azospirillum dengan tanaman diduga bersifat simbiosis karena Azospirillum menggunakan senyawa malat sebagai sumber karbon untuk pertumbuhannya. Dugaan ini diperkuat dengan
adanya aktivitas nitrogenase Azospirillum dalam kalus tebu ( Berg et al., 1980 ; Rusmana dan Hadijaya, 1994). Inokulasi campuran
Azospirillum sp. dengan mikroorganisme yang menguntungkan memungkinkan
terjadinya keseimbangan nutrisi untuk meningkatkan kandungan hara N, P, dan hara lainnya pada tanaman ( Bashan dan Holguin, 1997)
Azospirillum sp. diisolasi pertama kali dari permukaan akar
rumput-rumputan makanan ternak dan beberapa tanaman serealia. Selain pada Gramineae Azospirillum dapat juga diisolasi dari non Gramineae (Gamo dan Ahn, 1991;
Dua komponen dalam medium untuk pertumbuhan yang dapat mempengaruhi pembentukan asosiasi tanaman-bakteri, yaitu N dan C . Konsentrasi N di media mempengaruhi metabolisme Azospirillum (Pedrosa, 1988; Dubrovsky et al., 1994) serta pertumbuhan tanaman. Glukosa atau sukrosa biasanya digunakan sebagai sumber C untuk media pertumbuhannya (Wilson et al., 1990 ; Dubrovsky et al., 1994) Azospirillum tumbuh-aktif pada akar dalam
media tersebut yang mengeluarkan berbagai sumber C di eksudat akar dan dimetabolisme oleh bakteri rizosfir (Curl and Truelove, 1986; Dubrovsky et al., 1994
Pemberian pupuk N, selain digunakan untuk kebutuhan tanaman, dekomposisi bahan organik juga sangat ditentukan oleh ketersediaan N tanah, terutama N-NO
) yang dapat mempengaruhi fungsi yang efisiensi dari asosiasi akar-bakteri. Karena itu, penting untuk menemukan C dan N kombinasi yang tidak mengganggu asosiasi dan optimal untuk pertumbuhan mikroorganisme.
3 - yang berfungsi sebagai substrat jasad renik. Azospirillum sp.
juga memerlukan N sebagai sumber energi untuk kehidupannya sehingga pada akhirnya dapat menghasilkan N melalui aktivitasnya dalam memfiksasi N2
Peran Azospirillum sp.
( Nurmayulis dan Maryati, 2008).
menghasilkan vitamin berupa tiamin, niasindan pantotenin, yangbersamadenganhormon tumbuh berfungsi sebagai pemacu pertumbuhan dan produksi tanaman (Karti, 2005).
Salah satu organisme yang terlibat dalam mekanisme fiksasi N2 adalah Azozpirilum.
Bakteri Azospirillum mampu menyediakan unsur N dan P bagi pertumbuhan tanaman, serta sekaligus sebagai bakteri pemantap agregat tanahyang juga dapat merombak bahan organik kelompok karbohidrat, seperti selulosa dan amilosa, serta bahan organik yang mengandung sejumlah lemak dan protein di dalam tanah. Hidupnya dalam habitat rhizosfer tanaman dapat berasosiasi dan berinteraksi dengan perakaran sehingga berperan dalam mengubah morfologi akar. Seperti bertambahnya jumlah akar rambut, akar semakin panjang dan permukaan akr yang semakin luas (Widiawati dan Muharam , 2012).
Meskipun peran bakteri ini dalam memfikasi sedikit, namun berpotensi menyumbangkan nitrogen yang lebih besar dari pada pemfikasi lainnya tergantung pada kelangsungan hidup dalam tanah dan interaksi Azospirillum dengan bakteri di rizosfer lainnya (Holguin and Bashan, 1996).
Azospirillum sp. juga mempunyai kemampuan merombak bahan oganik di dalam
tanah. Bahan organik yang dimaksud adalah bahan organik yang berasal dari kelompok karbohidrat seperti selulosa, amilosa, dan bahan organik yang mengandung sejumlah lemak dan (Nurosid et al., 2008).
Nitrogen tanaman pada kentang meningkat dengan diberikannya inokulan Azospirillum. N tanaman meningkat karena aktivitas Azospirillum membentuk
Azospirillum sp menambat nitrogen pada kondisi mikroaerofil. Nitrogen
yang dihambat tersebut akan diserap oleh tanaman dalam bentuk NO3- dan NH4+
(Rao, 1982 ; Rusmana dan Hadijaya, 1994) kemudian diubah menjadi glutamin dan alanin menggunakan enzim nitrogenase (Widiawati dan Muharam, 2012). Azospirillum sp. memfiksasi N dengan kemampuannya menghasilkan nitrogenase
dengan memutuskan ikatan rangkap N2 dan menggabungkannya dengan fotosintat
untuk membentuk NH3. Selanjutnya di sitoplasme sel mikroba tersebut NH3 yang
terbentuk segera dirubah menjadi bentuk amonium (NH4+) yang digunakan
sebagai komponen untuk mensintesa berbagai molekul biologi penting lainnya seperti asam amino, protein, vitamin, asam nukleat dan material genetik seperti DNA. Secara umum reaksinya adalah : N2 + 16 ATP + 8 e- + 8H+→ 2NH3 + 16
ADP + 16 Pi + H2
Aplikasi Azospirillum sp. pada berbagai Tanaman (Hanafiah et al., 2009)
Dari hasil penelitian Gadagi et al. (2003) yang membandingkan pengaruh inokulasi Azospirillum sp. dengan pemupukan urea terhadap serapan nitrogen pada tanaman bunga Gaillardia pulchella menunjukkan bahwa serapan nitrogen tertinggi dari seluruh perlakuan adalah pemberian Azospirillum yang diisolasi dari bunga hias. Sedangkan pada penelitian Ferriera et al. (2013) menunjukkan hasil bahwa Azospirillum memberikan hasil yang nyata dengan berat kering tajuk dan berat kering akar tertinggi pada tanah liat. Dengan demikian dalam penelitian ini menyimpulkan bahwa inokulasi Azospirillum dilapangan lebih baik pada tanah liat.
(Eckert et, al. 2001; Widiawati dan Muharam, 2012).
Kim et al.(2010) pada penelitiannya menunjukkan bahwa Azospirillum sp. dapat meningkatkan serapan N pada tanaman cabe merah, tomat dan padi sebesar 12.0- 26.7%. Nurmayulis da Maryati (2008) juga menunjukkan bahwa hasil bobot kentang dan serapan N lebih tinggi pada aplikasi Azospirillum dari pada pemupukan N, Hungria et al.(2010) produksi jagung dan gandum meningkat
27-31%. Pada hasil penelitian Karti (2005) penambahan isolat bakteri Azospirillum sp. pada tanah podsolik merah kuning pada rumput yang toleran
( S. splendida) meningkatkan produksi dan kadar N tajuk, akar serta serapan N total
beberapa hasil penelitian seperti Pitriana (1999) juga telah menununjukkan bahwa pemberian inokulan Azospirillum memberikan hasil serapan N sebesar 187.96- 288.58% sedangkan
dengan pupuk NP sebesar 150.98-189%
Menurut Eckert et al. (2001) isolasi Azospirillum sp. dapat dilakukan dengan cara sebagai berikut. Akar tanaman tertentu dan tanah rhizosfer diambil dari lapangan di mana tanaman tersebut telah tumbuh lama di sana. Akar-akar tanaman dicuci dengan air steril dan kemudian digerus dalam larutan sukrosa 4% dengan menggunakan mortar dan pastel. Wadah kecil (sekitar 10 ml) yang mengandung 5 ml medium NFb semi-solid bebas nitrogen diinokulasi dengan larutan berseri dari gerusan akar atau suspensi tanah rhizosfer.
Inokulan Azospirillum sp menggunakan carrier Kompos
pada media pembawa seperti, gambut, kompos, dan lain-lain,. Adapun komposisi okon (Lampiran 1.) (Danapriatna dan Simarmata, 2011)
Inokulan bakteri adalah suatu formulasi yang mengandung satu atau beberapa strain bakteri bermanfaat di dalam suatu material bahan pembawa yang mudah digunakan dan ekonomis. Bahan pembawa merupakan medium yang digunakanuntuk memindahkan mikroorganisme hidup darilaboratorium atau pabrik ke lapang. Bahan pembawa harus mampu menopang pertumbuhan dan kelangsungan hidup mikroorganisme targetselama periode penyimpanan dan pengirimannya kelapang (Larasati et al., 2012).
Umumnya mikroba dalam pupuk hayati dikemas dalam bahan pembawa berbentuk serbuk atau bentuk cairan. Sebagai bahan pembawa inokulan serbuk, dapatdigunakan bahan organik seperti gambut, arang, sekam, dan kompos (Danapriatna dan Simarmata, 2011). Pada penelitian Widiawati et al. (2012) menggunakan gambut sebagai inokulan pembawa untuk bakteri Azospirillum dimana gambut perlu di sterilkan terlebih dahulu. Gambut halus steril sebagai bahan pembawa dicampur dengan inokulan cair dengan perbandingan 100 g
gambut dan 60 ml inokulan cair. Inokulan padat tersebut digunakan sebanyak 10 g per pot.
Kompos merupakan bahan organik yang telah mengalami proses dekomposisi oleh mikroorganisme pengurai, sehinga dapat dimanfatkan untuk memperbaiki sifat tanah. Bahan organik yang dapat digunakan sebagai sumber
kompos dapat berasal dari limbah hasil pertanian dan non pertanian (Setyorini et al., 2006). Kemungkinan bahan dasar kompos mengandung selulosa
3-5%, bahan larut panas dan dingin (gula, pati, asam amino, urea, garam, aonium) sebanyak 2-30% dan 1-5% lemak larut eter dan alkohol, minyak dan lain laun (Barat, 2006).
Disamping CO2, pengomposan juga mengakibatkan lepasnya N dalam
bentuk NH3 dan N2O. NH3 terbentuk jika kompos terlalu kering, sementara N2
Nisbah karbon dan nitrogen (nisbah C/N) sangat penting untuk memasok hara yang dibutuhkan mikroorganisme selama proses pengomposan berlangsung. Karbon diperlukan mikroorganisme sebagai sumber energi dan nitrogen untuk membentuk protein (Sutanto, 2002). Karbon dibutuhkan oleh mikroba sebagai sumber energi untuk pertumbuhannya dan nitrogen diperlukan untuk membentuk protein (Setyorini et al., 2006).. Hubungan antara C dan N yang hilang dalam proses pengomposan menunjukkan bahwa 85% dari total awal N kompos tersedia bagi mikrobia untuk tumbuh dan 70% dari C tersedia hilang sebagai CO
O terbentuk jika proses nitrifikasi dan denitrifikasi terjadi pada tumpukan kompos (Fukumoto et al., 2003). Lepasnya N akan menyebabkan ketersediaannya berkurang, sehingga perlu adanya mikroorganisme penambat N dari udara seperti Azozpirilum.
2
Pada proses dekomposisi bahan organik terutama yang mengandung kadar nitrogen rendah, nitrogen tersebut digunakan untuk menyusun jaringan-jaringan jasad renik (mikroorganisme tanah) ( Damanik et al., 2011). Azospirillum dapat mengunakan NH
selama proses immobilisasi(Sabrina et al., 2011).
4+, NO3-, N2 sebagai sumber N untuk pertumbuhannya (
bergantung pada ketersediaan N sebagai sumber nutrisi dan C sebagai sumber energi dalam rizosfer ( Nurmayulis dan Maryati, 2008)
Apabila ketersediaan karbon terbatas (nisbah C/N terlalu rendah) tidak cukup senyawa sebagai sumber energi yang dapat dimanfaatkan mikroorganisne untuk mengikat seluruh nitrogen bebas. Apabila ketersediaan karbon berlebihan (nisbah C/N >40) jumlah nitrogen sangat terbatas sehingga merupakan faktor pembatas pertumbuhan mikroorganisme (Sutanto, 2002).
Bahan organik yang diberikan pada tanah dapat menyediakan unsur hara yang optimal untuk pertumbuhan tanaman, mampu mempertahankan jalannya siklus hara dan dapat mengikat/mengadsorpsi kation dan anion serta sebagai sumber energi karbon dan mineral untuk mikrobia (Hanafiah et al., 2009). pemberian kompos dapat meningkatkan C-organik tanah, semakin banyak
kompos yang diberikan C-organik tanah akan semakin meningkat ( Zulkarnain et al., 2013).
Tanaman Tebu ( Sacharum officinarum L)
Tebu adalah tanaman penghasil gula yang menjadi salah satu sumber karbohidrat. Tanaman ini sangat dibutuhkan sehingga kebutuhannya terus meningkat seiring dengan pertambahan jumlah penduduk. Namun peningkatan konsumsi gula belum dapat diimbangi oleh produksi gula dalam negeri. Hal tersebut terbukti pada tahun 2010 - 2011 produksi gula dalam negeri hanya mencapai 3.159 juta ton dengan luas wilayah 473.923 Ha. Penyebab rendahnya produksi gula dalam negeri salah satunya dapat dilihat dari sisi on farm,
Tanaman tebu termasuk ke dalam tanaman Monocotyledone, ordo Glumaceae, famili Graminae, Kelompok Andropogonae dan genus Saccharum
dan species yang paling banyak dibudidayakan adalah Saccharum officinarum L. Spesies ini termasuk spesies yang diusahakan karena sebagai penghasil gula utama sedangkan yang lainnya haya memiliki kandungan gula rendah hingga sedang (Setyamidjaja dan Azhami, 1992 ; Musarofah, 2002).
Menurut James (2004 dalam Leovici 2012), tanaman tebu memiliki perakaran serabut, yang dapat dibedakan menjadi akar primer dan akar sekunder. Tebu memiliki batang yang beruas-ruas dibatasi oleh buku sebagai tempat duduk daun.. Bentuk batang konis, susunan antar ruas berbuku, dengan penampang melintang agak pipih, warna batang hijau kekuningan, lapisan lilin tipis, retakan tumbuh ada, tetapi tidak di semua ruas, cincin tumbuh melingkar datar di atas puncak mata, dengan warna kuning kecoklatan, teras dan lubang masif dengan penampang melintang agak pipih, bentuk buku ruas : konis terbalik, dengan 3-4 baris mata akar, baris paling atas tidak melewati puncak mata alur mata tidak ada (Purwanti, 2008).