ANALISIS DIOSMIN DAN PROTEIN TANAMAN
SELEDRI (
Apium
graveolens
L.) DARI DAERAH CIPANAS
DAN CIWIDEY
BINA LISTYARI PUTRI
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
BINA LISTYARI PUTRI. Analisis Diosmin dan Protein Tanaman Seledri (
Apium
graveolens
L.) dari Daerah Cipanas dan Ciwidey. Dibimbing oleh DJAROT
SASONGKO HAMI SENO dan EDY DJAUHARI PURWAKUSUMAH.
Tanaman seledri berkhasiat farmakologis, salah satunya sebagai antiinflamasi dan
senyawa yang berperan adalah diosmin. Penelitian ini bertujuan untuk membandingkan
kadar diosmin serta pola protein tanaman seledri yang ditanam pada daerah Cipanas dan
Ciwidey dengan masa tanam berbeda. Ekstrak diosmin dari tanaman seledri diperoleh
dengan cara merefluks dalam larutan DMSO 10% dalam metanol kemudian dilakukan
identifikasi dan penentuan kadar menggunakan Kromatografi Lapis Tipis (KLT) dan
Kromatografi Cair Kinerja Tinggi (KCKT). Ekstraks i protein dari tanaman seledri
menggunakan bufer ekstraksi protein dan untuk mengetahui konsentrasi protein total
menggunakan metode Lowry. Elektroforesis gel poliakrilamid SDS digunakan untuk
mengetahui pola serta bobot molekul protein tanaman seledri.
ABSTRACT
BINA LISTYARI PUTRI. Analysis of Diosmin and Protein in Celery Plant (
Apium
graveolens
L) from Cipanas and Ciwidey Areas. Under the direction of DJAROT
SASONGKO HAMI SENO and EDY DJAUHARI PURWAKUSUMAH
The celery plant has a pharmacological function, one of the example as an
anti-inflammation and compound having the role is Diosmin. This research was to compare
the diosmin content and find out the protein pattern in the ce lery plant grown in the
areas of Cipanas and Ciwidey in different periods of planting. Cipanas and Ciwidey are
ideal sites for the celery growth because the differences in the geographical aspect and
growing period may result in the differences in diosmin level and protein pattern in the
celery plant. Diosmin was extracted from the celery plant with a reflux technique in the
solution of DMSO 10% mixed with methanol, identified and measured for its content
by using the Thin Layer Chromatography (TLC) and High Performance Liquid
Chromatography (HPLC). Protein was extracted from the celery plant by means of
buffer method and the Lowry method was used to determine the total concentration of
protein. Sodium Dedocyl Sulphat Poly Acrilamide Gel Electrophoresis (SDS PAGE)
was used to find out the pattern and weight of protein molecules in the celery plant.
ANALISIS DIOSMIN DAN PROTEIN TANAMAN
SELEDRI (
Apium
graveolens
L.) DARI DAERAH CIPANAS
DAN CIWIDEY
BINA LISTYARI PUTRI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Program Studi Biokimia
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU P ENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Analisis Diosmin dan Protein Tanaman Seledri (
Apium
graveolens
L.) dari Daerah Cipanas dan Ciwidey
Nama : Bina Listyari Putri
NIM
: G 44102017
Disetujui
Komisi Pembimbing
Drs. Djarot Sasongko Hami Seno, MS Drs. Edy Djauhari PK, M.Si
Ketua Anggota
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Ir. Yonny Koesmaryono, MS
NIP 131473999
PRAKATA
Segala puja dan puji syukur penulis panjatkan kehadirat Allah SWT, Tuhan semesta
alam yang telah memberikan nikmat iman dan islam, dan atas hidayah-Nya dalam
memberikan kemudahan sehingga kegiatan penelitian ini dapat diselesaikan. Kegiatan
penelitian akan dilaksanakan dari bulan Maret sampai Juni 2006 bertempat di
Laboraturium Pusat Studi Biofarmaka IPB Taman Kencana dengan judul Analisis
Diosmin dan Protein Tanaman Seledri (
Apium
graveolens
L.) dari Daerah Cipanas dan
Ciwidey.
Ucapan terima kasih terutama penulis ucapkan kepada Drs. Djarot Sasongko Hami
Seno, MS selaku pembimbing I dan Drs. Edy Djauhari PK, M.Si selaku pembimbing II
yang telah banyak memberikan saran. Selain itu, terima kasih juga kepada seluruh staf
di laboratorium Biokimia dan laboratorium Pusat Studi Biofarmaka atas kerjasamanya
serta Icha, Hilya, Rita, Peni, Ayu, Laura, Agung, Reggy, dan Heru yang selalu
memberikan semangat. Terima kasih kepada ayah, ibu, Rakha, Nandi, dan Bayu atas
segala doa dan kasih sayangnya.
Hasil penelitian ini masih jauh dari kesempurnaan karena keterbatasan pengetahuan
serta wawasan yang dimiliki oleh penulis. Namun, semoga penelitian ini berguna bagi
penulis serta pihak-pihak yang membutuhkannya demi kemajuan ilmu pengetahuan.
Bogor, Juni 2006
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 6 Mei 1984 dari ayah Ir. Listyanto BK dan
ibu Dra. Nanan Sofiana. Penulis merupakan putri pertama dari tiga bersaudara.
Tahun 2002 penulis lulus dari SMU Islam Al Azhar Kemang Pratama Bekasi dan
pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk
IPB (USMI). Penulis memilih Program Studi Biokimia Fakultas Matematika dan Ilmu
Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... i
DAFTAR GAMBAR ... i
DAFTAR LAMPIRAN ... ii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Tanaman Seledri (
Apium graveolens
L) ... 1
Budidaya Tanaman Seledri ... 2
Khasiat Tanaman Se ledri ... 4
Kandungan Kimia Tanaman Seledri ... 4
Diosmin ... 4
Analisis Diosmin dengan Kromatografi Cair Kinerja Tinggi ... 5
Pola Protein Tanaman Seledri ... 5
Analisis Pola Protein dengan Elekroforesis Gel Poliakrilamid SDS ... 6
BAHAN DAN METODE
Bahan dan Alat ... 6
Rancangan Percobaan ... 6
Metode ... 6
HASIL DAN PEMBAHASAN
Analisis Tanah ………...………...…….... 8
Bobot Basah ……….……….... 8
Kadar air dan Kadar Abu ………...………...……. 9
Konsentrasi Protein Total ………..………...….. 9
Kromatografi Lapis Tipis ……….………...…. 9
Penentuan Kadar Diosmin ………..…... 11
Elektroforesis Gel Poliakrilamid SDS ………....………... 12
SIMPULAN DAN SARAN
Simpulan ……….…….…. 13
Saran ………..………..…………... 13
DAFTAR PUSTAKA ... 13
DAFTAR TABEL
Halaman
1 Konsentrasi protein total dan rendemen ekstrak tanaman seledri
daerah Cipanas ... 10
2 Konsentrasi protein total dan rendemen ekstrak tanaman seledri
daerah Ciwidey ... 10
3 Hasil rataan KLT ekstrak ta naman seledri ... 11
4 Waktu retensi dan luas area konsentrasi standar diosmin ... 11
5 Kadar diosmin tanaman seledri daerah Cipanas dan Ciwidey
dengan masa tanam 4, 6, dan 8 minggu ... 12
DAFTAR GAMBAR
Halaman
1 Tanaman Seledri (
Apium graveolens
L.) ... 2
2 Struktur Kimia Diosmin ... 4
3 Bobot basah tanaman seledri daerah Cipanas dan Ciwidey
dengan masa tanam 4, 6, dan 8 minggu ... 9
4 Kadar air tanaman seledri daerah Cipanas dan Ciwidey
dengan masa ta nam 4, 6, dan 8 minggu ... 9
5 Kadar abu tanaman seledri daerah Cipanas dan Ciwidey
dengan masa tanam 4, 6, dan 8 minggu ... 9
6 Kurva Hubungan antara kadar protein dan rendemen ekstrak
tanaman seledri daerah Cipanas ... 10
7 Kurva Hubungan antara kadar protein dan rendemen ekstrak
tanaman seledri daerah Ciwidey ... 10
8 Kurva standar hubungan antara konsentrasi
standar diosm in dan luas area ... 11
9 Pola SDS-PAGE protein dari tanaman seledri daerah Cipanas dan Ciwidey
DAFTAR LAMPIRAN
Halaman
1 Tahap penelitian ...………...… 15
2 Pembuatan buf er ekstraksi protein …….………... 15
3 Bahan pereaksi untuk penentuan
konsentrasi total protein dengan metode Lowry ... 15
4 Bahan pereaksi untuk SDS PAGE ... 16
5 Pembuatan gel SDS PAGE ………. 17
6 Kondisi lingkungan daerah Cipanas dan Ciwidey ……….. 18
7 Hasil analisis tanah ………. 18
8 Kriteria penilaian sifat kimia tanah ……...……….………….……… 19
9 Hasil kadar air, kadar abu, dan bobot basah tanaman seledri pada daerah
Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu ... 20
10 Hasil analisis statistik Rancangan Acak Kelompok (RAK)
berbagai parameter ... 22
11 Kurva standar Bovine Serum Albumin (BSA)
untuk masa tanam 4, 6, dan 8 minggu ... 23
12 Nilai Rf hasil kromatografi lapis tipis ekstrak tanaman seledri ...24
13 Foto hasil kromatografi lapis tipis ... 25
14 Rendemen ekstrak tanaman seledri ... 26
15 Contoh perhitungan konsentrasi diosmin ... 27
16 Hasil kromatogram KCKT standar diosmin ... 28
17 Hasil kromatogram KCKT sampel tanaman seledri ... 29
PENDAHULUAN
Peningkatan penggunaan obat sintet ik berlangsung dengan cepat, namun seiring bertambahnya waktu terjadi pula peningkatan kesadaran masyarakat terhadap dampak negatif dari penggunaan obat -obatan sintetik. Akibatnya masyarakat kembali memilih tumbuhan obat sebagai alternatif terhadap penyembuhan berbagai penyakit. Selain itu, efek samping yang ditimbulkan juga lebih kecil. Hal tersebut memicu peneliti untuk melakukan penelitian di bidang biofarmaka, yaitu mengenai obat -obatan alami yang berasal dari tumbuhan.
Indonesia memiliki keragaman h ayati flora dan fauna yang sangat melimpah, sehingga memiliki banyak sekali tumbuhan yang berkhasiat sebagai obat. Menurut Kassahara dan Hemmi (1986), dari 28.000 jenis tumbuhan yang ditemukan di Indonesia, kurang lebih 7.000 jenis diantaranya adalah tumbuhan obat.
Salah satu contoh tumbuhan obat adalah seledri ( Apium graveolens L) merupakan tumbuhan suku Umbelliferae yang berbentuk rumput. (Sunarjono, 2003). Pada awalnya seledri dikenal sebagai sayuran untuk campuran salad, sup, dan penambah aroma pada masakan. Namun, berdasarkan hasil analisis secara farmakologis ditemukan bahwa hampir semua bagian dari tumbuhan tersebut memiliki khasiat sebagai obat. Akar seledri berkhasiat sebagai peluruh kencing (diuretik) dan memacu enzim pencernaan (skomakik). Biji dan buahnya berkhasiat sebagai pereda kejang (antispasmodik), menurunkan kadar asam urat darah, antirematik, peluruh kencing (karminatif), perangsang (afrodisiak), dan penenang (sedatif). Sedangkan herba seledri tonik, skomakik, menurunkan tekanan darah (hipotensif), pembersih darah, memperbaiki fungsi hormon yang terganggu, mengeluarkan asam urat yang tinggi (Dalimartha 2000). Tanaman seledri dapat tumbuh dengan baik apabila didukung dengan proses budidaya yang baik pula. Semua kondisi yang menjadi faktor tumbuhnya akan menentukan keberhasilan dalam proses budidaya tersebut. Faktor-faktor tersebut antara lain tanah, iklim, dan gangguan terhadap hama dan penyakit. Selain dari faktor -faktor tersebut, perlu diperhatikan pula cara bercocok tanam yang tepat. Bercocok tanam seledri meliputi pengolahan tanah, pembibitan, penanaman, pemeliharaan, dan pemungutan hasil (Soewito 1989).
Bagian dari tanaman seledri, seperti herba, akar, dan biji memiliki beragam kandungan kimia. Senyawa-senyawa tersebut ada yang terlibat langsung dalam metabolisme, yaitu sebagai metabolit primer, bahkan senyawa metabolit sekunder. Aktivitas bercocok tanam para petani yang berbeda dapat mempengaruhi kadar senyawa-senyawa kimia tersebut. Diosmin merupakan kelompok senyawa flavonoid yang terdapat pada tanaman seledri dan memiliki aktifitas sebagai antiinflamasi (Damon et al 1987, diacu dalam Fitriyeni 2003). Sintesis senyawa flavonoid, seperti diosmin, memerlukan peranan dari suatu protein, yaitu enzim, sehingga perbedaan kadar diosmin pada tanaman seledri akan mempengaruhi konsentrasi total serta pola protein dari tanaman tersebut.
Penentuan pola protein dengan menggunakan metode elektroforesis sudah banyak digunakan sebagai metode yang ampuh untuk mengidentifikasi varietas, kultivar, atau klon dari berbagai jenis tanaman (Kuhns dan Fretz 1978). Berdasarkan penelitian sebelumnya bahwa kadar metabolit sekunder pada tanaman seledri yang ditanam pada lingkungan yang berbeda serta lingkungan yang tidak mendukung akan menghasilkan metabolit sekunder dalam jumlah berbeda (Nuhidayah, Sya’bana, Iswadi 2005). Dari laporan tersebut, penulis ingin mengetahui apakah cara bercocok tanam yang pada dua daerah yang berbeda akan memberikan pengaruh terhadap kadar diosmin dan pola protein yang berbeda pula.
Penelitian ini bertujuan untuk membandingkan kadar diosmin serta pola protein tanaman seledri pada dua daerah yang berbeda, yaitu Cipanas dan Ciwidey. Manfaat dari penelitian ini yaitu memberikan informasi kepada masyarakat bahwa sayuran yang biasa digunakan sehari-hari berkhasiat farmakologis.
TINJAUAN PUSTAKA
Tanaman Seledri
(Apium graveolens L.)
merupakan tanaman biennial, tetapi dapat dipanen dalam setahun (annual) untuk diambil bagian vegetatifnya. Siklus hidupnya dapat diselesaikan setahun apabila tanaman tersebut selama masa perkembangannya berada pada temperatur yang rendah. Masa panennya tergantung dari tipe, kultivar, dan permintaan pasar, tetapi bervariasi dari 2-3 bulan (Siemonsma dan Pileuk 1994). Tanaman seledri juga dapat tumbuh pada dataran rendah, tetapi batang yang dihasilkan lebih kecil daripada yang ditanam pada dataran tinggi (Soewito 1989).
Seledri merupakan keluarga umbelliferae dan satu keluarga dengan wortel, piterseli, ketumbar, dan mitsuba, serta termasuk genus apium dan spesies Apium graveolens L. (Reginawanti 1999). Berdasarkan bentu k (habitus) pohonnya, tanaman seledri dapat dibagi menjadi tiga golongan, yaitu seledri daun, seledri potong, dan seledri umbi.
Seledri daun (A. graveolus L.
Var.secalinum Alef.) Merupakan seledri yang
banyak ditanam di Indonesia. Tumbuh pada tanah agak kering dan dipanen pada bagian daunnya atau batangnya saja. Cara memanennya dengan langsung mencabutnya. Seledri potong (A. graveolus L. var. sylvestre
Alef.) tumbuh pada pasir atau kerikil yang banyak airnya, tetapi tidak menggenang. Dipanen bagian batangnya saja dan dengan cara memotong pada pangkal batangnya. Seledri umbi (A. graveolus L. var. rapaceum
Alef.) Batang seledri berumbi sehingga membengkak membentuk umbi. Dipanen bagian daunnya dan dengan cara memetik daunnya saja(Sunarjono 2003) .
Gambar 1 Tanaman Seledri (Apium
graveolens L.)
Syarat penting tumbuhnya seledri antara lain tanahnya banyak mengandung humus
(subur), gembur, mengandung garam dan mineral, kandungan bahan organik tinggi, berdrainase baik, tekstur lempung berpasir atau lempung berdebu, serta kisaran pH 5.5-6.5 (Reginawanti 1999 dan Sunarjono 2003). Seledri memerlukan suhu 9-20? C untuk berkecambah dan untuk pertumbuhan selanjutnya diperlukan suhu antara 15-24? C. Curah hujan optimum berkisar 60-100 mm/bulan dan kelembapannya berkisar 80-90% (Soewito 1989). Jika tanaman kekurangan natrium akan menjadi kerdil, kekurangan kalsium menyebabkan kuncup seledri menjadi kering, dan apabila kekurangan unsur boron menyebabkan batang dan tangkainya menjadi retak -retak (Sunarjono 2003).
Budidaya Tanaman Seledri
(Apium graveolens L.)
Perhatian yang khusus perlu diberikan terhadap usaha budidaya tanaman seledri, hal ini bertujuan agar produk yang dihasilkannya dapat maksimal. Para petani seledri juga harus dibekali dengan dasar usaha bertanam seledri yang meliputi pengolahan tanah, pembibitan, penanaman, pemeliharaan, dan pemungutan hasil (Sunarjono 2003).
Tanah merupakan tempat tumbuh bagi tumbuhan, karena tanah menyediakan unsur-unsur hara yang diperlukan bagi tumbuhan maka tanah memiliki peranan yang penting bagi keberhasilan pertumbuhan. Dibutuhkan kondisi tanah tertentu bagi pertumbuhan tanaman seledri, hal ini tergantung pada jenis tanaman seledri yang ditanam. Seledri daun merupakan jenis seledri yang paling bany ak ditanam di Indonesia. Jenis tanaman ini lebih suka tumbuh pada tanah yang agak kering, gembur, dan subur. Lahan tanah sebelum ditanami oleh bibit seledri, harus diolah terlebih dahulu. Kegiatan tersebut antara lain meliputi menggemburkan tanah, membuat bedengan, memupuk, serta meratakan tanah (Soewito1989).
Tanaman seledri menyukai tanah yang lembut (tidak keras), sehingga sebelum ditanami tanahnya harus digemburkan terlebih dahulu. Jenis tanaman seledri daun, karena tidak menyukai tanah yang basah, memerlukan bedengan yang berfungsi untuk mencegah agar tanaman tidak sampai tergenang oleh air terutama pada musim hujan. (Soewito 1989).
dengan membungkus biji tersebut menggunakan kain basah selama 24 jam. Penyemaian merupakan tempat untuk menumbuhkan biji seledri hingga menjadi benih dan kemudian ditanam pada lahan. Benih seledri dipindahkan ke lahan kurang lebih mencapai umur satu bulan (berdaun 3-5 helai) (Sunarjono 2003). Biji seledri dapat langsung ditabur pada lahan tanah, selain disemai, teta[i harus dibuat alur terlebih dahulu supaya dapat tumbuh teratur. Penebaran biji secara langsung rentan menimbulkan resiko daripada penyemaian. Resiko tersebut antara lain biji dapat hanyut apabila tersiram air hujan dan biji akan kekeringan apabila ditanam pada musim kemarau sehingga untuk melindungi biji dari resiko tersebut maka harus ditutup dengan jerami atau alang-alang (Soewito 1989). Biji seledri yang tumbuh kemudian memerlukan upaya pemeliharaan sebaik-sebaiknya agar diperoleh hasil yang maksimal. Upaya -upaya tersebut meliputi penyiraman, penyulaman, penjarangan, pendangiran, pemupukan, serta pembasmian hama dan penyakit. Penyiraman dilakukan sejak biji disemai atau ditabur sampai tanaman akan dipetik hasilnya karena tanaman seledri yang kekurangan air akan tumbuh kerdil, namun apabila curah hujan tinggi maka penyiraman tidak perlu dilakukan. Penyulaman dilakukan pada tanaman seledri yang berasal dari biji yang disemai dengan cara mencabut tanaman yang mati dan layu untuk diganti dengan bibit yang baru. Pada biji yang langsung ditabur pada lahan tanah tumbuhnya akan rapat sekali, untuk mengurangi banyaknya tanaman yang mati dan layu karena bersaing untuk memperoleh nutrisi maka dilakukan penjarangan. Ruang lahan antara tanaman seledri yang ditanam, baik dengan penyemaian maupun ditabur langsung pada lahan, akan ditumbuhi oleh rumput-rumput liar yang dapat mengganggu keberhasilan produk tanaman seledri. Rumput-rumput liar yang tumbuh harus dibersihkan untuk mengurangi resiko tersebut melalui upaya pemeliharaan, yaitu pendangiran. Selain untuk tujuan tersebut, pendangiran juga berfungsi untuk menggemburkan tanah disekitar tanaman.
Tumbuhan juga membutuhkan unsur hara sebagai asupan makanan untuk hidup, tumbuh, dan berkembang. Unsur hara yang terkandung di dalam tanah sehingga tidak mencukupi atau bahkan tidak ada maka kekurangannya dapat diperoleh melalui pupuk (Marsono & Sigit 2004). Menurut Novizan
(2002), pupuk didefinisikan sebagai material yang ditambahkan ke dalam tanah atau tajuk tanaman dengan tujuan untuk melengkapi unsur hara. Tanaman seledri, secara aplikasinya, menggunakan jenis pupuk organik dan anorganik. Pupuk organik yang digunakan adalah pupuk kandang dan kompos, sedangkan pupuk anorganik yang digunakan antara lain urea, SP-36, KCl, ZA, NPK (Novizan 2002 dan Marsono & Sigit 2004).
Kegagalan dalam bercocok tanam seledri disebabkan karena adanya serangan hama atau penyakit. Hama yang menyerang tanaman ini biasanya sejenis ulat daun (Agrotis ypsilon Hufn.), kutu-kutu daun (Aphis spp.), tungau/mites (Tetranychus spp.), dan cacing nematoda. Penyakit yang biasa menyerang tanaman seledri adalah cacar coklat kuning
(Cercospora apii), cacar hitam (Septoriaapii),
virus aster yellow, dan nematoda akar
(Belonalaimus gracilis, Heterodera schactii,
Bacillus gracilis) (Reginawanti 1999).
Kegiatan terakhir yang dilakukan dalam usaha bercocok tanam adalah pemetikan hasil. Tanaman seledri dapat dipanen pada saat 2-3 bulan dari saat penyebaran biji. Cara pemetikan hasil dilakukan tergantung dari jenis seledri yang ditanam. Pemetikan hasil dengan cara mencabut tanamannya dilakukan pada jenis seledri daun. Jenis seledri batang, dilakukan dengan memotong pangkal batangnya, sedangkan jenis seledri umbi dengan cara memetik daun-daunnya saja (Soewito 1989 dan Sunarjono 2003).
yaitu suplai dari fase padat, pH tanah, dan suplai air (Blair 1979).
Perbedaan lokasi budidaya tanaman seledri menyebabkan cara budidaya, kondisi tanah, ketinggian tempat, suhu, dan curah hujan yang berbeda sehingga kandungan senyawa yang dikandungnya juga berbeda, termasuk senyawa metabolit sekunder.
Khasiat Tanaman Seledri
Hampir semua bagian dari tanaman seledri memiliki khasiat sebagai obat. Menurut Dalimartha (2000), akar seledri berkhasiat stomakik dan diuretik, sedangkan buah dan bijinya berkhasiat sebagai antispasmodik, menurunkan kadar asam urat darah, antirematik, diuretik, karminatif, afrosidisiak, dan sedatif. Herba seledri yang memiliki rasa manis, berbau aromatik, sedikit pedas, dan sifatnya sejuk, berkhasiat sebagai tonik, stomakik, hipotensif, penghenti pendarahan (hemostatis), diuretik, peluruh haid, karminatif, mengeluarkan asam urat darah yang tinggi, pembersih darah, memperbaiki fungsi hormon yang terganggu. Nasution (1995) telah melakukan uji farmakologis antiinflamasi tanaman seledri terhadap tikus dan menyatakan bahwa tanaman seledri juga dapat digunakan sebagai antiinflamsi. Hal senada juga dibuktikan oleh Sya’bana (2005), Nuhidayah (2005), dan Martaningtyas (2005) yang menyatakan bahwa seledri berkhasiat sebagai antiinflamasi dan senyawa yang berperan sebagai antiinflamasi adalah diosmin.
Kandungan Senyawa Kimia Tanaman Seledri
Kandungan herba seledri tiap 100 g berisi 93 ml air, 0.9 g protein, 0.1 g lemak, 4 g karbohidrat, 0.9 g serat, 1.7 g abu, 130 IU vitamin A, 0.08 mg vitamin B1, 0.12 mg vitamin B2, 0,6 mg niacin, 15 mg vitamin C, 50 mg Ca, 40 mg P, 1 mg Fe, 151 mg Na, 85 g Mg, dan 400 mg K. Nilai energinya adalah 113 kJ/100 g (Dalimartha 2000). Seledri juga mengandung glukosida apiin, flavonoid, saponin, tanin, apigenin, minyak atsiri, kolin, lipase, asparaginase, tirosin, glutamin, serta diosmin (Siesonsma 1994, Sya’bana 2005, Nurhidayah 2005, dan Martaningtyas 2005). Berdasarkan penelitian Martaningtyas (2005), seledri kering menghasilkan kadar diosmin sebesar 54.50 % atau 5711.64 ppm, sedangkan menurut Nurhidayah (2005), tanaman seledri pada umur 10 minggu dengan penambahan NaCl 4000 ppm menghasilkan kadar diosmin sebesar 2.12. 10-3 % atau 423.38 ppm.
Diosmin
Tanaman menghasilkan metabolit yang berasal dari proses metabolisme primer dan metabolisme sekunder selama pertumbuhan. Hasil metabolisme primer adalah senyawa kimia yang digunakan untuk pertumbuhan seperti karbohidrat, protein, lemak, sitokrom dan klorofil. Senyawa-senyawa tersebut berada dalam jumlah besar pada tanaman. Senyawa kimia yang termasuk metabolit sekunder antara lain kelompok senyawa alkaloid, terpenoid, dan flavonoid. Metabolit tersebut tidak digunakan bagi pertumbuhan tanaman, misalnya flavonoid, tetapi berperan sebagai pertahanan terhadap mikroorganisme patogen dan juga terhadap herbivora maupun omnivora, selain itu sebagai pelindung dari efek sinar ultraviolet yang merusak (Heldt 1997 dan Salisbury & Ross 1995). Peranannya tersebut menyebabkan metabolit sekunder banyak dihasilkan di tanaman saat kondisi lingkungan pertumbuhannya tidak optimal atau pada saat ada ancaman yang mengancam pertumbuhannya.
Diosmin termasuk kelompok senyawa flavonoid dan secara kimia didefinisikan sebagai senyawa 5,7,3’ -trihidroksi-4’metoksiflavon-7-rutinosida (shafae & El-Domiaty 2001). Lonchampt et al (1989 dalam Fitriyeni 2003) membuktikan bahwa tablet Daflon (S-5682 ) yang mengandung 90% diosmin memiliki aktifitas antiinflamasi pada konsentrasi 2.10-8 mol/L dan 2.10-4 mol/L. Hasil ini membuktikan bahwa tablet tersebut memiliki aktivitas farmakologis terhadap hipermeabilitas membran, selain itu juga memiliki aktivitas antiinflamasi dan antideomatus. Hal senada juga dibuktikan melalui penelitian Damon et al (1987 dalam Fitriyeni 2003) bahwa tablet Daflon 500 mg memiliki aktivitas antiinflamasi pada granula tikus melalui penghambatan sintesis prostaglandin E2 (78,5%), prostaglandin F2 alfa (45,2%), dan tromboksan B2 (59%).
Analisis Diosmin dengan Kromatografi Cair Kinerja Tinggi
Ekstraksi diosmin dilakukan dengan cara refluks menggunakan pelarut 10% DMSO dalam metanol, hal ini berdasarkan penelitian yang telah dilakukan sebelumnya oleh El -Shafae dan El-Domiaty (2001) serta Fitriyeni (2003). Dimetil Sulfoksida (DMSO) merupakan pelarut yang bersifat polar
(www.chemicalland21.com), sehingga
diharapkan hanya senyawa yang bersifat polar yang terekstrak dalam pelarut. Salah satunya adalah flavonoid (Harborne 1987) dan diosmin merupakan salah satu senyawa flavonoid. (Martaningtyas 2005). DMSO juga merupakan pelarut yang biasa digunakan dalam ekstraksi terapetik (obat-obatan alam) sejak tahun 1963 (Jacob 2000).
Kromatografi Cair Kinerja Tinggi digunakan untuk mikroanalisis kuantitatif dan memiliki kepekaan yang tinggi terhadap analisis komponen flavonoid dalam campuran. Hal ini disebabkan kolom terbuat dari bahan kemasan dengan partikel berukuran kecil sehingga untuk mendapatkan laju alir yang memadai digunakan tekanan yang tinggi, sehingga metode ini dapat digunakan untuk mengidentifikasi dan mengetahui kadar diosmin secara kuantitatif. Namun sebagai analisis pendahuluan dilakukan Kromatografi Lapis Tipis (KLT) yaitu untuk mengidentifikasi secara kualitatif apakah pada ekstrak seledri mengandung diosmin atau tidak. KLT bertujuan membandingkan hasil sampel ekstrak seledri dengan standar diosmin dan pengukurannya berdasarkan perbandingan nilai Rf (Gritter et al 1991). (Hamilton dan Swel 1982). Analisis KCKT pada penelitian ini menggunakan metode fase terbalik, yaitu fase gerak yang digunakan bersifat polar (metanol) dan fase stasioner bersifat non polar. Keunggulan metode ini antara lain pengoperasian yang mudah, mempunyai efisiensi tinggi, stabilitas kolom, dan kemampuan untuk menganalisis secara simultan dengan spektrum yang luas (Krstulovic & Brown 1982).
Protein Tanaman Seledri
Tumbuhan mengandung ribuan protein yang beraneka ragam dengan berbagai macam fungsi. Fungsi protein pada tumbuhan antara lain katalisator, struktural, transpor, dan penyimpanan. Protein terdiri dari satu atau lebih rantai polipeptida yang masing-masing terdiri atas ratusan asam amino. Komposisi dan bobot molekul protein tergantung pada
jenis dan jumlah subunit asam amino (Salisbury dan Ross 1995).
Penelitian yang dilakukan oleh Noiraud, Maurousset, dan Lemoine (2001), menunjukkan bahwa floem pada tanaman seledri memiliki gen yang mengekspresikan transporter manitol, AgMaT1, dengan bobot molekul 56 kDa, selain itu penelitian yang dilakukan oleh Dinant et al (2003) menunjukkan bahwa floem pada tanaman seledri juga terdapat dua jenis gen yang mengekspresikan protein floem 2 (PP2), yaitu AgPP2-1 dan AgPP2-1 dengan masing-masing bobot molekul 19.8 dan 19.7 kDa.
Analisis Pola Protein dengan Elektroforesis Gel Poliakrilamid SDS (SDS PAGE)
Biosintesis senyawa metabolit sekunder, dalam hal ini diosmin yang termasuk ke dalam flavonoid, melibatkan protein, yaitu enzim, dan suatu prekursor melalui serangkaian jalur reaksi yang dikontrol secar a ketat terutama untuk enzim kuncinya. Untuk mengetahui enzim yang dapat mensintesis senyawa diosmin, terlebih dahulu harus diketahui bobot molekul dari protein yang terdapat pada sampel ekstrak seledri, sehingga analisis pola protein merupakan langkah awal yang perlu dilakukan. Kedua daerah yang dianalisis kemungkinan memiliki kandungan senyawa diosmin yang berbeda, sehingga pola protein yang diperoleh kemungkinan juga akan berbeda. Salah satu teknis yang digunakan untuk melihat pola protein dan menentukan bobot molekulnya menggunakan SDS PAGE. Prinsip dari elektroforesis adalah pergerakan suatu molekul bermuatan di dalam medan listrik (Stryer 1995). Pada elektroforesis gel poliakrilamid pergerakan protein, merupakan respon terhadap medan listrik, terjadi melalui pori di dalam matriks gel yang ukuran porinya dipengaruhi oleh konsentrasi akrilamid. Elektoforesis, sesuai dengan prinsip tersebut, dapat digunakan untuk memisahkan campuran kompleks protein, memeriksa komposisi subunit, mengetahui keseragaman pada sampel protein, serta untuk memurnikan protein yang akan dianalisis. Laju pergerakan protein ditentukan oleh kombinasi antara ukuran pori gel dan muatan, ukuran, serta bentuk protein (Coligan et al 1995).
mengurangi perubahan arus listrik yang terjadi sehingga pemisahan menjadi lebih efektif. Selain itu, gel juga bertindak sebagai saringan yang dapat meningkatkan daya pisah (Stryer 1995). Gel terbentuk melalui pencampuran larutan akrilamid dengan amonium persulfat dan TEMED (N, N, N’, N’-tetrametil etilendiamin), sehingga mengakibatkan monomer akrilamid mengalami polimerisasi. Penambahan senyawa N,N’- metilen bisakrilamid dalam proses polimerisasi membentuk penyilangan antar rantai panjang sehingga akan membentuk gel dengan tingkat porositas yang ditentukan oleh panjang rantai dan derajat penyilangan antar rantai (Muladno 2002). Sodium Dedosil Sulfat (SDS) merupakan deterjen anionik yang dapat bereaksi dengan bagian hidrofobik protein sehingga membentuk kompleks bermuatan negatif, akibatnya pada daerah yang bermuatan listrik protein akan bergerak ke muatan positif (Styer 1995 dan Waterborg dan Matthews 1984).
Tahapan kerja elektroforesis gel poliakrilamid SDS secara singkat adalah (1) Preparasi sampel menggunakan zat warna, (2) Persiapan stacking dan running gel (3) Memasukkan sampel ke dalam sumur gel, (4) Running SDS PAGE, (5) Visualisasi menggunakan coomasie blue, (6) Pencucian (Mamajis molecular kicthen 2000).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah DMSO, standar diosmin, N -butanol, asam asetat, akrilamid, N’, N’-bismetilen akrilamid, Tris-HCl 0.1 M, EDTA 1mM, merkaptoetanol 5mM, akuades, Tris base, 10% w/v amonium persulfat, TEMED, glisin, SDS, gliserol, 0.05% bromfenol biru, metanol (MeOH), asam asetat glasial, coomasie biru R 250, Na2CO3, CuSO4 1.5%, HCl pekat, pereaksi
Folin Ciocalteus, 2.5 M sukrosa, PVP, 2 mg/ml Bovine Serum Albumin, nitrogen cair, aseton, daun seledri yang berasal dari daerah Cipanas dan Ciwidey dan berumur 4, 6, dan 8 minggu.
Alat-alat yang digunakan ialah KCKT, lempeng silika gel GF254, lampu UV,
spektrofotometer, pH meter, autoklaf, pengaduk magnet, oven, alat -alat elektroforesis, erlenmeyer, labu takar, autopipet, neraca analitik, pipet tetes, sentrifus, serta alat-alat gelas lainnya.
Metode
Uji Pendahuluan
Penetuan Kadar Air
Botol timbang dicuci lalu dikeringkan dalam oven pada suhu 105?C selama 30 menit kemudian didinginkan dalam eksikator dan ditimbang. Sebanyak ± 2 gram sampel ditimbang dan dimasukkan ke dalam botol timbang dan dikeringkan dalam oven pada suhu 105?C sampai diperoleh bobot tetap (Martaningtyas 2005). Setelah didinginkan dalam eksikator ditimbang dengan neraca analitik, pekerjaan tersebut diulang tiga kali. Persamaan untuk menghitung kadar air :
Kadar air = (a-b)/a x 100%
a : Bobot bahan sebelum dikeringkan b : Bobot setelah dikeringkan
Penentuan Kadar Abu
Cawan porselin dicuci kemudian dikeringkan dalam tanur pada suhu 600?C selama 30 menit lalu didinginkan dalam ekstikator dan ditimbang. Sampel sebanyak ± 2 gram ditimbang lalu dimasukkan ke dalam cawan dandipanaskan dalam tanur pada suhu 600?C sampai sampel menjadi abu (± 60 menit). Setelah itu didinginkan dalam eksikator dan ditimbang dengan analitik, pekerjaan tersebut diulang sebanyak tiga kali. Persamaan untuk menghitung kadar abu :
Kadar abu = a/b x 100% a : Bobot abu sampel b : Bobot sampel
Analisis Tanah
Sampeltanah yang diambil sebanyak ± 10 gram dari daerah Cipanas dan Ciwidey kemdian analisis dilakukan di laboraturium tanah Fakultas Pertanian IPB Darmaga. Analisis ini betujuan untuk mengetahui kandungan hara makro (C, N, P, K), hara mikro (Ca, Mg, Na), dan pH tanah secara kuantitatif.
Penentuan Bobot Basah
Seluruh bagian tanaman seledri (daun, batang, dan akar) segar ditimbang menggunakan neraca kasar.
Ekstraksi Protein dari Tanaman Seledri
digerus, daun tersebut dihomogenkan dalam 20 ml bufer ekstraksi (lampiran 2), lalu disentrifugasi pada kecepatan 12.000 rpm selama 15 menit. Supernatan dipisahkan sebagai contoh yang akan dianalisis.
Penentuan Konsentrasi Protein Total Hasil Ekstraksi dengan Metode Lowry
Pembuatan Larutan Standar
Campuran larutan standar terdiri atas Bovine Serum Albumin (BSA) dengan konsentrasi 0, 20, 40, 60, 80, dan 100, kemudian ditambahkan dengan akuades dan pereaksi C yang dikocok serta didiamkan selama 10 menit, kemudian ditambahkan pereaksi D. Campuran tersebut dikocok dan didiamkan selama 30 menit, lalu diukur absorbansinya dengan panjang gelombang 742 nm. Selanjutnya, dibuat kurva standar hubungan antara absorban dan konsentrasi protein. Bahan -bahan pereaksi untuk metode Lowry dapat dilihat pada lampiran 3 (Watterborg & Matthews 1984).
Pengukuran Konsentrasi Protein
Sebanyak 1 ml sampel dimasukkan ke dalam tabung reaksi, kemudian ke dalam masing-masing tabung dimasukkan pereak si C sebanyak 5 ml, lalu dikocok dan didiamkan selama 10 menit. Selanjutnya, pereaksi D ditambahkan sebanyak 0,5 ml pada masing-masing tabung, lalu dikocok dan didiamkan selama 30 menit. Absorbansi dengan panjang gelombang 742 nm dan konsentrasi protein diukur berdasarkan kurva standar (Watterborg & Matthews 1984).
Analisis Diosmin Tanaman Seledri
Ekstraksi Diosmin dari Tanaman Seledri
Metode ini menggunakan metode El-Shafae dan El-Domiaty (2001). Sebanyak 10 g seledri segar direfluks dengan 50 ml DMSO 10% dalam metanol selama 30 menit dan dilakukan 3x. Kemudian ekstrak disaring, dikumpulkan, dipekatkan dengan rotavapor, dihitung besar rendemen, dan ditepatkan volumenya menjadi 100 ml dengan metanol. Larutan ini digunakan dalam preparasi larutan standar diosmin yang akan diinjeksikan ke dalam kolom KCKT. Sistem KCKT yang digunakan adalah sistem fase terbalik, dengan fase mobil bersifat polar dan fase stasioner bersifat nonpolar. Fase mobil yang digunakan adalah metanol (MeOH) 50% sedangkan fase stationer yang digunakan adalah kolom LiChrosorb RP-18 (Fitriyeni 2003).
Rendemen =
Bobot sampel setelah perlakuan x 100 % Bobot sampel sebelum perlakuan
Preparasi Larutan Stok Standar
Larutan stok standar diosmin dibuat dengan menimbang sebanyak 0.025 g standar diosmin kemudian dilarutkan di dalam DMSO 10% hingga volume 50 ml. Konsentrasi larutan stok standar yang diperoleh adalah 500 ppm (Fitriyeni 2003).
Preparasi Larutan Standar
Larutan standar dibuat dengan mengencerkan larutan stok standar sehingga diperoleh konsentrasi untuk kurva standar 10, 25, 50, 75, dan 100 ppm. Pelarut yang digunakan untuk pengenceran adalah MeOH 50% (Fitriyeni 2003)
Preparasi Sampel
Ekstrak sampel yang telah dipekatkan dengan rotavapor ditera menjadi 100 ml dengan metanol, kemudian diambil 1 ml dan diencerkan dengan MeOH sehingga mencapai volume 10 ml (Fitriyeni 2003).
Identifikasi Diosmin dengan KLT
Ekstrak sampel ditotolkan pada lempeng silika gel GF245 sebagai fase diam dan sebagai
fase gerak digunakan fase at as dari N -butanol : asam asetat : akuades (4 : 5 : 1)
Pengukuran Kadar Diosmin dengan KCKT
Sebanyak 10 µl larutan standar atau sampel
diinjeksikan ke dalam kolom KCKT dengan fase stationer kolom LiChrosorb RP-18 dan dielusi dengan menggunakan fase mobil yaitu metanol 50%. Deteksi dilakukan menggunakan detektor UV pada panjang gelombang 345 nm (Fitriyeni 2003).
Perhitungan Konsentrasi Diosmin
Konsentrasi diosmin pada sampel dihitung menggunakan kurva standar yang menunjukkan hubungan antara konsentrasi standar diosmin dan luas area.
Analisis Pola Protein dengan SDS PAGE
Elektroforesis protein dilakukan berdasarkan metode Laemmli (dalam Coligan
et al 1995). Gel poliakrilamid dicetak di
pisah 10% (lampiran 5) yang telah disiapkan dimasukkan ke dalam cetakan gel dengan menggunakan mikro pipet sampai batas tertentu, kemudian ditambahkan dengan akuades sampai penuh agar permukaan gel rata. Setelah gel mengering, akuades dibuang dan sisa air pada cetakan gel diserap dengan kertas saring. Kemudian larutan gel tumpuk (lampiran 5) yang telah dibuat dimasukkan ke dalam cetakan dan dipermukaan gel dipasang sisir berlubang lalu didiamkan sampai mengeras. Setelah gel mengeras, cetakan gel dipindahkan ke perangkat elektroforesis. Preparasi sampel dilakukan dengan memasukkan sampel yang telah disiapkan ke dalam tabung kemudian ditambahkan bufer sampel dengan perbandingan 1 :1 dan dipanaskan pada suhu 100? C selama 5 menit.
Sampel dimasukkan ke dalam sumur yang telah dicetak pada gel poliakrilamid sebanyak 15 µl, kemudian alat elektroforesis diberi tegangan 200 volt sampai pewarna mencapai ujung gel.
Visualisasi gel menggunakan coomasie biru dilakukan setelah gel dilepaskan dari cetakan, kemudian direndam di dalam larutan pewarna coomasie biru selama semalam dan digoyangkan dengan alat penggoyang. Selanjutnya, gel dicuci sebanyak dua kali dengan menggunakan larutan dekolorisasi masing-masing selama 15 menit. Setelah pita terlihat, gel dicuci dengan akuades.
Identifikasi dan analisis Pola SDS PAGE membandingkan antara pita protein yang telah dipisahkan sebelumnya dengan protein standar. Bobot molekul dari masing-masing protein ditentukan dengan cara menghitung nilai Rf dari masing-masing pita prot ein yang nampak, kemudian dibuat kurva standar hubungan antara log BM dengan Rf dari protein standar sehingga nilai BM protein dapat dihitung.
Rf = jarak pergerakan pita protein dari tempat awal (cm)
jarak pergerakan pewarna protein standar dari tempat awal (cm)
Analisis Statistik
Percobaan disusun dengan menggunakan Rancangan Acak Kelompok dua faktor. Faktor yang pertama (A) merupakan daerah budidaya yang terdiri atas dua taraf, yaitu
A0 = daerah Cipanas
A1 = daerah Ciwidey
Faktor yang kedua (B) merupakan masa tanam yang terdiri atas tiga taraf, yaitu
B0 = 4 minggu
B1 = 6 minggu
B2 = 8 minggu
Masing-masing masa tanam dilakukan pengulangan sebanyak tiga kali.
Model umum dari rancangan tersebut adalah (Mattjik & Sumertajaya 2002):
Yi j k = µ + a i + ßj + (aß)ij + eijk i = 1,2 ; j = 1,2,3 ; k = 1,2,3 dengan :
Yijk : pengaruh diosmin pada lokasi taraf ke-i
dalam waktu ke -j dan ulangan ke-k µ : rataan umum
ai : pengaruh tambahan yang t imbul pada
kadar diosmin akibat lokasi ke-k ßj : pengaruh tambahan yang timbul pada
kadar diosmin akibat waktu ke-j (aß)ij : interaksi antara faktor lokasi taraf ke
dan waktu ke-j
HASIL DAN PEMBAHASAN
Analisis Tanah
Analisis tanah menunjukkan bahwa pH tanah yang berasal dari Cipanas dan Ciwidey sebesar 5.11. dan 4.92. Kondisi tersebut kurang optimum bagi pertumbuhan seledri karena pH tanah yang optimum sebesar 5.5-6.5 (Reginawanti 1999 dan Sunarjono 2003). Walaupun dapat tumbuh pada kondisi tanah Cipanas dan Ciwidey, tetapi kualitas dan kuantitas tanaman yang dihasilkan tidak maksimum. Hasil yang maksimum dapat diperoleh melalui usaha lebih, seperti pemupukan unsur hara (N, P, K) serta pengapuran. Usaha ini bertujuan untuk melengkapi unsur hara dalam jumlah rendah. Berdasarkan klasifikasi dari Balai Penelitian Tanaman Rempah dan Obat (lampiran 8), kadar C organik pada tanah yang berasal dari Cipanas adalah tinggi, sedangkan kadar N total, K, dan Na sedang. Kadar Ca dan Mg rendah. Pada tanah yang berasal dari Ciwidey, kadar C organik sedang, sedangkan kadar N, Ca, Mg, K, dan Na rendah. Kadar P dan kejenuhan basa (KB) pada kedua jenis tanah sangat rendah (Lampiran 7).
Bobot Basah
dan 265.39 gram, sedangkan pada daerah Cipanas berturut-turut sebesar 50.25, 97.64, 168.56 gram (Gambar 3). Penambahan masa tanam pada kedua daerah meningkatkan bobot basah tanaman seledri.
Penelitian yang dilakukan oleh Hermawan (2005), menunjukkan bahwa perlakuan dengan pemberian pupuk nitrogen berpengaruh nyata terhadap bobot basah tanaman seledri. Nitrogen dibutuhkan dalam jumlah relatif besar pada setiap tahap pertumbuhan tanaman, terutama pertumbuhan vegetatif (perbanyakan melalui pembentukan tunas baru), sehingga pemberian kadar pupuk yang berbeda pada kedua daerah akan mempengaruhi biomassa tanaman seledri yang dihasilkan. Kebutuhan terhad ap nutrisi, terutama nitrogen, pada tanaman seledri dapat dipenuhi melalui pemberian pupuk NPK dan urea. Kedua jenis pupuk tersebut umum digunakan para petani pada budidaya tanaman seledri. Petani di daerah Ciwidey memberikan pupuk urea dan NPK masing-masing sebanyak 8 kg/400 m2, sedangkan petani di daerah Cipanas hanya memberikan pupuk urea sebanyak 5 kg/400 m2. Suplai nitrogen yang cukup ditunjukkan melalui aktivitas fotosintesis yang tinggi, pertumbuhan vegetatif yang baik, dan warna daun yang hijau tua (Tisdale et al 1985).
0 50 100 150 200 250 300
4 6 8
Masa tanam (minggu)
Bobot basah (gram)
Seledri Cipanas Seledri Ciwidey
Gambar 3 Bobot basah tanaman seledri daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu
Kadar Air dan Kadar Abu
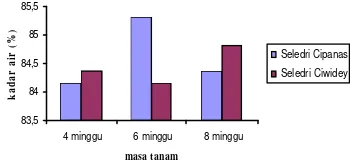
Budidaya tanaman seledri pada daerah Cipanas dan Ciwidey dengan menggunakan perlakuan masa tanam (4, 6, dan 8 minggu), berdasarkan analisis statistik kadar air, menunjukkan hasil yang tidak berbeda nyata dengan p= 0.7120. Tanaman seledri yang ditanam pada daerah Ciwidey dengan masa tanam 4 dan 8 minggu menunjukkan kadar air yang lebih tinggi daripada daerah Cipanas (Gambar 4), yaitu sebesar 84.38 % dan 84.83 %, sedangkan kadar air paling tinggi pada
tanaman seledri dengan masa tanam 6 minggu yaitu daerah Cipanas, sebesar 85.31 %. Apabila dihubungkan dengan bobot basah, tanaman seledri daerah Ciwidey memiliki bobot basah yang lebih tinggi daripada daerah Cipanas, sehingga mungkin bagian terbesar dari bobot basah tanaman seledri daerah Ciwidey adalah air. Tanaman seledri yang ditanam pada daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 miggu memiliki kadar air di atas 80 %. Penentuan kadar air bertujuan untuk mengetahui ketahanan terhadap penyimpanan suatu bahan, karena adanya kandungan air dalam suatu bahan merupakan tempat tumbuhnya bakteri dan organisme pengurai lainnya (Martaningtyas 2005).
Hasil analisis statistik kadar abu menunjukkan hasil tidak berbeda nyata dengan nilai p= 0.3415. Hasil kadar abu pada daerah Ciwidey lebih tinggi daripada daerah Cipanas (Gambar 5), nilainya berturut-turut 1.87 %, 1.55 %, dan 1.65 % menunjukkan bahwa tanaman seledri yang ditanam pada daerah Ciwidey memiliki kandungan mineral yang lebih tinggi daripada daerah Cipanas.
83,5 84 84,5 85 85,5
4 minggu 6 minggu 8 minggu
masa tanam
kadar air (%)
Seledri Cipanas Seledri Ciwidey
Gambar 4 Kadar air tanaman seledri daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu
0 0,5 1 1,5 2
4 minggu 6 minggu 8 minggu
Masa Tanam
Kadar Abu (%)
Seledri Cipanas
Seledri Ciwidey
Gambar 5 Kadar abu tanaman seledri daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu
Konsentrasi Protein Total
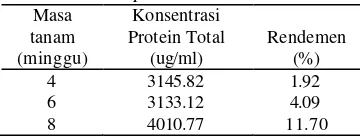
menunjukkan bahwa tanaman seledri dengan masa tanam 6 dan 8 minggu menunjukkan hasil kadar protein yang berbeda nyata. Kadar protein tertinggi diperoleh pada tanaman seledri yang ditanam pada daerah Cipanas dengan masa tanam 8 minggu, sebesar 4010.77 µg/ml, sedangkan kadar protein terkecil pada tanaman seledri daerah Ciwidey dengan masa tanam 6 minggu, yaitu sebesar 2111.60 µg/ ml (Tabel 1 dan Tabel 2). Nilai rendemen yang dihasilkan pada kedua daerah budidaya dengan perbedaan masa tanam, berdasarkan hasil analisis statistik rendemen, menunjukkan hasil yang berbeda nyata sedangkan untuk perbedaan daerah tanam tidak berbeda nyata dengan nilai p= 0.0426. Hasil uji lanjut Duncan menyatakan bahwa rendemen yang dihasilkan pada masa tanam 4 minggu berbeda nyata dengan rendemen pada masa tanam 6 dan 8 minggu. Tanaman seledri pada daerah Cipanas nilai rendemennya meningkat seiring dengan bertambahnya masa tanamnya, yaitu pada saat berumur 4, 6, dan 8 minggu berturut-turut besar rendemen yang dihasilkan adalah 1.92 %, 4.09 %, dan 11.70 %, sedangkan untuk daerah Ciwidey nilai rendemen yang paling tinggi diperoleh pada saat umur 4 minggu sebesar 7.33 %.
Distribusi nitrogen dari daun, terutama daun tua, ke biji atau buah lewat floem merupakan hal yang khas pada tumbuhan herba. Hal tersebut penting untuk menyalurkan nitrogen ke organ pengguna terkuat sehingga mencegah terjadi kekurangan nitrogen di organ tumbuhan. Konsentrasi protein total tanaman seledri daerah Cipanas meningkat seiring dengan penambahan masa tanam, sedangkan tanaman seledri daerah Ciwidey mengalami penurunan konsentrasi protein total. Distribusi nitrogen antar organ di tumbuhan kemungkinan yang menyebabkan perbedaan tersebut, hal tersebut dipengaruhi oleh faktor lingkungan budidaya, seperti pH tanah, suhu, ketinggian tempat, jenis tanah, dan asupan nutrisi yang diberikan. Jumlah konsentrasi protein total sebanding dengan jumlah rendemen ekstrak tanaman seledri.
Tabel 1 Konsentrasi protein total dan rendemen ekstrak tanaman seledri daerah Cipanas Masa tanam (minggu) Konsentrasi Protein Total (ug/ml) Rendemen (%) 4 3145.82 1.92 6 3133.12 4.09 8 4010.77 11.70
Tabel 2 Konsentrasi protein total dan rendemen ekstrak tanaman seledri daerah Ciwidey Masa tanam (minggu) Konsentrasi Protein Total (ug/ml) Rendemen (%) 4 2574.75 7.33 6 2111.60 3.98 8 2216.14 6.76
0 500 1000 1500 2000 2500 3000 3500 4000 4500
4 6 8
Masa Tanam (minggu)
Konsentrasi Protein Total
(ug/ml) 0 2 4 6 8 10 12 14 Rendemen (%)
Gambar 6 Kurva Hubungan antara konsentrasi protein total dan rendemen ekstrak tanaman seledri daerah Cipanas.
Konsentrasi protein (¦ ) dan rendemen ( ?)
0 500 1000 1500 2000 2500 3000
4 6 8
Masa Tanam (minggu)
Konsentrasi Protein Total
(ug/ml) 0 1 2 3 4 5 6 7 8 Rendemen (%)
Gambar 7 Kurva Hubungan antara konsentrasi protein total dan rendemen ekstrak tanaman seledri daerah Ciwidey. Konsentrasi protein (¦ ) dan rendemen ( ?)
Kromatografi Lapis Tipis (KLT)
254 dan 365 nm akan menghasilkan spot berwarna coklat, maka spot dangan Rf ± 0.73 dan warna yang sama diduga adalah diosmin. Penelitian sebelumnya yang dilakukan oleh Martaningtyas (2005), Nurhidayah (2005), dan Sya’bana (2005) menunjukkan Rf standar diosmin sebesar 0.57, 0.64, dan 0.62 dan berdasarkan Martaningtyas (2005) warna standar diosmin yang dihasilkan di bawah sinar UV adalah coklat. Semua hasil KLT, ekstrak tanaman seledri memiliki empat buah spot (Lampiran 13). Banyaknya spot menunjukkan adanya senyawa atau golongan lain yang ikut terekstrak.
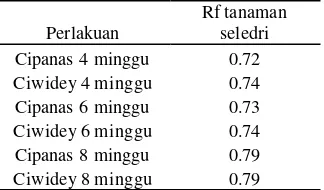
Tabel 3 Hasil rataan KLT ekstrak tanaman seledri
Perlakuan
Rf tanaman seledri Cipanas 4 minggu 0.72 Ciwidey 4 minggu 0.74 Cipanas 6 minggu 0.73 Ciwidey 6 minggu 0.74 Cipanas 8 minggu 0.79 Ciwidey 8 minggu 0.79 Nilai Rf standar diosmin : 0.73
Penentuan Kadar Diosmin
Konsentrasi larutan standar diosmin yang digunakan sebesar 10, 25, 50, 75, dan 100 ppm. Waktu retensi dan luas area konsentrasi standar disajikan pada Tabel 3
T abel 4 Waktu retensi dan luas area konsentrasi standar diosmin
konsentrasi larutan standar diosmin (ppm) Waktu retensi (menit) Luas Area 10 2.45 20931 25 2.42 45394 50 2.38 75922 75 2.36 96880 100 2.31 157439 0 20000 40000 60000 80000 100000 120000 140000 160000 180000
0 20 40 60 80 100 120
Konsentrasi Standar Diosmin (ppm)
Luas Area
y = 5862.19 + 1412.52 x R² = 0.9840
Gambar 8 Kurva standar hubungan antara konsentrasi standar diosmin dan luas area
Lima dari enam sampel yang dianalisis memiliki waktu retensi yang sama dengan standar diosmin. Tabel 4 menunjukkan hasil KCKT dan konsentrasi diosmin ekstrak tanaman seledri dengan perlakuan masa tanam 4, 6, dan 8 minggu.
inilah menyebabkan tanaman seledri pada daerah Cipanas menghasilkan senyawa diosmin lebih banyak untuk p ertahanan dirinya. Respon metabolit sekunder dihasilkan ketika kondisi lingkungan tanaman mengalami cekaman (Nurhidayah 2005).
Tabel 4 Kadar diosmin tanaman seledri daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu
Masa tanam (minggu) Waktu Retensi (menit) Luas Area Kandungan diosmin (ppm) Cipanas
4 2.47 71762 466.55 6 2.42 153734 1046.87 8 2.43 185942 1274.88
Ciwidey
4 2.41 160968 1098.08 6 2.43 12470 46.78 8 2.88 63374 *tt *tt : tidak terdeteksi
Elektroforesis Gel Poliakrolamid SDS
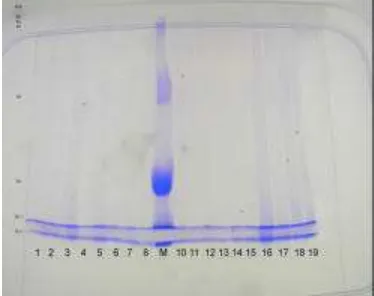
Hasil elektroforesis tanaman seledri pada daerah Cipanas dan Ciwidey dengan ketiga masa tanam yang berbeda menunjukkan adanya dua buah pita protein yang dominan masing-masing dengan bobot molekul 16.6 dan 17.4 kDa. Gambar 7 memperlihatkan pola protein tanaman seledri daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu. Kedua pita protein dengan umur 8 minggu memiliki intensitas ketebalan pita protein lebih tebal daripada umur yang lain. Namun ketebalan pita pada masing-masing umur yang lain tidak menunjukkan perbedaan ketebalan.
Gambar 9 Pola SDS-PAGE protein dari tanaman seledri daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu. No 1-3: Cipanas 4 minggu ulangan 1,
2, dan 3; no 4-6 : Ciwidey 4 minggu ulangan 1, 2, dan 3; no 7-10: Cipanas 6 minggu ulangan 1, 2, dan 3; no 11-13: Ciwidey 6 minggu ulangan 1, 2, dan 3; no 14-16: Cipanas 8 minggu ulangan 1, 2, dan 3; no 17-19: Ciwidey 8 minggu ulangan 1, 2, dan 3.
SIMPULAN DAN SARAN
Simpulan
Tanah pada daerah Cipanas dan Ciwidey memiliki pH sebesar 5.11 dan 4.92, sehingga tanah keduanya tergolong masam. Bobot basah tanaman seledri daerah Cipanas (68.14 gram) berbeda nyata dan lebih rendah daripada daerah Ciwidey (189.46 gram). Kadar air dan kadar abu tanaman seledri daerah Cipanas rata-rata sebesar 84.61 % dan 1.23 %, sedangkan pada daerah Ciwidey sebesar 84.44 % dan 1.59 %. Kadar air dan kadar abu kedua daerah tidak menunjukkan perbedaan secara nyata. Kadar protein pada daerah Cipanas berbeda nyata dengan daerah Ciwidey. Kadar protein daerah Cipanas secara umum mengalami peningkatan pada 4, 6, dan 8 minggu yaitu sebesar 3145.83, 3133.12, dan 4010.77 µg/ml, sedangkan pada daerah Ciwidey secara umum mengalami penurunan yaitu sebesar 2574.75, 2111.60, dan 2216.14 µg/ml. Hasil tersebut sebanding dengan hasil rendemen yang diperoleh dari ekstrak tanaman seledri.
Hasil KLT menunjukkan bahwa sampel yang dianalisis memiliki Rf yang mendekati dengan nilai Rf pada standar diosmin. Tanaman seledri daerah Cipanas mengalami peningkatan kadar diosmin pada umur 4, 6, dan 8 minggu sebesar 466.55, 1046.55, dan 1274.55 ppm, sedangkan tanaman seledri daerah Ciwidey mengalami penurunan kadar diosmin yaitu sebesar 1098.08, 46.78 ppm dan pada umur 8 minggu tidak terdeteksi.
Nilai rendemen ekstrak tanaman seledri pada daerah Cipanas dan Ciwidey menunjukkan hasil yang berkorelasi positif terhadap nilai konsentrasi protein total dan kadar diosmin.
Hasil SDS-PAGE menunjukkan adanya dua buah pita protein yang dominan dengan bobot molekul 16.6 dan 17.4 kDa.
Saran
Perlu dilakukan analisis diosmin dan protein pada bagian lain dari tanaman seledri, seperti batang dan akar.
lanjutan sehingga menemukan pelarut yang dapat memberikan ekstrak yang murni.
DAFTAR PUSTAKA
Agustina L. 2004. Dasar Nutrisi Tanaman. Jakarta: Asdi Mahasatya
Blair GJ. 1979. Plant Nutrition. England : University of New England
Budiani A. 1989. Ekstraksi protein dan isoenzim esterase dari daun kopi. Jurnal
Menara Perkebunan. 57(4) : 94 -98
Coligan et al. 1995. Current Protocol in
Protein Science. Volume ke-1. USA :
John Wiley and Sons
Dalimartha S. 2000. Atlas Tumbuhan Obat
Jilid ke-2. Jakarta : Trubus Agriwidya
El-Shafae AM, El-Domiaty M. 2001. Improve LC method for the determination of diosmin and/or hesperidin in plant extract and pharmaceutical formulations. Pharm.
And Biomed. Anal. 26: 539-545
Fitriyeni S. 2003 Pemisahan flavonoid dari daun wunggu (Graptophylum pictum L. Griff). [skripsi] Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor
Gritter R, Bobbot JM, Schwarting AE. 1991.
Pengantar Kromatografi Ed. Ke-2.
Padmawinata, penerjemah. Bandung: Penerbit ITB.
Hamilton RJ, Swel PA. 1982. Introduction to High Performance Liquid
Chromatography. London: Chapman and
Hall
Heldt HW. 1997. Plant Biochemistry &
Molecular Biology. New York : Oxford
University Press
Hermawan E. 2005. Pengaruh pemupukan nitrogen dan fosfor terhadap pertumbuhan dan produksi herba seledri. [skripsi]. Bogor : Fakultas Pertanian, Institut Pertanian Bogor
Kassahara S, Hemmi S. 1986. Medical Herb
Index in Indonesia. Ed. ke-2. Jakarta : PT
Eisai Indonesia, dalam Makiyyah 2003
Kuhns EJ, Fretz TA. 1978. Distinguishing rose cultivar by pPolyacrilamid gel electrophoresis, extaction and storage of protein and active enzymes from rose leaves. Amer. Soc. Hort. Sci. 103 (4): 503-508
Krstulovic MA, PR Brown. 1982. Reverse Phase High-Performance Liquid
Chromatography. NewYork :John Wiley
& Son
Malik CP, Singh MB. 1980. Plant
Enzymology and Histo Enzymology. New
Delhi: Kalyani Publisher
Mamajis Molecular Kitchen. 2000. Western blot and SDS PAGE.
http://lsvl.la.asu.edu/resources/mamajis/in dex.html [17 Agustus 2005]
Marsono, Sigit P. 2004. Pupuk Akar Jenis dan
Aplikasinya. Jakarta : Penebar Swadaya
Mattjik AA, Sumertajaya IM. 2002.
Perancangan Percobaan.Jilid ke-1. Ed
ke-2. Bogor: IPB Press
Muladno. 2002. Seputar Teknologi Rekayasa
Genetika Bogor: Pustaka Wirausaha
Muda
Novizan. 2002. Petunjuk Pemupukan yang
Efektif. Jakarta : Agro Media Pustaka,
dalam : Ana Sya’bana 2005
Nurhidayah A. 2005. Pengaruh salinitas dan masa panen terhadap kandungan diosmin pada tanaman seledri. [skripsi]. Bogor : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor
Reginawanti. 1999. Seledri (Apium
graveolens L).
http://www.kpel.or.id/TTGP/komoditi/SE LEDRI1.htm [25 Februari 2006]
Robyt JF, White BJ. 1987. Biochemical
Techniques Theory and Practice. USA :
Waveland Press.
Salisbury FB, Ross CW. 1995. Fisiologi
Tumbuhan. Diah RL dan Sumaryono,
Siemonsma JS, Pileuk K. 1994. Plant Resource of South Asia 8 Vegetables.
Bogor: Prosea Foundation
Soewito. 1989. Bercocok Tanam Seledri. Jakarta : Titik Terang
Stryer L. 1995. Biokimia. Sadikin et al, penerjemah; Soebianto S, editor. Jakarta: EGC. Terjemahan dari: Biochemistry
Sunarjono. 2003. Bertanam 30 Jenis Sayur. Jakarta : Penebar Swadaya
Turan M, Sezen Y. 2003. Effect of salt stress on plant nutrition uptake. Experimental
Botany Journal. 54 (392) : 2553-2562
Waterborg JH, Matthews HR. 1984. The lowry method for protein quantitation. Di dalam : Walker JM, editor. Methods in
Molecular Biology Volume I. New Jersey
Lampiran 1 Tahap penelitian
Sampel Seledri dari daerah Cipanas dan Ciwidey
berumur 4, 6, 8 minggu
Bagian daun
Uji Pendahuluan Analisis diosmin Analisis protein
Analisis Bobot Kadar Kadar Identifikasi Identifikasi Pengukuran Analisis Tanah basah air abu diosmin dan pengukuran konsentrasi pola protein dengan KLT diosmin dengan dengan dengan KCKT metode Lowry SDS PAGE
Lampiran 2 Pembuatan bufer ekstraksi protein (Robyt & White 1987)
Bufer ekstraksi protein pada daun :
? 0.1 M Tris HCl, pH 8.0 ? 0.25 M Sukrosa ? PVP (0.75 g/ 50 ml)
Lampiran 3 Bahan pereaksi untuk penentuan konsentrasi tota l protein dengan
Metode Lowry (Watterborg & Matthews 1984
)Bahan pereaksi yang digunakan antara lain :
Pereaksi A
Na2CO3 sebanyak 2 gram ditimbang dan ditambahkan dengan 0.4 gram NaOH kemudian
dilarutkan ke dalam akuades sebanyak 100 ml.
Pereaksi B
Sebanyak 0.05 gram CuSO4 dan 0.1 gram Na-tartrat dilarutkan ke dalam 10 ml akuades.
Pereaksi C
Pereaksi A dan pereaksi B dicampur dengan perbandingan 50 : 1
Pereaksi D
Lampiran 4 Bahan pereaksi untuk SDS PAGE (berdasarkan metode Laemmli
1970 dalam Coligan
et al
1995)
30% akrilamid/0.8% bisakrilamid
Sebanyak 30 gram akrilamid ditambahkan dengan 0.8 gram N,N’-metilenbisakrilamid ditimbang, kemudian dilarutkan dengan akuades sampai volume 100 ml. Setelah itu, larutan tersebut disaring dengan menggunakan kertas saring dan disimpan pada suhu 4? C dalam kondisi gelap. Larutan ini dapat disimpan sampai 30 hari.
4x Tris -Cl/SDS, pH 6.8
Sebanyak 6.05 gram Tris dilarutkan ke dalam 40 ml akuades dan dipekatkan dengan HCl sampai pH 6.8, kemudian ditera dengan akuades sampai volume 100 ml. Larutan tersebut disaring degan kertas saring, lalu ditambahkan 0.4 gram SDS. Larutan disimpan pada suhu 4? C dan tahan sampai 30 hari.
4x Tris -Cl/SDS, pH 8.8
Sebanyak 91 gram Tris dilarutkan ke dalam 300 ml akuades dan dipekatkan dengan HCl sampai pH 8.8, kemudian ditera dengan akuades sampai volume 500 ml. Larutan tersebut disaring degan kertas saring, lalu ditambahkan 2 gram SDS. Larutan disimpan pada suhu 4? C dan tahan sampai 30 hari.
Sampel Buffer
Sebanyak 0.3 gram Tris, 2 ml ß-merkaptoetanol, 0.92 gram SDS, 4 gram gliserol, 2 ml bromfenol biru (0.1% w/v) dilarutkan dalam 10 ml akuades. Setelah itu diukur pH sampai 6.8 menggunakan HCl, kemudian ditera denagan akuades sampai volume 20 ml. Larutan ini disimpan pada suhu 4? C dan tahan sampai 30 hari.
Buffer Elektroforesis
Sebanyak 6 gram Tris, 28.8 gram glisin, dan 2 gram SDS dilarutkan dengan akuades sampai volume 400 ml.
Larutan Pewarna
Larutan pewarna dibuat ketika akan digunakan. Pertama, sebanyak 0.25 gram coomasie biru R250 dimasukkan ke dalam 125 ml metanol kemudian ditambah dengan 25 ml asam asetat glasial dan 100 ml akuades.
Larutan Dekolo risasi
Lampiran 5 Pembuatan gel SDS PAGE (Metode Laemmli 1970 dalam Coligan
et al
1995)
Komposisi gel pisah 10%
Bahan Pereaksi Volume (ml)
30% akrilamid/ 10 0.8% bisakrilamid
4x Tris-Cl/SDS, 7.5 pH 8.8
akuades 12.5
10% (w/v) Amonium 0.1 Persulfat
TEMED 0.02
Semua bahan pereaksi, kecuali amonium persulfat dan TEMED dicampurkan ke dalam erlenmeyer dan divakumkan selama 5 menit. Kemudian amonium persulfat dan TEMED dimasukkan dan digoyang-goyang sampai campuran merata. Campuran tersebut langsung digunakan dengan memasukkannya ke dalam cetakan gel sampai batas tertentu dan jangan sampai terbentuk gelembung udara. Setelah itu, ditambahkan akuades pada permukaan gel dan tunggu sampai gel mengering. Apabila gel sudah mengering akuades dibuang dan sisa akuades diserap dengan kertas saring. Larutan 10% Amonium Persulfat dibuat langsung ketika akan digunakan.
Komposisi gel tumpuk
Bahan Pereaksi Volume (ml)
30% akrilamid/ 1.30 0.8% bisakrilamid
4x Tris-Cl/SDS, 2.50 pH 6.8
akuades 6.10
10% (w/v) Amonium 0.05 Persulfat
TEMED 0.001
Semua bahan pereaksi, kecuali amonium persulfat dan TEMED, dicampurkan ke dalam erlenmeyer dan divakumkan selama 5 menit. Kemudian amonium persulfat dan TEMED dimasukkan dan digoyang-goyang sampai campuran merata. Campuran tersebut langsung digunakan dengan memasukkannya ke dalam cetak an gel sampai batas maksimal dan jangan sampai terbentuk gelembung udara. Setelah itu, dimasukkan sisir supaya membentuk sumur sebagai tempat sampel dan tunggu sampai gel mengering. Apabila gel sudah mengering, sisir dilepaskan perlahan-lahan.
Lampiran 6 Kondisi lingkungan daerah Cipanas dan Ciwidey (Balai penelitian
Agroklimat Bogor)
Ciwidey Cipanas Garis lintang 06?30’ 06?45’
Garis bujur 107?30’ 107?01’ Ketinggian tempat (m) 1100 1100
Jenis tanah Andosol Andosol
Bulan basah (bulan) > 9 (curah hujan > 200 mm/bln) 7-9 (curah hujan >200 mm/bln) Bulan kering (bulan) < 2 (curah hujan < 100 mm/bln) < 2 (curah hujan <100 mm/bln)
Lampiran 7 Hasil analisis tanah
Parameter Cipanas Ciwidey pH 5.11 4.92 KCl 4.05 4.21
C-Organik (%) 3.51 2.53 N total (%) 0.25 0.19
P Bray -Olsen
(mg/kg) 7.34 6.05
Ca (me/100 g) 1.42 1.17 Mg (me/100 g) 0.78 0.48 K (me/100 g) 0.38 0.25 Na (me/100 g) 0.41 0.29 KTK (me/100 g) 29.04 24.52
KB (%) 15.4 16.6
Al (me/100 g) 0.2 ttd H (me/ 100 g) 0.21 0.18
Tekstur :
Pasir (%) 31.36 28.27 Debu (%) 29.85 35.08 Liat (%) 34.07 31.34
HCl 25% (ppm) 252.5 216.2 Keterangan :
Lampiran 8 Kriteria penilaian sifat kimia tanah (Balai Penelitian Tanaman
Rempah dan Obat)
Hara makro
Sifat Tanah Sangat Rendah Sedang Tinggi Sangat
Rendah Tinggi
C-Organik (%) < 1.00 1.00 – 2.00 2.01 – 3.00 3.03 – 5.00 > 5.00 N Total (%) < 0.01 0.01 – 0.20 0.21 – 0.50 0.51 – 0.75 > 0.75 P2O5 HCl 25%
(mg/100g) < 10 10 – 20 21 - 40 41 - 60 > 60 P2O5 Olsen
(ppm) < 10 10-25 26 - 45 46 - 60 > 60 K2O HCl 25%
(mg/100g) < 10 10 – 20 21 - 40 46 - 60 > 60 K (me/100g) < 0.1 0.1 – 0.2 0.3 – 0.5 0.6 – 1.0 > 1.0
Hara mikro
KTK (me/100g) < 5 5 - 16 17 - 24 25 - 40 > 40 Na (me/100g) < 0.1 0.1 – 0.3 0.3 – 0.5 0.6 – 1.0 > 1.0 Mg (me/100g) < 0,4 0.4 – 1.0 1.1 – 2.0 2.1 – 8.0 > 8.0 Ca (me/100g) < 2 2 – 5 6 - 10 11 - 20 > 20 Kejenuhan
Basa (KB)%
< 20 20 – 35 36 - 50 51 - 70 > 70
Kejenuhan Al% < 10 10 - 20 21 - 30 31 - 60 > 60
pH
Sangat Masam Masam Agak Masam Netral
Agak
Alkalis Alkalis < 4.5 4.5 – 5.5 5.6 – 6.5 6.6 – 7.5 7.6 – 8.5 > 8.5
Keterangan :
Lampiran 9 Hasil kadar air, kadar abu, dan bobot basah tanaman seledri pada
Daerah Cipanas dan Ciwidey dengan masa tanam 4, 6, dan 8 minggu
Tanaman seledri daerah Cipanas dengan masa tanam 4 minggu
Ulangan Bobot sampel (gram) Bobot cawan (gram)
Bobot cawan + sampel (gram) Kadar air (%) Kadar abu (%) Bobot Basah (gram) 1 1.0630 22.9823 23.1445 84.70 0.68 56.00 2 1.0173 16.7362 16.8925 84.54 0.65 43.57 3 1.1209 19.5103 19.6974 83.22 0.43 51.18 Rataan 84.15 0.59 50.25
Tanaman seledri daerah Cipanas dengan masa tanam 6 minggu
Ulangan Bobot sampel (gram) Bobot cawan (gram) Bobot cawan + sampel (gram) Kadar air (%) Kadar abu (%) Bobot basah (gram) 1 2 19.5442 19.8449 85.00 1.58 106.80 2 2 16.7359 17.0307 84.50 0.84 97.55 3 2 18.6622 18.9336 86.43 1.28 88.57 Rataan 85.31 1.23 97.64
Tanaman seledri daerah Cipanas dengan masa tanam 8 minggu
Ulangan Bobot sampel (gram) Bobot cawan (gram)
Bobot cawan + sampel (gram) Kadar air (%) Kadar abu (%) Bobot basah (gram) 1 2 16.7399 17.067 83.96 1.60 187.35 2 2 21.9733 22.2734 84.99 1.51 154.35 3 2 15.5449 19.8612 84.12 1.56 163.97 Rataan 84.36 1.56 168.56
Tanaman seledri daerah Ciwidey dengan masa tanam 4 minggu
Ulangan Bobot Sampel (gram) Bobot Cawan (gram)
Bobot cawan + Sampel (gram) Kadar Air (%) Kadar abu (%) Bobot basah (gram) 1 1.1649 18.6648 18.8492 84.17 0.98 67.79 2 1.1126 21.9734 22.1580 83.41 0.68 53.63 3 1.0209 19.5415 19.6890 85.55 3.95 48.15 Rataan 84.38 1.87 56.52
Tanaman seledri daerah Ciwidey dengan masa tanam 6 minggu
Ulangan Bobot sampel (gram) Bobot cawan (gram)
Lampiran 9 (Lanjutan)
Tanaman seledri daerah Ciwidey dengan masa tanam 8 minggu
Ulangan
Bobot sampel (gram)
Bobot cawan (gram)
Bobot cawan + sampel (gram)
Kadar air (%)
Kadar abu (%)
Bobot basah (gram) 1 2 18.6600 18.9618 84.49 1.90 302.64 2 2 22.9966 23.2897 85.34 1.32 279.59 3 2 19.4985 19.8055 84.65 1.72 213.93
Lampiran 10 Hasil analisis statistik Rancangan Acak Kelompok (RAK) berbagai
parameter
Kadar Air
Sumber Keragaman db JK K T F hit P Kelompok 2 0.2817 0.1409 0.10 0.9091**
Daerah 1 0.2112 0.2112 0.14 0.7120** Waktu 2 0.6697 0.3349 0.91 0.4328** Daerah*Waktu 2 0.1747 0.0874 0.06 0.9424**
Galat 10 14.6396 1.4640 Total 17 17.9771
Kadar Abu
Sumber Keragaman db JK K T F hit P
Kelompok 2 12.840 0.6420 1.06 0.3828** Daerah 1 0.6050 0.6050 1.00 0.3415** Waktu 2 12.110 0.6055 1.00 0.4024** Daerah*Waktu 2 11.526 0.5763 0.95 0.4190**
Galat 10 60.652 0.6065
Total 17 103.179
Rendemen
Sumber Keragaman db JK K T F hit P Kelompok 2 23.9730 11.9865 1.09 0.3739**
Daerah 1 0.0617 0.0617 0.01 0.9418** Waktu 2 96.9789 48.4894 4.40 0.0426* Daerah*Waktu 2 80.4317 40.2158 3.65 0.0646**
Galat 10 110.2550 11.0255 Total 17 311.7003
Kadar Protein
Sumber Keragaman db JK K T F hit P Kelompok 2 76545.1099 382712.5550 3.82 0.0585**
Daerah 1 5736618.3734 5736618.3734 57.26 0.0001* Waktu 2 723760.4722 361880.2361 3.61 0.0660** Daerah*Waktu 2 1148860.4808 574430.2404 5.73 0.0219*
Galat 10 1001794.6860 100179.4686 Total 17 9376459.1224
Bobot Basah
Sumber Keragaman db JK K T F hit P Kelompok 2 4812.3233 2406.1617 2.88 0.1027**
Daerah 1 9470.0909 9470.0909 11.34 0.0071* Waktu 2 72559.5315 36279.7658 43.46 0.0001* Daerah*Waktu 2 4159.9020 2079.9510 2.49 0.1324**
Galat 10 8348.1106 834.8110 Total 17 99349.9585
Keterangan : Alpha : 0.05
Lampira n 11 Kurva standar Bovine Serum Albumin (BSA)
4 minggu
6 minggu
8 minggu Konsentrasi standar BSA
(µg/ml) Absorban 0 0.046 20 0.212 40 0.340 60 0.409 80 0.505
100 0.593
Kurva Standar BSA
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7
0 20 40 60 80 100 120
Konsentrasi standar BSA (ug/ml)
Absorban
y = 0.0921 + 2,991.10¯ ³ x R² = 0,9898
Kurva Standar BSA
0 0,2 0,4 0,6 0,8
0 20 40 60 80 100 120
Konsentrasi Standar BSA (ug/ml)
Absorban
y = 0,0779 + 3,459.10¯ ³ x R² = 0,9937
Kurva Standar BSA
-0,1 0 0,1 0,2 0,3 0,4 0,5 0,6
0 1 2 3 4 5 6 7
Konsentrasi Standar BSA (ug/ml)
Absorban y = 0.0878 + 5.2614.10¯ ³ x R² = 0.9890
Keterangan :
* Larutan standar BSA yang digunakan 0-100 µ g/ml * ? 742 nm
Konsentrasi standar BSA
(µg/ml) Absorban
0 0.073
20 0.161
40 0.226
60 0.290
80 0.314
100 0.388
Konsentrasi standar BSA
Lampiran 12 Nilai Rf hasil Kromatografi Lapis Tipis ekstrak tanaman
seledri
Perlakuan Ulangan
Rf
tanaman seledri
Cipanas 4 minggu 1 0.72
2 0.69
3 0.75
Rataan 0.72
Ciwidey 4 minggu 1 0.76
2 0.73
3 0.79
Rataan 0.74
Cipanas 6 minggu 1 0.73
2 0.73
3 0.74
Rataan 0.73
Ciwidey 6 minggu 1 0.65
2 0.76
3 0.81
Rataan 0.74
Cipanas 8 minggu 1 0.80
2 0.79
3 0.79
Rataan 0.79
Ciwidey 8 minggu 1 0.80
2 0.80
3 0.78
Rataan 0.79
Keterangan :
Lampiran 13 Foto hasil Kromatografi Lapis Tipis
8 minggu 6 minggu 4 minggu
S 1 2 3 4 5 6
1 2 3 4 5 6
1 2 3 4 5 6
Keterangan :
* S : standar; 1 : Cipanas ulangan 1; 2 : Cipanas ulangan 2; 3 : Cipanas ulangan 3; 4 :
Lampiran 14 Rendemen ekstrak tanaman seledri
Lokasi tanam
Masa tanam
(minggu) Ulangan ke- Rendemen (%) Cipanas 4 1 1.17
2 0.41 3 4.20
Rataan 1.93 ± 2.01
6 1 6.56
2 9.51 3 5.91
Rataan 7.33 ± 1.92
8 1 3.30
2 5.66 3 3.31
Rataan 4.09 ± 1.36
Ciwidey 4 1 3.80
2 3.90 3 4.24
Rataan 3.98 ± 0.23
6 1 14.12
2 3.86 3 17.11
Rataan 11.70 ± 6.95
8 1 4.98
2 5.03 3 10.26
Lampiran 15 Contoh perhitungan konsentrasi diosmin
0 20000 40000 60000 80000 100000 120000 140000 160000 180000
0 20 40 60 80 100 120