INHIBISI XANTIN OKSIDASE
SECARA IN VITRO
OLEH
EKSTRAK ROSELA (
Hibiscus sabdariffa
) DAN CIPLUKAN
(
Physalis angulata
)
DEDE YULIANTO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DEDE YULIANTO. Inhibisi Xantin Oksidase secara
In Vitro
oleh Ekstrak Rosela
(
Hibiscus sabdariffa
) dan Ciplukan (
Physalis angulata
). Dibimbing oleh DYAH
ISWANTINI PRADONO dan LATIFAH KOSIM DARUSMAN.
Enzim xantin oksidase mengkatalis oksidasi xantin menjadi asam urat, yang berperan
penting dalam penyakit asam urat. Rosela dan ciplukan merupakan tanaman obat yang
biasa digunakan pada berbagai pengobatan tradisional karena banyak mengandung
senyawa metabolit sekunder sehingga berpotensi sebagai penghambat enzim xantin
oksidase. Dalam penelitian ini, pada ekstrak air dan etanol dari kelopak rosela dan herba
ciplukan dilakukan uji fitokimia, toksisitas pada
Artemia salina
, dan uji inhibisi pada
aktivitas xantin oksidase secara
in vitro
yang dibandingkan dengan alopurinol sebagai
kontrol positif, serta pengamatan laju pembentukan kristal natrium urat dari larutan lewat
jenuh dengan metode turbidimetri juga diamati. Uji fitokimia ciplukan memperlihatkan
adanya senyawa flavonoid, tanin, saponin, alkaloid dan steroid, namun pada ekstrak
rosela tidak ada alkaloid dan steroid. Hasil analisis probit ekstrak air dan etanol dari
kelopak rosela dan herba ciplukan menunjukkan nilai konsentrasi letal 50 (LC
50)
masing-masing sebesar 96.95, 40.03, 252.79, dan 63.83 ppm. Ekstrak etanol dan air ciplukan
(70.08 & 43.66%) memiliki daya inhibisi lebih kuat daripada ekstrak etanol dan air rosela
(35.53 & 20.42%) tetapi masih lebih rendah daripada alopurinol (98.63%) pada
konsentrasi 100 ppm. Dari keempat ekstrak, hanya ekstrak etanol ciplukan yang
memiliki nilai konsentrasi inhibisi 50 terendah sebesar 74.49 ppm sehingga berpotensi
sebagai obat. Metode turbidimetri tidak berhasil dalam mengamati pembentukan kristal
natrium urat.
ABSTRACT
DEDE YULIANTO.
In Vitro
Inhibition of Xanthine Oxidase by Roselle (
Hibiscus
sabdariffa
) and
Ciplukan
(
Physalis angulata)
Extracts. Supervised by DYAH
ISWANTINI PRADONO and LATIFAH KOSIM DARUSMAN.
INHIBISI XANTIN OKSIDASE
SECARA IN VITRO
OLEH
EKSTRAK ROSELA (
Hibiscus sabdariffa
) DAN CIPLUKAN
(
Physalis angulata
)
DEDE YULIANTO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Inhibisi Xantin Oksidase secara
In Vitro
oleh Ekstrak Rosela (
Hibiscus
sabdariffa
) dan Ciplukan (
Physalis angulata
).
Nama : Dede Yulianto
NIM : G44204079
Disetujui:
Pembimbing I
Dr. Dyah Iswantini Pradono, MAgr
NIP 19670730 199103 2 001
Pembimbing II
Prof. Dr. Latifah K Darusman, MS
NIP 19530824 197603 2 001
Diketahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. drh. Hasim, DEA
NIP 19610328 198601 1002
PRAKATA
Alhamdulillah, puji syukur hadirat Allah SWT, atas segala rahmat dan karunia-Nya
sehingga penulis dapat menyelesaikan karya ilmiah ini. Shalawat serta salam semoga
tercurah kepada suri tauladan umat manusia Nabi Muhammad SAW. Judul yang di pilih
pada karya ilmiah ini adalah Inhibisi Xantin Oksidase secara
In Vitro
oleh Ekstrak
Rosela (
Hibiscus sabdariffa
) dan Herba Ciplukan (
Physalis angulata
).
Terima kasih penulis ucapkan kepada Ibu Dr. Ir. Dyah Iswantini Pradono, M.Agr
sebagai pembimbing I dan Ibu Prof. Dr. Ir. Latifah K Darusman, MS selaku pembimbing
II atas bimbingannya selama penelitian dan penyusunan karya ilmiah ini. Ucapan terima
kasih penulis ucapkan untuk Mama, Bapa, Mbak, Asti dan segenap keluarga tercinta atas
segala dukungan baik moril, materil, serta doa selama penulis menempuh pendidikan
hingga selesainya karya ilmiah ini. Selain itu, penulis mengucapkan terima kasih kepada
pak Nano, pak Mail, bu Ai, Neneng, Ana, Ai, Budi, Aprian, teman-teman kimia 41 dan
42 serta staf Pusat Studi Biofarmaka yang telah banyak membantu selama pelaksanaan
penelitian. Semoga karya ilmiah ini dapat bermanfaat dan memberi sumbangsih bagi
kemajuan bangsa.
Bogor, November 2009
RIWAYAT HIDUP
Penulis dilahirkan di Serang pada tanggal 12 Desember 1984 dari ayah Dodo Zaelani
dan ibu Sutari. Penulis merupakan putra kedua dari tiga bersaudara. Tahun 2003 penulis
lulus dari SMUN 1 Serang dan pada tahun 2004 lulus seleksi penerimaan mahasiswa baru
(SPMB) IPB. Penulis memilih Program Studi Kimia, Fakultas Matematika dan Ilmu
Pengetahuan Alam.
DAFTRAR ISI
Halaman
DAFTAR TABEL ... v
DAFTAR GAMBAR ... v
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Rosela (Hibiscus sabdariffa)... 1
Ciplukan (Physalis angulata)
... 2
Gout (Asam Urat) ... 2
Xantin Oksidase ... 3
Flavonoid ... 4
Turbidimetri ... 5
BAHAN DAN METODE
Bahan dan Alat ... 5
Lingkup Kerja ... 5
HASIL DAN PEMBAHASAN
Kadar Air ... 7
Rendemen ... 8
Fitokimia Rosela dan Ciplukan ... 8
Toksisitas Pada Larva Udang ... 9
Inhibisi Ekstrak Kasar Rosela Dan Ciplukan Pada Aktivitas Xantin Oksidase
... 9
Pembentukan Kristal Natrium Urat ... 12
SIMPULAN DAN SARAN
Simpulan ... 13
Saran ... 13
DAFTAR PUSTAKA ... 13
DAFTAR TABEL
Halaman
1 Struktur senyawa flavonoid ... 4
2 Kandungan fitokimia simplisia kelopak rosela dan herba ciplukan ... 8
3 Kandungan fitokimia ekstrak air rosela dan ciplukan ... 8
4 Kandungan fitokimia ekstrak etanol rosela dan ciplukan ... 9
5 Nilai LC
50ekstrak rosela dan ciplukan terhadap
A. salina
.
... 9
6 Persamaan linear ekstrak rosela dan ciplukan ... 11
7 Nilai IC
50ekstrak rosela dan ciplukan terhadap xantin oksidase ... 12
8 Indeks laju turbiditas kristal natrium urat ... 12
DAFTAR GAMBAR
Halaman
1 Kelopak rosela ... 2
2 Tanaman ciplukan ... 2
3 Skema reaksi xantin oksidase yang mengkonversi hipoxantin menjadi xantin dan
asam urat ... 3
4 Kerangka dasar flavon ... 4
5 Persen inhibisi aktivitas xantin oksidase pada ekstrak air ... 10
6 Persen inhibisi aktivitas xantin oksidase pada ekstrak etanol ... 10
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ... 18
2 Ekstraksi air dan etanol ... 19
3 Pembuatan stok ekstrak dan penetasan kista
A. salina
... 20
4 Uji toksisitas ekstrak kasar terhadap larva udang
A. salina
... 21
5 Uji inhibisi aktivitas xantin oksidase ... 22
6 Kadar air kelopak rosela dan herba ciplukan... 23
7 Rendemen ekstrak kelopak rosela dan herba ciplukan ... 23
8 Aktivitas ekstrak rosela dan herba ciplukan terhadap larva A. Salina setelah 24
jam ... 25
9 Pembuatan kurva standar ... 28
10 Data hasil uji enzimatis berbagai ekstrak ... 28
11 Turbiditas asam urat dan Na asetat pada berbagai konsentrasi ... 33
PENDAHULUAN
Penyakit asam urat (gout) sudah dikenal sejak 2000 tahun yang lalu dan menjadi salah satu penyakit tertua yang dikenal manusia. Diperkirakan bahwa penyakit asam urat terjadi pada 840 orang setiap 100 000 orang (Juandy 2008). Penyakit asam urat sangat berhubungan dengan hiperurisemia akibat kelebihan produksi dari asam urat dan dipengaruhi oleh tingginya masukan makanan yang kaya akan asam nukleat, seperti jeroan, kacang-kacangan, makanan hasil laut, dan makanan hasil fermentasi (Owen & Jhons 1999).
Obat sintetik yang biasa dikonsumsi untuk mengobati asam urat adalah alopurinol. Alopurinol merupakan obat medis yang digunakan untuk menghambat enzim xantin oksidase (XO), tetapi obat ini memberikan banyak efek samping seperti radang hati dan reaksi alergi. Dengan demikian, perlu obat alternatif yang memiliki aktivitas pengobatan lebih baik dan efek samping yang rendah
(Chiang et al. 1994). Senyawa flavonoid dan
alkaloid pada tanaman dapat berperan sebagai obat untuk penyakit gout dengan menghambat
kerja XO (Cos et al. 1998; Milián et al. 2004).
Penggunaan bahan alam sebagai obat
memiliki kelebihan, yaitu meskipun
penggunaannya dalam waktu lama tetapi efek samping yang ditimbulkan relatif kecil sehingga dianggap lebih aman (Katno & Pramono 2002).
Penelitian penghambat aktivitas XO telah banyak dilakukan pada berbagai tanaman obat yang berpotensi sebagai obat antigout.
Penelitian yang dilakukan Kong et al. (2000)
melaporkan bahwa ekstrak metanol
Cinnamomum cassia, Chrysanthemum indicum, dan Lycopus europaeus memiliki aktivitas menghambat XO lebih besar dari
50%. Ekstrak tanaman Hexachlamys edulis
dan Tamus communis L. memiliki aktivitas penghambat XO karena mengandung senyawa
flavonoid dan tanin (Schmeda et al. 1996;
Boumerfeg et al. 2009). Senyawa
6-aminopurine yang berasal dari daun gandum memiliki daya inhibisi yang kuat dengan nilai
IC50 10.89 µM (Hsieh et al. 2007). Hasil
penelitian Iswantini dan Darusman (2003) menunjukan peran ekstrak kasar flavonoid herba sidaguri sebagai penghambat aktivitas XO dengan daya inhibisi terkuat bila dibandingkan dengan produk jamu komersial antigout lainnya yang beredar di pasaran. Kemampuan ekstrak kasar flavonoid sidaguri sebagai penghambat aktivitas XO mencapai
55.29% melalui mekanisme inhibisi
kompetitif (Hidayat 2007).
Kelopak rosela kaya flavonoid antosianin, asam sitrat, asam askorbat, tanin, saponin, dan
triterpenoid (Mlati et al. 2007). Sementara
ciplukan mengandung saponin, flavonoid (luteolin), polifenol, alkaloid, fisalin, asam
palmitat, dan asam stearat (Edeoga et al.
2005). Kandungan senyawa flavonoid, tanin, dan alkaloid pada ekstrak kasar herba ciplukan dan rosela berpotensi mampu
menghambat XO (Schmeda-Hirschmann et al.
1996; Cos et al. 1998; Milian et al. 2004).
Berdasarkan kandungan senyawa yang terdapat pada tanaman rosela dan ciplukan
dilakukan uji khasiat ekstrak tanaman
terhadap pengobatan gout melalui evaluasi pengamatan pada laju pembentukkan kristal natrium urat dari larutan lewat jenuh. Nilai indeks laju turbiditas (TRI) kristal natrium urat ditentukan untuk menunjukkan efek penghambatan ekstrak rosela dan herba ciplukan pada pembentukkan kristal natrium
urat. Penentuan nilai TRI dilakukan
menggunakan metode turbidimetri
berdasarkan metode Kavanagh et al. (2000)
dengan memodifikasi konsentrasi, jenis
kristal, dan penentuan waktu pengukuran.
Penelitian ini dilakukan untuk
membuktikan ekstrak kasar kelopak rosela dan ciplukan mampu menghambat aktivitas
XO secara in vitro dan mampu menurunkan
nilai TRI kristal natrium urat, serta
mengetahui potensinya sebagai antigout dan membandingkannya dengan obat alopurinol.
TINJAUAN PUSTAKA
Rosela (Hibiscus sabdariffa)
Rosela merupakan tanaman asli Afrika. Rosela didomestikasi pada awal abad 4000 SM di Sudan. Sekarang rosela secara luas menyebar ke negara-negara tropik dan subtropik. Tumbuhan ini umumnya dikenal
masyarakat dengan nama rosela, garnet
balonda (Sunda), mrambos {Jawa Tengah), dan kasturi roriha (Ternate). Berdasarkan ilmu taksonomi tumbuhan rosela dapat diklasifikasikan dalam divisi Spermatophyta, kelas Magnoliopsida, bangsa Malvales, suku
Malvaceae, marga Hibiscus, dan jenis H.
INHIBISI XANTIN OKSIDASE
SECARA IN VITRO
OLEH
EKSTRAK ROSELA (
Hibiscus sabdariffa
) DAN CIPLUKAN
(
Physalis angulata
)
DEDE YULIANTO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DEDE YULIANTO. Inhibisi Xantin Oksidase secara
In Vitro
oleh Ekstrak Rosela
(
Hibiscus sabdariffa
) dan Ciplukan (
Physalis angulata
). Dibimbing oleh DYAH
ISWANTINI PRADONO dan LATIFAH KOSIM DARUSMAN.
Enzim xantin oksidase mengkatalis oksidasi xantin menjadi asam urat, yang berperan
penting dalam penyakit asam urat. Rosela dan ciplukan merupakan tanaman obat yang
biasa digunakan pada berbagai pengobatan tradisional karena banyak mengandung
senyawa metabolit sekunder sehingga berpotensi sebagai penghambat enzim xantin
oksidase. Dalam penelitian ini, pada ekstrak air dan etanol dari kelopak rosela dan herba
ciplukan dilakukan uji fitokimia, toksisitas pada
Artemia salina
, dan uji inhibisi pada
aktivitas xantin oksidase secara
in vitro
yang dibandingkan dengan alopurinol sebagai
kontrol positif, serta pengamatan laju pembentukan kristal natrium urat dari larutan lewat
jenuh dengan metode turbidimetri juga diamati. Uji fitokimia ciplukan memperlihatkan
adanya senyawa flavonoid, tanin, saponin, alkaloid dan steroid, namun pada ekstrak
rosela tidak ada alkaloid dan steroid. Hasil analisis probit ekstrak air dan etanol dari
kelopak rosela dan herba ciplukan menunjukkan nilai konsentrasi letal 50 (LC
50)
masing-masing sebesar 96.95, 40.03, 252.79, dan 63.83 ppm. Ekstrak etanol dan air ciplukan
(70.08 & 43.66%) memiliki daya inhibisi lebih kuat daripada ekstrak etanol dan air rosela
(35.53 & 20.42%) tetapi masih lebih rendah daripada alopurinol (98.63%) pada
konsentrasi 100 ppm. Dari keempat ekstrak, hanya ekstrak etanol ciplukan yang
memiliki nilai konsentrasi inhibisi 50 terendah sebesar 74.49 ppm sehingga berpotensi
sebagai obat. Metode turbidimetri tidak berhasil dalam mengamati pembentukan kristal
natrium urat.
ABSTRACT
DEDE YULIANTO.
In Vitro
Inhibition of Xanthine Oxidase by Roselle (
Hibiscus
sabdariffa
) and
Ciplukan
(
Physalis angulata)
Extracts. Supervised by DYAH
ISWANTINI PRADONO and LATIFAH KOSIM DARUSMAN.
INHIBISI XANTIN OKSIDASE
SECARA IN VITRO
OLEH
EKSTRAK ROSELA (
Hibiscus sabdariffa
) DAN CIPLUKAN
(
Physalis angulata
)
DEDE YULIANTO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Inhibisi Xantin Oksidase secara
In Vitro
oleh Ekstrak Rosela (
Hibiscus
sabdariffa
) dan Ciplukan (
Physalis angulata
).
Nama : Dede Yulianto
NIM : G44204079
Disetujui:
Pembimbing I
Dr. Dyah Iswantini Pradono, MAgr
NIP 19670730 199103 2 001
Pembimbing II
Prof. Dr. Latifah K Darusman, MS
NIP 19530824 197603 2 001
Diketahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. drh. Hasim, DEA
NIP 19610328 198601 1002
PRAKATA
Alhamdulillah, puji syukur hadirat Allah SWT, atas segala rahmat dan karunia-Nya
sehingga penulis dapat menyelesaikan karya ilmiah ini. Shalawat serta salam semoga
tercurah kepada suri tauladan umat manusia Nabi Muhammad SAW. Judul yang di pilih
pada karya ilmiah ini adalah Inhibisi Xantin Oksidase secara
In Vitro
oleh Ekstrak
Rosela (
Hibiscus sabdariffa
) dan Herba Ciplukan (
Physalis angulata
).
Terima kasih penulis ucapkan kepada Ibu Dr. Ir. Dyah Iswantini Pradono, M.Agr
sebagai pembimbing I dan Ibu Prof. Dr. Ir. Latifah K Darusman, MS selaku pembimbing
II atas bimbingannya selama penelitian dan penyusunan karya ilmiah ini. Ucapan terima
kasih penulis ucapkan untuk Mama, Bapa, Mbak, Asti dan segenap keluarga tercinta atas
segala dukungan baik moril, materil, serta doa selama penulis menempuh pendidikan
hingga selesainya karya ilmiah ini. Selain itu, penulis mengucapkan terima kasih kepada
pak Nano, pak Mail, bu Ai, Neneng, Ana, Ai, Budi, Aprian, teman-teman kimia 41 dan
42 serta staf Pusat Studi Biofarmaka yang telah banyak membantu selama pelaksanaan
penelitian. Semoga karya ilmiah ini dapat bermanfaat dan memberi sumbangsih bagi
kemajuan bangsa.
Bogor, November 2009
RIWAYAT HIDUP
Penulis dilahirkan di Serang pada tanggal 12 Desember 1984 dari ayah Dodo Zaelani
dan ibu Sutari. Penulis merupakan putra kedua dari tiga bersaudara. Tahun 2003 penulis
lulus dari SMUN 1 Serang dan pada tahun 2004 lulus seleksi penerimaan mahasiswa baru
(SPMB) IPB. Penulis memilih Program Studi Kimia, Fakultas Matematika dan Ilmu
Pengetahuan Alam.
DAFTRAR ISI
Halaman
DAFTAR TABEL ... v
DAFTAR GAMBAR ... v
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Rosela (Hibiscus sabdariffa)... 1
Ciplukan (Physalis angulata)
... 2
Gout (Asam Urat) ... 2
Xantin Oksidase ... 3
Flavonoid ... 4
Turbidimetri ... 5
BAHAN DAN METODE
Bahan dan Alat ... 5
Lingkup Kerja ... 5
HASIL DAN PEMBAHASAN
Kadar Air ... 7
Rendemen ... 8
Fitokimia Rosela dan Ciplukan ... 8
Toksisitas Pada Larva Udang ... 9
Inhibisi Ekstrak Kasar Rosela Dan Ciplukan Pada Aktivitas Xantin Oksidase
... 9
Pembentukan Kristal Natrium Urat ... 12
SIMPULAN DAN SARAN
Simpulan ... 13
Saran ... 13
DAFTAR PUSTAKA ... 13
DAFTAR TABEL
Halaman
1 Struktur senyawa flavonoid ... 4
2 Kandungan fitokimia simplisia kelopak rosela dan herba ciplukan ... 8
3 Kandungan fitokimia ekstrak air rosela dan ciplukan ... 8
4 Kandungan fitokimia ekstrak etanol rosela dan ciplukan ... 9
5 Nilai LC
50ekstrak rosela dan ciplukan terhadap
A. salina
.
... 9
6 Persamaan linear ekstrak rosela dan ciplukan ... 11
7 Nilai IC
50ekstrak rosela dan ciplukan terhadap xantin oksidase ... 12
8 Indeks laju turbiditas kristal natrium urat ... 12
DAFTAR GAMBAR
Halaman
1 Kelopak rosela ... 2
2 Tanaman ciplukan ... 2
3 Skema reaksi xantin oksidase yang mengkonversi hipoxantin menjadi xantin dan
asam urat ... 3
4 Kerangka dasar flavon ... 4
5 Persen inhibisi aktivitas xantin oksidase pada ekstrak air ... 10
6 Persen inhibisi aktivitas xantin oksidase pada ekstrak etanol ... 10
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ... 18
2 Ekstraksi air dan etanol ... 19
3 Pembuatan stok ekstrak dan penetasan kista
A. salina
... 20
4 Uji toksisitas ekstrak kasar terhadap larva udang
A. salina
... 21
5 Uji inhibisi aktivitas xantin oksidase ... 22
6 Kadar air kelopak rosela dan herba ciplukan... 23
7 Rendemen ekstrak kelopak rosela dan herba ciplukan ... 23
8 Aktivitas ekstrak rosela dan herba ciplukan terhadap larva A. Salina setelah 24
jam ... 25
9 Pembuatan kurva standar ... 28
10 Data hasil uji enzimatis berbagai ekstrak ... 28
11 Turbiditas asam urat dan Na asetat pada berbagai konsentrasi ... 33
PENDAHULUAN
Penyakit asam urat (gout) sudah dikenal sejak 2000 tahun yang lalu dan menjadi salah satu penyakit tertua yang dikenal manusia. Diperkirakan bahwa penyakit asam urat terjadi pada 840 orang setiap 100 000 orang (Juandy 2008). Penyakit asam urat sangat berhubungan dengan hiperurisemia akibat kelebihan produksi dari asam urat dan dipengaruhi oleh tingginya masukan makanan yang kaya akan asam nukleat, seperti jeroan, kacang-kacangan, makanan hasil laut, dan makanan hasil fermentasi (Owen & Jhons 1999).
Obat sintetik yang biasa dikonsumsi untuk mengobati asam urat adalah alopurinol. Alopurinol merupakan obat medis yang digunakan untuk menghambat enzim xantin oksidase (XO), tetapi obat ini memberikan banyak efek samping seperti radang hati dan reaksi alergi. Dengan demikian, perlu obat alternatif yang memiliki aktivitas pengobatan lebih baik dan efek samping yang rendah
(Chiang et al. 1994). Senyawa flavonoid dan
alkaloid pada tanaman dapat berperan sebagai obat untuk penyakit gout dengan menghambat
kerja XO (Cos et al. 1998; Milián et al. 2004).
Penggunaan bahan alam sebagai obat
memiliki kelebihan, yaitu meskipun
penggunaannya dalam waktu lama tetapi efek samping yang ditimbulkan relatif kecil sehingga dianggap lebih aman (Katno & Pramono 2002).
Penelitian penghambat aktivitas XO telah banyak dilakukan pada berbagai tanaman obat yang berpotensi sebagai obat antigout.
Penelitian yang dilakukan Kong et al. (2000)
melaporkan bahwa ekstrak metanol
Cinnamomum cassia, Chrysanthemum indicum, dan Lycopus europaeus memiliki aktivitas menghambat XO lebih besar dari
50%. Ekstrak tanaman Hexachlamys edulis
dan Tamus communis L. memiliki aktivitas penghambat XO karena mengandung senyawa
flavonoid dan tanin (Schmeda et al. 1996;
Boumerfeg et al. 2009). Senyawa
6-aminopurine yang berasal dari daun gandum memiliki daya inhibisi yang kuat dengan nilai
IC50 10.89 µM (Hsieh et al. 2007). Hasil
penelitian Iswantini dan Darusman (2003) menunjukan peran ekstrak kasar flavonoid herba sidaguri sebagai penghambat aktivitas XO dengan daya inhibisi terkuat bila dibandingkan dengan produk jamu komersial antigout lainnya yang beredar di pasaran. Kemampuan ekstrak kasar flavonoid sidaguri sebagai penghambat aktivitas XO mencapai
55.29% melalui mekanisme inhibisi
kompetitif (Hidayat 2007).
Kelopak rosela kaya flavonoid antosianin, asam sitrat, asam askorbat, tanin, saponin, dan
triterpenoid (Mlati et al. 2007). Sementara
ciplukan mengandung saponin, flavonoid (luteolin), polifenol, alkaloid, fisalin, asam
palmitat, dan asam stearat (Edeoga et al.
2005). Kandungan senyawa flavonoid, tanin, dan alkaloid pada ekstrak kasar herba ciplukan dan rosela berpotensi mampu
menghambat XO (Schmeda-Hirschmann et al.
1996; Cos et al. 1998; Milian et al. 2004).
Berdasarkan kandungan senyawa yang terdapat pada tanaman rosela dan ciplukan
dilakukan uji khasiat ekstrak tanaman
terhadap pengobatan gout melalui evaluasi pengamatan pada laju pembentukkan kristal natrium urat dari larutan lewat jenuh. Nilai indeks laju turbiditas (TRI) kristal natrium urat ditentukan untuk menunjukkan efek penghambatan ekstrak rosela dan herba ciplukan pada pembentukkan kristal natrium
urat. Penentuan nilai TRI dilakukan
menggunakan metode turbidimetri
berdasarkan metode Kavanagh et al. (2000)
dengan memodifikasi konsentrasi, jenis
kristal, dan penentuan waktu pengukuran.
Penelitian ini dilakukan untuk
membuktikan ekstrak kasar kelopak rosela dan ciplukan mampu menghambat aktivitas
XO secara in vitro dan mampu menurunkan
nilai TRI kristal natrium urat, serta
mengetahui potensinya sebagai antigout dan membandingkannya dengan obat alopurinol.
TINJAUAN PUSTAKA
Rosela (Hibiscus sabdariffa)
Rosela merupakan tanaman asli Afrika. Rosela didomestikasi pada awal abad 4000 SM di Sudan. Sekarang rosela secara luas menyebar ke negara-negara tropik dan subtropik. Tumbuhan ini umumnya dikenal
masyarakat dengan nama rosela, garnet
balonda (Sunda), mrambos {Jawa Tengah), dan kasturi roriha (Ternate). Berdasarkan ilmu taksonomi tumbuhan rosela dapat diklasifikasikan dalam divisi Spermatophyta, kelas Magnoliopsida, bangsa Malvales, suku
Malvaceae, marga Hibiscus, dan jenis H.
Kelopak bunga rosela kaya akan antosianin, asam sitrat, dan pektin. Rosela mengandung flavonoid gosipetin, quarsetin, hibisketin dan sabdaretin. Selain itu juga mengandung mineral seperti zat besi, natrium, kalsium, kalium, karbohidrat, serat, gula, dan vitamin (Duke 2008). Dalam kelopak kering rosela mengandung 1.7–2.5% antosianin
(Blunden et al. 2005). Ekstrak rosela
mengandung 51% antosianin dan antioksidan
24% (Tsai et al. 2002). Salah et al. (2002)
melaporkan kandungan flavonoid kuarsetin, luteolin, dan luteolin glikoksida pada ekstrak rosela. Zat-zat seperti gosipetin, antosianin, dan hibiskin glikosida dipercaya sebagai diuretik (peluruh air seni) dan efek koleretik
(pengeluaran empedu oleh hati) (Blunden et
al. 2005).
Rosela biasa digunakan sebagai obat tradisional untuk penyakit tekanan darah
tinggi, penyakit hati, dan demam (Wang et al.
2000; Ross 2003; Mojiminiyi et al. 2007).
Pigmen merah antosianin pada kelopak rosela dapat digunakan sebagai pewarna makanan
(Esselen & Sammy 1975). Sementara
kandungan terbesar dalam ekstrak air rosela ialah asam sitrat, asam askorbat, dan malat
(Blunden et al. 2005).
Kamhi et al. (2000) merekomendasikan
penggunaan herba rosela kepada dokter sebagai pengganti obat medis hipertensi karena rasio dan risiko penggunaan herba rosela lebih aman dan lebih baik dibanding kandungan obat medis.
Ciplukan (Physalis angulata) Ciplukan adalah tumbuhan asli Amerika yang kini telah tersebar secara luas di daerah tropis. Di Jawa tumbuh secara liar di kebun, tegalan, tepi jalan, semak, dan tepi hutan. Ciplukan di masyarakat Sunda disebut
cecenet, sedangkan di Jawa disebut sebagai
ceplukan, serta di masyarakat Bali disebut
angket, kepok-kepokan, atau keceplokan. Di
Inggris dikenal dengan nama morel berry
(Gambar 2). Berdasarkan ilmu taksonomi
tumbuhan ciplukan dapat diklasifikasikan
dalam divisi Spermatophyta, kelas
Dicotyledonnae, bangsa Solanales, suku
Solanaceae, marga Physalis, dan jenis P.
angulata.
Ciplukan adalah tumbuhan yang tersebar
sepanjang daerah tropis dan subtropis dunia. Penggunaan tumbuhan ini populer dalam pengobatan menyembuhkan luka, radang hati, malaria, penyakit kelamin, rematik, sakit
telinga (Freiburghaus et al. 1996; Schimmer et
al. 2001; Ankrah et al. 2003; Choi.& Hwang
2003).
Ciplukan mengandung saponin, flavonoid (luteolin), polifenol, alkaloid, steroid, vitamin
C, asam palmitat, dan asam stearat (Edeoga et
al. 2005). Tanaman ciplukan bersifat analgetik
(penghilang nyeri), detoksikan (penetral racun) serta pengaktif fungsi kelenjar-kelenjar tubuh. Saponin dan alkaloid yang terkandung dalam ciplukan memberikan rasa pahit dan berkasiat sebagai anti tumor dan menghambat pertumbuhan kanker, terutama kanker usus
besar (Lin et al. 1992; Bastos et al. 2006).
Ekstrak etanol ciplukan memiliki aktivitas
antibakteri (Nayeemulla et al. 2006).
Asam Urat
Penyakit asam urat atau sering disebut artritis gout merupakan kelainan metabolik akibat deposisi kristal natrium urat pada jaringan atau akibat supersaturnasi asam urat di dalam cairan ekstra seluler. Asam urat adalah senyawa alkaloid turunan purin (xantin). Senyawa asam urat yang ditemukan pertama kali oleh Scheele pada tahun 1776 merupakan produk akhir dari metabolisme nitrogen. Asam urat diperoleh dari hasil ekskresi pada urin hewan pemakan daging.
Asam urat (C5H4N4O3) merupakan kristal
putih, tidak berbau dan berasa, mengalami dekomposisi dengan pemanasan menjadi asam sianida (HCN), sangat sukar larut dalam air, larut dalam gliserin dan alkali. Asam urat dapat larut pada larutan dengan pH tinggi dan
dapat pula dipanaskan untuk membantu kelarutannya hingga suhu 60 °C.
Natrium urat adalah kristal yang terbentuk akibat tingginya konsentrasi asam urat dalam darah. Kristal natrium urat terkumpul pada persendian dan tulang rawan. Natrium urat sama halnya dengan asam urat, sukar larut dalam air. Faktor yang mempengaruhi pembentukan kristal natrium urat ialah pH,
suhu, kekuatan ionik, dan konsentrasi Na+.
Bentuk geometris kristal natrium urat adalah triklin atau berbentuk jarum (Rinaudo & Boistelle 1982).
Penyakit asam urat umumnya menyerang lebih banyak pria daripada perempuan. Hal ini dikarenakan perempuan memiliki hormon estrogen yang ikut membuang asam urat
melalui urin (Mansjoer et al. 2004). Kadar
asam urat rata-rata di dalam darah atau serum bergantung pada usia dan jenis kelamin. Pada laki-laki, sebelum pubertas kadarnya sekitar
3,5 mg/dl. Setelah pubertas, kadarnya
meningkat secara bertahap dan dapat
mencapai 5,2 mg/dl. Pada perempuan kadar asam urat biasanya tetap rendah, baru pada usia pramenopause kadarnya di dalam darah rata-rata sekitar 4 mg/dl. Setelah menopause, kadarnya meningkat lagi sampai 4,7 mg/dl (Dalimartha 2006).
Hiperurisemia adalah peningkatan kadar
asam urat serum di atas nilai normal, yang pada laki-laki di atas 7 mg/dl dan pada
perempuan di atas 6 mg/dl. Hiperurisemia
bisa menimbulkan penyakit gout.
Pengobatan dan pencegahan asam urat
bisa dilakukan dengan beberapa cara.
Pengobatan secara medis, yaitu dengan menghambat proses sintesis asam urat melalui
pemberian alopurinol dan menghambat
masuknya leukosit ke dalam sendi yang terkena deposit asam urat dengan kolkisin,
atau dengan pemberian obat AINS (
anti-inflamasi nonsteroid) (Johnstone 2005). Pengobatan dan pencegahan penyakit gout bisa dilakukan dengan beberapa cara, yang pertama melakukan pola diet makanan, seperti
menghindari makanan kaya purin,
menghindari alkohol, dan banyak minum air
putih. Pengobatan dengan memberikan
ramuan tradisional telah terbukti melalui penelitian bahwa beberapa jenis tanaman mengandung berbagai senyawa aktif kimia yang dapat meluruhkan asam urat dengan cepat dan tuntas. Dalam pengobatan asam urat, obat tradisional memiliki beberapa fungsi, yaitu menetralisisr tumpukan sisa asam urat, toksin pada otot, tulang, dan sendi, serta membantu proses pembuangan. Selain
itu juga dapat melancarkan sirkulasi darah sehingga menghilangkan peradangan secara lembut dan aman serta mengurangi rasa nyeri (Dalimartha 2006).
Xantin Oksidase
Xantin aksidase (XO) berperan penting dalam katabolisme purin. XO mempunyai 2 bentuk, yaitu XO dan xantin dehidrogenase (XDH). XDH dapat dikonversi menjadi XO pada mamalia, baik dalam reaksi reversibel maupun irreversibel. XO merupakan enzim yang tersebar luas dalam beberapa spesies dari bakteri hingga manusia. Di dalam tubuh, XO ditemukan di sel hati dan otot, tetapi tidak ditemukan di dalam darah.
XO merupakan suatu kompleks enzim yang terdiri atas 1332 residu asam amino,
molibdenum (HO2SMo), FAD, dan Fe2S2
sebagai pusat reaksi redoks, dengan bobot molekul sebesar 275 000 Dalton membentuk 2
subunit yang saling setangkup (Hart et al.
1970). Menurut Westerfeld et al. (1959)
Senyawa yang dapat berfungsi sebagai penstabilisasi XO diantaranya adalah salisilat, sistein, histamin, dan versenat. Sementara senyawa yang dapat menginhibisi XO berupa ion logam, urea, purin-6-aldehida, dan 2-amino-4-hidroksipteridin-6 aldehida.
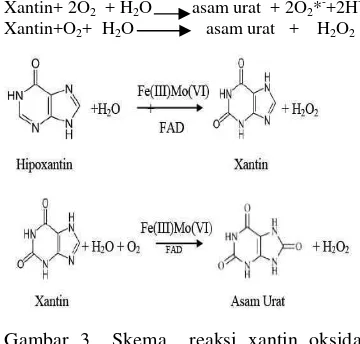
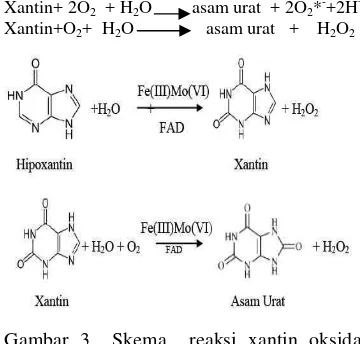
XO mengkatalis oksidasi hipoxantin
menjadi xantin lalu menjadi asam urat yang berperan penting pada penyakit gout. Pada saat bereaksi dengan xantin untuk membentuk asam urat, atom oksigen ditransfer dari molibdenum ke xantin. Perombakan pusat molibdenum yang aktif terjadi dengan
penambahan air (Cos et al. 1998) (Gambar 3).
Xantin+ 2O2 + H2O asam urat + 2O2*-+2H+
Xantin+O2+ H2O asam urat + H2O2
Gambar 3 Skema reaksi xantin oksidase yang mengkonversi hipoxantin menjadi xantin dan asam urat
Selama proses oksidasi molekul, oksigen
bertindak sebagai akseptor elektron
menghasilkan radikal superoksida (O2*) dan
hidrogen peroksida (Ramdhani 2004).
Satu unit XO dapat mengkonversi satu mikromol substrat (xantin) menjadi asam urat tiap satu menit pada pH optimum (pH 7.5) dan suhu optimum (25 °C). Apabila substratnya hipoxantin, aktivitasnya menjadi 50% atau setengahnya. XO dapat diisolasi dari berbagai macam sumber seperti susu, mikroorganisme, dan buttermilk.
XO memiliki pengaruh antitumor dan berperan aktif dalam timbulnya panas akibat penyimpanan hepatik ferritin dalam plasma. Selain itu, XO diketahui dapat mengkatalisis reduksi nitrat dan nitrit menjadi nitrit oksida
(Millr et al. 2002) dan sekaligus menyebabkan
pembentukan radikal superoksida yang dapat
menyebabkan peradangan (Bodamyali et al.
2002). Produksi asam urat berlebih dapat menyebabkan hiperurisemia namun ketika asam urat disimpan di dalam persendian akan menyebabkan peradangan dan penyakit gout. Penelitian untuk penghambat XO akan menguntungkan bukan saja untuk mengobati gout tetapi juga untuk menyerang berbagai
penyakit lain (Kadota et al. 2004).
Flavonoid
Flavonoid tersebar luas di alam, terutama dalam tumbuhan tingkat tinggi dan jaringan muda. Sekitar 5–10% metabolit sekunder
tumbuhan adalah flavonoid. Flavonoid
merupakan grup senyawa alami dengan ragam struktur fenolat yang dapat ditemukan pada buah, sayuran, gandum, batang, akar, cabang, bunga, teh, dan anggur (Middleton 1998).
Flavonoid mempunyai kerangka dasar yang terdiri atas 15 atom karbon dengan 2 cincin benzena terikat pada suatu rantai
propana membentuk susunan C6-C3-C6
(Gambar 4). Susunan tersebut dapat
menghasilkan 3 struktur, yaitu 1,3-diaril
propana (flavonoid), 1,2-diarilpropana
(isoflavonoid), dan 1,1-diarilpropana
(neoflavonoid) (Markham 1988).
Gambar 4 Kerangka dasar flavon
Flavonoid sebagai derivat benzo-γ-piron
mempunyai banyak kegunaan di samping fungsinya yang pokok sebagai vitamin P
untuk meningkatkan resistensi dan
menurunkan permeabilitas kapiler darah. Efek lain flavonoid sangat banyak macamnya terhadap berbagai organisme dan efek ini dapat menjelaskan mengapa tumbuhan yang
mengandung flavonoid dipakai dalam
pengobatan. Flavonoid dapat bekerja sebagai antivirus, antialergi, antimikroorganisme, dan antioksidan untuk mengendalikan radikal bebas yang dapat menyebabkan tumor (Middleton 1998).
Flavonoid dikenal sebagai antioksidan dan memberikan daya tarik sejumlah peneliti untuk meneliti flavonoid sebagai obat yang
berpotensi mengobati penyakit yang
disebabkan oleh radikal bebas. Flavonoid juga penghambat efektif dari beberapa enzim
termasuk XO, siklooksigenase, dan
lipooksigenase (Ruangrungsi et al. 1981;
Hoorn et al. 2002; Hayashi et al. 1988).
Flavonoid berpotensi dapat digunakan sebagai
obat untuk penyakit gout dan ischemia dengan
cara menurunkan konsentrasi asam urat dan penangkapan aktivitas superoksida dalam
jaringan manusia (Cotelle et al. 1992). Flavon
memiliki aktivitas inhibisi lebih kuat
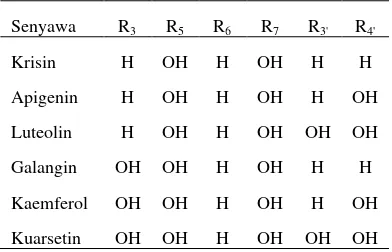
dibandingkan flavonol. Senyawa krisin,
apigenin, luteolin, galangin, kaempferol, dan quarsetin memiliki aktivitas penghambat XO dan senyawa yang memiliki aktivitas inhibisi
paling kuat adalah senyawa luteolin (Cos et
al. 1998). Struktur senyawa flavonoid
ditunjukan pada Table 1.
Tabel 1 Struktur senyawa flavonoid
Turbidimetri
The America Public Health Association (APHA) mendefinisikan dari sifat optik yang
menyebabkan cahaya dihamburkan dan
ditransmisikan secara lurus pada sampel. Turbiditas bukanlah ukuran langsung dari partikel suspensi dalam air, tetapi ukuran dari
Senyawa R3 R5 R6 R7 R3' R4'
Krisin H OH H OH H H
Apigenin H OH H OH H OH
Luteolin H OH H OH OH OH
Galangin OH OH H OH H H
Kaemferol OH OH H OH H OH
efek hamburan partikel yang terkena cahaya. Intensitas cahaya yang dihamburkan dan
diserap oleh suspensi adalah fungsi
konsentrasi jika kondisi lainnya konstan (Khopkar 1984).
Kavanagh et al. (2000) menyatakan bahwa
indeks laju turbiditas adalah nilai percobaan hasil pengukuran sifat turbiditas reaksi pembentukan suatu kristal. Dalam kaitannya dengan batu kristal natrium urat, nilai ini merupakan dugaan yang memadai terhadap nilai konstanta laju dan karakteristik bentuk kristal natrium urat, dan kedua parameter ini mewakili proses terbentuknya batu kristal natrium urat di dalam ginjal. Pendekatan pengukuran konstanta laju dan karakteristik kristal natrium urat berdasarkan perubahan turbiditasnya dapat dihitung dari persamaan berikut:
Ln (∆D/mint=0) ≈ ln (Ka) – n ln (Sprod) + (n x
0,81) ln ([Na]t=0) + n ln ([Urat]t=0)
Dimana (∆D/mint=0) = nilai perubahan
pembentukan kristal, K = konstanta laju, a =
karakteristik kristal, n = orde reaksi, Sprod =
perubahan kelarutan, [Na]t=0 dan [urat]t=0
adalah konsentrasi natrium dan urat pada saat t = 0. Indeks laju turbiditas dari kristal natrium urat didapatkan dari anti-ln intersep kurva
antara ln (∆D/mint=0) dan ln [Urat]t=0 .
Jika percobaan dilakukan dengan
penambahan konsentrasi urat yang berbeda-beda tapi pada pH, suhu, dan [Na] yang tetap,
kemudian diplotkan ln (∆D/min) pada ln
[Urat]maka akan diperoleh gradien garis lurus
dan sebuah intersep dimana berkaitan
langsung dengan ln (Ka) (Kavanagh et al.
2000).
BAHAN DAN LINGKUP KERJA
Alat dan Bahan
Bahan yang digunakan ialah serbuk kelopak rosela, serbuk herba ciplukan, alopurinol, xantin oksidase, xantin, Tween 80,
kista A. salina Leach, asam urat, dan natrium
asetat. Bahan baku kelopak rosela dan herba
ciplukan diperoleh dari UPT Kebun
Percobaan Pusat Studi Biofarmaka LPPM-IPB, Bogor.
Alat analitis yang digunaka ialah
spektrofotometer UV-Vis Hitachi 2800 dan turbidimeter 2100P HACH.
.
Lingkup Kerja
Penelitian ini dilakukan beberapa tahap, yaitu persiapan sampel, penentuan kadar air, ekstraksi, uji fitokimia, uji toksisitas ekstrak
terhadap A. salina Leach, uji inhibisi ekstrak
terhadap aktivitas xantin oksidase secara in
vitro. Diagram alir penelitian disajikan pada Lampiran 1.
Persiapan sampel
Kegiatan Sortasi basah bertujuan
memisahkan kotoran atau bahan-bahan asing lainnya dari tanaman yang akan diteliti. Pekerjaan dilanjutkan dengan pencucian untuk menghilangkan tanah dan pengotor lainnya yang masih menempel pada bahan yang sudah disortasi basah. Tahap berikutnya adalah perajangan bertujuan mempermudah proses pengeringan dan penggilingan. Tahap terakhir pengeringan dilakukan dengan udara kering hingga kadar air kurang dari 10% agar bahan yang diperoleh tidak mudah rusak akibat dari mikroorganisme.
Penentuan kadar air (AOAC 1984)
Cawan porselen dikeringkan dalam oven pada suhu 105 ºC selama 30 menit, lalu cawan porselen didinginkan dalam eksikator selama 30 menit dan ditimbang bobot kosongnya. Sampel ditimbang sekitar 3 g dan dimasukkan ke cawan porselen. Sampel beserta cawannya dipanaskan pada suhu 105°C selama 3 jam di dalam oven. Setelah didinginkan dalam eksikator selama 30 menit, cawan beserta isinya ditimbang. Prosedur dilakukan berulang kali sampai didapatkan bobot tetap dengan selisih kurang dari 1 mg. Penentuan kadar air dilakukan sebanyak 3 kali ulangan (triplo). Persen kadar air kelopak rosela dan herba ciplukan dihitung dengan persamaan:
% Kadar Air x100%
a b
a
-=
dengan
a = bobot sebelum dikeringkan (g)
b = bobot setelah dikeringkan (g)
Ekstraksi air (BPOM 2004)
Ekstraksi etanol (BPOM 2004)
Serbuk kelopak rosela dan herba ciplukan diekstraksi dengan nisbah sampel pelarut etanol 95% 1:10 menggunakan metode maserasi selama 6 jam sambil sekali-sekali diaduk, kemudian didiamkan sampai 24 jam. Maserat dipisahkan dan proses diulangi 1 kali dengan jenis dan jumlah pelarut yang sama. Semua maserat dikumpulkan dan diuapkan dengan radas penguap berputar hingga diperoleh ekstrak kental (Lampiran 2).
Penentuan rendemen ekstrak (Ramdani 2004)
Ekstrak sampel yang telah dipekatkan dengan radas penguap berputar ditambahkan beberapa ml etanol sampai semua etanol menguap. Ekstrak sampel ditimbang dan dihitung rendemennya dengan rumus sebagai berikut:
% Rendemen ekstrak x100%
x)b -(1
a
=
Keterangan: a = bobot ekstrak (g)
b = bobot sampel (g)
x = kadar air
Uji fitokomia (Harborne 1987)
Uji alkaloid. Sebanyak 1 g contoh dilarutkan dalam 10 ml kloroform dan 4 tetes
NH4OH kemudian disaring dan filtratnya
dimasukkan ke dalam tabung reaksi bertutup. Ekstrak kloroform dalam tabung reaksi
dikocok dengan 6 ml H2SO4 2 M dan lapisan
asamnya dipisahkan ke dalam tabung reaksi yang lain. Lapisan asam ini diteteskan pada lempeng tetes dan ditambahkan pereaksi Meyer, Wagner, dan Dragendrof yang akan menimbulkan endapan warna berturut-turut putih, cokelat, dan merah jingga.
Uji triterpenoid dan steroid. Sebanyak 1 g contoh dilarutkan dengan 25 ml etanol panas 50 ºC, kemudian disaring ke dalam pinggan porselen dan diuapkan sampai kering. Residu dilarutkan dengan eter dan dipindahkan ke dalam tabung reaksi, lalu ditambahkan 3 tetes
asam asetat anhidrat dan 1 tetes H2SO4 pekat
(uji Liebermen-Buchard. Warna merah atau ungu menunjukkan adanya triterpenoid dan warna hijau atau biru menunjukkan adanya steroid.
Uji flavonoid. Sebanyak 1 gram contoh ditambahkan 100 ml air panas kemudian dididihkan selama 5 menit dan disaring. Filtrat yang diperoleh kemudian diambil sebanyak 5 ml, ditambah dengan serbuk Mg 0.05 gram, 1 ml HCl pekat, dan 1 ml amil alkohol. Campuran dikocok kuat-kuat. Uji positif
ditandai dengan munculnya warna merah, kuning, atau jingga pada lapisan amil alkohol.
Uji saponin. Sebanyak 1 g contoh ditambahkan dalam 100 ml air panas kemudian dididihkan selama 5 menit lalu disaring. Sebanyak 5 ml filtrat dikocok dalam tabung reaksi tertutup selama 10 detik kemudian dibiarkan 10 menit. Adanya saponin ditunjukkan dengan terbentuknya buih stabil.
Uji tanin. Sebanyak 1 g contoh ditambah 100 ml air panas, dididihkan selama 5 menit, dan disaring. Sebagian filtrat yang diperoleh
ditambah larutan besi(III) klorida.
Terbentuknya warna hitam kehijauan
menunjukkan adanya tanin.
Uji kuinon. Sebanyak 1 g contoh ditambahkan ke dalam 100 ml air panas kemudian dididihkan selama 5 menit lalu disaring. Sebanyak 10 ml filtrat yang dihasilkan kemudian ditambahkan beberapa tetes larutan NaOH 1 N. Terbentuknya warna merah menunjukan adanya kuinon.
Uji toksisitas ekstrak terhadap A. salina
(Meyer et al. 1982)
Penetasan kista. Kista A. salina
ditimbang sebanyak 50 mg kemudian
dimasukkan ke dalam wadah yang berisi air laut yang sudah disaring. Setelah diaerasi kista
dibiarkan selama 48 jam di bawah
pencahayaan lampu agar menetas sempurna. Larva yang sudah menetas diambil untuk digunakan dalam uji toksisitas (Lampiran 3).
Uji toksisitas pada A. salina. Sebanyak
10 ekor larva A. salina dimasukkan ke dalam
vial yang berisi air laut lalu ditambahkan larutan ekstrak (air dan etanol) sehingga konsentrasi akhirnya menjadi 1000, 100, dan 10 ppm. Pengamatan dilakukan setelah 24 jam dengan menghitung jumlah larva yang mati dari total larva yang dimasukkan ke dalam botol vial. Perhitungan memakai bantuan kaca mata pembesar. Pengolahan data persen mortalitas kumulatif digunakan analisis probit
LC50 dengan selang kepercayaan 95%
(Lampiran 4).
Uji inhibisi aktivitas xantin oksidase secara
in vitro(Tamta et al. 2005)
Penentuan panjang gelombang (λ)
M untuk menghentikan reaksi. Serapan
campuran diukur menggunakan
spektrofotometer UV Hitachi 2800 pada
kisaran panjang gelombang (λ) 200–400 nm
untuk mengetahui λ maksimumnya.
Kurva standar. Larutan substrat (xantin) dibuat pada berbagai konsentrasi (0.1; 0.2; 0.3; 0.4; 0.5; 0.6; 0.7 ppm), kemudian diukur serapannya menggunakan spektrofotometer UV pada panjang gelombang 264 nm. Kurva hubungan antara konsentrasi dan serapan dibuat. Persamaan kurva linear tersebut digunakan untuk menghitung aktivitas XO.
Inhibisi Aktivitas Xantin Oksidase. Uji daya inhibisi ekstrak air dan etanol kelopak rosela dan herba ciplukan pada XO dilakukan pada kondisi optimumnya. Kondisi optimum pengujian mengacu pada Iswantini dan Darusman (2003), yaitu pada waktu inkubasi
45 menit, suhu 20 °C, pH 7.5, konsentrasi XO
0.1 unit/ml, dan konsentrasi substrat (xantin) 0.7 mM. Ekstrak dimasukkan ke dalam tabung
reaksi dengan beragam konsentrasi
berdasarkan hasil uji toksisitas pada A. salina,
dan ditambah larutan bufer kalium fosfat 50 mM pH 7.5 sehingga volumenya menjadi 1.9 ml. Campuran kemudian ditambah 1 ml xantin 2.1 mM dan xantin oksidase 0.1 unit/ml sebanyak 0.1 ml lalu diinkubasi pada suhu 20
0
C selama 45 menit. Setelah diinkubasi, campuran segera ditambahkan HCl 0.58 M sebanyak 1 ml untuk menghentikan reaksinya (Lampiran 5). Campuran diukur serapannya menggunakan spektrofotometer UV pada panjang gelombang 264 nm untuk melihat seberapa besar sisa xantin yang tidak bereaksi dalam sampel uji. Daya inhibisi yang diperoleh dibandingkan dengan alopurinol.
Preparasi urin buatan (Shmaefsky 2004) Sebanyak 36.4 g urea ditambahkan ke dalam 1.5 L air distilata dan diaduk sampai semua kristal larut. Kemudian ditambahkan 15 g NaCl dan 9 g KCl diaduk sampai larutan jernih. Keasaman (pH) diperiksa dengan
menggunakan kertas indikator untuk
menjamin agar pH berada pada kisaran urin normal yaitu 5–7. Jika pH berada di luar kisaran tersebut, ditambah HCl 1N untuk menurunkan pH atau NaOH 1N untuk menaikkan pH.
Larutan ini siap disimpan sebagai stok untuk larutan urin normal dan dapat didinginkan untuk beberapa minggu atau dibekukan untuk beberapa bulan. Sebelum digunakan larutan dibiarkan sampai mencapai suhu ruang. Untuk menjamin kesamaan dengan urin manusia, sebanyak 4 g kreatin
dan 100 mg albumin dapat dicampurkan secara perlahan ke dalam 2 L larutan.
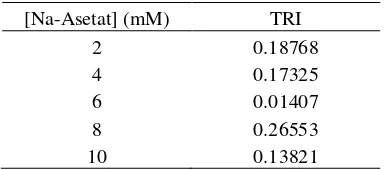
Penentuan waktu pengukuran, konsentrasi natrium dan konsentrasi asam urat (Kavanagh et al. 2000)
Urin buatan disiapkan dengan konsentrasi NaCl 2, 4, 6, 8, dan 10 mM, kemudian disiapkan pula larutan asam urat dengan konsentrasi 2, 5, 7, 10, 13, 15, 20, dan 25 mM.
Pengukuran turbiditas dilakukan
menggunakan turbidimeter. Sel turbidimeter diisi dengan 13.6 ml larutan natrium asetat dan secara cepat ditambahkan 1.4 ml larutan asam urat (waktu tetes pertama asam urat bercampur dengan natrium asetat dihitung sebagai waktu 0 menit). Campuran dikocok pelan selama 10 detik lalu sel dimasukkan ke dalam kompartemen turbidimeter dan diukur nilai turbiditasnya. Pengukuran nilai turbiditas dilakukan selama 16 menit dengan interval waktu satu menit setiap pengukuran.
Waktu pengukuran untuk pengukuran
selanjutnya ditentukan berdasarkan
kelinearitasan kurva turbiditas terhadap waktu yang diperoleh. Konsentrasi asam urat yang dipilih berdasarkan pada kelinearan kurva ln
(∆D/min) terhadap ln [asam urat] dan
pemilihan konsentrasi natrium berdasarkan
pada nilai TRI dari masing-masing
konsentrasi natrium.
Penentuan indeks laju turbiditas (TRI) kristal natrium urat
Penentuan nilai TRI kristal natrium urat
dilakukan berdasarkan metode kavanagh et al.
(2000) yang dimodifikasi jenis kristal yang digunakan dan penentuan waktu pengukuran. Pengukuran nilai turbiditas dilakukan selama 10 menit dengan interval waktu satu menit setiap pengukuran.
Pengaruh dari ekstrak rosela dan ciplukan
dilihat dengan menambahkan sampel
sebanyak 1 ml ke dalam sel turbidimeter yang berisis larutan natrium klorida, kemudian dengan segera ditambahkan larutan asam urat selanjutnya dilakukan metode yang sama sepaerti pada penentuan TRI kristal natrium urat tanpa sampel dengan ragam konsentrasi natrium dan asam urat yang sama.
HASIL DAN PEMBAHASAN
Kadar Air
untuk mengetahui cara penyimpanan terbaik bagi contoh dan menghindari pengaruh aktivitas mikrob. Selain itu juga dengan mengetahui kadar air suatu contoh dapat diperkirakan faktor koreksi dalam perhitungan rendemen hasil ekstraksi. Kadar air yang diperoleh dari serbuk kelopak rosela dan serbuk herba ciplukan masing-masing adalah
8.79 dan 7.77% (Lampiran 6). Kandungan air
pada sampel tersebut terbilang cukup rendah. Perolehan tersebut menunjukkan bahwa kelopak rosela dan herba ciplukan yang berupa serbuk dapat disimpan dalam waktu yang relatif lama untuk digunakan lebih lanjut. Hal ini sesuai dengan pernyataan Winarno (1997), yaitu bila kadar air yang terkandung dalam suatu bahan kurang dari 10% maka kestabilan optimum bahan akan tercapai dan pertumbuhan mikroba dapat dikurangi.
Rendemen Ekstrak
Mekanisme ekstraksi pada metode
maserasi adalah adanya proses difusi pelarut ke dalam dinding sel tumbuhan untuk
mengestrak senyawa yang ada dalam
tumbuhan tersebut. Alasan etanol digunakan sebagai larutan pengekstrak karena etanol memiliki 2 gugus fungsi yang berbeda kepolarannya diharapkan senyawa-senyawa dengan kepolaran yang berbeda dalam sampel akan terekstrak ke dalam etanol (Khopkar 2002). Rendemen ekstrak etanol rosela dan ciplukan masing-masing, yaitu 30.05 dan 6.28%. Rendemen ekstrak air rosela dan ciplukan masing-masing sebesar 38.68 dan 24.59% pada bobot keringnya (Lampiran 7). Rendemen terbesar dihasilkan pada ekstraksi menggunakan pelarut air hal ini dikarenakan kandungan senyawa polar pada kedua sampel lebih banyak sehingga lebih terekstrak pada pelarut air.
Fitokimia Rosela dan Ciplukan Uji fitokimia bertujuan untuk menguji keberadaan golongan senyawa metabolit sekunder seperti alkaloid, flavonoid, saponin, tanin, steroid, triterpenoid, dan kuinon dalam sampel. Uji pendahuluan ini dilakukan untuk mengetahui ada tidaknya flavonoid di dalam ekstrak dan senyawa-senyawa lain yang
kemungkinan dapat berperan dalam
menginhibisi XO.
Tabel 2 menunjukan bahwa simplisia herba ciplukan memiliki senyawa metabolit sekunder lebih banyak daripada simplisia kelopak rosela. Herba ciplukan mengandung
senyawa alkaloid dan steroid yang tidak ditemukan pada kelopak rosela. Hasil ini
sesuai dengan penelitian Edeoga et al. (2005)
yang melaporkan bahwa ciplukan
mengandung saponin, flavonoid (luteolin), polifenol, alkaloid, steroid (fisalin), asam palmitat, dan asam stearat.
Tabel 2 Kandungan fitokimia simplisia rosela dan ciplukan
Golongan senyawa
Hasil uji
Rosela Ciplukan
Alkaloid - +++
Flavonoid +++ +++
Saponin + ++
Tanin ++ ++
Triterpenoid - -
Steroid - ++
Kuinon - -
Keterangan:
tanda (+) menunjukkan tingkat intensitas warna dan (-) menunjukkan senyawa metabolit sekunder tidak terdapat pada ekstrak
Hasil uji fitokimia pada ekstrak air menunjukkan adanya senyawa flavonoid, tanin, dan saponin pada kedua sampel dengan intensitas yang berbeda. Intensitas warna senyawa flavonoid pada ekstrak air ciplukan lebih tinggi dari pada ekstrak air rosela. Hal ini diduga karena senyawa flavonoid yang terkandung dalam ekstrak air ciplukan lebih banyak. Selain itu dapat diduga karena jenis flavonoid yang terkandung dalam ekstrak air ciplukan berbeda dengan senyawa flavonoid yang terkandung dalam ekstrak air rosela. Senyawa metabolit sekunder lain yang hanya terdapat pada ekstrak air ciplukan adalah alkaloid dan steroid (Tabel 3).
Tabel 3 Kandungan fitokimia ekstrak air rosela dan ciplukan
Golongan senyawa
Hasil uji
Rosela Ciplukan
Alkaloid - +++
Flavonoid ++ +++
Saponin + ++
Tanin + +
Triterpenoid - -
Steroid - ++
Kuinon - -
Keterangan:
Ekstrak etanol rosela dan ciplukan menunjukkan senyawa yang sama seperti pada ekstrak air namun intensitas warna ekstrak etanol yang lebih besar terutama pada kandungan tanin. Hal ini diduga karena etanol memiliki gugus polar dan nonpolar, sehingga senyawa dengan kepolaran yang berbeda dapat terekstrak (Tabel 4). Kandungan senyawa pada rosela sesuai dengan penelitian
Mlati et al. (2007), yaitu kelopak rosela
menunjukkan adanya golongan senyawa flavonoid, tanin, saponin, dan triterpenoid. Namun dalam penelitian ini tidak terdeteksi adanya triterpenoid.
Tabel 4 Kandungan fitokimia ekstrak etanol rosela dan ciplukan
Golongan senyawa
Hasil uji
Rosela Ciplukan
Alkaloid - +++
Flavonoid ++ ++
Saponin + +
Tanin ++ ++
Triterpenoid - -
Steroid - ++
Kuinon - -
Keterangan:
tanda (+) menunjukkan tingkat intensitas warna dan (-) menunjukkan senyawa metabolit sekunder tidak terdapat pada ekstrak
Toksisitas pada Larva Udang Uji larva udang biasa digunakan untuk penapisan awal pada senyawa yang diduga berkhasiat sebagai antikanker (Anderson 1991). Pemeriksaan toksisitas diperlukan untuk mengetahui berapa konsentrasi yang
dapat menyebabkan keracunan sehingga
dapat diketahui jumlah penggunaan yang tepat. Hasil uji toksisitas ini dapat diketahui
dari jumlah kematian larva udang A. salina
karena pengaruh ekstrak atau senyawa bahan alam tertentu dari dosis yang telah ditentukan.
A. salina yang digunakan untuk uji toksisitas diperoleh dari hasil penetasan dengan bantuan aerator untuk memenuhi kadar oksigen yang terlarut. Larva udang yang digunakan berumur 24 jam setelah menetas karena pada umur ini
larva A. salina bersifat peka terhadap kondisi
lingkungan. Pengujian toksisitas terhadap ekstrak kasar air rosela dan ciplukan diperoleh
nilai konsentrasi letal 50 (LC50)
masing-masing sebesar 96.95 dan 252.79 ppm
(Lampiran 8). Nilai LC50 ekstrak etanol rosela
dan ciplukan masing-masing sebesar 40.03
dan 63.83 ppm (Tabel 5). Nilai LC50 ini
menunjukkan bahwa ekstrak kasar memiliki
potensi bioaktif karena menurut Meyer et al.
(1982) suatu senyawa memiliki potensi
bioaktif jika nilai LC50-nya di bawah 1000
ppm.
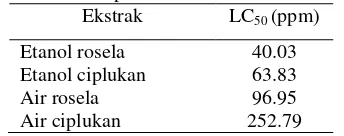
Tabel 5 Nilai LC50 ekstrak roseladan ciplukan
terhadap A. salina L
Ekstrak LC50 (ppm)
Etanol rosela 40.03
Etanol ciplukan 63.83
Air rosela 96.95
Air ciplukan 252.79
Nilai LC50 masing-masing ekstrak dapat
dijadikan sebagai batas konsentrasi tertinggi pada penentuan ragam konsentrasi ekstrak dalam uji enzimatik aktivitas XO. Hal ini dikarenakan pada formulasi obat akan lebih aman jika konsentrasinya dibuat di bawah
nilai LC50.
Inhibisi Ekstrak Kasar Rosela dan Ciplukan pada Aktivitas Xantin Oksidase
Penentuan panjang gelombang maksimum
dilakukan sebelum uji inhibisi XO.
Pengukuran dilakukan menggunakan
spektrofotometer ultarviolet (uv) pada kisaran panjang gelombang 200–400 nm karena senyawa yang akan diukur tidak berwarna. Selain itu, senyawa xantin yang akan diukur dari reaksi enzimatis diperkirakan memiliki panjang gelombang 263 nm (Westerfeld et al.
1959). Pengukuran menggunakan
spektrofotometer berkas ganda merk Hitachi 2800. Hasil uji pencarian panjang gelombang
maksimum diperoleh pada panjang
gelombang (λ) 264 nm. Hasil ini tidak berbeda
jauh dengan λmaks yang diperoleh Hakim
(2005), yaitu 262 nm. Terjadi pergeseran batokromik mungkin dikarenakan pengaruh
pelarut sehingga terjadi pergeseran λmaks
sebesar 2 nm.
Uji inhibisi inhibisi pada XO dilakukan pada semua ekstrak rosela dan ciplukan dengan menggunakan varian konsentrasi. Pengujian pada konsentrasi beragam ini
ditunjukkan untuk melihat pengaruh
penambahan konsentrasi ekstrak pada
peningkatan daya inhibisi. Ragam konsentrasi ekstrak yang digunakan ialah 10–100 ppm. Selain itu juga dilakukan pengamatan aktivitas enzim tanpa penambahan ekstrak (blangko) untuk melihat pengaruh inhibisi ekstrak tersebut pada aktivitas enzim.
Dengan demikian dapat diketahui berapa jumlah xantin yang dikonversi menjadi asam urat dalam reaksi enzimatis. Persamaan linier
kurva standar yang diperoleh adalah
y=2.0315x+0.2688 dan nilai R = 95.24%
(Lampiran 9). Y adalah serapan xantin dengan
penambahan ekstrak yang terukur dan x
adalah konsentrasi xantin sisa yang tidak terkonversi menjadi asam urat. Konsentrasi ini nantinya dapat diubah menjadi konsentrasi xantin yang bereaksi. Dengan diperolehnya konsentrasi xantin yang bereaksi, maka akan diketahui seberapa besar aktivitas xantin oksidase dalam mengubah xantin menjadi
asam urat, sekaligus dapat ditentukan
seberapa besar persen inhibisi ekstrak yang diujikan terhadap aktivitas XO.
Uji enzimatis dilakukan pada kondisi optimum seperti yang dilaporkan oleh
Iswantini & Darusman 2003. Kondisi
optimum tersebut adalah pada suhu inkubasi
20 oC, pH 7.5, konsentrasi xantin oksidase 0.1
unit/ml, konsentrasi xantin 0.7 mM, waktu inkubasi selama 45 menit, dan pada panjang gelombang 264 nm yang diperoleh dari
pencarian λmaks. Hasil uji menunjukkan bahwa
semua ekstrak yang diuji memiliki aktivitas yang lebih rendah dibandingkan dengan blangko. Daya inhibisi seluruh ekstrak rosela dan ciplukan baik dengan menggunakan pelarut air dan etanol menunjukkan bahwa hampir semua ekstrak berpotensi menghambat aktivitas XO. Secara keseluruhan, persen inhibisi aktivitas enzim meningkat seiring dengan meningkatnya konsentrasi ekstrak (Lampiran 10).
Ektrak air rosela dan ciplukan terbukti dapat menurunkan kerja enzim XO cukup baik pada konsentrasi rendah 10 ppm dengan % inhibisi masing-masing sebesar 18.75% dan 12.52%, sementara persen inhibisi tertinggi untuk rosela sebesar 20.82% pada konsentrasi 80 ppm dan persen inhibisi tertinggi ekstrak air ciplukan 43.66% pada konsentrasi 100 ppm (Gambar 5). Semakin tinggi konsentasi ekstrak air rosela persen inhibisi XO menurun. Hal ini mungkin disebabkan oleh kandungan asam organik pada ekstrak air rosela yang cukup tinggi sehingga mempengaruhi kerja
enzim XO. Blunden et al. (2005) melaporkan
tingginya konsentrasi asam organik pada ekstrak air kelopak rosela yang didominasi oleh asam sitrat, asam askorbat, dan malat sehingga keasaman rosela mencapai pH 3. Kerja enzim salah satunya dipengaruhi oleh pH sehingga apabila pH lingkungan tidak sesuai dengan pH optimumnya maka enzim akan berkurang aktivitasnya.
18.75 19.38 29.3 29.6 27 43.66 20.42 20.82 18.78 20.82 12.52 9.86 0 5 10 15 20 25 30 35 40 45 50
10 20 40 60 80 100
Konsentrasi (ppm) In h ib is i (% )
Ekstrak air rosela Ekstrak air ciplukan
Gambar 5 Persen inhibisi aktivitas xantin oksidase ekstrak air.
Daya inhibisi ekstrak air ciplukan
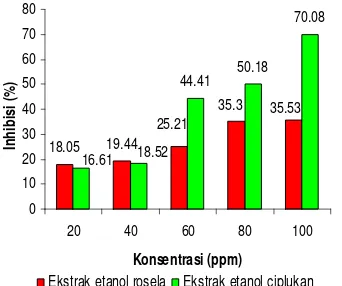
(43.66%) jauh lebih besar daripada ekstrak rosela (20.82%). Hal ini diduga karena tingginya kandungan alkaloid dan flavonoid pada ekstrak air herba ciplukan sehingga memiliki efek inhibitor XO lebih kuat dibandingkan dengan ekstrak air rosela. Hasil uji fitokimia menunjukkan bahwa ekstrak air herba ciplukan lebih banyak mengandung senyawa metabolit sekunder (Tabel 2). Efek sinergis metabolit sekunder pada ekstrak air ciplukan seperti alkaloid, flavonoid, tanin, dan steroid membuat daya inhibisi ekstrak air ciplukan lebih kuat daripada ekstrak air rosela. Gambar 6 menunjukkan daya inhibisi ekstrak etanol rosela dan ciplukan. Ekstrak etanol herba ciplukan menunjukkan daya inhibisi yang jauh lebih besar (70.08%) dibandingkan dengan ekstrak etanol rosela
(35.53%) pada konsentrasi 100 ppm.
Berdasarkan data tersebut diduga senyawa metabolit sekunder yang bersifat inhibisi lebih banyak terdapat pada ekstrak ciplukan.
18.05 19.44 44.41 50.18 70.08 35.53 35.3 25.21 16.61 18.52 0 10 20 30 40 50 60 70 80
20 40 60 80 100
Konsentrasi (ppm) In h ib is i (% )
Ekstrak etanol rosela Ekstrak etanol ciplukan
Gambar 6 Persen inhibisi aktivitas xantin oksidase ekstrak etanol
Berdasarkan uji fitokimia, senyawa
etanol ciplukan meliputi flavonoid, tanin, dan alkaloid yang terbukti melalui beberapa penelitian sangat berperan dalam menghambat
kerja XO (Schmeda-Hirschmann et al. 1996;
Cos et al. 1998; Milián et al. 2004). Hasil yang didapat sesuai dengan literatur, bahwa tanaman ciplukan mengandung saponin,
flavonoid (luteolin), polifenol (tanin),
alkaloid, dan steroid (Edeoga et al. 2005).
Ekstrak rosela mangandung golongan
senyawa flavonoid quarsetin, mirisetin,
luteolin, luteolin glikosida, tanin, dan
triterpenoid (Mlati et al. 2007). Senyawa
flavonoid diisolasi dari ekstrak etil asetat rosela secara kromatografi kertas preparatif. Isolat diduga merupakan senyawa flavonoid glikosida golongan flavon yang mempunyai gugus hidroksil pada posisi 5, 7, dan 4’ (Salah
et al. 2002; Mlati et al. 2007). Kandungan
flavonoid golongan kuersetin, mirsetin,
apigenin, dan luteolin dari ekstrak tumbuhan sebagai inhibitor XO terkuat disebabkan oleh
adanya gugus hidroksil (gugus OH) pada C5
dan C7. Selain itu juga disebabkan ikatan
rangkap antara C2 dan C3 sehingga cincin B
co-planar terhadap A, akibatnya lebih memudahkan interaksi dengan XO, sedangkan adanya ikatan rangkap pada flavonoid memungkinkan reaksi adisi (oksidasi oleh
xantin oksidase) (Cos et al. 1998; Van Hoorn
et al. 2002). Kemampuan flavonoid dalam
menghambat aktivitas XO berlangsung
melalui mekanisme inhibisi kompetitif dan interaksi dengan enzim pada gugus samping
(Nagao et al. 1999; Lin et al. 2002). Daya
inhibisi yang besar pada ekstrak ciplukan diduga karena kandungan senyawa luteolin. Daya inhibisi ekstrak etanol rosela dan ciplukan lebih tinggi daripada ekstrak air. Hal ini diduga karena kandungan senyawa metabolit sekunder yang bersifat semipolar pada ekstrak etanol memiliki efek yang cukup kuat dalam menghambat XO.
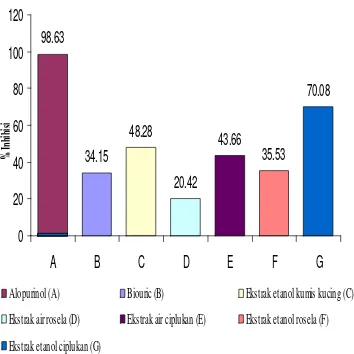
Gambar 7 menunjukkan perbandingan daya inhibisi setiap ekstrak sampel, ekstrak etanol kumis kucing, produk komersial, dan
kontrol positif (dengan penambahan
alopurinol) pada konsentrasi terbesar (100 ppm). Berdasarkan hasil penelitian ekstrak etanol ciplukan memiliki daya inhibisi
terbesar (70.08%) dibandingkan produk
komersial dan ekstrak etanol kumis kucing masing-masing sebesar 34.15 dan 48.28%. Akan tetapi jika dibandingkan alopurinol pada konsentrasi yang sama, daya inhibisi ekstrak masih di bawah alopurinol (98.63%).
98.63 34.15 48.28 20.42 43.66 35.53 70.08 0 20 40 60 80 100 120
A B C D E F G
%
In
hi
bi
si
Alopurinol (A) Biouric (B) Ekstrak etanol kumis kucing (C)
Ekstrak air rosela (D) Ekstrak air ciplukan (E) Ekstrak etanol rosela (F)
[image:30.595.328.505.94.271.2]Ekstrak etanol ciplukan (G)
Gambar 7 Persen inhibisi terbaik dari seluruh
ekstrak, kontrol negatif, dan
kontrol positif pada konsentrasi 100 ppm.
Hasil penelitian menunjukan daya inhibisi ekstrak etanol ciplukan (70.08%) lebih tinggi daripada ekstrak etanol meniran (31.43%) dan ekstrak kasar flavonoid sidaguri (29.83%) dengan konsentrasi yang sama pada penelitian sebelumnya yang dilakukan oleh Wardani (2008) dan Ramdhani (2004). Namun, daya inhibisi ekstrak etanol ciplukan (70.08%) masih lebih rendah jika dibandingkan dengan ekstrak air salam (82.54%) pada penelitian Muflihat (2008).
Data persen inhibisi masing-masing
ekstrak digunakan untuk menentukan kurva estimasi dengan program SPSS. Selanjutnya akan diperoleh persamaan kurva estimasi. Dari hasil pengujian didapatkan bahwa
inhibisi masing-masing ekstrak memiliki R2
lebih dari 80% pada kurva linear (Tabel 6). Persamaan untuk ekstrak air rosela memiliki
R2 lebih kecil dari 80% sehingga persamaan
tersebut tidak dapat digunakan untuk mencari
nilai IC50.
Tabel 6 Persamaan linear ekstrak rosela dan ciplukan
Ekstrak Persamaan
Air rosela y = 18.827+2.271Ln(x)
Air ciplukan y = 9.0474+0.3235 x
Etanol rosela y = 11.46+0.2541x
Etanol ciplukan y = 0.693x-1.62
Dari persamaan yang digunakan maka
dapat ditentukan nilai IC50 dari
masing-masing ekstrak. IC50 merupakan nilai
[image:30.595.325.514.619.694.2]menginhibisi enzim sampai 50% (Behera et
al. 2003). Nilai konsentrasi dari seluruh
ekstrak yang dapat menginhibisi XO sebesar 50% ditunjukkan dalam Tabel 7. Menurut
Noro et al. (1983), ekstrak dikatakan
berpotensi sebagai inhibitor XO dan bisa dimanfaatkan sebagai obat asam urat bila memiliki daya inhibisi lebih besar dari 50%.
Tabel 7 Nilai IC50ekstrak rosela dan ciplukan
terhadap xantin oksidase
Ekstrak IC50 (ppm)
Air ciplukan 128.81
Etanol rosela 151.67
Etanol ciplukan 74.49
Hasil penelitian menunjukkan ekstrak
etanol ciplukan memiliki nilai IC50 yang
paling rendah (74.49 ppm). Ekstrak etanol
ciplukan terbukti secara in vitro berpotensi
sebagai obat antigout karena dapat
menghambat enzim XO sampai 50% pada
konsentrasi di bawah 100 ppm. Nilai IC50
yang paling tinggi adalah ekstrak etanol rosela, yaitu 151.67 ppm dapat dikatakan ekstrak