KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
Oleh :
SAIFUDDIN ABDU F03499037
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
SAIFUDDIN ABDU F03499037
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
SAIFUDDIN ABDU F03499037
Dilahirkan pada tanggal 01 Mei 1981
Di Jombang, Jawa Timur
Tanggal Lulus :
Menyetujui,
Bogor, ... 2006
Dr. Ir. Erliza Noor Dr. Ir. Erliza Hambali, Msi
Saifuddin Abdu. F03499037. Kajian Proses Produksi Surfaktan MES dari Minyak Sawit dengan Menggunakan Reaktan H2SO4. Di bawah bimbingan :
Erliza Noor dan Erliza Hambali.
RINGKASAN
Surfaktan merupakan senyawa kimia yang memiliki aktifitas tinggi pada permukaan. Peranan surfaktan yang begitu berbeda dan beragam disebabkan oleh struktur molekulnya yang tidak seimbang. Karakteristik utama surfaktan adalah memiliki gugus polar dan non polar pada molekul yang sama. Surfaktan telah digunakan sebagai komponen bahan adhesif, bahan penggumpal, pembasah, pembusaan, emulsifier, dan bahan penetrasi serta telah diaplikasikan secara luas pada berbagai bidang industri farmasi, industri kosmetik, industri kimia, industri pertanian dan industri pangan.
MES merupakan salah satu kelompok surfaktan anionik yang paling banyak digunakan. Surfaktan ini dapat disintesis dari minyak nabati yaitu minyak sawit. Bila dibandingkan dengan surfaktan sejenis yang berbasis minyak bumi (petrokimia) yakni LAS, MES memperlihatkan karakteristik yang lebih baik diantaranya bersifat biodegradable, sifat detergensi yang baik pada tingkat kesadahan yang tinggi karena lebih toleran pada ion Ca2+.
Salah satu penggunaan MES dalam bidang pertambangan minyak bumi adalah pada sistem EOR. EOR adalah salah satu usaha peningkatan perolehan minyak bumi dengan injeksi surfaktan ke dalam reservoir. Metode ini bertujuan untuk mengambil sisa minyak bumi yang terperangkap dalam reservoir yang jumlahnya berkisar antara 60-70 persen dari volume minyak mula-mula. Adanya perbedaan derajat polaritas air dan minyak menyebabkan minyak tidak dapat keluar dari reservoir.
Penelitian ini bertujuan untuk memproduksi surfaktan MES dari metil ester CPO untuk proses oil well stimulation minyak bumi dengan menggunakan reaktan asam sulfat. Kondisi yang diteliti adalah pengaruh konsentrasi asam sulfat dan lama reaksi sulfonasi terhadap produk MES yang dihasilkan. Dalam penelitian ini dikaji pengaruh konsentrasi asam sulfat (faktor A) dan lama reaksi (faktor B) yang dibuat dalam suatu Rancangan Acak Lengkap Faktorial dengan dua kali ulangan. Taraf faktor A terdiri dari tiga taraf (60, 70, 80 persen) dan faktor B terdiri dari tiga taraf (60, 90, 120 menit). Parameter yang diukur adalah nilai pH, warna, bilangan asam, tegangan permukaan, tegangan antarmuka dan stabilitas emulsi.
Saifuddin Abdu F03499037. Study of Surfactant MES Production Process from Palm Oil by Using H2SO4 Reactant. Supervised by Erliza Noor and Erliza
Hambali.
SUMMARY
Surfactant represents compound of chemistry owning high surface activity. The role of surfactant differs and varies depend on its balance molecule structure. Main characteristic of surfactant is own a polar and non polar bunch at same molecule. Surfactant has been used as component of adhesive substance, coagulant, wetting agent, spume, emulsifier, and penetrating substance and its applications have widely in pharmaceutical, cosmetic, chemistry, agricultural and food industries.
Methyl Ester Sulphonate is one of the anionic surfactant group which usely in industries. Surfactant can be made from oil vegetation synthesis such as palm oil. MES compare to LAS, a surfactant based on petroleum, the shows better characteristic among them. MES is a biodegradable substance, nature of good detergency at high storey. One of the use MES in the field of petroleum mining is in Enhanced Oil Recovery System. EOR is one of petroleum improvement with hypodermic surfactant into reservoir.
This research aim was to produce MES surfactant from methyl ester of CPO using sulphate acid reactant. This research was investigated the influence of sulphate acid concentration and sulphonation reaction time on MES yielded. The influence of determining concentration sulphate acid (factor A) and the time of reaction ( factor B) were assessed in a Completely Factorial Randomized Design with two replicant. Each factor consisted of three level (60, 70, 80 gratuity for factor A and 60, 90, 120 minutes for factor B). Measurements were made on pH value, color, acid value, surface tension, interfacial tension and emulsion stability.
Result showed that MES characteristic included pH value of 2 to 5; L value of 67.28 to 77.90; a value of -13.07 to 0.80; b value of 65.46 to 78.06; acid value of 8.32 to 40.64 mg KOH/gr sample; emulsion stability values of 2.77 to 62.50 %.
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul :
KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
Adalah karya asli saya sendiri, dengan arahan dosen pembimbing akademik dan
pembimbing II, kecuali yang jelas ditunjukkan rujukannya.
Bogor, 2006
Yang membuat pernyataan
RIWAYAT HIDUP
Penulis dilahirkan di Jombang pada tanggal 01 Mei 1981. Penulis adalah
anak pertama dari tiga bersaudara dari pasangan Abdurrahman Ali (Alm) dan
Maslachah. Penulis menyelesaikan pendidikan dasar di SDN Jombatan V pada
tahun 1993 dan melanjutkan ke SMPN 2 Jombang hingga tamat pada tahun
1996. Pada tahun yang sama penulis masuk SMUN I Jombang dan lulus pada
tahun 1999. Lulus dari SMUN 1 Jombang, penulis melanjutkan studi pada Jurusan
Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian
Bogor melalui jalur USMI.
Selama menjalankan masa studi, penulis pernah melakukan kegiatan praktek
lapang di PT. Indofood Sukses Makmur Tbk, Banjarmasin pada bulan Maret -
Juni 2004. Judul praktek lapang yang diambil adalah “Mempelajari Proses
Produksi dan Pengawasan Mutu Mie Instan di PT. Indofood Sukses Makmur Tbk,
Banjarmasin”. Tugas akhir dilakukan oleh penulis yaitu penelitian dengan judul
“Kajian Proses Produksi Surfaktan MES dari Minyak Sawit dengan menggunakan
Reaktan H2SO4”di bawah bimbingan Dr. Ir. Erliza Noor dan Dr. Ir. Erliza
KATA PENGANTAR
Segala puji bagi Allah SWT yang senantiasa memberikan limpahan rahmat
dan hidayah-Nya sehingga penulis dapat menyelesaikan penulisan skripsi yang
berjudul “Kajian Proses Produksi Surfaktan MES dari Minyak Sawit dengan
Menggunakan Reaktan H2SO4”sebagai salah satu syarat untuk memperoleh gelar
Sarjana di Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Dalam pelaksanaannya, penulis banyak mendapatkan bimbingan dan
pengarahan serta dukungan dari berbagai pihak, untuk itu pada kesempatan ini
penulis ingin menyampaikan ucapan terima kasih kepada:
1. Dr.Ir. Erliza Noor selaku pembimbing I atas bimbingan, saran, dan nasihat
yang diberikan selama menempuh studi dan penyelesaian tugas akhir.
2. Dr. Ir. Erliza Hambali, MSi selaku pembimbing kedua yang telah meluangkan
waktu untuk membimbing penulis selama penyelesaian skripsi.
3. Dr. Ono Suparno, S. TP, MT selaku dosen penguji atas saran dan kritik yang
diberikan demi kesempurnaan skripsi ini.
4. Ibu dan adik-adikku tercinta atas segala pengorbanan, harapan, cinta dan
do’anya kepada penulis.
5. Ibu Sri Hidayati yang telah banyak membantu baik tenaga dan pikiran selama
penelitian.
6. Ibu Sri Mulyasih dari laboratorium Pengawasan Mutu, Ibu Rini Purnawati dari
Laboratorium Teknologi Kimia dan seluruh staf departemen TIN atas bantuan
yang diberikan selama penulis melaksanakan penelitian.
7. Teman-teman TIN 35, TIN 36 atas bantuan moril, tenaga dan motivasinya.
8. Semua pihak yang telah memberikan kontribusi dalam penyusunan laporan ini
Semoga kebaikan dan perhatiannya menjadi amal yang sholeh yang
dibalas Allah SWT. Amin.
Bogor, Januari 2006
DAFTAR ISI
A. MINYAK KELAPA SAWIT... 3
B. SURFAKTAN... 4
B. METODE PENELITIAN... 10
C. RANCANGAN PERCOBAAN ... 11
D. PARAMETER ... 12
IV. HASIL DAN PEMBAHASAN ... 13
A. PROSES SULFONASI... 13
B. ANALISA PARAMETER ... 14
1. Nilai pH MES ... 14
2. Bilangan Asam ... 15
3. Stabilitas Emulsi ... 17
4. Tegangan Permukaan Metode Du Nouy ... 18
KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
Oleh :
SAIFUDDIN ABDU F03499037
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
SAIFUDDIN ABDU F03499037
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
SAIFUDDIN ABDU F03499037
Dilahirkan pada tanggal 01 Mei 1981
Di Jombang, Jawa Timur
Tanggal Lulus :
Menyetujui,
Bogor, ... 2006
Dr. Ir. Erliza Noor Dr. Ir. Erliza Hambali, Msi
Saifuddin Abdu. F03499037. Kajian Proses Produksi Surfaktan MES dari Minyak Sawit dengan Menggunakan Reaktan H2SO4. Di bawah bimbingan :
Erliza Noor dan Erliza Hambali.
RINGKASAN
Surfaktan merupakan senyawa kimia yang memiliki aktifitas tinggi pada permukaan. Peranan surfaktan yang begitu berbeda dan beragam disebabkan oleh struktur molekulnya yang tidak seimbang. Karakteristik utama surfaktan adalah memiliki gugus polar dan non polar pada molekul yang sama. Surfaktan telah digunakan sebagai komponen bahan adhesif, bahan penggumpal, pembasah, pembusaan, emulsifier, dan bahan penetrasi serta telah diaplikasikan secara luas pada berbagai bidang industri farmasi, industri kosmetik, industri kimia, industri pertanian dan industri pangan.
MES merupakan salah satu kelompok surfaktan anionik yang paling banyak digunakan. Surfaktan ini dapat disintesis dari minyak nabati yaitu minyak sawit. Bila dibandingkan dengan surfaktan sejenis yang berbasis minyak bumi (petrokimia) yakni LAS, MES memperlihatkan karakteristik yang lebih baik diantaranya bersifat biodegradable, sifat detergensi yang baik pada tingkat kesadahan yang tinggi karena lebih toleran pada ion Ca2+.
Salah satu penggunaan MES dalam bidang pertambangan minyak bumi adalah pada sistem EOR. EOR adalah salah satu usaha peningkatan perolehan minyak bumi dengan injeksi surfaktan ke dalam reservoir. Metode ini bertujuan untuk mengambil sisa minyak bumi yang terperangkap dalam reservoir yang jumlahnya berkisar antara 60-70 persen dari volume minyak mula-mula. Adanya perbedaan derajat polaritas air dan minyak menyebabkan minyak tidak dapat keluar dari reservoir.
Penelitian ini bertujuan untuk memproduksi surfaktan MES dari metil ester CPO untuk proses oil well stimulation minyak bumi dengan menggunakan reaktan asam sulfat. Kondisi yang diteliti adalah pengaruh konsentrasi asam sulfat dan lama reaksi sulfonasi terhadap produk MES yang dihasilkan. Dalam penelitian ini dikaji pengaruh konsentrasi asam sulfat (faktor A) dan lama reaksi (faktor B) yang dibuat dalam suatu Rancangan Acak Lengkap Faktorial dengan dua kali ulangan. Taraf faktor A terdiri dari tiga taraf (60, 70, 80 persen) dan faktor B terdiri dari tiga taraf (60, 90, 120 menit). Parameter yang diukur adalah nilai pH, warna, bilangan asam, tegangan permukaan, tegangan antarmuka dan stabilitas emulsi.
Saifuddin Abdu F03499037. Study of Surfactant MES Production Process from Palm Oil by Using H2SO4 Reactant. Supervised by Erliza Noor and Erliza
Hambali.
SUMMARY
Surfactant represents compound of chemistry owning high surface activity. The role of surfactant differs and varies depend on its balance molecule structure. Main characteristic of surfactant is own a polar and non polar bunch at same molecule. Surfactant has been used as component of adhesive substance, coagulant, wetting agent, spume, emulsifier, and penetrating substance and its applications have widely in pharmaceutical, cosmetic, chemistry, agricultural and food industries.
Methyl Ester Sulphonate is one of the anionic surfactant group which usely in industries. Surfactant can be made from oil vegetation synthesis such as palm oil. MES compare to LAS, a surfactant based on petroleum, the shows better characteristic among them. MES is a biodegradable substance, nature of good detergency at high storey. One of the use MES in the field of petroleum mining is in Enhanced Oil Recovery System. EOR is one of petroleum improvement with hypodermic surfactant into reservoir.
This research aim was to produce MES surfactant from methyl ester of CPO using sulphate acid reactant. This research was investigated the influence of sulphate acid concentration and sulphonation reaction time on MES yielded. The influence of determining concentration sulphate acid (factor A) and the time of reaction ( factor B) were assessed in a Completely Factorial Randomized Design with two replicant. Each factor consisted of three level (60, 70, 80 gratuity for factor A and 60, 90, 120 minutes for factor B). Measurements were made on pH value, color, acid value, surface tension, interfacial tension and emulsion stability.
Result showed that MES characteristic included pH value of 2 to 5; L value of 67.28 to 77.90; a value of -13.07 to 0.80; b value of 65.46 to 78.06; acid value of 8.32 to 40.64 mg KOH/gr sample; emulsion stability values of 2.77 to 62.50 %.
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul :
KAJIAN PROSES PRODUKSI SURFAKTAN MES DARI MINYAK SAWIT DENGAN MENGGUNAKAN REAKTAN H2SO4
Adalah karya asli saya sendiri, dengan arahan dosen pembimbing akademik dan
pembimbing II, kecuali yang jelas ditunjukkan rujukannya.
Bogor, 2006
Yang membuat pernyataan
RIWAYAT HIDUP
Penulis dilahirkan di Jombang pada tanggal 01 Mei 1981. Penulis adalah
anak pertama dari tiga bersaudara dari pasangan Abdurrahman Ali (Alm) dan
Maslachah. Penulis menyelesaikan pendidikan dasar di SDN Jombatan V pada
tahun 1993 dan melanjutkan ke SMPN 2 Jombang hingga tamat pada tahun
1996. Pada tahun yang sama penulis masuk SMUN I Jombang dan lulus pada
tahun 1999. Lulus dari SMUN 1 Jombang, penulis melanjutkan studi pada Jurusan
Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian
Bogor melalui jalur USMI.
Selama menjalankan masa studi, penulis pernah melakukan kegiatan praktek
lapang di PT. Indofood Sukses Makmur Tbk, Banjarmasin pada bulan Maret -
Juni 2004. Judul praktek lapang yang diambil adalah “Mempelajari Proses
Produksi dan Pengawasan Mutu Mie Instan di PT. Indofood Sukses Makmur Tbk,
Banjarmasin”. Tugas akhir dilakukan oleh penulis yaitu penelitian dengan judul
“Kajian Proses Produksi Surfaktan MES dari Minyak Sawit dengan menggunakan
Reaktan H2SO4”di bawah bimbingan Dr. Ir. Erliza Noor dan Dr. Ir. Erliza
KATA PENGANTAR
Segala puji bagi Allah SWT yang senantiasa memberikan limpahan rahmat
dan hidayah-Nya sehingga penulis dapat menyelesaikan penulisan skripsi yang
berjudul “Kajian Proses Produksi Surfaktan MES dari Minyak Sawit dengan
Menggunakan Reaktan H2SO4”sebagai salah satu syarat untuk memperoleh gelar
Sarjana di Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Dalam pelaksanaannya, penulis banyak mendapatkan bimbingan dan
pengarahan serta dukungan dari berbagai pihak, untuk itu pada kesempatan ini
penulis ingin menyampaikan ucapan terima kasih kepada:
1. Dr.Ir. Erliza Noor selaku pembimbing I atas bimbingan, saran, dan nasihat
yang diberikan selama menempuh studi dan penyelesaian tugas akhir.
2. Dr. Ir. Erliza Hambali, MSi selaku pembimbing kedua yang telah meluangkan
waktu untuk membimbing penulis selama penyelesaian skripsi.
3. Dr. Ono Suparno, S. TP, MT selaku dosen penguji atas saran dan kritik yang
diberikan demi kesempurnaan skripsi ini.
4. Ibu dan adik-adikku tercinta atas segala pengorbanan, harapan, cinta dan
do’anya kepada penulis.
5. Ibu Sri Hidayati yang telah banyak membantu baik tenaga dan pikiran selama
penelitian.
6. Ibu Sri Mulyasih dari laboratorium Pengawasan Mutu, Ibu Rini Purnawati dari
Laboratorium Teknologi Kimia dan seluruh staf departemen TIN atas bantuan
yang diberikan selama penulis melaksanakan penelitian.
7. Teman-teman TIN 35, TIN 36 atas bantuan moril, tenaga dan motivasinya.
8. Semua pihak yang telah memberikan kontribusi dalam penyusunan laporan ini
Semoga kebaikan dan perhatiannya menjadi amal yang sholeh yang
dibalas Allah SWT. Amin.
Bogor, Januari 2006
DAFTAR ISI
A. MINYAK KELAPA SAWIT... 3
B. SURFAKTAN... 4
B. METODE PENELITIAN... 10
C. RANCANGAN PERCOBAAN ... 11
D. PARAMETER ... 12
IV. HASIL DAN PEMBAHASAN ... 13
A. PROSES SULFONASI... 13
B. ANALISA PARAMETER ... 14
1. Nilai pH MES ... 14
2. Bilangan Asam ... 15
3. Stabilitas Emulsi ... 17
4. Tegangan Permukaan Metode Du Nouy ... 18
6. Uji Warna ... 21
V. KESIMPULAN DAN SARAN ... 25
A. KESIMPULAN... 25
B. SARAN ... 25
DAFTAR PUSTAKA ... 26
DAFTAR TABEL
Halaman
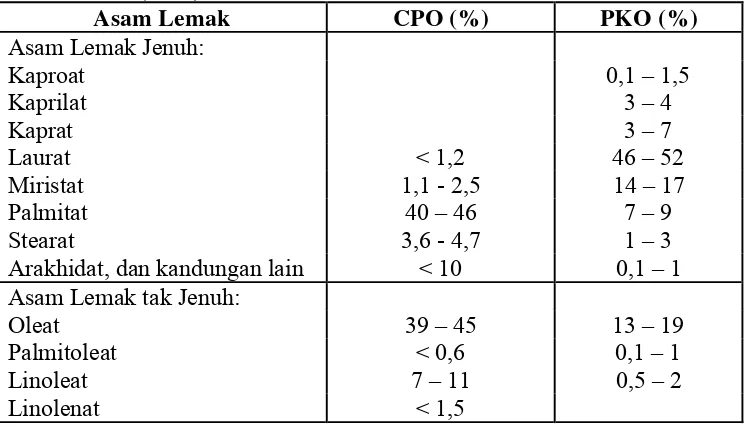
Tabel 1. Komposisi asam lemak pada minyak sawit (CPO) dan minyak
inti sawit (PKO)... ... 3
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur molekul kimia MES (Watkins, 2001) ... 6
Gambar 2. Reaksi sulfonasi menggunakan asam sulfat
(Kirk dan Othmer, 1964)... ... 8
Gambar 3. Grafik hubungan antara konsentrasi reaktan H2SO4
dan lama reaksi terhadap nilai pH MES ... 15
Gambar 4. Grafik hubungan antara konsentrasi H2SO4 dan lama
reaksi terhadap nilai bilangan asam ... 16
Gambar 5. Grafik pengaruh konsentrasi H2SO4 dan lama reaksi terhadap
kestabilan emulsi dari MES yang dihasilkan ... 18
Gambar 6. Grafik nilai tegangan permukaan MES ... 19
Gambar 7. Grafik hubungan nilai konsentrasi H2SO4 dan lama reaksi
terhadap nilai IFT... 21
Gambar 8. Grafik hubungan antara jumlah konsentrasi dan lama reaksi terhadap nilai L ... 22
Gambar 9. Grafik hubungan antara jumlah konsentrasi dan lama reaksi terhadap nilai a ... 23
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Diagram Alir Proses Sulfonasi ... 28
Lampiran 2. Prosedur Analisis Karakteristik MES... 29
Lampiran 3. Hasil Analisis Nilai pH MES... 33
Lampiran 4. Hasil Analisis Bilangan Asam... 35
Lampiran 5. Hasil Analisis Stabilitas Emulsi ... 37
Lampiran 6. Hasil Analisis Tegangan Permukaan... 38
Lampiran 7. Hasil Analisis Tegangan Antarmuka... 40
Lampiran 8. Hasil Analisis Warna (nilai L)... 42
Lampiran 9. Hasil Analisis Warna (nilai a) ... 44
I. PENDAHULUAN
A. LATAR BELAKANG
Sistem pertambangan minyak bumi seringkali menemui masalah dalam
hal pengeboran minyak. Masalahnya adalah adanya penurunan volume
minyak yang diambil yang berbanding terbalik dengan volume air yang ikut
terambil. Hal ini disebabkan adanya perbedaan tegangan permukaan air dan
minyak sehingga minyak tidak dapat keluar dari reservoir. Sebaliknya, air
cenderung mengisi ruang pengambilan minyak pada sistem pengeboran. Sisa
minyak di dalam reservoir berkisar antara 60 – 70 persen dari volume minyak
mula-mula. Untuk mengambil sisa minyak tersebut dapat digunakan metode
Enhanced Oil Recovery (EOR). EOR adalah salah satu usaha peningkatan
perolehan minyak dengan injeksi material ke dalam reservoir. Material yang
diinjeksikan biasanya adalah surfaktan. Injeksi tersebut bertujuan untuk
merubah sifat-sifat fisik fluida dan batuan reservoir sehingga dapat
meningkatkan produksi minyak.
Surfaktan adalah bahan aktif permukaan yang dapat diproduksi secara
sintesis kimia maupun biokimia. Surfaktan sendiri berfungsi untuk
menurunkan tegangan permukaan dan tegangan antar muka antara dua cairan
yang berbeda derajat polaritasnya. Pada umumnya surfaktan disintesis dari
turunan minyak bumi dan gas alam. Beberapa produknya antara lain linear
alkilbenzen sulfonat (LAS), alkil sulfat, alkil etoksilat dan alkil etoksilat
sulfat. Proses pembuatan surfaktan dari minyak bumi dan gas alam ini dapat
menimbulkan pencemaran terhadap lingkungan. Di samping itu, minyak bumi
dan gas alam merupakan sumber daya alam yang tidak dapat diperbarui
sehingga dengan penggunaan secara besar-besaran akan menyebabkan sumber
daya alam tersebut cepat habis. Alternatif yang dapat diambil adalah
penggunaan minyak nabati sebagai bahan baku pembuatan surfaktan.
Penggunaan surfaktan semakin meluas pada industri-industri modern.
Hal ini disebabkan surfaktan memiliki sifat menurunkan tegangan permukaan,
tegangan antar muka, dapat meningkatkan kestabilan partikel yang terdispersi
terserap ke dalam permukaan minyak atau air yang kemudian membentuk
suatu lapisan seperti film (berfungsi sebagai penghalang) sehingga dapat
menghambat proses penggabungan (coalescence) dari partikel terdispersi.
Secara umum surfaktan dapat dibagi menjadi empat kelompok
berdasarkan karakteristik ionisasi gugus yang dimilikinya. Kelompok tersebut
adalah kelompok surfaktan kationik, anionik, non ionik dan amfoterik.
Diantara kelompok surfaktan tersebut yang dibutuhkan dalam jumlah besar
adalah kelompok surfaktan anionik (Matheson, 1996). Beberapa contoh
surfaktan anionik adalah linear alkilbenzen sulfonat (LAS), alkohol sulfat
(AS), alkohol eter sulfat (AES), alfa olefin sulfonat (AOS), dan metil ester
sulfonat (MES). Metil ester sulfonat (MES) merupakan salah satu kelompok
surfaktan anionik yang dapat disintesis secara kimia yakni dengan proses
sulfonasi dengan bahan baku minyak sawit.
Proses sulfonasi umumnya dilakukan dengan mereaksikan agen sulfonasi
dengan minyak, asam lemak ataupun ester asam lemak. Agen sulfonasi yang
dapat digunakan adalah SO3, H2SO4, NaHSO3, NH2SO3H, dan ClSO3H.
Faktor-faktor penting yang perlu diperhatikan pada proses sulfonasi adalah
nisbah reaktan, suhu reaksi, dan lama reaksi.
Penelitian ini dilakukan untuk memproduksi surfaktan MES dari metil
ester CPO untuk proses Oil Well Stimulation minyak bumi dengan
menggunakan reaktan H2SO4. Kondisi sulfonasi yang diteliti adalah pengaruh
konsentrasi H2SO4 dan lama reaksi terhadap produk MES yang dihasilkan.
B. TUJUAN
Tujuan penelitian ini adalah:
1. Mendapatkan konsentrasi reaktan H2SO4 dan lama reaksi sulfonasi terbaik
pada proses produksi surfaktan metil ester sulfonat.
II. TINJAUAN PUSTAKA
A. MINYAK KELAPA SAWIT
Minyak kelapa sawit dapat dikelompokkan menjadi dua kelompok yaitu
minyak sawit (CPO) dan minyak inti sawit (PKO). Minyak kelapa sawit
mengandung asam lemak jenuh dan tidak jenuh dengan perbandingan yang
hampir sama. Asam lemak yang bersifat dominan di dalam minyak kelapa
sawit adalah asam palmitat dan asam oleat. Sebagian kecil lagi asam linoleat
dan asam stearat.
Minyak inti sawit mempunyai kandungan asam lemak tidak jenuh sekitar
21 persen dan asam lemak jenuh sekitar 79 persen. Minyak inti sawit lebih
dominan mengandung asam laurat (44-52 persen) dan asam miristat (12-17
persen) sedangkan kandungan asam palmitat dan asam stearat masing-masing
sekitar 6,5–9 persen dan 1-2,5 persen (Bernardini, 1983). Komposisi asam
lemak pada CPO dan PKO dapat dilihat pada Tabel 1.
Tabel 1. Komposisi asam lemak pada minyak sawit (CPO) dan minyak inti sawit (PKO)
Sumber: Eckey (1955) di dalam Ketaren (1986)
Minyak sawit dipilih sebagai bahan baku pembuatan surfaktan karena
komponen asam lemak penyusun trigliseridanya, yaitu asam lemak C16-C18
lemak C12-C14 berperan terhadap efek pembusaan (Yuliasari et al., 1997).
Beberapa proses yang dapat diterapkan untuk menghasilkan surfaktan adalah
proses sukrolisis untuk menghasilkan sukrosa ester, proses amidasi untuk
menghasilkan alkanolamida dan proses sulfonasi untuk menghasilkan metil
ester sulfonat (Libanan, 2002).
B. SURFAKTAN
Surfaktan merupakan senyawa aktif yang digunakan untuk menurunkan
energi pembatas yang membatasi dua cairan yang tidak saling melarut
(Matheson, 1996). Energi pembatas dua cairan ini disebut juga dengan
tegangan permukaan sehingga dapat pula dikatakan bahwa surfaktan
menurunkan tegangan permukaan. Dengan adanya penurunan tegangan
permukaan akan mengurangi daya kohesi dari molekul dan sebaliknya akan
meningkatkan daya adhesi (Suryani et al., 2000). Surfaktan mengandung
gugus hidrofilik dan gugus hidrofobik dalam molekul yang sama. Adanya
gugus tersebut menyebabkan surfaktan mampu berada pada daerah antar
muka yang berbeda derajat polaritasnya dan ikatan hidrogen seperti minyak
dan air. Pembentukan film pada daerah antar muka ini menurunkan energi
antar muka dan menyebabkan sifat-sifat khas molekul surfaktan (Georgiou et
al., 1992).
Molekul surfaktan dapat digambarkan seperti berudu yang terdiri dari
bagian kepala dan ekor. Bagian kepala bersifat hidrofilik yang merupakan
bagian yang sangat polar, dan bagian ekor yang bersifat hidrofobik bersifat
non polar. Kepala dapat berupa anion, kation dan non ion, sedangkan ekor
dapat berupa rantai linear atau cabang hidrokarbon. Konfigurasi kepala ekor
ini membuat surfaktan memiliki fungsi yang beragam di industri (Hui, 1996;
Hasenhuettl, 1997).
Jenis surfaktan dibagi menjadi empat. Jenis tersebut adalah surfaktan
anionik, kationik, non ionik dan amfoterik (Rieger, 1985). Surfaktan anionik
adalah senyawa yang pada bagian hidrofiliknya bermuatan negatif.
Keberadaan gugus sulfat atau sulfonat menyebabkan sifat hidrofilik.
positif. Sifat hidrofilik ini umumnya disebabkan karena garam ammonium.
Surfaktan non ionik adalah senyawa yang tidak bermuatan atau tidak terjadi
ionisasi molekul pada gugus hidrofiliknya. Sifat hidrofiliknya disebabkan
karena keberadaan gugus oksigen eter atau karboksil. Kelompok surfaktan
non ionik ini dibagi menjadi dua kelompok yakni ester asam lemak dari
polihidrik alkohol dan turunan polialkoksilat (Rieger, 1985). Surfaktan
amfoterik adalah senyawa yang bermuatan positif dan negatif pada
molekulnya. Muatannya tergantung pada nilai pH. Pada kisaran nilai pH
rendah, senyawa ini akan bermuatan negatif, dan pada kisaran nilai pH tinggi
akan bermuatan positif (Matheson, 1996).
Tegangan permukaan atau energi bebas permukaan didefinisikan sebagai
usaha untuk memperluas permukaan cairan per satuan luas. Pengertian yang
sama juga digunakan untuk tegangan antar muka antara dua cairan yang
immisibel (Shaw, 1980). Tegangan permukaan udara-air dan tegangan antar
muka minyak-air dapat diukur dengan metode tensiometer Du Nouy. Pada
satuan cgs tegangan permukaan dan antar muka dinyatakan dalam erg/cm2
atau dyne/cm, sedangkan dalam satuan SI dinyatakan dalam N/m. Kedua
besaran tersebut saling berhubungan. 1 dyne/cm = 1 mN/m (Hasenhuettl,
2000).
Karakteristik utama surfaktan adalah pada aktifitas permukaannya.
Surfaktan mampu meningkatkan kemampuan menurunkan tegangan
permukaan dan antar muka suatu cairan, meningkatkan kemampuan
pembentukan emulsi minyak dalam air, mengubah kecepatan agregasi partikel
terdispersi yaitu dengan menghambat dan mereduksi flokulasi dan
coalescence partikel yang terdispersi sehingga kestabilan partikel yang
terdispersi makin meningkat. Surfaktan juga mampu mempertahankan
gelembung atau busa yang terbentuk lebih lama (Bergenstahl, 1997).
C. METIL ESTER
Definisi metil ester menurut SNI (1999) adalah ester lemak yang dibuat
melalui proses esterifikasi asam lemak dengan alkohol, berwujud cairan.
lebih tahan terhadap oksidasi dan tidak mudah berubah warna (Darnoko et al.,
2001). Metil ester dapat dihasilkan melalui proses esterifikasi asam lemak
atau transesterifikasi trigliserida. Esterifikasi adalah reaksi antara asam
dengan alkohol dengan bantuan katalis NaOH untuk membentuk ester (Hui,
1996).
RCOOH + R’ OH RCOOR’ + H2O
Asam lemak Alkohol Ester Air
Transesterifikasi adalah penggantian gugus alkohol dari suatu ester
dengan alkohol lainnya dalam suatu proses yang menyerupai hidrolisis.
Dalam hal ini alkohol menggantikan air. Reaksi ini disebut juga dengan
alkoholisis (Hui, 1996). Persamaan reaksinya adalah sebagai berikut.
RCOOR’ + R”OH RCOOR” + R’OH
Ester Alkohol Ester Alkohol
D. METIL ESTER SULFONAT (MES)
Surfaktan metil ester sulfonat termasuk dalam golongan surfaktan
anionik. Struktur molekul kimia MES dapat dilihat pada Gambar 1.
O
R CH C OCH3
SO3Na
Gambar 1. Struktur molekul kimia MES (Watkins, 2001)
Swern (1979) menyatakan bahwa kemampuan surfaktan dalam
hubungannya dengan peningkatan kestabilan emulsi tergantung dari
kontribusi gugus polar dan gugus non polar, yang dapat dilihat dari ukuran
HLB (Hydrophyle Lipophyle Balance). Surfaktan yang memiliki nilai HLB
rendah akan cenderung larut dalam minyak. Sebaliknya, semakin tinggi nilai
surfaktan adalah 2–18. Surfaktan dengan nilai HLB antara 2–8 akan
cenderung larut dalam minyak. Sedangkan surfaktan dengan nilai HLB antara
14-18 akan cenderung larut dalam air (Suryani et al., 2000).
Panjang molekul sangat kritis untuk keseimbangan kebutuhan gugus
hidrofilik dan lipofilik. Apabila rantai hidrofobik terlalu panjang akan
menyebabkan kelarutan dalam air terbatas. Sebaliknya, apabila rantai
hidrofobik terlalu pendek akan memiliki keterbatasan kelarutan dalam
minyak. Pada umumnya, panjang rantai terbaik untuk surfaktan adalah asam
lemak dengan 10-18 atom karbon (Swern, 1979).
MES dapat dihasilkan dari minyak nabati. MES dari minyak nabati
dengan ikatan atom karbon C10, C12, C14 biasa digunakan untuk light duty
diwashing detergent, sedangkan MES yang mempunyai ikatan atom karbon
C16- C18 biasa digunakan untuk detergen bubuk dan cair (Watkins, 2001).
Menurut Matheson (1996) MES telah mulai dimanfaatkan sebagai bahan
aktif pada produk-produk pembersih. Pemanfaatan surfaktan jenis ini karena
MES meperlihatkan karakteristik dispersi yang baik, sifat detergensi yang
baik dengan tidak adanya fosfat, serta bersifat mudah didegradasi.
Karakteristik surfaktan MES komersial disajikan pada Tabel 2.
Tabel 2. Karakteristik surfaktan MES komersial
Spesifikasi MES Palm Stearin (C16-C18)
Metil Ester Sulfonat (MES), (% b/b) 83
Disodium Karboksi Sulfonat (Disalt), (%
b/b) 3,5
Sadi (1994) menyatakan umumnya surfaktan dapat disintesis dari minyak
nabati melalui senyawa antara metil ester dan fatty alkohol. Beberapa proses
alkanolamida, proses sukrolisis untuk menghasilkan sukrosa ester dan proses
sulfonasi untuk menghasilkan MES.
Proses sulfonasi menghasilkan produk turunan yang terbentuk melalui
reaksi kelompok sulfat dengan minyak, asam lemak dan alkohol lemak.
Proses ini disebut dengan proses sulfonasi karena proses ini melibatkan
penambahan sulfat pada senyawa organik. Jenis minyak yang biasa
disulfonasi adalah minyak yang mengandung ikatan rangkap ataupun grup
hidroksil pada molekulnya. Di industri, bahan baku minyak yang digunakan
adalah minyak berwujud cair yang kaya akan ikatan rangkap (Bernardini,
1993).
Agen sulfonat yang dapat dipakai untuk proses sulfonasi antara lain asam
sulfat (H2SO4), oleum (larutan SO3 di dalam H2SO4), sulfur dioksida bebas,
sulfur trioksida (SO3) dan asam klorosulfonat (Bernardini, 1993).
Menurut Swern (1979), reaksi sulfonasi molekul asam lemak dapat
terjadi pada tiga sisi, yaitu pada gugus hidroksil, bagian atom karbon dan
rantai tidak jenuh (ikatan rangkap). Proses sulfonasi dengan menggunakan
oleum dapat dilakukan secara batch maupun kontinu. Kelemahan pemakaian
oleum adalah dihasilkan sisa H2SO4 dalam jumlah besar sehingga berdampak
negatif terhadap peralatan akibat sifatnya yang korosif (Kirk dan Othmer,
1964; Foster, 1996). Apabila menggunakan H2SO4 maka akan dihasilkan
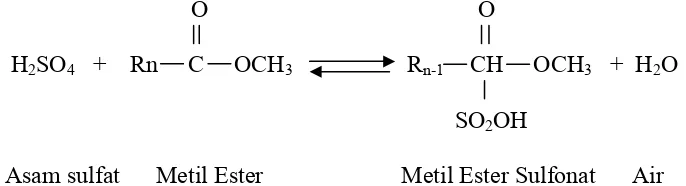
produk samping berupa air (de Groot, 1991). Gambar 2 berikut menunjukkan
reaksi sulfonasi metil ester dengan menggunakan H2SO4.
O O
H2SO4 + Rn C OCH3 Rn-1 CH OCH3 + H2O
SO2OH
Asam sulfat Metil Ester Metil Ester Sulfonat Air
Gambar 2. Reaksi sulfonasi menggunakan asam sulfat (Kirk dan Othmer,
Menurut de Groot (1991) konsentrasi H2SO4 yang digunakan pada proses
sulfonasi adalah sekitar 80 persen. Air sebagai produk samping yang
dihasilkan pada proses sulfonasi dapat menghambat terjadinya reaksi
sulfonasi. Karena itu diperlukan H2SO4 berlebih dalam jumlah banyak dengan
tujuan agar reaksi sulfonasi terjadi hingga selesai. Kondisi ideal untuk proses
sulfonasi yang dilakukan secara batch adalah nisbah reaktan 80 persen dan
alkilbenzena antara 1,6-1,8; total waktu reaksi yaitu 1-1,5 jam dengan suhu
III. METODOLOGI
A. BAHAN DAN ALAT
1. Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah meliputi
bahan baku utama dan bahan-bahan kimia. Bahan baku utama yang
digunakan adalah metil ester dari CPO. Bahan kimia yang diperlukan
untuk proses produksi surfaktan MES adalah H2SO4 teknis, NaOH,
metanol, H2O2. Adapun bahan-bahan kimia untuk analisa yaitu xylene,
etanol, larutan HCl, akuades, toluene, isopropil alkohol, alkohol, serta
bahan-bahan lain untuk analisis.
2. Alat
Alat-alat yang digunakan dalam penelitian ini adalah reaktor
sulfonasi empat leher dengan kapasitas 1 L skala laboratorium, kondensor,
separator, termometer, timbangan analitik, peralatan gelas, pipet, oven.
Peralatan untuk analisa yaitu densitometer, tensiometer Du Nuoy,
spinning drop interfacial tensiometer, microscope system, tabung reaksi,
vortex mixer, pipet, tabung ulir, stopwatch, chromameter dan hotplate
stirrer.
B. METODE PENELITIAN 1. Perlakuan dalam Penelitian
Pada penelitian ini dicoba pengaruh konsentrasi reaktan dan lama
reaksi terhadap produksi surfaktan dari metil ester sulfonat (MES) dengan
metode sulfonasi. Kondisi proses dan operasi produksi surfaktan MES
yang dikaji adalah konsentrasi H2SO4 (60, 70, 80 persen) dan lama reaksi
(60, 90, 120 menit).
2. Tata Laksana Penelitian
Penelitian dilakukan untuk memproduksi surfaktan dari metil ester
minyak sawit kasar (CPO) dengan menggunakan metoda sulfonasi. Proses
sulfonasi dilakukan dengan menggunakan reaktor empat leher dan
Proses sulfonasi dilakukan dengan memberikan perlakuan yang
berbeda terhadap konsentrasi reaktan (antara metil ester dan H2SO4) dan
lama reaksi dengan tiga taraf yang diujikan. Proses dilakukan secara
batch, dengan mencampurkan bahan baku dan pereaksi di dalam reaktor.
Penambahan H2SO4 dilakukan secara sedikit demi sedikit dengan kondisi
proses dalam pengadukan. Perbandingan mol metil ester dan H2SO4 yang
ditambahkan adalah 1:1,4. Selama proses berlangsung kecepatan
pengadukan pada hot plate stirer dan suhu reaksi dipertahankan stabil
pada nilai 1500 rpm dengan suhu 55-600 C.
Produk yang dihasilkan kemudian dimurnikan dengan menggunakan
pelarut metanol dan H2O2 pada suhu 55-600C. Proses pemurnian diawali
dengan menambahkan metanol ke dalam reaktor secara perlahan dan
berkesinambungan. Jumlah metanol yang ditambahkan adalah 60 persen
dari volume keseluruhan sistem. Setelah dilakukan penambahan metanol,
proses pemurnian dilanjutkan dengan penambahan H2O2 dengan cara yang
sama dengan volume H2O2 sebesar 10 persen dari volume keseluruhan
sistem.
Proses netralisasi dilakukan setelah diperoleh produk yang telah
terpisah dengan endapannya. Proses netralisasi dilakukan dengan cara
titrasi MES menggunakan NaOH 50 persen dengan suhu 55 – 600C.
C. RANCANGAN PERCOBAAN
Dalam penelitian ini digunakan rancangan percobaan acak lengkap
faktorial dengan dua faktor, yaitu lama reaksi (tiga taraf) dan konsentrasi
reaktan (tiga taraf). Pengulangan dilakukan dua kali. Model rancangan
percobaannya adalah:
Yijk = µ + Ai + Bj + (AB)ij + εk(ij)
Dimana:
Yijk = hasil pengamatan pada ulangan ke-k, lama reaksi ke-i dan
rasio konsentrasi reaktan ke-j
Ai = pengaruh lama reaksi ke-i (i = 1, 2, 3)
Bj = pengaruh rasio konsentrasi reaktan ke-j (i = 1, 2, 3)
(AB)ij = pengaruh interaksi lama reaksi ke-i dan rasio konsentrasi
reaktan ke-j εk(ij) = galat eksperimen
D. PARAMETER
Parameter yang diukur pada produk yang dihasilkan meliputi pH,
tegangan antarmuka (IFT), tegangan permukaan Du Nouy, stabilitas emulsi,
bilangan asam dan warna. Prosedur analisis parameter tersebut dapat dilihat
IV. HASIL DAN PEMBAHASAN
A. PROSES SULFONASI
Proses sulfonasi dilakukan dengan cara mencampurkan metil ester
dengan reaktan H2SO4 (dengan perbandingan rasio mol 1 : 1,4) ke dalam
reaktor empat leher. Basis massa yang digunakan adalah 100 ml metil ester
dengan konsentrasi H2SO4 adalah 60, 70, 80 persen. Proses sulfonasi diawali
dengan penetesan larutan H2SO4 secara perlahan ke dalam reaktor dengan
kondisi proses suhu berkisar antara 55-600C. Metil ester terlebih dahulu
dimasukkan ke dalam reaktor dan diaduk menggunakan stirer. Pengadukan
dimaksudkan agar H2SO4 yang ditambahkan dapat terdispersi secara merata
dengan metil ester. Adanya penetapan suhu reaksi sebesar 55-600C bertujuan
untuk mempercepat laju reaksi.
Proses sulfonasi dilanjutkan dengan tahap digestion, yakni membiarkan
reaksi berlangsung pada suhu dan lama reaksi yang telah ditentukan (60, 90,
120 menit). Pada tahap ini H2SO4 yang bereaksi dengan metil ester
diharapkan dapat berlangsung dengan maksimal.
Produk yang dihasilkan adalah MES dengan warna kehitaman. Warna
produk yang kehitaman diduga disebabkan adanya asam sulfat sisa reaksi dan
adanya perubahan molekul karena panas (golongan keton dan aldehid). Panas
dapat membuat minyak/ lemak menjadi hitam akibat proses oksidasi.
Oleh karena produk hasil sulfonasi (MES) berwarna kehitaman, maka
diperlukan proses pemurnian. Pemurnian bertujuan untuk menghilangkan
warna kehitaman yang tidak diinginkan. Proses pemurnian dilakukan dengan
menggunakan metanol 60 persen (v/v) dan untuk proses pemucatan digunakan
H2O2 10 persen (v/v). Metanol berfungsi untuk melarutkan air hasil samping
reaksi dan asam sisa yang tidak bereaksi. Air sebagai produk samping dapat
menghambat terjadinya reaksi sulfonasi (de Groot, 1991). Di samping itu
metanol juga dapat berfungsi untuk memperluas permukaan reaksi. Dengan
demikian diharapkan jumlah asam sulfat sisa dapat menurun. Proses
(1986) proses pemucatan dengan hidrogen peroksida banyak dilakukan pada
proses pemucatan minyak. Pemucatan tersebut menggunakan prinsip oksidasi.
MES hasil proses pemucatan selanjutnya dipisahkan dari produk
sampingnya dengan menggunakan labu pemisah. Proses pemisahan dilakukan
dengan cara MES dibiarkan dalam labu pemisah selama 24 jam. Produk
samping MES dapat berupa air, metanol, asam peroksida dan asam sulfat
yang tidak bereaksi. Selama pemisahan akan terbentuk dua lapisan cairan
yang terpisah. Lapisan cairan yang berada di bawah adalah produk samping
MES, sedangkan lapisan cairan yang berada di atas adalah MES. Proses
pemisahan selain berguna untuk pemisahan, juga berguna untuk menghemat
NaOH yang digunakan pada proses netralisasi. Hal ini disebabkan dalam
produk samping masih terdapat adanya asam sulfat sisa yang tidak bereaksi.
Proses netralisasi dilakukan dengan menambahkan NaOH ke dalam MES
dengan adanya variabel suhu yang telah ditetapkan. Suhu netralisasi yang
digunakan adalah 550C. NaOH yang ditambahkan akan bereaksi dengan MES
membentuk natrium-metil ester sulfonat yang menyebabkan pH larutan
menjadi netral. Efek samping dari proses netralisasi ini adalah terbentuknya
disodium karboksi sulfonat (disalt). Disalt adalah MES yang mengikat 2
kation Na+ pada gugus esternya. Keberadaan disalt akan menyebabkan
kelarutan MES dalam air dingin menjadi rendah, sifat detergensinya turun,
dan umur simpan lebih pendek.
B. ANALISIS PARAMETER
1. Nilai pH MES
Pengukuran nilai pH dari MES yang dihasilkan bertujuan untuk
melihat derajat keasaman dari surfaktan yang dihasilkan pada kondisi
proses yaitu pada suhu 55-600C. Metode yang digunakan adalah metode
kertas lakmus. Nilai hasil pengukuran menunjukkan kisaran pH MES
sebelum proses netralisasi adalah 2 hingga 5.
Hasil analisis keragaman dengan tingkat kepercayaan 95 persen
menunjukkan bahwa faktor konsentrasi berpengaruh nyata terhadap nilai
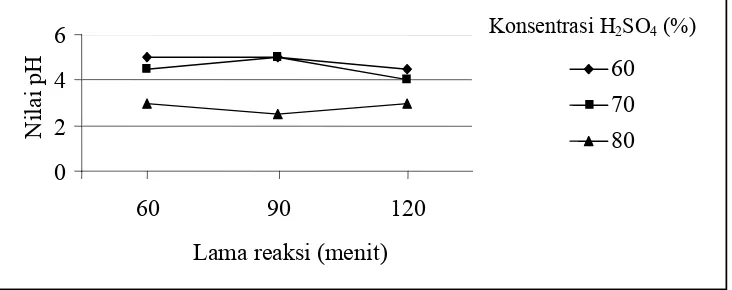
Grafik hubungan antara konsentrasi reaktan H2SO4 dan lama reaksi
terhadap nilai pH MES disajikan pada Gambar 3.
Gambar 3. Grafik hubungan antara konsentrasi reaktan H2SO4 dan lama
reaksi terhadap nilai pH MES
Dari grafik di atas terlihat bahwa nilai pH cenderung mengalami
penurunan seiring dengan semakin besarnya konsentrasi H2SO4 dan lama
reaksi. Penurunan nilai pH disebabkan karena makin besar jumlah
konsentrasi H2SO4 yang digunakan, sehingga kemungkinan terbentuknya
gugus sulfonat pada reaktan metil ester semakin besar. Demikian juga
dengan variabel lama reaksi. Makin lama waktu reaksi pada berbagai nilai
konsentrasi H2SO4, nilai pH cenderung turun. Hal ini menunjukkan bahwa
semakin lama waktu reaksi maka semakin besar pula kemungkinan
terbentuknya gugus sulfonat pada metil ester sehingga derajat keasaman
pun semakin tinggi yang ditunjukkan dengan semakin rendahnya nilai pH
MES. Keberadaan gugus sulfonat yang bersifat asam inilah yang
menyebabkan derajat keasaman semakin tinggi.
Hasil uji lanjut Duncan menunjukkan bahwa pengaruh konsentrasi
H2SO4 60 persen terhadap pH berbeda nyata dengan konsentrasi H2SO4 (70
dan 80 persen). Namun konsentrasi H2SO4 70 persen dan 80 persen tidak
2. Bilangan Asam
Bilangan asam adalah banyaknya mg KOH yang diperlukan untuk
menetralkan satu gram lemak atau minyak dengan prinsip pelarutan contoh
lemak/ minyak dalam pelarut organik tertentu (alkohol netral 95 persen)
yang dilanjutkan dengan penitrasian menggunakan basa (SNI
01-3555-1999).
Hasil pengukuran bilangan asam MES menunjukkan kisaran nilai 8,32
hingga 40,64 mg KOH/gr sampel (Lampiran 4). Dari data yang diperoleh,
nilai bilangan asam mengalami peningkatan. Nilai ini berbanding lurus
dengan nilai konsentrasi H2SO4 dan lama reaksi. Analisis keragaman
menunjukkan bahwa faktor konsentrasi dan lama reaksi berpengaruh nyata
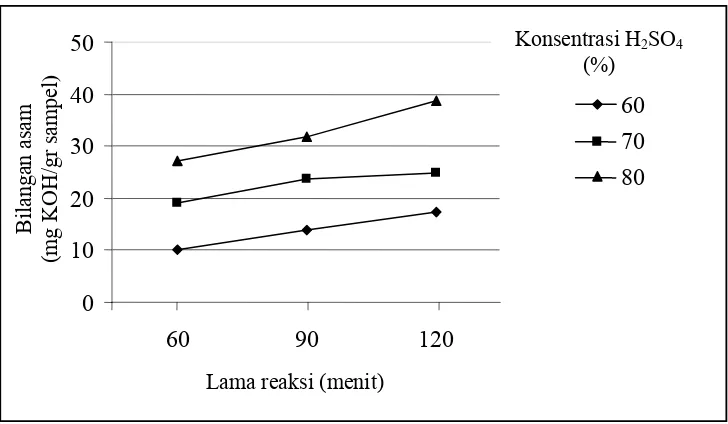
pada nilai bilangan asam (Lampiran 4). Grafik hubungan antara
konsentrasi H2SO4 dan lama reaksi terhadap nilai bilangan asam disajikan
pada Gambar 4. Konsentrasi H2SO4
(%)
Gambar 4. Grafik hubungan antara konsentrasi H2SO4 dan lama reaksi
terhadap nilai bilangan asam
Peningkatan bilangan asam yang berbanding lurus dengan faktor
konsentrasi H2SO4 dan lama reaksi diperkirakan karena semakin besar
jumlah konsentrasi H2SO4 dan lama waktu reaksi pembentukan gugus
sulfonat akan semakin tinggi. Keberadaan gugus sulfonat yang bersifat
teori Brownsted and Lowry, adanya ion H+ dalam suatu reaksi kimia
mengindikasikan adanya asam. Hal ini berakibat pada nilai derajat
keasaman yang semakin tinggi dan nilai bilangan asam yang meningkat.
Pengujian lebih lanjut dengan uji lanjut Duncan menyatakan bahwa
pengaruh konsentrasi H2SO4 terhadap peningkatan bilangan asam (60, 70,
80 persen) semuanya berbeda nyata. Hal yang sama juga ditunjukkan oleh
variasi lama reaksi. Lama reaksi (60, 90, dan 120 menit) menunjukkan
bahwa masing-masing nilai berbeda nyata.
3. Stabilitas Emulsi
Ada beberapa definisi mengenai emulsi. Namun pada dasarnya dapat
dinyatakan bahwa emulsi adalah dispersi atau suspensi cairan dalam cairan
lain yang tidak bercampur dalam keadaan biasa. Molekul kedua cairan
tersebut bersifat antagonistik yang disebabkan oleh perbedaan sifat
kepolarannya (Suryani et al., 2000). Emulsi terbentuk ketika suatu cairan
tidak saling melarut (immiscible) terpecah menjadi tetesan (droplet) dan
terdispersi ke cairan immiscible lainnya dengan bantuan surfaktan
(Hasenhuettl, 2000). Surfaktan dapat berperan sebagai emulsifier ketika
dua fasa yang berbeda derajat kepolaran dapat bercampur secara homogen.
Hal ini karena surfaktan mampu menyatukan dua fasa yang berbeda
derajat kepolarannya. Kemampuan surfaktan sebagai emulsifier didukung
dengan adanya gugus hirofilik dan hirofobik yang dimiliki molekul
surfaktan.
Pengujian stabilitas emulsi dilakukan pada air sebagai fasa polar dan
xylene sebagai fasa non polar. Hasil analisis keragaman menunjukkan
bahwa faktor konsentrasi berpengaruh nyata pada nilai kestabilan emulsi
(Lampiran 5). Lama reaksi dan faktor interaksi keduanya menunjukkan
nilai yang tidak berpengaruh nyata. Grafik nilai kestabilan emulsi dari
Gambar 5. Grafik pengaruh konsentrasi H2SO4 dan lama reaksi terhadap
kestabilan emulsi dari MES yang dihasilkan
Dari grafik tersebut terlihat bahwa nilai kestabilan emulsi cenderung
naik dengan peningkatan konsentrasi H2SO4 dan lama reaksi. Peningkatan
konsentrasi H2SO4 dan lama reaksi akan mempengaruhi pembentukan
gugus hidrofilik dan hidrofobik dari molekul surfaktan yang terbentuk.
Semakin besar nilai konsentrasi dan lama reaksi memungkinkan semakin
banyak pula gugus hirofilik yang terbentuk. Dengan demikian
terbentuknya surfaktan semakin besar pula, sehingga terjadi peningkatan
kestabilan emulsi. Efisiensi emulsifikasi dari surfaktan berhubungan
dengan polaritas pada molekulnya. Hal ini berkaitan dengan kontribusi
relatif dari gugus hidrofilik yang polar dan gugus hidrofobik yang non
polar (Jungermann, 1979).
Uji lanjut Duncan menyatakan bahwa konsentrasi H2SO4 (60 persen
dan 70 persen) tidak berbeda nyata pengaruhnya terhadap kestabilan
emulsi, namun berbeda nyata dengan konsentrasi H2SO4 80 persen.
Berdasarkan nilai kestabilan emulsi, hasil terbaik ditunjukkan oleh
perlakuan konsentrasi H2SO4 80 persen dengan lama reaksi 120 menit.
4. Tegangan Permukaan Metode Du Nouy
Terbentuknya tegangan permukaan pada suatu cairan disebabkan
karena adanya gaya tarik menarik antara molekul-molekul pada cairan
dengan udara (Durrant, 1953). Gaya tarik menarik antara molekul-molekul
pada molekul di permukaan cenderung menggerakkan
molekul-molekul tersebut menuju bagian pusat cairan sehingga menyebabkan cairan
berperilaku membentuk lapisan tipis. Gaya tersebut dihitung sebagai
tegangan permukaan.
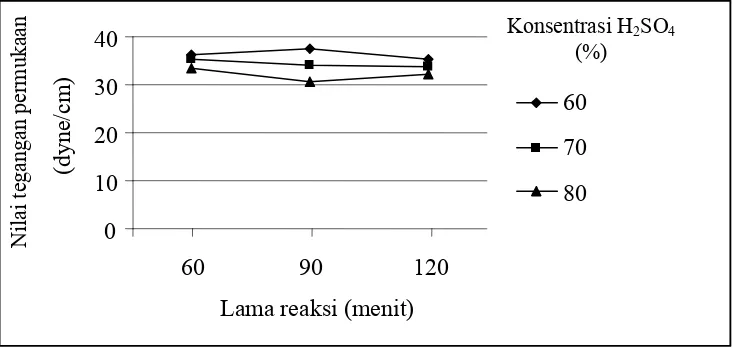
Hasil pengukuran tegangan permukaan air menunjukkan nilai 48,5
mN/m. Nilai ini sama dengan 48,5 dyne/cm. Setelah penambahan MES,
kisaran nilai yang didapatkan adalah 30,10 hingga 37,70 dyne/cm. Hal ini
berarti dengan adanya penambahan MES, nilai tegangan permukaan air
turun sebesar 10,8 hingga 18,4 dyne/cm. Penurunan nilai ini ekivalen
dengan nilai dalam persen sebesar 22,26-37,93 persen. Hasil analisis
keragaman menunjukkan bahwa faktor konsentrasi dan lama reaksi
berpengaruh signifikan terhadap nilai tegangan permukaan. Sedangkan
faktor interaksinya juga berpengaruh signifikan (Lampiran 6). Grafik nilai
tegangan permukaan air setelah penambahan MES disajikan dalam
Gambar 6.
ilai tegangan permukaan
(dyne/cm)
60
70
80
Konsentrasi H2SO4
(%)
Gambar 6. Grafik nilai tegangan permukaan MES
Berdasarkan grafik di atas, nilai tegangan permukaan cenderung
menurun dengan peningkatan konsentrasi H2SO4 dan lama reaksi. Hal ini
disebabkan dengan semakin tingginya nilai konsentrasi asam sulfat yang
digunakan, kemungkinan tumbukan antar partikel zat yang akan bereaksi
juga semakin besar. Dengan demikian kemungkinan terjadi reaksi juga
terikatnya gugus sulfonat dari asam sulfat pada atom karbon metil ester.
Semakin besar terikatnya gugus sulfonat pada rantai karbon akan
meningkatkan jumlah gugus hidrofilik dari MES. Gugus hidrofilik ini akan
menurunkan gaya kohesi dari molekul air sehingga akan menurunkan
tegangan permukaan.
Faktor lama reaksi juga berpengaruh terhadap penurunan tegangan
permukaan. Hal ini diperkirakan dengan semakin lama waktu reaksi,
kemungkinan terbentuknya surfaktan semakin besar. Tegangan permukaan
akan semakin menurun dengan semakin banyaknya molekul surfaktan
yang terbentuk (Cox et al.,1997). Selain itu, menurunnya tegangan
permukaan juga diduga karena adanya zat pengotor lain, selain surfaktan
yang dapat mempengaruhi gaya kohesi dari air sehingga dapat menurunkan
tegangan permukaan. Akan tetapi keberadaan zat pengotor ini tidak
memberikan pengaruh besar terhadap penurunan tegangan permukaan
(Chemistry, 2005).
Uji lanjut Duncan memperlihatkan bahwa masing-masing konsentrasi
H2SO4 (60, 70, 80 persen) berbeda nyata satu sama lain terhadap nilai
tegangan permukaan. Lama reaksi 120 menit berbeda nyata dengan lama
reaksi (60 dan 90 menit). Namun antara lama reaksi (60 dan 90 menit)
tidak berbeda nyata.
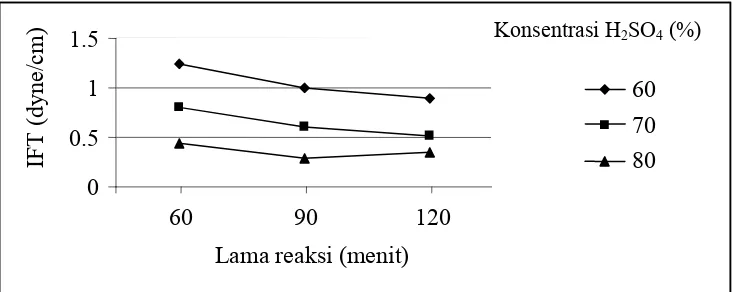
5. Tegangan Antar Muka (IFT)
Pengujian nilai tegangan antar muka dilakukan dengan menggunakan
dua jenis pelarut yang berbeda polaritasnya, yaitu air yang sangat polar
dengan minyak bumi yang bersifat tidak polar. Hasil pengukuran IFT
menunjukkan bahwa nilai IFT berbanding terbalik dengan nilai konsentrasi
H2SO4 dan lama reaksi. Hasil analisis keragaman menunjukkan bahwa
faktor konsentrasi dan lama reaksi berpengaruh signifikan terhadap nilai
IFT (Lampiran 7). Grafik hubungan nilai konsentrasi H2SO4 dan lama
Gambar 7. Hubungan nilai konsentrasi H2SO4 dan lama reaksi terhadap
nilai IFT
Berdasar grafik di atas, peningkatan konsentrasi H2SO4 dan lama
reaksi akan menurunkan nilai IFT. Semakin tinggi nilai konsentrasi asam
sulfat dalam larutan, konsentrasi air dalam larutan akan semakin
berkurang. Keberadaan air akan menghambat proses sulfonasi. Dengan
terbatasnya kadar air, kemungkinan tumbukan antar partikel yang akan
bereaksi semakin besar. Dengan demikian reaksi pembentukan gugus
sulfonat juga akan semakin tinggi. Hal ini didukung dengan waktu reaksi
yang semakin tinggi. Gugus sulfonat akan mengikat air pada gugus
hidrofiliknya yang menyebabkan gaya kohesi menurun dan sebaliknya
gaya adhesi semakin meningkat. Hal ini akan menyebabkan turunnya nilai
tegangan antar muka.
Pengujian lebih lanjut dengan menggunakan uji lanjut Duncan
menyatakan bahwa masing-masing konsentrasi H2SO4 (60, 70, 80 persen)
yang diuji masing-masing berbeda nyata terhadap IFT. Faktor lama reaksi
60 menit, 90 menit dan 120 menit masing-masing menunjukkan nilai yang
berbeda nyata pula terhadap IFT.
6. Uji Warna
Pengujian warna dilakukan dengan pendekatan Hunter Trimulus
Colorimeter. Warna didefinisikan sebagai distribusi energi dari sinar yang
dipantulkan oleh suatu obyek atau ditransmisikan oleh suatu obyek
nilai L, a dan b. Nilai L (lightness) menunjukkan tingkat kecerahan. Nilai
L berkisar dari nol hingga seratus (0-100). Semakin tinggi nilai L, tingkat
kecerahan dari warna yang diukur juga semakin tinggi. Pada tingkat nilai
L sama dengan nol, zat mampu seluruhnya menyerap spektrum cahaya.
Sedangkan pada tingkat nilai seratus, zat mampu seluruhnya memantulkan
spektrum cahaya. Nilai a menunjukkan kromatik warna (hijau-merah)
dengan parameter sebagai berikut. Nilai a negatif akan menunjukkan warna
hijau, nol adalah abu-abu, dan nilai a positif menunjukkan warna merah.
Nilai b menyatakan warna kromatik kuning apabila bernilai positif,
abu-abu apabila bernilai nol dan warna biru apabila bernilai negatif. Analisis
keragaman menunjukkan bahwa konsentrasi dan lama reaksi berpengaruh
nyata terhadap nilai L. Demikian pula dengan interaksi antar keduanya
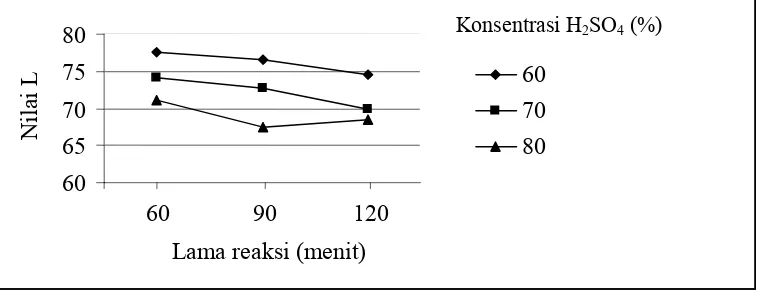
juga berpengaruh nyata terhadap nilai L. Grafik hubungan antara jumlah
konsentrasi dan lama reaksi terhadap nilai L dapat dilihat pada Gambar 8.
Gambar 8. Grafik hubungan antara jumlah konsentrasi dan lama reaksi
Dari g i atas, terlihat bahwa dengan semakin
men
77,90.
terhadap nilai L
ambar grafik d
ingkatnya konsentrasi H2SO4 dan lama reaksi akan menyebabkan
turunnya nilai L yang menunjukkan tingkat kecerahan. Dengan demikian
dengan meningkatnya konsentrasi H2SO4 dan lama reaksi akan
menyebabkan tingkat kecerahan warna dari surfaktan yang dihasilkan
Uji lanjut Duncan menyatakan bahwa nilai masing-masing konsentrasi
H2SO4 (60, 70, 80 persen) berbeda nyata terhadap masing-masing
kons
eragaman menunjukkan bahwa faktor konsentrasi dan
lama
0,80. Berdasarkan nilai tersebut, MES yang dihasilkan cenderung berwarna
hijau
enunjukkan bahwa faktor
konsentrasi berpengaruh nyata terhadap nilai b. Lama reaksi dan interaksi entrasi. Demikian halnya dengan lama reaksi, masing-masing waktu
reaksi yakni 60, 90 dan 120 menit berbeda nyata terhadap masing-masing
nilai lama reaksi.
Nilai a dan b merupakan parameter warna yang menyatakan cahaya
pantul. Analisis k
reaksi tidak berpengaruh nyata terhadap nilai a. Namun interaksi
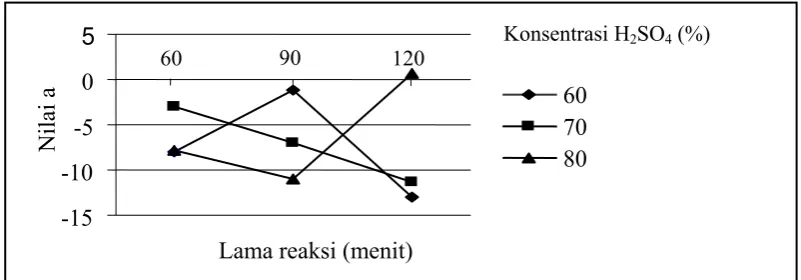
antara kedua faktor berpengaruh nyata terhadap nilai a. Grafik hubungan
antara jumlah konsentrasi dan lama reaksi terhadap nilai a dapat dilihat
pada Gambar 9.
Gambar 9. Grafik hubungan antara jumlah konsentrasi dan lama reaksi
terhadap nilai a
Dari pengukuran nilai a, rentang nilainya berkisar antara -13,07 hingga
. Berdasarkan grafik, dengan semakin meningkatnya konsentrasi
H2SO4 dan lama reaksi akan menyebabkan nilai a menjadi cenderung
turun. Walaupun ada beberapa nilai analisis nilai a yang menunjukkan
peningkatan. Dengan demikian dengan meningkatnya konsentrasi H2SO4
dan lama reaksi akan menyebabkan warna dari surfaktan yang dihasilkan
menjadi cenderung kromatis kuning kemerahan.
Hasil pengukuran nilai b menunjukkan bahwa nilai b berkisar antara
anta
asarkan kisaran nilai b, MES yang
diha
gus ester
dan
ra kedua faktor tidak berpengaruh nyata terhadap nilai b. Grafik
hubungan antara jumlah konsentrasi dan lama reaksi terhadap nilai b dapat
dilihat pada Gambar 10.
Gambar 10. Grafik hubungan antara jumlah konsentrasi dan lama reaksi terhadap nilai b
Dari gambar grafik di atas, terlihat bahwa dengan semakin
meningkatnya konsentrasi H2SO4 dan lama reaksi akan menyebabkan
terjadinya peningkatan nilai b. Berd
silkan berwarna kuning. Dengan demikian dengan meningkatnya
konsentrasi H2SO4 dan lama reaksi akan menyebabkan warna dari
surfaktan yang dihasilkan menjadi cenderung kromatis kekuningan.
Uji lanjut Duncan menyatakan bahwa konsentrasi H2SO4 70 persen
berbeda nyata terhadap konsentrasi H2SO4 (60 dan 80 persen). Namun
konsentrasi H2SO4 60 persen dan 80 persen tidak berbeda nyata.
Reaksi antara metil ester dengan asam sulfat membentuk
kecenderungan gugus sulfonat terikat pada atom karbon alfa walaupun
tidak menutup kemungkinan gugus sulfonat juga terikat pada gu
ikatan rangkapnya. Metil ester merupakan polimer hidrokarbon yang
memiliki gugus ikatan rangkap. Asam sulfat sendiri adalah oksidator kuat.
Reaksi asam sulfat dengan keberadaan oksigen pada sistem dapat
mengoksidasi ikatan rangkap pada metil ester. Teroksidasinya ikatan
rangkap metil ester akan menyebabkan terbentuknya gugus aldehid yang
bersifat polar. Keberadaan gugus ini akan memberikan warna gelap pada
V. KESIMPULAN DAN SARAN
KESIM
A. PULAN
Proses sulfona 4 dapat menghasilkan
surfaktan MES. MES yang dihasilkan berwarna kehitaman. Warna tersebut
dap ui proses pemurnian dengan menggunakan metanol dan
asam
/cm. Nilai tegangan antar muka (IFT) yang didapatkan
adal
B.
dihasilkan berwarna gelap sehingga diperlukan proses
pemurnian. Untuk itu, perlu didapatkan metode proses pemurnian MES yang
leb
si metil ester dengan pereaksi H2SO
at direduksi melal
peroksida. Berdasarkan hasil analisis, dapat disimpulkan bahwa kondisi
proses terbaik untuk memproduksi MES adalah perlakuan H2SO4 dengan
konsentrasi 80 persen dan lama reaksi 90 menit. Parameter untuk menentukan
perlakuan terbaik adalah dilihat dari kemampuan menurunkan tegangan
permukaan dan tegangan antar muka. Hal ini mengingat keberadaan surfaktan
identik dengan adanya kemampuan menurunkan tegangan permukaan dan
antar muka tersebut.
Karakteristik yang didapatkan dari MES yang dihasilkan dari perlakuan
ini adalah mampu menurunkan tegangan permukaan air hingga 37,93 persen
atau sebesar 18,4 dyne
ah 2,6 x 10-1 dyne/cm, dengan stabilitas emulsi sebesar 52,77 persen. Uji
warna menunjukkan nilai L sebesar 68,59 dengan nilai a sebesar -10.96 serta
nilai b sebesar 68.81.
SARAN
Metil ester yang
DAFTAR PUSTAKA
Bergenstahl, B. 1997. Physicochemical Aspect of an Emulsifier Functionality. In :
G. L. Hasenhuettl d Food Emulsifier and Their
Applications. Chapm
hemist hemistry.nz/surfactants.htm
an R. W. Hartel (Eds.). an & Hall, New York.
Bernardini, E. 1983. Vegetable Oils and Fats Processing. Volume II. Interstampa, Rome.
ry. 2005. Surface Active Agent.
C http://www.c .
oc. 74 (7) : 847 – 859.
e Groot hnology in the Detergent House. Kluwer
urrant, .,
oster, N ion Processes. In: Spitz, L. (Ed). Soap
asenhu iew of Food Emulsifier. In : G. L. Hasenhuettl dan
th
ungerm Oil and
th
Cox, M. F. and U. Weerasooriya. 1997. Methyl ester ethoxilates. J. of Am. Oil Chem. S
arnoko, D., T. Herawan dan P. Guritno. 2001. Teknologi Produksi Biodiesel dan
D
Prospek Pengembangannya di Indonesia. Warta PPKS, 9 (1) : 17 – 27.
, W. H. 1991. Sulphonation Tec
d
Academic Publisher, Netherland.
P. J. 1953. General and Inorganic Chemistry. Longmans, Green and Co D
London.
. C. 1996. Sulfonation and Sulfat
F
and Detergents: A Theoretical and Practical Review. AOCS Press, Champaign, Illinois.
Georgiou, G., C. L. Sung and M. M. Shara. 1992. Surface Active Compounds from Microorganism. Bio/tech 10 : 60 – 65.
ettl, G. L. 1997. Overv
H
R. W. Hartel (Eds.). Food Emulsifier and Their Applications. Chapman & Hall, New York.
Hasenhuettl, G. L. 2000. Design and Application of Fat-Based Surfactants. In : R. D. O’Brien, W. E. Farr, and P. J. Wan (Eds.). Introduction to Fat and Oils Technology. 2nd Edition. AOCS Press, Champaign, Illinois.
Hui, Y. H. 1996. Bailey’s Industrial and Fat Product. 5 edition. Vol. 3. John Willey & Sons, Inc., New York.
ann, E. 1979. Fat-Based Surface-Active agent. Bailey’s Industrial J
Fat Product. 14 editions. John Willey and Son, New York.
Kirk, R. E. And D. F. Othmer. 1964. Sulfonation and Sulfation. Di Dalam : Kirk-Othmer Encyclopedia of Chemical Technology. Vol. 19. Interscience
nnai, India.
n, Illinois.
ieger, M. M. (Ed). 1985. Surfactant in Cosmetics. Surfactant Science series,
adi, S. 1994. Gliserolisis Minyak Sawit dan Inti Sawit dengan Piridin. Buletin
haw, D. J. 1980. Introduction to Colloid and Surface Chemistry. Butterworths,
heats, W. B. and B. W. Mac Arthur. 2002. Methyl Ester Sulfonate Product. The Publisher, Inc., New York.
Libanan, A. 2000. Coconut Product Diversification and Processing
Cocochemicals. Proceeding of the XXXXVII Cocotech Meeting/ ICC 2000. 24 – 28 July 2000, Che
Matheson, K. L. 1996. Surfactant Raw Materials : Classification, Synthesis and Uses. In : Spitz, L. (Ed). Soap and Detergents : A Theoretical and Practical Review. AOCS Press, Champaig
Pore, J. 1993. Oils and Fats Manual. Intercept Ltd, Andover, Uk, Paris, New York.
R
Marcel Dekker, Inc. New York.
S
PPKS. 2 (3) : 155 – 164.
S
Oxford, England.
S
Chemiton Corporation. http://www.chemithon.com.
NI. 1999. Metil Ester. Badan Standarisasi Nasional, Standar Nasional Indonesia.
uryani, A.,E. Hambali., I. Sailah dan M. Rivai. 2000. Teknologi Emulsi. Jurusan
wern, D. 1979. Bailey’s Industrial Oil and Fat Products. 14th editions. John
atkins, C. 2001. All Eyes are on Texas. INFORM 12 : 1152 – 1159.
Yuliasar rawan. 1997. Asam Lemak Sawit Distilat
Sebagai Bahan Baku Pembuatan Sabun Transparan. Indonesian J. Of S
06-6048-1999.
S
Teknologi Industri-FATETA-IPB, Bogor.
S
Willey and Son, New York.
W
i, R., P. Guritno dan T. He
Oil Palm Research. 5 (3) : 205 – 213.
Lampiran 1. Diagram Alir Proses Sulfonasi
Metil Ester Dari CPO
Proses sulfonasi, suhu 550C dengan kecepatan pengadukan = 1500 rpm H2SO4 (%)
60, 70, 80
Pemucatan, suhu 550C dengan kecepatan pengadukan = 1500rpm
Pemisahan
Netralisasi, suhu 550C dengan kecepatan pengadukan=1500rpm
Asam sisa, air, metanol
NaOH 20%
Lampiran 2. Prosedur Analisis Surfaktan
1. Bilangan Asam (AOAC, 1995)
Minyak yang akan diuji ditimbang sebanyak 5 gram dalam labu erlenmeyer
250 ml dan ditambahkan 50 ml alkohol netral 95%, lalu dipanaskan selama
10 menit dalam penangas air sambil diaduk. Setelah ditambahkan 2 tetes
indikator penolphtalein 1%, larutan dititrasi dengan KOH 0,1 N sampai
berwarna merah jambu yang tidak hilang dalam beberapa detik. Selanjutnya
dihitung jumlah miligram KOH yang digunakan untuk menetralkan asam
dalam satu gram minyak atau lemak.
A x N x 56,1 Bilangan Asam =
G
Keterangan : A = ml KOH untuk titrasi
N = normalitas larutan KOH
G = berat contoh (gram)
2. Pengukuran pH (BSI, 1996)
Metode ini digunakan untuk menganalisa derajat keasaman (pH) surfaktan.
Nilai pH dari larutan contoh ditentukan dengan pengukuran menggunakan
kertas lakmus komersial. Nilai pH dibaca dengan mencelupkan kertas lakmus
pada larutan surfaktan. Pembacaan dilakukan dengan mencocokkan warna
yang terbaca dengan angka pada label.
3. Tegangan Permukaan (Metode DuNouy)
Metode pengujian ini dilakukan untuk menentukan tegangan permukaan
larutan surfaktan dengan menggunakan alat Tensiometer Du Nouy. Peralatan
dan wadah contoh yang akan digunakan harus dibersihkan terlebih dahulu.
Wadah yang digunakan biasanya terbuat dari bahan gelas dengan diameter
lebih besar dari 6 cm. Wadah gelas dicuci dengan larutan chromic-sulfuric
acid, kemudian dibilas dengan air destilata. Cincin platinum merupakan
digunakan, cincin dicuci terlebih dahulu dengan pelarut yang sesuai dan
dibilas dengan air destilata, lalu dikeringkan.
Posisi alat diatur supaya horisontal dengan water pass dan diletakkan pada
tempat yang bebas dari gangguan, seperti getaran, angin, sinar matahari dan
panas. Larutan contoh dimasukkan ke dalam gelas dan diletakkan di atas
dudukan (platform) pada Tensiometer. Suhu cairan sampel diukur dan dicatat.
Selanjutnya cincin platinum dicelupkan ke dalam sampel tersebut (lingkaran
logam tercelup 3-5 mm di bawah permukaan cairan), dengan cara menaikkan
dudukan (platform). Skala vernier Tensiometer di set pada posisi nol dan
jarum penunjuk harus berada pada posisi berhimpit dengan garis pada kaca.
Selanjutnya platform diturunkan perlahan, dan pada saat yang bersamaan
skrup kanan diputar sedemikian rupa sehingga jarum penunjuk tetap berimpit
dengan garis pada kaca. Proses ini diteruskan sampai film cairan tepat putus.
Pada saat cairan putus skala dibaca dan dicatat sebagai nilai tegangan
permukaan. Pengukuran dilakukan paling sedikit dua kali. Kemampuan
surfaktan dalam menurunkan tegangan permukaan dapat dilakukan dengan
menambahkan konsentrasi surfaktan sebanyak 10 persen (dalam air). Nilai
tegangan permukaan setelah ditambahkan surfaktan diukur kembali.
Kemudian dibandingkan nilai tegangan permukaan air dan sesudah
ditambahkan surfaktan.
4. Tegangan Antar Permukaan (Metode Spinning Drop)
Langkah awal, dibuat pelarut dari air formasi yang mengandung 2% alkohol
(isobutanol). Kemudian surfaktan ditimbang sebanyak x gram dan dilarutkan
ke dalam 50 ml pelarut, hingga dihasilkan larutan surfaktan MES dengan
konsentrasi 1,0 - 3,2% (b/b). Setelah itu larutan surfaktan diaduk
menggunakan magnetic strirrer sampai homogen. Selanjutnya larutan
surfaktan tersebut diukur tegangan antar permukaan minyak-air dengan
menggunakan alat Spinning Drop Interfacial Tensiometer.
Cara kerja Spinning Drop sebagai berikut : panaskan alat spinning drop,
kemudian set pada suhu 40oC (kondisi percobaan) dan periode pada 10,10
msec/rev. Setelah kondisi tersebut stabil, ke dalam glass tube diisikan larutan