AKTIVITAS ANTIOKSIDAN DAN ANTIINFLAMASI IN
VITRO SERTA KANDUNGAN KURKUMINOID DARI
TEMULAWAK DAN KUNYIT ASAL WONOGIRI
REZA WISNU KUSUMA
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
REZA WISNU KUSUMA. Aktivitas Antioksidan dan Antiinflamasi
In Vitro
Serta Kandungan Kurkuminoid dari Temulawak dan Kunyit Asal Wonogiri.
Dibimbing oleh SYAMSUL FALAH dan WARAS NURCHOLIS.
Penelitian ini menguji aktivitas antioksidan dan antiinflamasi dari kunyit dan
temulawak asal Wonogiri. Senyawa bioaktif yang berperan utama dalam
antioksidan dan antiinflamasi adalah kurkuminoid. Hasil penelitian sebelumnya
menyebutkan senyawa kurkuminoid terdapat pada temulawak dan kunyit.
Pengujian aktivitas antioksidan menggunakan metode DPPH (
2,2-difenil-1-pikrilhidrazil
). Dari hasil pengujian didapatkan potensi antioksidan temulawak
Wonogiri lebih tinggi dibandingkan kunyit Wonogiri. Nilai IC
50yang didapatkan
sebesar 53.13 ppm untuk temulawak Wonogiri dan sebesar 61.72 ppm untuk
kunyit Wonogiri. Aktivitas antiinflamasi dianalisis dengan metode inhibisi enzim
COX-2 secara
in vitro
. Hasil yang diperoleh menunjukkan daya inhibisi terbaik
terhadap COX-2 ialah sampel kunyit Wonogiri sebesar
47.45% sedangkan
temulawak Wonogiri sebesar 87.19%. Kandungan kurkuminoid pada kunyit dan
temulawak diukur menggunakan
High Performance Liquid Chromatography
(HPLC)
.
Dari hasil pengukuran didapatkan kandungan kurkuminoid pada kunyit
sebesar 74.57 mg/g dan temulawak sebesar 20.04 mg/g.
ABSTRACT
REZA WISNU KUSUMA. In Vitro Antioxidant and Anti-inflamantory Activity
and Curcuminoid Contents of
Curcuma xanthorrhiza
RoxB. and
Curcuma
domestica
Val. From Wonogiri. Supervised by SYAMSUL FALAH and WARAS
NURCHOLIS.
This research examined antioxidant and anti-inflamantory activities of
Curcuma xanthorrhiza
RoxB. and
Curcuma domestica
Val. from Wonogiri. The
main bioactive compounds functioning as antioxidant and anti-inflamantory are
curcuminoid. The previous research reported that curcuminoid compound is
present in
C. xanthorrhiza
RoxB. and
C. domestica
Val. The antioxidant potency
of the sample was detected by DPPH (
2,2-difenil-1-pikrilhidrazil
) method. Results
showed that the antioxidant potency of
C. xanthorrhiza
RoxB. is higher than that
of
C. domestica
Val. from Wonogiri. IC
50value of
C. xanthorrhiza
RoxB. was
53.13 ppm and
C. domestica
Val. Was 61.72 ppm. Anti-inflamantory activity was
analyzed by
in vitro
cyclooxygenase 2 (COX2) inhibition method. The best
inhibition activity against of COX2 is showed by
C. domestica
Val. in amount of
47.45% and value of
C. xanthorrhiza
RoxB is 87.19%. Curcuminoid Content of
C. xanthorrhiza
RoxB. and
C. domestica
Val. was measured by High Performance
Liquid Chromatography
(HPLC). Results showed that curcuminoid content of
C.
domestica
Val. was 74.57 mg/g and
C. xanthorrhiza
RoxB. was 20.04 mg/g.
Key word
: Curcuminoid, antioxidant, anti-inflamantory,
Curcuma xanthorrhiza
AKTIVITAS ANTIOKSIDAN DAN ANTIINFLAMASI IN
VITRO SERTA KANDUNGAN KURKUMINOID DARI
TEMULAWAK DAN KUNYIT ASAL WONOGIRI
REZA WISNU KUSUMA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Biokimia
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Aktivitas Antioksidan dan Antiinflamasi
In Vitro
serta
Kandungan Kurkuminoid dari Temulawak dan Kunyit Asal
Wonogiri
Nama
: Reza Wisnu Kusuma
NRP
: G84080060
Disetujui
Komisi Pembimbing
Dr. Syamsul Falah, S.Hut, M.Si Waras Nurcholis, S.Si, M.Si
Ketua
Anggota
Diketahui
Dr. Ir. I Made Artika, M.App. Sc.
Ketua Departemen Biokimia
PRAKATA
Puji dan syukur kita panjatkan kepada Tuhan Yang Maha Esa yang telah
memberikan rahmat dan kemudahan dalam penyusunan karya ilmiah hasil
penelitian ini yang berjudul Aktivitas Antioksidan dan Antiinflamasi Secara
In
Vitro
Serta Kandungan Kurkuminoid Dari Temulawak dan Kunyit Asal Wonogiri.
Penelitian ini dilaksanakan pada bulan November 2011 hingga Februari 2012 di
Laboratorium Pusat Studi Biofarmaka IPB, Institut Pertanian Bogor. Penelitian ini
merupakan bagian dari Kegiatan Penelitian Hibah Kompetitif tingkat Nasional.
Ucapan terima kasih penulis sampaikan kepada Dr. Syamsul Falah, S.Hut,
M.Si dan Waras Nurcholis, M.Si selaku komisi pembimbing atas segala
kesabarannya dalam memberikan bimbingan, arahan serta masukan kepada
penulis dalam penyusunan karya ilmiah ini. Ucapan terima kasih juga
dipersembahkan kepada kedua orang tua penulis yaitu Bapak U. Dahlan dan Ibu
Yanti Suriaatmadja beserta kakak Vika Dahlianti yang tidak pernah berhenti
memberikan dukungan moril maupun materiil sehingga karya ilmiah hasil
penelitian ini dapat diselesaikan dengan baik. Penulis juga menyampaikan ucapan
terima kasih kepada Prof. Dr. Ir. Latifah K Darusman selaku Kepala Pusat Studi
Biofarmaka IPB yang telah mengijinkan penulis melaksanakan kegiatan penelitian
di laboratorium PSB, serta seluruh staf laboratorium PSB, khususnya Ibu Nunu,
Mbak Wiwik, Mas Endi, dan Pak Zaim. Atas bantuan teknis dan saran yang
diberikan selama penelitian. Penulis menyampaikan terima kasih kepada seluruh
dosen dan staf Departemen Biokimia IPB atas bantuan dan saran yang telah
diberikan.
Penulis juga mengucapkan terima kasih kepada Nurul Syifa, Ni Luh Putu
Eka Kartika Sari, David Akbar, Rizka Arusima, Mas Anggara, Mas Harry dan
Mas Anjar atas doa, semangat, dukungan moril ataupun materiil serta segala
motivasi untuk selalu berusaha menjadi lebih baik. Semoga karya ilmiah ini dapat
memberikan manfaat bagi seluruh pembaca serta dapat menjadi langkah awal
penulis untuk berjalan mencapai impiannya.
Bogor, Agustus 2012
RIWAYAT HIDUP
Reza Wisnu Kusuma merupakan anak kedua dari ayah Ujang Dahlan dan
Ibu Yanti Suriaatmadja yang lahir pada 11 Januari 1990. Penulis menyelesaikan
pendidikan jenjang menengah atas di SMA Negeri 3 Bogor, Jawa Barat pada
tahun 2008. Pada tahun yang sama penulis melanjutkan pendidikan di
Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut
Pertanian Bogor (IPB) melalui jalur Ujian Saringan Masuk IPB (USMI)
Selama mengikuti kegiatan perkuliahan, penulis pada tahun 2010 mendapat
kesempatan untuk mengikuti kegiatan PKM-P (Program Kreatifitas Mahasiswa
bidang Penelitian) yang didanai oleh Dikti. Pada tahun 2011 penulis
melaksanakan kegiatan praktik lapang di Laboratorium Sistematika Molekuler
LIPI dengan karya ilmiah yang berjudul Isolasi dan Amplifikasi DNA Untuk
Mengkaji Keragaman Populasi Tumbuhan Taka.
DAFTAR ISI
Halaman
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Kunyit
(Curcuma domestica
Val.) ... 1
Temulawak
(Curcuma xanthorrhiza
Roxb) ... 2
Kurkuminoid ... 2
Radikal Bebas ... 3
Senyawa Antioksidan ... 3
Metode
2,2 diphenyl-1-picryl-hydrazil
(DPPH) ... 4
Inflamasi ... 4
BAHAN DAN METODE
Bahan dan Alat ... 5
Metode Penelitian ... 5
HASIL DAN PEMBAHASAN
Ekstraksi Sampel ... 7
Kadar Kurkuminoid Ekstrak Rimpang Temulawak dan Kunyit Wonogiri ... 7
Aktivitas Antioksidan Ekstrak Rimpang Temulawak dan Kunyit Wonogiri ... 8
Aktivitas Antiinflamasi Ekstrak Rimpang Temulawak dan Kunyit Wonogiri ... 9
DAFTAR PUSTAKA ... 10
LAMPIRAN ... 12
SIMPULAN DAN SARAN ………... 9
DAFTAR GAMBAR
Halaman
1 Rimpang Kunyit ... 2
2 Rimpang Temulawak ... 2
3 Struktur Kimia Kurkuminoid ... 3
4 Format
Micro plate
Inhibisi COX-2 ... 6
5 Kadar Kurkuminoid Ekstrak Etanol Temulawak dan Kunyit Wonogiri ... 8
6 Nilai Absorbansi DPPH oleh sampel Temulawak dan Kunyit ... 8
7 Aktivitas Penghambatan Radikal Bebas DPPH pada Temulawak dan Kunyit .. 9
8 Aktivitas Penghambatan COX-2 oleh Temulawak dan Kunyit Wonogiri ... 9
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 12
2 Prosedur ekstraksi (BPOM 2005) ... 13
3 Uji aktivitas antioksidan dengan metode DPPH ... 14
4 Preparasi larutan untuk uji inhibisi COX-2 ... 15
5 Kadar air ekstrak kunyit dan temulawak Wonogiri ... 16
6 Rendemen hasil ekstraksi ... 17
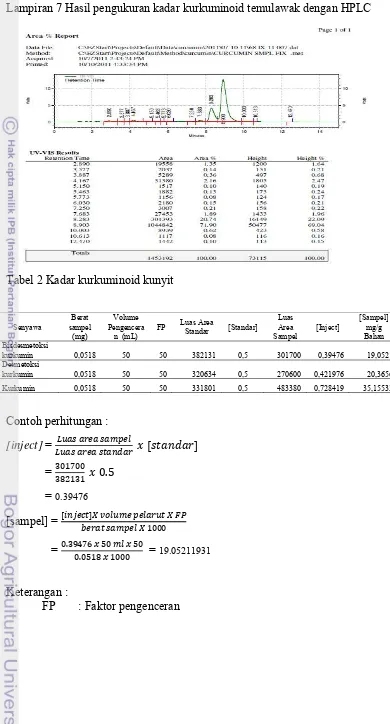
7 Hasil pengukuran kadar kurkuminoid temulawak dengan HPLC... 18
8 Hasil pengukuran kadar kurkuminoid kunyit dengan HPLC ... 19
9 Data absorban ekstrak temulawak wonogiri ... 21
10 Data absorban ekstrak kunyit wonogiri... 22
11 Grafik hubungan % inhibisi dengan konsentrasi sampel ... 23
12 Nilai IC50 masing-masing sampel ... 24
13 Kurva standar uji inhibisi COX-2 ... 25
14 Data uji daya inhibisi ekstrak rimpang temulawak dan kunyit Wonogiri…….26
PENDAHULUAN
Indonesia merupakan Negara agraris terbesar di dunia.Hal ini tentu membuat Indonesia memiliki berbagai tanam-tanaman yang memiliki berbagai potensi, salah satunya sebagai obat.Indonesia yang dikenal sebagai negara dengan megabiodiversitas, memiliki keanekaragaman hayati flora dan fauna yang sangat melimpah.Dari 28.000 jenis tumbuhan yang ditemukan di Indonesia, kurang lebih 7.000 jenis di antaranya adalah tumbuhan obat (Kassahara & Hemmi 1986).
Penggunaan tanam-tanaman sebagai obat tradisional ternyata telah lama dikenal oleh masyarakat Indonesia jauh sebelum pelayanan kesehatan menggunakan obat-obatan sintetik.Peningkatan penggunaan obat-obatan tersebut seiring dengan peningkatan kesadaran masyarakat terhadap dampak negatif dari penggunaannya.Masyarakat kembali memilih tanaman obat sebagai alternatif terhadap penyembuhan berbagai penyakit.Selain itu, efek samping yang ditimbulkan juga lebih kecil.Hal tersebut memicu peneliti untuk melakukan penelitian di bidang biofarmaka, yaitu mengenai obat-obatan alami yang berasal dari tumbuhan.
Tumbuhan obat adalah kelompok tumbuhan yang umumnya digunakan sebagai obat dan sumber bahan baku obat. Pemanfaatan lain dari tumbuhan obat adalah sebagai bumbu masak, makanan, minuman, kosmetik, dan parfum (Wahid & Sudarno 1993). Tumbuhan obat yang digunakan biasanya dalam bentuk simplisia yang berupa akar, daun, buah, dan biji. Temulawak
(Curcuma xanthorriza Roxb.) merupakan
salah satu tumbuhan obat suku Zingiberaceae yang banyak tumbuh di Indonesia (Sidik et al 1995).
Temulawak diketahui memiliki banyak manfaat antara lain sebagai antihepatitis, antikarsinogenik, antimikroba, antioksidan, antihiperlipidemia, antiviral, antiinflamasi, dan detoksifikasi (WHO 1999). Selain itu, temulawak merupakan sumber bahan pangan, pewarna, bahan baku industri seperti kosmetika, maupun dibuat makanan atau minumansegar (Dalimartha 2000). Kunyit merupakan salah satu tanaman herbal yang dapat menangkal radikal bebas.Kunyit mengandung komponen aktif yang berfungsi sebagai antioksidan.Komponen aktif dalam kunyit yang berperan adalah kurkuminoid.Komponen ini juga terdapat pada beberapa jenis temu-temuan lain seperti temulawak. Kurkuminoid adalah komponen yang memberikan warna kuning yang bersifat
sebagai antioksidan dan berkhasiat antara lain sebagai hipokolesterolemik, kolagogum, koleretik, bakteriostatik dan spasmolitik. Berbagai penelitian telah membuktikan khasiat kurkuminoid dalam pengobatan terutama sebagai antihepatoksik dan antikolesterol, serta obat tumor dan kanker (Nagabhushan & Bhide 1992).Kunyit dan temulawak memiliki potensi sebagai antioksidan dan antiinflamasi.Antioksidan ini berfungsi untuk menghambat terjadinya penyakit degeneratif karena radikal bebas.Potensi antiinflamasi dari kedua sampel tersebut dapat menghambat terjadinya peradangan.
Sampel pada penelitian ini berasal dari Wonogiri.Wonogiri merupakan salah satu daerah budidaya kunyit dan temulawak yang berada di Jawa Tengah.Tujuan penelitian ini adalah mendapatkan nilai aktivitas antioksidan dan antiinflamasi terbaik yang ditandai dengan %inhibisi terbesar dan nilai konsentrasi ppm terkecil serta kandungan kurkuminoid dari kedua sampel.
Hipotesis penelitian ini adalah kunyit dan temulawak memiliki nilai aktivitas antioksidan dan antiinflamasi yang berbeda walaupun berasal dari daerah yang sama. Penelitian ini diharapkan dapat memberikan informasi potensi aktivitas antioksidan dan antiinflamasi dari kunyit dan temulawak yang berasal dari Wonogiri.
TINJAUAN PUSTAKA Kunyit
Indonesia sebagai negara tropis yang dikenal dengan biodiversitas terbesar kedua di dunia, memiliki banyak tanaman yang diketahui secara empiris berkhasiat sebagai obat.Kunyit merupakan salah satu jenis tumbuhan yang secara umum banyak digunakan sebagai obat, baik dalam bentuk tunggal maupun kombinasi campuran. Penggunaan kunyit tidak hanya sebatas sebagai bumbu untuk menambah rasa dan memberi warna, tetapi juga sebagai bahan baku minuman sehat seperti kunyit asam atau kunyit instan. Secara empiris kunyit banyak digunakan sebagai obat mag, penurun kolesterol, diare, nyeri haid, sakit kuning, dan obat luka.
rimpang.Ke sekitar 16 c rimpang mu Tiap rumpu rimpang ant 11-15 tanam tergolong d Spermatoph kelas Mono suku Zingi spesies Cur kunyit dapa yang berkis hujan 1500-Kunyit m berperan seb dalam ku kurkuminoid pada bebera temu lawak yang memb sebagai anti sebagai koleretik, b zat antioksi diketahui cu telah mem dalam pe antihepatoks tumor dan 1992).Komp menghamba mempunyai kunyit juga kanker usus Gambar Temula berupa tumb Indonesia te nama daerah koneng ged koneng, ko temulobak ( (Sulawesi S
dalaman rim cm, panjang uda 1,61 cm da un tanaman k
tara 7-10 buah man(Gambar 1 dalam kingd hyta, sub di ocotyledonae,
iberaceae, ge
rcuma xanthor at hidup deng sar antara 20
2000 mm/tahu mengandung k bagai antioksi unyit yang
d.Komponen apa jenis temu k. Kurkumino
erikan warna ioksidan dan b hipokolestero bakteriostatik, idan dalam re ukup tinggi. mbuktikan kh
engobatan sik dan antik
kanker (Nag ponen fenolik at pertumbu aktivitas anti a dapat me , payudara, pa
1 Rimpang K
Temul awak merupa buhan rumpun emulawak dik
h, misalnya te de, temu raya oneng tegel, (Madura), tom Selatan) atau T
mpang dalam akar 22,5 cm an rimpang tu kunyit dapat h, dan anakan 1). Tumbuhan dom Plantae,
ivisi Angiosp ordo Zingib enus Curcum rrhiza Val. T gan baik pad 0-300C dengan
un (Rukmana komponen ak idan. Kompon berperan ini juga t u-temuan lain id adalah kom
kuning yang berkhasiat ant omik, kola spasmolitik, empah- remp Berbagai pe hasiat kurku terutama kolesterol, ser
gabhushan & k dalam kuny uhan kanke imutagenik.Se
nekan pertum aru-paru, dan k
Kunyit
lawak akan tanaman n berbatang se enal dengan b emulawak (Su a, temu be
temulawak mmo (Bali), t Ternate denga
m tanah m, tebal ua 4 cm.
tumbuh n antara n kunyit , divisi permae, berales,
ma dan
Tanaman da suhu n curah 2008) ktif yang nen aktif adalah terdapat n seperti mponen bersifat tara lain agogum, , Kadar ah juga enelitian uminoid sebagai rta obat & Bhide yit dapat r dan elain itu mbuhan kulit.
n obat emu. Di berbagai umatra), sar, aci (Jawa), tommon an nama karbaga (Dal dari bahasa a sedangkan x Yunani xanto yang berarti botani, temul Plantae, div Angiospemae Zingiberales, Curcuma d xanthorrhiza alami temula lahan - lahan sinar matah tanaman ini t pohon bamb temulawak ju terik, seperti d
Tanaman tinggi terhad beriklim trop budidaya tana Tim Lentera curah hujan mm/tahun. T dataran renda 750 meter d Sudarman da bahwa temu ketinggian 1 laut. Deng temulawak c atas. Wala memilih jeni namun temul pada tanah y 1985).
Temulawa yang tumbuh dari 1 m tet hijau atau terbentuk de kuat, berwar mempunyai d bundar mem warna daun h sampai gelap lebar 10-18 termasuk hela termasuk tipe dari pelepah daun. Perbun sisik berbentu cm dan leba banyak yan sebanding de bunga berwa mm, mahkota
limartha 2000 arab kurkum y xanthorriza b
os yang berar akar. Sesuai lawak termas visi Spermato
e, kelas Mon famili Zin dan nama
Roxb. (Ruk
awak tumbuh n yang teduh hari.Di habita
tumbuh subur bu dan jati.M uga dapat tum
di tanah tegala ini memiliki dap berbagai pis.Suhu udar aman ini antar
2003).Tanam n tahunan a Temulawak ah dan tinggi, di atas permu an Harsono ( ulawak dapa 800 meter d gan perakara epat menguru aupun temula s tanah untuk lawak akan t yang subur d
akmerupakan tegak dengan tapi kurang d coklat ge engan sempur
rna hijau g daun 2 -9 he manjang samp hijau atau cok p, panjang da
cm, panja aian 43 -80 cm e daun sempur
daun, tangk gaan lateral, t uk garis, pan ar 4-6 cm, ng panjangny
engan mahko arna putih ber a bunga berbe
0). Curcuma b yang berarti k
erasal dari b rti kuning dan
dengan klas suk dalam kin ophyta, sub nocotyledonae
ngiberaceae, spesies Cu kmana 2006).
h dengan ba dan terlindun at alami, ru r di bawah na Meskipun dem mbuh di tempa
an.
daya adaptas i cuaca di ra yang baik
ra 19-30° (Af man ini meme antara 1.500 dapat tumbu , sampai ketin ukaan laut, b (1980) meny at tumbuh h
di atas perm an yang da uskan lapisan awak tidak k tempat hidu tumbuh sanga dan gembur (W
tumbuhan ta n tinggi hingga dari 2 m, ber lap.Akar rim rna dan berc elap. Tiap b elai dengan b pai bangun klat keunguan aun 31-84 cm ang tangkai m(Gambar 2) rna, artinya te kai daun, dan tangkai rampin njang tangkai berdaun peli ya melebihi ota bunga. K
rbulu, panjang entuk tabung d
2
panjang kes berbentuk b dengan ujun merah, panj (Sidik et al
Gambar
Kurkumi zat yang t senyawa kur Kurkuminoi kuning jingg sedikit pah asam asetat Kurkumin ti Kurkuminoi tidak bersifa Sifat kim menarik ada perubahan asam, kurk kuning jingg berwarna m sifat kurkum selain terjad basa kurkum membentuk Degradasi i dalam lingk yang relatif berarti bah singkat tid karena pros juga oleh s degradasi, warna ku mempengaru terjadi. Sifa adalah akti kurkumin dekomposis kurkumin (Tonnesen & Kurkumi kurkumin, seluruhan 4.5 bundar meman ng yang berwa jang 1.25-2
1995).
2 Rimpang T
Kurk inoid rimpang erdiri atas c rkumin dan d id mempunya ga, berbentuk hit, larut dala
t glasial, dan idak larut dal id mempunya at toksik (Kiso mia kurkumino
alah sifat peru pH lingkung kuminoid ber
ga, sedangkan merah. Keunik min dalam su di proses dis
min dapat m asa ferulat ini terjadi bi kungan pH 8,5 f lama, wala hwa dalam
ak terjadi d ses degradasi
uhu lingkung yaitu ferulo uning cok uhi warna me at kurkuminoi ivitasnya terh
terkena cah i struktur atau terjadi & Karsen 1985
inoid memili desmetoksi
5 cm, helaian njang berwarn arna merah da cm dan leba
emulawak
kuminoid g kunyit adala campuran kom desmetoksi ku ai warna kuni k serbuk deng
am aseton, a n alkali hidr am air dan di ai aroma kh o 1985).
oid (Gambar ubahan warna gan. Dalam rwarna kunin n dalam suasa kan lain terja uasana basa, osiasi, pada mengalami de
dan ferulloi ila kurkumin 5 – 10,0 dalam aupun hal in
waktu yang degradasi ku i sangat dipe gan. Salah sa ilmetan mem klat yang
erah yang seh id lain yang hadap cahay haya, akan
berupa s degradasi 5).
ki 3 senyawa i kurkumin
n bunga na putih adu atau ar 1 cm
ah suatu mponen urkumin. ing atau gan rasa alkohol, roksida. ietileter. as, dan 3) yang a akibat susana ng atau ana basa adi pada karena suasana egradasi ilmetan. berada m waktu ni tidak relatif urkumin, engaruhi atu hasil mpunyai akan harusnya penting ya. Bila terjadi siklisasi struktur a, yaitu n dan bisdemetoksi Kurkumin C21H20O6 d
g/mol,sedang mempunyai r bobot molek molekul untu C19H16O4 den
(Gambar 3).
R1 R2
Keterangan: R1 R2
-OCH3 -OC
-OCH3 -H
-H -H
Gambar Radikal b reaktif karen berpasangan dapat bereak dengan cara dan menyeb menghasilkan bebas dapat baik kompon membran) m yaitu enzim d
Radikal molekul yan sehingga u elektron sen merusak jarin mekenisme b bila radikal enzim atau menyebabkan (Anies 2009)
Radikal b cara, yaitu Secara eksog polusi luar m makanan, d endogen radik menerus pa konsekuensi d sistem transp seperti sikl kurkumin mempunyai dengan bobo gkan rumus moleku kul sebesar 3 uk bisdemetok ngan bobot m
H3 = kurkum
= demeto = bisdem
r 3 Struktur ki (Basnet 20
Radikal B bebas adalah m na memiliki e
pada orbital ksi dengan m
mengikat ele babkan reak n radikal be bereaksi den nen struktural maupun kom dan DNA (Wid bebas meru ng sifatnya s untuk memp nyawa ini s
ngan. Sebena biokimia tubu
bebas sempa lemak tak j n kerusakan
.
bebas dapat di secara eksog gen radikal b melalui jalan p
dan penyerap kal bebas dipr ada tubuh
dari metabolis ort normal, da looksigenase.
(Afifah rumus m ot molekul demetoksikur ul C20H18O5 d
338 g/mol. R ksikurkumin molekul 308 min oksikurkumin metoksikurkum imia kurkumin 011) Bebas molekul yang elektron yang l luarnya seh molekul sel ektron sel ter ksi berantai ebas baru. R ngan kompon (molekul pen mponen fung djaja 1997). upakan atom sangat tidak peroleh pas sangat reakti arnya, radikal
uh normal. N at bertemu d jenuh, maka
awal pada
ibentuk melal gen dan end bebas didapa pernafasan, di pan kulit.
roduksi secara manusia s sme normal m an aktivitas ok
4
diproduksi di dalam sel oleh mitokondria, membran plasma, lisosom, peroksisom, retikulum endoplasma, dan inti sel.
Beberapa kerusakan yang dapat timbul oleh serangan radikal bebas antara lain kerusakan protein, DNA, peroksidasi lipid, kerusakan membran sel terutama penyusun membran yang berupa asam lemak tidak jenuh yang merupakan bagian dari fosfolipid dan mungkin juga protein, menimbulkan autoimun, dan proses penuaan. Akan tetapi, radikal bebas tidak selalu merugikan. Misalnya, radikal bebas berperan dalam pencegahan penyakit yang disebabkan mikrobia melalui sel-sel khusus yang disebut fagosit (Tuminah& Sulistiyowati 2000).
Salah satu target dari serangan radikal bebas dalam sel makhluk hidup adalah lipid dari membran sel, terutama asam-asam lemak tidak jenuh. Reaksi oksidasi lipid terbagi menjadi tiga tahap yaitu inisiasi, propagasi, dan terminasi.
Senyawa Antioksidan
Secara alamiah tubuh manusia mempunyai pertahanan endogen untuk meredam dampak negatif radikal bebas yaitu berupa senyawa antioksidan. Antioksidan adalah suatu senyawa yang dapat menetralkan dan melawan zat toksik (radikal bebas) dan menghambat terjadinya oksidasi pada sel sehingga mengurangi terjadinya kerusakan sel. Berdasarkan sumbernya antioksidan dapat digolongkan menjadi dua golongan, yaitu antioksidan sintetik dan alami. Antioksidan sintetik diperoleh dari hasil sintesa reaksi kimia, seperti butylated hydroxyanisole (BHA) dan butylated hidroxytoluene (BHT) sangat efektif dalam menghambat reaksi oksidasi lemak. Akan tetapi, penggunaan antioksidan sintetik telah diketahui memiliki efek samping yang berbahaya antara lain menyebabkan kerusakan hati. Antioksidan alami diperoleh dari hasil ekstraksi bahan alami. Senyawa antioksidan alami antara lain seperti flavonoid, vitamin E, C, dan beta-karoten dapat diperoleh dari sumber-sumber alami seperti pada rempah, herbal, sayuran, dan buah. Senyawa alami memiliki kelebihan karena kemungkinan lebih aman untuk dikonsumsi (Kikuzaki & Nakatani 1993).
Antioksidan dapat berupa enzim atau zat bukan enzim. Antioksidan berupa enzim (yang terdapat dalam tubuh) adalah katalase, superoksida dismutase, dan glutation peroksidase. Zat scavenger (pembersih) nonenzim adalah vitamin E, vitamin A, vitamin C, beta-karoten, metionin, selenium,
dan tirosin. Berdasarkan mekanisme pencegahan dampak negatif radikal bebas, antioksidan dapat dibagi menjadi dua golongan yaitu, antioksidan pencegah yang mengurangi kecepatan inisiasi (permulaan) rantai reaksi, dan antioksidan pemecah rantai yang akan memotong perbanyakan reaksi berantai (Murrayet al 2003). Proses penghambatan oksidasi lipid oleh antioksidan terjadi melalui berbagai mekanisme yaitu pemberian elektron, pemberian hidrogen, penambahan lipid pada cincin aromatik antioksidan dan pembentukan komplek antara lipid dan cincin aromatik antioksidan (Ketaren 1986).
Vitamin E (α- tokoferol) adalah senyawa antioksidan yang bersifat lipofilik, dapat bekerja pada membran sel dan lipoprotein sebagai donor ion hidrogen sehingga radikal bebas menjadi molekul yang stabil. D-alfa-tokoferol mempunyai distribusi alami yang paling luas dan aktifitas biologik terbesar (Widjaja 1997). Sumber vitamin E yang terbanyak adalah minyak biji-bijian terutama minyak biji gandum, minyak kedelai, minyak jagung, beras merah, oatmeal, dan sereal (Kartawiguna 1998).
Inflamasi
Inflamasi adalah respon terhadap cedera jaringan dan infeksi. Ketika proses inflamasi berlangsung, terjadi reaksi vaskular dimana cairan, elemen-elemen darah, sel darah putih (leukosit), dan mediator kimia berkumpul pada tempat cedera jaringan atau infeksi. Proses inflamasi merupakan suatu mekanisme perlindungan dimana tubuh berusaha untuk menetralisir dan membasmi agen-agen yang berbahaya pada tempat cedera dan untuk mempersiapkan keadaan untuk perbaikan jaringan (Mitchell 2006). Inflamasi bertujuan untuk menghancurkan mikroorganisme, menghilangkan aktivitas toksinnya, dan mempersiapkan jaringan bagi kesembuhan serta perbaikan. Meskipun pada dasarnya merupakan respon yang bersifat protektif, namun inflamasi dapat pula berbahaya, respon ini dapat menyebabkan reaksi hipersensitivitas yang bisa membawa kematian atau kerusakan organ (Hayes & Kee 1996).
5
inflamasi yang terjadi ketika agen penyebabnya sudah dieliminasi dan mediator yang disekresikan dihilangkan, mekanisme anti-inflamasi yang aktif juga turut terlibat. Inflamasi memiliki pola yang akut dan kronik yaitu inflamasi akut dan inflamasi kronik. Inflamasi akut adalah onset yang dini, durasi yang pendek dengan melibatkan proses eksudasi cairan (edema) dan emigrasi sel polimorfonuklear (neutrofil). Inflamasi kronik adalah onset yang terjadi kemudian dan durasi yang lebih lama dengan melibatkan limfosit serta makrofag dan menimbulkan proliferasi pembuluh darah serta pembentukan jaringan baru. Terdapat empat tanda klinis yang klasik pada inflamasi (yang paling menonjol pada inflamasi akut) yaitu; panas, merah, edema (tumor), nyeri. Gangguan fungsi dapat pula dianggap sebagai tanda klinis inflamasi (Hayes & Kee 1996).
Adanya pencederaan jaringan akan membebaskan berbagai jenis mediator inflamasi, seperti prostaglandin, bradikinin, histamin dan sebagainya. Mediator inflamasi dapat mengaktivasi nosiseptor yang menyebabkan munculnya nyeri. Tahapan inflamasi berawal dari perubahan fosfolipid menjadi asam arakidonat yang merupakan substrat bagi enzim prostaglandin
endoperoxide synthase (PGHS; COX,
cyclooxygenase) menjadi PGG2, dan reduksi
peroksidatif PGG2 menjadi PGH2. Selanjutnya sebagai bahan baku prostaglandin, endoperoksidan PGH2 diubah menjadi berbagai prostaglandin. Saat ini dikenal dua iso-enzim COX, yaitu COX-1 dan COX-2. COX-1 sebagai enzim constitutive yaitu mengubah PGH2 menjadi berbagai jenis prostaglandin (PGI2, PGE2) dan tromboxan (TXA2) yang dibutuhkan dalam fungsi homeostatis. COX-2 yang terdapat di dalam sel-sel imun (makrofag dan lainnya), sel endotel pembuluh darah dan fibroblast sinovial sangat mudah diinduksi oleh berbagai mekanisme, akan merubah PGH2 menjadi PGE2 yang berperan dalam kejadian inflamasi, nyeri dan demam. Oleh karena itu COX-2 dikenal sebagai enzim inducible. Pada kenyataannya, baik COX-1 dan COX-2 adalah isoenzim yang dapat diinduksi (Lelo 2001).
BAHAN DAN METODE Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini, diantaranya rimpang temulawak asal Wonogiri, kunyit asal Wonogiri, etanol 70 % (E.Merck), metanol, DPPH (2,2 difenil-1-pikril hidrazil), kit clorimetric COX (ovine)
inhibitor screeningassay No. 560131
(Cayman Chem Com 2011), akua tridestillata, DMSO (E.Merck), aluminium foil.
Alat-alat yang digunakan dalam penelitian ini, diantaranya gelas piala, gelas ukur, tabung reaksi, gelas arloji, labu takar, cawan petri, sudip, spatula, pipet mikro, tip, vortex, micro
plate, oven, rotavapor, penggiling 100
mesh,freezer, neraca digital, dan ELISAreader EPOCH.
Metode Penelitian Persiapan Sampel
Sampel basah terdiri dari 20 kg rimpang temulawak dan 20 kg rimpang kunyit. Masing-masing sampel dibersihkan dan dicuci menggunakan air mengalir sampai semua tanah dan kotoran yang menempel pada simplisia hilang. Selanjutnya sampel dipotong-potong kecil sehingga cepat kering. Selanjutnya semua simplisia dikeringkan di bawah sinar matahari selama 5 hari. Kemudian setiap simplisia kasar dari masing-masing sampel digiling dengan ukuran 100 mesh. Ukuran serbuk simplisia masing-masing sampel yang digunakan adalah 100 mesh (telah menjadi simplisia kering dengan kadar air ≤ 10%).
Penentuan Kadar Air (AOAC 2006)
Cawan porselen kosong dikeringkan pada suhu 1050C selama 30 menit di dalam oven. Cawan porselen tersebut selanjutnya didinginkan di dalam eksikator dan ditimbang sebagai bobot kosong cawan. Sebanyak 2 gram simplisia dimasukkan ke dalam cawan dan dikeringkan pada suhu 1050C selama 3 jam. Setelah itu, cawan yang berisi simplisia didinginkan dalam eksikator, dan ditimbang kembali sebagai bobot kering sampel. Perlakuan dilakukan sebanyak tiga kali ulangan.
Ekstraksi Sampel (BPOM 2005)
6
kental. Ekstrak simpilisia yang telah pekat siap digunakan untuk penelitian selanjutnya. Analisis Kadar Komponen Bioaktif Temulawak Menggunakan HPLC (Jayaprakasha et al. 2002)
Dua puluh lima mg sampel ditimbang dan dilarutkan ke dalam 5 ml metanol. Larutan disaring dengan kertas saring 0.45 μm dan ditempatkan pada vial HPLC. Sebanyak 10 μL dari larutan ekstrak sampel temulawak dan kunyit asal Wonogiri diinjeksikan ke dalam HPLC. Senyawa standar kurkuminoid dibuat dengan konsentrasi 0.1%. Kondisi HPLC untuk analisis ini digunakan jenis kolom C18
detektor UV-Vis dengan volume injeksi 10 μl, elusi gradien dan suhu kolom yang digunakan yaitu 480 C. Analisis kadar kurkuminoid dengan HPLC ini menggunakan fase gerak non polar yaitu metanol.
Uji Antioksidan dengan Metode DPPH (Blois 1958, diacu dalam Hanani et al. 2005 dengan Modifikasi)
Ekstrak kental dari sampel temulawak dan kunyit Wonogiri dari hasil maserasi dilarutkan dengan metanol dan dimasukkan ke dalam tabung reaksi. Modifikasi metode dilakukan dengan mengubah konsentrasi ekstrak yang digunakan untuk analisis yaitu 12.5, 25, 50, 100 dan 200 ppm. Larutan induk untuk masing-masing sampel temulawak dan kunyit Wonogiri yaitu 200 ppm dibuat dengan menimbang 1 gram sampel dan ditambahkan 5 ml metanol. Sebanyak 1.23 mg DPPH yang diencerkan dengan metanol hingga 25 ml menggunakan labu takar (Juniarti 2009). Kemudian untuk membuat larutan sampel dengan konsentrasi 12.5 ppm, 25 ppm, 50 ppm, 100 ppm dan 200 ppm. Sebanyak 40 μL setiap sampel dengan masing-masing konsentrasi dimasukkan ke dalam masing-masing sumur (well plate) dan dilakukan masing-masing tiga kali ulangan. Pada masing-masing sumur ditambahkan 160 μL larutan DPPH 0.1 M hingga volume akhir yang terdapat pada sumur yaitu 200 μL. Selanjutnya, diinkubasi pada suhu 370C selama 30 menit dan diukur serapannya menggunakan ELISA reader dengan panjang gelombang 517 nm. Nilai absorbansi yang diperoleh selanjutnya digunakan untuk mendapatkan persen penangkapan radikal bebas oleh sampel dan digunakan untuk mendapatkan persamaan regresi linier dengan rumus: Y= a + b ln x. Nilai IC50 dihitung
dengan menggunakan rumus persamaan regresi tersebut. Nilai IC50 yang paling rendah
menunjukkan aktivitas sampel sebagai
senyawa antioksidan yang paling tinggi dibandingkan yang lainnya.
Uji Daya Inhibisi Ekstrak Etanol Rimpang Temulawak dan Kunyit Wonogiri terhadap Enzim COX-2 Secara In Vitro (Cayman Chemical Catalog No. 560131)
Ekstrak diuji daya inhibisinya terhadap enzim COX-2. Uji daya inhibisi dilakukan dengan metode ELISA, dengan menggunakan COX Inhibitor Screening Assay Kit (Cayman
Chemical Catalog No. 560131) ) (Lampiran
4). Uji daya ekstrak etanol rimpangtemulawak dan kunyit dilakukan pada plat yang telah disiapkan (Gambar 4).
1 2 3 4 5 6 7
A Blk S1 S1 BC2 BC2 H H B Blk S2 S2 % % H H C NSB S3 S3 % % H H D NSB S4 S4 H H H H E B0 S5 S5 H H H H
F B0 S6 S6 H H H H
G B0 S7 S7 H H H H
H TA S8 S8 H H H H
Gambar 4 Format plat inhibisi COX-2
Keterangan gambar: Blk : blanko TA : aktivitas total NSB : non specific binding
B0 : maksimum binding
S1-S8 : standar 1-8
BC2 : background COX-2
% :100% initial activity samples
H : COX inhibitor samples
Preparasi larutan-larutan yang digunakan pada uji aktivitas enzim COX-2 dapat dilihat pada Lampiran 4. Sebanyak 100 μl buffer EIA dimasukkan pada sumurNSB. Kemudian 50 μl buffer EIA pada sumurB0. Larutan standar
prostaglandin diisi ke dalam sumur S8-S1. Sumur BC diisi dengan 50 μl larutan background, sebanyak 50 μl larutan aktivitas awal COX-2 dengan pengenceran 2000 kali pada sumur (%), selanjutnya pada sumur inhibitor COX-2 diisi dengan larutan ekstrak etanol rimpang temulawak dan kunyit yang telah diencerkan 2000 kali. Tahap berikutnya, setiap sumur ditambahkan prostaglandin asetilkolinesterase (PG AchE tracer) kecuali pada sumur TA dan Blk, setiap sumur ditambahkan 50 μl antiserum prostaglandin kecuali sumur TA dan NSB kemudian plat ditutup dan diinkubasi selama 18 jam pada suhu ruang.
7
Ellman sebanyak 0,2 ml dan sumur TA diisi dengan prostaglandin asetilkolinesterase (tracer) 5 μl. Plate ditutup dengan plastik film dan diikubasi pada ruang gelap selama 60-90 menit lalu diukur menggunakan Elisa reader dengan panjang gelombang 412 nm. Persiapan larutan untuk uji dapat dilihat pada lampiran 5 yang sesuai dengan Cayman Chemical Catalog No. 560131).
Penentuan IC50. Inhibition concentration 50
atau IC50 merupakan nilai konsentrasi minimal
ekstrak yang dapat menginhibisi sampai 50%. Nilai IC50 diperoleh dari masing-masing kurva
ekstrak sampel dengan memasukkan nilai Y=50.
Y = a + bX (fungsi linier)
Y = aX2 + bX +c (fungsi kuadratik) Y = a+ b ln (X) (fungsi ln)
Keterangan: a dan b = konstanta X = IC50
Persamaan dipilih satu yang paling sesuai untuk masing-masing sampel dengan melihat nilai R2 tertinggi yang diperoleh.
HASIL DAN PEMBAHASAN Ekstrak sampel
Penelitian ini menggunakan rimpang temulawak dan kunyit yang berumur sekitar 9 bulan.Mutu rimpang sangat ditentukan oleh umur, tempat tumbuh dan jenis tanah. Menurut Rahmat (1995), Panen rimpang dapat dilakukan pada saat kandungan karbohidrat tinggi, yaitu pada umur 9-10 bulan, ukuran rimpang sudah optimal dengan warna kuning kecoklatan.Ekstraksi serbuk rimpang temulawak dan kunyit dilakukan dengan cara maserasi dengan menggunakan pelarut etanol 70%.
Metode maserasi dilakukan selama 3 x 24 jam. Rendemen yang dihasilkan dari suatu proses ekstraksi akan meningkat seiring dengan peningkatan waktu ektraksi (Basalmah 2006). Semakin lama waktu ekstraksi, maka semakin lama waktu kontak antara sampel dan pelarut yang menghasilkan semakin banyak senyawa yang berdifusi keluar sel.Penelitian ini melakukan ekstraksi dengan ukuran butir serbuk 100 mesh, suhu 50 oC, dan pengadukan yang hanya dilakukan sesekali. Pemilihan suhu penguapan sebesar 50 °C pada proses ekstraksi ini didasarkan pada pertimbangan bahwa etanol memiliki titik didih sekitar 78 °C dan bersifat volatil meskipun pada suhu ruang sehingga perlakuan suhu yang terlalu tinggi dapat mengakibatkan penguapan
pelarut yang lebih besar dan dapat merusak senyawa yang tidak tahan panas.
Hasil maserasi (Tabel 1) dari rimpang temulawak dan kunyitWonogiri masing-masing dihasilkan maserat atau ekstrak. Berdasarkan hasil tersebut didapatkan rendemen masing-masing ekstrak sebesar 9.68% untuk temulawak dan 15.28% untuk kunyit.Hasil rendemen kunyit lebih besar dibandingkan temulawak karena mengandung senyawa yang lebih banyak dibandingkan temulawak. Kunyit mengandung senyawa kurkumin, demetoksi kurkumin dan bisdemetoksi kurkumin, sedangkan temulawak sedikit mengandung bisdemetoksi kurkumin(Afifah 2003).
Berdasarkan hasil tersebut kunyit memiliki nilai rendemen lebih tinggi dibandingkan temulawak. Senyawa bioaktif yang terlarut dalam etanol 70% tersebut diharapkan memiliki potensi aktivitas antioksidan dan antiinflamasi yang akan diuji pada tahap selanjutnya. Perbedaan jumlah rendemen pada ekstrak dikarenakan ekstrak dengan rendemen tertinggi mengandung lebih banyak senyawa yang mudah larut dalam etanol 70%.
Tabel 1 Persentase rendemen ekstrak temulawak dan kunyit Wonogiri
Jenis sampel Rendemen (%)
Temulawak 9.68 Kunyit 15.28
Kadar Kurkuminoid Ekstrak Rimpang Temulawak dan Kunyit Wonogiri
Penentuan kadar kurkuminoid menggunakan dengan HPLC (High
Performance Liquid Chromatography). Dari
penentuan tersebut didapatkan kadar kurkuminoid (Gambar 5) pada kunyit Wonogiri sebesar 74.57 mg/g dan temulawak Wonogiri sebesar 20.04 mg/g. Dari hasil tersebut dapat disimpulkan bahwa kandungan kurukuminoid pada kunyit lebih banyak dibandingkan dengan temulawak yang berasal dari Wonogiri.
dan se (Lechtenber
Hasil pe berbagai fak sangat m sekunder lingkungan y matahari, su tanah dan lingkungan dari tanama tinggi cekam maka meta tersebut ak karena tan dirinya da meningkatka Menurut Nu sekunder dih tanaman me Gambar 5Ka ek as Aktivita Temul Pengujia ekstrak rim ditentukan m 2-pikrilhidra diukur pada 200 ppm, 10 ppm yang n untuk tiap s dengan 3 sampel.Peng yaitu meng menggunaka Berdasar data absorb sampel yaitu 50 ppm, menghasilka rendah (Ga sampel ya aktivitas ant Kandungan k u rk u m inoid (m g/g) enyawa rg et al. 2004) enelitian ini ju
ktor lingkunga mempengaruhi
pada suat yang berperan uhu udara, ke mikroorgani lainnya adal an rimpang te man yang dira
abolit sekun kan meningk
aman terseb ari cengkam an jumlah me urhidayah (200 hasilkan ketik engalami ceka
adar kurkumin kstraketanoltem sal Wonogiri
as Antioksida lawak dan Ku an aktivitas mpang temu
menggunakan azil (DPPH) a pengujian a 00 ppm, 50 pp nantinya akan sampel. Pengu
kali ulan gukuran awal gukur absorb an ELISA rea rkan hasil pe ban, semakin u dimulai dar
100 ppm, an nilai abso ambar 6). A ang semakin tioksidan yang 0 20 40 60 80 C. dome 74.5 demetoksiku . uga disebabk an.Faktor ling hasil m tu rimpang n, diantaranya etersediaan ai isme patogen lah berupa c ersebut. Jika s
asakan oleh ta nder dari t kat. Hal ini
ut memperta man dengan etabolit sekun 05), responm ka kondisi ling
man.
noidpada mulawakdank
an Ekstrak Ri unyit Wonog antioksidan ulawak dan n metode 1,1
. Konsentras antioksidan in pm, 25 ppm, d n diperoleh ni ukuran ini di ngan pada l pada pengu ban sampel ader.
engukuran di n tinggi kon ri 12.5 ppm, 2 200 ppm orban yang s Artinya, kon n tinggi m g semakin ting
estica C. xanthorrhi 57 20.04 urkumin kan oleh gkungan metabolit g.Faktor a cahaya ir, jenis n.Faktor cekaman semakin anaman, tanaman terjadi ahankan n cara ndernya. metabolit gkungan kunyit impang giri n pada kunyit difenil-si yang ni yaitu dan 12.5
ilai IC50
lakukan setiap ujian ini dengan iperoleh nsentrasi 25 ppm, m akan semakin nsentrasi memiliki ggi pula iza 4 sehingga mam lebih banyak ditandai den ungu.Penurun diukur oleh E DPPH yang meningkatnya Setelah m semua konsen IC50 didapatk
absorban didapatkan ( berasal dari ppm, sedang dari temulaw ppm. Hasil te memiliki nila tinggi diband Wonogiri.Blo suatu baha antioksidan y IC50 kurang d
penelitian ya temulawak memiliki nila Gambar 6Pen DP ku 0 0.2 0.4 0.6 0.8 1 P e nguk uran
absorban pada 517 nm
48 50 52 54 56 58 60 62 Aktivitas a n ti o k si da n, n ilai IC50 (ppm) mpu mengha k.Peghambatan ngan peluruh nan nilai abs ELISA reader
semakin pud a konsentrasi mendapatkan
ntrasi, dihitun kan dari perhi yang diper (Gambar 7) Wonogiri me gkan nilai ak wak Wonogi
ersebut menu ai aktivitas ant dingkan kunyi ois (1958) m an memiliki
yang baik apa dari 200 ppm ang diperole yang berasa ai aktivitas ant
nghambatan ra PPHoleh samp unyit Wonogir 12.5 25 C. domestica 53.13
C. xanthorriz
Konsentrasi
ambat radikal n radikal beb han warna sorban karena adalah warna dar seiring d
sampel. nilai absorba nglah nilai IC5
itungan berda roleh.Hasil
pada kunyit emiliki nilai 6 ktivitas antio iri sebesar 5 unjukkan temu tioksidan yang it yang berasa mengatakan i nilai ak abila memilik m. Berdasarkan
h, kunyit m al dari Wo tioksidan yang
adikal bebas pel temulawak ri
50 100 2
a C. xanthorrh
61.47
za C. domestica
Gambar 7Ha Day Temulawa (C. dom Pengujia langsung me dengan ob ada.Obat si enzim sikloo efek sam lambung.Pen tidak adany enzim C antiinflamas pada enzim tidak terha protasiklin lambung. Pengujia terhadap CO Inhibitor S Chemical konsentrasi inhibisi s menggunaka gelombang diperoleh a persen inhib Adanya Siklooksigen pada konsen ppm menun dan kunyit antiinflamas denganpeng sebesar 47.4 dan 87.19% 8). Perbed antiinflamas Wonogiridik yang berbed Perbedaa kunyit dan dikarenakan dikandung k temulawak. hasil inhibi antiinflamas kurkuminoid kurkuminoid terhadap p siklooksigen didapatkan konsentrasi ini hanya
asil uji antiok temulawak da ya Inhibisi Ek ak (C. xantho mestica) Won Aktivitas C an antiinflama enghambat en bat sintetik intetik antiinf oksigenase se mping be ndarahan lam ya protasikli COX-1.Keung si ini adalah la m COX-2 sehi ambat dan yang berfung
an daya in OX-2 menggu Screening As
Catalog N
100 ppm.H sampel ini an ELISA R
517 nm. Ni akan diolah s bisi COX-2. penghambat nase-2 (COX-ntrasi inhibito njukkan bahw t memiliki si.Hal gujian yang 45% untuk t % untuk kunyi daan % inh si pada tem karenakan k da pada setiap
an % inhibi n temulawa n kadar k
kunyit lebih b Hal inilah isi karena y si ada d.Timmerman d memiliki a penghambatan nase.Pada pe nilai IC50.H
yang diguna satu konsen
sidan ekstrak an kunyit kstrak Rimpa orrhiza) dan K nogiri Terhad
COX-2 asi pada penel
nzim COX-2 b antiinflamasi flamasi meng ehingga menim erupa pen mbung ini diak
in yang dih ggulan pe angsung meng ingga enzim tetap mengh gsi sebagai p
nhibisi samp unakan metod ssay Kit (C No. 56013 Hasil reaksi d
diukur Reader pada p
ilai absorbans sehingga did
tan aktivitas -2) yang cuku or (sampel) ya wa ekstrak tem bioaktivitas ini dib
mendapatka temulawak W it Wonogiri (G
ibisi dari a mulawak dan
kadar kurku sampel. isi yang dih ak asal W kurkuminoid banyak diband
yang memb yang menjadi
alah s
n(1995) mela aktivitas yang n aktivitas engujian ini Hal ini dika akan pada pe ntrasi.Nilai I
ang Kunyit dap litian ini berbeda i yang ghambat mbulkan darahan kibatkan hasilkan enelitian ghambat COX-1 hasilkan proteksi pel ini de COX Cayman dengan dari uji dengan panjang si yang dapatkan enzim up tinggi aitu 100 mulawak sebagai buktikan an hasil Wonogiri Gambar aktivitas kunyit uminoid hasilkan Wonogiri yang dingkan bedakan i faktor senyawa aporkan g tinggi enzim i tidak renakan engujian IC50bisa
didapatkan a konsentrasi dihitung nilai Gambar 8Ak o d k SIM Hasil pen Wonogiri me ppm dan tem ppm seba antiinflamasi ppm memilik dan temulaw kurkuminoid dan temulawa Diperluka mengenai temulawak beberapa mendapatkan untuk menge bisa mengham
[AOAC] T Analyt Metho Washi Officia [BPOM RI] Makan Gerak Jakarta Afifah E. Temul Aneka Jakarta 0 20 40 60 80 100 Inhi bi si COX ‐ 2 (%) apabila memi yang variat i IC50.
ktivitas peng olehtemulawak dan kunyit(C konsentrasi 10
MPULAN DAN Simpu nelitian ini m emiliki nilai I mulawak Wono
agai antiok kunyit pad ki persen inhib wak sebesar
pada kunyit ak sebesar 20.
Sara an adanya pen
aktivitas a dan kunyit konsentrasi n nilai IC50.
etahui besarny mbat inflamas
DAFTAR PU The Associa
tical Chemis ods of Ana
ington DC: al Analytical C
Badan Pen nan Republik kan Nasional M
a : BPOM RI.
2003. Khas lawak: Rimp
Penyakit. A a. C. domestica x 87.19 iliki beberapa tif sehingga
ghambatan C k (C. xanthor C. Domestica 00 ppm
N SARAN ulan
menunjukan IC50 sebesar 6
ogiri sebesar 5 ksidan. Ak da konsentras bisi sebesar 8 47.45%.Kand sebesar 74.57 .04 mg/g. an nelitian lebih antiinflamasi t Wonogirid sehingga Hal ini dila ya konsentras si .
USTAKA ation of O
st. 2006. O alysis. Ed
Associatio Chemist. ngawas Oba k Indonesia. Minum Temu .
10
Anies. 2009. Judul Cepat Tua akibat Radiasi?. Jakarta: Penerbit Elex Media Komputindo. Hal 127-128
Basnet P, Natasa SB. 2011. Curcumin: An anti-inflammatory molecule from a curry spiceon the path to cancer treatment. Molecules 16: 4567-4598. Blois MS. 1958.Antioxidant determination by
the use of stable free radical.Nature 181: 1191-1200.
Dalimartha S. 2000. Atlas Tumbuhan Obat Jilid ke-2. Jakarta: Trubus Agriwidya. Hanani E, Munim A, Sekarini R. 2005.
Identifikasi senyawa antioksidan dalam spons Callyspongia sp dari Kepulauan Seribu.Majalah Ilmu Kefarmasian 3: 127-133.
Harborne JB. 1987. Metode Fitokimia Penuntun Cara Modern Menganalisis
Tumbuhan. Bandung: ITB Press.
Hayes E.R, Kee J.L. 1996. Farmakologi.Pendekatan Proses Keperawatan.Anugerah P, penerjemah; Asih Y, editor. Jakarta: EGC. Terjemahan dari: Pharmacology. A nursing process approach.
Heldt HW. 1997. Plant Biochemistry &
Molecular Biology. New York:
OxfordUniversity Press
Jayaprakasha GK, Rao LJ, Sakariah KK. 2002. Improved HPLC method for determination of curcumin, demethoxycurcumin, and bisdemethoxycurcumin. Agric. Food.
Chem. 50: 3668-3672.
Kassahara S, Hemmi S. 1986. Medical
HerbIndex in Indonesia. Ed. ke-2.
Jakarta:PT. Eisai Indonesia, dalam Makiyyah2003
Ketaren, S. 1986. Pengantar Teknologi
Minyak dan Lemak Pangan. Cetakan
Pertama. Jakarta : UI-Press.
Kilkuzaki H, Nakatani. 1993. Antioxidant effects of some ginger constituents. J. Food. Sci: 58 (6): 1407-1410
Kiso.1985.Antihepatotonic Principles of Curcuma Longa Rhizome.Simposium
Nasional Temulawak.Bandung :
UNPAD.
Lechtenberg M, Quandt B, Nahrstedt A. 2004. Quantitative determination of
curcuminoids in Curcuma rhizomes and rapid differentiation of Curcuma
domestica Val. and Curcuma
xanthorrhiza Roxb.by capillary
electrophoresis. Phytochem.Anal. 15: 152–158.
Lelo A. 2001. Pertimbangan yang muncul dari OAINS yang digunakan. Naskah Lengkap Temu Ilmiah Rematologi 2001. (eds. Setyohadi B, Kasjmir YI). Jakarta: Ikatan Reumatologi Indonesia.
Mitchell R.N. 2006. Buku Saku Dasar Patologis Penyakit Robbins & Cotran,
Ed. 7. Hartono A, penerjemah;
Handayani S et al, editor. New York: Elsevier Inc. Terjemahan dari: Pocket Companion To Robbins & Cotran
Pathologic Basis of Disease, 7th
edition.
Molyneux P. 2004. The use of stable free radical dyphenilpicryl-hydrazil (DPPH) for estimating antioxidant activity. J. Sci. Technol: 211-219. Murray RK, Granner DK, Mayes PA, Rodwel
VW. 2003. Biokimia Harper. Jakarta: Buku Kedokteran EGC.
Nagabhushan M, Bhide SV. 1992. Curcumin as an inhibitor of cancer. J. Am. Clin. Nutr. 11: 192-198
Rukmana R. 2006. Temulawak, Tanaman
Rempah dan Obat. Yogyakarta:
Kanisius.
Rukmana R. 2008. Temu-temuan, Apotik Hidup di Pekarangan.Ed ke-5. Yogyakarta: Kanisius.
Sidik, Mulyono MW, Mutadi A. 1995. Temulawak (Curcuma xanthorriza Roxb). Jakarta: Phyto Medika
Tonnesen HH, Karlsen J. 1985. Studies On Curcumin and Curcuminoids Alkaline Degradation of Curcuming Z.Lebens, Unters, Forsch.180 : 132-134
Tuminah, Sulistyowati. 1999. Pencegahan Kanker dengan Antioksidan.Jurnal
Cermin Dunia Kedokteran. 122
Wahid P, Sudiarto. 1985. Pembudidayaan tanaman temulawak. Prosiding
symposium nasional
temulawak.Bandung: Lembaga
11
WHO.1999. WHO Monograph on selected medicinal plants. Vol I.ISBN 92-125178.
Widjaja E. 1997. Konservasi jenis-jenis bambu di Indonesia.Prosiding Seminar Nasional Konservasi Flora
Nusantara.Bogor: UPT Balai
Pengembangan Kebun Raya Bogor.
11
12
Lampiran1 Diagram alir penelitian
-
Dicuci
-
Dipotong
-
Dikeringkan
-
Digiling
-
Ekstrak dengan etanol 70 %
(maserasi)
-
Evaporator
-
% rendemenen
Rimpang kunyit dan temulawak
Wonogiri
Ekstrak kunyit dan temulawak
Wonogiri
Uji bioaktifitas potensi hayati
ekstrak temulawak
Uji aktivitas
antioksidan DPPH
Uji antiinflamasi
dengan inhibisi COX-2
Uji kandungan
kurkuminoid dengan
HPLC
Simplisia 100 mesh
13
Lampiran 2 Prosedur ekstraksi (BPOM 2005)
Diamkan selama 24 jam
Maserat dipisahkan dan ekstrak
diuapkan hingga kental dengan
evaporator pada suhu 50
0C
Serbuk simplisia temulawak dan kunyit
100 mesh dengan kadar air < 10%
1 kg sampel dilarutkan dalam 10 L
etanol 70 % (1:10)
Direndam dan diaduk
dalam maserator
14
Lampiran 3 Uji aktivitas antioksidan dengan metode DPPH
Timbang 1 mg sampel dan dilarutkan
dengan 5 ml metanol sehingga
konsentrasi stok 200 ppm
Timbang 1.23 mg DPPH diencerkan
hingga 25 ml dengan metanol
Sampel dimasukkan ke dalam
micro
o
plate
dengan konsentrasi 200, 100, 50,
25, 12.5 ppm
100
μ
Llarutan DPPH
ditambahkan pada setiap sampel
Sampel diinkubasi selama 30 menit
pada suhu 37
0C
Sampel dibaca dengan Elisa
15
Lampiran 4 Preparasi larutan untuk uji inhibisi COX-2
Penyiapan sampel uji
Pembuatan standar
prostaglandin
Tahap pengenceran pada reaksi
COX
Penyiapan pelarut
16
Lampiran 5 Kadar air ekstrak kunyit dan temulawak
Jenis sampel Ulangan
Bobot cawan kosong (gr)
Bobot contoh (gr)
Bobot cawan &
contoh kering (gr)
Kadar air
(%) Kadar air rata-rata
(%)
Temulawak 1 20.7403 2.0783 22.6032 10.36
10.09
2 26.6249 2.3243 28.7149 10.08
3 17.4521 2.1193 19.3632 9.82
Kunyit 1 27.6655 2.1436 29.5905 10.19
9.96
2 27.8575 2.0375 29.6994 9.6
3 27.7882 2.0820 29.6599 10.10
Contoh perhitungan:
Kadar air temulawak =
& x %=
. . ..
x 100%
= 10.36%
Kadar air rata-rata =
=
. . .17
Lampiran 6 Rendemen hasil ekstraksi
Jenis sampel Ulangan Bobot sampel (gr)
Bobot ekstrak (gr)
Rendemen (%)
Rendemen rata-rata (%) Temulawak 1 50.5406 4.5101 8.92
9.68
2 50.0232 4.5227 9.04
3 50.1195 5.5622 11.09
Kunyit 1 50.0604 8.6680 17.32
15.28
2 50.1831 6.842 13.64
3 50.1008 7.3528 14.89
Contoh perhitungan:
Rendemen temulawak (%) =
x %=
..
x 100%
= 8.92 %
Rendemen rata-rata temulawak (%) =
=
. . .18
Lampiran 7 Hasil pengukuran kadar kurkuminoid temulawak dengan HPLC
Tabel 2 Kadar kurkuminoid kunyit
Contoh perhitungan :
[inject]
=
=
.5
= 0.39476
[sampel] =
=
..
= 19.05211931
Keterangan :
FP
: Faktor pengenceran
Senyawa
Berat sampel
(mg)
Volume Pengencera
n (mL)
FP Luas Area
Standar [Standar] Luas Area Sampel
[Inject]
[Sampel] mg/g Bahan Bisdesmetoksi
kurkumin 0,0518 50 50 382131 0,5 301700 0,39476 19,0521 Desmetoksi
kurkumin 0,0518 50 50 320634 0,5 270600 0,421976 20,3656 74,57
19
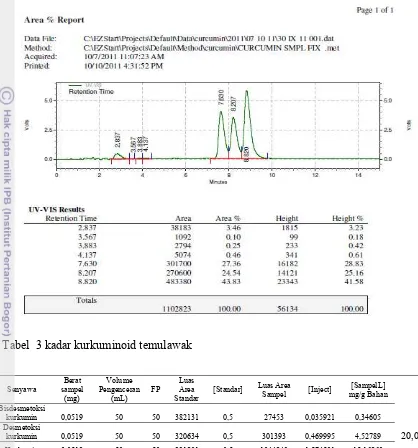
Lampiran 8 Hasil pengukuran kadar kurkuminoid kunyit dengan HPLC
Tabel 3 kadar kurkuminoid temulawak
Contoh perhitungan :
[inject]
=
=
.5
= 0.03592
[sampel] =
=
..
=
0,346059033Keterangan :
FP
: Faktor pengenceran
Senyawa
Berat sampel
(mg)
Volume Pengenceran
(mL) FP
Luas Area Standar
[Standar] Luas Area
Sampel [Inject]
[SampelL] mg/g Bahan
Bisdesmetoksi
kurkumin 0,0519 50 50 382131 0,5 27453 0,035921 0,34605 Desmetoksi
kurkumin 0,0519 50 50 320634 0,5 301393 0,469995 4,52789 20,04
20
Lampiran 9 Data absorbansi aktivitas antioksidan ekstrak temulawak Wonogiri pada
panjang gelombang 517 nm
Sampel Ulangan Konsentrasi (ppm)
Absorban sampel
Absorban
blanko % Inhibisi IC50 (ppm)
IC50 rata-rata
(ppm)
Temulawak 1
200 0,155
0,334
78,14
67,06395
53,1332
100 0,174 65,27
50 0,252 38,62
25 0,324 19,46
12.5 0,349 10,18
2
200 0,118
0,364
90,11
52,3198
100 0,152 74,18
50 0,261 41,21
25 0,323 26,37
12.5 0,371 11,54
3
200 0,128
0,442
89,59
40,01598
100 0,137 82,13
50 0,281 47,06
25 0,322 39,59
12.5 0,394 21,95
Contoh perhitungan :
% Inhibisi =
%
=
. ..
%
21
Lampiran 10 Data absorban aktivitas antioksidan ekstrak kunyit Wonogiri pada
panjang gelombang 517 nm
Sampel Ulangan Konsentrasi (ppm)
Absorban sampel
Absorban
blanko % Inhibisi IC50 (ppm)
IC50 rata-rata
(ppm)
Kunyit 1
200 0,115
0,407
93,36609
60,50294
61,47175
100 0,22 61,17936
50 0,301 36,60934
25 0,364 21,13022
12.5 0,413 9,090909
2
200 0,114
0,396
93,43434
60,15918
100 0,216 61,11111
50 0,342 24,49495
25 0,356 20,9596
12.5 0,332 27,0202
3
200 0,109
0,386
94,55959
63,75313
100 0,211 61,39896
50 0,317 29,01554
25 0,368 15,80311
12.5 0,38 12,6943
Contoh perhitungan :
% Inhibisi =
%
=
. ..
%
22
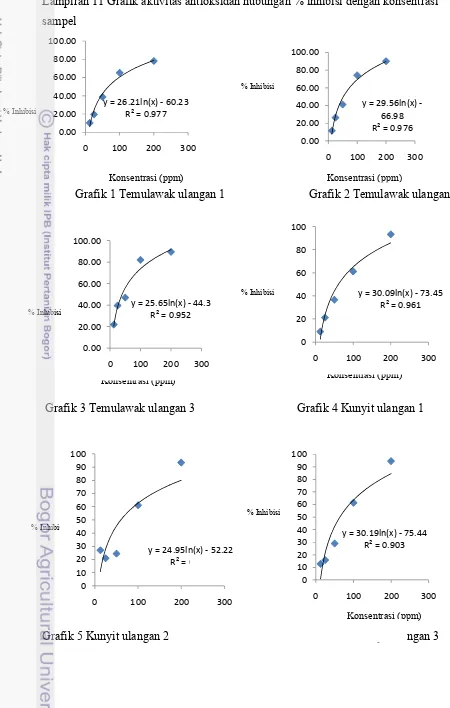
% Inhibisi
Lampiran 11 Grafik aktivitas antioksidan hubungan % inhibisi dengan konsentrasi
sampel
Grafik 1 Temulawak ulangan 1 Grafik 2 Temulawak ulangan 2
[image:32.595.71.521.94.802.2]Grafik 3 Temulawak ulangan 3 Grafik 4 Kunyit ulangan 1
Grafik 5 Kunyit ulangan 2
Grafik 6 Kunyit ulangan 3
Konsentrasi (ppm) Konsentrasi (ppm)
% Inhibisi
% Inhibisi
Konsentrasi (ppm)
% Inhibisi
Konsentrasi (ppm)
Konsentrasi (ppm)
% Inhibisi
% Inhibisi
Konsentrasi (ppm)
y = 30.09ln(x) ‐73.45
R² = 0.961
0 20 40 60 80 100
0 100 200 300
y = 29.56ln(x) ‐ 66.98 R² = 0.976 0.00
20.00 40.00 60.00 80.00 100.00
0 100 200 300
y = 30.19ln(x) ‐75.44
R² = 0.903
0 10 20 30 40 50 60 70 80 90 100
0 100 200 300
y = 24.95ln(x) ‐52.22
R² = 0.762
0 10 20 30 40 50 60 70 80 90 100
0 100 200 300
y = 26.21ln(x) ‐60.23
R² = 0.977
0.00 20.00 40.00 60.00 80.00 100.00
0 100 200 300
y = 25.65ln(x) ‐44.3
R² = 0.952
0.00 20.00 40.00 60.00 80.00 100.00
23
Lampiran 12 Nilai IC
50aktivitas antioksidan masing-masing sampel
Sampel Ulangan Persamaan garis Nilai IC50 (ppm)
Rataan IC50 (ppm) Temulawak 1 y = 26,21ln(x) - 60,23 67.06395
53.13 2 y = 29,56ln(x) - 66,98 52.3198
3 y = 25,65ln(x) - 44,3 40.01598 Kunyit 1 y = 30,09ln(x) - 73,45 60.50294
61.47 2 y = 24,95ln(x) - 52,22 60.15918
3 y = 30,19ln(x) - 75,44 63.75313
Contoh perhitungan:
y = a + b ln x
50 = 26.21 ln x – 60.23
ln x =
..
x = 67.06395 ppm
Rataan IC
50=
. . .= 53.13 ppm
Lampiran 13 Kurva standar uji inhibisi COX-2
Konsentrasi (pg/ml)
% B/B0
25
y = ‐25.9ln(x) + 216.0 R² = 0.988
0 20 40 60 80 100 120 140 160
Lampiran 14 Data uji daya inhibisi ekstrak rimpang temulawak dan kunyit Wonogiri
Contoh perhitungan:
(B0)
(S1)
(IA2)
Absorban terkoreksi = Absorbans rerata – NSB
% B/B0 =
S
%
[PG] terkoreksi =
([PG] x FP) – ([PG]BC-2 x FPAbsorban terkoreksi = 0.304166667 – (- 0.0005) % B/B0 =
..
%
= 1084942 – 37369.36
= 0.304666667
= 0.259299781
= 1047573.101
Temulawak (100)
FP = BC = 100
% Inhibisi =
%
IA2 = 2000
=
. ..
%
= 47.45 %
Sampel = 2000
Keterangan :
PG
: Prostaglandin
FP
: Faktor pengenceran
%B/B
0: % Maksimum
binding
BC
:
Background
COX-2
IA2 :
Total activity tracer