ii
OPTIMASI DAN EVALUASI MIKROKAPSUL IBUPROFEN
TERSALUT LILIN LEBAH
GINA PRAGUSTIANA SOEMANTRI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
i
Ibuprofen Tersalut Lilin Lebah. Dibimbing oleh TETTY KEMALA dan AHMAD
SJAHRIZA.
Ibuprofen merupakan obat antiradang nonsteroid untuk mengobati rematik.
Waktu paruh eliminasinya cepat sehingga dapat menimbulkan iritasi lambung,
maka diperlukan sistem pelepasan obat secara terkendali, antara lain dengan
teknik mikroenkapsulasi. Pada penelitian ini, mikroenkapsulasi ibuprofen
dilakukan
dengan
metode
emulsi-penguapan
pelarut.
Variasi
nisbah
ibuprofen:lilin lebah (1:1, 1:2, dan 1:3) dan konsentrasi pengemulsi gelatin (1, 1.5,
2, dan 2.5%) diujikan untuk mendapatkan mikrokapsul yang optimum. Persen
rendemen mikrokapsul yang dihasilkan sebesar 77.17
–
88.84%. Efisiensi
enkapsulasi ibuprofen tertinggi ialah 93.78%, diperoleh pada mikrokapsul dengan
nisbah ibuprofen:lilin lebah 1:1 dan konsentrasi gelatin 2%. Variasi konsentrasi
gelatin berpengaruh signifikan terhadap efisiensi enkapsulasi pada nisbah 1:3.
Mikrokapsul dengan efisiensi enkapsulasi tertinggi mengalami pelepasan
ibuprofen sebesar 38.22% dalam medium simulasi cairan usus selama 6 jam.
Kinetika pelepasan ibuprofen mengikuti model Korsmeyer-Peppas. Mikrokapsul
yang dihasilkan memiliki kisaran ukuran 200
–
250 µm. Berdasarkan hasil tersebut,
dapat disimpulkan bahwa mikroenkapsulasi ibuprofen dengan penyalut lilin lebah
dapat menahan laju pelepasan obat dalam usus.
ABSTRACT
GINA PRAGUSTIANA SOEMANTRI. Optimization and Evaluation of
Beeswax-Coated Ibuprofen Microcapsules. Supervised by TETTY KEMALA and
AHMAD SJAHRIZA.
iii
Judul Skripsi : Optimasi dan Evaluasi Mikrokapsul Ibuprofen Tersalut Lilin Lebah
Nama
: Gina Pragustiana Soemantri
NIM
: G44096002
Disetujui
Pembimbing I
Dr Tetty Kemala, SSi, MSi
NIP 19710407 199903 2 001
Pembimbing II
Drs Ahmad Sjahriza
NIP 19620406 198903 1 002
Diketahui
Ketua Departemen Kimia
Prof Dr Ir Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
iv
rahmat, hidayah, serta karunia yang diberikan kepada penulis sehingga dapat
menyelesaikan karya ilmiah dengan judul Optimasi dan Evaluasi Mikrokapsul
Ibuprofen Tersalut Lilin Lebah. Shalawat serta salam semoga selalu tercurahkan
kepada Nabi Muhammad SAW, keluarganya, dan semoga kita semua menjadi
pengikutnya hingga akhir zaman.
Penulis mengucapkan terima kasih kepada Ibu Dr Tetty Kemala, SSi, MSi
dan Bapak Drs Ahmad Sjahriza selaku pembimbing yang senantiasa memberikan
arahan, dorongan semangat, dan doa kepada penulis selama melaksanakan
penelitian. Penulis juga mengucapkan terima kasih atas bantuan serta masukan
selama penelitian berlangsung kepada staf laboran Laboratorium Anorganik (Pak
Syawal, Pak Mulyadi, Pak Caca, dan Bu Nurul), Pak Sabur dari Laboratorium
Kimia Organik, Pak Suherman, dan Bu Nunung dari Laboratorium Kimia
Analitik, Bapak Sulis dari Batan-Serpong.
Terima kasih tak terhingga penulis ucapkan kepada Papa, Mama, Kakak,
Adikku, dan Angga Prayoga serta seluruh keluarga, atas doa, dan kasih
sayangnya. Tidak lupa saya ucapkan terima kasih kepada teman-teman
seperjuangan penelitian di Laboratorium Kimia Anorganik, yaitu Randi, Oji,
Endi, dan Niswa yang telah membantu memberi masukan dan saran, serta kepada
Fitri, Lia, Putri, Doni, Dika, Eris, Yana, dan rekan-rekan mahasiswa S1 Program
Alih Jenis.
Penulis berharap karya ilmiah ini dapat bermanfaat bagi perkembangan ilmu
pengetahuan.
Bogor, Juni 2012
v
RIWAYAT HIDUP
Penulis dilahirkan di Tangerang pada tanggal 15 Agustus 1987, merupakan
putri kedua dari H. Tjitji S Soemantri dan Hj. Ai Maesaroh SPd. Tahun 2005
penulis lulus dari SMA Negeri 5 Kota Tangerang dan pada tahun yang sama
melanjutkan pendidikan di Politeknik TEDC Bandung Program DIII Analisis
Kimia. Pada tahun 2008 penulis mengikuti Pendidikan Akta di STKIP Bale
Bandung, dan pada tahun 2009 melanjutkan Studi S1 melalui Program Alih Jenis
Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Institut
Pertanian Bogor (IPB).
vi
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
METODE
Bahan dan Alat ... 1
Lingkup Kerja ... 2
HASIL DAN PEMBAHASAN
Mikroenkapsulasi Ibuprofen ... 2
Panjang Gelombang Maksimum dan Kurva Standar... 3
Efisiensi Enkapsulasi ... 3
Pelepasan Obat... 4
Kinetika Pelepasan Obat ... 4
Morfologi Mikrokapsul ... 5
SIMPULAN DAN SARAN
Simpulan ... 6
Saran ... 6
DAFTAR PUSTAKA ... 6
vii
DAFTAR TABEL
Halaman
1
Nisbah mikrokapsul ibuprofen tersalut lilin lebah dan variasi
konsentrasi gelatin ... 2
2
Kinetika pelepasan ibuprofen dari mikrokapsul formula AC ... 5
DAFTAR GAMBAR
Halaman
1
Mikrokapsul ibuprofen tersalut lilin lebah (1:1) dengan konsentrasi
gelatin 2% ... 3
2
Efisiensi enkapsulasi mikrokapsul ibuprofen dengan konsentrasi
gelatin 1%; 1.5%; 2% ; dan 2.5%.. ... 4
3
Profil pelepasan ibuprofen dari mikrokapsul formula AC terhadap
waktu (menit) ulangan 1 dan ulangan 2 ... 4
4
Foto mikroskop mikrokapsul dengan konsentrasi gelatin 2% pada
perbesaran 40
... 5
5
Foto SEM mikrokapsul (1:1) dengan konsentrasi gelatin 2% pada
viii
Halaman
1
Diagram alir penelitian ... 9
2
Rendemen mikrokapsul ... 10
3
Spektrum absorpsi larutan ibuprofen
10 ppm ... 11
4
Kurva
standar ibuprofen (
maks=221.5 nm) ... 125
Efisiensi enkapsulasi ibuprofen dalam mikrokapsul tersalut lilin
lebah ... 13
6
Persentase rerata pelepasan ibuprofen dalam uji disolusi medium usus
dari mikrokapsul tersalut lilin lebah formula AC ... 14
7
Pelepasan ibuprofen dalam mikrokapsul pada waktu
t
... 15
ix
ix
OPTIMASI DAN EVALUASI MIKROKAPSUL IBUPROFEN
TERSALUT LILIN LEBAH
GINA PRAGUSTIANA SOEMANTRI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
PENDAHULUAN
Ibuprofen merupakan turunan asam fenilasetat dengan nama kimia asam 2-(4-isobutilfenil)propionat termasuk golongan obat non-steroid yang memberikan efek antiradang, antipretik, dan analgesik. Obat ini digunakan untuk menghilangkan nyeri dan peradangan pada saat migrain, nyeri pascaoperasi, dan sakit gigi (Rao et al. 2011). Dosis pemberian ibuprofen ialah 400 mg setiap 4–6 jam. Obat ini mudah diserap oleh saluran pencernaan dan kadar tertinggi dalam darah dicapai dalam waktu 1–2 jam setelah pemberian oral. Ekskresi ibuprofen terjadi dengan cepat dan sempurna. Lebih dari 90% dosis yang diberikan diekskresi melalui urin sebagai metabolit asam sekundernya (Gilman et al. 1996). Waktu paruh eliminasi yang cepat menyebabkan obat ini harus lebih sering dikonsumsi. Pengonsumsian obat secara berulang dalam dosis yang besar dapat menyebabkan iritasi pada saluran pencernaan. Untuk mengatasi hal tersebut, diperlukan sistem pelepasan ibuprofen terkendali, antara lain dengan pendekatan mikroenkapsulasi.
Mikroenkapsulasi merupakan teknik menyalut suatu senyawa menggunakan bahan penyalut berukuran sangat kecil dengan diameter rerata 15–20 mikron (Yoshizawa 2004). Teknik ini banyak digunakan sebagai sistem pengantaran obat karena dapat mengurangi efek samping, meningkatkan efektivitas terapi obat yang diberikan, dan mengendalikan pelepasan obat (Raval et al. 2011). Tantangan aplikasi teknologi mikroenkapsulasi terletak pada pemilihan teknik, bahan inti, dan bahan penyalut yang tepat sehingga kapsul dapat berfungsi sebagaimana mestinya (Yuliani et al. 2007). Bahan penyalut yang digunakan dapat beragam, dengan syarat dapat terdegradasi dan biokompatibel dalam tubuh.
Pada penelitian ini bahan penyalut yang digunakan adalah lilin lebah. Menurut Garnier et al. (2002), lilin lebah sangat kompleks, terbuat dari n-alkana jenuh dan tak jenuh, ester rantai panjang, asam lemak, diester, hidroksiester, dan konstituen minor lainnya, seperti flavonoid. Menurut Ranjha et al. (2010) lilin lebah dapat memiliki beberapa kelebihan sebagai bahan pembuat mikrosfer, yaitu stabil pada beberapa nilai pH dan tingkat kelembapan, biokompatibel, tidak imunogenik, dan memiliki efek yang minimum pada saluran pencernaan. Gowda et al. (2009) melakukan mikroenkapsulasi
indometasin menggunakan lilin lebah dengan metode emulsi-penguapan pelarut.
Metode emulsi-penguapan pelarut telah banyak digunakan untuk menyalut obat hidrofobik melalui proses emulsifikasi minyak dalam air (o/w) (Park et al. 2005). Mikrokapsul dibuat dengan melarutkan penyalut dan bahan inti dalam pelarut yang mudah menguap. Campuran didispersikan ke dalam air hingga terbentuk emulsi. Emulsi tidak stabil sehingga memerlukan penambahan zat pengemulsi. Gelatin telah banyak digunakan sebagai pengemulsi dalam pembuatan mikrokapsul (Sinuhaji 2012; Abdurohman 2011; Ranjha et al. 2010). Variasi nisbah penyalut dengan bahan inti serta konsentrasi pengemulsi akan berpengaruh terhadap mikrokapsul yang dihasilkan dan banyaknya obat yang tersalut (Kemala 2010).
Penelitian ini bertujuan menghasilkan mikrokapsul optimum, menentukan pengaruh variasi nisbah ibuprofen:lilin lebah dan konsentrasi pengemulsi terhadap efisiensi penyalutan ibuprofen, dan membuat profil pelepasan ibuprofen. Dari profil tersebut, ditentukan model kinetika pelepasan ibuprofen berdasarkan kriteria koefisien determinasi (R2) dari persamaan reaksi orde ke-0 dan ke-1, Higuchi, Hixson-Crowell, dan Korsmeyer-Peppas, serta mekanisme pelepasan obat yang dominan berdasarkan eksponen pelepasan (n) dari persamaan Korsmeyer-Peppas. Morfologi mikrokapsul yang dihasilkan juga dianalisis.
METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah lilin lebah yang diperoleh dari Sukabumi, ibuprofen p.a yang diperoleh dari PT Kalbe Farma, gelatin (bloom number 200), diklorometana, dan bufer fosfat (NaH2PO4-Na2HPO4) pH 7.2.
2
Lingkup Kerja
Penelitian ini dilakukan dalam beberapa tahapan (Lampiran 1). Mikrokapsul ibuprofen dibuat dengan variasi nisbah ibuprofen:lilin lebah dan konsentrasi gelatin. Mikrokapsul yang dihasikan diukur efisiensi penyalutan ibuprofennya, diuji disolusi, serta dicirikan dengan mikroskop dan SEM.
Pembuatan Mikrokapsul Ibuprofen Tersalut Lilin Lebah
Lilin lebah dilarutkan dalam diklorometana, diaduk hingga homogen. Setelah itu, ibuprofen yang telah dilarutkan dalam diklorometana dicampurkan. Campuran dibuat dengan variasi nisbah ibuprofen:lilin lebah kemudian didispersikan menggunakan motor pengaduk ke dalam air yang telah mengandung variasi konsentrasi gelatin (Tabel 1). Campuran didekantasi hingga mikrokapsul yang terbentuk mengendap. Mikrokapsul disaring, dicuci dengan akuades, dikeringudarakan selama 1 hari.
Tabel 1 Nisbah mikrokapsul ibuprofen tersalut lilin lebah dan variasi konsentrasi gelatin
Formula Nisbah ibuprofen: lilin lebah
Konsentrasi gelatin (%)
AA 1:1 1
AB 1:1 1.5
AC 1:1 2
AD 1:1 2.5
BA 1:2 1
BB 1:2 1.5
BC 1:2 2
BD 1:2 2.5
CA 1:3 1
CB 1:3 1.5
CC 1:3 2
CD 1:3 2.5
Penentuan Panjang Gelombang Maksimum dan Pembuatan Kurva Standar
Larutan ibuprofen dalam bufer fosfat pH 7.2 dengan konsentrasi 10 ppm diukur absorbansnya pada panjang gelombang ( ) 210–240 nm menggunakan spekrofotometer UV. Panjang gelombang maksimum ( maks)
yang diperoleh digunakan untuk analisis selanjutnya.
Kurva standar dibuat dengan mengukur absorbans larutan ibuprofen dengan konsentrasi 2, 4, 6, 8, 10, 12, 14, 16, 18, dan 20 ppm pada panjang gelombang maksimum. Hasil yang diperoleh merupakan hubungan konsentrasi ibuprofen dengan absorbans.
Efisiensi Enkapsulasi
Sebanyak 25 mg mikrokapsul ditimbang dan dilarutkan dalam 50 mL bufer fosfat pH 7.2. Campuran dikocok selama 24 jam lalu disaring (Tayade & Kale 2004). Filtrat diencerkan 10 kali dan dibaca absorbansnya dengan spektrofotometer UV pada maks
(221.5 nm). Absorbans yang diperoleh digunakan untuk menentukan konsentrasi ibuprofen dengan bantuan kurva standar.
Uji Disolusi secara In Vitro (Depkes 1995)
Uji disolusi mikrokapsul dilakukan dengan alat disolusi tipe 2 (tipe dayung). Sebanyak 200 mg mikrokapsul ditimbang dan dimasukkan ke dalam bejana disolusi. Uji disolusi dilakukan dalam medium simulasi cairan usus (larutan bufer fosfat pH 7.2) selama 6 jam pada suhu (37 ± 0.5)°C dengan kecepatan pengadukan 100 rpm. Volume medium disolusi yang digunakan sebanyak 500 mL. Pengambilan alikuot dilakukan setiap 15 menit dengan volume setiap pengambilan 10 mL. Setiap pengambilan alikuot, volume medium yang terambil digantikan dengan larutan medium baru dengan volume dan suhu yang sama. Konsentrasi ibuprofen dalam alikuot diukur menggunakan spektrofotometer UV pada maks (221.5 nm). Dari data yang
diperoleh, dibuat kurva hubungan antara persen pelepasan ibuprofen dan waktu disolusi, serta dikaji kinetika pelepasannya.
Morfologi Mikrokapsul
Pengamatan morfologi mikrokapsul dilakukan terhadap mikrokapsul kosong dan yang terisi ibuprofen dengan menggunakan mikroskop dan SEM. Pengamatan menggunakan SEM dilakukan dengan cara melapisi mikrokapsul dengan logam emas dan dilihat pada pembesaran 500× dan 1500×.
HASIL DAN PEMBAHASAN
Mikroenkapsulasi Ibuprofen
karena bahan yang disalut terdispersi secara homogen pada matriks polimer. Penyalutan ini dianggap ideal untuk sistem pengantaran obat.
Pada metode ini, lilin lebah dan ibuprofen dilarutkan dalam diklorometana yang memiliki titik didih 39 ºC. Penguapan yang cepat pada pelarut akan menghasilkan mikrokapsul dengan lebih cepat sehingga efisiensi enkapsulasi lebih besar. Menurut Yeo dan Park (2004), diklorometana menghasilkan mikrokapsul lebih cepat daripada kloroform dan benzena karena memiliki kelarutan yang lebih baik dalam air. Kelarutan yang lebih baik dalam air akan membuat transfer massa antara fase terdispersi dan fase pendispersi relatif cepat sehingga polimer lebih cepat terendapkan.
Larutan kemudian didispersikan ke dalam air yang telah ditambahkan gelatin. Diklorometana akan menguap dari emulsi dan mikrokapsul akan mengendap. Gelatin berfungsi sebagai pengemulsi yang akan menurunkan tegangan permukaan antarfase, sehingga menstabilkan emulsi (Milanovic et al. 2010). Gelatin merupakan pengemulsi yang lebih terikat pada air dan akan membantu dispersi minyak dalam air (o/w). Gugus hidrofilik gelatin akan berikatan dengan molekul air, sedangkan gugus lipofiliknya akan berikatan dengan pelarut organik.
Variasi nisbah ibuprofen:lilin lebah dan konsentrasi gelatin menghasilkan mikrokapsul yang sama secara visual yaitu serbuk halus, kering, dan berwarna putih (Gambar 1). Rendemen yang dihasilkan dari berbagai variasi berkisar 77.17–88.84% (Lampiran 2). Rendemen terbesar diperoleh dari formula BB. Kecepatan pengadukan yang digunakan adalah 1000 rpm. Menurut Ranjha et al. (2010), kecepatan pengadukan ini akan menghasilkan rendemen yang tinggi.
Gambar 1 Mikrokapsul ibuprofen tersalut lilin lebah (1:1) dengan konsentrasi gelatin 2%.
Panjang Gelombang Maksimum dan Kurva Standar
Penentuan maks dilakukan pada daerah
ultraviolet karena larutan ibuprofen tidak berwarna. Pengukuran pada maks akan
menghasilkan perubahan absorbans untuk setiap satuan perubahan konsentrasi paling besar sehingga memiliki kepekaan yang maksimum (Sutrisna 2005). maks yang
diperoleh pada penentuan ini ialah 221.5 nm (Lampiran 3), mendekati nilai teoretis yaitu 222 nm (Depkes 1995).
Pelarut yang digunakan dalam pembuatan larutan ibuprofen adalah bufer fosfat pH 7.2. Nilai pH bufer tersebut dipilih untuk menyesuaikan dengan pH usus yang lazim digunakan sebagai medium disolusi tablet ibuprofen (Depkes 1995).
Persamaan regresi untuk kurva standar adalah y = 0.0451x + 0.0082 dengan nilai R2 sebesar 0.9997 (Lampiran 4). Hal ini sesuai dengan syarat yang ditetapkan oleh AOAC (2002) dengan nilai R2minimum 0.9900. Nilai koefisien determinasi yang tinggi menunjukkan hubungan yang linear antara sinyal detektor yang terukur dan jumlah ibuprofen dalam contoh. Persamaan yang diperoleh digunakan dalam perhitungan efisiensi enkapsulasi dan persentase pelepasan ibuprofen.
Efisiensi Enkapsulasi
Efisiensi enkapsulasi merupakan salah satu parameter keberhasilan proses enkapsulasi. Parameter ini menunjukkan persentase senyawa aktif (ibuprofen) yang berhasil disalut dalam mikrokapsul. Semakin tinggi efisiensi enkapsulasi, kemampuan obat untuk tersalut oleh mikrokapsul semakin baik (Kemala 2010).
4
Gambar 2 Efisiensi enkapsulasi mikrokapsul ibuprofen dengan konsentrasi gelatin = 1%; = 1.5%; = 2%; = 2.5%.
Variasi konsentrasi gelatin tidak memiliki pengaruh yang signifikan pada efisiensi enkapsulasi (Gambar 2). Kenaikan konsentrasi gelatin menjadi 2.5% cendrung menurunkan efisiensi enkapsulasi. Hal ini dapat dikarenakan konsentrasi pengemulsi yang terlalu tinggi menyebabkan mikrokapsul terbentuk lebih cepat sebelum pelarut menguap. Akibat pembentukan mikrokapsul yang belum sempurna, mikrokapsul mudah pecah pada saat pengadukan (Kemala 2010).
Pelepasan Obat
Salah satu tujuan mikroenkapsulasi ibuprofen adalah memodifikasi pelepasan ibuprofen (Kemala 2010). Uji disolusi dilakukan secara in vitro menggunakan alat disolusi tipe 2 (dayung) dalam medium bufer pH 7.2 untuk melihat laju pelepasan ibuprofen dalam usus. Mikrokapsul yang diuji disolusi adalah formula AC yang memiliki efisiensi enkapsulasi optimum, dilakukan sebanyak 2 ulangan. Rerata hasil pelepasan ibuprofen pada mikrokapsul adalah 12.53–38.22% b/b menit-1. Pelepasan ibuprofen mulai terjadi dari menit ke-15. Konsentrasi ibuprofen tertinggi terukur pada menit ke-150 dengan nilai 38.22% b/b menit-1 dan setelah itu, mengalami penurunan hingga menit ke-360. Hasil uji disolusi mikrokapsul ibuprofen diperlihatkan pada Lampiran 6 dan 7.
Profil disolusi dibuat dengan menghubungkan persen ibuprofen yang terlepas setiap 15 menit dengan waktu dalam
menit (Gambar 3). Terlihat bahwa penyalut lilin lebah dapat menurunkan kadar pelepasan ibuprofen dalam medium simulasi usus. Lapisan lilin lebah berfungsi sebagai matriks penghalang yang akan mengontrol pelepasan ibuprofen dari dalam matriks. Sutriyo et al. (2005) menyatakan, penambahan sejumlah bahan penyalut sebagai pembentuk dinding mikrokapsul akan menurunkan laju pelepasan obat. Penurunan laju pelepasan akan memberikan efek terapetik dalam jangka waktu yang lama.
Gambar 3 Profil pelepasan ibuprofen dari mikrokapsul formula AC terhadap waktu (menit) ulangan 1 dan ulangan 2 .
Kinetika Pelepasan Obat
Model kinetika pelepasan ibuprofen ditentukan berdasarkan koefisien determinasi yang diperoleh dari alur antara banyaknya obat yang lepas dan waktu. Pendekatan kinetika yang digunakan meliputi persamaan orde ke-0 (Q = Q0 + kt), orde ke-1 (ln [Q]t= ln [Q]0 - kt), Higuchi (Q = kt
1/2
), Hixson-Crowell (Q1/3= k(t)+ Q01/3), dan Korsmeyer-Peppas (Q
= k⋅tn) (Ranjha et al. 2010).
Kinetika pelepasan ibuprofen dikaji menggunakan data uji disolusi mikrokapsul formula AC (Lampiran 8). Model Korsmeyer-Peppas memiliki nilai R2 yang lebih besar daripada model kinetika lainnya, yaitu 0.9682 (Tabel 2). Hasil ini menunjukkan bahwa pelepasan ibuprofen dari mikrokapsul formula AC mengikuti mekanisme ini. Mekanisme pelepasan ibuprofen yang dominan dapat ditentukan dari nilai n (kemiringan) persamaan ini, yaitu nilai eksponensial difusi. Nilai n yang didapat adalah 0.45<n<0.89,
Tabel 2 Kinetika pelepasan ibuprofen dari mikrokapsul formula AC
Orde ke-0 Orde ke-1 Higuchi Hixson-Crowell Korsmeyer-Peppas
R2 k R2 k R2 k R2 k R2 n
0.8875 0.2734 0.8037 1.2370 0.9414 2.7680 0.8351 0.0018 0.9682 0.4763
0 10 20 30 40 50 60 70 80 90 100
1:1 1:2 1:3
E fi si e n si e n k a p su la si ( % )
menunjukkan mekanisme transpor difusi non-Fick (anomalous diffusion), suatu kombinasi antara mekanisme difusi dan erosi (Sanam et al. 2012). Pelepasan ibuprofen dari matriks lilin lebah dimulai sejak matriks kontak dengan medium disolusi, terjadi difusi cairan ke dalam matriks. Ibuprofen pada lapisan yang terdekat dengan permukaan matriks berdifusi pertama kali, dengan disertai pengikisan mikrokapsul oleh medium disolusi.
Morfologi Mikrokapsul
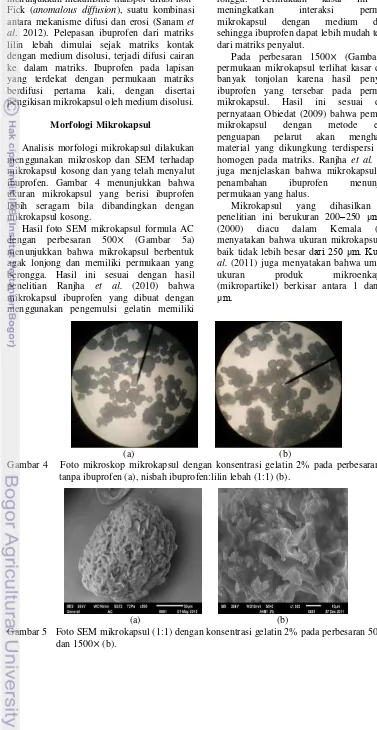
Analisis morfologi mikrokapsul dilakukan menggunakan mikroskop dan SEM terhadap mikrokapsul kosong dan yang telah menyalut ibuprofen. Gambar 4 menunjukkan bahwa ukuran mikrokapsul yang berisi ibuprofen lebih seragam bila dibandingkan dengan mikrokapsul kosong.
Hasil foto SEM mikrokapsul formula AC dengan perbesaran 500 (Gambar 5a) menunjukkan bahwa mikrokapsul berbentuk agak lonjong dan memiliki permukaan yang berongga. Hasil ini sesuai dengan hasil penelitian Ranjha et al. (2010) bahwa mikrokapsul ibuprofen yang dibuat dengan menggunakan pengemulsi gelatin memiliki
rongga. Permukaan kasar ini dapat meningkatkan interaksi permukaan mikrokapsul dengan medium disolusi sehingga ibuprofen dapat lebih mudah terlepas dari matriks penyalut.
Pada perbesaran 1500 (Gambar 5b), permukaan mikrokapsul terlihat kasar dengan banyak tonjolan karena hasil penyalutan ibuprofen yang tersebar pada permukaan mikrokapsul. Hasil ini sesuai dengan pernyataan Obiedat (2009) bahwa pembuatan mikrokapsul dengan metode emulsi-penguapan pelarut akan menghasilkan material yang dikungkung terdispersi secara homogen pada matriks. Ranjha et al. (2010) juga menjelaskan bahwa mikrokapsul tanpa penambahan ibuprofen menunjukkan permukaan yang halus.
Mikrokapsul yang dihasilkan pada penelitian ini berukuran 200–250 m. Jain (2000) diacu dalam Kemala (2010), menyatakan bahwa ukuran mikrokapsul yang baik tidak lebih besar dari 250 m. Kumar et al. (2011) juga menyatakan bahwa umumnya ukuran produk mikroenkapsulasi (mikropartikel) berkisar antara 1 dan 1000
m.
(a) (b)
Gambar 4 Foto mikroskop mikrokapsul dengan konsentrasi gelatin 2% pada perbesaran 40 : tanpa ibuprofen (a), nisbah ibuprofen:lilin lebah (1:1) (b).
(a) (b)
SIMPULAN DAN SARAN
Simpulan
Mikroenkapsulasi ibuprofen dengan penyalut lilin lebah dengan variasi nisbah ibuprofen:lilin lebah dan konsentrasi gelatin menghasilkan mikrokapsul dengan bentuk visual serbuk halus, kering, dan berwarna putih. Rendemen yang dihasilkan 77.17– 88.84%. Efisiensi enkapsulasi ibuprofen dipengaruhi oleh nisbah ibuprofen:lilin lebah. Variasi konsentrasi pengemulsi tidak memberikan pengaruh yang besar pada efisiensi enkapsulasi. Efisiensi enkapsulasi ibuprofen berkisar 65.08–93.78% dengan nilai tertinggi pada formula AC. Uji disolusi mikrokapsul optimum dalam medium simulasi cairan usus menunjukkan pelepasan 38.22%. Pola pelepasan ibuprofen yang lambatdengan adanya penyalut lilin lebah ini mengikuti model kinetika Korsmeyer-Peppas. Morfologi mikrokapsul ibuprofen menunjukkan bahwa ibuprofen tersebar pada matriks dengan ukuran 200–250 m.
Saran
Variasi pengemulsi dapat diteliti agar didapatkan mikrokapsul dengan permukaan yang lebih baik dan uji disolusi pada pH lambung dapat dilakukan untuk mengetahui persen pelepasan ibuprofen. Selain itu, ukuran dan distribusi mikrokapsul perlu diteliti lebih lanjut mengunakan penganalisis ukuran partikel.
DAFTAR PUSTAKA
Abdurohman R. 2011. Optimasi dan evaluasi mikrokapsul tersalut polipaduan
poliasamlaktat−lilin lebah [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
[AOAC] Association of Official Analytical Chemists. 2002. AOAC International methods committee guidelines for validation of qualitative and quantitative food microbiological official methods of analysis [terhubung berkala]. J AOAC Int. 85:1–5. [3 Jan 2012]
[Depkes] Departemen Kesehatan. 1995. Farmakope Indonesia. Ed ke-4. Jakarta: Depkes.
Garnier N, Olive´ CC, Rolando N, Regert M. 2002. Characterization of archaeological beeswax by electron ionization and electrospray ionization mass spectrometry. Anal Chem 74:4868-4877.
Gilman AG, Hardman JG, Limbird LE. 1996.
Goodman & Gilmans. The
Pharmacological Basic’s of Therapeutics.
Ed ke-9. New York: McGraw Hill.
Gowda DV, Ravi V, Shivakumar HG, Hatna S. 2009. Preparation, evaluation and bioavailability studies of indomethacin-bees wax microspheres. J Mater Sci: Mater Med 20:1447–1456.
Halder A, Sa B. 2006. Preparation and in vitro evaluation of polystyrene-coated ditiazem-resin complex by oil-in-water emulsion solvent evaporation method. AAPS Pharm Sci Tech 7:E1-E8.
Kemala T. 2010. Mikrosfer polipaduan poli(asam laktat) dengan poli(ɛ -kaprolakton) sebagai pelepasan terkendali ibuprofen secara in vitro [disertasi]. Depok: Program Pascasarjana, Universitas Indonesia.
Kumar A, Kumar AP, Arunabh B. 2011. Microencapsulation as a novel drug delivery system.Int Pharm Sci. 1(1):1-7.
Milanovic J, Manojlovic V, Levic S, Rajic N, Nevodic V, Bugarski B. 2010. Microencapsulation of flavors in carnauba wax. Sensor 10:901-912.
Obeidat WM. 2009. Recent patents review in microencapsulation of pharmaceuticals using the emulsion solvent removal methods. Recent Patents on Drug Delivery & Formulation. 3:178-192.
Park JH, Yee M, Park K. 2005. Biodegradable polymers for microencapsulation of drugs. Molecules 10:146-161.
Ranjha NM, Khan H, Naseem S. 2010. Encapsulation and characterization of controlled release flurbiprofen loaded microspheres using beeswax as an encapsulating agent. J Mater Sci: Mater Med 21:1621-1630.
7
Raval JP, Naik DR, Amin KA, Patel PS. 2011. Controlled-release and antibacterial studies of doxycycline-loaded poly(ɛ -caprolactone) microspheres Jignesh P. J Saudi Chem Soc4:1-8.
Sanam S, Halder S, Shuma Ml, Kabir Akl, Rashid Ro, Rouf Ass. 2012. Design and in-vitro evaluation of indapamide sustained release tablet using Methocel K15 MCR and Methocel K100M LVCR. Int J Parm Sci Res 3(4):1011-1017.
Sinuhaji PM. 2011. Mikroenkapsulasi ibuprofen tersalut poli(asam laktat)-lilin lebah dengan pengemulsi gelatin [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sutrisna EM. 2005. Uji efek penurunan kadar glukosa darah ekstrak air buah jambu biji (Psidium guajava L.) pada kelinci. Pharmacon 6(1):23-26.
Sutriyo, Joshinta D, Indah R. 2005. Perbandingan pelepasan propanolol
hidroklorida dari matriks kitosan, etil selulosa, dan hidroksipropil metil selulosa. Maj Ilmu Kefarmasian 2:145-153.
Tayade PT, Kale RD. 2004. Encapsulation of water-insoluble drug by a cross-linking technique: effect of process and formulation variables on encapsulation efficiency, particle size, and in vitro dissolution rate. AAPS Pharm Sci 6:1-8.
Yeo Y, Park K. 2004. Control of encapsulation efficiency and initial burst in polymeric microparticle system. Arch Pharm Res 27(1):1-12.
Yuliani S, Desmawarni, Harimurti N. 2007. Pengaruh laju alir umpan dan suhu inlet spray drying pada karakteristik mikrokapsul oleoresin jahe. J Pascapanen 4(1): 18-26.
9
Lampiran 1 Diagram alir penelitian
diklorometana
Ibuprofen Lilin lebah
diklorometana
Larutan gelatin 1.5%
Larutan gelatin 2.0% Larutan gelatin
1.0%
Karakteristik mikrokapsul Penentuan panjang gelombang maksimum dan kurva standar
Mikroskop dan SEM
M I K R O K A P S U L
Uji efisiensi
Lampiran 2 Rendemen mikrokapsul
Formula Bobot Hasil (%)
Lilin lebah (g) Ibuprofen (g) Mikrokapsul (g)
AA 0.5526 0.5582 0.8601 77.43
AB 0.5062 0.5088 0.8197 80.76
AC 0.5177 0.5069 0.8218 80.21
AD 0.5289 0.5264 0.8392 79.52
BA 0.5154 0.2541 0.6485 84.28
BB 0.5005 0.2547 0.6709 88.84
BC 0.5099 0.2510 0.6265 82.34
BD 0.5028 0.2502 0.5811 77.17
CA 0.5117 0.1679 0.5253 77.30
CB 0.5124 0.1695 0.597 87.55
CC 0.5023 0.1675 0.566 84.50
CD 0.5056 0.1667 0.5794 86.18
Contoh perhitungan:
endemen bobot bobot ibuprofenbobot mikrokapsul
(0.552 0.55 2) g0. 0 g
11
Lampiran 3 Spektrum absorpsi larutan ibuprofen
10 ppm
maks (nm) Absorbans
Lampiran 4 Kurva
standar ibuprofen (
maks = 221.5 nm)[ibuprofen]
(ppm) Absorbans
2.00 0.105
4.00 0.186
6.00 0.276
8.00 0.365
10.00 0.462
12.00 0.548
14.00 0.637
16.00 0.736
18.00 0.824
20.00 0.908
13
Lampiran 5 Efisiensi enkapsulasi ibuprofen dalam mikrokapsul tersalut lilin
lebah
Formula
Massa ibuprofen
(g)
a (g) b (g) c [ibuprofen] (ppm) fp
Efisiensi enkapsulasi
(%) AA 0.5582 0.8601 0.0251 0.678 14.8514 20 91.17 AB 0.5088 0.8197 0.0251 0.660 14.4523 20 92.76 AC 0.5069 0.8218 0.0251 0.663 14.5188 20 93.78 AD 0.5264 0.8392 0.0250 0.620 13.5654 20 86.51 BA 0.2541 0.6485 0.0252 0.800 17.5565 10 88.90 BB 0.2547 0.6709 0.0250 0.753 16.5144 10 87.00 BC 0.2510 0.6265 0.0252 0.753 16.5144 10 81.79 BD 0.2501 0.5811 0.0252 0.751 16.4701 10 75.90 CA 0.1679 0.5253 0.0252 0.481 10.4834 10 65.08 CB 0.1695 0.5970 0.0250 0.506 11.0377 10 77.75 CC 0.1675 0.5660 0.0250 0.582 12.7228 10 85.98 CD 0.1667 0.5794 0.0250 0.551 12.0355 10 83.66
Keterangan:
a : massa total kapsul yang diperoleh
b : massa kapsul yang digunakan untuk penentuan efisiensi mikroenkapsulsi c : absorbans filtrat hasil disolusi kapsul setelah diencerkan 10 kali
fp : faktor pengenceran
Contoh perhitungan (formula AA): y = 0.0082 + 0.0451x
0.678 = 0.0082 + 0.0451x x = 14.8514
Lampiran 6 Persentase rerata pelepasan ibuprofen dalam uji disolusi medium usus
dari mikrokapsul tersalut lilin lebah formula AC
Waktu (menit)
Persentaese pelepasan ibuprofen (%b/b) Rerata persentase pelepasan ibuprofen
(%b/b) Ulangan 1 Ulangan 2
0 0 0 0
15 11.83 13.24 12.53
30 19.07 20.28 19.68
45 21.05 21.77 21.41
60 29.90 28.09 29.00
75 34.03 30.00 32.01
90 34.24 33.38 33.81
105 35.16 34.75 34.96
120 35.43 35.43 35.43
135 36.86 36.47 36.67
150 38.50 37.94 38.22
165 35.40 33.45 34.42
180 34.90 34.22 34.56
195 34.57 33.29 33.93
210 32.28 32.21 32.24
225 33.26 33.10 33.18
240 32.29 32.09 32.19
255 31.99 31.54 31.77
270 32.12 31.19 31.65
285 30.65 31.38 31.02
300 31.87 30.32 31.10
315 30.27 29.26 29.77
330 30.33 29.49 29.91
345 29.99 28.91 29.45
15
Lampiran 7 Pelepasan ibuprofen dalam mikrokapsul pada waktu
t
Mikrokapsul Formula AC (Ulangan I)
Bobotmikrokapsul (g)
Waktu
(menit) Absorbans
[Ibuprofen] (ppm) Persentase pelepasan ibuprofen (%b/b) 0.2016
0 0.0000 0 0
15 0.2234 4.7716 11.83
30 0.3550 7.6896 19.07
45 0.3910 8.4878 21.05
60 0.5520 12.0576 29.90
75 0.6270 13.7206 34.03
90 0.6308 13.8049 34.24
105 0.6476 14.1774 35.16
120 0.6524 14.2838 35.43
135 0.6785 14.8625 36.86
150 0.7083 15.5233 38.50
165 0.6519 14.2727 35.40
180 0.6428 14.0710 34.90
195 0.6369 13.9401 34.57
210 0.5951 13.0133 32.28
225 0.6130 13.4102 33.26
240 0.5953 13.0177 32.29
255 0.5900 12.9002 31.99
270 0.5923 12.9512 32.12
285 0.5656 12.3592 30.65
300 0.5878 12.8514 31.87
315 0.5586 12.2040 30.27
330 0.5598 12.2306 30.33
345 0.5535 12.0909 29.99
360 0.5172 11.2860 27.99
Mikrokapsul Formula AC (Ulangan II) Bobot
mikrokapsul (g)
Waktu
(menit) Absorbans
[Ibuprofen] (ppm) Persentase pelepasan ibuprofen (%b/b) 0.2017
0 0.0000 0 0
15 0.2490 5.3392 13.24
30 0.3772 8.1818 20.28
45 0.4043 8.7827 21.77
60 0.5192 11.3304 28.09
75 0.5540 12.1020 30.00
90 0.6155 13.4656 33.38
105 0.6405 14.0200 34.75
120 0.6527 14.2905 35.43
135 0.6717 14.7118 36.47
150 0.6985 15.3060 37.94
165 0.6167 13.4922 33.45
180 0.6307 13.8027 34.22
195 0.6139 13.4302 33.29
210 0.5942 12.9933 32.21
225 0.6104 13.3525 33.10
240 0.5920 12.9446 32.09
255 0.5820 12.7228 31.54
270 0.5756 12.5809 31.19
285 0.5791 12.6585 31.38
300 0.5598 12.2306 30.32
315 0.5406 11.8049 29.26
330 0.5447 11.8958 29.49
345 0.5341 11.6608 28.91
Contoh perhitungan (mikrokapsul formula AC ulangan 1 menit ke-15):
100% l(g)
mikrokapsu massa
Vol.bufer 1000mL
1L 1000mg
1g fp ibuprofen ibuprofen
%pelepasan
100% 0.2016g
500mL 1000mL
1L 1000mg
1g 10 L mg 4.7716
(b/b)
11.83%
Lampiran 8 Kinetika pelepasan ibuprofen formula AC
Model kinetika Persamaan regresi R2
Orde ke-0 Q = 0.0033 + 0.27343 t 0.8875
i
ABSTRAK
GINA PRAGUSTIANA SOEMANTRI. Optimasi dan Evaluasi Mikrokapsul
Ibuprofen Tersalut Lilin Lebah. Dibimbing oleh TETTY KEMALA dan AHMAD
SJAHRIZA.
Ibuprofen merupakan obat antiradang nonsteroid untuk mengobati rematik.
Waktu paruh eliminasinya cepat sehingga dapat menimbulkan iritasi lambung,
maka diperlukan sistem pelepasan obat secara terkendali, antara lain dengan
teknik mikroenkapsulasi. Pada penelitian ini, mikroenkapsulasi ibuprofen
dilakukan
dengan
metode
emulsi-penguapan
pelarut.
Variasi
nisbah
ibuprofen:lilin lebah (1:1, 1:2, dan 1:3) dan konsentrasi pengemulsi gelatin (1, 1.5,
2, dan 2.5%) diujikan untuk mendapatkan mikrokapsul yang optimum. Persen
rendemen mikrokapsul yang dihasilkan sebesar 77.17
–
88.84%. Efisiensi
enkapsulasi ibuprofen tertinggi ialah 93.78%, diperoleh pada mikrokapsul dengan
nisbah ibuprofen:lilin lebah 1:1 dan konsentrasi gelatin 2%. Variasi konsentrasi
gelatin berpengaruh signifikan terhadap efisiensi enkapsulasi pada nisbah 1:3.
Mikrokapsul dengan efisiensi enkapsulasi tertinggi mengalami pelepasan
ibuprofen sebesar 38.22% dalam medium simulasi cairan usus selama 6 jam.
Kinetika pelepasan ibuprofen mengikuti model Korsmeyer-Peppas. Mikrokapsul
yang dihasilkan memiliki kisaran ukuran 200
–
250 µm. Berdasarkan hasil tersebut,
dapat disimpulkan bahwa mikroenkapsulasi ibuprofen dengan penyalut lilin lebah
dapat menahan laju pelepasan obat dalam usus.
ABSTRACT
GINA PRAGUSTIANA SOEMANTRI. Optimization and Evaluation of
Beeswax-Coated Ibuprofen Microcapsules. Supervised by TETTY KEMALA and
AHMAD SJAHRIZA.
PENDAHULUAN
Ibuprofen merupakan turunan asam fenilasetat dengan nama kimia asam 2-(4-isobutilfenil)propionat termasuk golongan obat non-steroid yang memberikan efek antiradang, antipretik, dan analgesik. Obat ini digunakan untuk menghilangkan nyeri dan peradangan pada saat migrain, nyeri pascaoperasi, dan sakit gigi (Rao et al. 2011). Dosis pemberian ibuprofen ialah 400 mg setiap 4–6 jam. Obat ini mudah diserap oleh saluran pencernaan dan kadar tertinggi dalam darah dicapai dalam waktu 1–2 jam setelah pemberian oral. Ekskresi ibuprofen terjadi dengan cepat dan sempurna. Lebih dari 90% dosis yang diberikan diekskresi melalui urin sebagai metabolit asam sekundernya (Gilman et al. 1996). Waktu paruh eliminasi yang cepat menyebabkan obat ini harus lebih sering dikonsumsi. Pengonsumsian obat secara berulang dalam dosis yang besar dapat menyebabkan iritasi pada saluran pencernaan. Untuk mengatasi hal tersebut, diperlukan sistem pelepasan ibuprofen terkendali, antara lain dengan pendekatan mikroenkapsulasi.
Mikroenkapsulasi merupakan teknik menyalut suatu senyawa menggunakan bahan penyalut berukuran sangat kecil dengan diameter rerata 15–20 mikron (Yoshizawa 2004). Teknik ini banyak digunakan sebagai sistem pengantaran obat karena dapat mengurangi efek samping, meningkatkan efektivitas terapi obat yang diberikan, dan mengendalikan pelepasan obat (Raval et al. 2011). Tantangan aplikasi teknologi mikroenkapsulasi terletak pada pemilihan teknik, bahan inti, dan bahan penyalut yang tepat sehingga kapsul dapat berfungsi sebagaimana mestinya (Yuliani et al. 2007). Bahan penyalut yang digunakan dapat beragam, dengan syarat dapat terdegradasi dan biokompatibel dalam tubuh.
Pada penelitian ini bahan penyalut yang digunakan adalah lilin lebah. Menurut Garnier et al. (2002), lilin lebah sangat kompleks, terbuat dari n-alkana jenuh dan tak jenuh, ester rantai panjang, asam lemak, diester, hidroksiester, dan konstituen minor lainnya, seperti flavonoid. Menurut Ranjha et al. (2010) lilin lebah dapat memiliki beberapa kelebihan sebagai bahan pembuat mikrosfer, yaitu stabil pada beberapa nilai pH dan tingkat kelembapan, biokompatibel, tidak imunogenik, dan memiliki efek yang minimum pada saluran pencernaan. Gowda et al. (2009) melakukan mikroenkapsulasi
indometasin menggunakan lilin lebah dengan metode emulsi-penguapan pelarut.
Metode emulsi-penguapan pelarut telah banyak digunakan untuk menyalut obat hidrofobik melalui proses emulsifikasi minyak dalam air (o/w) (Park et al. 2005). Mikrokapsul dibuat dengan melarutkan penyalut dan bahan inti dalam pelarut yang mudah menguap. Campuran didispersikan ke dalam air hingga terbentuk emulsi. Emulsi tidak stabil sehingga memerlukan penambahan zat pengemulsi. Gelatin telah banyak digunakan sebagai pengemulsi dalam pembuatan mikrokapsul (Sinuhaji 2012; Abdurohman 2011; Ranjha et al. 2010). Variasi nisbah penyalut dengan bahan inti serta konsentrasi pengemulsi akan berpengaruh terhadap mikrokapsul yang dihasilkan dan banyaknya obat yang tersalut (Kemala 2010).
Penelitian ini bertujuan menghasilkan mikrokapsul optimum, menentukan pengaruh variasi nisbah ibuprofen:lilin lebah dan konsentrasi pengemulsi terhadap efisiensi penyalutan ibuprofen, dan membuat profil pelepasan ibuprofen. Dari profil tersebut, ditentukan model kinetika pelepasan ibuprofen berdasarkan kriteria koefisien determinasi (R2) dari persamaan reaksi orde ke-0 dan ke-1, Higuchi, Hixson-Crowell, dan Korsmeyer-Peppas, serta mekanisme pelepasan obat yang dominan berdasarkan eksponen pelepasan (n) dari persamaan Korsmeyer-Peppas. Morfologi mikrokapsul yang dihasilkan juga dianalisis.
METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah lilin lebah yang diperoleh dari Sukabumi, ibuprofen p.a yang diperoleh dari PT Kalbe Farma, gelatin (bloom number 200), diklorometana, dan bufer fosfat (NaH2PO4-Na2HPO4) pH 7.2.
2
Lingkup Kerja
Penelitian ini dilakukan dalam beberapa tahapan (Lampiran 1). Mikrokapsul ibuprofen dibuat dengan variasi nisbah ibuprofen:lilin lebah dan konsentrasi gelatin. Mikrokapsul yang dihasikan diukur efisiensi penyalutan ibuprofennya, diuji disolusi, serta dicirikan dengan mikroskop dan SEM.
Pembuatan Mikrokapsul Ibuprofen Tersalut Lilin Lebah
Lilin lebah dilarutkan dalam diklorometana, diaduk hingga homogen. Setelah itu, ibuprofen yang telah dilarutkan dalam diklorometana dicampurkan. Campuran dibuat dengan variasi nisbah ibuprofen:lilin lebah kemudian didispersikan menggunakan motor pengaduk ke dalam air yang telah mengandung variasi konsentrasi gelatin (Tabel 1). Campuran didekantasi hingga mikrokapsul yang terbentuk mengendap. Mikrokapsul disaring, dicuci dengan akuades, dikeringudarakan selama 1 hari.
Tabel 1 Nisbah mikrokapsul ibuprofen tersalut lilin lebah dan variasi konsentrasi gelatin
Formula Nisbah ibuprofen: lilin lebah
Konsentrasi gelatin (%)
AA 1:1 1
AB 1:1 1.5
AC 1:1 2
AD 1:1 2.5
BA 1:2 1
BB 1:2 1.5
BC 1:2 2
BD 1:2 2.5
CA 1:3 1
CB 1:3 1.5
CC 1:3 2
CD 1:3 2.5
Penentuan Panjang Gelombang Maksimum dan Pembuatan Kurva Standar
Larutan ibuprofen dalam bufer fosfat pH 7.2 dengan konsentrasi 10 ppm diukur absorbansnya pada panjang gelombang ( ) 210–240 nm menggunakan spekrofotometer UV. Panjang gelombang maksimum ( maks)
yang diperoleh digunakan untuk analisis selanjutnya.
Kurva standar dibuat dengan mengukur absorbans larutan ibuprofen dengan konsentrasi 2, 4, 6, 8, 10, 12, 14, 16, 18, dan 20 ppm pada panjang gelombang maksimum. Hasil yang diperoleh merupakan hubungan konsentrasi ibuprofen dengan absorbans.
Efisiensi Enkapsulasi
Sebanyak 25 mg mikrokapsul ditimbang dan dilarutkan dalam 50 mL bufer fosfat pH 7.2. Campuran dikocok selama 24 jam lalu disaring (Tayade & Kale 2004). Filtrat diencerkan 10 kali dan dibaca absorbansnya dengan spektrofotometer UV pada maks
(221.5 nm). Absorbans yang diperoleh digunakan untuk menentukan konsentrasi ibuprofen dengan bantuan kurva standar.
Uji Disolusi secara In Vitro (Depkes 1995)
Uji disolusi mikrokapsul dilakukan dengan alat disolusi tipe 2 (tipe dayung). Sebanyak 200 mg mikrokapsul ditimbang dan dimasukkan ke dalam bejana disolusi. Uji disolusi dilakukan dalam medium simulasi cairan usus (larutan bufer fosfat pH 7.2) selama 6 jam pada suhu (37 ± 0.5)°C dengan kecepatan pengadukan 100 rpm. Volume medium disolusi yang digunakan sebanyak 500 mL. Pengambilan alikuot dilakukan setiap 15 menit dengan volume setiap pengambilan 10 mL. Setiap pengambilan alikuot, volume medium yang terambil digantikan dengan larutan medium baru dengan volume dan suhu yang sama. Konsentrasi ibuprofen dalam alikuot diukur menggunakan spektrofotometer UV pada maks (221.5 nm). Dari data yang
diperoleh, dibuat kurva hubungan antara persen pelepasan ibuprofen dan waktu disolusi, serta dikaji kinetika pelepasannya.
Morfologi Mikrokapsul
Pengamatan morfologi mikrokapsul dilakukan terhadap mikrokapsul kosong dan yang terisi ibuprofen dengan menggunakan mikroskop dan SEM. Pengamatan menggunakan SEM dilakukan dengan cara melapisi mikrokapsul dengan logam emas dan dilihat pada pembesaran 500× dan 1500×.
HASIL DAN PEMBAHASAN
Mikroenkapsulasi Ibuprofen
karena bahan yang disalut terdispersi secara homogen pada matriks polimer. Penyalutan ini dianggap ideal untuk sistem pengantaran obat.
Pada metode ini, lilin lebah dan ibuprofen dilarutkan dalam diklorometana yang memiliki titik didih 39 ºC. Penguapan yang cepat pada pelarut akan menghasilkan mikrokapsul dengan lebih cepat sehingga efisiensi enkapsulasi lebih besar. Menurut Yeo dan Park (2004), diklorometana menghasilkan mikrokapsul lebih cepat daripada kloroform dan benzena karena memiliki kelarutan yang lebih baik dalam air. Kelarutan yang lebih baik dalam air akan membuat transfer massa antara fase terdispersi dan fase pendispersi relatif cepat sehingga polimer lebih cepat terendapkan.
Larutan kemudian didispersikan ke dalam air yang telah ditambahkan gelatin. Diklorometana akan menguap dari emulsi dan mikrokapsul akan mengendap. Gelatin berfungsi sebagai pengemulsi yang akan menurunkan tegangan permukaan antarfase, sehingga menstabilkan emulsi (Milanovic et al. 2010). Gelatin merupakan pengemulsi yang lebih terikat pada air dan akan membantu dispersi minyak dalam air (o/w). Gugus hidrofilik gelatin akan berikatan dengan molekul air, sedangkan gugus lipofiliknya akan berikatan dengan pelarut organik.
Variasi nisbah ibuprofen:lilin lebah dan konsentrasi gelatin menghasilkan mikrokapsul yang sama secara visual yaitu serbuk halus, kering, dan berwarna putih (Gambar 1). Rendemen yang dihasilkan dari berbagai variasi berkisar 77.17–88.84% (Lampiran 2). Rendemen terbesar diperoleh dari formula BB. Kecepatan pengadukan yang digunakan adalah 1000 rpm. Menurut Ranjha et al. (2010), kecepatan pengadukan ini akan menghasilkan rendemen yang tinggi.
Gambar 1 Mikrokapsul ibuprofen tersalut lilin lebah (1:1) dengan konsentrasi gelatin 2%.
Panjang Gelombang Maksimum dan Kurva Standar
Penentuan maks dilakukan pada daerah
ultraviolet karena larutan ibuprofen tidak berwarna. Pengukuran pada maks akan
menghasilkan perubahan absorbans untuk setiap satuan perubahan konsentrasi paling besar sehingga memiliki kepekaan yang maksimum (Sutrisna 2005). maks yang
diperoleh pada penentuan ini ialah 221.5 nm (Lampiran 3), mendekati nilai teoretis yaitu 222 nm (Depkes 1995).
Pelarut yang digunakan dalam pembuatan larutan ibuprofen adalah bufer fosfat pH 7.2. Nilai pH bufer tersebut dipilih untuk menyesuaikan dengan pH usus yang lazim digunakan sebagai medium disolusi tablet ibuprofen (Depkes 1995).
Persamaan regresi untuk kurva standar adalah y = 0.0451x + 0.0082 dengan nilai R2 sebesar 0.9997 (Lampiran 4). Hal ini sesuai dengan syarat yang ditetapkan oleh AOAC (2002) dengan nilai R2minimum 0.9900. Nilai koefisien determinasi yang tinggi menunjukkan hubungan yang linear antara sinyal detektor yang terukur dan jumlah ibuprofen dalam contoh. Persamaan yang diperoleh digunakan dalam perhitungan efisiensi enkapsulasi dan persentase pelepasan ibuprofen.
Efisiensi Enkapsulasi
Efisiensi enkapsulasi merupakan salah satu parameter keberhasilan proses enkapsulasi. Parameter ini menunjukkan persentase senyawa aktif (ibuprofen) yang berhasil disalut dalam mikrokapsul. Semakin tinggi efisiensi enkapsulasi, kemampuan obat untuk tersalut oleh mikrokapsul semakin baik (Kemala 2010).
4
Gambar 2 Efisiensi enkapsulasi mikrokapsul ibuprofen dengan konsentrasi gelatin = 1%; = 1.5%; = 2%; = 2.5%.
Variasi konsentrasi gelatin tidak memiliki pengaruh yang signifikan pada efisiensi enkapsulasi (Gambar 2). Kenaikan konsentrasi gelatin menjadi 2.5% cendrung menurunkan efisiensi enkapsulasi. Hal ini dapat dikarenakan konsentrasi pengemulsi yang terlalu tinggi menyebabkan mikrokapsul terbentuk lebih cepat sebelum pelarut menguap. Akibat pembentukan mikrokapsul yang belum sempurna, mikrokapsul mudah pecah pada saat pengadukan (Kemala 2010).
Pelepasan Obat
Salah satu tujuan mikroenkapsulasi ibuprofen adalah memodifikasi pelepasan ibuprofen (Kemala 2010). Uji disolusi dilakukan secara in vitro menggunakan alat disolusi tipe 2 (dayung) dalam medium bufer pH 7.2 untuk melihat laju pelepasan ibuprofen dalam usus. Mikrokapsul yang diuji disolusi adalah formula AC yang memiliki efisiensi enkapsulasi optimum, dilakukan sebanyak 2 ulangan. Rerata hasil pelepasan ibuprofen pada mikrokapsul adalah 12.53–38.22% b/b menit-1. Pelepasan ibuprofen mulai terjadi dari menit ke-15. Konsentrasi ibuprofen tertinggi terukur pada menit ke-150 dengan nilai 38.22% b/b menit-1 dan setelah itu, mengalami penurunan hingga menit ke-360. Hasil uji disolusi mikrokapsul ibuprofen diperlihatkan pada Lampiran 6 dan 7.
Profil disolusi dibuat dengan menghubungkan persen ibuprofen yang terlepas setiap 15 menit dengan waktu dalam
menit (Gambar 3). Terlihat bahwa penyalut lilin lebah dapat menurunkan kadar pelepasan ibuprofen dalam medium simulasi usus. Lapisan lilin lebah berfungsi sebagai matriks penghalang yang akan mengontrol pelepasan ibuprofen dari dalam matriks. Sutriyo et al. (2005) menyatakan, penambahan sejumlah bahan penyalut sebagai pembentuk dinding mikrokapsul akan menurunkan laju pelepasan obat. Penurunan laju pelepasan akan memberikan efek terapetik dalam jangka waktu yang lama.
Gambar 3 Profil pelepasan ibuprofen dari mikrokapsul formula AC terhadap waktu (menit) ulangan 1 dan ulangan 2 .
Kinetika Pelepasan Obat
Model kinetika pelepasan ibuprofen ditentukan berdasarkan koefisien determinasi yang diperoleh dari alur antara banyaknya obat yang lepas dan waktu. Pendekatan kinetika yang digunakan meliputi persamaan orde ke-0 (Q = Q0 + kt), orde ke-1 (ln [Q]t= ln [Q]0 - kt), Higuchi (Q = kt
1/2
), Hixson-Crowell (Q1/3= k(t)+ Q01/3), dan Korsmeyer-Peppas (Q
= k⋅tn) (Ranjha et al. 2010).
Kinetika pelepasan ibuprofen dikaji menggunakan data uji disolusi mikrokapsul formula AC (Lampiran 8). Model Korsmeyer-Peppas memiliki nilai R2 yang lebih besar daripada model kinetika lainnya, yaitu 0.9682 (Tabel 2). Hasil ini menunjukkan bahwa pelepasan ibuprofen dari mikrokapsul formula AC mengikuti mekanisme ini. Mekanisme pelepasan ibuprofen yang dominan dapat ditentukan dari nilai n (kemiringan) persamaan ini, yaitu nilai eksponensial difusi. Nilai n yang didapat adalah 0.45<n<0.89,
Tabel 2 Kinetika pelepasan ibuprofen dari mikrokapsul formula AC
Orde ke-0 Orde ke-1 Higuchi Hixson-Crowell Korsmeyer-Peppas
R2 k R2 k R2 k R2 k R2 n
0.8875 0.2734 0.8037 1.2370 0.9414 2.7680 0.8351 0.0018 0.9682 0.4763
0 10 20 30 40 50 60 70 80 90 100
1:1 1:2 1:3
E fi si e n si e n k a p su la si ( % )
menunjukkan mekanisme transpor difusi non-Fick (anomalous diffusion), suatu kombinasi antara mekanisme difusi dan erosi (Sanam et al. 2012). Pelepasan ibuprofen dari matriks lilin lebah dimulai sejak matriks kontak dengan medium disolusi, terjadi difusi cairan ke dalam matriks. Ibuprofen pada lapisan yang terdekat dengan permukaan matriks berdifusi pertama kali, dengan disertai pengikisan mikrokapsul oleh medium disolusi.
Morfologi Mikrokapsul
Analisis morfologi mikrokapsul dilakukan menggunakan mikroskop dan SEM terhadap mikrokapsul kosong dan yang telah menyalut ibuprofen. Gambar 4 menunjukkan bahwa ukuran mikrokapsul yang berisi ibuprofen lebih seragam bila dibandingkan dengan mikrokapsul kosong.
Hasil foto SEM mikrokapsul formula AC dengan perbesaran 500 (Gambar 5a) menunjukkan bahwa mikrokapsul berbentuk agak lonjong dan memiliki permukaan yang berongga. Hasil ini sesuai dengan hasil penelitian Ranjha et al. (2010) bahwa mikrokapsul ibuprofen yang dibuat dengan menggunakan pengemulsi gelatin memiliki
rongga. Permukaan kasar ini dapat meningkatkan interaksi permukaan mikrokapsul dengan medium disolusi sehingga ibuprofen dapat lebih mudah terlepas dari matriks penyalut.
Pada perbesaran 1500 (Gambar 5b), permukaan mikrokapsul terlihat kasar dengan banyak tonjolan karena hasil penyalutan ibuprofen yang tersebar pada permukaan mikrokapsul. Hasil ini sesuai dengan pernyataan Obiedat (2009) bahwa pembuatan mikrokapsul dengan metode emulsi-penguapan pelarut akan menghasilkan material yang dikungkung terdispersi secara homogen pada matriks. Ranjha et al. (2010) juga menjelaskan bahwa mikrokapsul tanpa penambahan ibuprofen menunjukkan permukaan yang halus.
Mikrokapsul yang dihasilkan pada penelitian ini berukuran 200–250 m. Jain (2000) diacu dalam Kemala (2010), menyatakan bahwa ukuran mikrokapsul yang baik tidak lebih besar dari 250 m. Kumar et al. (2011) juga menyatakan bahwa umumnya ukuran produk mikroenkapsulasi (mikropartikel) berkisar antara 1 dan 1000
m.
(a) (b)
Gambar 4 Foto mikroskop mikrokapsul dengan konsentrasi gelatin 2% pada perbesaran 40 : tanpa ibuprofen (a), nisbah ibuprofen:lilin lebah (1:1) (b).
(a) (b)
[image:32.595.106.483.106.836.2]6
SIMPULAN DAN SARAN
Simpulan
Mikroenkapsulasi ibuprofen dengan penyalut lilin lebah dengan variasi nisbah ibuprofen:lilin lebah dan konsentrasi gelatin menghasilkan mikrokapsul dengan bentuk visual serbuk halus, kering, dan berwarna putih. Rendemen yang dihasilkan 77.17– 88.84%. Efisiensi enkapsulasi ibuprofen dipengaruhi oleh nisbah ibuprofen:lilin lebah. Variasi konsentrasi pengemulsi tidak memberikan pengaruh yang besar pada efisiensi enkapsulasi. Efisiensi enkapsulasi ibuprofen berkisar 65.08–93.78% dengan nilai tertinggi pada formula AC. Uji disolusi mikrokapsul optimum dalam medium simulasi cairan usus menunjukkan pelepasan 38.22%. Pola pelepasan ibuprofen yang lambatdengan adanya penyalut lilin lebah ini mengikuti model kinetika Korsmeyer-Peppas. Morfologi mikrokapsul ibuprofen menunjukkan bahwa ibuprofen tersebar pada matriks dengan ukuran 200–250 m.
Saran
Variasi pengemulsi dapat diteliti agar didapatkan mikrokapsul dengan permukaan yang lebih baik dan uji disolusi pada pH lambung dapat dilakukan untuk mengetahui persen pelepasan ibuprofen. Selain itu, ukuran dan distribusi mikrokapsul perlu diteliti lebih lanjut mengunakan penganalisis ukuran partikel.
DAFTAR PUSTAKA
Abdurohman R. 2011. Optimasi dan evaluasi mikrokapsul tersalut polipaduan
poliasamlaktat−lilin lebah [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
[AOAC] Association of Official Analytical Chemists. 2002. AOAC International methods committee guidelines for validation of qualitative and quantitative food microbiological official methods of analysis [terhubung berkala]. J AOAC Int. 85:1–5. [3 Jan 2012]
[Depkes] Departemen Kesehatan. 1995. Farmakope Indonesia. Ed ke-4. Jakarta: Depkes.
Garnier N, Olive´ CC, Rolando N, Regert M. 2002. Characterization of archaeological beeswax by electron ionization and electrospray ionization mass spectrometry. Anal Chem 74:4868-4877.
Gilman AG, Hardman JG, Limbird LE. 1996.
Goodman & Gilmans. The
Pharmacological Basic’s of Therapeutics.
Ed ke-9. New York: McGraw Hill.
Gowda DV, Ravi V, Shivakumar HG, Hatna S. 2009. Preparation, evaluation and bioavailability studies of indomethacin-bees wax microspheres. J Mater Sci: Mater Med 20:1447–1456.
Halder A, Sa B. 2006. Preparation and in vitro evaluation of polystyrene-coated ditiazem-resin complex by oil-in-water emulsion solvent evaporation method. AAPS Pharm Sci Tech 7:E1-E8.
Kemala T. 2010. Mikrosfer polipaduan poli(asam laktat) dengan poli(ɛ -kaprolakton) sebagai pelepasan terkendali ibuprofen secara in vitro [disertasi]. Depok: Program Pascasarjana, Universitas Indonesia.
Kumar A, Kumar AP, Arunabh B. 2011. Microencapsulation as a novel drug delivery system.Int Pharm Sci. 1(1):1-7.
Milanovic J, Manojlovic V, Levic S, Rajic N, Nevodic V, Bugarski B. 2010. Microencapsulation of flavors in carnauba wax. Sensor 10:901-912.
Obeidat WM. 2009. Recent patents review in microencapsulation of pharmaceuticals using the emulsion solvent removal methods. Recent Patents on Drug Delivery & Formulation. 3:178-192.
Park JH, Yee M, Park K. 2005. Biodegradable polymers for microencapsulation of drugs. Molecules 10:146-161.
Ranjha NM, Khan H, Naseem S. 2010. Encapsulation and characterization of controlled release flurbiprofen loaded microspheres using beeswax as an encapsulating agent. J Mater Sci: Mater Med 21:1621-1630.
ii
OPTIMASI DAN EVALUASI MIKROKAPSUL IBUPROFEN
TERSALUT LILIN LEBAH
GINA PRAGUSTIANA SOEMANTRI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
7
Raval JP, Naik DR, Amin KA, Patel PS. 2011. Controlled-release and antibacterial studies of doxycycline-loaded poly(ɛ -caprolactone) microspheres Jignesh P. J Saudi Chem Soc4:1-8.
Sanam S, Halder S, Shuma Ml, Kabir Akl, Rashid Ro, Rouf Ass. 2012. Design and in-vitro evaluation of indapamide sustained release tablet using Methocel K15 MCR and Methocel K100M LVCR. Int J Parm Sci Res 3(4):1011-1017.
Sinuhaji PM. 2011. Mikroenkapsulasi ibuprofen tersalut poli(asam laktat)-lilin lebah dengan pengemulsi gelatin [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sutrisna EM. 2005. Uji efek penurunan kadar glukosa darah ekstrak air buah jambu biji (Psidium guajava L.) pada kelinci. Pharmacon 6(1):23-26.
Sutriyo, Joshinta D, Indah R. 2005. Perbandingan pelepasan propanolol
hidroklorida dari matriks kitosan, etil selulosa, dan hidroksipropil metil selulosa. Maj Ilmu Kefarmasian 2:145-153.
Tayade PT, Kale RD. 2004. Encapsulation of water-insoluble drug by a cross-linking technique: effect of process and formulation variables on encapsulation efficiency, particle size, and in vitro dissolution rate. AAPS Pharm Sci 6:1-8.
Yeo Y, Park K. 2004. Control of encapsulation efficiency and initial burst in polymeric microparticle system. Arch Pharm Res 27(1):1-12.
Yuliani S, Desmawarni, Harimurti N. 2007. Pengaruh laju alir umpan dan suhu inlet spray drying pada karakteristik mikrokapsul oleoresin jahe. J Pascapanen 4(1): 18-26.
9
Lampiran 1 Diagram alir penelitian
diklorometana
Ibuprofen Lilin lebah
diklorometana
Larutan gelatin 1.5%
Larutan gelatin 2.0% Larutan gelatin
1.0%
Karakteristik mikrokapsul Penentuan panjang gelombang maksimum dan kurva standar
Mikroskop dan SEM
M I K R O K A P S U L
Uji efisiensi
Lampiran 2 Rendemen mikrokapsul
Formula Bobot Hasil (%)
Lilin lebah (g) Ibuprofen (g) Mikrokapsul (g)
AA 0.5526 0.5582 0.8601 77.43
AB 0.5062 0.5088 0.8197 80.76
AC 0.5177 0.5069 0.8218 80.21
AD 0.5289 0.5264 0.8392 79.52
BA 0.5154 0.2541 0.6485 84.28
BB 0.5005 0.2547 0.6709 88.84
BC 0.5099 0.2510 0.6265 82.34
BD 0.5028 0.2502 0.5811 77.17
CA 0.5117 0.1679 0.5253 77.30
CB 0.5124 0.1695 0.597 87.55
CC 0.5023 0.1675 0.566 84.50
CD 0.5056 0.1667 0.5794 86.18
Contoh perhitungan:
endemen bobot bobot ibuprofenbobot mikrokapsul
(0.552 0.55 2) g0. 0 g
11
Lampiran 3 Spektrum absorpsi larutan ibuprofen
10 ppm
maks (nm) Absorbans
Lampiran 4 Kurva
standar ibuprofen (
maks = 221.5 nm)[ibuprofen]
(ppm) Absorbans
2.00 0.105
4.00 0.186
6.00 0.276
8.00 0.365
10.00 0.462
12.00 0.548
14.00 0.637
16.00 0.736
18.00 0.824
20.00 0.908
13
Lampiran 5 Efisiensi enkapsulasi ibuprofen dalam mikrokapsul tersalut lilin
lebah
Formula
Massa ibuprofen
(g)
a (g) b (g) c [ibuprofen] (ppm) fp
Efisiensi enkapsulasi
(%) AA 0.5582 0.8601 0.0251 0.678 14.8514 20 91.17 AB 0.5088 0.8197 0.0251 0.660 14.4523 20 92.76 AC 0.5069 0.8218 0.0251 0.663 14.5188 20 93.78 AD 0.5264 0.8392 0.0250 0.620 13.5654 20 86.51 BA 0.2541 0.6485 0.0252 0.800 17.5565 10 88.90 BB 0.2547 0.6709 0.0250 0.753 16.5144 10 87.00 BC 0.2510 0.6265 0.0252 0.753 16.5144 10 81.79 BD 0.2501 0.5811 0.0252 0.751 16.4701 10 75.90 CA 0.1679 0.5253 0.0252 0.481 10.4834 10 65.08 CB 0.1695 0.5970 0.0250 0.506 11.0377 10 77.75 CC 0.1675 0.5660 0.0250 0.582 12.7228 10 85.98 CD 0.1667 0.5794 0.0250 0.551 12.0355 10 83.66
Keterangan:
a : massa total kapsul yang diperoleh
b : massa kapsul yang digunakan untuk penentuan efisiensi mikroenkapsulsi c : absorbans filtrat hasil disolusi kapsul setelah diencerkan 10 kali
fp : faktor pengenceran
Contoh perhitungan (formula AA): y = 0.0082 + 0.0451x
0.678 = 0.0082 + 0.0451x x = 14.8514
Lampiran 6 Persentase rerata pelepasan ibuprofen dalam uji disolusi medium usus
dari mikrokapsul tersalut lilin lebah formula AC
Waktu (menit)
Persentaese pelepasan ibuprofen (%b/b) Rerata persentase pelepasan ibuprofen
(%b/b) Ulangan 1 Ulangan 2
0 0 0 0
15 11.83 13.24 12.53
30 19.07 20.28 19.68
45 21.05 21.77 21.41
60 29.90 28.09 29.00
75 34.03 30.00 32.01
90 34.24 33.38 33.81
105 35.16 34.75 34.96
120 35.43 35.43 35.43
135 36.86 36.47 36.67
150 38.50 37.94 38.22
165 35.40 33.45 34.42
180 34.90 34.22 34.56
195 34.57 33.29 33.93
210 32.28 32.21 32.24
225 33.26 33.10 33.18
240 32.29 32.09 32.19
255 31.99 31.54 31.77
270 32.12 31.19 31.65
285 30.65 31.38 31.02
300 31.87 30.32 31.10
315 30.27 29.26 29.77
330 30.33 29.49 29.91
345 29.99 28.91 29.45
15
Lampiran 7 Pelepasan ibuprofen dalam mikrokapsul pada waktu
t
Mikrokapsul Formula AC (Ulangan I)
Bobotmikrokapsul (g)
Waktu
(menit) Absorbans
[Ibuprofen] (ppm) Persentase pelepasan ibuprofen (%b/b) 0.2016
0 0.0000 0 0
15 0.2234 4.7716 11.83
30 0.3550 7.6896 19.07
45 0.3910 8.4878 21.05
60 0.5520 12.0576 29.90
75 0.6270 13.7206 34.03
90 0.6308 13.8049 34.24
105 0.6476 14.1774 35.16
120 0.6524 14.2838 35.43
135 0.6785 14.8625 36.86
150 0.7083 15.5233 38.50
165 0.6519 14.2727 35.40
180 0.6428 14.0710 34.90
195 0.6369 13.9401 34.57
210 0.5951 13.0133 32.28
225 0.6130 13.4102 33.26
240 0.5953 13.0177 32.29
255 0.5900 12.9002 31.99
270 0.5923 12.9512 32.12
285 0.5656 12.3592 30.65
300 0.5878 12.8514 31.87
315 0.5586 12.2040 30.27
330 0.5598 12.2306 30.33
345 0.5535 12.0909 29.99
360 0.5172 11.2860 27.99
Mikrokapsul Formula AC (Ulangan II) Bobot
mikrokapsul (g)
Waktu
(menit) Absorbans
[Ibuprofen] (ppm) Persentase pelepasan ibuprofen (%b/b) 0.2017
0 0.0000 0 0
15 0.2490 5.3392 13.24
30 0.3772 8.1818 20.28
45 0.4043 8.7827 21.77
60 0.5192 11.3304 28.09
75 0.5540 12.1020 30.00
90 0.6155 13.4656 33.38
105 0.6405 14.0200 34.75
120 0.6527 14.2905 35.43
135 0.6717 14.7118 36.47
150 0.6985 15.3060 37.94
165 0.6167 13.4922 33.45
180 0.6307 13.8027 34.22
195 0.6139 13.4302 33.29
210 0.5942 12.9933 32.21
225 0.6104 13.3525 33.10
240 0.5920 12.9446 32.09
255 0.5820 12.7228 31.54
270 0.5756 12.5809 31.19
285 0.5791 12.6585 31.38
300 0.5598 12.2306 30.32
315 0.5406 11.8049 29.26
330 0.5447 11.8958 29.49
345 0.5341 11.6608 28.91
Contoh perhitungan (mikrokapsul formula AC ulangan 1 menit ke-15):
100% l(g)
mikrokapsu massa
Vol.bufer 1000mL
1L 1000mg
1g fp ibuprofen ibuprofen
%pelepasan
100% 0.2016g
500mL 1000mL
1L 1000mg
1g 10 L mg 4.7716
(b/b)
11.83%
Lampiran 8 Kinetika pelepasan ibuprofen formula AC
Model kinetika Persamaan regresi R2
Orde ke-0 Q = 0.0033 + 0.27343 t 0.8875