i
ANALISIS KAPASITAS ANTIOKSIDAN DAN KANDUNGAN
TOTAL FENOL PADA BUAH
ZAHRA MUSTHAFAVI
DEPARTEMEN GIZI MASYARAKAT
FAKULTAS EKOLOGI MANUSIA
INSTITUT PERTANIAN BOGOR
BOGOR
iii
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Analisis Kapasitas Antioksidan dan Kandungan Total Fenol pada Buah adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, November 2014
Zahra Musthafavi
iii
ABSTRAK
ZAHRA MUSTHAFAVI. Analisis Kapasitas Antioksidan dan Kandungan Total Fenol pada Buah. Dibimbing oleh HARDINSYAH.
Buah merupakan salah satu potensi sumber antioksidan. Penelitian mengenai kapasitas antioksidan dan kandungan total fenol buah dari Indonesia masih sangat terbatas. Tujuan dari penelitian ini adalah untuk menganalisis kapasitas antioksidan dan kandungan total fenol dari berbagai jenis buah yang diperjualbelikan dan dikonsumsi di Indonesia. Tiga puluh jenis buah dipilih secara purposif di pasar Anyar, Bogor. Kapasitas antioksidan buah dianalisis menggunakan metode DPPH dan total fenol dianalisis menggunakan metode
Folin-Ciocalteau. Hasil menunjukkan bahwa asam jawa memiliki kapasitas antioksidan tertinggi dengan 76.15±0.09 mg AEAC/100 g. Pisang mas memiliki kapasitas antioksidan terendah dengan 1.29±0.14 mg AEAC/100 g. Buah berwarna tua memiliki rata-rata kapasitas antioksidan lebih tinggi dibandingkan dengan buah berwarna muda. Markisa memiliki kandungan total fenol tertinggi dengan 3.25±1.70 mg TAE/100 g, dan pisang kepok terendah dengan 0.12±0.29 mg TAE/100 g. Penelitian ini juga menunjukkan adanya korelasi positif antara kapasitas antioksidan dan kandungan total fenol (p<0.05; r=0.545).
Kata kunci: antioksidan, buah, total fenol
ABSTRACT
ZAHRA MUSTHAFAVI. Analysis of Antioxidant Capacity and Total Phenolic Content of Fruits. Supervised by HARDINSYAH
Fruit is one of potential sources of antioxidant. Very limited studies have been done in determining the antioxidant capacity and phenolic content of fruits of Indonesia. The objective of this study was to analyze the antioxidant capacity and phenolic content of various types of fruits is traded and consumed in Indonesia. Thirty kind of fruits were selected purposively in Anyar traditional market of Bogor. The antioxidant capacity of the fruits was evaluated by applying DPPH method and total phenolic content was analized by applying the Folin-Ciocalteau method. The results showed that tamarind has the highest antioxidant capacity of 76.15±0.09 mg AEAC/100 g Mas banana is the lowest antioxidant capacity of 1.29±0.14 mg AEAC/100 g. Dark-colored fruits have a higher antioxidant capacity than the light-colored fruit. Passion fruit has the highest total phenolic content of 3.25±1.70 mg TAE/100 g and kepok banana has the lowest total phenolic content of 0.12±0.29 mg TAE/100 g. This study also showed that the positive correlation between antioxidant capacity and total phenolic content (p<0.05; r=0.545).
v
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Gizi
dari Program Studi Ilmu Gizi pada Departemen Gizi Masyarakat
ANALISIS KAPASITAS ANTIOKSIDAN DAN KANDUNGAN
TOTAL FENOL PADA BUAH
ZAHRA MUSTHAFAVI
DEPARTEMEN GIZI MASYARAKAT FAKULTAS EKOLOGI MANUSIA
INSTITUT PERTANIAN BOGOR BOGOR
ix
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Topik penelitian yang dilaksanakan sejak bulan Maret 2014 ini ialah Analisis Kapasitas Antioksidan dan Kandungan Total Fenol pada Buah.
Penulis mengucapkan terima kasih kepada Bapak Prof. Dr. Ir. Hardinsyah, MS. selaku dosen pembimbing akademik dan pembimbing skripsi yang telah banyak memberikan saran dan dukungan dalam penulisan karya ilmiah ini. Ibu Dr. Katrin Roosita, SP., M.Si selaku dosen penguji yang telah memberikan banyak saran yang bermanfaat. Bapak Mashudi yang telah memberikan masukan terkait metode dan penggunaan alat, beserta seluruh laboran dan staf Departemen Gizi Masyarakat yang telah membantu selama penelitian.
Ungkapan terima kasih juga penulis sampaikan kepada kedua orangtua tercinta Lukito Muhammad dan Hatidjah, beserta kakak adik tersayang, M. Abdul Haqq, M. Ali Al Haqq dan Syarif Husain Alwi atas kasih sayang, doa, nasihat, dukungan, semangat, dan pengertian kalian sehingga penulis dapat berjuang dalam menyelesaikan skripsi ini dengan sebaik mungkin. Sahabat-sahabat tersayang yang telah memberikan bantuan dan motivasinya yaitu Agustina, Marisya Fitriyani, Raden Apriliani, Rotua Yulianti, Pvatmaya S Burhani, dan Lidyawati Gunawan. Rekan-rekan seperjuangan yang telah membantu penulis dalam melakukan penelitian, Dyah Pramudita Kristin, Nurisnani Putri Mandarini, Evi Nurlatifah, dan Rizki Amalia Thoif, serta rekan-rekan Gizi Masyarakat 47 dan semua pihak yang tidak bisa disebutkan satu persatu.
Semoga karya ilmiah ini bermanfaat.
Bogor, November 2014
v
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
Latar Belakang 1
Tujuan 2
Manfaat 2
METODE 2
Waktu dan Tempat 2
Alat dan Bahan 2
Tahapan 3
Pengolahan dan Analisis Data 6
HASIL DAN PEMBAHASAN 6
Karakteristik Buah 6
Rendemen Ekstrak 9
Kapasitas Antioksidan 10
Kandungan Total Fenol 16
Korelasi antara Kandungan Total Fenol dengan Kapasitas Antioksidan 18
SIMPULAN DAN SARAN 18
Simpulan 18
Saran 18
DAFTAR PUSTAKA 19
LAMPIRAN 23
vi
DAFTAR TABEL
1 Jenis buah yang dianalisis 3
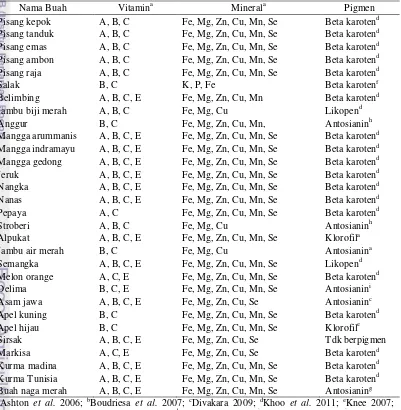
2 Nama buah, kandungan vitamin, mineral, dan pigmen dominannya 7
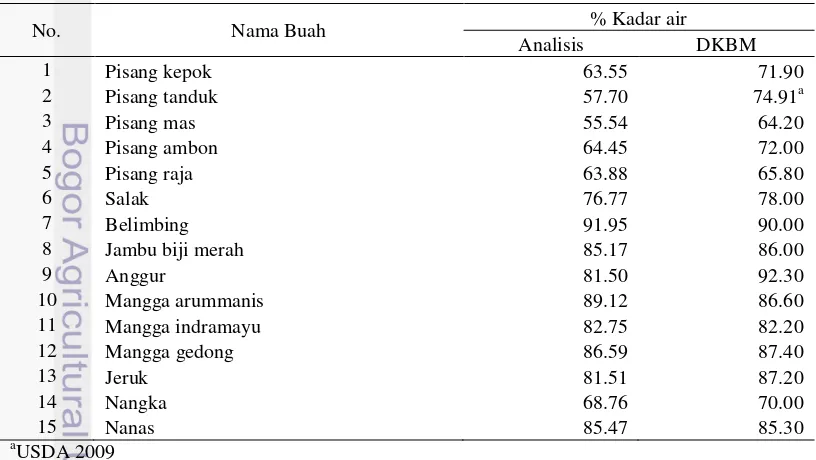
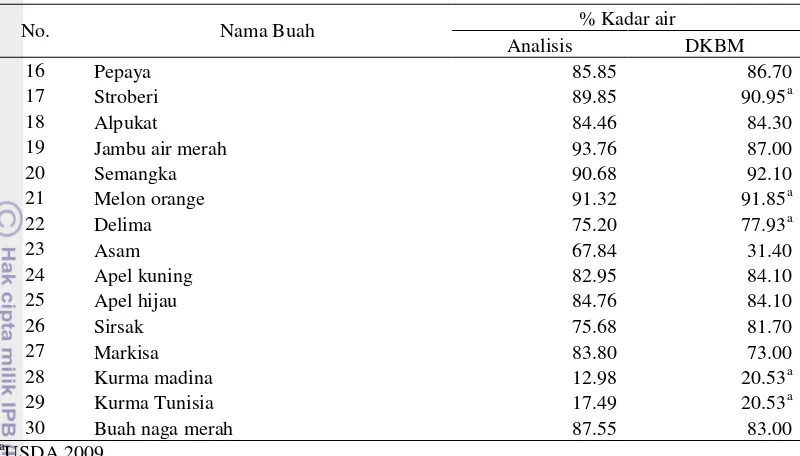
3 Kadar air 8
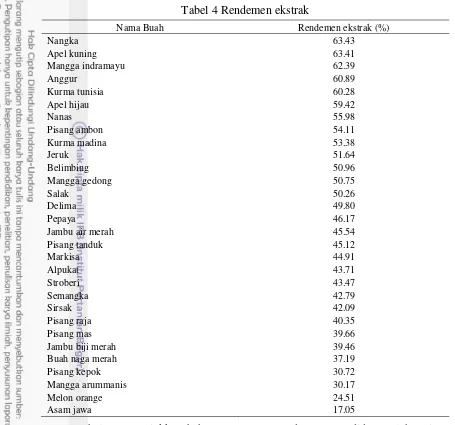
4 Rendemen ekstrak 10
5 Kemampuan meredam radikal bebas buah berwarna muda 13 6 Kemampuan meredam radikal bebas buah berwarna tua 14 7 Kapasitas antioksidan pada kelompok buah berwarna muda dan tua 16
8 Kandungan total fenol buah berwarna muda 17
9 Kandungan total fenol buah berwarna tua 17
DAFTAR GAMBAR
1 Tahap preparasi sampel 4
2 Tahapan analisis kadar air 4
3 Tahap ekstraksi sampel dengan maserasi 4
4 Tahap analisis kapasitas antioksidan 5
5 Tahap analisis kemampuan meredam radikal bebas DPPH 5 6 Tahap analisis kandungan total fenol dengan metode Folin-Ciocalteau 6
7 Kapasitas antioksidan buah berwarna muda 11
8 Kapasitas antioksidan buah berwarna tua 12
9 Kapasitas antioksidan 30 jenis buah 15
DAFTAR LAMPIRAN
1
Kadar air metode pemanasan langsung (AOAC 2006) 232 Rendemen ekstrak 24
3 Analisis kapasitas antioksidan 26
4 Analisis kandungan total fenol 28
5 Aktivitas peredaman radikal bebas DPPH 30
6 Rekapitulasi kemampuan meredam radikal bebas DPPH 35 7 Analisis kemampuan meredam radikal bebas DPPH 36 8 Uji korelasi antara kapasitas antioksidan dan kandungan total fenol 37
1
PENDAHULUAN
Latar Belakang
Senyawa bioaktif yang terkandung dalam bahan pangan salah satunya yaitu antioksidan. Antioksidan adalah senyawa yang mampu menangkap radikal bebas. Menurut Balch (2006), meningkatnya radikal bebas akibat pola makan tinggi lemak jenuh dan gula, serta rendah serat akan menyebabkan masalah kegemukan, gizi lebih, dan dapat memicu munculnya penyakit degeneratif.
Radikal bebas merupakan atom atau molekul yang mempunyai satu atau lebih elektron yang tidak berpasangan di orbit terluarnya . Radikal bebas dapat timbul dari proses metabolisme dalam tubuh dan dapat juga berasal dari lingkungan, seperti pencemaran udara, bahan kimia dari makanan dan air, alkohol, rokok, radiasi UV dan sebagainya. Radikal bebas ini bersifat reaktif dan tidak stabil sehingga untuk mencapai kestabilan atom atau molekul, radikal bebas akan bereaksi dengan molekul sel tubuh dengan cara mengikat elektron molekul tersebut. Proses ini pada akhirnya akan menimbulkan radikal bebas baru terhadap molekul yang elektronya diambil sehingga jumlahnya terus bertambah. Oleh karena itu, reaksi radikal bebas cenderung berupa reaksi berantai. Reaksi berantai ini akan terus menerus berlangsung dalam tubuh dan bila tidak segera dicegah dapat merusak sel-sel penting dalam tubuh. Hal ini akan menimbulkan berbagai penyakit seperti kanker, jantung, katarak, penuan dini, serta penyakit degeneratif lainya. Salah satu upaya untuk mengantisipasi kerusakan akibat radikal bebas tersebut maka tubuh memerlukan suatu substansi penting yaitu antioksidan yang mampu menangkap radikal bebas tersebut sehingga tidak dapat menginduksi suatu penyakit (Kikuzaki et al. 2002).
Antioksidan tidak hanya diperoleh dari asupan makanan yang banyak mengandung vitamin dan mineral, melainkan juga senyawa fenolik (Cavalcante et al. 2010). Senyawa golongan fenol diketahui sangat berperan terhadap aktivitas antioksidan, semakin besar kandungan senyawa golongan fenolnya maka semakin besar aktivitas antioksidannya (Kiessoun et al. 2010; Shahwar et al. 2010). Menurut Eklund et al. (2005), senyawa fenolik yang terdapat pada antioksidan alami mempunyai pengaruh biologis kuat khususnya sebagai antibakteri, antivirus, dan antitrombotik. Beberapa penelitian tentang aktivitas antioksidan dari senyawa fenolik mengatakan bahwa struktur dari senyawa tersebut dapat berkontribusi terhadap aktivitasnya (Apak et al. 2007). Aktivitas struktur dari fenolik sangat bergantung pada jumlah dan lokasi gugus fenol-OH yang berperan dalam menetralkan radikal bebas.
Salah satu bahan pangan yang mengandung senyawa fenolik dan memiliki aktivitas antioksidan adalah buah (Prakash 2001). Indonesia merupakan negara tropis yang kaya akan biodiversitas termasuk buah (Whitmore 1980). Kekayaan keanekaragaman jenis buah asli Indonesia juga cukup tinggi. Tidak kurang dari 329 jenis buah merupakan jenis asli Indonesia (Uji 2007).
2
Selain itu akan dilihat hubungan antara kapasitas antioksidan dengan kandungan total fenol.
Berdasarkan latar belakang yang telah diuraikan maka rumusan permasalahan yang akan menjadi fokus penelitian adalah berapa kapasitas antioksidan yang terkandung pada buah, berapa kandungan total fenol pada buah, dan bagaimana hubungan antara kapasitas antioksidan dan kandungan total fenol pada buah.
Tujuan
Tujuan umum dari penelitian ini adalah menganalisis kapasitas antioksidan dan kandungan total fenol dalam berbagai jenis buah yang diperjualbelikan dan dikonsumsi di Indonesia.
Adapun tujuan khusus dari penelitian ini adalah:
1. Menganalisis kapasitas antioksidan pada buah yang dikelompokkan berdasarkan buah berwarna muda dan berwarna tua.
2. Menganalisis kandungan total fenol pada buah.
3. Menganalisis hubungan antara kapasitas antioksidan dan kandungan total fenol pada buah.
Manfaat
Penelitian ini diharapkan mampu memberikan informasi mengenai kandungan senyawa aktif khususnya antioksidan pada buah yang umum dikonsumsi masyarakat. Selain itu, informasi ini diharapkan dapat meningkatkan kualitas hidup masyarakat dengan memilih pangan dengan kandungan antioksidan.
METODE
Waktu dan Tempat
Penelitian dilakukan dari bulan Maret hingga September 2014. Preparasi, ekstraksi, dan analisis kapasitas antioksidan dilakukan di Laboratorium Analisis Zat Gizi Departemen Gizi Masyarakat, Fakultas Ekologi Manusia. Selain itu sebagian tahap ekstraksi dilakukan di Laboratoroium Kultur Jaringan Departemen Agronomi dan Hortikultura, Laboratorium Nitrogen Departemen Manajemen dan Sumberdaya Lahan, serta Laboratorium Bakteriologi Departemen Proteksi Tanaman, Fakultas Pertanian-IPB,
Alat dan Bahan
Alat yang digunakan adalah freeze dryer, blender, timbangan digital,
3 reagen Folin Ciocalteau 50%, larutan natrium karbonat (Na2CO3) 2%, serta air bebas ion. Bahan pangan yang dianalisis berupa 30 jenis buah (Tabel 1).
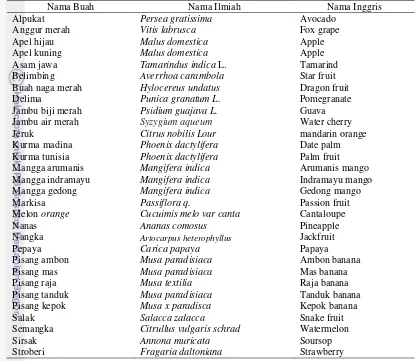
Tabel 1 Jenis buah yang dianalisis
Nama Buah Nama Ilmiah Nama Inggris
Alpukat Persea gratissima Avocado
Anggur merah Vitis labrusca Fox grape
Apel hijau Malus domestica Apple
Apel kuning Malus domestica Apple
Asam jawa Tamarindus indica L. Tamarind
Belimbing Averrhoa carambola Star fruit
Buah naga merah Hylocereus undatus Dragon fruit
Delima Punica granatum L. Pomegranate
Jambu biji merah Psidium guajava L. Guava
Jambu air merah Syzygium aqueum Water cherry
Jeruk Citrus nobilis Lour mandarin orange
Kurma madina Phoenix dactylifera Date palm
Kurma tunisia Phoenix dactylifera Palm fruit
Mangga arumanis Mangifera indica Arumanis mango
Mangga indramayu Mangifera indica Indramayu mango
Mangga gedong Mangifera indica Gedong mango
Markisa Passiflora q. Passion fruit
Melon orange Cucuimis melo var canta Cantaloupe
Nanas Ananas comosus Pineapple
Nangka Artocarpus heterophyllus Jackfruit
Pepaya Carica papaya Papaya
Pisang ambon Musa paradisiaca Ambon banana
Pisang mas Musa paradisiaca Mas banana
Pisang raja Musa textilia Raja banana
Pisang tanduk Musa paradisiaca Tanduk banana
Pisang kepok Musa x paradisca Kepok banana
Salak Salacca zalacca Snake fruit
Semangka Citrullus vulgaris schrad Watermelon
Sirsak Annona muricata Soursop
Stroberi Fragaria daltoniana Strawberry
Tahapan
Penelitian ini mencakup analisis kapasitas antioksidan dan kandungan total fenol yang dimulai dari sampling pangan, dilanjutkan dengan preparasi sampel, analisis kadar air, kapasitas antioksidan, kandungan total fenol, dan hubungan antara kandungan total fenol dengan kapasitas antioksidan.
Sampling Buah
4
Uji Laboratorium
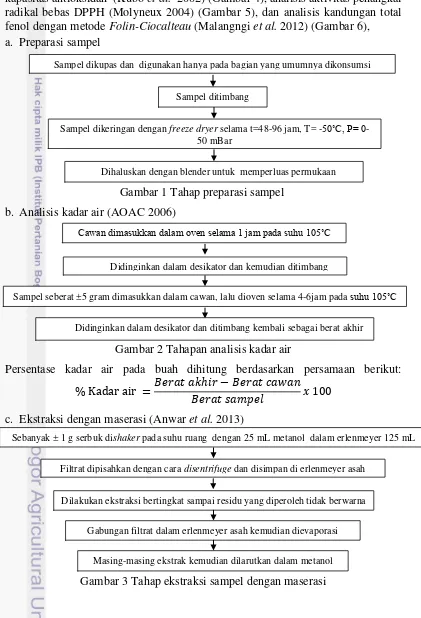
Tahapan uji laboratorium yang dilakukan meliputi preparasi sampel (Gambar 1), analisis kadar air dengan metode pemanasan langsung (AOAC 2006) (Gambar 2), ekstraksi dengan maserasi (Anwar et al. 2013) (Gambar 3), analisis kapasitas antioksidan (Kubo et al. 2002) (Gambar 4), analisis aktivitas penangkal radikal bebas DPPH (Molyneux 2004) (Gambar 5), dan analisis kandungan total fenol dengan metode Folin-Ciocalteau (Malangngi et al. 2012) (Gambar 6), a. Preparasi sampel
Gambar 1 Tahap preparasi sampel b. Analisis kadar air (AOAC 2006)
Gambar 2 Tahapan analisis kadar air
Persentase kadar air pada buah dihitung berdasarkan persamaan berikut:
% Kadar air = − 100
c. Ekstraksi dengan maserasi (Anwar et al. 2013)
Gambar 3 Tahap ekstraksi sampel dengan maserasi
Sebanyak ± 1 g serbuk dishaker pada suhu ruang dengan 25 mL metanol dalam erlenmeyer 125 mL
Dilakukan ekstraksi bertingkat sampai residu yang diperoleh tidak berwarna
Gabungan filtrat dalam erlenmeyer asah kemudian dievaporasi
Masing-masing ekstrak kemudian dilarutkan dalam metanol Filtrat dipisahkan dengan cara disentrifuge dan disimpan di erlenmeyer asah
Cawan dimasukkan dalam oven selama 1 jam pada suhu 105˚C
Didinginkan dalam desikator dan kemudian ditimbang beratnya
Sampel seberat ±5 gram dimasukkan dalam cawan, lalu dioven selama 4-6jam pada suhu 105˚C
Didinginkan dalam desikator dan ditimbang kembali sebagai berat akhir Sampel ditimbang
Sampel dikeringan dengan freeze dryer selama t=48-96 jam, T= -50˚C, P= 0 -50 mBar
Dihaluskan dengan blender untuk memperluas permukaan
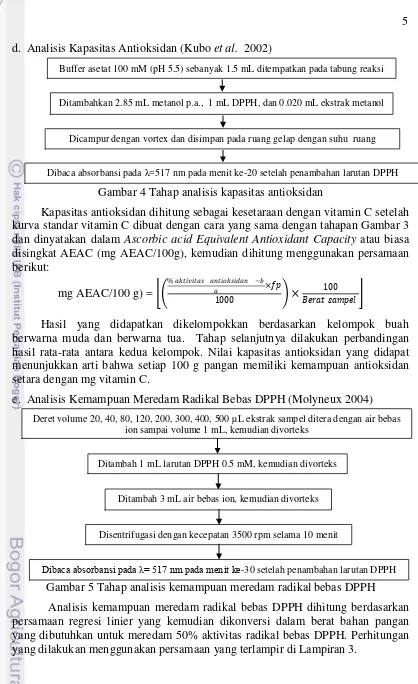
5 d. Analisis Kapasitas Antioksidan (Kubo et al. 2002)
Gambar 4 Tahap analisis kapasitas antioksidan
Kapasitas antioksidan dihitung sebagai kesetaraan dengan vitamin C setelah kurva standar vitamin C dibuat dengan cara yang sama dengan tahapan Gambar 3 dan dinyatakan dalam Ascorbic acid Equivalent Antioxidant Capacity atau biasa disingkat AEAC (mg AEAC/100g), kemudian dihitung menggunakan persamaan berikut:
mg AEAC/100 g) =
% −
×
1000 ×
100
Hasil yang didapatkan dikelompokkan berdasarkan kelompok buah berwarna muda dan berwarna tua. Tahap selanjutnya dilakukan perbandingan hasil rata-rata antara kedua kelompok. Nilai kapasitas antioksidan yang didapat menunjukkan arti bahwa setiap 100 g pangan memiliki kemampuan antioksidan setara dengan mg vitamin C.
e. Analisis Kemampuan Meredam Radikal Bebas DPPH (Molyneux 2004)
Gambar 5 Tahap analisis kemampuan meredam radikal bebas DPPH
Analisis kemampuan meredam radikal bebas DPPH dihitung berdasarkan persamaan regresi linier yang kemudian dikonversi dalam berat bahan pangan yang dibutuhkan untuk meredam 50% aktivitas radikal bebas DPPH. Perhitungan yang dilakukan menggunakan persamaan yang terlampir di Lampiran 3.
Deret volume 20, 40, 80, 120, 200, 300, 400, 500 µL ekstrak sampel ditera dengan air bebas ion sampai volume 1 mL, kemudian divorteks
Ditambah 1 mL larutan DPPH 0.5 mM, kemudian divorteks
Ditambah 3 mL air bebas ion, kemudian divorteks
Disentrifugasi dengan kecepatan 3500 rpm selama 10 menit
Dibaca absorbansi pada = 517 nm pada menit ke-30 setelah penambahan larutan DPPH
Buffer asetat 100 mM (pH 5.5) sebanyak 1.5 mL ditempatkan pada tabung reaksi
Ditambahkan 2.85 mL metanol p.a., 1 mL DPPH, dan 0.020 mL ekstrak metanol
Dicampur dengan vortex dan disimpan pada ruang gelap dengan suhu ruang
6
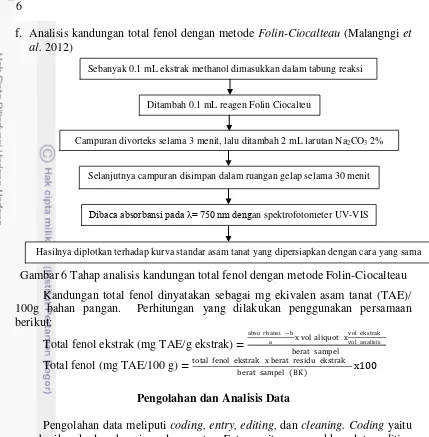
f. Analisis kandungan total fenol dengan metode Folin-Ciocalteau (Malangngi et al. 2012)
Gambar 6 Tahap analisis kandungan total fenol dengan metode Folin-Ciocalteau Kandungan total fenol dinyatakan sebagai mg ekivalen asam tanat (TAE)/ 100g bahan pangan. Perhitungan yang dilakukan penggunakan persamaan berikut:
Total fenol ekstrak (mg TAE/g ekstrak) =
abso rbansi −b
a x vol aliquot x
vol ekstrak vol analisis
berat sampel
Total fenol (mg TAE/100 g) =total fenol ekstrak x berat residu ekstrak
berat sampel (BK ) x100
Pengolahan dan Analisis Data
Pengolahan data meliputi coding, entry, editing, dan cleaning. Coding yaitu memberikan kode sebagai panduan entry. Entry yaitu memasukkan data, editing
yaitu pengecekan data, dan cleaning yaitu pengecekan ulang untuk memastikan tidak terdapat kesalahan dalam memasukkan data. Selanjutnya data diolah dengan program Microsoft excel 2010 dan dianalisis menggunakan Statistical Programme for Social Science (SPSS) version 16.0 for windows.
HASIL DAN PEMBAHASAN
Karakteristik Buah
Buah adalah organ pada tumbuhan berbunga yang merupakan perkembangan dari bakal buah (ovarium). Sebagai salah satu produk tumbuhan, buah memiliki nilai ekonomis yang tinggi sebagai pangan, karena didalamnya terkandung berbagai produk hasil metabolisme tumbuhan meliputi karbohidrat, protein, lemak, vitamin, mineral, bahkan terpena, dan terpenoid. Selain itu kandungan senyawa golongan fenolik dan polifenolik, membuatnya berperan sebagai pangan yang mengandung antioksidan. Menurut Dungira et al. (2012),
Sebanyak 0.1 mL ekstrak methanol dimasukkan dalam tabung reaksi
Ditambah 0.1 mL reagen Folin Ciocalteu
Campuran divorteks selama 3 menit, lalu ditambah 2 mL larutan Na2CO3 2%
Selanjutnya campuran disimpan dalam ruangan gelap selama 30 menit
Dibaca absorbansi pada = 750 nm dengan spektrofotometer UV-VIS
7 senyawa-senyawa golongan tersebut banyak terdapat di alam, terutama pada tumbuh-tumbuhan, dan memiliki kemampuan untuk menangkap radikal bebas. Zat lain pada buah yang juga berperan sebagai antioksidan antara lain vitamin E, vitamin C, dan karotenoid.
Buah mengandung senyawa fitokimia yang dapat memberikan cita rasa, aroma dan warna khas. Warna khas pada buah berasal dari pigmen tertentu yang terkandung di dalamnya. Pigmen atau zat pewarna yang paling dominan akan memberikan warna paling kuat pada makanan tertentu. Menurut Khoo et al.
(2011), pigmen menghasilkan warna karena memiliki kemampuan ikatan kimia untuk menyeleksi gelombang cahaya yang diserap dan dipantulkan. Bahan makanan berwana kuning, misalnya, jika disinari maka warna selain kuning akan diserap, dan yang dipantulkan ke mata kita hanyalah warna kuning. Begitu juga dengan warna lainnya. Penelitian ini menggunakan 30 jenis buah dan berikut disajikan karakteristik dari buah yang digunakan berdasarkan zat gizi dan kandungan pigmen dominannya.
Tabel 2 Nama buah, kandungan vitamin, mineral, dan pigmen dominannya
Nama Buah Vitamina Minerala Pigmen
8
Tabel 2 menunjukkan bahwa buah mengandung berbagai jenis vitamin dan mineral. Menurut Fang et al. (2002), beberapa jenis vitamin dan mineral seperti vitamin A, vitamin C, vitamin E, selenium, seng, zat besi, tembaga, mangan, magnesium dapat berperan dalam menangkal radikal bebas. Selain itu senyawa fitokimia yang memberikan warna pada buah pun beragam. Senyawa inilah yang juga ikut berperan sebagai antioksidan.
Kadar Air
Tahap pertama setelah sampel dipreparasi adalah melakukan analisis kadar air. Kadar air adalah banyaknya air yag terkandung oleh bahan yang dinyatakan dalam satuan persen. Analisis ini penting dilakukan karena terkait penampakan, tekstur, dan kesegaran suatu bahan pangan. Kadar air yang terlalu tinggi dapat menyebabkan suatu bahan pangan mudah rusak akibat bakteri, kapang, dan khamir (Suarni 2009).
Analisis kadar air yang dilakukan pada penelitian ini menggunakan metode pemanasan langsung (direct heating) (AOAC 2006). Menurut Wulandari (2011), prinsip dasar penetapan kadar air metode tersebut adalah menguapkan air yang terkandung dalam bahan dengan pemanasan secara langsung. Suatu bahan yang telah mengalami pengeringan lebih bersifat hidroskopis daripada bahan asalnya. Oleh karena itu selama pendinginan sebelum penimbangan, bahan harus ditempatkan di ruangan tertutup yang kering seperti desikator. Berat bahan yang konstan setelah pemanasan menujukkan semua air yang terkandung telah diuapkan. Metode ini dipilih karena relatif murah dan mudah.
Metode ini diawali dengan mengeringkan cawan logam dalam oven dengan suhu 105ºC selama 1 jam. Hal ini dilakukan untuk mengetahui berat konstan dari cawan. Selanjutnya cawan didinginkan dalam desikator dan siap ditimbang. Sampel sebanyak 3-5gram dimasukkan dalam cawan dan dilakukan pengeringan dengan suhu 105ºC selama 3 jam. Cawan sampel dimasukkan dalam desikator untuk pendinginan dan siap ditimbnag untuk pencatatan berat akhir. Berikut adalah hasil dari analisis kadar air yang telah dilakukan.
9 Tabel 3 Kadar air lanjutan
No. Nama Buah % Kadar air dilakukan, dimana sampel buah-buahan memiliki rata-rata kadar air sebesar 75.30% dan dapat dikatakan mengandung kadar air yang cukup tinggi. Hal ini sesuai dengan Julianti (2011), bahwa kadar air buah mencapai 65-90%. Tingginya kadar air membuat buah menjadi komoditi yang mudah rusak dikarenakan bakteri, kapang, dan khamir mudah berkembang.
Jambu air merah memiliki hasil analisis kadar air tertinggi dengan 93.76% dan kurma madina terendah dengan 12.98%. Namun hal ini berbeda dengan kadar air berdasarkan literatur yang menunjukkan melon orange memiliki kadar air tertinggi dengan 93.00% (Bankole et al. 2005) dan terendah asam jawa dengan 31.40% (DKBM 2007). Perbedaan hasil tersebut dapat disebabkan adanya perbedaan topografi, musim, dan penanganan sampel. Menurut Kurniawan & Widjanarko (2013), topografi, musim dan penanganan yang berbeda yang akan mengakibatkan perbedaan kualitas produk hortikultura yang dihasilkan. Selain itu perbedaan metode yang digunakan dapat menyebabkan perbedaan hasil analisis.
Rendemen Ekstrak
10
Tabel 4 Rendemen ekstrak
Nama Buah Rendemen ekstrak (%)
Nangka 63.43
Apel kuning 63.41
Mangga indramayu 62.39
Anggur 60.89
Kurma tunisia 60.28
Apel hijau 59.42
Nanas 55.98
Pisang ambon 54.11
Kurma madina 53.38
Jeruk 51.64
Belimbing 50.96
Mangga gedong 50.75
Salak 50.26
Delima 49.80
Pepaya 46.17
Jambu air merah 45.54
Pisang tanduk 45.12
Markisa 44.91
Jambu biji merah 39.46
Buah naga merah 37.19
Pisang kepok 30.72
Mangga arummanis 30.17
Melon orange 24.51
Asam jawa 17.05
Tabel 4 menunjukkan bahwa persentase rendemen yng didapat oleh setiap jenis sampel berbeda-beda. Sampel nangka memiliki persentase rendemen tertinggi yaitu sebesar 63.43% dan asam jawa terendah sebesar 17.05%. Menurut Cunha et al. (2004), beberapa faktor yang mempengaruhi rendemen antara lain mutu bahan baku (kondisi tanaman, umur panen), penanganan pascapanen (pengeringan dan penyimpanan) dan proses ekstraksi. Selain itu ukuran partikel dalam proses ektraksi akan mempengaruhi rendemen ekstrak yang dihasilkan, karena ukuran partikel sangat mempengaruhi internal difusi dari pelarut ke dalam padatan (Hernani 2009).
Kapasitas Antioksidan
11 sederhana, cepat, sensitif, dan hanya membutuhkan sedikit sampel. Selain itu metode DPPH juga merupakan metode uji kapasitas antioksidan yang paling banyak dilakukan. Prinsip analisis dengan menggunakan metode uji antioksidan DPPH adalah reaksi penangkapan radikal DPPH oleh hidrogen dari senyawa antioksidan (Molyneux 2004).
Analisis kapasitas antioksidan menggunakan asam askorbat (vitamin C) sebagai standar pengukuran sehingga satuan pengukuran dinyatakan sebagai AEAC (Ascorbic Acid Equivalent Antiokxidant Capacity). Vitamin C digunakan karena merupakan salah satu vitamin yang memiliki aktivitas antioksidan sebagai penangkal radikal bebas. Perbandingan antar sampel didasarkan pada bahan pangan dalam basis kering. Berikut disajikan kapasitas antioksidan pada kelompok buah berwarna muda terhadap kemampuan antioksidan vitamin C dalam basis kering dan basis basah (Gambar 7).
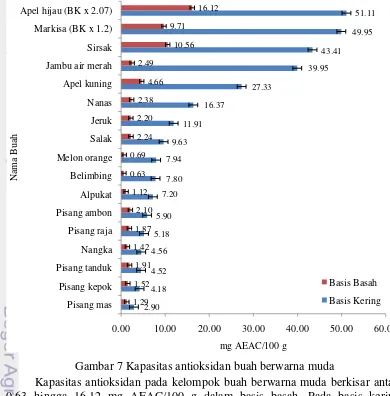
Gambar 7 Kapasitas antioksidan buah berwarna muda
Kapasitas antioksidan pada kelompok buah berwarna muda berkisar antara 0.63 hingga 16.12 mg AEAC/100 g dalam basis basah. Pada basis kering, kapasitas antioksidan berkisar antara 2.90 hingga 105.80 mg AEAC/100 g. Apel hijau memiliki kapasitas antioksidan tertinggi dengan 105.80 mg AEAC/100 g yang berarti setiap 100 g apel hijau memiliki kemampuan antioksidan setara dengan 105.80 mg vitamin C. Pisang mas memiliki kapasitas antioksidan terendah dengan 2.90 mg AEAC/100 g.
2.90
0.00 10.00 20.00 30.00 40.00 50.00 60.00
Pisang mas Apel hijau (BK x 2.07)
12
Tingginya kapasitas antioksidan pada apel hijau dikarenakan kandungan senyawa fitokimianya. Senyawa fitokimia pada apel hijau yang memiliki aktivitas sebagai antioksidan adalah senyawa fenolik, golongan flavonoid, turunan asam sinamat, kumarin, tokoferol dan asam-asam organik polifungsional (Susanto & Setyohadi 2011). Daging buah apel juga mengandung senyawa karotenoid. Karotenoid merupakan kelompok pigmen dan antioksidan alami yang dapat menangkal radikal bebas (Stahl & Sies 2003). Menurut Khoo et al. (2011), senyawa karotenoid yang terkandung pada apel yaitu alfa karoten 0.001-0.03 mg/100 g, beta karoten 0.031-0.072 mg/100g, dan likopen 0.209 mg/100 g. Selain itu kandungan klorofil pada bagian kulit buah dapat berkontribusi terhadap kapasitas antioksidannya, yaitu dengan kandungan klorofil berkisar antara 161.55-234.66 g/g berat kering (Pelayo et al. 2014). Berikut disajikan kapasitas antoksidan pada kelompok buah berwarna tua.
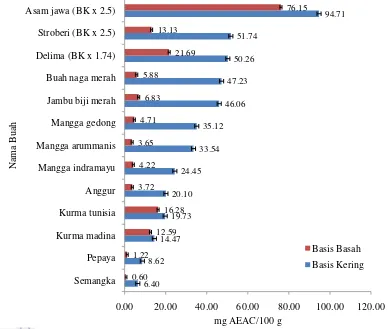
Gambar 8 Kapasitas antioksidan buah berwarna tua
Kapasitas antioksidan pada kelompok buah berwarna tua berkisar antara 0.60 hingga 76.15 mg AEAC/100 g dalam basis basah. Pada basis kering, kapasitas antioksdian berkisar antara 6.40 hingga 236.78 mg AEAC/100 g. Asam jawa memiliki kapasitas tertinggi dengan 236.78 mg AEAC/100 g dan semangka terendah dengan 6.40 mg AEAC/100 g. Kapasitas antioskidan yang tinggi pada asam jawa diduga karena kandungan senyawa yang memiliki aktivitas antioksidan. Senyawa dalam bahan pangan yang memiliki aktivitas antioksidan adalah vitamin A, vitamin C, vitamin E, tanin, mineral, dan asam organik lainnya (Nurjanah et al.
2011).
0.00 20.00 40.00 60.00 80.00 100.00 120.00
13 Menurut penelitian Osawa et al. (1995), bahwa ekstrak asam jawa menunjukkan aktivitas antioksidan. Asam jawa memiliki kandungan fitokimia lain yang termasuk limonene, geraniol (antioksidan alami), safrole (yang merupakan minyak alami juga ditemukan di sassafras), asam sinamat, metil salisilat (esensi tanaman dengan kontra – iritan sifat), pyrazine, dan alkylthiazoles (rasa alami dan wewangian yang berasal dari tanaman dan sayuran). Selain adanya senyawa aktif tersebut, kandungan mineral juga memberikan kontribusi terhadap aktivitas antiokisidan. Mineral akan berperan sebagai komponen antioksidan tubuh (endogen). Salah satunya adalah selenium yang merupakan komponen pentng pembentukkan glutation peroxidase dan seng yang akan membantu mencegah oksidasi lemak serta diperlukan oleh tubuh untuk memproduksi antioksidan superoksida dismutase. Menurut USDA (2009), setiap 100 g asam jawa mengandung 2.8 mg zat besi, 92 mg magnesium, 113 mg fosfor, 0.1 mg seng, dan 1.3 µg.
Kemampuan meredam radikal bebas oleh buah dilakukan oleh metode DPPH. Hasil yang didapatkan menunjukkan berat radikal bebas yang dapat diredam setiap 100 g bahan pangan. Tabel 5 menunjukkan kemampuan meredam radikal bebas berwarna muda.
Tabel 5 Kemampuan meredam radikal bebas buah berwarna muda
Nama Buah Kemampuan Meredam (mg/100 g)
Basis Kering Basis Basah
Apel hijau 2282.83±0.10 347.90±0.10
Markisa 1250.72±0.23 202.61±0.23
Sirsak 846.96±0.13 205.98±0.13
Jambu air merah 760.53±0.13 47.45±0.13
Jeruk 555.92±0.07 102.79±0.07
Apel kuning 551.47±0.14 94.02±0.14
Nanas 384.14±0.05 55.81±0.05
Alpukat 329.12±0.08 51.14±0.08
Salak 215.27±0.13 50.00±0.13
Belimbing 179.03±0.13 14.41±0.13
Melon orange 173.33±0.06 15.04±0.06
Pisang ambon 125.40±0.38 44.58±0.38
Pisang raja 125.10±0.27 45.18±0.27
Nangka 102.46±0.05 32.00±0.05
Pisang tanduk 94.78±0.08 40.09±0.08
Pisang kepok 81.15±0.30 29.57±0.30
Pisang mas 70.02±0.14 31.13±0.14
14
Tabel 6 Kemampuan meredam radikal bebas buah berwarna tua
Nama Buah Kemampuan Meredam (mg/100 g)
Basis Kering Basis Basah
Asam jawa 5020.15±0.09 1614.48±0.09
Stroberi 2978.57±0.01 302.32±0.01
Jambu biji merah 2056.91±0.03 305.03±0.03
Delima 1836.17±0.09 455.36±0.09
Mangga gedong 1653.15±0.17 221.68±0.17
Buah naga merah 988.95±0.32 123.12±0.32
Mangga arummanis 677.15±0.28 73.67±0.28
Mangga indramayu 518.82±0.12 89.49±0.12
Anggur 442.60±0.14 81.88±0.14
Kurma Tunisia 383.84±0.05 316.70±0.05
Pepaya 335.22±0.10 47.43±0.10
Kurma madina 298.01±0.41 259.33±0.41
Semangka 135.22±0.01 12.60±0.01
15
Gambar 9 Kapasitas antioksidan 30 jenis buah
Secara keseluruhan berdasarkan hasil kesetaraan kemampuan dengan vitamin c dan kemampuan meredam, asam jawa memiliki kapasitas antioksidan tertinggi dibandingkan dengan jenis buah lainnya. Asam jawa adalah sejenis buah yang masam rasanya dan biasa digunakan sebagai bumbu dalam banyak masakan Indonesia sebagai perasa atau penambah rasa asam dalam
2.90
0.00 20.00 40.00 60.00 80.00 100.00 120.00
16
makanan, misalnya pada sayur asam (Mun’im et al. 2009). Tingginya kapasitas antioksidan pada asam jawa, tidak sebanding dengan pemanfaatan dan pengolahan buah tersebut selain digunakan sebagai bumbu.
Perbandingan Kapasitas Antioksidan Buah Berwarna Muda dan Tua
Analisis kapasitas antioksidan tidak hanya dilakukan dengan pengelompokkan berdasarkan warnanya, namun juga dilakukan perbandingan antar kelompok tersebut. Kapasitas antioksidan pada pada masing-masing kelompok disajikan pada tabel berikut.
Tabel 7 Kapasitas antioksidan pada kelompok buah berwarna muda dan tua
Kelompok Kemampuan Meredam (mg/100 g)
Basis Kering Basis Basah
Berwarna Muda 478.13 82.92
Berwarna Tua 1332.67 300.24
Tabel 7 menunjukkan bahwa kelompok buah berwarna tua memiliki kapasitas antioksidan lebih tinggi dibandingkan dengan kelompok buah berwarna muda. Hal ini ditunjukkan dengan kemampuan meredam radikal bebas DPPH yang lebih tinggi. Selain itu penelitian pada beberapa jenis beras dengan warna yang berbeda, menunjukkan bahwa beras berwarna lebih gelap seperti beras hitam mengandung antosianin yang lebih tinggi. Tingginya kandungan antosianin inilah yang ikut berperan terkadap kapasitas antioksidan (Suliartini et al. 2011). Menurut Yodmanee et al. (2011), semakin gelap warna suatu pangan menunjukkan semakin tingginya kandungan senyawa fenolik pada pangan tersebut yang dapat mempengaruhi kapasitas antioksidan. Kandungan senyawa fenolik yang terkandung pada pangan merupakan salah satu penentu aktivitas antioksidan. Hubungan yang kuat ditemukan antara pengaruh kandungan total fenol yang terkandung dalam buah pada aktivitas antioksidan secara keseluruhan (Luxomin et al. 2003).
Kandungan Total Fenol
Analisis kandungan total fenol yag dilakukan menggunakan metode Folin-Ciocalteu. Prinsip dari metode ini adalah adanya reaksi oksidasi dan reduksi kolorimetrik untuk mengukur semua senyawa fenolik dalam sampel yang diuji. Selama reaksi belangsung, gugus fenolik-hidroksil bereaksi dengan pereaksi
Folin-Ciocalteu, membentuk kompleks fosfotungstat-fosfomolibdat berwarna biru dengan struktur yang belum diketahui dan dapat dideteksi dengan spektrofotometer. Warna biru yang terbentuk akan semakin pekat setara dengan konsentrasi ion fenolat yang terbentuk, artinya semakin besar konsentrasi senyawa fenolik maka semakin banyak ion fenolat yang akan mereduksi asam heteropoli sehingga warna biru yang dihasilkan semakin pekat (Singleton dan Rossi 1965).
17 Tabel 8 Kandungan total fenol buah berwarna muda
Nama Buah Total Fenol (mg TAE/100g)
Basis Kering Basis Basah
Markisa 20.09±1.70 3.25±1.70
Apel hijau 10.80±0.26 1.64±0.26
Sirsak 7.56±0.38 1.84±0.38
Apel kuning 5.81±0.87 0.99±0.87
Jambu air merah 4.13±0.12 0.25±0.12
Nanas 3.41±0.05 0.49±0.05
Jeruk 2.99±0.15 0.55±0.15
Alpukat 2.86±0.20 0.44±0.20
Nangka 2.33±0.16 0.72±0.16
Belimbing 1.80±0.05 0.14±0.05
Salak 1.46±0.11 0.33±0.11
Pisang ambon 1.09±0.11 0.39±0.11
Pisang tanduk 1.03±0.26 0.43±0.26
Melon orange 1.01±0.12 0.08±0.12
Pisang raja 0.69±0.10 0.25±0.10
Pisang mas 0.59±0.06 0.26±0.06
Pisang kepok 0.34±0.29 0.12±0.29
Kandungan total fenol berkisar antara 0.34 hingga 20.09 mg TAE/100 g dalam basis kering. Pada basis basah menunjukkan kisaran antara 0.12 hingga 3.25 mg TAE/100 g. Markisa memiliki kandungan total fenol tertinggi dibandingkan dengan 16 jenis buah lain yang temasuk dalam kelompok berwarna muda. Pisang kepok memiliki kandungan terendah. Selanjutnya disajikan kandungan total fenol kelompok buah berwarna tua.
Tabel 9 Kandungan total fenol buah berwarna tua
Nama Buah Total Fenol (mg TAE/100g)
Basis Kering Basis Basah
Delima 7.20±0.32 1.78±0.32
Stroberi 4.67±0.29 0.47±0.29
Jambu biji merah 4.34±0.13 0.64±0.13
Buah naga merah 3.63±0.43 0.45±0.43
Kurma Tunisia 3.27±0.37 2.70±0.37
Anggur 2.99±0.19 0.41±0.19
Kurma madina 2.49±0.06 2.16±0.06
Mangga arummanis 2.45±0.03 0.26±0.03
Asam jawa 2.23±0.49 0.71±0.49
Mangga gedong 1.92±0.00 0.25±0.00
Pepaya 1.71±0.17 0.24±0.17
Semangka 1.32±0.34 0.12±0.34
Mangga indramayu 0.43±0.53 0.07±0.53
Kelompok buah berwarna tua memiliki kisaran kandungan total fenol antara 0.43 hingga 7.20 mg TAE/100 g dalam basis kering dan 0.07 hingga 1.78 mg TAE/100 g dalam basis basah. Delima memiliki kandungan total fenol tertinggi dan mangga indramayu terendah.
18
seluruh senyawa yang terkandung oleh bahan pangan tersebut dan tidak spesifik mengukur aktivitas antioksdian dari kandungan senyawa fenoliknya (Kiay et al.
2011).
Korelasi antara Kandungan Total Fenol dengan Kapasitas Antioksidan
Uji korelasi dilakukan untuk mengetahui hubungan antara kandungan total fenol terhadap aktivitas antioksidan. Hasil uji hubungan pearson menunjukkan terdapat hubungan yang signifikan antara kandungan total fenol dengan kapasitas antioksidan (p<0.05) dengan nilai koefisien korelasi 0.545. koefisien korelasi tersebut memiliki arti bahwa 54.5% kapasitas antioksidan pada buah yang dianalisis dipengaruhi oleh kandungan total fenolnya.
Menurut Sandrasari (2009), senyawa fenolik berupa flavonoid yaitu flavonol dan flavon dapat berperan sebagai antioksidan. Aktivitas flavonoid sangat bergantung terhadap jumlah dan lokasi gugus –OH dimana dalam hal ini berperan dalam menetralkan radikal bebas. Kemampuan flavonoid dalam menekan radiikal bebas pun berkaitan dengan kemampuanya mendonorkan elektron. Hal inilah yang menyebabkan hubungan antara kandungan total fenol dengan aktovitas antioksidan. Semakin tinggi nilai total fenol mmakan semakin tingi kemampuan antioksidan dala mendonorkan eletronnya dalam hal menekan perkembangan radikal bebas. Komponen fenolik merupakan senyawa utama dalam peranan antioksidan (Al-Farsi et al. 2007; Zhao et al. 2007).
SIMPULAN DAN SARAN
Simpulan
Pangan yang dianalisis meliputi 30 jenis buah yang terdiri dari 17 buah berwarna muda dan 13 buah berwarna tua. Kapasitas antioksidan tertinggi pada kelompok buah berwarna muda adalah apel hijau dan terendah pada pisang mas. Kapasitas antioksidan tertinggi pada kelompok buah berwarna tua adalah asam jawa dan terendah pada semangka. Secara keseluruhan, asam jawa memiliki kapasitas antioksidan tertinggi diantara 30 jenis buah yang dianalisis. Kandungan total fenol tertinggi pada kelompok buah berwarna muda adalah markisa dan terendah pada pisang kepok. Kandungan total fenol tertinggi pada kelompok buah berwarna tua adalah delima dan terendah pada mangga indramayu. Hasil uji korelasi menunjukkan bahwa terdapat korelasi yang positif antara kandungan total fenol dengan kapasitas antioksidan. Penelitian ini membuktikan bahwa apel hijau dan asam jawa memiliki kapasitas antioksidan yang tinggi.
Saran
19 mendapatkan daftar lengkap terkait kapasitas antioksidan pada seluruh jenis buah yang diperjualbelikan dan dikonsumsi di Indonesia.
DAFTAR PUSTAKA
Al-Farsi M, Alasalvar C, Al-Abid M, Al-Shoaily K, Al-Amry M, Al-Rawahy F. 2007. Compositional and functional characteristics of dates, syrups, and their by-products. Food Chemistry. 104(3): 943-947.
Anwar F, Kalsoom U, Sultana B, Mushtaq M, Mehmood T, Arshad HA. 2013. Effect of drying method and extraction solvent on the total phenolics and antioxidant activity of cauliflower (Brassica oleracea L.) extracts. Inter. Food Research J. 20(2): 653 – 659.
AOAC. 2006. Official Methods of Analysis of The Association of Official Analytical Chemistry. 14th Ed. Virginia : AOC, Inc.
Apak R, Guclu K, Demirata B, Ozyurek, Celik SE, Bektasoglu B, Berker KI, Ozyurt. 2007. Comparative evauation of various total antioxidant capacity assays appled to phenolic compounds with the CUPRAC assays. Review. Molecules.
Ashton OB, Wong M, McGhie TK, Vather R, Wang Y, Requejo-Jackman C, Ramankutty P, Woolf AB.
2006.
Pigments in avocado tissue and oil. J Agric Food Chem. 54(26):10151-8.Balch PA. 2006. Prescription for Nutritional Healing. United States of America (USA): Penguin Grup
Bankole SA, Osho A, Joda AO, Enikuomehin AO. 2005. Effect of drying method on the quality and storability of melon (Cucuimis melo).African Journal of Biotechnology. 4(8):799-803.
[BAPPEDA] Badan Perencanaan Pembangunan Daerah Kota Bogor. 2010. RPJMD Kota Bogor 2010-2014. Bogor: BAPPEDA Kota Bogor.
Boudriesa H, Kefalasa P, Mendez DH. 2007. Carotenoid composition of Algerian date varieties (Phoenix dactylifera) at different edible maturation stages.
Journal of food chem. 101(4):1372–1377.
Cavalcante JMS, Tiago BSS, Anna CAT, Davi A S, Maria F. 2010. Steroidal and phenolic compounds from Sidastrum paniculatum (L.) Frxell and evaluation of cytotoxic and anti-inflammatory activities. Quim. Nova, 33(4): 846-849. Cunha IBS, Alexandra CHF, Caetanob FM, Shimizua MT, Marcucci MC,
Drezzaa FT, Poviaa GS, Carvalhoa PO. 2004. Factors that influence the yield and composition of brazilian propolis extracts. J. Braz Chem Soc.
15(6):964-970.
Divakara. 2009. Variation and character association for various pulp biochemical traits in tamarindus indica l.135(1).
[DKBM] Daftar Komposisi Bahan Makanan. 2007. Jakarta: LIPI.
Dungira SG, Katjaa DG, Kamua VS. 2012. Aktivitas antioksidan ekstrak fenolik dari kulit buah manggis (Garcinia mangostana l.) Jurnal Mipa Unsrat.
20
Eklund PC, langvik KO, Warna JP, Salmi TO, Walfor , rainer ES. 2005. Chemical studies on antiokxiant mechanism and free radical scavenging properties of lignans. Org Biomol Chem. 3:3336-3347.
Fang YZ, Yang S, Wu G. 2002. Free radical, antioxidant and nutrition. Journal of Nutrition. 18:872-879.
Hernani. 2009. Pengaruh pemberian ekstrak daun belimbing wuluh terhadap penurunan tekanan darah pada hewan uji. Jurnal Pascapanen. 24(2):45-51. Julianti E. 2011. Pengaruh tingkat kematangan dan suhu penyimpanan terhadap
mutu buah terong belanda (Cyphomandra betacea). J. Hort. Indonesia
2(1):14-20.
Khoo HE, Prasad KN, Kong KW, Jiang Y, Ismail A. 2011. Carotenoids and their isomers: color pigments in fruits and vegetables. Molecules. 16(2011):1710-1738.
Kiay N, Suryanto E, Mamahit L. 2011. Efek lama perendaman ekstrak kalamansi (Citrus microcarpa) terhadap aktivitas antioksidan tepung pisang goroho (Musa spp.). Chemistry Progress. 4: 27-33.
Kiessoun K, Souza A, Meda NTR, Coulibaly AY, Kiendrebeogo M., Lamien-Meda A, Lamidi M, Millogo-Rasolodimby J, Nacoulma OG. 2010. Polyphenol contents, antioxidant and anti-inflammatory activities of six malvaceae species traditionally used to treat hepatitis b in burkina faso.
European Journal of Scientific Research. 44(4): 570-580.
Kikuzaki H, Hisamoto M., Hirose K., Akiyama K., and Taniguchi H. 2002. Antioxidants properties of ferulic acid and its related compound. J. Agric.Food Chem. 50:2161-2168.
Knee M. 2007. Methods of measuring green colour and chlorophyll content of apple fruit. International Journal of Food Science & Technology. 15(5): 493–500.
Kubo I, Masuda N, Xiao P, Haraguchi H. 2002. Antioxidant activity of deodecyl gallate. J. Agric. Food Chem. 50: 3533-3539 .
Kurniawan J, Widjanarko SB. 2013. Studi kasus analisa proksimat, kandungan kalori, dan aspek keamanan pangan minuman es di sekitar universitas brawijaya. Jurnal Pangan dan Agroindustri. 1(1):56-64.
Lestari R, Ebert G, Keil SH. 2013. Fruit quality changes of salak “pondoh” fruits (Salacca zalacca (gaertn.) Voss) during maturation and ripening. Journal of Food Research. 2(1):204-216.
Luximon-Ramma A, Bahorun T, Crozier A. 2003. Antioxidant actions and phenolic and vitamin C contents of common Mauritian exotic fruits. J Sci Food Agric. 2003(83):496–502.
Malangngi LP, Sangi MS, Paendong JJE. 2012. Penentuan kandungan tanin dan uji aktivitas antioksidan ekstrak biji buah alpukat (Persea americanaMill.).
J. MIPA Unsrat Online. 1(1):5–10.
Molyneux. P. 2004. The use of the stabil free radical diphenylpicrilhydrazyl (DPPH) for estimating antioxidant activity. J Sci Tech 26:211-219.
Mun’im A, Hanani E, Ramnadiah. 200λ. Karakterisasi ekstrak etanolik daun asam
jawa (Tamarindus indica L.). Jurnal Ilmu Kefarmasian. 6(1): 38-44.
21 Osawa T, Sugiyama Y, Inayoshi M, Kawakishi S. 1995. Antioxidant activity of
tetrahydrocurcuminoids. Bioschi Biotechnol Biochem. 59: 1609-1612.
Pelayo RD, Guerrero LG, Mendez DH. 2014. Chlorophyll and carotenoid pigments in the peel and flesh of commercial apple fruits varieties. J of Food Research.
Prakash A. 2001 Antioxidant activity. Medallion Laboratories: Analithycal Progress.19(2):1–4.
Rebecca OPS, Boyce AN, Chandran S. 2010. Pigment identification and antioxidant properties of red dragon fruit (Hylocereus polyrhizus). African Journal of Biotechnology. 9(10):1450-1454.
Sandrasari DA. 2009. Kapasitas Antioksidan dan Hubungannya dengan Nilai Total Fenol Ekstrak Sayuran Indigenous [Tesis]. Bogor (ID): Institut Pertanian Bogor.
Shahwar D, Shafiq-ur-Rehman, Ahmad N, Ullah S, Raza MA. 2010. Antioxidant activities of the selected plants from the family euphorbiaceae, lauraceae, malvaceae and balsaminaceae. African Journal of Biotechnology. 9(7): 1086-1096.
Simhon Z, Judeinstein S, Nadler T, Trainin T, Ya'akov I, Borochov-Neori H, Holland D. 2011. A pomegranate (Punica granatum L.) WD40-repeat gene is a functional homologue of Arabidopsis TTG1 and is involved in the regulation of anthocyanin biosynthesis during pomegranate fruit development.234(5):865-81.
Singh DR, Singh S, Salim KM. 2012. Estimation of phytochemicals and antioxidant activity of underutilized fruits of Andaman Islands (India). Int J Food Sci Nutr. 63(4):446-52.
Singleton VL, Rossi JA. 1965. Colorimetry of total phenolic with phosphomolybdic-phosphotungstic acid reagent, am. J Enol. Vitic.16, 147. Silva FL, Bailo MTE, Alonso JP, Julia C, Gonzalo R, Buelga CS. 2007.
Anthocyanin pigments in strawberry. J. Food Science and Technology.
40(2):374-382.
Stahl W, Sies H. 2003. Antioxidant activity of carotenoids. Molecular Asfects of Medicine. 24:345-351.
Suarni. 2009. Prospek pemanfaatan tepung jagung untuk kue kering (cookies).
Jurnal Litbang Pertanian. 28(2):5-10.
Suliartini NWS, Sadimantara GR, Wijayanto T, Muhidin. 2011. Pengujian kadar antosianin padi gogo beras merah hasil koleksi plasma nutfah Sulawesi Tenggara. Crop Agro. 4(2): 43-48.
Susanto WH, Setyoadi BS. 2011. Pengaruh varietas apel (Malus sylvestris) dan lama fermentasi oleh khamir saccharomyces cerivisiae sebagai perlakuan pra-pengolahan terhadap karakteristik sirup. Jurnal Teknologi Pertanian.
12(3): 135-142.
Uji T. 2007. Keanekaragaman jenis buah-buahan asli Indonesia dan potensinya. J Biodiversitas. 8(2):157-167.
[USDA] United State Departement of Agricultural.2009. USDA National Nutrient Database for Standard Reference – Release 22. Beltsville: Agricultural
Research Service.
22
Wulandari. 2011. Sifat fisik minyak sawit kasar dan korelasinya dengan atribut mutu. Jurnal Teknologi dan Industri Pangan. 22(2):10-18.
Yodmanee S, Karrila TT, Pakdeechanuan P. 2011. Physical, chemical and antioxidant properties of pigmented rice brown in Soutern Thailand.
International Food Research Journal. 18: 901-906.
23
LAMPIRAN
Lampiran 1 Kadar air metode pemanasan langsung (AOAC 2006)
Nama buah Berat cawan Berat sampel Berat akhir % Kadar air
*BB= Basis basah; BK= Basis kering
24
Lampiran 2 Rendemen ekstrak
25 Lampiran 2 Rendemen ekstrak lanjutan
No. Nama Buah Ulangan
Berat sampel kering (g)
Berat ekstrak
(g)
Rendemen Ekstrak
(%)
Rata-rata (%)
25 Apel hijau 1 1.00 0.59 59.20 59.42
2 1.02 0.61 59.64
26 Sirsak 1 1.01 0.39 38.09 42.09
2 1.05 0.49 46.10
27 Markisa 1 1.20 0.30 24.86 44.91
2 1.25 0.81 64.96
28 Kurma madina 1 1.08 0.58 54.00 53.38
2 1.05 0.55 52.76
29 Kurma tunisia 1 1.30 0.74 56.72 60.28
2 1.19 0.76 63.84
30 Buah naga merah 1 1.04 0.42 40.46 37.19
2 1.02 0.35 33.92
Contoh perhitungan:
% Rendemen ekstrak = × 100 % % Rendemen ekstrak buah naga merah (1) = 0.42
1.04 × 100 %
26
Lampiran 3 Analisis kapasitas antioksidan
Kurva Standar Vitamin C
Sampel Basis basah Basis kering
27 Lampiran 3 Analisis kapasitas antioksidan lanjutan
Sampel Basis basah Basis kering
Jambu air merah 20.69 1.29 4 0.506 29.00 2.58 2.49 41.42 39.95 0.13
Aktivitas antioksidan; bFaktor pengenceran
28
Lampiran 4 Analisis kandungan total fenol
Kurva Standar Asam Tanat
Nama Buah
29 Lampiran 4 Analisis kandungan total fenol lanjutan
Sampel
Berat sampel Berat residu
Contoh perhitungan buah naga merah:
Total fenol ekstrak =
Total fenol (basis basah) =total fenol ekstrak x berat residu ekstrak berat sampel (basis basah) x100
=96.60 mg TAE/g x 0.3840 mg
1.0328 g x100
30
Lampiran 5 Aktivitas peredaman radikal bebas DPPH
Kurva aktivitas peredaman radikal bebas DPPH
Pisang kepok Pisang tanduk
Pisang mas
31 Lampiran 5 Aktivitas peredaman radikal bebas DPPH lanjutan
y = 0.103x - 0.923
Belimbing Jambu biji merah
Anggur Mangga arummanis
32
Lampiran 5 Aktivitas peredaman radikal bebas DPPH lanjutan
33 Lanjutan 5 Aktivitas peredaman radikal bebas DPPH lanjutan
y = 0.268x - 0.425
Jambu air merah Semangka
Melon orange Delima
34
Lampiran 5 Aktivitas peredaman radikal bebas DPPH lanjutan
Apel hijau Sirsak
Markisa
Kurma madina
35 Lampiran 6 Rekapitulasi kemampuan meredam radikal bebas DPPH
Sampel
Aktivitas antioksidan; bAscorbic acid antioxidant capacity; cFaktor pengenceran; dStandar deviasi
36
Lampiran 7 Analisis kemampuan meredam radikal bebas DPPH Contoh hasil analisis kapasitas antioksidan buah naga merah
Volume
Absorbansi Kapasitas AO
37 Lampiran 8 Uji korelasi antara kapasitas antioksidan dan kandungan total fenol
Correlations
KandunganTF TransformAO
KandunganTF Pearson Correlation 1 .545**
Sig. (2-tailed) .002
N 30 30
TransformAO Pearson Correlation .545** 1
Sig. (2-tailed) .002
N 30 30
38
Lampiran 9 Pangan yang dianalisis
Pisang kepok Pisang tanduk
Pisang mas Pisang ambon
Pisang raja Salak
Belimbing Jambu biji merah
Anggur Mangga arummanis
Mangga indramayu Mangga gedong
39 Lampiran 9 Pangan yang dianalisis lanjutan
Nanas Pepaya
Stroberi Alpukat
Jambu air merah Semangka
Melon orange Delima
Asam jawa Apel kuning
Apel hijau Sirsak
Markisa Kurma madina
41
RIWAYAT HIDUP
Zahra Musthafavi merupakan anak ketiga dari empat bersaudara dari pasangan Lukito Muhammad dan Hatidjah. Lahir di Jakarta 3 Juli 1992. Penulis menempuh pendidikan di SMP Negeri 30 Jakarta pada tahun 2004- 2007 dan melanjutkan pendidikan di SMA Negeri 52 Jakarta pada tahun 2007-2010. Penulis melanjutkan studi di Institut Pertanian Bogor (IPB) pada tahun 2010 melalui jalur Undangan Seleksi Masuk IPB (USMI).
Selama perkuliahan, penulis aktif di organisasi Himpunan Mahasiswa Ilmu Gizi (HIMAGIZI) 2011-2012 sebagai Bendahara Umum II. Penulis juga aktif mengikuti kegiatan kepanitiaan diantaranya staf divisi Tata Tertib pada Masa Perkenalan Departemen (MPD) 2012, staf divisi Acara pada
Nutrition Fair 2012, staf divisi Konsumsi pada Nutrition Fair 2013, Rakernas Ikatan Sarjana Gizi (ISAGI) I dan Deklarasi ISAGI Jawa Barat, serta pelatihan Beragam, Bergizi, Berimbang, Aman, dan Halal oleh Badan Ketahanan Pangan Jawa Barat. Penulis pernah mengikuti pelatihan Kepemimpinan dan Managemen Mahasiwa yang diadakan oleh Lembaga Kemahasiswaan IPB.