69
Lampiran 1. Deskripsi ubi jalar oranye (Var. Beta 1)
Asal : Hasil persilangan bebas induk betina MSU 01015.
MSU 01015 berasal dari persilangan varietas Kidal dengan BB 97281-16
Tipe tanaman : Menyebar
Umur panen : 4-4,5 bulan
Diameter buku ruas : Tipis Panjang buku ruas : Pendek Warna dominan sulur : Hijau
Warna sekunder sulur : Ungu pada buku-buku Bentuk daun dewasa
- Bentuk kerangka daun : Segitiga sama sisi - Kedalaman cuping daun: Tidak ada
- Jumlah cuping : Bercuping satu - Bentuk cuping pusat : Gerigi
Ukuran daun dewasa : Sedang Warna tulang daun
permukaan bawah : Semua tulang daun berwarna ungu Warna helai daun
- Warna daun dewasa : Hijau
- Warna daun muda : Hijau dengan ungu melingkari tepi daun Pigmentasi dan panjang tangkai daun
- Pigmentasi pada
tangkai daun : Hijau, pangkal dan tangkai ungu - Panjang tangkai daun : Sedang
Bentuk ubi : Elip panjang Susunan pertumbuhan ubi : Menyebar Panjang tangkai ubi : Pendek
Warna kulit ubi : Merah (oranye tua) Warna daging ubi : Oranye tua
- Vitamin C (basis basah): 16,5 mg/100g - Betakaroten
(basis basah) : 12.032 μg/100g Ketahanan terhadap hama/
penyakit : Agak tahan penyakit kudis (Sphaceloma batatas) dan agak tahan hama boleng (Cylas formicarius) Rata-rata hasil : 25,6 ton/Ha
Keterangan lain : Kandungan betakaroten tinggi, rasa enak, cocok
ditanam pada lahan tegalan dan sawah sesudah tanaman padi
Pemulia : M. Jusuf, St. A. Rahayuningsih, Tinuk S. W, Joko Restuono, Gatot Santoso
71
Lampiran 2. Deskripsi ubi jalar kuning (Var. Kalasan)
Asal : Introduksi dari AVRDC Taiwan.
Hasil rata-rata : 40 ton/Ha (31,2-47,5) ton/Ha ubi segar
Umur panen : 65-100 hari
Panjang batang : 75-160 cm
Tipe tumbuh : Kompak, semi tegak
Bentuk daun : Besar, berbentuk hati, kadang-kadang bersirip Warna daun muda : Hijau
Warna daun tua : Hijau
Warna tulang daun : Hijau muda, pangkal tulang daun utama bagian bawah ungu
Warna petiole : Hijau dengan lingkar ungu pada bagian pangkal dan ujung
Warna batang : Hijau muda
Warna kulit ubi : Cokelat muda (kulit sawo) Warna daging ubi : Kuning
Bentuk ubi : Bulat sedikit memanjang
Rasa : Agak manis
Ketahanan terhadap hama : Agak tahan Cylas formicarius Ketahanan terhadap penyakit : Tahan karat daun
Keterangan lain : Cukup baik ditanam di daerah iklim kering
maupun basah dan mampu beradaptasi pada lahan marginal.
Pemulia : Sri Widodo, A. Farid Fadly, Djamaluddin, dan A.
Lampiran 3. Deskripsi ubi jalar madu (Var. Sari)
Asal : Persil, Genjah Rante X Lapis
Daya hasil : 30-35 ton/Ha
Umur panen : 3,5-4 bulan
Tipe tanaman : Semi kompak Diameter buku ruas : Pendek Warna dominan sulur : Hijau
Bentuk kerangka daun : Segitiga samasisi
Kedalam cuping daun : Tepi daun berlekuk dangkal Jumlah cuping daun : Bercuping lima
Bentuk cuping pusat : Lancelatus Ukuran daun dewasa : Kecil
Warna tulang daun : Hijau (bagian bawah)
Warna daun dewasa : Hijau dengan ungu melingkari tepi daun Warna daun muda : Agak ungu
Panjang tangkai daun : Sangat pendek
Bentuk ubi : Bulat telur melebar pada ujung ubi Pertumbuhan ubi : Terbuka
Panjang tangkai ubi : Sangat pendek
Kadar betakaroten : 380,92 μg/100g Kadar vitamin C : 21,52 mg/100g
Ketahanan terhadap hama : Agak tahan boleng (Cylas formicarius) dan tahan hama penggulung daun
Ketahanan terhadap penyakit : Tahan kudis (S. batatas) dan bercak daun (Cercospora sp.)
73
Lampiran 4. Deskripsi ubi jalar ungu (Var. Ayamurasaki)
Asal : MSU 03028
Potensi hasil : 15-20 ton/Ha
Warna kulit : Ungu
Warna daging : Ungu
Tipe pertumbuhan : Menjalar
Bentuk daun : Bercabang-cabang Susunan daun : Tunggal
Bentuk daun : Spiral, helaian dan membundar telur Permukaan daun : Rata
Bentuk cuping : Menjari
Jumlah bunga : Terbatas atau tunggal Bentuk mahkota bunga : Corong
Warna bunga : Putih atau lembayung muda dengan ungu bagian dalam tabungnya
Lampiran 5. Data pengamatan, daftar analisis ragam, dan uji LSR efek utama pengaruh varietas ubi jalar terhadap kadar air ubi jalar.
Data pengamatan kadar air ubi jalar
Perlakuan Ulangan Total Rataan
1 2 3
Ubi Jalar Oranye 71,1314 71,6524 71,8290 214,6128 71,3919 Ubi Jalar Madu 64,2812 63,8824 63,6599 191,8235 64,0817 Ubi Jalar Ungu 55,5731 55,7450 53,5888 164,9069 55,6591 Ubi Jalar Kuning 66,0319 65,2793 65,7158 197,0270 65,6556 Daftar analisis ragam kadar air (%) ubi jalar
SK db JK KT F.hit
75
Lampiran 6. Data pengamatan, daftar analisis ragam, dan uji LSR efek utama pengaruh varietas ubi jalar terhadap kadar pati ubi jalar.
Data pengamatan kadar pati ubi jalar
Perlakuan Ulangan Total Rataan
1 2 3
Ubi Jalar Oranye 31,3949 31,1702 32,4058 94,9709 31,6570 Ubi Jalar Madu 51,6125 48,5798 48,6922 148,8845 49,6282 Ubi Jalar Ungu 37,2355 36,1123 35,7754 109,1232 36,3744 Ubi Jalar Kuning 39,5942 36,7862 36,4493 112,8297 37,6099 Daftar analisis ragam kadar pati (%) ubi jalar
SK db JK KT F.hit
Lampiran 7. Data pengamatan, daftar analisis ragam, dan uji LSR efek utama pengaruh varietas ubi jalar terhadap kadar air tepung ubi jalar.
Data pengamatan kadar air tepung ubi jalar
Perlakuan Ulangan Total Rataan Daftar analisis ragam kadar air (%) tepung ubi jalar
SK db JK KT F.hit
77
Lampiran 8. Data pengamatan, daftar analisis ragam, dan uji LSR efek utama pengaruh varietas ubi jalar terhadap kadar abu tepung ubi jalar.
Data pengamatan kadar abu tepung ubi jalar
Perlakuan Ulangan Total Rataan Daftar analisis ragam kadar abu (%) tepung ubi jalar
SK db JK KT F.hit
Lampiran 9. Data pengamatan, daftar analisis ragam, dan uji LSR efek utama pengaruh varietas ubi jalar terhadap kadar lemak tepung ubi jalar.
Data pengamatan kadar lemak tepung ubi jalar
Perlakuan Ulangan Total Rataan Daftar analisis ragam kadar lemak (%) tepung ubi jalar
SK db JK KT F.hit
79
Lampiran 10. Data pengamatan, daftar analisis ragam, dan uji LSR efek utama pengaruh varietas ubi jalar terhadap kadar protein tepung ubi jalar.
Data pengamatan kadar protein tepung ubi jalar
Perlakuan Ulangan Total Rataan
1 2 3
Ubi Jalar Oranye 4,6200 4,5500 4,2000 13,3700 4,4600 Ubi Jalar Madu 4,6200 3,8500 3,8500 12,3200 4,1100 Ubi Jalar Ungu 3,9900 4.3400 4,0600 12,3900 4,1300 Ubi Jalar Kuning 3,9900 4,7600 4,8300 13,5800 4,5300 Daftar analisis ragam kadar protein (%) tepung ubi jalar
SK db JK KT F.hit
F.tabel
0,05 0,01
Perlakuan 3 0,4259 0,1420 1,1362 tn 4,07 7,59 Galat 8 0,9996 0,1250
Total 11
Keterangan : FK = 222,3963 KK = 4,9180 ** = sangat nyata
Lampiran 11. Data pengamatan, daftar analisis ragam, dan uji LSR efek utama pengaruh varietas ubi jalar terhadap kadar karbohidrat tepung ubi jalar.
Data pengamatan kadar karbohidrat tepung ubi jalar
Perlakuan Ulangan Total Rataan
1 2 3
Ubi Jalar Oranye 83,2555 83,5391 83,4971 250,2918 83,4306 Ubi Jalar Madu 84,9592 86,0002 85,9002 256,8596 85,6199 Ubi Jalar Ungu 84,7032 84,4094 84,6806 253,7932 84,5977 Ubi Jalar Kuning 84,4554 84,9647 84,7007 255,1208 85,0403 Daftar analisis ragam kadar karbohidrat (%) tepung ubi jalar
SK db JK KT F.hit
81
Lampiran 12. Data pengamatan total antosianin (mg/100 g) ekstrak ubi jalar ungu. Data total antosianin tepung ubi jalar (mg/100 g)
Perlakuan Ulangan Total Rataan
1 2 3
Lampiran 13. Data pengamatan dan daftar analisis ragam,pengaruh perlakuan diet folat terhadap berat badan induk mencit.
Dafta
General Linear Model: Berat Badan versus Kelompok; Hari Factor Type Levels Values
Kelompok fixed 4 1; 2; 3; 4 Hari fixed 7 1; 2; 3; 4; 5; 6; 7
Analysis of Variance for Berat Badan, using Adjusted SS for Tests
Sumber db JK KT F. hit F. tabel Unusual Observations for Berat Badan
Obs Berat Badan Fit SE Fit Residual St Residual
83
Uji LSR efek utama pengaruh perlakuan terhadap peningkatan berat badan mencit
LSR Pengaruh
Rataan Notasi
0,05 0,01 perlakuan 0,05 0,01
- - P1 23,95 c B
1,604 2,121 P2 25,67 bc AB
1,688 2,211 P3 26,83 ab AB
Lampiran 15. Uji korelasi hubungan kadar air dan kadar pati ubi jalar dengan kandungan folat dan total antosianin.
Parameter Kadar air Kadar pati
Total
antosianin Kadar folat
Kadar air 1 -0,6056 -0,8755 -0,8755
Kadar pati -0,6056 1 0,2129 0,2129
Total antosianin -0,8755 0,2129 1 1
85
Lampiran 16. Uji korelasi hubungan parameter karakteristik kimia tepung ubi jalar dengan kandungan folat dan total antosianin
Parameter
Kadar air
Kadar abu
Kadar lemak
Kadar protein
Kadar karbohidrat
Total antosianin
Kadar folat Kadar air 1 0,0019 -0,3082 -0,2806 -0,5019 0,8899 0,8899 Kadar abu 0,0019 1 0,8279 0,6005 -0,8578 -0,4538 -0,4538 Kadar
lemak -0,3082 0,8279 1 0,2346 -0,4998 -0,6405 -0,6405 Kadar
protein -0,2806 0,6005 0,2346 1 -0,4628 -0,5415 -0,5415 Kadar
karbohidrat -0,5019 -0,8578 -0,4998 -0,4628 1 -0,0535 -0,0535 Total
Lampiran 17. Hasil analisis kandungan folat
87
Ekstrak ubi orange
89
Lampiran 18. Foto-Foto Penelitian Empat Varietas Umbi Jalar
v
Umbi jalar ungu Umbi jalar oranye
Ubi jalar madu Umbi jalar kuning
Umbi jalar ungu Umbi jalar oranye
Umbi jalar madu Umbi jalar kuning
Tepung Empat Varietas Umbi Jalar
Tepung umbi jalar oranye Tepung umbi jalar madu
Ekstrak empat varietas umbi jalar
Peralatan Pengujian In Vivo Mencit Percobaan
Kandang pemeliharaan Jarum sonde
Timbangan Tempat minum
Perlakuan Pengujian In Vivo Mencit Percobaan
Perlakuan perkawinan Pemberian ekstrak sonde oral
91
Pengamatan Mencit Percobaan Jumlah janin (anakan mencit)
P
3U
4P
4U
4P
4U
5
P
2U
6P
2U
4P
2U
1Ukuran badan janin (anakan mencit)
P
4U
6P
3U
4P
4
U
4P
4U
563
DAFTAR PUSTAKA
Almahdy, A. 2001. Skrining hipokratik, LD 50 serta efek teratogenitas Uncaria gambir roxb. Jurnal Sains dan Teknologi Farmasi. 6(2) : 47-59.
Almatsier, S. 2001. Prinsip Dasar Ilmu Gizi. Gramedia Pustaka Utama, Jakarta.
Anggraeni, Y. P., dan Yuwono, S. S. 2014. Pengaruh fermentasi alami pada chips ubi jalar (Ipomoea batatas) terhadap sifat fisik tepung ubi jalar terfermentasi. Jurnal Pangan dan Agroindustri. 2 (2): 59-69.
Anggorodi. 1979. Ilmu Makanan Ternak Umum. Gramedia Pustaka Utama, Jakarta.
Antarlina, S. S. dan Utomo, J. S. 1999. Proses pembuatan dan penggunaan tepung ubi jalar untuk produk pangan. Balai Penelitian Tanaman Kacang-kacangan dan Umbi-umbian No. 15, Malang.
Antarlina, S. S. 1998. Utilization of sweet potato flour for making cookies and cakes. Research accomplishment of root crops for agricultural development in indonesia. 13-23.
AOAC, 1995. Official Methods of Analysis of The Association of Official Analytical Chemists. AOAC, Washington
Apriyantono, A., Fardiaz , D., Puspitasari, N. L., Soedarnawati, dan Budiyanto. S. 1989. Analisis Pangan. PAU Pangan dan Gizi IPB, Bogor.
Arcot, J. dan Shrestha, A. 2005. Folate : method of analysis. Trend in Food Science and Technology. 253-266.
Arrington, L. R. 1972. Introductory Laboratory Animal Science, The Breeding, Care and Management of Experimental Animal. The Interstate Printers and Publisers, Amerika.
Asgar, A. dan Marpaung, L. 1998. Pengaruh umur panen dan lama penyimpanan terhadap kualitas kentang goreng. Balai Penelitian Tanaman Sayuran.
Astriana. 2014. Pengaruh Obesitas pada Profil Lipid Mencit Hamil dan Berat Badan Anak. Tesis Program Studi Ilmu Fisiologis Biomedis. Universitas Hassanuddin, Makasar. BPOM. 2008. Natural Kos. Editorial. 3(7) : 1-13. Anthocyanin and folic acid content.
Jurnal of Food Science. 64(1) : 37-41.
Claudia, R., Estiasih, T., Ningtyas, D. W., dan Widyastuti. E. 2015. Pengembangan biskuit dari tepung ubi jalar oranye (Ipomea batatas L.) dan tepung jagung (Zae mays) fermentasi. Jurnal Pangan dan Agroindustri. 3(4) : 1589-1595.
de Man, J. M. 1989. Principle of Food Chemistry. The Avi Publishing, Westport. Departemen Kesehatan. 2011. Profil Kesehatan Indonesia, Sumatera Utara.
Departemen Pertanian. 2013. Prospek pengembangan ubi jalar mendukung diversifikasi pangan dan ketahanan pangan 2015].
Dutta, D., Chaudhuri, U. R., dan Chakraborty, R. 2005. Structure, Health Benefits, Antioxidant Property and Processing and Storage of Carotenoids. Jadavpur University, India.
Eisen, E. J. 1974. Result of growth analysis in mice and rats. Journal of Animal Science. 42(1) : 1008-1023.
Enri, N. S. 2010. Efektivias Penggunaan Jenis Asam dalam Proses Ekstraksi Pigmen Antosianin Kulit Manggis (Garcinia Mangostana L.) dengan Penambahan Aseton 60%. Skripsi. Jurusan Teknologi Hasil Pertanian. Universitas Sebelas Maret, Surakarta.
FAO/WHO. 2001. Chapter 12 : Iodine in : human vitamin and mineral requirements. Report of a Joint FAO/WHO Expert Consultation Bangkok, Thailand, Food and Nutrition Division, FAO Rome JP. 181-194.
FAO. 2010. Produktivitas ubi jalar [Diakses pada 3 Maret 2016].
Febrianti, A., Dwiyanti, G., dan Siswaningsih , W. 2014. Pengaruh suhu dan lama pemanasan terhadap aktivitas antioksidan dan total antosianin minuman sari ubi jalar (Ipomea batatas L.). Jurnal Sains dan Teknologi Kimia. 5(2) : 85-95.
Felicia, D., Fredy, F. C., dan Iskandar, W. J. 2010. Suplementasi asam folat sebagai pencegahan preeklamsia pada ibu hamil di Indonesia. Jurnal Ilmiah Mahasiswa Kedokteran Indonesia. 1(1) : 30-35.
Fiqueiredo. J., Grau, M., Sandler, R. Summer, R., dan Bresailer, R. 2009. Folic acid and risk of prostate cancer : result from a randomized clinical trial. Journal of the National Cancer Institute. 101(6) : 432-435.
Gardner, F. P., Perace, R. B. dan Mitchel, R. L. 1999. Fisiologi Tanaman Budidaya. Penerjemah: H. Susilo. UI-Press, Jakarta.
65
Hayati, E., Budi, U., dan Hermawan, R. 2012. Konsentrasi total senyawa antosianin ekstrak kelopak bunga rosella (Hisbiscus sabdariffal) : pengaruh temperatur dan pH. Jurnal Kimia UIN Maulana Malik Ibrahim Malang. 2(1) : 138-147.
Herawati H. dan Widowati, S. 2009. Karakteristik beras mutiara dari ubi jalar (Ipomea batatas). Buletin Teknologi Pertanian. 5(1) : 1-8.
Hofstetter, J. 1991. Analytical methods for vitamins in food/pharma premixes. Roche, USA.
IPB Bogor. 2009. Deskripsi Varietas Unggul Ubi Jalar tahun 1997-2009.
Istiadjid, E. S. M. 2004. Pengaruh defisiensi asam folat terhadap fertilitas induk dan kualitas janin tikus. Jurnal Kedokteran Brawijaya. 20(1).
Iversen, C. K. 1999. Black Currant Nectar: Effect of Processing and Storage on Anthocyanin and Ascorbic Acid Content in Heat Moisture Treatment. Skripsi Universitas Brawijaya, Malang.
Jaya, E. F. P. 2013. Pemanfaatan antioksidan dan betakaroten ubi jalar ungu pada pembuatan minuman non-beralkohol. Media Gizi Mayarakat Indonesia. 2(2) : 54-57.
Karyadi. 1997. Suplemen makanan. http//www.indomedia.com [Diakses pada 20 juli 2009].
Kumalaningsih, S. 2007. Antioksidan Alami Penangkal Radikal Bebas. Trubus Agrisarana, Surabaya.
Kurnia, J. 2008. Tinggalkan tepung impor pilihlah tepung lokal. http://juliuskurnia.com [Diakses pada 17 November 2008].
Leeda, M., Riyati, N. R., Devries, J., Jakobs, C., Geijn, H. V., dan Dekker, G. A. 1998. Effects of folic acid and vitamin B6 supplementation on women with hyperhomocysteinemia and a history of preeklampsia of fetal growth restriction. Am Journal Obstet Gynecol. 179(1) : 135-144.
Leifer, G. 2007. Introduction to Maternity and Pediatary Nursing. Elsivier, Kanada.
Malik, S. 2003. Rekomendasi pengendalian organisme penganggu tumbuhan pada tanaman ubi kayu dan ubi jalar. Direktoriat Perlindungan Tanaman, Jakarta.
Malole, M. B. M. dan Pramono, C. S. U. 1989. Pengantar hewan-hewan percobaan di Laboratorium. Pusat Antara Universitas Bioteknologi IPB, Bogor.
Martini, D., Wulandari, A. L., Sari, I. L., dan Astuti, T. Y. 2013. Khasiat “ si biji manis bertongkol” menjadi susu sebagai alternatif penambahan asam folat selama kehamilan. Seminar Nasional XI Pendidikan Biologi FKIP Universitas Surakarta. 1-4.
Mortensen A. 2006. Carotenoid and other pigmens as natural colorant. Paper Based on a Presentation at the 14. International Symposium on Carotenoid, Edinburg, Scotland.1477-1557.
Murtiningrum, E., Basawer F., Istalaksana, P., dan Jading, A. 2012. Karakteristik umbi dan pati ima kultivar ubi kayu. Jurnal Agroteknologi. 3(1) : 1-10.
Prawirokusumo, S. 1991. Biokimia Nutrisi (Vitamin). BPFE, Yogyakarta.
Purawisastra, S. 2001. Penelitian pengaruh isolat galaktomannan kelapa terhadap penurunan kadar kolesterol serum. http://digilib.ekologi.litbang.depkes.go.id [Diakses pada 12 Januari 2009].
Purnomo, H. 1995. Aktivitas Air dan Perannya dalam Pengawetan Pangan. UI- Press, Jakarta.
Republika. 2006. Kandungan ubi jalar [Diakses pada 2 Maret 2016].
Rismana, E. 2006. Langsing dan sehat lewat limbah perikana [Diakses pada 23 Maret 2016].
Rosidah. 2010. Potensi ubi jalar sebagai bahan baku industri pangan. Tekbunaga. 2(2) : 4-52.
Santoso, W. E. A. dan Estiasih, T. 2014. Kopigmentasi ubi jalar ungu (Ipomea batatas Var. Ayamurasaki) dengan kopigmen Na-kaseinat dan protein whey serta stabilitasnya terhadap pemanasan. Jurnal Pangan dan Agroindustri. 2(4) : 121-127.
Sari, D. P dan Saati, E. A. 2003. Pengujian Efektivitas Penggunaan Jenis Pelarut dan Asam dalam Ekstraksi Pigmen Antosianin Bunga Kanan. Skripsi Universitas Muhammadiyah, Malang.
Silalahi, J. 2006. Makanan Fungsional. Kanisius, Yogyakarta.
Smith, J. B., dan S. Mangkoewidjojo. 1988. Pemeliharaan, Pembiakan dan Penggunaan Hewan Percobaan di Daerah Tropis. Tikus Laboratorium (Rattus norvegicus). UI-Press, Jakarta.
67
Suda, I., Oki, T., Masuda, M., Kobayashi, M., Nishiba, Y., dan Furuta, S. 2003. Review: Physiological functionality of purple-fleshed seet potatoes containing anthocyanins and their utilization in foods. Japan Agricultural Research Quarterly. 37(1) : 167-173.
Sudarmadji, S. 1989. Analisa Bahan Makanan dan Pertanian. Liberti, Yogyakarta.
Sudarmadji, S., Haryono, B., dan Suhardi. 1996. Analisa Bahan Makanan dan Pertanian. Liberti, Yogyakarta.
Susenas. 2001. Badan Pusat Statistik, Jakarta.
Toelihere, M. R. 1979a. Fisiologi Reproduksi pada Ternak. Angkasa, Bandung. Toelihere, M. R. 1979b. Inseminasi Buatan pada Ternak. Angkasa, Bandung.
Ticolu, G. D., Yunianta, dan Maligan J. M. 2016. Pemanfaatan ubi jalar ungu (Ipomea batatas) sebagai minuman berantosianin dengan proses hidrolisis enzimatis. Jurnal Pangan dan Agroindustri. 4(1) : 46-55.
US National Academy of Sciences. 1998. Estimated average requirement and recommended nutrient intake
[Diakses pada 28 Juni 2015].
Warwick, E. J., Astuti, J. M. dan Hardjosubroto, W. 1983. Pemuliaan Ternak. UGM- Press, Yogyakarta.
Widjanarko, S. 2008. Tepung ubi jalar dan komposisi kimianya. http://simonbwidjanarko.com [Diakses pada 20 Juli 2008].
Wikipedia. 2015a. Karbohidrat
[Diakses pada 15 Juli 2015].
Wikipedia. 2015b. Gambar ubi jalar kuning
[Diakses pada 23 Juli 2015].
Wikipedia. 2015c. Gambar ubi jalar madu
[Diakses pada 23 Juli 2015].
Wikipedia. 2015d. Gambar ubi jalar oranye
[Diakses pada 23 Juli 2015].
Wikipedia. 2015e. Gambar ubi jalar ungu
[Diakses pada 23 Juli 2015].
Wilson, G. D. 1973. The Psychology of Conservatism. Academic Press, London. Winarno, F. G. 1982. Kimia Pangan dan Gizi. Gramedia Pustaka Utama, Jakarta. Winarno, F. G. 2002. Kimia Pangan dan Gizi. Gramedia Pustaka Utama, Jakarta.
Winarti, S., Sarofa, U., dan Anggrahini, D. 2008. Ekstraksi dan stabilitas warna ubi jalar ungu (Ipomoea batatas L.) sebagai pewarna alami. Jurnal Teknik Kimia. 3(1) : 207-214.
Yoshimoto. 2001. Antimutagenicity of deacylated anthocyanisin in purple-fleshed sweet potato. Biochemistry. 65(7) : 1652-1655.
23
BAHAN DAN METODA
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan September 2015 - Januari 2016 di Laboratorium Analisa Kimia Bahan Pangan Fakultas Pertanian dan Laboratorium Fisiologi dan Anatomi Hewan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Medan. Pengujian folat dilakukan di Laboratorium Embrio Biotekindo, Bogor.
Bahan Penelitian
Bahan utama yang digunakan dalam penelitian ini adalah empat varietas ubi jalar dengan daging berwarna ungu, oranye, dan kuning tua (ubi madu) yang diperoleh dari petani di Brastagi, Kabupaten Tanah Karo, dan ubi jalar kuning yang diperoleh dari petani di Kecamatan Sei Binge Kabupaten Langkat, Binjai.
Bahan-bahan kimia yang digunakan adalah heksan, H2SO4 pekat, NaOH 50%, HCl
0,02 N, NaOH 0,02 N, alkohol 95%, alkohol 80%, HCl 25%, NaOH 45%, asam 3,5 dinitrosalisilat NaK Tartarat, fenol, Na-metabisulfit, buffer pH 1, buffer pH 4,5 KCl 0,025 M, Na-asetat 0,4 M, CH3COOH 2%, dan metanol. Hewan uji yang digunakan adalah
mencit putih betina berjumlah 24 ekor dan mencit putih jantan berjumlah 8 ekor dengan galur Wistar, umur 3 bulan dengan berat ± 22 g dan sehat.
Alat Penelitian
spatula kaca, erlenmenyer, mikropipet, bulb, tabung sentrifuse, alat sentrifugal dan rotary evaporatory. Pengujian folat menggunakan HPLC IKP/ K-12. Peralatan yang digunakan dalam penelitian pengaruh folat terhadap fertilitas induk dan morfologi janin mencit secara in vivo meliputi kandang pemeliharaan, injeksi oral, tempat minum, botol ekstrak timbangan analitik merk Ohaus dan alat bedah.
Metode Penelitian
Penelitian terdiri dari empat tahap yaitu :
Tahap I : Pembuatan tepung dan pengamatan karakteristik kimia tepung ubi jalar. Tahap II: Pembuatan ekstrak empat varietas ubi jalar
Penelitian tahap I dan tahap II dilakukan dengan menggunakan Rancangan Acak Lengkap (RAL) Non Faktorial dengan perlakuan tunggal berupa varietas ubi jalar (V), yang terdiri 4 taraf, yaitu :
V1 = Ubi jalar oranye
V2 = Ubi jalar madu
V3 = Ubi jalar ungu
V4 = Ubi jalar kuning
Tahap III: Dilakukan analisis folat dan total antosianin.
Tahap IV : Pengujian in vivo pengaruh diet folat terhadap fertilitas induk dan morfologi janin mencit.
25
Jumlah sampel yang digunakan berdasarkan pada rumus Federer (Purawisastra, 2001) sebagai berikut :
(k-1) (n-1) > 15
n = Jumlah sampel dalam tiap kelompok
Pada penelitian ini jumlah sampel untuk tiap kelompok terdiri 6 ekor mencit dengan jumlah kelompok mencit ada 4 sehingga penelitian ini membutuhkan 24 mencit betina dan 8 mencit jantan dari populasi yang ada.
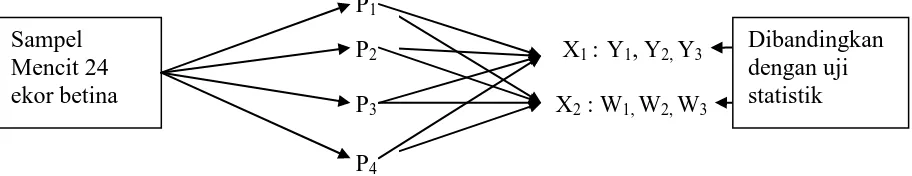
Gambar 7. Desain penelitian pengujian in vivo pengaruh folat terhadap fertilitas induk dan morfologi janin mencit percobaan
P1 = Kelompok kontrol yaitu pemberian akuades selama 28 hari
P2 = Kelompok diet rendah folat : 0,1 ml (5µg) dan 0,2 ml akuades,
X1 = Tingkat fertilitas induk
X2 = Morfologi janin mencit
W1 = Berat badan anakan mencit
W2 = Ukuran badan anakan mencit
W3 = Penampilan fisik
Pengamatan terhadap jumlah anakan mencit, berat badan induk, berat badan anakan, ukuran badan anakan, dan penampilan fisik. Pengamatan dilakukan selama 28 hari.
Model Rancangan
Model rancangan penelitian Rancangan Acak Lengkap (RAL) Non Faktorial adalah sebagai berikut:
Ŷij= µ + αi+ + εij
dimana:
Ŷij : Hasil pengamatan dari faktor V pada taraf ke-i dalam ulangan ke-j µ : Efek nilai tengah
αi : Efek faktor V pada taraf ke-i
εij : Efek galat dari faktor V pada taraf ke-i dalam ulangan ke-j.
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji dilanjutkan dengan uji beda rataan dengan menggunakan uji LSR (Least Significant Range).
Pelaksanaan Penelitian
Penelitian ini dilaksanakan dalam empat tahap yakni seperti berikut :
Penelitian tahap I : Pembuatan tepung ubi jalar dan pengamatan karakteristik kimia tepung ubi jalar
27
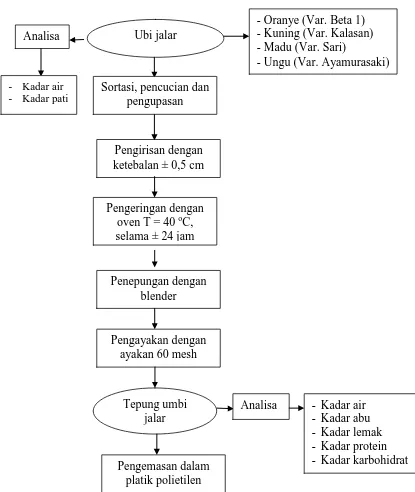
Kemudian dihaluskan dengan blender dan diayak dengan ayakan 60 mesh. Tepung ubi jalar yang dihasilkan dikemas dalam kemasan plastik polietilen. Pembuatan tepung ubi jalar dapat dilihat pada Gambar 8. Tepung ubi jalar yang dihasilkan kemudian dianalisa karakteristik kimia berupa komposisi proksimat yaitu kadar air, kadar abu, kadar lemak, kadar protein, dan kadar karbohidrat.
Penelitian tahap II : Pembuatan ekstrak empat varietas ubi jalar
Tepung ubi jalar dari empat varietas ditimbang sebanyak 5 g dan dimasukkan ke dalam erlenmeyer 500 ml, ditambahkan 300 ml CH3COOH 2% kemudian dipanaskan
pada suhu 95-100 oC pada penangas air selama 20 menit. Setelah itu dilakukan sonifikasi selama 5 menit dan didinginkan, kemudian dipindahkan secara kuantitatif ke dalam labu takar 500 ml, ditambahkan 125 ml metanol, dan dihimpitkan dengan CH3COOH 2%
hingga batas tera. Suspensi yang dihasilkan selanjutnya di sentrifuse dan kemudian dievaporasi dengan rotary evaporator selama 4 jam sehingga diperoleh ekstrak ubi jalar. Pembuatan ekstrak ubi jalar dapat dilihat pada Gambar 9.
Penelitian tahap III : Dilakukan analisis folat dan total antosianin pada ekstrak ubi jalar
Pada tahap ini ekstrak ubi jalar yang dihasilkan, kemudian dianalisis kandungan folat dengan HPLC IKP/ K-12 dan dilakukan analisis total antosianin untuk mengetahui hubungan pigmen antosianin dengan kandungan folat.
Pengamatan dan Parameter Penelitian Kadar air (AOAC, 1995)
sampai dingin kemudian ditimbang. Pemanasan dan pendinginan dilakukan berulang sampai diperoleh berat sampel konstan. Kadar air dihitung berdasarkan formula sebagai berikut.
Kadar Air = Berat awal – Berat akhir Berat awal
x 100%
Kadar abu (SNI-01-3451-1994)
Sampel sejumlah 5 g dimasukkan ke dalam cawan porselen kering yang telah diketahui beratnya (yang terlebih dulu dikeringkan dalam oven dan didinginkan dalam desikator). Kemudian sampel dipijarkan diatas kompor listrik kira-kira 1 jam sampai sampel berbentuk arang. Kemudian cawan porselen yang berisi arang dimasukkan ke dalam tanur dengan suhu 500 – 600 oC sampai terbentuk abu. Cawan porselen didinginkan kemudian dikeluarkan dari tanur dan dimasukkan ke dalam desikator selam 15 menit kemudian ditimbang beratnya. Kadar abu dihitung dengan formula sebagai berikut.
Kadar abu = Bobot akhir (g) Bobot awal (g)
x 100 %
Kadar lemak (AOAC, 1995)
29
Kadar lemak = Bobot lemak (g) Bobot sampel (g)
x 100%
Kadar protein (Metode KjeIdahl, AOAC, 1995).
Sampel sebanyak 0,2 g dimasukkan ke dalam labu kjedahl 30 ml selanjutnya ditambahkan dengan 2,5 ml H2SO4 pekat, 1 g campuran katalis selenium dan batu didih.
Kemudian sampel dipanaskan pada suhu 350 oC selama 3-4 jam atau sampai cairan berwarna putih. Labu beserta isinya didinginkan lalu isinya dipindahkan ke dalam alat destilasi dan ditambahkan larutan NaOH 40%, kemudian dibilas dengan air suling. Labu erlenmeyer berisi asam borat (H3BO3) 10 ml diletakkan di bawah kondensor, sebelum
ditambahkan ke dalamnya 2-4 tetes indikator conway. Ujung tabung kondensor harus terendam dalam labu larutan asam borat, kemudian dilakukan destilasi hingga sekitar 125 ml destilat dan ditampung di dalam erlenmeyer lalu dititrasi dengan HCl 0,05 N sampai terjadi perubahan warna hijau menjadi merah muda. Kadar protein dihitungan dengan formula sebagai berikut.
A = ml NaOH untuk tittrasi blanko B = ml NaOH untuk titrasi sampel N = Normalitas HCl
Kadar karbohidrat (by difference).
Kadar pati (Hidrolisis asam, Apriyantono dkk., 1989).
Sampel sebanyak 2-5 g yang telah dihaluskan dimasukkan ke dalam beaker glass 250 ml, selanjutnya ditambahkan 50 ml alkohol 80% dan diaduk selama 1 jam. Suspensi tersebut disaring dengan kertas saring dan dicuci dengan air sampai volume filtrat 250 ml. Filtrat ini mengandung karbohidrat yang terlarut dan dibuang. Residu pati yang terdapat pada kertas saring dicuci sebanyak 5 kali dengan 10 ml eter. Dibiarkan eter menguap dari residu, kemudian cuci kembali dengan 150 ml alkohol 10% untuk membebaskan lebih lanjut karbohidrat yang terlarut. Residu dipindahkan dari kertas saring ke dalam erlenmeyer dengan cara pencucian dengan 200 ml air dan ditambahkan 20 ml HCl 25%. Kemudian ditutup dengan penangas balik dan dipanaskan diatas penangas air sampai mendidih selama 2,5 jam pada suhu 100 oC. Dibiarkan dingin dan dinetralkan dengan larutan NaOH 45% dan diencerkan sampai volume 500 ml sampai ± pH 7. Disaring kembali campuran diatas pada kertas saring, setelah itu ditentukan kadar gula yang dinyatakan sebagai glukosa dari filtrat yang diperoleh. Kadar pati dihitung dengan formula sebagai berikut.
Faktor pengenceran x Kadar gula pereduksi (mg/ml) x 100 % x 0,9 Kadar pati =
Bobot sampel (g)
Total antosianin (Ticolu dkk., 2016).
Persiapan larutan sampel (Winarti, dkk., 2008).
Sebanyak 10 g tepung ubi jalar di timbang dengan teliti kedalam erlenmeyer 100 ml. Ditambahkan 3,2 ml etanol, 0,6 ml CH3COOH, dan 16,1 ml air, dan di diamkan
31
Pembuatan buffer pH 1
Untuk membuat buffer pH 1 digunakan KCl sebanyak 1,86 g dicampur dengan 980 ml akuades dan diatur hingga mencapai pH 1 dengan menggunakan HCl pekat. Selanjutnya larutan dipindahkan ke dalam labu ukur 1 L dan ditambahkan akuades sampai tanda batas.
Pembuatan buffer pH 4,5
Untuk buffer pH 4,50 digunakan CH3CO2Na. 3H2O sebanyak 54,43 g dicampur
dengan 950 ml akuades. Kemudian pH diukur dan diatur dengan HCl pekat hingga diperoleh larutan dengan pH 4,5. Selanjutnya larutan dipindahkan ke dalam labu ukur 1000 ml dan diencerkan dengan akuades sampai volume mencapai 1000 ml.
Pengukuran dan perhitungan konsentrasi antosianin total
Faktor pengenceran yang tepat untuk sampel harus ditentukan terlebih dahulu dengan cara melarutkan sampel dengan larutan penyangga KCl pH 1 hingga diperoleh absorbansi kurang dari 1,20 pada panjang gelombang 530 nm. Selanjutnya diukur absorbansi akuades pada panjang gelombang yang akan digunakan (530 dan 700 nm) untuk mencari titik nol. Panjang gelombang 530 adalah panjang gelombang maksimum untuk sianidin-3-glukosida, sedangkan panjang gelombang 700 nm untuk mengoreksi endapan yang masih terdapat pada sampel. Jika sampel benar-benar jernih maka absorbansi pada 700 nm adalah 0.
sebagai blanko. Absorbansi (A) dari sampel yang telah di larutkan ditentukan dengan rumus :
A = (A530-A700)pH 1 – (A530-A700)pH 4,5
Kandungan pigmen antosianin pada sampel dihitung dengan rumus : Total antosianin =
(mg/100 g) ε x L
A x BM x FP x 1000
Keterangan :
A = Absorbansi
BM = Berat molekul = 449,20 (sianidin-3-glikosida) FP = Faktor pengencer
ε = Koefisien absorbsivitas molar = 26900 (sianidin-3-glikosida)
Pengujian Folat (Hofstetter, 1991) Persiapan larutan standar
Standar ditimbang dengan teliti sebanyak 1 g ke dalam labu takar 100 ml dan ditambahkan sebanyak 60 ml CH3COOH 2% dan metanol sebanyak 25 ml.
Kemudian dihimpitkan dengan CH3COOH 2%, dikocok sampai homogen. Diambil larutan
standar dengan menggunakan siring, lalu dipasang siring dengan disk filter 0,45. Kemudian dilarutkan filtrat siap untuk diinjeksikan pada HPLC.
Persiapan larutan sampel
Sebanyak 1-2 g sampel di timbang dengan teliti dan dimasukkan ke dalam erlenmeyer 100 ml. Ditambahkan 60 ml CH3COOH 2%, dipanaskan pada suhu 95-100 oC
33
terjadi pemisahan dengann cairan jernihnya. Larutan sampel diambil dengan menggunakan siring dan dipasang siring dengan disk filter 0,45 mm dan larutan filtrat siap untuk dinjeksikan pada HPLC.
Analisis sampel dengan HPLC
Dilakukan warm up HPLC selama 30-45 menit sampai kondisi baseline stabil terhadap fase gerak yang akan digunakan. Disuntikan larutan standar pada HPLC, lalu suntikan larutan sampel pada HPLC. Dilakukan bilas injektor valve dengan akuades minimal 3 kali menggunakan siring plastik 10 ml. Kemudian bilas HPLC dengan menggunakan akuades dan metanol masing-masing selama 30 menit.
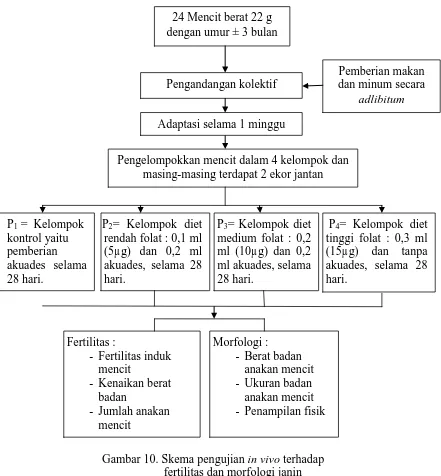
Penelitian tahap IV : Pengujian in vivo pengaruh diet folat terhadap fertilitas induk dan morfologi janin mencit percobaan
Sebanyak 24 mencit betina galur wistar dibagi menjadi 4 kelompok, setiap kelompok terdiri dari 6 mencit betina dengan 2 mencit jantan. Kelompok I adalah kelompok kontrol hanya diberikan akuades, kelompok II adalah diet rendah folat (0,1 ml = 5 μg), kelompok III adalah diet medium folat (0,2 ml = 10 μg), dan kelompok IV adalah
diet tinggi folat (0,3 ml = 15 μg). Pemberian diet masing-masing kelompok dilakukan selama 28 hari. Mencit setelah diberikan diet selama 7 hari selanjutnya dikawinkan dan ditunggu sampai kebuntingan.
Pengamatan dan Parameter Penelitian Dosis dan jumlah ekstrak yang diberikan
Ekstrak ubi jalar yang digunakan adalah ekstrak dengan konsentrasi folat yang tertinggi. Diet folat yang diberikan sesuai dengan literatur Istiadjid (2004) yaitu diet rendah folat (5μg), diet medium folat (10 μg), dan diet tinggi folat (15μg). Total ekstrak yang
Berdasarkan hasil analisis kandungan folat pada ekstrak ubi jalar ungu adalah 9,44 mg/kg bahan sehingga untuk mendapatkan dosis 5 µg folat dalam 0,1 ml ekstrak, dilakukan pengenceran terhadap ekstrak sebagai berikut :
Berat total ekstrak = 1000 g
Dosis folat yang diberikan 5 µg/0,1 ml = 0,05 mg/ml Banyak akuades yang ditambahkan adalah sebagai berikut : 9,44 mg =
Berdasarkan hasil perhitungan konsentrasi ekstrak 0,05 mg/ml, maka ke dalam 1000 g ekstrak ubi jalar ungu ditambahkan 188,8 ml akuades. Volume ekstrak yang diberikan ke mencit untuk mendapatkan dosis sesuai dengan perlakuan dapat dilihat pada Tabel 8. Tabel 8. Volume ekstrak folat yang diberikan pada mencit untuk diet rendah, medium, dan
tinggi folat.
Diet folat Volume ekstrak yang diberi ke mencit (ml/ ekor mencit)
Mencit betina galur wistar yang digunakan dalam penelitian ini sebanyak 28 ekor dan 8 ekor jantan yang diadaptasikan selama kurang lebih satu minggu terhadap makanan dan lingkungan.
Persiapan kandang
35
Pemberian pakan
Jenis ransum yang diberikan yaitu pelet yang dibeli dari P.T. Charoen Pokhphan Medan. Pemberian diet folat ubi jalar yang dilakukan selama 28 hari. Makanan dan minuman yang diberikan secara adlibitum.
Fertilitas induk mencit
Dilakukan pengamatan terhadap fertilitas induk berdasarkan kecepatan terjadinya kebuntingan. Pengamatan dilakukan dengan penimbangan berat badan dan pengamatan secara visual terhadap induk mencit setelah dikawinkan setiap 3 hari sekali selama 21 hari. Mencit ditimbang dengan timbangan merk Ohaus. Terjadinya kebuntingan ditandai adanya peningkatan berat badan. Ciri-ciri mencit hamil dapat diketahui secara visual adalah perut terlihat membesar dan buncit, putting susu mencit terlihat sangat menonjol, dan tidak terlalu banyak bergerak atau keaktifan mencit berkurang seperti sebelum hamil (Astriana, 2014).
Berat badan induk mencit
Pengamatan dilakukan terhadap berat badan induk mencit dilakukan dengan penimbangan berat badan induk mencit setiap 3 hari selama 21 hari setelah dikawinkan. Penimbangan dengan timbangan analitik merk Ohaus dengan ketelitian dua angka. Tujuan penimbangan berat badan induk untuk mengetahui terjadinya kebuntingan.
Jumlah anakan mencit
Berat badan anakan mencit
Pengamatan terhadap berat badan anakan mencit dilakukan setelah pembedahan secara histerotomi dengan menggunakan alat bedah pada usia kebuntingan mencapai 21 hari, kemudian dilakukan penimbangan berat badan anakan menggunakan timbangan analitik merk Ohaus dengan ketelitian dua angka.
Ukuran badan anakan mencit
Pengamatan terhadap berat badan anakan mencit dilakukan setelah pembedahan secara histerotomi dengan menggunakan alat bedah pada usia kebuntingan mencapai 21 hari, kemudian dilakukan pengukuran panjang anakan dengan meletakkan anakan pada kertas millimeter. Setiap kotak pada kertas millimeter berukuran 1 mm.
Penampakkan fisik anakan mencit
37
- Kadar folat - Total antosianin
(Umbi ungu) Analisa
Penambahan CH3COOH 2%
3000 ml
Pemanasan T = 95-100 oC selama 20 menit
Sonifikasi selama 5 menit
Pemindahan secara kuantitatif pada labu takar 5000 ml
Sentrifugasi 4500 rpm
Evaporasi dengan rotary evaporator
Ekstrak ubi jalar
Gambar 9. Skema pembuatan ekstrak ubi jalar 1000 g tepung ubi
jalar
- Oranye (Var. Beta 1) - Kuning (Var. Kalasan) - Madu (Var. Sari)
- Ungu (Var. Ayamurasaki)
Pendinginan
39
Pengelompokkan mencit dalam 4 kelompok dan masing-masing terdapat 2 ekor jantan
Karakteristik Kimia dari Empat Varietas Ubi Jalar
Dari hasil penelitian yang dilakukan terhadap empat varietas ubi jalar menunjukkan perbedaan kandungan kadar air, dan kadar pati. Karakteristik kimia dari empat varietas dapat dilihat pada Tabel 9.
Tabel 9. Pengaruh varietas ubi jalar terhadap karakteristik kimia ubi jalar
Jenis ubi jalar Parameter
Kadar air (%) Kadar pati (%)
Oranye 71,3919 ± 0,3627a,A 31,6570 ± 0,6581c,C
Madu 64,0817 ± 0,3147c,C 49,6282 ± 1,7194a,A
Ungu 55,6591 ± 1,1984d,D 36,3744 ± 0,7646b,B
Kuning 65,6556 ± 0,3779b,B 37,6099 ± 1,7267b,B
Keterangan : - Angka yang diikuti huruf yang berbeda dalam baris yang sama menunjukkan berbeda nyata pada taraf 5% dan dengan huruf besar yang berbeda sangat nyata pada taraf 1% dengan uji LSR.
- Data terdiri dari 3 ulangan ± Standar deviasi
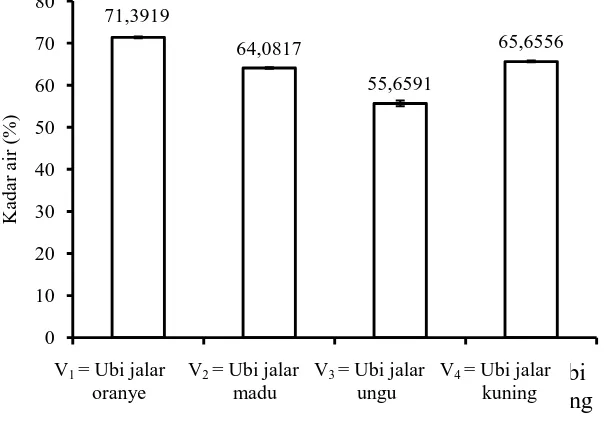
Kadar air
41
dengan kadar antosianin dan kadar folat ubi jalar. Semakin tinggi kadar air maka total antosianin dan folat semakin rendah.
Gambar 11. Kadar air dari empat varietas ubi jalar
Kadar pati
Dari daftar analisis sidik ragam (Lampiran 6) dapat dilihat bahwa keempat varietas ubi jalar memiliki kadar pati yang berbeda sangat nyata (P<0,01). Kadar pati dari empat varietas ubi jalar dapat dilihat pada Gambar 12. Nilai kadar pati tertinggi terdapat pada ubi jalar madu sebesar 49,6282% dan terendah pada ubi jalar oranye sebesar 31,6570%. Perbedaan varietas, lokasi, dan musim tanam dapat menyebabkan perbedaan komposisi kimia pada varietas ubi jalar (Herawati dan Widowati, 2009). Kandungan pati di dalam bahan baku dipengaruhi oleh umur tanaman dan lama penyimpanan setelah panen (Anggraeni dan Yuwono, 2014). Menurut Antarlina dan Utomo (1999) kandungan pati pada ubi jalar sangat ditentukan oleh umur panen dan adanya penyimpanan. Pada (Lampiran 15) menunjukkan adanya korelasi nyata (bernilai negatif) kadar pati dengan kadar air. Semakin tinggi kadar pati maka kadar air semakin rendah.
Gambar 12. Kadar pati dari empat varietas ubi jalar Karakteristik Kimia dari Tepung Empat Varietas Ubi Jalar
Tabel 10 menunjukkan karakteristik kimia dari tepung empat varietas ubi jalar (oranye, madu, ungu, dan kuning) berdasarkan kadar air, kadar abu, kadar lemak, kadar protein, dan kadar karbohidrat.
Tabel 10. Pengaruh varietas ubi jalar terhadap karakteristik kimia tepung ubi jalar Parameter Tepung ubi
Keterangan : - Angka yang diikuti huruf yang berbeda dalam baris yang sama menunjukkan berbeda nyata pada taraf 5% dan dengan huruf besar yang berbeda sangat nyata pada taraf 1% dengan uji LSR.
- Angka yang tidak diikuti huruf menunjukkan berbeda tidak nyata - Data terdiri dari 3 ulangan ± Standar deviasi
43
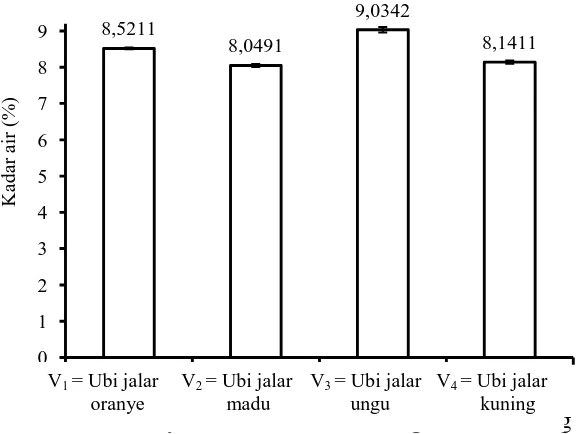
Kadar air
Gambar 13. Kadar air tepung dari empat varietas ubi jalar
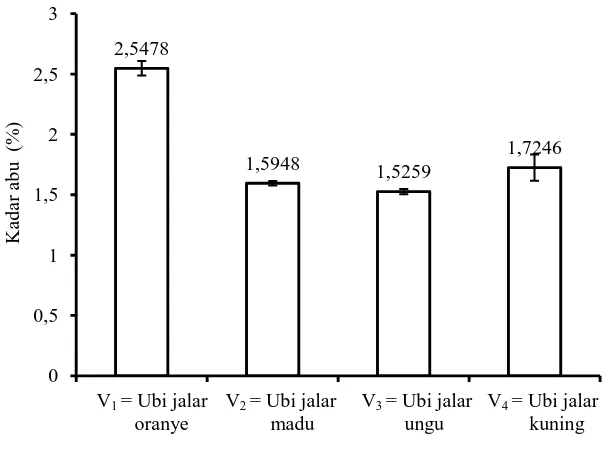
Kadar abu
Berdasarkan analisis sidik ragam (Lampiran 8) dapat dilihat bahwa varietas tepung ubi jalar memiliki kadar abu yang berbeda sangat nyata (P<0,01). Kadar abu tepung dari empat varietas ubi jalar dapat dilihat pada Gambar 14. Kadar abu tertinggi terdapat pada tepung ubi jalar oranye sebesar 2,5478% dan terendah pada tepung ubi jalar ungu sebesar 1,5259%. Perbedaan kadar abu pada masing-masing tepung ubi jalar disebabkan adanya kandungan mineral yang berbeda pada masing-masing ubi jalar (Sudarmadji, dkk., 1996). Selain itu tahapan proses pembuatan tepung seperti pencucian merupakan salah satu faktor berkurangnya kadar abu pada tepung ubi jalar, karena adanya mineral yang larut akibat proses pencucian. Proses pencucian dan perendaman secara berulang-ulang dapat menyebabkan tercuci mineral yang terkandung didalam suatu bahan (de Man, 1989). Kadar abu maksimal pada tepung ubi jalar sebesar 2,58%. Oleh karena itu kandungan abu pada tepung ubi jalar menunjukkan jumlah yang cukup baik untuk penyimpanan
45
(Widjanarko, 2008). Pada (Lampiran 16) menunjukkan adanya korelasi sangat nyata (bernilai positif) kadar abu dengan kadar lemak. Semakin tinggi kadar abu maka kadar lemak semakin tinggi. Kadar abu menunjukkan korelasi nyata (bernilai positif) terhadap kadar protein. Semakin tinggi kadar abu maka kadar protein semakin tinggi. Kadar abu menunjukkan korelasi sangat nyata (benilai negatif) dengan kadar karbohidrat. Semakin tinggi kadar abu maka kadar karbohidrat semakin rendah.
Gambar 14. Kadar abu tepung dari empat varietas ubi jalar
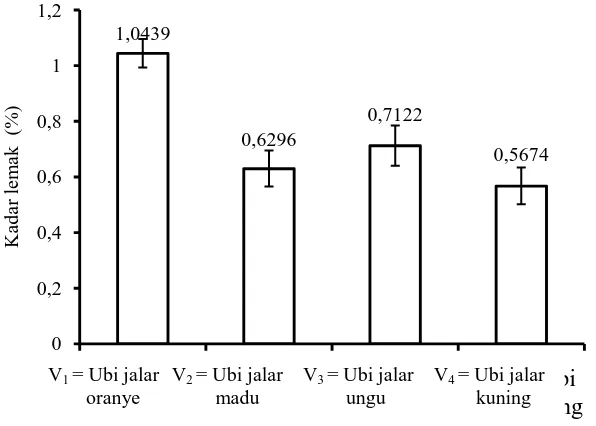
Kadar lemak
Dari daftar analisis ragam (Lampiran 9) dapat dilihat bahwa varietas ubi jalar yang berbeda memiliki nilai kadar lemak yang berbeda sangat nyata (P<0,01). Kadar lemak tepung dari empat varietas ubi jalar dapat dilihat pada Gambar 15. Kadar lemak tertinggi terdapat pada tepung ubi jalar oranye sebesar 1,0439% dan terendah pada tepung ubi jalar kuning sebesar 0,5674%. Perbedaan varietas, lokasi dan musim tanam dapat menyebabkan perbedaan komposisi kimia pada varietas ubi jalar (Herawati dan Widowati, 2009). Kandungan lemak pada ubi jalar dipengaruhi adanya pigmen yang mengikat lemak.
Menurut Dutta, dkk. (2005) betakaroten merupakan pigmen yang bersifat lipofilik yang larut dalam lemak sehingga adanya pigmen ini dapat melindungi lemak yang terdapat pada ubi jalar. Pigmen betakaroten bersifat sebagai antioksidan yang terbukti dapat mencegah proses oksidasi lemak. Hal inilah yang menyebabkan kandungan lemak tertinggi terletak pada ubi jalar oranye (Silalahi, 2006). Pada (Lampiran 16) menunjukkan adanya korelasi sangat nyata (bernilai positif) kadar lemak dengan kadar abu. Semakin tinggi kadar lemak maka kadar abu semakin tinggi. Kadar lemak menunjukkan korelasi nyata (bernilai negatif) terhadap kadar antosianin dan folat. Semakin tinggi kadar lemak maka kandungan antosianin dan folat semakin rendah.
Gambar 15. Kadar lemak tepung dari empat varietas ubi jalar
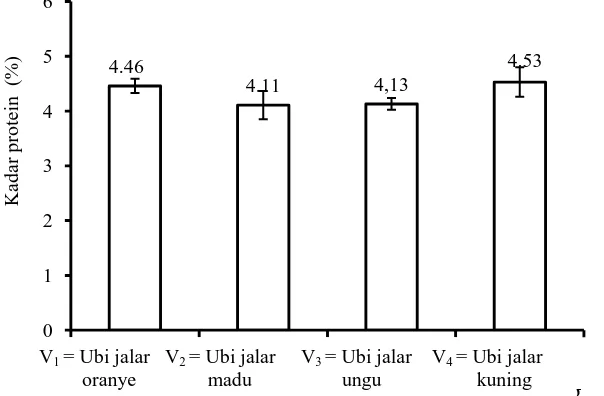
Kadar protein
Dari daftar analisis ragam (Lampiran 10) dapat dilihat bahwa varietas ubi jalar yang berbeda memberikan pengaruh yang berbeda tidak nyata (P>0,05). Kadar protein tepung dari empat varietas ubi jalar dapat dilihat pada Gambar 16. Perbedaan kandungan protein tepung sangat dipengaruhi oleh proses pengolahannya. Proses pengeringan dapat
47
menyebabkan kandungan protein menjadi berkurang karena protein sangat mudah rusak akibat reaksi Maillard pada suhu 30-35 oC (de Man, 1989). Pada (Lampiran 16) menunjukkan adanya korelasi nyata (bernilai positif) kadar protein dengan kadar abu. Semakin tinggi kadar protein maka kadar abu semakin tinggi. Kadar protein menunjukkan korelasi nyata (bernilai positif) terhadap kadar antosianin dan folat. Semakin tinggi kadar protein maka kandungan antosianin dan folat semakin tinggi.
Gambar 16. Kadar protein tepung dari empat varietas ubi jalar
Kadar karbohidrat
Dari daftar analisis ragam (Lampiran 11) dapat dilihat bahwa varietas ubi jalar yang berbeda memiliki kandungan karbohidrat berbeda sangat nyata (P<0,01). Kadar karbohidrat tepung dari empat varietas ubi jalar dapat dilihat pada Gambar 17. Kadar karbohidrat tertinggi terdapat pada tepung ubi jalar madu sebesar 85,6199% dan terendah pada tepung ubi jalar oranye sebesar 83,4306%. Perbedaan pada masing-masing jenis ubi jalar disebabkan faktor eksternal seperti kegiatan pascapanen, umur panen, dan lingkungan panen. Menurut Widjanarko (2008) kandungan karbohidrat pada ubi jalar sangat dipengaruhi oleh perbedaan umur panen dan lingkungan tumbuhnya. Kandungan
karbohidrat pada ubi jalar bergantung pada varietas dan umur panennya (Kurnia, 2008). Pada (Lampiran 16) menunjukkan adanya korelasi nyata (bernilai negatif) kadar karbohidrat dengan kadar air. Semakin tinggi kadar karbohidrat maka kadar air semakin rendah.
Gambar 17. Kadar karbohidrat tepung dari empat varietas ubi jalar Kandungan Folat dari Ekstrak Empat Varietas Ubi Jalar
Tabel 11. menunjukkan jumlah kandungan folat dari ekstrak empat varietas ubi jalar yaitu oranye, madu, ungu dan kuning. Berdasarkan hasil penelitian yang diperoleh diketahui bahwa folat dapat dideteksi hanya pada ekstrak ubi jalar ungu.
Tabel 11. Pengaruh varietas ubi jalar terhadap kandungan folat dari ekstrak empat varietas ubi jalar
Keterangan : ND (Tidak terdeteksi)
LoD (Batas terdeteksi = 0,06 mg/kg)
49
Ekstrak ubi jalar ungu memiliki kandungan folat sebesar 9,44 mg/kg, sedangkan pada tiga jenis ekstrak ubi jalar lainnya tidak terdeteksi kandungan folat, disebabkan batas minimum kapasitas HPLC sebesar 0,06 mg/kg. Menurut Jaya (2013) kelebihan dari ubi jalar adalah kandungan folat yang cukup bermakna. Kandungan folat dominan pada ekstrak ubi jalar ungu sangat sesuai dengan Republika (2006) salah satu jenis ubi jalar yang mengandung folat adalah varietas ubi jalar ungu memiliki kandungan serat, karbohidrat kompleks, vitamin B6, dan asam folat. Hasil pengamatan terhadap komposisi ubi jalar dan tepung ubi
jalar pada Tabel 9 dan Tabel 10 menunjukkan terdapat hubungan antara kandungan kadar air, kadar pati, dan kadar karbohidrat dengan kandungan folat. Pada (Lampiran 16) menunjukkan adanya korelasi sangat nyata (bernilai positif) folat dengan kadar air. Semakin tinggi folat maka kadar air semakin tinggi. Folat menunjukkan korelasi nyata (bernilai negatif) terhadap kadar lemak dan protein. Semakin tinggi folat maka kadar lemak dan protein semakin rendah.
Hubungan kadar air dengan kandungan folat pada umbi jalar, semakin tinggi kadar air maka kandungan folat akan sedikit. Hal ini disebabkan sifat folat yang mudah rusak oleh oksigen yang dapat menyebabkan proses respirasi dan transpirasi lebih cepat dan adanya suhu dapat menyebabkan penguapan air sehingga terjadi pengurangan kadar air dan folat. Menurut Wikipedia (2016e) folat sangat sensitif terhadap cahaya, oksigen, dan suhu. Folat yang terdapat dalam bahan dalam bentuk tereduksi dengan sifat yang labil sehingga sangat mudah hilang dan rusak (Almatsier, 2001). Oleh karena itu kadar air terendah terdapat pada umbi jalar ungu yang menunjukkan kandungan folat yang tinggi.
Menurut Murtiningrum, dkk. (2012) pati dengan jumlah fraksi terlarut lebih banyak memiliki ukuran granula pati yang besar dan memiliki suhu gelatinisasi yang tinggi sehingga lebih tahan terhadap proses pemanasan.
Total Antosianin
Pada (Lampiran 12) menunjukkan bahwa kandungan pigmen antosianin yang terdapat pada ekstrak ubi jalar ungu sebesar 877,0811 mg/100 g. Menurut Kumalaningsih (2007) pigmen antosianin yang berasal dari ubi jalar memiliki stabilitas yang tinggi dibandingkan dengan sumber antosianin lainnya. Antosianin merupakan pigmen alami yang menghasilkan warna biru, ungu, dan violet (Santoso dan Estiasih, 2014). Antosianin bersifat larut dalam air biasanya terletak pada sel-sel permukaan tanaman. Kestabilan antosianin sangat dipengaruhi oleh cahaya, suhu, dan pH (Yoshimoto, dkk., 2001). Menurut Arcot dan Shresta (2005) karakteristik asam folat yaitu larut dalam air dan kestabilan asam folat sangat dipengaruhi oleh pH yang stabil pada kondisi asam. Hal ini menunjukkan bahwa karakteristik dan kestabilan folat mirip dengan antosianin. Pada (Lampiran 16) menunjukkan adanya korelasi sangat nyata (bernilai positif) total antosianin dengan kadar air. Semakin tinggi total antosianin maka kadar airnya semakin tinggi. Total antosianin menunjukkan korelasi nyata (bernilai negatif) terhadap kadar lemak dan protein. Semakin tinggi total antosianin maka kadar lemak dan protein semakin rendah.
Pengujian In Vivo Ekstrak Ubi Jalar Ungu terhadap Mencit Percobaan
51
a. Berat badan induk mencit 1. Fertilitas induk mencit
Tingkat fertilitas ditentukan berdasarkan terjadinya kebuntingan dan kecepatan kebuntingan pada induk mencit. Hasil pengamatan menunjukkan semakin tinggi diet folat yang diberikan maka kecepatan kebuntingan akan semakin cepat dan semakin banyak mencit yang bunting. Pengamatan terhadap kebuntingan mencit pada masing-masing perlakuan dapat dilihat pada Tabel 12. Setelah dikawinkan diharapkan terjadinya kebuntingan pada masing-masing kelompok. Mencit kelompok P1 (kontrol) tidak bunting
sampai 21 hari setelah dikawinkan. Pada kelompok P2 terdapat tiga mencit yang
mengalami kebuntingan pada 14 hari setelah dikawinkan dan tiga mencit di antaranya tidak bunting. Pada kelompok P3 terdapat satu mencit yang bunting setelah 7 hari dikawinkan,
dua mencit tidak bunting dan dua mencit mati pada masa percobaan. Pada kelompok P4
terdapat tiga mencit yang mengalami kebuntingan setelah 7 hari dikawinkan dan tiga mencit belum bunting.
Tabel 12. Pengamatan kebuntingan induk
Keterangan : + = Bunting (Implantasi) ++ = Bunting (Fetus)
- = Tidak bunting
* = Kebuntingan terjadi setelah 14 hari dikawinkan ** = Kebuntingan terjadi setelah 7 hari dikawinkan
Berat badan induk mencit
Hasil analisis ragam (ANOVA) (Lampiran 13) menunjukkan bahwa kelompok diet folat yang berbeda memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap berat badan mencit. Hasil pengamatan menunjukkan bahwa semakin tinggi diet folat yang diberikan maka berat badan induk mencit akan semakin besar. Berat badan induk mencit dapat dilihat pada Gambar 18. Hasil uji LSR (Lampiran 14) menunjukkan bahwa kelompok diet tinggi folat (P4) berbeda tidak nyata dengan P3 tetapi berbeda nyata dengan
P2 dan P1, dan diet rendah folat (P2) berbeda tidak nyata dengan P1 (kontrol)..
Menurut Almahdy (2001) salah satu faktor yang menyebabkan berat badan mencit meningkat yaitu berkembangnya fetus dan bertambahnya volume cairan aminion, plasenta, selaput amnion, dan jumlah fetus yang menunjukkan terjadinya kebuntingan. Oleh karena itu semakin besar kenaikan berat badan induk, kemungkinan semakin banyak mencit yang mengalami kebuntingan.
53
Gambar 18. Berat badan induk mencit masing-masing kelompok dengan perlakuan diet folat yang berbeda
b.Jumlah anakan mencit
Tabel 13 menunjukkan bahwa jumlah anakan mencit yang diamati pada hari ke-21 ada yang dalam tahap implantasi dan ada yang sudah berbentuk fetus. Implantasi adalah peristiwa penempelan embrio pada endometrium uterus induk yang terjadi setelah proses fertilisasi. Fetus adalah embrio dewasa dengan organ tubuh yang sempurna. Hasil pengamatan menunjukkan bahwa pada kelompok P2 terdapat 3 ekor induk mencit yang
menghasilkan anakan mencit dalam bentuk implantasi, pada induk mencit pertama terdapat 12 implantasi terdiri 6 di bagian kanan dan 6 di bagian kiri, pada induk mencit kedua terdapat 9 implantasi terdiri 4 di bagian kanan dan 5 di bagian kiri, sedangkan pada induk mencit ketiga terdapat 12 implantasi terdiri 5 di bagian kanan dan 7 di bagian kiri. Pada kelompok P3 hanya terdapat satu induk mencit yang bunting dengan jumlah anakan
sebanyak 9 anakan dalam bentuk fetus terdiri 5 di bagian kanan dan 4 di bagian kiri. Pada kelompok P4 terdapat 3 ekor induk mencit yang bunting dalam bentuk fetus. Pada induk
mencit pertama memiliki 9 fetus terdiri 5 di bagian kanan dan 4 di bagian kiri. Pada induk
mencit kedua memilik 5 fetus terdiri 2 di bagian kanan dan 3 di bagian kiri. Pada induk mencit ketiga memiliki 6 fetus terdiri 3 di bagian kanan dan 3 di bagian kiri.
Menurut Eisen (1974) jumlah anak sepelahiran adalah banyaknya jumlah anakan yang hidup dan mati. Banyaknya anakan yang dilahirkan dalam periode yang sama rata-rata sebanyak 6 ekor, meskipun mencit dapat melahirkan 15 ekor per kelahiran (Smith dan Mangkoewidjojo, 1988). Hasil penelitian menunjukkan terdapat pengaruh diet folat terhadap jumlah anakan mencit, semakin tinggi diet folat yang diberikan maka jumlah anakan mencit lebih banyak. Kelompok P4 yang merupakan kelompok diet tinggi folat
memiliki jumlah anakan yang paling tinggi yaitu ada 6, 5 dan 9 anakan dalam bentuk fetus dari 3 ekor induk mencit yang bunting sedangkan pada P3 yang merupakan kelompok diet
medium folat hanya terdapat 1 ekor induk mencit yang bunting dengan jumlah anakan dalam bentuk 9 fetus, dan pada P2 yang merupakan kelompok diet rendah folat sampai hari
ke-21 induk mencit baru bunting dalam bentuk implantasi. Banyaknya jumlah anakan dipengaruhi oleh beberapa faktor yaitu jenis ternak, umur induk, musim kelahiran, makanan, persilangan induk, dan kondisi lingkungan (Toelihere, 1979a). Menurut Anggorodi (1979) terjadinya kekurangan asupan makanan dapat menyebabkan fetus dalam uterus mengalami kematian atau kelahiran anak yang lemah. Sementara jumlah sel telur yang dihasilkan dan tingkat awal kematian embrio sangat erat hubungannya dengan jumlah anakan pada periode yang sama (Warwick, dkk., 1983).
Tabel 13. Jumlah anakan mencit Kelompok
Jumlah anakan mencit ke-
1 2 3 4 5 6
55
c. Berat badan anakan mencit
Pengamatan terhadap berat anakan mencit dengan kelompok diet folat yang berbeda dapat dilihat di Tabel 14. Hasil pengamatan menujukkan diet folat berpengaruh terhadap berat badan anakan mencit, semakin tinggi diet folat yang diberikan maka berat badan anakan mencit semakin besar. Pada kelompok P1 tidak ada pengukuran berat badan
anakan disebabkan induk mencit tidak bunting selama 21 hari dikawinkan. Pada kelompok P2 terdapat 3 ekor induk yang bunting setelah 21 hari dikawinkan, tetapi anakan masih
dalam bentuk implantasi, sehingga tidak dapat dilakukan pengukuran berat badan. Tabel 14 menunjukkan bahwa pada kelompok P3 terdapat 1 ekor induk mencit yang bunting dan
menghasilkan berat anakan rata-rata yaitu 0,67 g, sedangkan pada kelompok P4 terdapat 3
ekor induk mencit yang memiliki anakan dalam bentuk fetus dengan berat rata-rata yaitu 0,48, 0,94, dan 0,32 g. Hasil ini menunjukkan pada kelompok P4 yang merupakan
kelompok mencit dengan diet tinggi folat meskipun ada 2 ekor induk yang menghasilkan fetus dengan berat badan anakan rata-rata lebih rendah dari kelompok P3, tetapi pada
kelompok ini terdapat 3 ekor induk yang bunting dan 1 ekor yang memiliki rata-rata berat badan anakan mencit yang jauh lebih tinggi. Menurut Malole dan Pramono (1989) kisaran bobot lahir anakan mencit yaitu 0,5-1,5 g/ekor, dan menurut Smith dan Mangkoewidjojo (1988) berkisar 0,5-1 g/ekor. Berdasarkan hasil yang diperoleh maka rata-rata berat badan anakan mencit kelompok P3 dan P4 menunjukkan berat normal.
bobot anakan mencit pada waktu dilahirkan menjadi abnormal. Menurut Arrington (1972) bobot lahir anakan sangat dipengaruhi oleh kondisi suhu pemeliharaan yang optimal berkisar 21,11-22,22 oC dengan kelembaban udara 45-55%. Menurut Yuwono, dkk. (1994) suhu ruangan untuk pemeliharaan mencit yaitu berkisar antara 15-20 oC dengan kelembaban 45-55%. Kondisi suhu yang tinggi dapat menyebabkan nafsu makan yang rendah pada induk sehingga dapat terjadi defisiensi zat pakan yang akan diperlukan fetus untuk perkembangannya dan menyebabkan berat anakan menjadi rendah.
Tabel 14. Berat badan anakan mencit Kelompok
Rata-rata berat badan anakan dari masing-masing induk mencit
1 2 3 4 5 6
P1 0 0 0 0 0 0
P2 0 0 0 0 0 0
P3 0 0 0 0 0,67* 0
P4 0 0 0 0,48*** 0,94** 0,32*
Keterangan : * = Rata-rata dari 9 anakan ** = Rata-rata dari 5 anakan *** = Rata-rata dari 6 anakan
d.Ukuran badan anakan mencit
Pengamatan ukuran badan anakan mencit dengan kelompok diet folat yang berbeda dapat dilihat pada Tabel 15. Hasil penelitian menunjukkan bahwa pada kelompok P1 tidak
dilakukan pengamatan ukuran badan anakan disebabkan induk mencit tidak bunting selama 21 hari dikawinkan. Pada kelomopok P2 terdapat 3 ekor induk yang bunting setelah 21 hari
dikawinkan, tetapi anakan masih dalam bentuk implantasi sehingga tidak dilakukan pengukuran ukuran badan anakan.
Pengukuran ukuran anakan mencit dilakukan pada kelompok P3 dan P4 yang
menghasilkan anakan dalam bentuk fetus. Pada kelompok P3 terdapat 1 ekor mencit yang
57
ukuran badan yang berbeda. Pada induk mencit pertama menghasilkan 9 anakan dengan rata-rata ukuran badan anakan 0,6 mm. Pada induk mencit kedua menghasilkan 5 anakan dengan rata-rata ukuran badan 1,62 mm. pada induk mencit ketiga menghasilkan 6 anakan dengan rata-rata ukuran badan anakan yang jauh lebih tinggi yaitu 2,23 mm. Pada kelompok P4 dapat diketahui bahwa diet folat berpengaruh terhadap ukuran badan anakan
mencit sehingga semakin tinggi diet folat maka ukuran badan anakan mencit akan semakin besar.
Menurut Wilson (1973) adanya gangguan penghambatan perkembangan fetus dalam uterus menyebabkan berkurangnya panjang fetus. Terjadinya penghambatan pada pertumbuhan fetus disebabkan beberapa faktor proliferasi sel, interaksi sel, dan pengurangan laju biosintesis yang berkaitan dengan hambatan sintesis asam nukleat, protein, dan mukopolisakarida.
Tabel 15. Ukuran badan anakan Kelompok
Ukuran badan anakan ke- (mm)
1 2 3 4 5 6
e. Penampilan fisik anakan mencit
Pengamatan terhadap penampilan fisik pada masing-masing perlakuan dapat dilihat pada Gambar 19. Hasil pengamatan menunjukkan bahwa diet folat berpengaruh terhadap morfologi anakan mencit. Pada kelompok P1 tidak satupun mencit yang bunting hingga 21
implantasi selama masa percobaan. Pada kelompok P3 diketahui bahwa penampakan fisik
anakan mencit sudah dalam bentuk fetus, namun terlihat adanya bagian tubuh yang belum terbentuk sempurna. Sementara pada kelompok P4 diketahui bahwa bentuk fetus dewasa
dengan bagian tubuh yang sudah terbentuk sempurna.
59
Kelompok P2 Implantasi
Kelompok P3 Fetus belum
sempurna
Kelompok P4 Fetus
Sempurna
Kesimpulan
Dari hasil penelitian pengaruh varietas ubi jalar terhadap karakteristik kimia tepung ubi jalar dana diet folat terhadap parameter yang diamati dapat diambil kesimpulan sebagai berikut :
1. Varietas ubi jalar memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar air dan kadar pati pada ubi jalar. Kadar air tertinggi terdapat pada ubi jalar oranye sebesar 55,6591% dan terendah pada ubi jalar ungu sebesar 55,6591% dan kadar pati tertinggi pada ubi jalar madu sebesar 49,6282% dan terendah pada ubi jalar oranye sebesar 31,6570%.
2. Varietas ubi jalar memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar air, kadar abu, kadar lemak, dan kadar karbohidrat tepung ubi jalar. Namun varietas ubi jalar memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap kadar protein. 3. Kandungan folat secara signifikan hanya terdapat pada ubi jalar ungu saja sebesar 9,44
mg/kg. Sementara pada varietas ubi jalar lainnya tidak terdeteksi.
4. Kandungan pigmen antosianin hanya terdapat pada ubi jalar ungu sebesar 877,0811 mg/100g. Semakin tinggi total antosianin maka kandungan folat akan semakin tinggi. 5. Kelompok diet folat yang berbeda berpengaruh terhadap tingkat fertilitas induk
61
6. Kelompok diet folat yang berbeda berpengaruh terhadap berat badan induk mencit yang berbeda sangat nyata (P<0,01). Semakin tinggi diet folat yang di berikan maka berat badan induk mencit semakin besar.
7. Kelompok diet folat yang berbeda berpengaruh terhadap jumlah anakan mencit. Semakin tinggi diet folat yang diberikan maka jumlah anakan mencit lebih banyak. Pada kelompok P4 dengan diet tinggi folat (0,3 ml = 0,15 μg) menunjukkan jumlah
anakan mencit dari 3 ekor induk mencit sebanyak 6, 5, dan 9.
8. Kelompok diet folat yang berbeda memberikan pengaruh terhadap berat badan anakan. Semakin tinggi diet folat yang diberikan maka berat badan anakan semakin besar. Pada kelompok P4 dengan diet tinggi folat (0,3 ml = 0,15 μg) menunjukkan
rata-rata berat badan anakan mencit dari 3 ekor induk mencit yaitu 0,48, 0,94, dan 0,32 g.
9. Kelompok diet folat yang berbeda memberikan pengaruh terhadap ukuran badan anakan mencit. Semakin tinggi diet folat yang diberikan makan ukuran badan akan semakin besar. Pada kelompok P4 dengan diet tinggi folat (0,3 ml = 15 µg)
menunjukkan rata-rata ukuran badan anakan mencit dari 3 ekor induk mencit yaitu 0,6, 1,62, dan 2,23 mm.
10. Kelompok diet folat yang berbeda memberikan pengaruh terhadap penampilan fisik. Diet tinggi folat (0,3 ml = 15 µg) memberikan pengaruh terhadap penampilan fisik anakan mencit yang ditinjau dari aspek bentuk dan ukuran yang normal secara visual. Saran
2. Perlu dilakukan penelitian lanjutan mengenai berbagai metode ekstraksi untuk memperoleh folat dalam jumlah yang lebih banyak. Penggunan berbagai pelarut dengan tingkat kepolaran yang sama dengan folat sehingga dapat diketahui jenis pelarut yang paling tepat untuk menghasilkan folat dalam jumlah yang lebih banyak. 3. Perlu dilakukan penelitian lanjutan mengenai bioavailabilitas folat pada berbagai
produk olahan ubi jalar.
Ucapan Terima Kasih
6
TINJAUAN PUSTAKA
Ubi Jalar
Ubi jalar mempunyai nama ilmiah Ipomea batatas L. Berikut taksonomi dan klasifikasi tanaman ubi jalar (Malik, 2003) adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledonae Ordo : Concolvulales Famili : Concolvulaceae Genus : Ipomea
Species : Ipomea batatas L Sin
Varietas ubi jalar yang dikenal di Indonesia umumnya dikelompokkan berdasarkan warna daging ubi jalar yaitu berwarna putih, kuning, merah, dan ungu (Rosidah, 2010). Ubi jalar oranye (Var. Beta 1)
Gambar 1. Ubi jalar oranye (Wikipedia, 2015b) Ubi jalar kuning (Var. Kalasan)
Karakteristik ubi jalar kuning (Var. Kalasan) adalah bentuk ubi agak lonjong dengan permukaan kulit tidak merata, warna daging kuning, dan lebih lunak (basah) yang menyebabkan kandungan patinya juga lebih rendah hanya berkisar 13-19% (Pantastico, 1986). Deskripsi Var. Kalasan dapat dilihat pada (Lampiran 2) (IPB Bogor, 2009). Penampakkan ubi jalar kuning dapat dilihat pada Gambar 2.
Gambar 2. Ubi jalar kuning (Wikipedia, 2015c) Ubi jalar madu (Var. Sari)
8
Gambar 3. Ubi jalar madu (Wikipedia, 2015d) Ubi jalar ungu (Var. Ayamurasaki)
Karakteristik ubi jalar ini yaitu memiliki bentuk ubi yang lonjong dengan permukaan yang rata, warna daging ungu muda sampai ungu pekat, dagingnya bertekstur keras akibat kandungan air yang rendah, dan rasanya manis. Keunggulan ubi jalar ungu yaitu pigmen antosianin yang berperan sebagai antioksidan dengan jumlah yang tinggi secara signifikan dibandingkan dengan varietas lainnya (Rosidah, 2010). Deskripsi ubi jalar Var. Ayamurasaki dapat dilihat pada (Lampiran 4) (IPB Bogor, 2009). Penampakkan fisik ubi jalar ungu dapat dilihat pada Gambar 4.
Gambar 4. Ubi jalar ungu (Wikipedia, 2013e)
Kandungan Gizi Ubi Jalar
dikembangkan menjadi berbagai jenis produk olahan. Ubi jalar memiliki kandungan vitamin B yaitu B6 dan folat (B9) yang berperan dalam mencegah terjadinya inflamasi pertumbuhan dan perkembangan sel otak (Jaya, 2013). Kandungan gizi pada berbagai varietas ubi jalar dalam 100 g dapat dilihat pada Tabel 4.
Tabel 4. Kandungan gizi ubi jalar dalam 100 g No Komposisi gizi Ubi
10
Tepung ubi Jalar
Tepung ubi jalar merupakan produk hasil pengolahan ubi jalar segar yang sudah terjadi pengurangan kadar air setelah dilakukan proses pengolahan berupa pengeringan. Pengeringan yang digunakan dapat secara alami atau dengan menggunakan alat pengering. Tujuan pengolahan ubi jalar menjadi tepung atau produk setengah jadi sehingga dapat memperpanjang masa simpan dan memperkecil volume ruang penyimpanan. Sifatnya yang praktis sehingga jaminan ketersediaan tepung ubi jalar sangat efektif digunakan sebagai bahan baku industri pangan dan non-pangan. Varietas ubi jalar yang bervariasi akan menghasilkan berbagai tepung ubi jalar (Claudia, dkk., 2015). Kandungan gizi pada tepung ubi jalar dalam 100 g dapat dilihat pada Tabel 5.
Tabel 5. Kandungan gizi tepung ubi jalar dalam 100 g
Komposisi kimia Jumlah
Air (%) 7,0
Protein (%) 3,16
Lemak (%) 0,5
Abu (%) 2,13
Karbohidrat (%) 85,26
Serat (%) 1,95
Sumber : Claudia, dkk., 2015
Kadar air maksimal yang aman untuk penyimpanan tepung ubi jalar sebesar 15%. Perbedaan kandungan kadar air pada ubi jalar sangat dipengaruhi oleh tahapan proses yaitu pengeringan (Antarlina, 1998). Menurut Purnomo (1995) air bebas sangat mudah hilang akibat pemanasan.
menguap seperti K, Na, Ca, Cl, dan P pada saat pemijaran. Kadar abu maksimal yang terkandung pada ubi jalar sebesar 2,38% (Widjanarko, 2008).
Kadar lemak dipengaruhi oleh kandungan pigmen yang terdapat di dalam suatu bahan. Pigmen betakaroten merupakan pigmen yang bersifat lipofilik yang larut dalam lemak sehingga adanya pigmen ini dapat mempertahankan lemak tepung ubi jalar (Dutta, dkk., 2005). Pigmen betakaroten bersifat sebagai antioksidan yang terbukti mencegah proses oksidasi lemak (Silalahi, 2006). Sementara untuk kadar protein dipengaruhi adanya perlakuan pemanasan yang dapat menurunkan kandungannya di dalam suatu bahan. Protein merupakan senyawa yang sangat mudah mengalami kerusakan akibat proses pengolahan yang menggunakan panas. Protein sangat mudah rusak akibat reaksi Maillard yang terjadi pada suhu 30-35 oC (de Man, 1989).
Kadar karbohidrat selain dipengaruhi oleh pascapanen, umur panen, dan lingkungan panen juga dipengaruhi oleh varietas dan umur panennya (Kurnia, 2008). Kandungan karbohidrat pada tepung ubi jalar sangat dipengaruhi oleh perbedaan umur panen dan lingkungan tumbuhnya (Widjanarko, 2008). Karbohidrat yang terdapat pada bahan nabati yaitu gula sederhana, heksosa, pentosa, maupun karbohidrat dengan berat molekul tinggi seperti pati, pektin, selulosa dan lignin. Selulosa dan lignin berperan sebagai penyusun dinding sel sehingga dapat melindungi komponen yang ada di dalamnya (Winarno, 1982).