APLIKASI TEKNOLOGI NEAR INFRARED UNTUK
PENDUGAAN VIABILITAS BENIH PADI (
Oryza sativa
)
VARIETAS CIHERANG
JONNI FIRDAUS
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis Aplikasi Teknologi Near Infrared
untuk Pendugaan Viabilitas Benih Padi (
Oryza sativa
) Varietas Ciherang adalah
karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam
bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang
berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari
penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di
bagian akhir tesis ini.
Bogor, Januari 2013
JONNI FIRDAUS. Aplication of Near Infrared to Determine Viability of
‘
Ciherang
’
Paddy (
Oryza sativa
) Seed. Supervised by ROKHANI HASBULLAH,
USMAN AHMAD, and M. RAHMAD SUHARTANTO.
Near infrared (NIR) spectroscopy in the range of 1000-2500 nm was studied for
its ability to predict the seed viability such as germability, vigor index, maximum
growth potential and the biochemistry composition such as water content, soluble
protein, and free faty acid of the ciherang paddy seed following 0, 2, 4, 6 and 8
days acclerated aging (45
oC, RH >90%). A total of 60 sample groups consist of 40
g paddy seed per sample ware used. Fourty samples were used for calibration and
20 samples were used for validation. Artificial neural network (ANN) and partial
least squares (PLS) regression methods were used to build the prediction model.
The good model should have a low standard error of calibration (SEC), a low
standard error of performance (SEP), a high correlation coefficient, a small
difference between SEC and SEP and have ratio performance deviation (RPD)
higher than 2.5. The result showed that kind of original and pre processing spectra
influenced the value of evaluation ANN and PLS model. The structure of ANN
also influence the value of evaluation model. The best model to predict
germability was 10-5-3 ANN using standard normal variate of reflectan spectra
with RPD = 2.2359 and r validation = 0.8947, to predict vigor index was 10-5-1
ANN using 2
ndderivative of reflectan spectra with RPD=3.6842 and r validation
0.9645, to predict maximum growth potential was 10-5-1 ANN using 2
ndderivative of reflectan spectra with RPD=2.5572 and r validation 0.9204, to
predict water content was PLS using absorbant spectra with RPD=9.6028 and r
validation 0.9946, to predict soluble protein was 5-5-1 ANN using 2
ndderivative
of reflectan spectra with RPD=3.9615 and r validation 0.9686, and to predict free
faty acid was 10-20-1 ANN model using 2
ndderivative of absorbant spectra with
RPD=4.0290 and r validation 0.9688.
JONNI FIRDAUS. Aplikasi Teknologi
Near Infrared
untuk Pendugaan Viabilitas
Benih Padi (
Oryza sativa
) Varietas Ciherang. Dibimbing oleh ROKHANI
HASBULLAH, USMAN AHMAD, dan M. RAHMAD SUHARTANTO.
Benih memiliki peranan yang penting dalam peningkatan produksi padi.
Kebutuhan benih bermutu cenderung meningkat seiring dengan tuntutan
peningkatan produksi padi nasional untuk mengimbangi laju pertumbuhan
penduduk. Kebutuhan benih nasional, berdasarkan luas panen pada tahun 2011
seluas 13.204.000 ha dengan asumsi penggunaan benih 20 kg/ha, mencapai
264.080 ton (Kementan 2012). Untuk memenuhi kebutuhan tersebut diperlukan
upaya dari seluruh komponen sistem perbenihan agar benih dapat diperoleh petani
dengan mudah pada saat dibutuhkan.
Salah satu komponen sistem perbenihan adalah subsistem pengendalian
mutu yang berperan dalam menjamin mutu benih yang beredar di pasaran.
Parameter penting dalam menentukan mutu benih adalah kemampuan benih untuk
hidup (viabilitas benih). Indikasi viabilitas benih merupakan kinerja yang
menunjukkan bahwa benih hidup dan dapat diduga melalui daya berkecambah
benih.
Saat ini, pengujian viabilitas membutuhkan waktu yang cukup lama (5-14
hari) (SNI 01-6233.1 2003). Sementara itu, tingginya tingkat kebutuhan benih di
lapangan harus segera dipenuhi agar petani dapat menanam tepat waktu. Jika
benih bermutu tidak tersedia di pasaran saat musim tanam, maka petani akan
menggunakan benih seadanya yang memiliki mutu rendah akibatnya produksi
yang dicapai juga rendah. Oleh karena itu dibutuhkan suatu cara pengujian
viabilitas benih yang lebih cepat
Salah satu alternatif metode yang dapat digunakan adalah penggunaan
gelombang
Near Infrared
(NIR). NIR dapat diaplikasikan untuk mendeteksi
bahan organik yang kaya dengan ikatan O-H (seperti air, karbohidrat, lemak),
ikatan C-H dan ikatan N-H (protein, asam amino). Sementara itu secara kimia di
dalam benih berisi cadangan makanan dan senyawa yang berpengaruh terhadap
perkecambahan benih. Pada benih viabel terdapat kandungan protein yang lebih
tinggi dari yang tidak viabel yang ditunjukkan pada panjang gelombang 1722 dan
2110 nm. Selain itu lemak juga berpengaruh terhadap perkecambahan dimana
terdapat pemisahan yang jelas antara benih yang viabel dengan yang tidak viabel
yang dapat dideteksi pada panjang gelombang 1350 nm.
Bahan yang digunakan adalah benih padi sawah varietas Ciherang yang
diperoleh dari Balai Besar Penelitian Tanaman Padi Sukamandi, yang dipanen
pada Februari 2012. Alat yang digunakan adalah NIR spectroscopy, komputer,
environmental chamber, alat pengecambah benih, dan timbangan digital.
Sebanyak 40 gram x 12 unit sampel (untuk setiap lama pengusangan) benih
direndam dalam 1 liter larutan
dithane
(2 g/liter) selama 15 menit lalu dibilas
sekali dengan 1 liter aquades, kemudian ditiriskan dan dikeringanginkan selama 3
jam pada ruangan ber-AC dengan suhu 25
oC. Benih dibagi menjadi 12 unit dan
dimasukkan ke dalam kantung streamin. Selanjutnya sampel diusangkan pada
suhu 45
oC dan RH>90% selama 0, 2, 4, 6 dan 8 hari.
Sampel yang telah diusangkan diambil data reflektannya pada panjang
gelombang 1000-2500 nm. Sampel yang telah diambil data reflektannya
kemudian dianalisa parameter kimianya berupa kadar air, protein terlarut, dan
asam lemak bebas. Kemudian benih dikecambahkan, menggunakan metode uji
kertas digulung dalam plastik, sebanyak 50 bulir dengan 3 ulangan. Pengamatan
dilakukan pada hari kelima dan ketujuh dan dihitung kecambah normal, abnormal
dan benih mati yang didasarkan pada SNI 01-6233.1 (2003). Kemudian dihitung
parameter viabilitas berupa daya berkecambah, indeks vigor, dan potensi tumbuh
maksimum.
Hasil pengukuran NIR diperoleh 180 data reflektan. Data reflektan
ditransformasi menjadi data absorban dengan persamaan log(1/Reflektan).
Selanjutnya terhadap data reflektan dan absorban dilakukan pra pengolahan data
berupa normalisasi 0-1,
standard normal variate
, turunan pertama
Savitzky-Golay
dan turunan kedua
Savitzky-Golay
.
Model jaringan saraf tiruan (JST) yang digunakan adalah
back propagation
yang terdiri dari 3 lapisan yaitu
input, hidden
dan
output
. Fungsi aktivasi yang
digunakan adalah fungsi sigmoid pada lapisan
hidden
dan fungsi identitas pada
lapisan
output. Input
jaringan berupa komponen utama dari spektra asli maupun
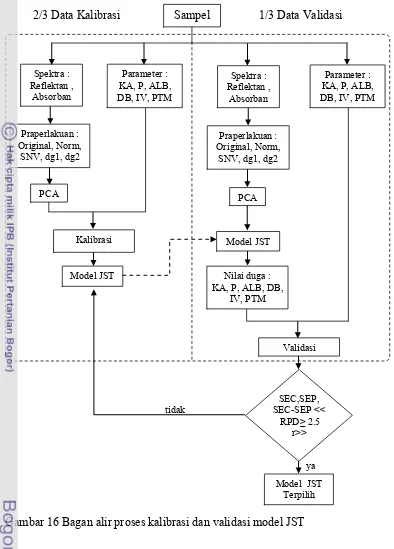
yang telah diberi praperlakuan. Sebelum dilakukan penentuan komponen utama,
terlebih dahulu dilakukan pembagian data spektra yaitu data kalibrasi 2/3 bagian
(120 data) dan data validasi 1/3 bagian (60 data). Analisa komponen utama (PCA)
menggunakan software SPSS Statistic 19. Variasi jumlah komponen utama yang
digunakan adalah 5, 10, 15 dan 20 komponen.
Output layer
terdiri dari 2 variasi
yaitu
single output
dan
multi output
yang merupakan kombinasi dari nilai
parameter .
Hidden layer
ditentukan dengan jumlah unit 5, 10, 15, 20. Variasi
input, hidden
dan
ouput layer
dikombinasikan menjadi 800 skenario. Setiap
skenario dilatih menggunakan
software
MATLAB R2008b. Proses pelatihan
bertujuan meminimumkan total eror, pelatihan akan berhenti bila eror pada set
validasi tidak turun lagi sebanyak 5 iterasi. Laju pelatihan yang digunakan adalah
0.01 dan koefisien momentum 0.9.
menunjukkan model yang dibangun semakin akurat.
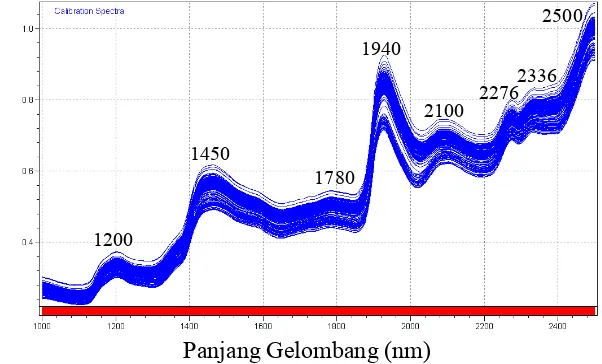
Dari hasil penelitian diketahui bahwa karakteristik spektra absorban benih
padi menunjukkan beberapa puncak gelombang yang menggambarkan komposisi
kimia dominan benih padi yaitu pati (1200, 1450, 2100, 2276, 2500 nm), selulosa
(1780, 2336 nm), dan air (1450, 1940 nm). Spektra pada rentang 1000-1015,
2070-2085, 2148-2178 nm yang merupakan wilayah penyerapan protein dan pada
1350, 1415 nm yang merupakan wilayah penyerapan lemak memiliki bentuk
gelombang yang sama antar lama waktu pengusangan namun intensitas
penyerapannya berbeda.
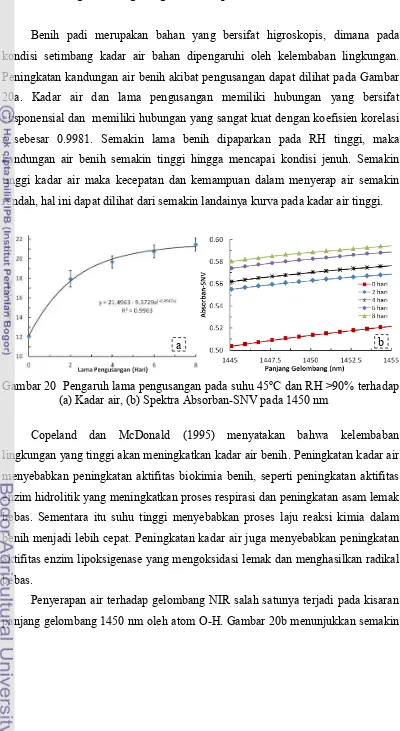
Semakin lama waktu pengusangan menyebabkan peningkatkan kadar air
benih, penurunan kandungan protein terlarut dan peningkatan asam lemak bebas
yang juga diindikasikan oleh intensitas spektra absorban-SNV pada wilayah
penyerapan masing-masing serta diikuti oleh penurunan viabilitas benih.
Model terbaik untuk menduga kadar air adalah PLS dengan input
absorban, protein terlarut adalah JST 5-5-1 dengan input turunan kedua reflektan,
asam lemak bebas adalah JST 5-20-1 dengan input turunan kedua absorban, daya
berkecambah adalah JST 10-5-3 dengan input standar normal variate reflektan,
indeks vigor adalah JST 10-5-1 dengan input turunan kedua reflektan dan potensi
tumbuh maksimum adalah JST 10-5-1 dengan input turunan kedua reflektan.
Berdasarkan nilai RPD parameter yang terakurat dilakukan pendugaannya
dengan NIR beturut-turut adalah kadar air benih, kandungan asam lemak bebas,
protein terlarut, indeks vigor, potensi tumbuh maksimum dan terakhir daya
berkecambah. Berdasarkan nilai r, SEC, SEP dan RPD pada parameter viabilitas
(daya berkecambah, indeks vigor, potensi tumbuh maksimum), aplikasi NIR
berpotensi digunakan untuk menduga nilai viabilitas benih secara non-destruktif.
©
Hak Cipta Milik IPB, Tahun 2013
Hak Cipta Dilindungi Undang-Undang
Dilarang
mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan
atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan,
penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau
tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan
yang wajar IPB
APLIKASI TEKNOLOGI NEAR INFRARED UNTUK
PENDUGAAN VIABILITAS BENIH PADI (
Oryza sativa
)
VARIETAS CIHERANG
JONNI FIRDAUS
Tesis
sebagai salah satu syarat untuk memperoleh gelar
Magister Sains pada
Program Studi Teknik Mesin Pertanian dan Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
NRP
: F151100101
Disetujui oleh
Komisi Pembimbing
Dr. Ir. Rokhani Hasbullah, M.Si
Ketua
Dr. Ir. Usman Ahmad, M.Agr
Anggota
Dr. Ir. M. Rahmad Suhartanto, M.Si
Anggota
Diketahui oleh
Ketua Program Studi
Teknik Mesin Pertanian dan Pangan
Dr. Ir. Setyo Pertiwi, M.Agr
Dekan Sekolah Pascasarjana
Dr. Ir. Dahrul Syah, M.Sc.Agr
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas segala nikmat
yang diberikan kepada penulis sehingga karya ilmiah
dengan judul “
Aplikasi
Teknologi
Near Infrared
untuk Pendugaan Viabilitas Benih Padi (
Oryza sativa
)
Varietas Ciherang
”
berhasil diselesaikan.
Terima kasih penulis sampaikan kepada Dr. Ir. Rokhani Hasbullah, M.Si,
Dr. Ir Usman Ahmad, M.Agr. dan Dr. Ir. M. Rahmad Suhartanto, M.Si. selaku
komisi pembimbing yang telah meluangkan waktu dan memberikan arahan dalam
penyusunan karya ilmiah ini.
Penulis juga mengucapkan terima kasih kapada :
1.
Orang tua tercinta Rustam Effendi dan Asnidarwati, istri tercinta Andi
Dalapati, STP, MP, anak-anak tercinta Muhammad Mujahid Pangera dan
Ahmad Zikrillah Pangera, serta adik-adik tercinta Safril Hidayat, SKom,
Mukhlis Junaidi, SP dan Khairil Hamdi atas doa, nasehat dan dukungan yang
diberikan kepada penulis selama menempuh pendidikan.
2.
Badan Litbang Pertanian yang telah memberikan beasiswa kepada penulis
selama menempuh pendidikan.
3.
Balai Pengkajian Teknologi Pertanian Sulawesi Tengah yang telah
menugaskan penulis untuk menempuh pendidikan.
4.
Rekan-rekan Mayor Teknik Mesin Pertanian dan Pangan 2010 yang telah
membantu pelaksanaan penelitian ini.
5.
Semua pihak yang telah membantu pelaksanaan penelitian ini.
Semoga karya ilmiah ini bermanfaat bagi pengembangan dan pemanfaatan
ilmu pengetahuan.
Bogor, Januari 2013
Penulis dilahirkan di Desa Balimbingan, Kecamatan Tanah Jawa,
Kabupaten Simalungun, Sumatera Utara pada tanggal 19 Juni 1981 dari pasangan
Bapak Rustam Effendi dan Ibu Asnidarwati. Penulis merupakan anak pertama dari
empat bersaudara.
Penulis mengikuti pendidikan di SD Negeri 091504 (1987-1993), SMP
Negeri 1 (1993-1996) dan SMU Negeri 1 (1996-1999) di Kecamatan Tanah Jawa,
Kabupaten Simalungun. Selanjutnya penulis mengikuti pendidikan tinggi pada
Program Studi Teknik Pertanian (1999-2003), Universitas Sumatera Utara,
Medan.
Halaman
DAFTAR TABEL ... xix
DAFTAR GAMBAR ... xxi
DAFTAR LAMPIRAN ... xxiii
PENDAHULUAN ... 1
Latar Belakang ... 1
Perumusan Masalah ... 3
Tujuan ... 3
Kegunaan... 3
TINJAUAN PUSTAKA ... 5
Viabilitas Benih ... 5
Kemunduran Benih ... 6
Pengusangan Cepat (
Rapid Aging
)... 8
Komposisi Benih Padi ... 9
Near Infrared Spectroscopy
... 11
Pendugaan Viabilitas Benih Menggunakan NIR ... 13
Jaringan Saraf Tiruan ... 14
Analisis Komponen Utama ... 18
METODOLOGI ... 21
Waktu dan Tempat ... 21
Alat dan Bahan ... 21
Prosedur Penelitian... 23
Persiapan Sampel ... 23
Pengukuran Spektra Reflektan NIR ... 25
Pengujian Viabilitas Benih ... 27
Pengukuran Kadar Air ... 28
Pengukuran Kadar Protein Terlarut ... 28
Pengukuran Kadar Asam Lemak Bebas ... 29
Pembangunan Model Jaringan Saraf Tiruan ... 30
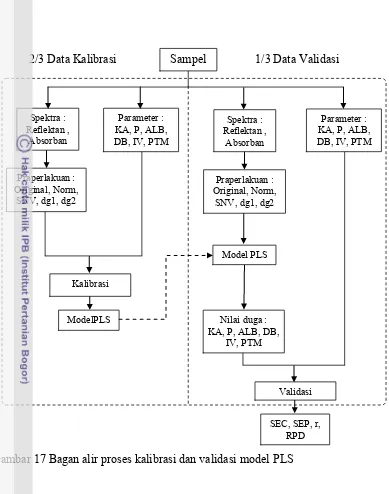
Pembangunan Model Kalibrasi NIR dengan Model PLS ... 31
Evaluasi Model JST dan PLS ... 32
HASIL DAN PEMBAHASAN ... 35
Karakteristik Gelombang NIR Benih Padi ... 35
Pengaruh Pengusangan terhadap Kadar Air Benih Padi ... 37
Pengaruh Pengusangan terhadap Protein Terlarut ... 38
Pengaruh Pengusangan terhadap Asam Lemak Bebas... 39
Model PCA
–
JST Propagasi Balik ... 42
Deskripsi Data ... 42
Halaman
1 Komposisi kimia beras pecah kulit (
brown rice
) ... 9
2 Komposisi kimia sekam padi ... 10
3 Komposisi asam lemak pada beras pecah kulit (%) ... 10
4 Panjang gelombang yang berhubungan dengan protein ... 12
5 Ikatan atom dan struktur kimia yang merupakan puncak gelombang pada
spektra absorban benih padi ... 36
6 Karakteristik nilai parameter benih padi yang digunakan dalam kalibrasi dan
validasi ... 42
7 Persentase variasi kumulatif 20 komponen utama ... 43
8 Model JST terbaik untuk setiap parameter pengamatan ... 46
9 Karakteristik nilai parameter benih padi yang digunakan dalam kalibrasi dan
Halaman
1 Benih padi varietas ciherang ... 21
2
Near Infrared Spectroscopy
... 22
3
Environmental chamber
... 22
4
Germinator
... 22
5
Chamber
Plastik ... 22
6 Benih di dalam kantung strimin ... 23
7 Sampel dalam chamber plastik ... 23
8 Penempatan kain kanebo ... 23
9 Bagan alir persiapan sampel ... 24
10 Bagan alir pengambilan data ... 25
11 Penempatan
chamber
plastik di dalam
environmental chamber
... 25
12 Pengecambahan metode uji kertas digulung dalam plastik pada germinator 25
13 Penempatan sampel pada petridish dan NIRFlex saat pengambilan spektra 26
14 Mekanisme pengambilan data spektra sampel pada NIRFlax petri solid ... 26
15 Contoh struktur jaringan saraf tiruan ... 31
16 Bagan alir proses kalibrasi dan validasi model JST ... 33
17 Bagan alir proses kalibrasi dan validasi model PLS ... 34
18 Spektra reflektan benih padi ... 35
19 Spektra absorban benih padi ... 36
20 Pengaruh lama pengusangan pada suhu 45
oC dan RH >90% terhadap (a)
Kadar air, (b) Spektra Absorban-SNV pada 1450 nm ... 37
21 Pengaruh lama pengusangan pada suhu 45
oC dan RH >90% terhadap (a)
protein terlarut, (b) Spektra Absorban-SNV pada 1000-1015nm, (c) Spektra
Absorban-SNV pada 2070-2085 nm, (d) Spektra Absorban-SNV pada
2148-2178nm ... 38
22 Pengaruh lama pengusangan pada suhu 45
oC dan RH >90% terhadap (a) asam
lemak bebas, (b) Spektra SNV pada 1350 nm, (c) Spektra
absorban-SNV pada 1415 nm ... 40
23 Pengaruh lama pengusangan pada suhu 45
oC dan RH 90% dengan daya
Halaman
1 Berbagai praperlakuan terhadap spektra reflektan dan absorban ... 63
2 Total variasi kumulatif dari 20 komponen utama ... 65
3 Skenario dan hasil kalibrasi-validasi untuk setiap parameter ... 67
4 Kode pemrograman dan struktur input dan target JST pada MATLAB
R2008b ... 111
5 Kombinasi struktur JST terbaik untuk setiap jenis spektra ... 113
6 Jenis spektra terbaik untuk setiap kombinasi jumlah output JST ... 119
7 Hasil kalibrasi dan validasi model PLS untuk setiap parameter dengan
Latar Belakang
Benih memiliki peranan yang penting dalam peningkatan produksi padi.
Kebutuhan benih bermutu cenderung meningkat seiring dengan tuntutan
peningkatan produksi padi nasional untuk mengimbangi laju pertumbuhan
penduduk. Kebutuhan benih nasional, berdasarkan luas panen pada tahun 2011
seluas 13.204.000 ha dengan asumsi penggunaan benih 20 kg/ha, mencapai
264.080 ton (Kementan 2012). Untuk memenuhi kebutuhan tersebut diperlukan
upaya dari seluruh komponen sistem perbenihan agar benih dapat diperoleh petani
dengan mudah pada saat dibutuhkan.
Salah satu komponen sistem perbenihan adalah subsistem pengendalian
mutu yang berperan dalam menjamin mutu benih yang beredar di pasaran.
Subsistem pengendalian mutu melakukan serangkaian pengujian di laboratorium
hingga dikeluarkan sertifikat yang menyatakan bahwa benih tersebut telah
memenuhi standar mutu yang ditentukan. Salah satu parameter penting dalam
menentukan mutu benih adalah kemampuan benih untuk hidup (viabilitas benih).
Indikasi viabilitas benih merupakan kinerja yang menunjukkan bahwa benih hidup
dan dapat diduga melalui daya berkecambah benih.
Saat ini, pengujian viabilitas membutuhkan waktu yang cukup lama (5-14
hari) (SNI 01-6233.1 2003). Sementara itu, tingginya tingkat kebutuhan benih di
lapangan harus segera dipenuhi agar petani dapat menanam tepat waktu. Jika
benih bermutu tidak tersedia di pasaran saat musim tanam, maka petani akan
menggunakan benih seadanya yang memiliki mutu rendah, akibatnya produksi
yang dicapai juga rendah. Oleh karena itu dibutuhkan suatu cara pengujian
viabilitas benih yang lebih cepat.
Salah satu alternatif metode yang dapat digunakan untuk mempercepat
waktu pengujian viabilitas benih adalah penggunaan gelombang
Near Infrared
yang sederhana, dan tidak memerlukan bahan kimia. Pemanfaatan NIR dilakukan
dengan mengkorelasikan secara statistik sinyal
Near Infrared
pada beberapa
panjang gelombang tertentu dengan karakteristik atau kandungan bahan yang
diukur.
Aplikasi NIR diawali oleh Noris dan Hart pada tahun 1965 yang mengukur
kadar air dalam biji dengan menggunakan
transmittance spectroscopy
pada
panjang gelombang 1940 nm (Andrianyta 2006). Selanjutnya, Jordon menyatakan
bahwa NIR dapat diaplikasikan untuk bahan-bahan organik yang kaya dengan
ikatan O-H seperti kadar air, karbohidrat, dan lemak, ikatan C-H seperti
bahan-bahan organik turunan minyak bumi, dan ikatan N-H seperti protein dan asam
amino (Ruiz 2001).
Secara kimia di dalam benih berisi cadangan makanan dan senyawa yang
berpengaruh terhadap perkecambahan benih (Copeland dan McDonald 1995).
Pada benih viabel terdapat kandungan protein yang lebih tinggi dari yang tidak
viabel yang ditunjukkan pada panjang gelombang 1722 dan 2110 nm (Soltani
2003). Selain itu lemak juga berpengaruh terhadap perkecambahan, dimana
terdapat pemisahan yang jelas antara benih bayam yang viabel dengan yang tidak
viabel yang dapat dideteksi pada panjang gelombang 1350 nm (Olesen
et al
.
2110).
Penelitian terdahulu mengenai pemanfaatan NIR untuk menduga viabilitas
benih bayam bersifat kualitatif yaitu hanya sebatas pemisahan antara benih viabel
dan non viabel pada benih tunggal (Olesen
et al
. 2110). Pada penelitian ini
teknologi NIR yang dikombinasikan dengan jaringan saraf tiruan digunakan untuk
menduga nilai viabilitas secara kuantitatif dari kelompok benih.
Perumusan Masalah
Tingkat kebutuhan benih yang tinggi pada tingkat
petani tidak dapat segera
dipenuhi secara cepat oleh para komponen perbenihan. Salah satu penyebab
terjadinya hal tersebut dikarenakan oleh pengujian viabilitas benih membutuhkan
waktu yang relatif lama. Salah satu alternatif solusi untuk masalah ini adalah
penggunaan gelombang NIR untuk menduga viabilitas benih secara cepat dan
akurat.
Tujuan
Secara umum penelitian ini bertujuan untuk mengembangkan metode
evaluasi viabilitas benih padi sawah menggunakan gelombang NIR.
Secara khusus penelitian ini bertujuan untuk :
1.
mempelajari karakteristik gelombang NIR pada benih padi
2.
mempelajari perubahan kadar air, protein terlarut, asam lemak bebas, dan
viabilitas benih akibat lama waktu pengusangan
3.
mempelajari perubahan spektra NIR benih padi akibat lama waktu
pengusangan pada panjang gelombang yang berhubungan dengan kadar air,
protein terlarut, dan asam lemak bebas
4.
menentukan model jaringan saraf tiruan (JST) dan partial least square (PLS)
terbaik untuk pendugaan viabilitas benih.
Kegunaan
Viabilitas Benih
Viabilitas benih adalah kemampuan benih untuk tumbuh normal pada
kondisi optimum (Sadjad
et al
. 1999). Viabilitas benih dapat diindikasikan
sebagai kinerja yang menunjukkan bahwa benih dalam keadaan hidup. Viabilitas
benih didefenisikan sebagai daya hidup benih yang dapat ditunjukkan melalui
gejala metabolisme benih atau gejala pertumbuhan. Menguji viabilitas benih
bertujuan untuk mengetahui kemampuan benih tumbuh di lapang sebelum
ditanam (Sadjad 1972).
Ada dua jenis viabilitas benih yaitu viabilitas optimum dan viabilitas
suboptimum. Viabilitas optimum adalah kemampuan hidup benih untuk tumbuh
menjadi tanaman normal dan berproduksi normal pada kondisi lingkungan yang
optimum. Kondisi optimum bagi benih adalah bila air, oksigen dan cahaya
tersedia serta suhu di sekitar benih optimum (Qadir 1994).
Tolok ukur viabilitas benih potensial adalah daya berkecambah benih dan
berat kering kecambah normal. Pengujian daya berkecambah perlu dilakukan
karena suatu kelompok benih terdiri dari populasi individu benih, dimana
masing-masing memiliki kemampuan sendiri untuk tumbuh menjadi tanaman dewasa
(Copeland & McDonald 1995). Daya berkecambah merupakan proporsi benih
yang tumbuh menjadi kecambah normal pada kondisi lingkungan yang optimum.
Peubah ini paling banyak digunakan dalam penilaian viabilitas benih (Qadir
1994).
benih sudah harus ditanam karena telah terjadi penurunan viabilitas walaupun
kondisi penyimpanan dilakukan secara ideal.
Benih merupakan benda hidup, yang di dalamnya terdapat berbagai
komponen kimiawi seperti karbohidrat, lemak, protein, air, dan substansi lain
(Sudjindro 1994). Menurut Copeland dan McDonald (1995), secara kimia di
dalam benih berisi cadangan makanan dan substansi yang berpengaruh terhadap
perkecambahan benih.
Masuknya air dan oksigen ke dalam benih tidak selalu diikuti oleh proses
pertumbuhan. Perombakan bahan cadangan dapat terjadi tetapi energi yang
dihasilkan tidak dimanfaatkan untuk proses translokasi sintesa melainkan
terbuang sia-sia sehingga terjadi kemunduran benih dalam kurun waktu
penyimpanan (Sadjad 1994).
Kemunduran Benih
Kemunduran benih adalah mundurnya mutu fisiologi benih yang dapat
menimbulkan perubahan menyeluruh di dalam benih baik fisik, fisiologis maupun
biokimia (Sadjad 1972; Kapoor
et al
. 2011) yang dapat menurunkan viabilitas
(Sadjad 1972; Kapoor
et al.
2011), vigor (Kapoor
et al.
2011), kapasitas hidup,
kekuatan tumbuh dan daya berkecambah yang akhirnya benih menjadi mati
(Sadjad 1972).
Benih dengan tingkat kemunduran masing-masing dapat dicerminkan dari
nilai uji viabilitas (Sadjad 1972). Salah satu kriteria terjadinya kemunduran yang
telah diakui secara luas adalah menurunnya daya berkecambah (Kapoor
et al
.
2011).
Kecepatan kemunduran dipengaruhi oleh kadar air dan suhu selama
penyimpanan, peningkatan kadar air dan suhu dapat mempercepat proses
kemunduran benih (Kapoor
et al
. 2011).
(2011) menerangkan bahwa kerusakan membran sel adalah salah satu penyebab
dari kemunduran benih.
Membran sel terdiri dari
lipid bilayer
(fosfolipid) yang mengandung protein.
Sangat banyak asam lemak yang tergabung pada struktur lipid membran yaitu
asam lemak jenuh (palmitat dan stearat) dan asam lemak tak jenuh (oleat, linoleat,
linolenat).
Lipid bilayer
berfungsi sebagai penyangga seluruh proses keluar
masuknya material dari dalam maupun keluar sel (Bewley 1986).
Benih yang memiliki kadar air tinggi, diatas 14%, akan mengalami
peroksidasi lemak akibat aktifitas enzim lipoksigenase dan menghasilkan radikal
bebas. Radikal bebas akan merusak lemak membran sehingga permeabilitasnya
meningkat. Peningkatan permeabilitas tersebut erat hubungannya dengan
kemunduran benih. Selain itu pada kadar air yang tinggi pospolipid akan
mengalami hidrolisis yang menghasilkan gliserol dan asam lemak bebas.
Akumulasi asam lemak bebas yang terus-menerus mengakibatkan penurunan pH
seluler, lebih lanjut akan merusak enzim dan menurunkan aktifitasnya (Copeland
dan McDonald 1995).
Radikal bebas yang terbentuk akibat peroksidasi lemak tidak hanya
menyerang komponen lemak membran, tetapi juga menyerang struktur protein
benih (Copeland dan McDonald 1995). Robert (1972) juga menyatakan bahwa
penurunan viabilitas disebabkan adanya denaturasi protein yang terjadi pada asam
nukleat yang dapat menyebabkan kerusakan inti sel sehingga mempengaruhi
fungsi sel secara menyeluruh. Selain itu terjadi juga denaturasi lipoprotein
membran yang menyebabkan menurunya integritas membran, serta rusaknya
protein enzim yang menyebabkan menurunya reaksi biologis pada saat benih
dikecambahkan.
Pengusangan Cepat (
Rapid Aging
)
Sadjad (1972) menyebutkan
rapid aging method
e digunakan dalam
mengukur daya simpan benih dengan memberikan kondisi suhu dan kelembaban
yang tinggi kepada benih untuk terjadi proses kemunduran secara buatan.
Kecepatan kehilangan vigor selama penyimpanan dipengaruhi oleh faktor
lingkungan seperti suhu, kelembaban dan konsentrasi O
2atau CO
2. Harington
(1972) menyebutkan bahwa setiap penurunan kadar air 1% atau penurunan suhu 5
o
C dari kondisi penyimpanan normal dapat memperpanjang masa simpan benih
menjadi duakalinya.
Gholami dan Golpayegani (2011) mengasumsikan bahwa benih mengalami
kemunduran 500 kali lebih cepat pada suhu 40
oC dengan kadar air 18% bila
dibandingkan pada kondisi suhu 20
oC dengan kadar air 8%. Oleh karena itu
pengusangan cepat dapat dikembangkan sebagai suatu teknik pengusangan
tersendiri. Untuk mempelajari perubahan fisiologi dan biokimia yang terjadi pada
kemunduran benih, pengusangan cepat telah banyak digunakan. Pada
pengusangan cepat, benih mengalami kemunduran dengan sendirinya dengan
penggunaan kelembaban dan suhu tinggi
(> 90%
, ≥
40 ºC).
Kapoor
et al
. (2011) melaporkan bahwa penggunaan pengusangan cepat 45
o
C dan RH 100% pada padi selama 96 jam memperlihatkan adanya penurunan
daya berkecambah, kandungan gula, dan kadar protein terlarut serta peningkatan
kadar air benih. Sementara itu dengan perlakuan yang sama selama 5 hari
Gholami dan Golpayegani (2011) melaporkan terjadi penurunan daya
berkecambah dan penurunan aktifitas peroxidase serta peningkatan kadar asam
lemak bebas dan kebocoran ion.
Dari data hasil penelitian yang dilakukan oleh Cutrisni (2011) yang
melakukan pengusangan cepat menggunakan suhu 45
oC dan RH 100% terhadap 2
varietas dan 3 genotipe padi sawah dapat ditentukan hubungan antara lama waktu
pengusangan dengan rata-rata daya berkecambah benih yang memenuhi
persamaan :
DB = 0.0008056t
2- 0.714t + 87.11
dimana DB adalah daya berkecambah (%) dan t adalah lama waktu pengusangan
(jam)
Komposisi Benih Padi
Benih padi terdiri dari beras dan sekam. Bagian beras terdiri dari 90.4-
90.6% endosperm, 0.8
–
1.1 embrio%, 2.0-2.1% skutellum, serta perikarp, testa,
dan aleuron 6.5%. Komposisi kimia utama beras pecah kulit adalah karbohidrat
disamping senyawa-senyawa lain seperti protein, lemak, abu dan serat kasar
(Saenong
et a.l
1989). Komposisi kimia beras dapat dilihat pada Tabel 1.
Sementara sekam menempati 18-28% dari benih (Juliano 1972) dengan komposisi
seperti
Tabel
2
.
Tabel 1 Komposisi kimia beras pecah kulit (
brown rice
)
Komponen
Persentase
Karbohidrat
84.83
Protein
9.78
Lemak
2.20
Abu (mineral)
2.09
Serat Kasar
1.10
Sumber : Leonard dan Martin (1963)
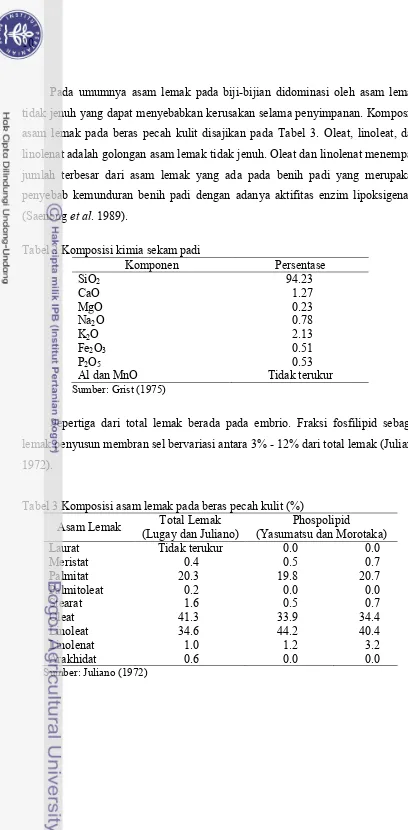
Pada umumnya asam lemak pada biji-bijian didominasi oleh asam lemak
tidak jenuh yang dapat menyebabkan kerusakan selama penyimpanan. Komposisi
asam lemak pada beras pecah kulit disajikan pada Tabel 3. Oleat, linoleat, dan
linolenat adalah golongan asam lemak tidak jenuh. Oleat dan linolenat menempati
jumlah terbesar dari asam lemak yang ada pada benih padi yang merupakan
penyebab kemunduran benih padi dengan adanya aktifitas enzim lipoksigenase
(Saenong
et al
. 1989).
Tabel 2 Komposisi kimia sekam padi
Komponen
Persentase
SiO
294.23
CaO
1.27
MgO
0.23
Na
2O
0.78
K
2O
2.13
Fe
2O
30.51
P
2O
50.53
Al dan MnO
Tidak terukur
Sumber: Grist (1975)
Sepertiga dari total lemak berada pada embrio. Fraksi fosfilipid sebagai
lemak penyusun membran sel bervariasi antara 3% - 12% dari total lemak (Juliano
1972).
Tabel 3 Komposisi asam lemak pada beras pecah kulit (%)
Asam Lemak
Total Lemak
(Lugay dan Juliano)
Phospolipid
(Yasumatsu dan Morotaka)
Laurat
Tidak terukur
0.0
0.0
Meristat
0.4
0.5
0.7
Palmitat
20.3
19.8
20.7
Palmitoleat
0.2
0.0
0.0
Stearat
1.6
0.5
0.7
Oleat
41.3
33.9
34.4
Linoleat
34.6
44.2
40.4
Linolenat
1.0
1.2
3.2
Arakhidat
0.6
0.0
0.0
Near Infrared Spectroscopy
Near Infrared
merupakan gelombang elektromagnetik di antara gelombang
tampak dan gelombang
infrared
dengan kisaran panjang gelombang antara 750 -
2600 nm (Murray & Williams 1990).
Semua bahan organik terdiri dari atom-atom, terutama karbon, oksigen,
hidrogen, nitrogen, pospor dan sulfur. Atom-atom tersebut terikat secara kovalen
dan elektrovalen membentuk molekul. Ketika molekul-molekul tersebut mendapat
energi radiasi dari luar, maka molekul-molekul tersebut mengalami perubahan
energi potensial. Molekul-molekul akan bergetar pada frekuensi yang sebanding
dengan panjang gelombang tertentu pada zona
infrared
. Analisis spektra
Near
Infrared Reflectance
(NIR) merupakan suatu metode yang menggunakan dan
menginterpretasikan getaran-getaran tersebut kepada prosedur analisis yang
sederhana, cepat dan tidak menimbulkan limbah (Murray & Williams 1990).
Spektrum pantulan NIR dihasilkan karena ada korespondensi dengan
frekuensi vibrasi dari molekul-molekul yang ada dalam bahan organik yang
bersifat spesifik, sedangkan yang tidak berkorespondensi tidak memantulkan
gelombang
infrared
(Osborne
et al.
1993).
Muray dan Williams (1990) menerangkan bahwa radiasi elektromagnetik
dapat diekspresikan dalam batasan-batasan seperti frekuensi (f), panjang
gelombang ( ),
dan jumlah gelombang (v
1). Frekuensi dinyatakan dalam satuan
seperdetik yang menunjukkan jumlah gelombang secara lengkap yang terjadi
dalam satu unit waktu. Panjang gelombang adalah jarak dalam mikrometer atau
nanometer antara titik yang ekivalen pada gelombang secara berturut-turut.
Sedangkan jumlah gelombang adalah banyaknya gelombang dalam tiap satu
sentimeter rentetan gelombang yang ditulis sebagai resiprokal sentimeter.
Hubungan ketiga parameter tersebut dijelaskan sebagai berikut:
f = c
………..………(1)
v
1= 1/ ………...…………(2)
dimana:
f = frekuensi dalam siklus per detik (Hertz, Hz)
= panjang gelombang (m)
Untuk mempermudah dalam NIR spektroskopi frekuensi dinyatakan dalam
panjang gelombang dengan formula
(nm) = 10,000,000 / v1
(cm
-1)
……….(3)
Perbandingan antara intensitas energi datang (I) dengan energi yag terjadi
pada bahan (I
o) disebut
transmittance
(T)
T= I/I
o………(4)Berdasarkan hukum Beer/Lambert, jumlah intensitas yang diserap oleh
bahan atau
absorbance
(A)
Log
10(I
o/I) = log
10(I/T) = kcl = A
………(5)
Saat radiasi mengenai partikel-partikel sampel maka radiasi dipantulkan,
diserap atau diteruskan. Nilai yang terukur berupa nilai radiasi pantulan (reflektan,
R) yang dapat ditransformasikan kedalam radiasi yang diserap (absorban) dengan
persamaan:
A= log
10(1/R)
………(6)
[image:40.595.53.488.2.826.2]Komponen utama dari substansi organik adalah protein, karbohidrat, lemak,
air, mineral dan vitamin (Murray dan Williams 1990). Jordon menyatakan bahwa
NIR diaplikasikan untuk bahan bahan organik yang kaya dengan ikatan O-H
(seperti kadar air, karbohidrat, dan lemak), ikatan C-H (seperti bahan-bahan
organik turunan minyak bumi), dan ikatan N-H (seperti protein dan asam amino)
(Ruiz 2001). Beberapa panjang gelombang yang berhubungan dengan protein
disajikan pada Tabel 4.
Tabel 4 Panjang gelombang yang berhubungan dengan protein
Ikatan atom yang berasosiasi dengan Protein
Panjang
Gelombang
Kombinasi ikatan atom : N-H bend 2
ndovertone; Kombinasi
C-H stretch/C-O stretch; Kombinasi C=O stretch/N-C-H plane/C-N
stretch
2148-2200 nm
C=O carbonyl stretch 2
ndovertone dari amida primer (Amida I)
2030-2080 nm
C-H stretch aromatik 1
stovertone
1620-1700 nm
N-H stretch 1
stovertone
1480-1550 nm
N-H stretch 2
ndovertone
975-1015 nm
Pendugaan Viabilitas Benih Menggunakan NIR
Aplikasi
Near inrfrared
telah banyak digunakan dalam bidang petanian.
NIR dapat digunakan untuk mengklasifikasikan sampel benih dalam bentuk
bulk
maupun tunggal. Dalam spektra NIR juga mengandung informasi mengenai
karakter fisik benih seperti berat, ukuran dan
bulk density
. Selain itu NIR dapat
mengklasifikasikan viabilitas benih dalam kemunduran benih dan dapat
mengidentifikasi benih kosong. Selanjutnya NIR juga dapat digunakan dalam
membedakan beberapa varietas dari biji-bijian. Dalam perbenihan NIR juga dapat
digunakan dalam mengkuantifikasi kadar air dan kandungan kimia seperti protein
dan minyak (lemak). Penggunaan NIR juga telah mengarah kepada pembuatan
alat sortasi berdasarkan pada perbedaan karakteristik benih (Lestander 2003).
Penelitian yang dilakukan oleh Soltani (2003) menyimpulkan bahwa benih
beechnuts
(
Fagus orientalis
) viabel dapat dibedakan dari benih non-viabel dengan
menggunakan NIR yang dianalisa dengan PLS dan menunjukkan error yang
rendah. Pada benih viabel ditemukan bahwa terdapat kandungan protein yang
lebih tinggi dari yang tidak viabel karakteristik ini ditunjukkan oleh puncak
gelombang pada 1722 nm dan 2110 nm.
Olesen
et al.
(2011) telah melakukan penelitian penggunaan NIR dalam
penentuan viabilitas benih bayam (
Spinacia oleracea
L.) secara individu dengan
menggunakan
extended canonical variates analysis
(ECVA). Dari hasil
penelitiannya lemak berperan dalam pengusangan dan perkecambahan. Pada
Pengusangan cepat
lipid peroksidasi
menyebabkan kerusakan pada membran sel
dan berkontribusi dalam penurunan viabilitas benih. Perubahan kimia tersebut
menyebabkan pemisahan yang jelas antara benih yang diusangkan dengan benih
yang tidak diusangkan. Perbedaan tersebut disebabkan adanya perbedaan dalam
penyerapan golombang pada struktur CH
2, CH
3and HC=CH yang merupakan
Jaringan Saraf Tiruan
Jaringan saraf tiruan (JST) adalah sistem pemroses informasi yang memiliki
karakteristik seperti jaringan saraf biologis. Jaringan saraf yang saling
berhubungan ini memiliki kemampuan untuk merespon setiap masukan yang
diberikan dan dapat mempelajari, mengadaptasi setiap kondisi lingkungan yang
diberikan (Peterson 1995).
Fungsi utama dari saraf biologi adalah menghasilkan keluaran berdasarkan
jumlah dari perkalian sinyal antar neuron dengan karateristik fungsi
pseudostep
.
Fungsi kedua neuron adalah untuk mengubah laju transmisi pada sinapsis untuk
optimasi jaringan secara keseluruhan. Model jaringan saraf tiruan menirukan
perkalian input-input dan satu output, penggantian fungsi hubungan input-output
dan pembobot sinapsis yang adaptif (Takagi 1997).
JST pada dasarnya digunakan untuk model yang tidak linear, JST sangat
baik digunakan sebagai alat untuk melakukan analisa karena mempunyai
algoritma yang fleksibel, bisa dilatih dengan cepat dan toleran terhadap
error
yang besar. Berbagai kelebihan yang ditawarkan oleh JST membuat permodelan
ini banyak digunakan dalam berbagai aplikasi (Mardison 2010).
Cara kerja JST adalah dengan menjumlahkan seluruh masukan setelah
diberi suatu pembobot dan memasukan hasil penjumlahan ini dalam suatu fungsi
aktifasi yang berfungsi untuk mengubah suatu nilai yang tidak terbatas menjadi
nilai yang terbatas atau dikenal dengan fungsi pemampat. Untuk mendapatkan
kemampuan noda yang lebih tinggi maka dirangkaikan beberapa buah noda
mengikuti konfigurasi seri paralel membentuk JST. Noda-noda lapisan input tidak
melakukan perhitungan tapi hanya mendistribusikan masukan (Andrianyta 2006).
Peterson (1995), mengklasifikasikan JST berdasarkan strategi pelatihan atas tiga
kelas yaitu:
1.
Pelatihan terawasi, setiap contoh diberi nilai input dan target, nilai output
hasil perhitungan selama proses pelatihan dibandingkan dengan nilai target
untuk menentukan besarnya galat
2.
Pelatihan
reinforcement
, nilai target tidak diberikan, hanya diberikan indikasi
apakah nilai output JST sudah benar atau salah dan tugas JST adalah
memperbaiki kinerja jaringan
3.
Pelatihan tak terawasi, sampel hanya diberi nilai input, tanpa nilai target,
sistem harus menemukan dan beradaptasi dengan perbedaan dan persamaan
dalam nilai input yang diberikan.
Pelatihan
backpropagation
meliputi 3 fase. Fase pertama adalah fase maju.
Pola masukan dihitung maju mulai dari layar masukan hingga layar keluaran
menggunakan fungsi aktifasi yang ditentukan. Fase kedua adalah fase mundur.
Selisih antara keluaran jaringan dengan target yang diiinginkan merupakan
kesalahan yang terjadi. Kesalahan tersebut dipropogasikan mundur, dimulai dari
yang berhubungan langsung dengan unit keluaran. Fase ketiga adalah modifikasi
bobot untuk menurunkan kesalahan (Siang 2005).
Algortima pelatihan
backpropagation
dengan satu layar tersembunyi yang
menggunakan fungsi aktivasi sigmoid biner diterangkan sebagai berikut (Siang
2005):
Langkah 0
Inisialisasi semua bobot dengan bilangan acak kecil.
Langkah 1
Jika kondisi pelatihan belum terpenuhi, dilakukan langkah 2
–
9.
Langkah 2
Untuk setiap pasang data pelatihan, dilakukan langkah 3
–
8
Fase I : Propogasi maju
Langkah 3
Langkah 4
Hitung semua keluaran di unit tersembunyi z
j(j = 1, 2,…,p)
………...(7)
………..(8)
Langkah 5
Hitung semua keluaran jaringan di unit y
k(k = 1, 2, …, m)
………..(λ)
………(10)
Fase II : Propogasi Mundur
Langkah 6
Hitung fak
tor δ unit keluaran berdasarkan kesalahan
di setiap unit keluaran
y
k(k = 1, 2, …, m)
……….(11)
δk
merupakan unit kesalahan yang akan digunakan dalam perubahan bobot
layar
sebelumnya (Langkah 7)
Hitung suku perubahan bobot w
kj(yang akan digunakan dalam merubah
bobot w
kj) dengan laju percepatan α∆
w
kj= α δk
z
j(
k = 1, 2, …, m ; j = 0, 1, …, p
)
……….(12)
Langkah 7
Hitung fak
tor δ unit tersembunyi berdasarkan kesalahan disetiap unit
tersembunyi z
j(j = 1,
2, …,p)
………(13)
Faktor
δ unit tersembunyi μ
……….(14)
Hitung suku perubahan bobot v
jk(yang akan digunakan untuk merubah
bobot v
jk)
∆
v
ji= α δj
x
i(
j = 1, 2, …, p ; i = 0, 1, …, n
)
……….(15)
Fase III : Perubabahan bobot
Langkah 8
Hitung semua perubahan bobot
Perubahan bobot yang menuju ke unit keluaran :
Perubahan bobot yang menuju ke unit tersembunyi :
v
ji(baru) = v
ji(lama) + ∆ vji j
;(
j = 1,2,…,p ; i = 0,1,…,n)………(17)
Langkah 9
Uji kondisi pemberhentian (akhir iterasi).
Setelah selesai pelatihan, jaringan dapat digunakan untuk mengenali pola
dimana hanya propogasi maju (langkah 4 dan 5) saja yang digunakan untuk
menetukan keluaran jaringan.
Laju pelatihan dan momentum diperlukan dalam JST untuk mencapai
kondisi optimal. Kondisi yang diinginkan dari suatu JST adalah galat yang kecil
hingga mencapai minimum global bukan minimum lokal. Peterson (1995)
menyatakan bahwa
koefisien laju pelatihan η dalam
delta rule
secara umum
menentukan ukuran penyesuaian pembobot yang dibuat pada tiap-tiap iterasi dan
itu mempengaruhi laju konvergensi. Apabila pemilihan laju pelatihan terlalu besar
maka untuk mencapai konvergensi akan lebih lambat daripada penurunan error
langsung. Sebaliknya laju pelatihan terlalu kecil penurunan error akan maju sangat
kecil sehingga butuh waktu yang lama untuk mencapai konvergensi.
Untuk memperbaiki laju konvergensi dapat juga dilakukan dengan cara
menambahkan
momentum.
Penambahan
momentum
dapat
membantu
menghaluskan penurunan eror dengan mencegah perubahan ekstrim gradien
karena anomali lokal (Peterson 1995). Burks
et al.
(2000) melaporkan bahwa nilai
koefisien laju pelatihan dan momentum mempengaruhi akurasi
backpropagation
training
. Kisaran nilai momentum yang digunakan adalah 0.8-0.95 sedangkan
nilai laju pelatihan berkisar antara 0.001-0.200.
Penggunaan JST sebagai alat pengolah data spektra NIR telah banyak
digunakan dalam bidang pertanian. Senduk (2002) menggunakan kombinasi
masukan 5, 10 dan 15 komponen utama spektra NIR dengan lapisan tersembunyi
4, 6, 8, 10, dan 12 unit menghasilkan RMSE 0.0077 sampai 0.00073 untuk
menduga tingkat kematangan dan ketuaan sawo.
kombinasi 5, 10, 15, dan 20 unit. Arsitektur JST terbaik yang diperoleh adalah
20-10-3 dengan nilai RMSEP 3.718%, 1.314% dan 1.989% untuk kadar minyak,
asam lemak bebas dan kadar air. Sedangkan nilai koefisien korelasinya
berturut-turut adalah 0.848, 0.872, dan 0.993.
Shao
et al.
(2007) melakukan pengukuran kandungan gula dan keasaman
pada
yogurt
menggunakan VIS/NIR. Dari hasil penelitiannya diketahui bahwa
penggunaan JST memberikan nilai koefisien determinasi R
2dan RMSEP lebih
baik dari PLS. Pada JST diperoleh R
2sebesar 0.92 dan 0.91, RMSEP sebesar 0.33
dan 0.04 masing-masing untuk kandungan gula dan keasaman. Sedangkan pada
PLS diperoleh R
2sebesar 0.91 dan 0.90, RMSEP sebesar 0.36 dan 0.04.
Liu
et al.
(2010) melakukan pengukuran total padatan terlarut buah jeruk
menggunakan NIR dan membandingkan model pendugaan antara PLS dan
principal component analysis-backpropagation neural network
(PCA-BPNN).
Dari hasil penelitian diperoleh model terbaik adalah PCA-BPNN dengan nilai
korelasi pendugaan 0.90-0.91 dan RMSEP pendugaan 0.68-0.71.
Li
et al.
(2007) menentukan varietas
bayberry
cina secara nondestruktif
menggunakan visible/NIR dan
principal component analysis-artificial neural
network
(PCA-ANN). Dari hasil penelitian, JST dengan arsitektur 20-24-1 dapat
menentukan 95% dengan benar.
Analisis Komponen Utama
Analisis komponen utama (
Principal Component Analysis
, PCA)
merupakan suatu teknik mereduksi data multivariat (banyak data) menjadi suatu
set kombinasi linear yang lebih sedikit akan tetapi menyerap sebagian besar
jumlah varian dari data awal. Tujuan utamanya adalah menjelaskan sebanyak
mungkin jumlah varian data asli dengan sedikit mungkin komponen utama yang
mencakup sebagian besar informasi dari data asli (Supranto 2004).
Misalkan sebuah vektor data berdimensi n dituliskan dengan matriks X
pxndimana p adalah contoh ke-p dan n adalah variable ke-n, analisis komponen utama
bertujuan untuk mendapatkan sebuah vektor yang berdimensi m, dimana m<n
sehingga vektor berdimensi m mencakup seluruh variasi data. Untuk
mendapatkannya, vektor berdimensi n diproyeksikan kedalam vektor m dengan
memilih setiap komponen utama dalam arah maksimum, akan tetapi
komponen-komponen utama tersebut saling tegak lurus (Paterson 1995).
Algoritma analisis koponen utama (Peterson 1995) adalah:
1.
Komponen utama pertama dipilih dalam arah variasi maksimum
y
1 =Xw
1...(18)
dimana y
1dan w
1merupakan vektor kolom
Nilai ini harus dibatasi karena variasi data dapat dibuat semakin besar dengan
cara menaikan w
1. Pembatasan ini dilakukan dengan cara
w
1ꞌw
1= Σi
w
i12= 1
………
(19)
dimana w
1ꞌ= vektor
transpose
dari w
12.
Jumlah kuadrat y
1dimaksimumkan
y
1ꞌy
1= w
1ꞌXꞌXw1……….
……….
(20)
Untuk memaksimumkan persamaan diatas digunakan metode Lagrange.
Fungsi komposit L dibentuk dengan penggunakan persamaan (19) dan (20)
sehingga
L = w
1ꞌXꞌXw1 – 1(w
1ꞌw
1–
1)
………
.
…
(21)
Dimana
1merupakan
multiplier
Lagrange, sedangkan nilai L maksimum
diperoleh dari turunan partial terhadap w
1sama dengan nol
∂L/∂w1 = 2 XꞌXw1
–
2
1w
1………...(22)
XꞌXw1 = 1
w
1………..
…..
(23)
Dari persamaan (20) dan (23) diperoleh
y
1ꞌy
1= w
1ꞌ 1w
1 = 1w
1ꞌc w
1=
1...(24)
Solusi y
1merupakan komponen utama pertama dengan variasi maksimum
1dimana
1juga merupakan nilai eigen
XꞌX
3.
Untuk memperoleh komponen utama y
2, prosedur untuk mendapatkan y
1digunakan, tetapi y
2tegak lurus terhadap y
1sehingga
4.
Jumlah kuadrat y
2pada persamaan (25) dimaksimumkan dengan dua fungsi
kendala berikut
w
2ꞌw
2= 1 dan w
1ꞌw
2= 0
……….
(26)
Fungsi komposit Lagrange untuk memaksimalkan persamaan (25) dengan
fungsi kendala persamaan (25) adalah
L = w
2ꞌXꞌXw2 – 2(w
2ꞌw
2–
1) -
w1ꞌ
w
2………..…(27)
Dimana
2dan merupakan
multiplier
Lagrangian
Turunan partial terhadap w
2sama dengan nol dilakukan seperti proses
sebelumnya sehingga :
= 2w1ꞌXꞌXw2 = 2 x 0 = 0 dan XꞌXw2 =
2w
2...(28)
5.
Dengan melanjutkan proses tersebut diatas, nilai eigen
1, 2,
3… pyang
berhubungan dengan matriks orthogonal (tegak lurus) W =[ w
1, w
2, w
3… wp]
dimana p komponen utama dari X didapatkan dari matriks Y=XW dan
matriks
YꞌY= WꞌXꞌXW =
Λ =
m
erupakan matriks diagonal. Karena Λ merup
akan matriks diagonal maka
komponen-komponen utama yang diekstrak dari variabel asal saling tegak
lurus atau tidak berkorelasi satu sama lain.
6.
Total variasi X dapat dijelaskan sebagai berikut :
Σx1
2+ Σx2
2+ … + Σxp
2= Trace (XꞌX) = Trace (WꞌXꞌXW) =
………..…
(29)
7.
Proporsi variasi komponen utama ke-j dari X dihitung dengan persamaaan
berikut :
Proporsi variasi =
………
...(30)
8.
Kumulatif variasi X dengan menggunakan komponen utama ke-m didapatkan
dengan menjumlahkan nilai eigen ke-m dibagi dengan total variasi X sebagai
berikut :
Waktu dan Tempat
Penelitian dilakukan pada bulan Maret
–
Agustus 2012 di Laboratorium
Teknik Pengolahan Pangan dan Hasil Pertanian (TPPHP), Laboratorium Ilmu
Teknologi Benih, dan Laboratorium Analisis Tanaman, Institut Pertanian Bogor.
Alat dan Bahan
Bahan yang digunakan dalam penelitian adalah benih padi sawah varietas
Ciherang yang diperoleh dari Balai Besar Penelitian Tanaman Padi Sukamandi,
yang dipanen pada bulan Februari 2012. Bahan lainnya adalah kertas saring kasar
dengan berat spesifik 5 mg/cm
2berukuran 60 x 60 cm yang dibagi 12 dengan
ukuran 10 x 30 cm, kantung plastik LLDPE ukuran 14 x 35 cm, kantung strimin,
dan dithane 2gr/liter.
Bahan untuk pengukuran protein terlarut adalah reagent A (7 mM K-Na
Tartrate.4H
2O (Garam Rochelle), 0.81 M Na
2CO
3dalam 500 ml NaOH 1 N, H
2O
sampai 1 l), reagent B (70 mM K-Na Tartrate.4H
2O, 40 mM CuSO4.5H
2O dalam
10 ml NaOH 1 N, H
2O sampai 100 ml), reagent C (1 ml Folin-Ciocalteau
dilarutkan dengan 15 ml H
2O), buffer phosphat 0.1M pH 7.5, TCA 10%, NaOH
0.01N dan larutan standar BSA (Bouvine Serum Albumine). Bahan untuk
penentuan kadar asam lemak bebas adalah chloroform, kertas thimble, NaOH 0.01
N, dan Indikator Indikator fenolftalein (PP) 5%
Alat yang digunakan adalah NIR spectroscopy NIRFlex N-500 produksi
BUCHI, komputer,
environmental chamber
KCL-2000W produksi Eyela,
chamber
plastik dengan diameter atas 29.3 cm, diameter bawah 25.5 cm dan
tinggi 28 cm, petridish berdiameter 9 cm dan tinggi 2 cm, alat pengecambah benih
(germinator) tipe IPB 73-2A/B, oven, dan timbangan digital.
Alat yang digunakan untuk penentuan protein terlarut adalah mortar dan
pestle, pipet Mohr volumetrik, pipet mikro 100 µl, pipet mikro 1000 µl,
microtube
2 ml, tabung teaksi 10 ml,
waterbath, spektrofotometer,
timbangan digital 4 digit,
spatula, beaker glass, labu takar, pH-Meter, sentrifuge.
[image:50.595.39.488.31.782.2]Alat yang digunakan untuk penentuan asam lemak bebas adalah blender,
pipet Mohr volumetrik, pipet mikro 100 µl, timbangan digital, spatula, labu takar,
buret, perangkat ekstraksi soxhlet Buchi E-816, magnetic stirrer.
Gambar 2
Near Infrared Spectroscopy
Gambar 3
Environmen-
tal chamber
Prosedur Penelitian
Persiapan Sampel
Sampel benih padi dibersihkan lalu ditimbang sebanyak 480 gram (12
sampel @ 40 gram) untuk satu taraf lama waktu pengusangan, selanjutnya sampel
direndam dalam 1 liter larutan
dithane
dengan dosis 2 gr/liter selama 15 menit
kemudian dibilas satu kali dengan 1 liter aqudes. Setelah itu sampel ditiriskan dan
dikeringanginkan selama 3 jam pada ruangan ber-AC dengan suhu 25
oC.
Selanjutnya benih dibagi menjadi 12 unit sampel dan dimasukkan ke dalam
kantung streamin (Gambar 6).
Selanjutnya sampel benih diusangkan pada suhu 45
oC dan RH > 90%
dengan taraf waktu 0, 2, 4, 6, dan 8 hari. Sebelum benih diusangkan, terlebih
dahulu dilakukan persiapan alat pengusangan. Air bersuhu 50
oC dimasukan ke
dalam
chamber
plastik, selanjutnya rak dipasang dan sampel disusun sedemikian
rupa (Gambar 7) agar sampel tidak bertumpuk.
Chamber
plastik terdiri dari 4
tingkat rak dimana setiap rak memuat 3 sampel. Selanjutnya termometer dan RH
meter dimasukan kedalam
chamber
plastik dan disusun sedemikian rupa agar alat
tersebut tidak mengenai sampel dan skala pembacaan dapat terlihat dari luar. Pada
bagian bawah tutup
chamber
diberi kain kanebo/chemois lembab (Gambar 8) agar
sampel tidak terkena tetesan air kondesat. Setelah suhu air dalam
chamber
plastik
mencapai 45
oC
chamber
plastik ditutup dengan rapat.
Bersamaan dengan persiapan sampel,
environmental chamber
diset pada
suhu 45
oC dan ditunggu hingga stabil. Setelah persiapan sampel selesai dan suhu
stabil,
chamber
plastik dimasukkan ke dalam
environmental chamber
(Gambar
11) dan waktu pengusangan dimulai. Bagan alir persiapan sampel dapat dilihat
pada Gambar 9 dan pengambilan sampel dapat dilihat pada Gambar 10.
Gambar 6 Benih di dalam
kantung strimin
Gambar 7 Sampel dalam
chamber
plastik
Gambar 9 Bagan alir persiapan sampel
Benih ditimbang 40g x 12/taraf waktu pengusangan
Benih direndam dalam larutan dithane 15 menit
Larutan dithane 2 g/liter (1 liter air + 2 g
dithane)
Benih dibilas dalam aquades 1 liter (1 kali pembilasan)
Benih ditiriskan dan dikeringanginkan selama 3
jam pada suhu ruang
Benih dibagi menjadi 12 sampel dan dimasukan ke
kantung strimin Benih dibersihkan dari
gabah hampa, gabah pecah dan kotoran
EC diset pada 45 o
C dan ditunggu hingga stabil
Cember plastik dimasukkan ke
dalam EC
Waktu pengusangan dimulai dan proses dilakukan untuk setiap pengusangan 2, 4, 6 dan 8 hari 2 liter air bersuhu 50
o
C dimasukkan ke dalam chamber plastik
Sampel dimasukan ke chember
plastik, diletakkan diatas rak (3 sampel/rak)
Bagian paling atas rak diberi kain chemois
/kanebo lembab
Setelah suhu air mencapai 45 o C,
chamber plastik ditutup rapat
Termometer dan RH meter dimasukkan ke
chamber plastik
Environmental chamber (EC) dinyalakan
Sampel benih yang telah diusangkan Sampel benih tidak
diusangkan/kontrol (pengusangan 0 hari)
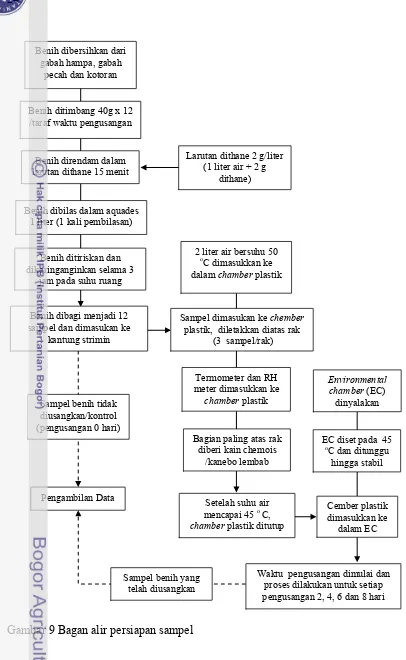
Gambar 10 Bagan alir pengambilan data
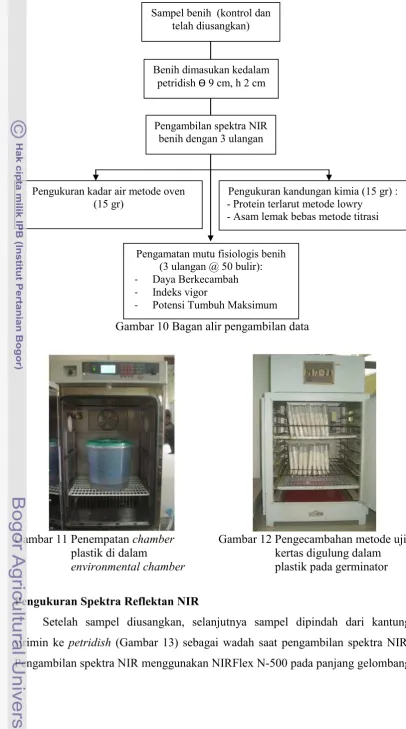
Gambar 11 Penempatan
chamber
plastik di dalam
environmental chamber
Gambar 12 Pengecambahan metode uji
kertas digulung dalam
plastik pada germinator
Pengukuran Spektra Reflektan NIR
Setelah sampel diusangkan, selanjutnya sampel dipindah dari kantung
strimin ke
petridish
(Gambar 13) sebagai wadah saat pengambilan spektra NIR.
Pengambilan spektra NIR menggunakan NIRFlex N-500 pada panjang gelombang
Sampel benih (kontrol dan
telah diusangkan)
Benih dimasukan kedalam
petridish
Ѳ
9 cm, h 2 cm
Pengambilan spektra NIR
benih dengan 3 ulangan
Pengukuran kadar air metode oven
(15 gr)
Pengukuran kandungan kimia (15 gr) :
- Protein terlarut metode lowry
- Asam lemak bebas metode titrasi
Pengamatan mutu fisiologis benih
(3 ulangan @ 50 bulir):
-
Daya Berkecambah
-
Indeks vigor
1000
–
2500 nm sebanyak 3 kali (3 kali scan) pada posisi berbeda sehingga
jumlah spektra yang dihasilkan dari 60 sampel sebanyak 180 spektra.
Selama proses pengambilan data reflektan, tempat sampel akan berputar
360
osearah jarum jam kemudian berputar kearah berlawanan sejauh 360
oberhenti
di tempat semula menandakan pengambilan data selesai. Mekanisme pengambilan
data reflektan dapat dilihat pada Gambar 14.
Sampel benih padi berbentuk granular yang heterogen sehingga dalam
pengambilan data spektra reflektan akan terjadi bias karena adanya efek
scattering
.
Gambar 13 Penempatan sampel pada petridish dan NIRFlex saat pengambilan
spektra
1 Detektor
2 Sensor magnet
3 Tombol start
4 Tombol stop
5 Refrensi internal
6
Coding
magnet
8 Sampel
9 Petridish
10 Dudukan
petridish
11 Bidang berputar
12 Motor
[image:54.595.56.487.26.814.2]13,17 Lensa
14 Penahan cahaya
15,16 Cermin
Data tersimpan ke komputer dan disajikan dalam bentuk grafik spektra dan
tabel, selanjutnya diubah ke dalam format Microsoft Excel. Data diolah lebih
lanjut untuk penentuan komponen utama dengan
principal component analysis
(PCA) menggunakan
software
SPSS Statistic 19. Komponen utama akan
digunakan sebagai input pada pembangunan model JST.
Pengujian Viabilitas Benih
Sampel yang telah diambil data spektranya kemudian diuji daya
berkecambahnya. Dari setiap unit sampel diambil contoh uji sebanyak 50 bulir
sebanyak 3 ulangan. Benih dikecambahkan menggunakan metode uji kertas
digulung dalam plastik. Kertas yang digunakan sebagai media pengecambahan
adalah kertas saring segi empat dengan ukuran 10 x 30 cm.
Kertas saring direndam dalam air, setelah lembab diangkat dan ditiriskan
hingga air tidak menetes lagi. Benih padi sebanyak 25 bulir ditanam diatas 2
lembar media kertas saring yang dibawahnya dilapisi plastik. Setelah benih
ditanam, kemudian ditutup dengan 2 lembar kertas saring lembab kemudian
digulung. Gulungan diletakan dalam alat germinator tipe IPB 73-2A/B (Gambar
12). Pengamatan terhadap kecambah normal, abnormal dan mati dilakukan pada
hari kelima dan ketujuh setelah tanam.
1.
Daya berkecambah (DB) :
………(32)
dimana:
∑ KN I
=
Jumlah kecambah normal pada hari kelima setelah
dikecambahkan.
∑ KN II
=
Jumlah kecambah normal pada hari ketujuh setelah
dikecambahkan.
Kriteria kecambah normal mengacu pada SNI 01-6233.1 (2003)
2.
Indeks Vigor (IV)
Pengamatan IV dilakukan terhadap jumlah kecambah normal pada hitungan
pertama yaitu pada hari ke-5.
……….……..(33)
(%) =
�
+
��
�ℎ
�
�
× 100%
��
(%) =
�
∑ KN I
=
Jumlah kecambah normal pada hari kelima setelah
dikecambahkan.
Kriteria kecambah normal mengacu pada SNI 01-6233.1 (2003)
3.
Potensi Tumbuh Maksimum (PTM)
PTM dihitung berdasarkan persentase jumlah benih yang tumbuh dengan
kriteria minimal tumbuh radikula pada akhir pengamatan yaitu pada hari ke
tujuh
………...…………(34)
∑ KN
=
Jumlah kecambah normal
∑ KAN
=
Jumlah kecambah abnormal
Kriteria kecambah normal & abnormal mengacu pada SNI 01-6233.1 (2003)
Pengukuran Kadar Air (KA)
Penetapan kadar air, dilakukan dengan metode langsung yaitu menggunakan
metode oven bersuhu tinggi pada suhu 130
oC selama 2 jam (ISTA 2010), dimana
sebelumnya benih digrinder terlebih dahulu untuk memperkecil luas permukaan
sehingga penetapan kadar air benih lebih akurat. Benih yang digunakan sebanyak
± 5 gr dengan 3 kali ulangan. Rumus menghitung kadar air :
………...…(35)
keterangan:
M1 = berat cawan (gram)
M2 = berat cawan + benih sebelum dioven (gram)
M3 = berat cawan + benih setelah dioven (gram)
Pengukuran Kadar Protein Terlarut
Penentuan kadar protein terlarut (P) dilakukan dengan metode lowry.
Sebanyak 5 g benih dihaluskan, kemudian ditimbang 0.1 g bahan halus dan
dimasukan kedalam mikrotube. Selanjutnya ditambahkan 2 ml buffer phosphate
ke dalam mikrotube kemudian disentrifuge 4500 rcf selama 10 menit. Supernatan
diambil menggunakan pipet sebanyak 100 µl dan dimasukan kedalam tabung
reaksi dan ditambahkan TCA 10% kemudian disentrifuge 4500 rcf selama 10
�
(%) =
+
�ℎ
�
�
× 100%
=
2
3
menit. Supernatan dibuang dan kedalam residu ditambahkan 1000 µl 0.01 N
NaOH. Reagent A ditambahkan sebanyak 900 µl dan dipanaskan didalam
waterbath
pada suhu 50
OC selama 10 menit. Setelah didinginkan, kedalam
tabung ditambahkan 100 µl reagen B dan 3 ml reagen C kemudian dipanaskan
didalam
waterbath
pada suhu 50
OC selama 10 menit. Setelah selesai, diukur
menggunakan spektrofotometer pada panjang gelomban 650 nm.
Selanjutnya dilakukan proses penambahan reagen A, B, dan C seperti
diatas terhadap larutan standar Boufin serum albumin (BSA) dengan konsentrasi
30, 40, 50, 100, 200 µg/l dan larutan standar BSA diukur menggunakan
spektrofotometer pada 650 nm. Kemudian dibandingkan larutan contoh terhadap
larutan standar berdasarkan pada persamaan kalibr