Irma Suraya 08 0405 001
Universitas Sumatera Utara
LAMPIRAN A
PERHITUNGAN NERACA MASSA
Basis perhitungan : 1 hari operasi
Kapasitas TBS : 45 ton/jam
Konversi TBS ke POME : 60 %(Novaviro Technology, 2010)
Maka, jumlah produksi POME = 60 % x 45 ton/jam = 27 ton/jam
=
tahun hari 300 hari jam 20 jam ton
27 x x
= 162.000 ton/tahun Jumlah kebutuhan POME =
hari 365
tahun 1 x tahun
ton 000 . 162
= 443,8356164 ton/hari = 443,8356164 m3/hari = 443.835,6164 L/hari Karakteristik POME :
COD input : 53000 mg/L ...(Senafati, 2010). % Dekomposisi COD : 65%...(Sompong dkk., 2007)
COD input :
hari .L 6164 , 835 . 443 L mg
53000 x
: 23.523,2877 kg/hari COD output : COD input – 0,65 x COD input
: 23.523,2877kg/hari – 0,65 x 23.523,2877kg/hari : 8.233,1507 kg/hari
COD terkonversi : 23.523,2877kg/hari – 8.233,1507kg/hari : 15.290,1370 kg/hari
Komposisi Biohidrogen, % Volume (Sompong dkk., 2007) 61 % H2
38,9915 % CO2
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Densitas masing-masing gas (Hysys) H2 = 0,0811 kg/m3
CO2 = 1,7780 kg/m3 H2S = 1,3790 kg/m3
Densitas campuran biohidrogen
ρcampuran = (%.ρ)H2 + (%.ρ)CO2 + (%.ρ) H2S
= (0,61.0,0811) + (0,389915 . 1,7780) + (0,000085. 1,3790) = 0,7429 kg/m3
A.1 Tangki Pre-treatment (M-103)
Fungsi: sebagai tempat menon-aktifkan bakteri yang memproduksi gas metana, sehingga produksi gas hidrogen yang dihasilkan lebih besar.
FC
1
3
J-106
L-104
C-105
2
3
M-103
TC
LCPKS memiliki komposisi 46,1% karbohidrat (C5H10O5)900, 11,2% protein dan 27,9% lipid (Yoshimasa, 2010). Namun pada rancangan ini perhitungan neraca massa LCPKS hanya dihitung sebagai komponen yang terbesar dalam LCPKS yaitu karbohidrat yang akan dihidrolisis menjadi glukosa dan dikonversikan menjadi biohidrogen.
NaOH yang diperlukan pada pre-treatment adalah 10% NaOH 1 M (Syafawati dkk.,2012)
Neraca massa komponen:
LCPKS : F1(C5H10O5)900 = 204.608,2192 kg/hari F1H2O = 239.227,3972 kg/hari F1 = 443.835,6164 kg/hari NaOH : F2NaOH =
1000gr kg mol
gr 40 1 , 0 hari
L 6164 , 835 . 443 %
Irma Suraya 08 0405 001
Universitas Sumatera Utara
= 1.775,3425 kg/hari Neraca massa total:
F1 = F2 + F3
F3= 443.835,6164 kg/hari – 1.775,3425 kg/hari F3= 445.610,9589 kg/hari
A.2 Tangki Pencampur (M-107)
Fungsi: sebagai tempat mencampur LCPKS dari Tangki Pre-Treatment dengan nutrisi.
Karakteristik LCPKS Rambutan (Yoshimasa,2010) : Fe yang terkandung dalam LCPKS = 70 mg/L
C : N : P = 350 : 5,4 : 0,4
Nutrisi yang diperlukan dalam fermentasi biohidrogen (Sompong dkk., 2007) : Fe2+ = 257 mg/L
C : N = 74 C : P = 559
Neraca massa komponen: FeCl2 :
FC
FC 3
6
TC J-112
4 5
J-106
M-107
1000000mg kg 1 hari
L 6164 , 835 . 443 L mg
70 x x
kg/hari 0685
Irma Suraya 08 0405 001
Universitas Sumatera Utara
F4FeCl2 = 82,9973kg/hari
mg 1000000
kg 1 hari
.L 6164 , 835 . 443 L mg
187 x x
Na2HPO4.2H2O : F5Na2HPO4.2H2O
Neraca Massa total : F3 + F4+ F5 = F6
445.610,9589 kg/hari + 82,9973kg/hari+ 15,1969 kg/hari = F6 F6 = 445.709,1531 kg/hari
A.3 Bioreaktor Hidrogen (R-201)
Fungsi : sebagai tempat berlangsungnya reaksi pembentukan hidrogen dengan menggunakan bakteri termofilik.
FC
FC
R-201
6
7
LI
TC
J-202
8
J-112
Kesetimbangan reaksi yang terjadi di dalam reaktor fermentasi : Reaksi:
(C5H10O5)900 + H2O 750 C6H12O6 (Barnali dkk.,2008) 750C6H12O6 + 500H2O(l) + H2S(l) 2000H2(g) + 500C2H4O2(l) +
500C4H8O2(l) + 1500CO2(g) + H2S(g) (Sompong dkk., 2009)
Neraca Massa Total : F6 = F7 + F8
F7 = COD terkonversi = 15.290,1370 kg/hari
mg 1000000
kg 1 hari
.L 6164 , 835 . 443 L mg
34,24 x x
Irma Suraya 08 0405 001
Universitas Sumatera Utara F8 = F6– F7
= 445.709,1531 kg/hari - 15.290,1370 kg/hari = 430.419,0161 kg/hari
Neraca Komponen : Alur 6
F6 = 445.709,1531 kg/hari F6(C5H10O5)900 = 204.608,2192 kg/hari F6H2O = 239.227,3972 kg/hari F6 NaOH = 1.775,3425 kg/hari F6 FeCl2 = 82,9973kg/hari F6 Na2HPO4.2H2O =15,1969 kg/hari Alur 7
F7 = 15.290,1370 kg/hari
= 15.290,1370 kg/hari / 0,7429 kg/m3 = 20.582,5403 m3/hari
F7H2 = 0,61 x 20.582,5403 m3/hari = 12.555,3496 m3/hari = 1.018,4900 kg/hari
F7 CO2 = 0,389915 x 20.582,5403 m3/hari = 8.025,4412 m3/hari
= 14.269,2344 kg/hari
F7 H2S = 0,000085 x 20.582,5403 m3/hari = 1,7495m3/hari
= 2,4126 kg/hari Alur 8
F8 = 430.419,0161 kg/hari F8(C5H10O5)900 = 193.050 kg/hari
Irma Suraya 08 0405 001
Universitas Sumatera Utara
F8 Na2HPO4.2H2O =15,1969 kg/hari A.4 Bioreaktor Biogas (R-203)
Fungsi : sebagai tempat berlangsungnya reaksi pembentukan biogas dengan menggunakan bakteri termofilik.
8
R-203
LI
FC
BK-205
9
10
J-204
Kesetimbangan reaksi yang terjadi di dalam reaktor fermentasi : Reaksi:
(C5H10O5)900 + H2O 750 C6H12O6 (Barnali dkk.,2008) 750C6H12O6 + 500H2O(l) + H2S(l) 2000H2(g) + 500C2H4O2(l) +
500C4H8O2(l) + 1500CO2(g) + H2S(g) (Sompong dkk., 2009)
F8 = 430.419,0161kg/hari F8 COD = 8.233,1507 kg/hari
% Dekomposisi COD : 84,9%...(Senafati, 2010) F9 = 0,849 x 8.233,1507 kg/hari
= 6.989,9449 kg/hari F9 CH4 = 2.525,5175 kg/hari F9 CO2 = 4.430,4986 kg/hari F9 H2O = 33,0001 kg/hari F9 H2S = 0,9287 kg/hari Neraca Massa Total :
F8 = F9 + F10
Irma Suraya 08 0405 001
Universitas Sumatera Utara
F10 = 430.419,0161kg/hari - 6.989,9449 kg/hari F10 = 423.429,0712 kg/hari
A.5 Biodesulfurisasi
Fungsi : untuk menyerap gas H2S yang terkandung dalam biohidrogen, gas H2S terserap sempurna.
PC
R-303
LI
TC 14
16 17
19
18 15
13 12
T-301
F-306
Diketahui dibutuhkan inokulum + medium fermentasi 4,7 L/jam untuk umpan gas 300 L/jam. Inokulum sebanyak 1 L. Sedangkan, medium terdiri dari 0,66 mol/L Na+ dan 1,34 mol/L K+ sebagai karbonat. Selanjutnya, médium mengandung (dalam g/ 1 L dari air demineralisasi) : 1 K2HPO4; 0,83 NaNO3; 6 NaCl ; 0,2 MgCl2.6H2O (Van den Bosch dkk., 2007).
Gas yang masuk = F12 = 20.582,5403 m3/hari
jam 24
1 m
1000 dm
1
1
3 3
3
hari x
dm x
L
x
= 857.605,8458 L/jam Jadi, medium fermentasi yang dibutuhkan :
L/jam 58 857.605,84
x L/jam
300 L/jam 7 , 3
x = 10.577,1388L/jam Diketahui :
Irma Suraya 08 0405 001
Universitas Sumatera Utara K2HPO4 = 2,44 g/ cm3 NaNO3 = 2,257 g/ cm3 NaCl = 2,165 g/ cm3 MgCl2.6H2O = 1,569 g/ cm3 NaOH = 2,1 g/ cm3
KOH = 2,044 g/ cm3 (Wikipedia,2012)
Air demineralisasi = a L/jam atau 1000a x 10-3 Liter/jam K2HPO4= 1 gr/L x a L = 3
g/cm 2,44
gram a
= 0,4098a cm3 = 0,4098a x 10-3 L/jam
NaNO3 = 0,83 gr/L x a L = 3 g/cm 2,257
83 ,
0 agram
= 0,3677a cm3 = 0,3677a x 10-3 L/jam
NaCl = 6 gr/L x a L = 3 g/cm 2,165
6agram
= 2,7714a cm3 = 2,7714a x 10-3 L/jam
MgCl2.6H2O = 0,2 gr/L x a L = 3 g/cm 1,569
2 ,
0 agram
= 0,1275a cm3 = 0,1275a x 10-3 L/jam NaOH = (0,66 mol/L x10.577,1388 L/jam x 40 g/mol)/(2,1 gr/cm3x1000) = 132,9697 L/jam
KOH = (1,34 mol/L x 10.577,1388 L/jam x 56 g/mol/)(2,044 gr/cm3x1000) = 388,3114 L/jam
Medium fermentasi = air demineralisasi + K2HPO4 + NaNO3 + NaCl + MgCl2.6H2O + NaOH + KOH
10.577,1388 L/jam = (1000a + 0,4098a + 0,3677a + 2,7714a + 0,1275a) x 10-3 + 132,9697+388,3114 L/jam
10.055,8577L/jam = 1,0036986a L/jam a = 10.018,802
Air demineralisasi = 10.018,802L/jam x 1 kg/L = 10.018,802kg/jam
Irma Suraya 08 0405 001
Universitas Sumatera Utara
NaOH = 0,66 mol/L x10.577,1388L/jam x 40 g/mol = 279.236,5 gr/jam = 279,2365 kg/jam
KOH = 1,34 mol/L x 10.577,1388L/jam x 56 g/mol = 793.708,5 gr/jam = 793,7086 kg/jam
Jadi total medium fermentasi dalam kg/jam yaitu :
Medium fermentasi = 10.0818,801 kg/jam + 10,0818 kg/jam + 8,3156 kg/jam + 60,1128 kg/jam + 2,0038 kg/jam + 279,2365 kg/jam + 793,7086 kg/jam
= 101.972,2601 kg/jam x 24 jam/hari = 268.132,7519 kg/hari A.5.1 Absorber (T-301)
PC
14
16 15
12 T-301
Alur 12
F12 = 15.290,1370 kg/hari F12H2 = 1.018,4900 kg/hari F12 CO2 = 14.269,2344 kg/hari F12 H2S = 2,4126 kg/hari Alur 14
F14 = Medium fermentasi = 268.132,7519 kg/hari Alur 15
Irma Suraya 08 0405 001
Universitas Sumatera Utara Alur 16
F16 = 268.135,1645 kg/hari F16medium = 268.132,7519 kg/hari F16H2S = 2,4126 kg/hari Neraca Massa Total :
F12 + F14 = F15 + F16
(15.290,1370 +268.132,7519) kg/hari=(15.287,7244+268.135,1645) kg/hari 283.422,8889 kg/hari = 283.422,8889 kg/hari
A.5.2 Bioreaktor Desulfurisasi (R-303)
R-303
TC 14
16 17
19
13 LI
H2S = 2,4126 kg/hari =
g/mol 34
g/hari 6 , 2412
=70,9588 mol/hari
H2S + ½O2 S + H2O (Konversi 84%) Awal 70,9588 mol 0,5 x 70,9588
29,80271 mol
Reaksi 0,84 x 70,9588 29,80271 mol 59,6054 mol 59,6054 mol 59,6054 mol
Sisa 11,3534 mol - 59,6054 mol 59,6054 mol So = 59,6054 mol/hari x 32 g/mol = 1.907,3731 g/hari = 1,9074 kg/hari O2 = 29,80271 mol/hari x 32 g/mol = 953,6867 g/hari = 0,9537 kg/hari H2O = 59,6054 mol/hari x 17 g/mol = 1.013,2920 g/hari = 1,0133 kg/hari H2S = 11,3534 mol/hari x 33 g/mol = 374,6622 g/hari = 0,3747 kg/hari
Alur 16
Irma Suraya 08 0405 001
Universitas Sumatera Utara
F16medium = 268.132,7519 kg/hari F16H2S = 2,4126 kg/hari Alur 19
F19 = 268.132,7519 kg/hari F19medium = 268.132,3659 kg/hari F19H2S = 0,386 kg/hari
Alur 14
F14 = Medium fermentasi = 268.132,7519 kg/hari Alur 17
F17 = 268.136,1182 kg/hari F17medium = 268.133,8248 kg/hari F17H2S = 0,386 kg/hari
F17 So = 1,9074 kg/hari Alur 13
F13 = O2 = 0,9537 kg/hari
Neraca Massa Total :
F16+ F19+ F13= F14 + F17
(268.135,1645 +268.132,7519+0,9537)kg/hari=(268.132,7519+268.136,1182)kg/hari 536.268,7991 kg/hari = 536.268,7991 kg/hari
A.5.3 Settler (TK-304)
17 19
18
F-306
Alur 17
Irma Suraya 08 0405 001
Universitas Sumatera Utara
F17 So = 1,9074 kg/hari Alur 19
F19 = 268.132,7519 kg/hari F19medium = 268.132,3659 kg/hari F19H2S = 0,386 kg/hari
Alur 18
F18 = 3,3663 kg/hari F18medium = 1,4589 kg/hari F18So = 1,9074 kg/hari
Neraca Massa Total :
F17 = F18 + F19
268.136,1182 kg/hari = 3,3663 kg/hari +268.132,7519 kg/hari 268.136,0472 kg/hari = 268.136,0472 kg/hari
A.6 Kolom Absorpsi-Stripping
Fungsi : untuk menyerap CO2 yang terkandung dalam biogas dan melepaskan CO2. Jumlah CO2 yang dikeluarkan dari sistem 99% (Twigg, 1989) dari alur 18. Larutan Benfield (K2CO3) (BM= 138 kg/kmol). K2CO3 yang digunakan adalah K2CO3 30 %, temperatur K2CO3 masuk absorber adalah 50 0C.
Reaksi pengikatan CO2 :
K2CO3 + CO2 + H2O ↔ 2KHCO3 ……….. (1) Reaksi pelepasan CO2:
Irma Suraya 08 0405 001
Universitas Sumatera Utara
T-308
E-311
E-310 T-313
22 21
26 20
PC
TC
FC
J-312
23
25
J-309
JC-403
24 27
PC
15
Dimana semua CO2 yang terserap dilepaskan pada kolom stripper. Jumlah CO2 yang terabsorpsi 99% dari jumlah CO2 umpan, maka :
F24 = 99 % x F15CO2
= 0,99 x 14.269,2344 kg/hari = 14.126,5421 kg/hari
Maka mol CO2 yang terbentuk dari reaksi (2) : N24 =
2 24
CO BM
CO F
=
44 1 14.126,542
= 321,0587 kmol/hari
Jumlah CO2 yang terbentuk = 321,0587 kmol/hari Jumlah KHCO3 yang bereaksi = 642,1156 kmol/hari
Neraca Massa Total:
F15 = F21 +F24
Irma Suraya 08 0405 001
Universitas Sumatera Utara Alur 21
F21H2 = F15 H2
= 1.018,4900 kg/hari
F21CO2 = F21– F15H2 = 142,6923 kg/hari Alur 22
N22KHCO3 = 642,1156 kmol/hari F22KHCO3 = N22KHCO3 x BM KHCO3
= 642,1156 kmol/hari x 100 kg/kmol = 64.211,56 kg/hari
F22H2O = 97.601,5636 kg/hari
Alur 20
Jumlah K2CO3 bereaksi = 321,0587 kmol/hari
= 321,0587 kmol/hari x 138 kg/kmol
= 44.305,9730 kg/hari
K2CO3 yang digunakan 30% berat, maka
Total umpan (F20) = 44.305,9730 kg/hari x 100/30
= 147.686,5765 kg/hari
Jumlah H2O = 70 % x 147.868,5765 kg/hari
= 103.380,6036 kg/hari
Jumlah H2O bereaksi = 321,0587 kmol/hari
= 321,0587 x 18 kg/kmol
= 5.770,0400 kg/hari
Jumlah H2O tidak bereaksi = 103.380,6036 kg/hari –5.770,0400 kg/hari
= 97.601,5636 kg/hari
F20 = 147.868,5765 kg/hari
F20K2CO3 = 44.305,9730 kg/hari F20H2O = 103.380,6036 kg/hari
Irma Suraya 08 0405 001
Universitas Sumatera Utara
F24 = 14.126,5421 kg/hari F24CO2 = 14.126,5421 kg/hari F25 = F20 = 147.686,5765 kg/hari
F25K2CO3 = 44.305,9730 kg/hari F25H2O = 103.380,6036 kg/hari F23 = F22 = 161.813,1186 kg/hari F23KHCO3 = 64.211,56 kg/hari
F23H2O = 97.601,5636 kg/hari
A.7 Pressure swing adsorbtion (T-316)
PC PC
T-316
31
32
30
Aliran gas yang diubah harus berisi paling sedikit 70% mol hidrogen sebelum dapat diproses dan untuk dibersihkan didalam unit PSA (Mann, 1995). Kemurnian hidrogen yang dapat dihasilkan melalui unit PSA adalah sebesar 99,99% mol dan metana (inert) 0,1 % mol (Monereau, dkk., 2006).
F30H2 = 1.018,4900 kg/hari F30CO2 = 142,6923 kg/hari Maka dalam mol :
N30H2 = 509,2450 kmol/hari N30CO2 = 3,2430 kmol/hari Jumlah H2 yang dihasilkan 99,9 % mol, maka :
Irma Suraya 08 0405 001
Universitas Sumatera Utara
= 99,9% N30H2 + N32H2 N32H2 = (100-99,9)% N30H2
= 0,5092 kmol/hari N31H2 = 508,7357 kmol/hari F31H2 = 1017,4715 kg/hari F32H2 = 1,0185 kg/hari N32 CO2 = 3,2430 kmol/hari F32 CO2 = 142,6923 kg/hari Maka jumlah gas yang terserap :
Irma Suraya 08 0405 001
Universitas Sumatera Utara
LAMPIRAN B
PERHITUNGAN NERACA ENERGI
Basis perhitungan : 1 hari operasi Satuan operasi : kJ/hari Temperatur basis : 25oC
Neraca panas ini menggunakan rumus-rumus perhitungan sebagai berikut: Perhitungan panas untuk bahan dalam fasa cair dan gas
Qi = Hi = (Van Ness, 1975)
Perhitungan panas penguapan QV= N ΔHVL
Perhitungan Cp beberapa padatan (J/mol.K) dengan menggunakan metode Hurst dan Harrison, dimana nilai kontribusi unsur atom.
Tabel LB.1 Nilai kontribusi Unsur Atom
Unsur Atom ΔE
C 10,89
H 7,56
O 13,42
Fe 29,08
Cl 24,69
Na 26,19
K 28,78
S 12,36
P 26,63
Sumber : Perry, 1999 Rumus Metode Hurst dan Harrison:
ni
Ei i
pS
N
C
1
T
298 1 T
Irma Suraya 08 0405 001
Universitas Sumatera Utara Dimana :
Cps = Kapasitas panas padatan pada 298,15 K ( J/mol.K ) n = Jumlah unsur atom yang berbeda dalam suatu senyawa Ni = Jumlah unsur atom I dalam senyawa
ΔEi = Nilai dari distribusi atom I pada tabel LB.1 Menghitung Cp glukosa:
Cp = 6.ΔEC + 12.ΔEH + 6.ΔEO
= 6 (10,89) + 12 (7,56) + 6(13,42) = 236,58 J/mol.K
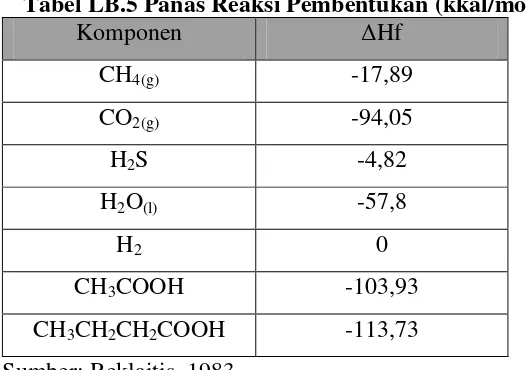
Tabel LB.2 Kapasitas panas beberapa senyawa pada 298,25 K (J/mol.K)
Komponen Cp
(C5H10O5)900 177.435
C6H12O6 236,58
NaOH 47,17
FeCl2 78,46
Na2HPO4.2H2O 182,21
S 12,36
K2CO3 108,71
KHCO3 87,49
K2HPO4 145,43
NaNO3 85,19
NaCl 50,88
MgCl2.6H2O 243,31
KOH 49,76
Persamaan untuk menghitung kapasitas panas (Reklaitis, 1983) : 3
2
dT cT bT a
Cp ... (1) Jika Cp adalah fungsi dari temperatur maka persamaan menjadi :
dT dT CT bT a CpdT
T
T
T
T
)
( 2 3
2
1
2
1
Irma Suraya 08 0405 001
Universitas Sumatera Utara
)
Untuk sistem yang melibatkan perubahan fasa persamaan yang digunakan adalah :
Perhitungan energi untuk sistem yang melibatkan reaksi :
Tabel LB.3 Data Kapasitas Panas (J/ mol. K)
Komponen a b C d e
CH4(g) 38,387 -0,0736639 0,000290981 -2,63849E-07 8,00679E-11 CO2(g) 19,0223 0,0796291 -7,37067E-05 3,74572E-08 -8,13304E-12
H2(g) 17,6386 0,0670055 -1,31485E-04 1,05883E-07 -2,91803E-11 H2S(g) 34,5234 -0,0176481 6,76664E-05 -5,32454E-08 1,40690E-11
O2(g) 29,8832 -0,0113842 4,33779E-05 -3,70062E-08 1,01006E-11 H2O(g) 34,0471 -0,00965064 3,29983E-05 -2,04467E-08 4,30228E-12 Sumber: Reklaitis, 1983
Data Cp untuk fasa cair:
Tabel LB.4 Data Kapasitas Panas (J/ mol. K)
Senyawa a b c d
-1,66566.10-3 -7,23130.10-3
Irma Suraya 08 0405 001
Universitas Sumatera Utara
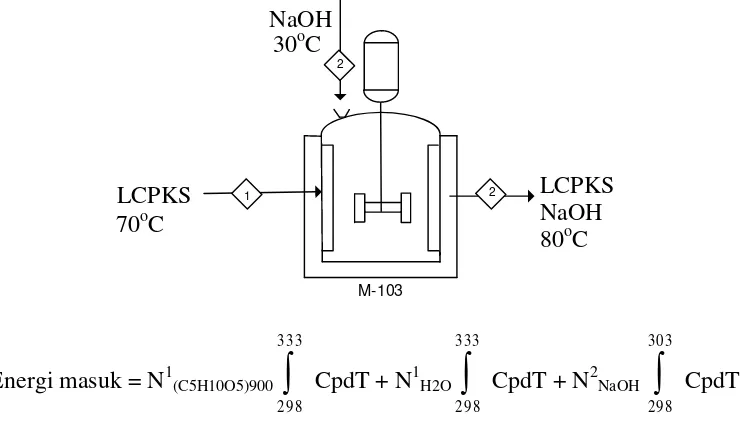
Tabel LB.5 Panas Reaksi Pembentukan (kkal/mol)
Komponen ΔHf
CH4(g) -17,89
CO2(g) -94,05
H2S -4,82
H2O(l) -57,8
H2 0
CH3COOH -103,93
CH3CH2CH2COOH -113,73 Sumber: Reklaitis, 1983
Perhitungan ΔHf0 (kkal/mol) dengan menggunakan metode Benson et al, dimana kontribusi gugusnya adalah:
Tabel LB.6 Tabel Kontribusi Gugus dengan Metode Benson et al
Sumber : Perry, 1999 Rumus metode Benson et al:
ΔHf o298 = 68,29 + Ni x Δhi
Dimana : ΔHf o298 = entalpi pembentukkan pada 298 K (kJ/mol) Ni = jumlah group atom i di dalam molekul
Δhi = nilai dari kontribusi gugus atom pada tabel LB.6 ΔHf o298 = 68,29 + Ni x Δhi
Irma Suraya 08 0405 001
Universitas Sumatera Utara
= -870,9 kJ/mol = -208,15 kkal/mol LB.1 Tangki Pre-Treatment (M-103)
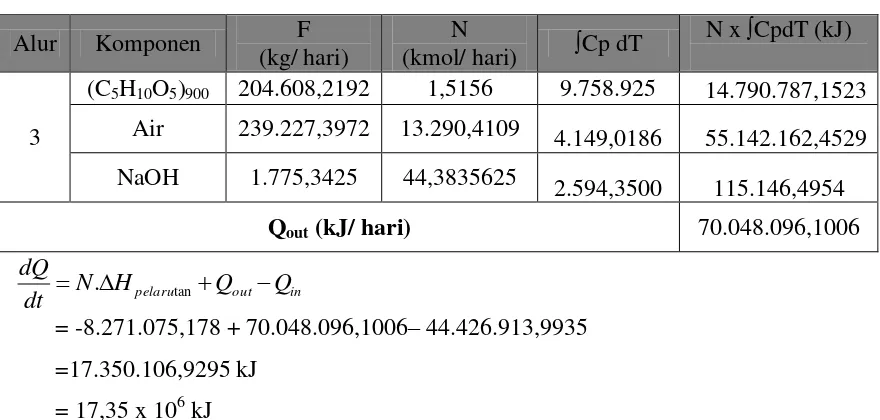
Fungsi: sebagai tempat menon-aktifkan bakteri yang memproduksi gas metana, sehingga produksi gas hidrogen yang dihasilkan lebih besar.
2
1 2
M-103
Energi masuk = N1(C5H10O5)900
333298
CpdT + N1H2O
333298
CpdT + N2NaOH
303298
CpdT
Tabel LB.7 Perhitungan Energi yang masuk kedalam Tangki Pre-Treatment
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
1
(C5H10O5)900 204.608,2192 1,5156 6.210.225 9.412.319,0969 Air 239.227,3972 13.290,4109 2.633,7882 35.004.127,0334
2 NaOH 1.775,3425 44,3835625 235,85 10.467,8632
Qin (kJ/ hari) 44.426.913,9935
Dari data termodinamika Perry, 1999 :
panas pelarutan NaOH dalam air = -44,51 kkal/mol = -186.354,468 kJ/kmol N . H = 44,3835625 x -186.354,468
= -8.271.075,178 kJ
Temperatur pada alur keluar, Tout = 80 oC = 353 K
Energi keluar = N3(C5H10O5)900
353298
CpdT + N3H2O
353298
CpdT + N3NaOH
353298
CpdT 70oC
80oC 30oC
LCPKS LCPKS
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Tabel LB.8 Perhitungan Energi yang Keluar dari Tangki Pre-Treatment
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
3
(C5H10O5)900 204.608,2192 1,5156 9.758.925 14.790.787,1523 Air 239.227,3972 13.290,4109 4.149,0186 55.142.162,4529 NaOH 1.775,3425 44,3835625 2.594,3500 115.146,4954
Qout (kJ/ hari) 70.048.096,1006
in out pelaru Q Q
H N dt dQ
. tan
= -8.271.075,178 + 70.048.096,1006– 44.426.913,9935 =17.350.106,9295kJ
= 17,35 x 106 kJ
Steam yang digunakan adalah saturated pada suhu (150 oC), tekanan 1 atm dan keluar sebagai liquid pada suhu 150oC, tekanan 1 atm. Dari steam tabel (Smith, 2001) diperoleh :
Saturated steam pada 1 atm, 1500C, Hv(1500C) = 2745,4 kJ/kg Saturated liquid pada 1 atm, 1500C, Hl(1500C) = 632,1 kJ/kg q = [Hv(150oC) – Hl(150oC)]
q = [2745,4 –632,1] q = 2.113,3 kJ/kg
Jumlah steam yang diperlukan :
m =
q dT dQ
kg/hari 8.209,9593
kJ/kg 3 , 113 . 2
kJ/hari ,9295
17.350.106 m
Irma Suraya 08 0405 001
Universitas Sumatera Utara
LB.2 Tangki Pencampur ( M-107)
Fungsi : sebagai tempat mencampur LCPKS dari Tangki Pre-Treatment dengan nutrisi.
M-107
5 4
3 6
Panas masuk alur 3 sama dengan panas keluar tangki Pre-treatment yaitu 70.048.096,1006 kJ/hari.
Energi masuk = N3(C5H10O5)900
353298
CpdT + N3H2O
353298
CpdT + N3NaOH
353298
CpdT +
N4FeCl2
303298
CpdT + N5Na2HPO4.2H2O
303298
CpdT
Tabel LB.9 Perhitungan Energi yang Masuk ke dalam Tangki Pencampur
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
3
(C5H10O5)900 204.608,2192 1,5156 9.758.925 14.790.787,1523 Air 239.227,3972 13.290,4109 4.149,0186 55.142.162,4529 NaOH 1.775,3425 44,3835625 2.594,3500 115.146,4954
4 FeCl2 82,9973 0,654811045 392,3000 256,8823731
5 Na2HPO4.2H2O 15,1969 0,085399831 986,6500 84,25974366 Qin (kJ/ hari) 70.048.437,2427
Dari data termodinamika Perry, 1999 :
panas pelarutan FeCl2 dalam air = +17,9 kkal/mol = 74.943,72 kJ/kmol 80oC
79,971oC 30oC 30oC
LCPKS NaOH
FeCl2
Na2HPO4.2H2O
LCPKS NaOH FeCl2
Irma Suraya 08 0405 001
Universitas Sumatera Utara
panas pelarutan Na2HPO4.2H2O dalam air = -0,82 kkal/mol = -3.400,376 kJ/kmol
N . H = (0,654811045 x 74.943,72) + (0,085399831x -3.400,376) = 48.783,5841kJ
Untuk mengetahui suhu keluaran dari M-107, maka dilakukan trial error, sehingga didapatkan suhu 79,96oC,
Tabel LB.10 Perhitungan Temperatur Keluar dari Tangki Pencampur (M-107)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
6
(C5H10O5)900 204.608,2192 1,5156 9.751.691,63 14.779.824,14 Air 239.227,3972 13.290,4109 4.145,922858 55.101.018,58 NaOH 1.775,3425 44,3835625 2.592,427 115.061,1481 FeCl2 82,9973 0,654811045 4.312,1014 2.823,6117 Na2HPO4.2H2O 15,1969 0,085399831 10.845,1056 926,1702
Qout (kJ/ hari) 69.999.653,6446
LB.3 Bioreaktor Hidrogen ( R-201 )
Fungsi : sebagai tempat berlangsungnya reaksi pembentukan hidrogen dengan menggunakan bakteri thermofilik.
R-201
7
TC LI
6 8
LCPKS NaOH FeCl2
Na2HPO4.2H2O 79,971oC
30oC
60oC LCPKS NaOH FeCl2
Na2HPO4.2H2O H2
Irma Suraya 08 0405 001
Universitas Sumatera Utara Temperatur basis = 25oC Reaksi :
(C5H10O5)900 + H2O 750 C6H12O6 (Barnali dkk.,2008) ( Hr1)
750C6H12O6 + 500H2O(l) + H2S(l) 2000H2(g) + 500C2H4O2(l) + 500C4H8O2(l) + 1500CO2(g) + H2S(g) (Sompong dkk., 2009) ( Hr2)
H2S yang terbentuk dari hasil pembusukan oleh mikroorganisme pada fasa cair terionisasi menjadi fasa gas (Speece, R.E., 1996)
Hl H2S = 568 kal/ mol Hv H2S = 4.463 kal/ mol (Perry,1999)
Hr1 =750. Hfo C6H12O6(s) - ( Hfo C5H10O5(s) + Hfo H2O(l) ) = (750 x -208,15) – (-158,4273-57,8)
= -155.745,9227 kkal/mol = -651.640.940,6 kJ/kmol r1 =
t karbohidra BM
sisa t karbohidra F
-awal t karbohidra F
=
000 . 135
185 . 193 92 204.608,21
= 0,085 kmol/hari
Hr2 = [ 2000. Hfo H2(g) + 500. Hfo C2H4O2(l) + 500. Hfo C4H8O2(l) +1500. HfoCO2(g)] – [750. Hfo C6H12O6(s) +500. Hfo H2O(l)] + [Hv H2S -.Hl H2S]
= [(2000x0) + (500x -103,93) + (500x -113,73) + (1500x -94,05)] – [750x -208,15 + (500x -57,8)] + [4,463 – 0,568]
= -64.888,605 kkal/mol = -271.493.923,3 kJ/kmol r2 =
glukosa BM
sisa glukosa F
Irma Suraya 08 0405 001
Universitas Sumatera Utara =
180
03743 , 256 . 18 26
18.907,397
= 3,618666 kmol/hari
r. Hr = (r1. Hr1) + (r2. Hr2)= (-55.389.479,95) + (-982.536.508,4951) = - 1.037.925.988,4441 kJ/hari
Panas masuk reaktor (R-201) = panas keluar tangki pencampur (M-107) = 69.999.653,6446 kJ
Entalpi biohidrogen = N8H2
303298
CpdT + N8CO2
303298
CpdT + N8H2S
303298
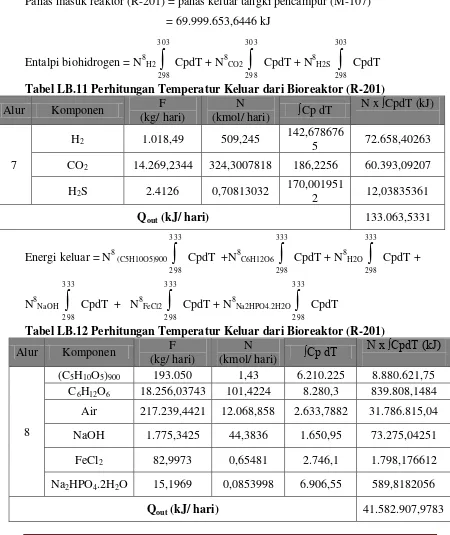
CpdT Tabel LB.11 Perhitungan Temperatur Keluar dari Bioreaktor (R-201)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
7
H2 1.018,49 509,245 142,678676
5 72.658,40263 CO2 14.269,2344 324,3007818 186,2256 60.393,09207 H2S 2.4126 0,70813032 170,001951
2 12,03835361
Qout (kJ/ hari) 133.063,5331
Energi keluar = N8 (C5H10O5)900
333298
CpdT +N8C6H12O6
333298
CpdT + N8H2O
333298
CpdT +
N8NaOH
333298
CpdT + N8FeCl2
333298
CpdT + N8Na2HPO4.2H2O
333298
CpdT
Tabel LB.12 Perhitungan Temperatur Keluar dari Bioreaktor (R-201)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
8
(C5H10O5)900 193.050 1,43 6.210.225 8.880.621,75 C6H12O6 18.256,03743 101,4224 8.280,3 839.808,1484 Air 217.239,4421 12.068,858 2.633,7882 31.786.815,04 NaOH 1.775,3425 44,3836 1.650,95 73.275,04251
FeCl2 82,9973 0,65481 2.746,1 1.798,176612
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Qin Hr r Qout dT
dQ
= (41.582.907,9783+133.063,5331) + (- 1.037.925.988,4441) – 69.999.653,6446 = -1.066.209.670,5773kJ
= -10,66 x 108 kJ
Air pendingin yang digunakan pada suhu 30 oC dan keluar sebagai air pendingin bekas pada suhu 60 oC.
H (60 oC) = 251,1 H (30 oC) = 125,7
Jumlah air pendingin yang diperlukan :
m =
H dT dQ
kg/hari 462
8.502.469,
kJ/kg ) 1 , 251 7 , 125 (
kJ/hari 10
x 10,66 -m
8
LB.4 Bioreaktor Biogas ( R-203 )
Fungsi : sebagai tempat berlangsungnya reaksi pembentukan biogas dengan menggunakan bakteri termofilik.
R-203
9
TC LI
8 10
Temperatur basis = 25oC
60oC 55oC
30oC CH4 CO2 H2S H2O
LCPKS NaOH FeCl2
Na2HPO4.2H2O LCPKS
NaOH FeCl2
Irma Suraya 08 0405 001
Universitas Sumatera Utara Reaksi :
(C5H10O5)900 + H2O 750C6H12O6 (Barnali dkk.,2008) ( Hr1) 750C6H12O6 (S)+750H2O(l)+H2S(l) 2250CH4(g)+2250CO2(g)+750H2O(g)+ H2S(g)
(Sompong dkk., 2009) ( Hr2)
H2S yang terbentuk dari hasil pembusukan oleh mikroorganisme pada fasa cair terionisasi menjadi fasa gas
(Speece, R.E., 1996) Hl H2S = 568 kal/ mol Hv H2S = 4.463 kal/ mol Hl H2O = 1.436 kal/ mol Hv H2O= 9.729 kal/ mol (Perry,1999)
Hr1 =750. Hfo C6H12O6(s) - ( Hfo C5H10O5(s) + Hfo H2O(l) ) = (750 x -208,15) – (-158,4273-57,8)
= -155.745,9227 kkal/mol = -651.640.940,6 kJ/kmol r1 =
t karbohidra BM
sisa t karbohidra F
-awal t karbohidra F
=
000 . 135
735 . 183 185 .
193
= 0,07 kmol/hari ΔH r2 = [2250.ΔH
f° CH4(g)+ 2250.ΔHf° CO2(g)] – [750.ΔHf° C6H12O6 (S)] +[Hv H2S - Hl H2S] + [Hv H2O(g) - Hl H2O(l)]
= [(2250x -17,89) + (2250x -94,05)] – (750x -208,15) + (4,463 - 0,568) + (9,729 – 1,436) kkal/mol
= -95.470,312 kkal/mol = -399.447.785,4 kJ/kmol r 2=
glukosa BM
sisa glukosa F
-awal glukosa F
=
180
2657 , 958 . 17 43
18.256,037
Irma Suraya 08 0405 001
Universitas Sumatera Utara
r. Hr = (r1. Hr1) + (r2. Hr2)= (-45.614.865,84) + (-660.801.271,9) = - 706.416.137,8 kJ/hari
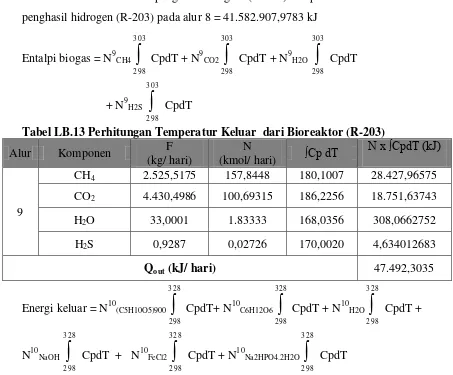
Panas masuk bioreaktor penghasil biogas (R-201) = panas keluar bioreaktor penghasil hidrogen (R-203) pada alur 8 = 41.582.907,9783 kJ
Entalpi biogas = N9CH4
303298
CpdT + N9CO2
303298
CpdT + N9H2O
303298
CpdT
+ N9H2S
303298
CpdT
Tabel LB.13 Perhitungan Temperatur Keluar dari Bioreaktor (R-203)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
9
CH4 2.525,5175 157,8448 180,1007 28.427,96575 CO2 4.430,4986 100,69315 186,2256 18.751,63743
H2O 33,0001 1.83333 168,0356 308,0662752
H2S 0,9287 0,02726 170,0020 4,634012683
Qout (kJ/ hari) 47.492,3035
Energi keluar = N10(C5H10O5)900
328298
CpdT+ N10C6H12O6
328298
CpdT + N10H2O
328298
CpdT +
N10NaOH
328298
CpdT + N10FeCl2
328298
CpdT + N10Na2HPO4.2H2O
328298
CpdT
Tabel LB.14 Perhitungan Temperatur Keluar dari Bioreaktor (R-203)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
10
(C5H10O5)900 183.735 1,361 7.097,4 708.094,4193 C6H12O6 17.958,2658 99,7681 5.323.050 7.244.671,05
Air 219.862,27 12.214,571 2.256,084 27.557.093,06 NaOH 1.775,3425 44,3836 1,415,1 62.807,17929
FeCl2 82,9973 0,65481 2.353,8 1.541,294239
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Qin Hr r Qout dT
dQ
= (47.492,3035 +35.574.712,5656) + (-706.416.137,8) – 41.582.907,9783 = -712.376.840,8714 kJ
= -71,24 x 107 kJ
Air pendingin yang digunakan pada suhu 30 oC dan keluar sebagai air pendingin bekas pada suhu 60 oC.
H (60 oC) = 251,1 H (30 oC) = 125,7
Jumlah air pendingin yang diperlukan :
m =
H dT dQ
kg/hari 052
5.680.836,
kJ/kg ) 1 , 251 7 , 125 (
kJ/hari 10
x 71,24 -m
7
LB.5 Cooler ( E-207 )
Fungsi : Untuk mendinginkan gas dan cairan yang berasal dari kompresor (JC-206) sebelum diumpankan ke absorber (T-301)
E-421
11 12
Aliran 11 adalah aliran gas dan cairan keluar kompresor (JC-206). Dari perhitungan pada spesifikasi JC-206, diketahui T11 = 149,778oC. Entalpi gas dan cairan keluaran kompresor dapat dilihat pada tabel LB-15.
Air pendingin
Air pendingin 30oC, 1 atm 60oC, 1 atm
H2 CO2 H2S
149,778oC,
83,89 atm 35
o
C, 83,89 atm H2
Irma Suraya 08 0405 001
Universitas Sumatera Utara
))
Tabel LB.15 Entalpi gas dan cairan masuk ke Cooler (E-207)
Komponen N (kmol) ∫Cp dT H
H2 509,245 3.633,7354 1.850.461,603
CO2 324,3008 4.955,1245 1.606.950,734
H2S 0,0708 4.332,8196 306,8201
Hin (kJ) 3.457.719,1576
Irma Suraya 08 0405 001
Universitas Sumatera Utara
))
Tabel LB.16 Entalpi gas dan cairan keluar dari Cooler (E-207)
Komponen N (kmol) ∫Cp dT H
H2 509,245 285,6884 145.485,3977
CO2 324,3008 373,5605 121.145,9547
Irma Suraya 08 0405 001
Universitas Sumatera Utara H (30 oC) = 125,7
Jumlah air pendingin yang diperlukan :
m = H
dT dQ
kg/hari 2
25.446,841
kJ/kg ) 1 , 251 7 , 125 (
kJ/hari 10
x 3,19103
-m
6
LB.6 Absorber Desulfurisasi (T-301)
Fungsi : untuk menyerap gas H2S yang terdapat pada hasil fermentasi biohidrogen dengan menggunakan medium dari bioreaktor.
16
T-301
12 15
14
Energi masuk alur 14 = N14H2O
308298
CpdT + N14K2HPO4
308298
CpdT + N14NaNO3
308298
CpdT + N14NaCl
308298
CpdT +N14MgCl2.6H2O
308298
CpdT
+N14NaOH
308298
CpdT + N14KOH
308298
CpdT H2
CO2 H2S 35oC H2 CO2 30oC
30oC 30oC H2O K2HPO4 NaNO3 NaCl
MgCl2.6H2O NaOH KOH
H2O K2HPO4 NaNO3 NaCl
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Tabel LB.17 Perhitungan Energi Masuk ke dalam Absorber (T-301)
Alur Komponen F
Air 24.0451,248 13.358,4027 749,9460 10.018.07999
K2HPO4 240,4512 1,3803 1.454,3 2007,3948
NaNO3 199,5744 2,3481 851,9 2.000,329801
NaCl 1.442,7072 24,6869 508,8 12.560,7362
MgCl2.6H2O 48,0912 0,2365 2433,1 575,5285
NaOH 6.701,676 167,5419 471,7 79.029,5142
KOH 19.049,0064 340,1608 497,6 1.69264,0283
Qin (kJ/ hari) 10.283.517,52
Energi masuk absorber keseluruhan = Energi keluar dari cooler (E-207)+ Energi masuk ke dalam absorber pada alur 14
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Tabel LB.18 Perhitungan Energi Keluar dari Absorber (T-301)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
15
H2 1.018,49 509,245 285,6884 14.5485,3977
CO2 14.269,2344 324,3008 373,5605 121.145,9547 Qout (kJ/ hari) 266.631,3524
Energi keluar pada alur 16 = N16H2O
308298
CpdT + N16K2HPO4
308298
CpdT + N16NaNO3
308298
CpdT+ N16NaCl
308298
CpdT +N16MgCl2.6H2O
308298
CpdT
+N16NaOH
308298
CpdT + N16KOH
308298
CpdT + N16H2S
308298
CpdT
Tabel LB.19 Perhitungan Energi Keluar dari Absorber (T-301)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
16
Air 240.451,248 13.358,4027 749,946 10.018.079,99 K2HPO4 240,4512 1,3803 1.454,3 2.007,3948
NaNO3 199,5744 2,3481 851,9 2.000,3298
NaCl 1.442,7072 24,6869 508,8 12.560,7362
MgCl2.6H2O 48,0912 0,2365 2.433,1 575,5285
NaOH 6.701,676 167,5419 471,7 79.029,51423
KOH 19.049,0064 340,1608 497,6 169.264,0283
H2S 2,4126 0,07081 761,3532 53,9137
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Tabel LB.20 Neraca Energi pada Absorber (T-301)
Komponen Masuk (kJ/hari) Keluar (kJ/hari)
12 14 15 16
H2O 10.018.079.99 - - 10.0180.79.99
K2HPO4 2.007,3948 - - 2.007.3948
NaNO3 2.000,329801 - - 2.000.3298
NaCl 12.560,7362 - - 12.560.7362
MgCl2.6H2O 575,5285 - - 575,5285
NaOH 79.029,5142 - - 79.029,51423
KOH 169.264,0283 - - 169.264,0283
H2 - 145.485,3977 145.485,3977 -
CO2 - 121.145,9547 121.145,9547 -
H2S - 53,9137 - 53.91373021
Sub Total 10.283.517,52 266.685,2662 266.631,3524 10.283.571,4341
r.∆Hr - -
Total 10.550.202,7866 10.550.202,7866
LB.7 Bioreaktor Desulfurisasi ( R-303)
Fungsi : Sebagai tempat berlangsungnya reaksi oksidasi pembentukan sulfur dari gas H2S dengan menggunakan mikroba.
R-303
TC 14
16 17
LI
19
13
H2O K2HPO4 NaNO3 NaCl
MgCl2.6H2O NaOH KOH H2S
H2O K2HPO4 NaNO3 NaCl
MgCl2.6H2O NaOH KOH 35oC
30oC O2
H2O K2HPO4 NaNO3 NaCl
MgCl2.6H2O NaOH KOH H2S S H2O K2HPO4 NaNO3 NaCl
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Panas masuk bioreaktor desulfurisasi alur 16 (R-303) = Panas keluar absorber alur 16 (T-301)
= 10.283.571,4341kJ Reaksi yang terjadi pada reaktor desulfurisasi :
H2S(l) +
2 1
O2(g) S(s) + H2O(l) (Van den Bosch,2007) ΔHr = [ΔH
f° H2O(l) + ΔHf° S(s)] – [ΔHf° H2S(l) + 0,5 .ΔHf° O2(g)] = [(-57,8) + (0)] – [(-4,82) + (0)] kkal/mol
= -52,98 kkal/mol = -221.668,32 kJ/kmol r =
S H BM
sisa S H F -awal S H F
2 2 2
=
07 , 34
3747 , 0 4126 ,
2
= 0,05982 kmol/hari
r. Hr = -13.259,1098 kJ/hari
Dari data termodinamika Perry, 1999 :
Panas pelarutan KOH dalam air = 12,91 kkal/mol = 54.051,588 kJ/kmol Panas pelarutan NaCl dalam air = -1,164 kkal/mol = -4.873,4352 kJ/kmol Panas pelarutan MgCl2.6H2O dalam air =3,4 kkal/mol=14.235,12 kJ/kmol Panas pelarutan NaNO3 dalam air = -5,5 kkal/mol = -23.027,4 kJ/kmol Panas pelarutan K2HPO4 dalam air = 4,7 kkal/mol = 19.677,96 kJ/kmol Panas pelarutan NaOH dalam air =-44,51 kkal/mol= -186.354,468 kJ/kmol
N.H = (340,1608 x 54.051,588) + (24,6869 x -4.873,4352) + (0,2365 x 14.235,12) + (2,3481 x 23.027,4) + (1,3803 x 19.677,96) + (167,5419 x -186.354,468)
= -12.979.800,3 kJ 35oC
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Energi masuk pada alur 13 = N13O2
Tabel LB.21 Perhitungan Energi Masuk ke Bioreaktor (R-303)
Alur Komponen F
NaNO3 199,5741 2,34808 851,9 2.000,3269
NaCl 1.442,7051 24,6869 508,8 12.560,718
MgCl2.6H2O 48,09113 0,23654 2.433,1 575,52766
NaOH 6.701,6663 167,5417 471,7 79.029,3997
KOH 19.048,9788 340,1603 497,6 169.263,783
H2S 0,386 0,0113 761,3532 8,6258
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Energi keluar pada alur 17 = N17H2O
308298
CpdT + N17K2HPO4
308298
CpdT + N17NaNO3
308298
CpdT+ N17NaCl
308298
CpdT +N17MgCl2.6H2O
308298
CpdT
+N17NaOH
308298
CpdT + N17KOH
308298
CpdT + N17H2S
308298
CpdT
Tabel LB.22 Perhitungan Energi Keluar dari Bioreaktor (R-303)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
17
H2O 240.452,321 13.358,4623 749,946 10.018.124,69 K2HPO4 240,4512 1,38032 1454,3 2.007,3948
NaNO3 199,5744 2,3481 851,9 2.000,3298
NaCl 1.442,7072 24,687 508,8 12.560,7362
MgCl2.6H2O 48,0912 0,2365 2433,1 575.5285
NaOH 6701.676 167,5419 471,7 79.029,51423
KOH 19.049,0064 340,1608 497,6 169.264,0283
H2S 0,386 0,01135 761,3532 8,6436
S 1,9074 0,05947 123,6 7,3513
Qout (kJ/ hari) 10.283.578,22
Qin Hr r Qout dT
dQ
= (10.283.517,5204 + 10.283.578,22) + (-13.185,589) – (8,7836 + 10.283.571,43 + 10.283.511,25)
= -12.992.981,58 kJ = -1,2993 x 107 kJ
Air pendingin yang digunakan pada suhu 30 oC dan keluar sebagai air pendingin bekas pada suhu 60 oC.
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Jumlah air pendingin yang diperlukan :
m =
Fungsi : Untuk menyerap gas CO2 yang terdapat dalam campuran gas.
T-308 desulfurisasi = 266.631,3524 kJ
Alur 20, T= 75oC
Larutan benfield masuk pada suhu 75 0C, 1 atm
Irma Suraya 08 0405 001
Universitas Sumatera Utara
kJ x CO
K dT NCps
6 348
298
3 2
10 1,7451
298) -(348 x 108,71 x 0578 , 321 ) (
Q (20) = 23,3950 x 106 kJ Maka Qin absorber = Q(15) + Q(20)
= 23,6616 x 106 kJ Absorber bersifat adiabatis, sehingga:
0 Qin -Hr Qout dt
dQ
Qout +Hr = Qin = 13,4716 x 106 kJ Reaksi yang terjadi pada absorber :
CO2 + K2CO3 + H2O 2KHCO3 Hr = -6,43 kkal/mol ( Reina,2011) r (Jumlah K2CO3 yang bereaksi) = 321,0587 kmol
rHr = -2,0644 x 103 kJ Qout = 13,4737 x 106 kJ
Untuk mencari suhu keluar dari absorber maka dilakukan trial error, sehingga diperoleh suhu keluar 72,41970C (345,4197 K)
Tabel LB.23 Perhitungan Energi Keluar dari Absorber (T-308)
Alur Komponen F
(kg/ hari)
N
(kmol/ hari) ∫Cp dT
N x ∫CpdT (kJ)
21
H2 1.018,49 509,245 3.171,56945 1.615.105,8845 CO2 142,6923 3,2430 1.809,6970 5.868,85976 22 H2O 97.601,5636 5.422,3091 3.573,89199 19.378.747,0202
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Tabel LB.24 Neraca Energi pada Absorber (T-308)
Komponen
Masuk (kJ/hari) Keluar (kJ/hari)
15 20 21 22
Sub Total 266.631,3524 23.395.002,54 1.620.974,7443 22.042.723,5532
r.∆Hr - -2.064,40744
Total 23.661.633,89 23.661.633,89
LB.9 Heat Exchanger ( E-310 )
Fungsi : Untuk menukarkan panas antara larutan amine solution yang keluar dari stripper dengan larutan rich solution yang keluar dari absorber.
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Irma Suraya 08 0405 001
Universitas Sumatera Utara
))
Tabel LB.25 Neraca Energi pada Heat Exchanger (E-310)
Komponen
Masuk (kJ/hari) Keluar (kJ/hari)
22 25 23 26
KHCO3 2.663.976,533 - 30.386.370,7144 -
H2O 19.378.747,0202 37.845.011,5087 3.017.083,831 27.321.933,0928
K2CO3 - 3.036.490.596 - 2.198.838,018
Sub total 22.042.723,55 40.881.502,1 33.403.454,5458 29.520.771,11
Total 62.924.225,66 62.924.225,66
LB.10 Stripper ( T-313 )
Fungsi : Untuk melepaskan CO2 dari larutan rich solution.
Irma Suraya 08 0405 001
Universitas Sumatera Utara Alur 23, T= 99,1131oC Reaksi yang terjadi pada stripper:
Irma Suraya 08 0405 001
Universitas Sumatera Utara r = 321,0587 kmol
rHr (panas pelepasan CO2) = 2.064,4074kJ
Qin -Hr Qout dt
dQ
= (40,8815 x 106 + 1,0887 x 106) + (2.064,4074) – (33,4034 x 106) = 8,5688 x 106 kJ
Steam yang digunakan adalah saturated pada suhu (150 oC), tekanan 1 atm dan keluar sebagai liquid pada suhu 150oC, tekanan 1 atm. Dari steam tabel (Smith, 2001) diperoleh :
Saturated steam pada 1 atm, 1500C, Hv(1000C) = 2745,4 kJ/kg Saturated liquid pada 1 atm, 1500C, Hl(1000C) = 632,1 kJ/kg q = [Hv(150oC) – Hl(150oC)]
q = [2745,4 –632,1] q = 2.113,3 kJ/kg
Jumlah steam yang diperlukan :
m =
q dT dQ
kg/hari 4.054,6847
kJ/kg 3 , 113 . 2
kJ/hari 10
x 8,5688 m
6
Tabel LB.26 Neraca Energi pada Stripper (T-313)
Komponen
Masuk (kJ/hari) Keluar (kJ/hari)
23 24 25
CO2 - 1.088.653,2216 -
KHCO3 3.017.083,831 - -
H2O 30.386.370,7144 - 37.845.011,5087
K2CO3 - - 3.036.490,596
Sub total 33.403.454,55 1.088.653,2216 40.881.502,1
rΔHr - 2.064,4074
Q 8.568.765,188 -
Irma Suraya 08 0405 001
Universitas Sumatera Utara LB.11 Cooler ( E-311 )
Fungsi : Mendinginkan larutan amine solution sebelum diumpankan menuju absorber kembali.
Larutan benfield masuk pada suhu 75 0C, 1 atm
))
Air pendingin
75oC, 1 atm
Irma Suraya 08 0405 001
Universitas Sumatera Utara
kJ x CO
K dT NCps
6 348
298
3 2
10 1,7451
298) -(348 x 108,71 x 0578 , 321 ) (
Q (20) = 23,3950 x 106 kJ
Qin -Qout dt
dQ
= 23,3950 x 106 kJ - 29,5208 x 106 kJ = -6,1258 x 106 kJ
Air pendingin yang digunakan pada suhu 30 oC dan keluar sebagai air pendingin bekas pada suhu 60 oC.
H (60 oC) = 251,1 H (30 oC) = 125,7
Jumlah air pendingin yang diperlukan :
m =
H dT dQ
kg/hari 1
48.849,829
kJ/kg ) 1 , 251 7 , 125 (
kJ/hari 10
x 6,1258
-m
6
Tabel LB.27 Neraca Energi pada Cooler (E-311)
Komponen
Masuk (kJ/hari)
Keluar (kJ/hari)
26 27
H2O 27.321.933,0928 21.649.893,0059 K2CO3 2.198.838,018 1.745.109,5380
Q -6.125.768,5667 -
Irma Suraya 08 0405 001
Universitas Sumatera Utara LB.12 Cooler ( E-404 )
Fungsi : Mendinginkan gas CO2 sebelum disimpan dalam tangki penyimpanan gas CO2.
E-404
27 28
Aliran 27 adalah aliran gas CO2 keluar kompresor (JC-403). Dari perhitungan pada spesifikasi JC-420, diketahui T27 = 213,541 oC. Entalpi gas CO2 keluaran kompresor dapat dilihat pada tabel LB-28.
)
Tabel LB.28 Entalpi gas output Kompresor (JC-403)
Komponen N (kmol) ∫Cp dT H
CO2 321,0578 7.706,5922 2.474.261,3373
Gas sebelum disimpan suhunya diturunkan hingga 40 0C dengan menggunakan air pendingin, sehingga dapat dihitung Entalpi gas pada suhu 40 0C,
)
Air pendingin
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Tabel LB.29 Entalpi gas output Cooler (E-404)
Komponen N (kmol) ∫Cp dT H
CO2 321,0578 561,9938 180.432,4764
Qin -Qout dt
dQ
= 180.432,4764 kJ - 2.474.261,3373 kJ = -2,294 x 106 kJ
Air pendingin yang digunakan pada suhu 30 oC dan keluar sebagai air pendingin bekas pada suhu 60 oC.
H (60 oC) = 251,1 H (30 oC) = 125,7
Jumlah air pendingin yang diperlukan :
m = H
dT dQ
kg/hari 2
18.292,096
kJ/kg ) 1 , 251 7 , 125 (
kJ/hari 10
x 2,294 -m
6
Tabel LB.30 Neraca Energi pada Cooler (E-404)
Komponen
Masuk (kJ/hari)
Keluar (kJ/hari)
27 28
CO2 2.474.261,3373 180.432,4764
Q -2.293.828,8609 -
Irma Suraya 08 0405 001
Universitas Sumatera Utara LB.13 Cooler ( E-315 )
Fungsi : Untuk menurunkan suhu gas sebelum memasuki kolom PSA.
E-315
29 30
Aliran 29 adalah aliran gas dan cairan keluar kompresor (JC-314). Dari perhitungan pada spesifikasi JC-314, diketahui T29 = 179,8182oC. Entalpi gas dan cairan keluaran kompresor dapat dilihat pada tabel LB-31
))
Tabel LB.31 Entalpi gas dan cairan output Kompresor (JC-314)
Komponen N (kmol) ∫Cp dT H
H2 509,245 4.522,4084 2.303.013,8506
CO2 3,243 6.234,7795 20.219,43244
Hin (kJ) 2.323.233,2831
Air pendingin
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Gas dan cairan sebelum diumpankan ke kolom PSA T-316 suhunya diturunkan hingga 60 0C dengan menggunkan air pendingin, sehingga dapat dihitung Entalpi gas dan cairan pada suhu 60 0C,
Tabel LB.32 Entalpi gas dan cairan output Cooler (E-315)
Komponen N (kmol) ∫Cp dT H
H2 509,245 1.005,267837 511.927,6197
CO2 3,243 1.326,494884 4.301,831952
Hout (kJ) 516.229,4517
Jumlah air pendingin yang diperlukan :
m = H
dT dQ
Irma Suraya 08 0405 001
Universitas Sumatera Utara
kg/hari
Fungsi : Mendinginkan gas H2 sebelum disimpan dalam tangki penyimpanan gas H2.
E-407
33 34
Aliran 33 adalah aliran gas CO2 keluar kompresor (JC-406). Dari perhitungan pada spesifikasi JC-406, diketahui T33 = 73,0275oC. Entalpi gas CO2 keluaran kompresor dapat dilihat pada tabel LB-2
)
Tabel LB.33 Entalpi gas output Kompresor (JC-406)
Komponen N (kmol) ∫Cp dT H
H2 508,7358 1.382,8966 703.528,9269
gas sebelum disimpan suhunya diturunkan hingga 40 0C dengan menggunakan air pendingin, sehingga dapat dihitung Entalpi gas pada suhu 40 0C,
Air pendingin
Irma Suraya 08 0405 001
Universitas Sumatera Utara
)
Tabel LB.34 Entalpi gas output Cooler (E-407)
Komponen N (kmol) ∫Cp dT H
CO2 508,7358 429,0165 218.256,0432
Qin -Qout dt
dQ
= 218.256,0432 kJ - 703.528,9269 kJ = -4,8527 x 105 kJ
Air pendingin yang digunakan pada suhu 30 oC dan keluar sebagai air pendingin bekas pada suhu 60 oC.
H (60 oC) = 251,1 H (30 oC) = 125,7
Jumlah air pendingin yang diperlukan :
m =
Tabel LB.35 Neraca Energi pada Cooler (E-407)
Komponen
H2 703.528,9269 218.256,0432
Q -485.272,8837 -
Irma Suraya 08 0405 001
Universitas Sumatera Utara
LAMPIRAN C
PERHITUNGAN SPESIFIKASI PERALATAN
LC.1 Bak Umpan LCPKS (BK-101)
Fungsi : Menampung LCPKS
Bentuk : Bak Silinder vertikal dengan alas datar Bahan konstruksi : Beton Kedap air
Jumlah : 1 unit
Kondisi operasi : P = 1 atm T = 30 0C
Waktu tinggal ( τ ) : 3 hari
Laju alir massa (F) = 443.835,6164 kg/hari Densitas () = 983,24 kg/m3
Faktor kelonggaran = 20 % (Perry dan Green,1999)
Menghitung volume tangki :
Laju alir volumetrik (Q) = 3
kg/m 983,24
/ 64
443.835,61 kg hari
= 451,4011 m3/hari Volume larutan = τ x Q = 3 hari x 451,4011 m3/hari = 1354,203 m3 Volume tangki, VT = ( 1+ 0,2 ) x 1354,203 m3
= 1.625,044 m3 Perhitungan ukuran bangunan Ukuran bak :
Panjang bak (p) = 2 x lebar bak (l) maka p = 2l Tinggi bak (t) = ½ x lebar bak (l) maka t = ½ l Maka :
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Panjang bak (p) = 22,9412 m Tinggi bak (t) = 5,735 m
Lebar bak (l) = 11,47 m Tinggi larutan dalam bak = x 5,74 m
1625,044 1354,2033
= 4,78 meter LC.2 Pompa (J-102)
Fungsi : Memompa LCPKS ke Bak Neutralisasi Jenis : Pompa screw pump
Bahan konstruksi : Commercial Steel
Jumlah : 1 unit
Kondisi operasi :
Tekanan = 1 atm Temperatur = 60 oC
Laju alir massa (F) = 443.835,6164 kg/hari = 11,325 lbm/sec Densitas () = 983,24 kg/m3 = 61,3815 lbm/ft3 Viskositas () = 0,4688 cP = 0,000315 lbm/ft.s
Laju alir volumetrik, 3
m m
ft / lb 61,3815
/sec lb 11,325 ρ
F
Q 0,1845 ft3/sec
= 0.005225 m3/sec
Desainpompa:Asumsi aliran turbulen
Dopt = 0,363 (Q)0,45(ρ)0,13 (Peters,et.al., 2004) = 0,363 x (0.005225)0,45x (983,24)0,13
= 0,0836 m = 3,2904 in
Dari Appendiks A.5 Geankoplis (1997), dipilih pipa commercial steel : Ukuran nominal : 312 in
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Diameter Dalam (ID) : 3,548 in = 0,2956 ft Diameter Luar (OD) : 4,00 in = 0,3333 ft Inside sectional area : 0,0687 ft2
Kecepatan linear, v = Q/A = 2 Friction loss :
1 Sharp edge entrance= hc = 0,55
= 0,1681 ft.lbf/lbm
1 check valve = hf = n.Kf.
=0,2242 ft.lbf/lbm
Irma Suraya 08 0405 001
Universitas Sumatera Utara
1 Sharp edge exit = hex =
Dari persamaan Bernoulli :
Irma Suraya 08 0405 001
Universitas Sumatera Utara
LC.3Tangki Pre-Treatment (M-103)
Fungsi : Mencampur LCPKS dengan NaOHdan dilakukan pemanasan untuk menonaktifkan bakteri metanasi.
Bentuk : Silinder vertikal dengan alas datar dan tutup elipsoidal Bahan Konstruksi : Carbon steel SA-285 grade C
Jumlah : 1 unit Kondisi operasi :
P = 1 atm T = 80 0C
Waktu tinggal ( τ ) = 1 jam
Laju alir massa (F) = 445.610,959 kg/hari Densitas () = 216,57 kg/m3 Viskositas () = 0,357 cP
Faktor kelonggaran = 20 % (Perry dan Green,1999)
Menghitung volume tangki :
Laju alir volumetrik (Q) = 3 kg/m 216,57
/ 9
445.610,95 kg hari
= 2057,5507 m3/hari Volume bahan = τ x Q =1 jam x (1 hari/24 jam) x 2.057,5507 m3/hari
= 85,7313 m3
Volume tangki, VT = ( 1+ 0,2 ) x 85,7313 m3 = 102,8775 m3
Perbandingan tinggi tangki dengan diameter tangki (HS : DT ) = 1:1 Volume silinder =
: 1:1
4
1 2
T S S
T H H D
D
= 3
4 1
T
D
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Diameter tutup = diameter tangki = 5,079 m Asumsi Hh : Di = 1 : 4
Tinggi tutup = 1,27 m
Tinggi total = 5,079 + 1,27 = 6,35 m Menghitung tebal shell tangki
(Perry, 1999)
Dimana:
t = tebal shell (in)
P = tekanan desain (Psia) R = jari-jari dalam tangki (in) S = allowable stress (Psia) E = joint efficiency
n = umur alat (tahun)
C = corrosion allowance (m/tahun) Volum larutan = 85,7313 m3 Volum tangki = 102,8775 m3 Tinggi larutan dalam tangki = Tekanan hidrostatik
P = ρ x g x l
= 216,5735 kg/m3 x 9,8 m/det2 x 5,2911 m = 11.229,9318 Pa = 1,6289 psia
Faktor kelonggaran = 20 % Maka, Pdesain = (1,2) (P operasi)
= 1,2 ( 14,696 + 1,6289) = 19,5899 psia
Dari Walas, 1988 diperoleh bahwa tekanan desain dari bejana yang beroperasi pada tekanan 0-10 psig adalah 40 psig atau 54,696 psia.
- Direncanakan bahan konstruksi Carbon Steel SA-285 grade C - Allowable working stress (S) : 13.700 psia (Peters et.al., 2004) - Joint efficiency (E) : 0,85
- Corossion allowance (C) : 0,125 in/tahun C
n P SE
PR
t .
6 ,
0
m x6,35 5,2911 8775
, 102
7313 ,
Irma Suraya 08 0405 001
Universitas Sumatera Utara - Umur alat : 10 tahun
t = 1,721 in
tebal shell standar yang digunakan adalah 1 3/4 in (Brownell&Young,1959) menghitung tebal tutup tangki
Tutup atas tangki terbuat dari bahan yang sama dengan shell
Tebal tutup atas = 1 3/4 in (Brownell&Young,1959)
Perancangan Sistem pengaduk
Jenis : flat 6 blade turbin impeller Baffle : 4 buah
Kecepatan putaran (N) : 1 rps (Geankoplis, 2003) Efisiensi motor : 80 %
Pengaduk didesain dengan standar berikut :
Da : Dt = 0,3 J : Dt = 1 : 12 W : Da = 1 : 5
L : Da = 1 : 4 E : Da = 1:1 (Geankoplis, 2003) Jadi :
1. Diameter impeller (Da) = 0,3 x Dt = 1,52 m = 4,999 ft 2. Tinggi pengaduk dari dasar (E) = Da = 1,52 m
3. Lebar baffle ( J) = 0,42 m 4. Lebar daun baffle (W) = 0,3 m 5. Panjang daun impeller (L) = 0,38 m Daya untuk pengaduk :
Bilangan Reynold (NRe) =
357 , 0
5735 , 216 52
, 1
1 2
2
a D N
= 1.409.077,48
NRe>10.000, sehingga daya tidak tergantung pada bilangan reynold, persamaan menjadi :
c 5 3 T
g Da N k
P (McCabe dkk., 1999)
kT = 0,32
54,696
10 0,125
6, 0 ) 85 , 0 13700 (
9781 , 199 2 1 696 , 54
x x
x x
t
Irma Suraya 08 0405 001
Universitas Sumatera Utara
P = 2
3 5
5 3
3
det . / . 147 , 32
/ 5207 , 13 99
, 4 det 1 32 , 0
lbf ft lbm
ft lbm ft
= 420,3374 ft.lbf/det = 0,7642 hp Efisiensi motor, η = 80 %
Jadi daya motor = 0,9553 hp Menghitung Jaket Steam,
Jumlah steam (1500C) = 13.297,141 kg/hari Densitas steam = 2,5458 kg/m3
Laju alir steam (Qw) =
kg/m 2,5458
kg/hari 13.297,141
3 = 5.223,117 m
3/hari Diameter dalam jaket = diameter dalam + (2 x tebal dinding)
= 199,9781 in + [2(1,75 in)] = 203,4781 in
Tinggi jaket = tinggi tangki = 5,0795 m Ditetapkan jarak jaket = 5 in
Diameter luar jaket (D) = 203,4781 in + (2 ×5) in = 213,4781 in = 22,9346 m Luas yang dilalui steam (A),
A =
4
(D2-d2) =
4
(213,47812– 203,47812) = 3.273,1058 in2 = 2,117 m2 Kecepatan steam (v),
v =
A Qw
= 2
3
m 2,117
/hari m 5.223,117
= 2.473,4352 m/hari Tebal dinding jaket (tj),
Pdesain = 19,5899 psia
Jenis sambungan = Double welded butt joint Joint Efficiency = 0,85
Allowable Stress = 13.700 lb/in2 (Peters et.al., 2004) Korosi yang diizinkan (c) = 0,125 in/tahun
Tebal shell jaket (t), c SE
2 D P (t) jaket
Tebal t
Irma Suraya 08 0405 001
Universitas Sumatera Utara
dimana : t = tebal dinding jaket (in) P = tekanan desain (lb/in2) Dt = diameter dalam jaket (in) S = allowable working stress(lb/in2) E = efisiensi pengelasan
c = korosi yang diizinkan (in)
in 0,3046
125 , 0 85 , 0 700 . 13 2
4781 , 213 19,5899 d
Dipilih tebal jaket standar 1/2 in.
LC. 4 Gudang Penyimpanan Natrium Hidroksida(NaOH) (L-104) Fungsi : Menyimpan NaOH selama 3 hari
Bahan Konstruksi : Dinding dari beton, lantai aspal dan atap dari seng Bentuk : Prisma segi empat beraturan
Jumlah : 1 unit
Data Perhitungan:
Temperatur, T =30oC
Tekanan, P = 1 atm
Kebutuhan perancangan, t = 3 hari
Laju alir massa, F = 1.775,343 kg/hari ρ NaOH, ρ = 2.100 kg/m3
(Wikipedia, 2012) Kapasitas gudang = 1.775,343 kg/hari × 3 hari = 5.326,028 kg.
NaOH dikemas dalam goni plastik dengan kapasitas 20 kg/goni. Maka goni yang dibutuhkan =
goni kg
kg / 20
028 , 326 . 5
266,3014 goni Tinggi gudang:
Asumsi tebal 1 goni plastik = 15 cm Maksimal tumpukan goni = 20 buah Faktor kelonggaran = 30%
Irma Suraya 08 0405 001
Universitas Sumatera Utara Panjang gudang:
Direncanakan susunan goni = 30 goni × 15 goni Dimana panjang 1 goni = 40 cm
Faktor kelonggaran = 30% Untuk jalan dalam gudang = 30%
Panjang gudang yang dibutuhkan = 1,3 × 40 cm × 30 = 15,6 m = 16 m.
Lebar gudang :
Faktor kelonggaran = 30 % Dimana lebar 1 goni 20 cm
Lebar gudang yang dibutuhkan = 1,3 × 20 cm × 15 = 390 cm = 3,9 m ≈ 4 m.
LC.5 Belt Conveyor (C-105)
Fungsi : mengangkut NaOH ke M-103 Jenis : Continuous belt conveyor Bahan : Carbon steel
Kondisi operasi : Temperatur = 300C Tekanan = 1 atm Laju bahan : 1.775,343 kg/hari Faktor kelonggaran : 12 % Kapasitas total belt conveyor:
= 1,12 Laju bahan = 1,12 1.775,343 kg/hari = 1.988,384 kg/hari = 0,0828 ton/jam
Untuk belt conveyor kapasitas < 32 ton/jam, spesifikasi :
(Tabel 21–9, Perry, dkk., 1999)
- Lebar beltconveyor = 14 in - Luas permukaan muatan = 0,11 ft2 - Lapisan belt maksimum = 5
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Perhitungan daya yang dibutuhkan (P):
L m 0,0027
P 0,82 (Peters, dkk., 2004) Dimana: P = daya (kW)
m = laju alir massa (kg/s) L = panjang conveyor (m) m = 0,0828 ton/jam = 0,023 kg/s
L = 25 ft = 7,62 m
Maka P0,0027(0,023)0,82(7,62)0,000934kW
= 0,001252 hP Digunakan daya 0,05 hP. LC.6 Pompa (J-106)
Fungsi : Memompa campuran pre-treatment ke Tangki Pencampur
Jenis : Pompa screw pump Bahan konstruksi : Commercial Steel
Jumlah : 1 unit
Kondisi operasi :
Tekanan = 1 atm Temperatur = 80 oC
Laju alir massa (F) = 445.610,9589 kg/hari = 11,3703 lbm/sec Densitas () = 216,5735 kg/m3 = 13,5201 lbm/ft3 Viskositas () = 0,3569 cP = 0,00024 lbm/ft.s
Laju alir volumetrik, 3
m m
ft / lb 13,5201
/sec lb 11,3703 ρ
F
Q 0,8409 ft3/sec
= 0.0238 m3/sec
Desainpompa:Asumsi aliran turbulen
Irma Suraya 08 0405 001
Universitas Sumatera Utara = 0,1359 m = 5,3491 in
Dari Appendiks A.5 Geankoplis (1997), dipilih pipa commercial steel : Ukuran nominal : 6 in
Schedule number : 40
Diameter Dalam (ID) : 6,065 in = 0,5054 ft Diameter Luar (OD) : 6,625 in = 0,5521 ft Inside sectional area : 0,2006 ft2
Kecepatan linear, v = Q/A = 2
Dari Fig.2.10-3 Geankoplis (1997), diperoleh harga f = 0,0041 Friction loss :
1 Sharp edge entrance= hc = 0,55
= 0,4097 ft.lbf/lbm
1 check valve = hf = n.Kf.
Irma Suraya 08 0405 001
Universitas Sumatera Utara
Pipa lurus 30 ft = Ff = 4f
Dari persamaan Bernoulli :
Irma Suraya 08 0405 001
Universitas Sumatera Utara =
s lbf ft
hp / . 550
1 x ft.lbf/lbm
58,3065 lbm/s
11,3707
= 1,205 Hp
Maka dipilih pompa dengan daya motor = 1 1/4 Hp
LC.7Tangki Pencampur LCPKS dan nutrisi (M-107)
Fungsi : Mencampur campuran dengan nutrisi
Bentuk : Silinder vertikal dengan alas datar dan tutup elipsoidal Bahan Konstruksi : Carbon steel SA-285 grade C
Jumlah : 1 unit Kondisi operasi :
P = 1 atm T = 79,97 0C
Waktu tinggal ( τ ) = 1 hari
Laju alir massa (F) = 445.709,1531 kg/hari Densitas () = 216,6175 kg/m3 Viskositas () = 0,357 cP
Faktor kelonggaran = 20 % (Perry dan Green,1999)
Menghitung volume tangki :
Laju alir volumetrik (Q) = 3
kg/m 216,6175
/ 31
445.709,15 kg hari
= 2057,5859 m3/hari Volume bahan = τ x Q =1 hari x 2057,5859 m3/hari
= 2057,5859 m3
Volume tangki, VT = ( 1+ 0,2 ) x 2057,5859 m3 = 2.469,1031 m3
Perbandingan tinggi tangki dengan diameter tangki (HS : DT ) = 1:1 Volume silinder =
: 1:1
4
1 2
T S S
T H H D D
= 3
4 1
T
D