1
PENGUJIAN
METHYLENE BLUE
TEST
PADA ARSIP MIKROFILM
I. PENDAHULUAN
A. Latar Belakang
Dalam rangka mendukung preservasi dan pelayanan arsip
terhadap publik, dilakukan salah satunya proses alih media arsip
kertas ke dalam bentuk mikrofilm. Dalam proses alih media
tersebut, diperlukan suatu tahapan processing. Hasil tahapan processing mikrofilm sangat memegang peranan penting dalam penentuan kualitas microfilm. Proses pencucian mikrofilm yang
tidak sempurna akan menyebabkan hilangnya density dari gambar
dan akan menyebabkan terbentuknya noda pada daerah yang
memiliki density yang rendah. Proses kerusakan ini akan
dipercepat oleh kondisi tempat penyimpanan yang tidak sesuai.
Salah satu parameter yang menunjukkan kualitas optimal
tidaknya processing microfilm adalah penentuan kadar residu thiosulfat, yang dapat diuji pada mikrofilm yang telah mengalami
proses pencucian. Semakin rendah kadar thiosulfat, semakin baik
proses pencucian.
Sesuai dengan tugas dan fungsi Subdit Instalasi Laboratorium
yaitu diantaranya adalah melaksanakan pengujian hasil reproduksi
arsip, maka program kerja Subdit Instalasi laboratorium tahun
anggaran 2008 adalah melaksanakan pengujian methylene blue test pada arsip microfilm. Hal ini tertuang dalam Peraturan kepala
Arsip Nasional Republik Indonesia Nomor 01 A Tahun 2008
Tentang Rencana Kinerja Tahunan Arsip Nasional Republik
2 B. Maksud dan Tujuan
Maksud pengujian ini adalah untuk mengetahui kandungan
thiosulfat pada arsip microfilm sehingga diketahui kualitas arsip
microfilm hasil processing.
Adapun tujuannya adalah untuk mendukung pelestarian
microfilm sehingga dapat digunakan bagi para pengguna secara
maksimal.
II. PELAKSANAAN
1. Waktu dan Tempat Pelaksanaan
Pelaksanaan kegiatan dilakukan selama 12 (dua belas) bulan,
dari bulan Januari hingga Desember 2008.
Pengujian dilakukan di Subdit Instalasi Laboratorium,
Gedung D lantai 2, sedangkan sampling dilakukan di ruang
processing Subdit Reproduksi Arsip, Gedung D lantai 3.
2. Pelaksana
Koordinator pengujian adalah Yanah Suryanah, Dipl.Kim.
sedangkan pelaksana pengujian adalah staf laboratorium yaitu
Sari Hasanah, S.Si dan Roby Syafurjaya, A.Md. Adapun Sampling
dilakukan oleh Umar Yakub dari subdit Reproduksi Arsip.
3. Limitasi
Pengujian yang dilakukan pada tahap ini masih dalam
tahapan pra penelitian / trial and error mengingat pengujian methylene blue test ini belum pernah dilakukan sebelumnya oleh
Subdit Instalasi laboratorium dan peralatan pengujian ini baru
3 4. Peralatan dan bahan
a. Peralatan
1. Spektrofotometer visible double beam;
2. Buret;
3. Vial/tabung reaksi;
4. Gunting;
5. Erlenmeyer;
6. Gelas piala;
7. Pengaduk;
8. Labu ukur;
9. Botol semprot.
b. Bahan Kimia
1. KI;
2. KH2PO4;
3. KBH4;
4. NaOH 0.2 M; 5. FeC13.6H20;
6. N,N-dimethy-p-phenylenediamine sulfate; 7. KIO3/K2Cr2O7;
8. Aseton;
9. Natrium karbonat;
10. Akuadest.
c. Contoh
Arsip microfilm hasil processing.
C. Metode Pengujian
Berdasarkan ISO 1897 tentang photography-Determination of
4 photographic materials-methods using methylene blue test, tahapan
kerja yang dilakukan dalam pengujian methylene blue test adalah
sebagai berikut:
1. Sampling
Sampel uji microfilm diambil dari satu kali processing yang
terdiri dari ± 10 reel microfilm yang kemudian disambung
menjadi satu gulungan besar dalam magazine. Ujung film yang
disambung dipotong ± 5 cm (contoh film yang tidak ada gambar
dan berwarna hitam). Pengujian methylene blue test ini harus
segera dilaksanakan selama dalam jangka waktu 2 minggu
setelah processing.
2. Pembuatan Pereaksi
a. Eluen
Larutkan 1,0 g ± 0,1 g KI dan 1,0 g ± 0,1 g KH2PO4 dengan air dalam labu ukur 1 liter. Encerkan hingga batas dan kocok.
Pereaksi ini stabil selama 1 bulan.
b. Pereaksi Borohydrate
Larutkan 3.0 g KBH4 (Potassium tetrahydroborate) segar dalam 100 ml larutan NaOH 0.2 M (8.0 g/l). Pereaksi ini
stabil selama l minggu di tempat dingin. Bila wadah sudah
dibuka 1 kali, maka harus dibuang pada akhir pemeriksaan.
c. Aseton
d. Feri klorida
Pada kira-kira 50 ml air dalam beaker, tambahkan hati-hati
sambil diaduk, 37.5 ml HCI. Larutkan 8.45 g ± 0.01 g
feriklorida hexahidrat (FeC13.6H20) dalam asam encer, dinginkan sampai suhu ruang dan pindahkan ke labu
volumetri 100 ml. Encerkan dengan air sampai batas dan
5 e. NND
Pada kira-kira 50 ml air dalam beaker, tambahkan hati-hati
sambil diaduk, 12,5 ml HCI. Larutkan 3,00 g ± 0.01 g
N,N-dimethy-p-phenylenediamine sulfate dalam asam encer,
dinginkan sampai suhu ruang dan pindahkan ke labu
volumetrik 100 ml. Encerkan dengan air sampai batas dan
kocok baik-baik. Pereaksi ini stabil paling tidak 1 minggu.
3. Pembuatan kurva kalibrasi
Kurva kalibrasi baru dibuat ketika pereaksi yang baru
digunakan. Kurva diperiksa dalam interval waktu tertentu
misalnya satu kali dalam setiap minggu.
a. Persiapan larutan standar thiosulfat (larutan disiapkan pada
saat hanya akan digunakan)
Pipet 25.0 ml larutan thiosulfat 0.1 M ke dalam labu
volumetnik 500 ml dan encerkan dengan air sampai tanda
batas. Tutup dan balikkan labu 8 sampai 10 kali. Pipet 5.0 ml
larutan diatas ke labu volumetrik 250 ml dan encerkan
dengan air sampai tanda batas.Tutup dan balikkan labu 8
sampai 10 kali. Larutan ini mengandung 11,2 µg/mI
thiosulfat.
b. Pembuatan deret standar
Deret standar dibuat dengan mengencerkan larutan
6
No Volume larutan
standar
Dari masing-masing labu volumetrik dipipet larutan sebanyak
5 ml ke dalam 7 buah vial.
c. Pengukuran Absorbansi
1. Pindahkan pereaksi borohydride (1.b.); aseton; pereaksi
feriklorida (1.d); pereaksi NND (1.e.) ke dalam 4 buret
terpisah.
2. Kepada masing-masing vial yang berisi larutan 5 ml
larutan standar (3b.) ditambahkan masing-masing
pereaksi berikut tanpa delay time/langsung antara penambahan.
a. Tambahkan 0.25 ml pereaksi borohydrate, aduk
supaya campur.
b. Tambahkan 0.50 ml aseton, aduk supaya campur
c. Tambahkan 0.25 ml pereaksi feri klorida dan 0.25 ml
pereaksi NND.
3. Vial segera ditutup kuat-kuat dan dikocok selama 1
menit. Kemudian secara hati-hati dikeluarkan tekanan
yang terbentuk dengan adanya gas hidrogen, pastikan
bahwa vial jauh dan muka, lalu segera diukur dengan
7 4. Analisa blangko dilakukan dengan menggantikan 5 ml
larutan standar tiosulfat dengan 5 ml eluent.
4. Analisa Sampel
a. Potong 1 cm2 sample microfilm kemudian letakkan sample pada vial yang bersih dan kering. Tambahkan 10.0 ml eluent
(1.a.) dan biarkan campuran selama 10 menit, sekali-kali
dikocok (l menit - 3 menit). Pipet 5.0 ml ekstrak ke sample
vial yang lain.
b. Ke dalam vial ditambahkan masing-masing pereaksi berikut
tanpa delay time antara penambahan.
a. Tambahkan 0.25 ml pereaksi borohydrate, aduk supaya
campur.
b. Tambahkan 0.50 ml aseton, aduk supaya campur
c. Tambahkan 0.25 ml pereaksi feri klorida dan 0.25 ml
pereaksi NND.
c. Vial segera ditutup kuat-kuat dan dikocok selama 1 menit.
Kemudian secara hati-hati dikeluarkan tekanan yang
terbentuk dengan adanya gas hidrogen, pastikan bahwa vial
jauh dan muka, lalu segera diukur dengan
spektrophotometer pada panjang gelombang 665 nm.
D. Hasil Pengujian dan Pembahasan
Sebagai pengujian awal dalam Pengujian Methylene Blue Test
pada Arsip Mikrofilm, maka dalam pengujian ini laboratorium
mencoba untuk melakukan pengujian/pengukuran larutan standar
untuk dibuat kurva kalibrasi dengan berbagai macam variasi
perlakuan. Hal ini dikarenakan kurva kalibrasi sangat memegang
peranan penting dalam penentuan konsentrasi sampel uji.
1. Dalam analisa blangko, seharusnya digunakan 5 ml eluent
8 digunakan 5 ml air suling dalam analisa blangko, maka akan
menunjukkan absorbansi dengan hasil negative.
2. Pengujian methylene blue test ini sangat memerlukan
ketelitian yang tinggi sehingga harus dibuat galat/kesalahan
seminimal mungkin karena akan terdeteksi di dalam alat
spektrofotometer. Untuk menghasilkan kurva kalibrasi yang
bagus (R ~ 1), dilakukan beberapa kali uji coba pembuatan
kurva kalibrasi:
o Percobaan 1
Deret standar yang dibuat termuat dalam Tabel 1.
Berikut:
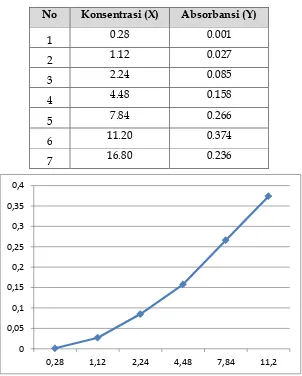
Tabel 1. Absorbansi larutan standar
No Konsentrasi (X) Absorbansi (Y)
1 0.28 0.001 2 1.12 0.027 3 2.24 0.085 4 4.48 0.158 5 7.84 0.266 6 11.20 0.374 7 16.80 0.236
Gambar 1. Kurva kalibrasi
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35 0,4
9 Dari Gambar 1. di atas dibuat 7 (tujuh) konsentrasi
larutan standar dan menghasilkan tingkat kemiringan kurva
R1 sebesar 0.665 dan R2 sebesar 0.443. Namun, kurva
kalibrasi ini tidak bisa digunakan untuk menghitung
konsentrasi sample karena kurva kalibrasi tidak linier,
bahkan untuk konsentrasi 16.80, absorbansi yang seharusnya
naik menjadi turun (Tabel 1.)
o Percobaan 2
Deret standar yang dibuat termuat dalam Tabel 2. Berikut:
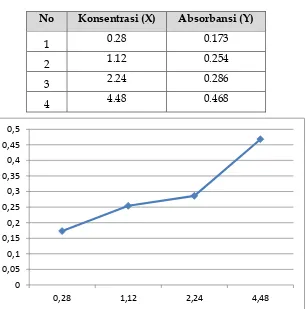
Tabel 2.Absorbansi Larutan Standar
No Konsentrasi (X) Absorbansi (Y)
1 0.28 0.173 2 1.12 0.254 3 2.24 0.286 4 4.48 0.468
Gambar 2.Kurva Kalibrasi
Tingkat kemiringan kurva pada gambar 2. di atas lebih
baik dari kurva pada Gambar 1. yaitu sebesar R1 0.988 dan
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35 0,4 0,45 0,5
10 R2 0.976. Namun, kurva kalibrasi ini tetap tidak bisa
digunakan dalam penghitungan sample uji.
o Percobaan 3
Percobaan ini menggunakan blangko (eluent) sehingga
dalam table di plot sebagai standar 1.
Tabel 3. Absorbansi Larutan Standar
No Konsentrasi (X) Absorbansi (Y)
1 0.00 0.084 2 0.14 0.211 3 0.28 0.223 4 1.12 0.239 5 2.24 0.281 6 4.48 0.330
Gambar 3.Kurva Kalibrasi
Tingkat kemiringan masih jauh dari mendekati 1 yaitu R1
0.691 dan R2 0.478.
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35
11 o Percobaan 4
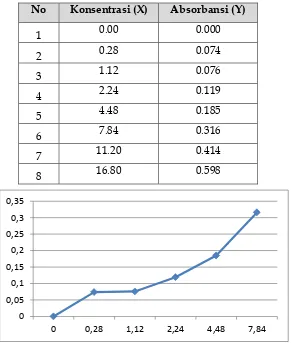
Tabel 4. Absorbansi larutan standar
No Konsentrasi (X) Absorbansi (Y)
1 0.00 0.000 2 0.28 0.074 3 1.12 0.076 4 2.24 0.119 5 4.48 0.185 6 7.84 0.316 7 11.20 0.414 8 16.80 0.598
Gambar 4. Kurva Kalibrasi
Gambar 4 memiliki R yang bagus (dua angka dibelakang
koma mencapai 9) yaitu R1 0.995 dan R2 0.991. Sampel uji
dari microfilm kemudian di plot ke dalam kurva kalibrasi
ini dan menghasilkan konsentrasi sebesar 0.00 (table 5).
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35
12 Tabel 5. Konsentrasi Sampel uji
No Absorbansi Konsentrasi
1 0.016 0.00 2 0.025 0.00
o Percobaan 5
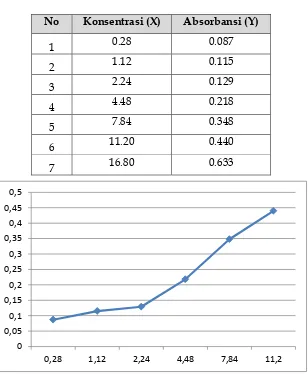
Tabel 6. Absorbansi Larutan Standar
No Konsentrasi (X) Absorbansi (Y)
1 0.28 0.087 2 1.12 0.115 3 2.24 0.129 4 4.48 0.218 5 7.84 0.348 6 11.20 0.440 7 16.80 0.633
Gambar 5. Kurva Kalibrasi
Kurva kalibrasi pada percobaan 5 ini memiliki kurva
kalibrasi dengan kemiringan yang baik yaitu R1 0.998 dan
R2 0.997. Konsentrasi sample uji pada setiap reel microfilm
termuat dalam Tabel 7.
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35 0,4 0,45 0,5
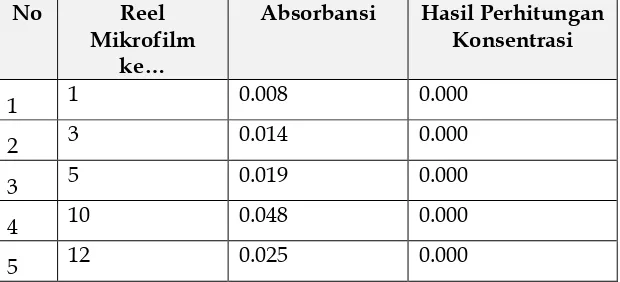
13 Tabel 7. Konsentrasi Sampel Uji
No Reel Mikrofilm
ke…
Absorbansi Hasil Perhitungan Konsentrasi
microfilm lainnya dan dapat dilihat pada Tabel 8. Dan Tabel
9.
Tabel 8. Konsentrasi Sampel Uji pada Reel Mikrofilm yang
Sama
No Reel
Mikrofilm ke… Absorbansi Perhitungan Hasil Konsentrasi
1 9 0.047 0.000 2 9 0.038 0.000 3 9 0.054 0.000
Tabel 9. Konsentrasi Sampel Uji pada Reel Mikrofilm yang
Sama
terdeteksi). Banyak factor yang mempengaruhi hasil uji ini
diantaranya sampling, preparasi sampel uji, kesalahan
14 pengukuran kadar thiosulfat perlu dilakukan pengujian
lanjutan sehingga didapatkan hasil yang reliable.
III. HAMBATAN
Hambatan yang dialami dalam pelaksanaan pengujian ini adalah :
1. Subdit Instalasi Laboratorium ANRI belum pernah melakukan
pengujian methylene blue test ini sebelumnya dikarenakan bahan
kimia dan peralatan pengujian ini baru terealisasi.
2. Belum adanya sampel arsip microfilm hasil processing karena
keterlambatan pengadaan bahan kimia untuk processing.
3. Belum adanya laboratorium di Indonesia yang melakukan
pengujian methylene blue test ini sesuai ISO 1897 ( photography-Determination of residual thiosulfate and other reelated chemicals in processed photographic materials-methods using methylene blue test). 4. Sulit untuk mengaplikasikan teori ke bentuk praktek karena
merupakan pengetahuan baru.
IV.UPAYA MENGATASI HAMBATAN
Dilakukan uji coba/trial and error di laboratorium ANRI sehingga
didapatkan hasil pengujian yang terpercaya. Sampel diambil bukan dari
arsip microfilm hasil processing, tetapi microfilm yang bukan berisi arsip
yang telah diprocessing.
V.PENUTUP
A. KESIMPULAN
1. Pengujian methyelene blue test ini memerlukan keterampilan
khusus yang hanya bisa diperoleh melalui praktek langsung di
15 2. Hasil yang didapatkan dalam pengujian kali ini adalah didapatkan
kurva kalibrasi yang linier (R ~ 1) yaitu dengan R1 = 0.998 dan R2=
0.997 pada percobaan 5 dengan blangko eluent.
B. SARAN
1. Perlu dilakukan penelitian lanjutan dalam penanganan sample
microfilm sehingga dapat diketahui kadar thiosulfat yang
sebenarnya.
2. Perlu praktek pengujian di laboratorium yang berkompeten di
bidang pengujian methylene blue test yaitu Arsip Nasional
Singapura.
Jakarta, Desember 2008
Mengetahui
Kasubdit Instalasi Laboratorium
Yanah Suryanah, Dipl.Kim 360 000 466
Sekretaris Tim Uji
16