PENCIRIAN SURFAKTAN NONIONIK ESTER GLUKOSA
STEARAT DAN ESTER GLUKOSA OLEAT SEBAGAI
PENGEMULSI, DETERGEN, DAN PEMBUSA
RINI SUFRIYANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2006
ABSTRAK
RINI SUFRIYANI. Pencirian Surfaktan Nonionik Ester Glukosa Stearat dan Ester Glukosa Oleat sebagai Pengemulsi, Detergen, dan Pembusa. Dibimbing oleh KOMAR SUTRIAH dan HENNY PURWANINGSIH.
Ester glukosa stearat dan ester glukosa oleat adalah surfaktan nonionik yang berasal dari minyak nabati dan karbohidrat dengan sifat-sifat, yaitu mudah terdegradasi, tidak menimbulkan iritasi, dan digunakan sebagai zat aditif dalam berbagai industri, seperti makanan, kosmetik, detergen, dan farmasi. Pencirian surfaktan nonionik yang dilakukan meliputi nilai HLB (hydrophile lypophile balance), pH, tegangan permukaan, tegangan antarmuka, stabilitas emulsi, daya detergensi, dan stabilitas pembusaan. Hasil pencirian menunjukkan nilai konsentrasi misel kritis (KMK) ester glukosa stearat dan ester glukosa oleat berturut-turut adalah 0.0024% (b/v) dan 0.0013% (b/v). Penurunan tegangan antarmuka maksimum yang dicapai oleh ester glukosa stearat dan ester glukosa oleat pada konsentrasi 0.0040% (b/v) berturut-turut adalah 27.11 dyne/cm dan 15.14 dyne/cm. Penurunan tegangan permukaan maksimum yang dicapai oleh ester glukosa stearat dan ester glukosa oleat berturut-turut adalah 42.64 dyne/cm dan 28.36 dyne/cm. Nilai HLB ester glukosa stearat dan ester glukosa oleat berturut-turut adalah 7.25 dan 3.85. Daya detergensi dan stabilitas pembusaan terbaik dicapai oleh ester glukosa oleat. Stabilitas emulsi oil in water (O/W) terbaik dicapai oleh ester glukosa stearat, sedangkan stabilitas emulsi water in oil (W/O) terbaik dicapai oleh ester glukosa oleat. Nilai pH dari ester glukosa stearat dan ester glukosa oleat berturut-turut adalah 6.40 dan 6.86.
ABSTRACT
RINI SUFRIYANI. Characterization of Nonionic Surfactant Glucose Stearate
Ester and Glucose Oleate Ester as Emulsifier, Detergent, and Foaming Agent.
Supervised by KOMAR SUTRIAH and HENNY PURWANINGSIH.
Glucose stearate ester and glucose oleate ester are nonionic surfactants from
vegetable oil and carbohydrate which are biodegradable, non-irritant, and can be
used as additive substances in various industries, such as food, cosmetics,
detergent, and pharmacy. Characterization of glucose stearate ester and glucose
oleate ester were HLB
(hydrophile lypophile balance) value, pH value, surface tension, interfacial tension, emulsion stability, detergency power, and foam stability. The result showed that CMC (critical micelle concentration) of glucose stearate ester and glucose oleate ester were 0.0024% (w/v) and 0.0013% (w/v), respectively. The maximum interfacial tension achieved by glucose stearate ester and glucose oleate ester at concentration 0.0040% (w/v) were 27.11 dyne/cm and 15.14 dyne/cm, respectively. The maximum surface tension achieved by glucose stearate ester and glucose oleate ester were 42.64 dyne/cm and 28.36 dyne/cm, respectively. HLB value of glucose stearate ester and glucose oleate ester were 7.25 and 3.85, respectively. The best detergency power and foam stability achieved by glucose oleate ester. The best oil in water (O/W) emulsion stability achieved by glucose stearate ester. The best water in oil (W/O) emulsion stability achieved by glucose oleate ester. pH value achieved by glucose oleate ester and glucose stearate ester were 6.86 and 6.40, respectively.PENCIRIAN SURFAKTAN NONIONIK ESTER GLUKOSA
STEARAT DAN ESTER GLUKOSA OLEAT SEBAGAI
PENGEMULSI, DETERGEN, DAN PEMBUSA
RINI SUFRIYANI
Skripsi
Sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2006
Judul Skripsi : Pencirian Surfaktan Nonionik Ester Glukosa Stearat dan Ester
Glukosa Oleat sebagai Pengemulsi, Detergen, dan Pembusa.
Nama
: Rini Sufriyani
NIM
:
G44201052
Menyetujui:
Pembimbing I, Pembimbing II,
Drs. Komar Sutriah, M.S. Henny Purwaningsih, S.Si., M.Si.
NIP 131950979 NIP 132311914
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Dr. Ir. Yonny Koesmaryono, M.S.
NIP 131473999
PRAKATA
Bismillahirrahmanirrahim…
Alhamdulillah, segala puji bagi Allah SWT karena atas rahmat dan karunia-Nya penulis dapat menyelesaikan karya ilmiah ini. Karya ilmiah ini berjudul Pencirian Surfaktan Nonionik Ester Glukosa Stearat dan Ester Glukosa Oleat sebagai Pengemulsi, Detergen, dan Pembusa yang merupakan hasil penelitian yang dilaksanakan sejak bulan Desember 2005 sampai Maret 2006 di Laboratorium Kimia Organik dan Kimia Fisik Departemen Kimia IPB. Penelitian ini didanai oleh Program Hibah Kompetisi A2, Departemen Kimia IPB.
Penulis mengucapkan terima kasih kepada Bapak Drs. Komar Sutriah, M.S., dan Ibu Henny Purwaningsih Suyuti, S.Si., M.Si. selaku pembimbing yang telah banyak memberikan masukan dan pengarahan kepada penulis. Ungkapan terima kasih juga disampaikan kepada Prof. Dr. Tun Tedja Irawadi, Drs. Muhammad Farid, Muhammad Khotib, S.Si., dan Budi Arifin, S.Si. atas diskusi-diskusi berharga yang berkaitan dengan penelitian ini. Terima kasih kepada Prof. Dr. Suminar S. Achmadi, seluruh dosen dan staf di lingkungan Departemen Kimia IPB, dan Keluarga Besar Laboratorium Kimia Fisik, Kimia Organik, dan Laboratorium Terpadu atas bantuannya selama penelitian berlangsung.
Ungkapan terima kasih yang terdalam dihaturkan kepada keluargaku tercinta atas segala doa, nasihat, dorongan, semangat, dan kasih sayangnya kepada penulis. Ucapan terima kasih juga disampaikan kepada Sekar, Selvi, Desi (telah menjadi sahabat-sahabat terbaik di saat suka maupun duka dalam menjalani hari-hari berat penelitian), Surfactants Team, Mexindo Crew (Quenty, Ujel, Tyas, Poponk, Mbak Riya, Mbak Uji, dan Mbak Ayu) dan rekan-rekan Kimia 38 (khususnya Woro) untuk semua bantuan dan kebersamaan yang indah.
Semoga karya ilmiah ini dapat bermanfaat bagi kita semua.
Bogor, Mei 2006
RIWAYAT HIDUP
Penulis dilahirkan di Serang pada tanggal 23 Desember 1982 sebagai anak pertama dari tiga bersaudara, dari pasangan Sufrani dan Husnaiyah (Alm).
Tahun 2001 penulis lulus dari SMUN I Serang dan pada tahun yang sama diterima di Departemen Kimia Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB (USMI). Selama menjadi mahasiswi, penulis aktif dalam organisasi kemahasiswaan Himpunan Mahasiswa Kimia IPB (Himasika) pada tahun 2002/2003. Penulis juga aktif menjadi asisten di berbagai mata kuliah, di antaranya asisten pratikum Kimia Dasar II, asisten Kimia Fisik S1 Biokimia, dan asisten Kimia Koloid D3 Analisis Kimia. Penulis juga pernah melakukan praktik kerja lapangan di Pusat Penelitian dan Pengembangan
DAFTAR ISI
Halaman
DAFTAR TABEL... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... viii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Surfaktan... 1
Ester Asam Lemak-Karbohidrat ... 2
Tegangan Permukaan dan Tegangan Antarmuka ... 2
Emulsi... 2
Busa ... 2
Kesetimbangan Hidrofil Lipofil (HLB)... 3
Daya Detergensi ... 3
BAHAN DAN METODE Bahan dan Alat ... 4
Metode Penelitian ... 4
HASIL DAN PEMBAHASAN Tegangan Permukaan dan KMK ... 5
Tegangan Antarmuka ... 6 Nilai HLB ... 6 Kestabilan Emulsi... 6 Stabilitas Pembusaan ... 7 Daya Detergensi ... 8 pH ... 8
SIMPULAN DAN SARAN Simpulan ... 8
Saran ... 9
DAFTAR PUSTAKA ... 9
DAFTAR TABEL
Halaman
1 Pengaruh HLB pada kelarutan surfaktan dalam air ... 3
2 pH ester glukosa... 8
DAFTAR GAMBAR
Halaman 1 Fenomena tegangan permukaan... 22 Tegangan permukaan ester glukosa stearat dan ester glukosa oleat ... 6
3 Tegangan antarmuka ester glukosa stearat dan ester glukosa oleat ... 6
4 S
tabilitas emulsi O/W ester glukosa stearat dan ester glukosa oleat ...
75 Stabilitas emulsi W/O ester glukosa stearat dan ester glukosa oleat ...
76 Stabilitas pembusaan ester glukosa stearat dan ester glukosa oleat... 8
7 Daya detergensi ester glukosa stearat ...
88 Daya detergensi ester glukosa oleat ...
8DAFTAR LAMPIRAN
Halaman 1 Penentuan tegangan permukaan... 112 Penentuan tegangan antarmuka... 13
3 Penentuan nilai HLB... 14
4 Penentuan kestabilan emulsi ... 15
5 Penentuan daya pembusaan ... 16
6 Penentuan daya detergensi ... 17
PENDAHULUAN
Indonesia mempunyai kekayaan alam yang sangat melimpah. Di antaranya adalah minyak nabati dan karbohidrat. Minyak nabati dan karbohidrat merupakan sumber daya alam yang dapat diperbaharui dan tersedia terus menerus. Sumber minyak nabati adalah minyak kelapa sawit, minyak jarak, minyak nilam, sedangkan sumber karbohidrat adalah padi, singkong, ubi, jagung, dan lain-lain.
Salah satu industri yang menggunakan minyak nabati dan karbohidrat adalah industri surfaktan. Surfaktan (surface active agent) merupakan zat aktif permukaan yang berfungsi menurunkan tegangan permukaan karena mempunyai dua gugus dalam satu molekul yang masing-masing memiliki tingkat kepolaran yang berbeda, yaitu gugus hidrofilik (polar) dan lipofilik (nonpolar) (Holmberg et al. 2003). Perbedaan sifat tersebut juga menyebabkan surfaktan dapat dijadikan sebagai bahan tambahan dalam berbagai industri, seperti margarin, susu, detergen, cat, kosmetik, dan lain-lain.
Salah satu contoh bahan dasar surfaktan yang sangat potensial adalah minyak kelapa sawit. Kandungan asam lemak yang beragam dalam kelapa sawit menjadi keunggulan yang kompetitif dalam meningkatkan diversifikasi produk olahannya, misalnya asam lemak rantai C12:0-C16:0 berperan dalam sifat
detergensi (Lynn 1993).
Ester glukosa stearat dan ester glukosa oleat merupakan suatu surfaktan nonionik berbahan dasar minyak nabati dan karbohidrat yang memperlihatkan pencirian yang baik, yaitu mudah terdegradasi, tidak menimbulkan iritasi, dan digunakan sebagai bahan baku dalam industri detergen, farmasi, makanan, dan kosmetik (Obaje 2005). Pemanfaatan surfaktan jenis ini memiliki keunggulan, yaitu mampu bersaing dengan surfaktan jenis lain, seperti LAS (Linear Alkil Sulfonat) dan ABS (Alkil Benzena Sulfonat) yang dihasilkan dari minyak bumi.
Penelitian ini bertujuan mencirikan ester glukosa stearat dan ester glukosa oleat sebagai pengemulsi, detergen, dan pembusa. Pencirian dilakukan untuk mengetahui kemampuan dan sifat-sifat utama kedua ester tersebut sebagai surfaktan. Pencirian yang dilakukan meliputi tegangan permukaan, tegangan antarmuka, stabilitas emulsi O/W dan W/O, nilai HLB, nilai pH, stabilitas pembusaan, dan daya detergensi.
TINJAUAN PUSTAKA
Surfaktan
Surfaktan merupakan senyawa yang bersifat sebagai zat aktif permukaan (Sawyert dan McCarty 1978). Molekul surfaktan terdiri atas dua gugus yang memiliki perbedaan kecenderungan kepolaran, yaitu hidrofilik (polar) dan lipofilik (nonpolar). Gugus hidrofilik dapat bermuatan positif, negatif, amfoterik, atau tidak bermuatan (nonionik), yang larut dalam pelarut polar. Gugus lipofilik surfaktan dapat terdiri atas rantai hidrokarbon linear atau bercabang yang tidak larut dalam pelarut polar. Kehadiran gugus hidrofilik dan lipofilik yang berada dalam satu molekul menyebabkan molekul surfaktan cenderung berorientasi pada permukaan antarmuka dalam sebuah sistem dan menurunkan tegangan permukaan (Gervasio 1996).
Surfaktan dapat diproduksi dengan menggunakan dua jenis bahan dasar, yaitu minyak bumi dan minyak nabati. Surfaktan berbahan dasar minyak bumi dan minyak nabati dimodifikasi secara kimia membentuk molekul surfaktan. Surfaktan berbahan dasar minyak nabati memiliki keunggulan dibandingkan minyak bumi, yaitu mudah diperbaharui, mudah terurai secara biologi, dan tidak mencemari lingkungan (Swern 1997).
Menurut Flider (2001), surfaktan berbasis bahan alami dibagi menjadi empat kelompok, yaitu (1) berbahan dasar minyak nabati, seperti monogliserida, digliserida, poligliserol ester, (2) berbahan dasar karbohidrat, seperti alkil poliglukosida, dan n-metil glukamida, (3) ekstrak bahan alami, seperti lesitin dan saponin, (4) biosurfaktan yang diproduksi oleh mikroorganisme, seperti ramnolipid dan soforolipid.
Secara umum surfaktan dikelompokkan berdasarkan pembentukan ionnya dalam air (swern 1997), yaitu
1. Surfaktan anionik, merupakan surfaktan yang gugus hidrofiliknya bermuatan negatif (anion), misalnya ester sulfonat dan alkohol sulfat.
2. Surfaktan kationik, merupakan surfaktan yang memiliki gugus hidrofilik berupa ion bermuatan positif (kation), misalnya senyawa amonium kuaterner.
3. Surfaktan nonionik, merupakan surfaktan yang tidak memiliki muatan pada gugus hidrofiliknya,
2
misalnya alkohol etoksilat dan ester asam lemak-karbohidrat.
4. Surfaktan amfoterik merupakan surfaktan yang memiliki muatan positif sekaligus muatan negatif pada molekul yang sama, seperti pada asam amino.
Ester Asam Lemak-Karbohidrat
Ester asam lemak-karbohidrat merupakan surfaktan nonionik yang memiliki kemampuan baik dalam mengaktifkan permukaan, mudah didegradasi, tidak beracun, tidak menyebabkan iritasi dan alergi, dan memiliki daya busa yang rendah. Jenis surfaktan ini dapat digunakan sebagai zat tambahan untuk produk makanan, kosmetik, farmasi, bahan pembersih, dan pengemulsi yang baik (Akoh dan Swanson 1990).
Ester asam lemak-karbohidrat yang digunakan dalam penelitian ini adalah ester glukosa stearat dan ester glukosa oleat. Perbedaan dari kedua ester ini terletak pada jenis ikatan pada rantai alkil asam lemak.
Tegangan Permukaan dan Tegangan Antarmuka
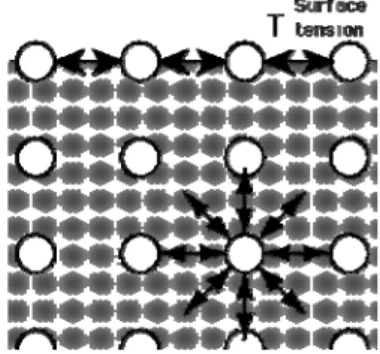
Tegangan permukaan dan tegangan antarmuka merupakan fenomena gaya antarmolekul. Ada dua jenis gaya antarmolekul, yaitu gaya antarmolekul sejenis (kohesi) dan gaya antarmolekul tidak sejenis (adhesi). Tegangan permukaan suatu cairan terbentuk karena adanya ketidakseimbangan gaya antarmolekul cairan di permukaan dengan molekul di badan cairan (Gambar 1). Molekul di badan cairan mengalami gaya tarik menarik yang sama dari segala arah, sedangkan molekul-molekul di permukaan cairan hanya ditarik oleh molekul-molekul lain yang ada di permukaan (sebelah kiri dan kanannya) dan di bawah permukaan sehingga resultan gaya akan mengarah ke badan cairan. Metode yang digunakan untuk mengukur tegangan permukaan pada penelitian ini adalah metode cincin (du Nouy method) (Holmberg et al. 2003).
Tegangan antarmuka didefinisikan sebagai energi yang diperlukan untuk memperluas permukaan 1 cm2 (Adamson 1982). Tegangan
antarmuka yang diamati adalah tegangan antarmuka air dan xilena. Molekul surfaktan yang bersifat ampifilik, yaitu gugus polar mengarah ke molekul-molekul air, sedangkan gugus nonpolar mengarah ke molekul-molekul xilena sehingga molekul-molekul-molekul-molekul
surfaktan akan berada di daerah antarmuka air dan xilena (Holmberg et al. 2003).
Gambar 1 Fenomena tegangan pemukaan molekul surfaktan
Emulsi
Emulsi adalah dispersi cairan dalam cairan lain yang tidak saling bercampur. Emulsi dapat dibentuk dari dua atau tiga fase. Terdapat dua jenis emulsi, yakni emulsi minyak dalam air (O/W) dan emulsi air dalam minyak (W/O). Dalam emulsi O/W, tetesan-tetesan minyak terdispersi dalam medium pendispersi air, sedangkan dalam emulsi W/O tetesan-tetesan air terdispersi dalam medium pendispersi minyak (Holmberg et al. 2003).
Emulsifikasi merupakan fenomena aplikasi adsorpsi pada proses emulsi di daerah antarmuka. Beberapa surfaktan memiliki gugus hidrofilik yang lebih besar dibandingkan gugus lipofiliknya sehingga lebih mudah larut dalam air. Sebaliknya surfaktan yang memilki gugus lipofilik yang lebih besar dibandingkan gugus hidrofiliknya lebih mudah larut dalam minyak atau pelarut-pelarut nonpolar. Faktor-faktor yang memengaruhi pembuatan emulsi di antaranya adalah jenis pengemulsi, suhu, konsentrasi dan struktur surfaktan, dan perbandingan volume dari kedua fase cairan (Adamson 1982). Pecahnya suatu emulsi dapat disebabkan oleh beberapa faktor berikut ini, yaitu proses pembentukan krim (creaming), flokulasi, dan penggabungan (koalesensi) (Friberg dan Jones 1993).
Busa
Busa adalah molekul-molekul gas yang terjebak dalam lapisan tipis cairan yang mengandung sejumlah molekul surfaktan yang teradsorpsi pada lapisan tipis tersebut. Busa akan terbentuk jika larutan surfaktan diaduk atau dialiri udara. Dalam gelembung,
3
gugus lipofilik surfaktan akan mengarah ke gas, sedangkan gugus hidrofilik surfaktan mengarah ke larutan. Saat gelembung keluar dari badan cairan, gelembung akan dilapisi oleh lapisan tipis cairan yang mengandung molekul-molekul surfaktan (Durian dan Weitz 1993).
Beberapa faktor berikut ini yang memengaruhi pembentukan busa, yaitu interaksi surfaktan di daerah antarmuka, struktur surfaktan, dan konsentrasi surfaktan, sedangkan stabilitas busa ditentukan oleh tingkat elastisitas lapisan tipisnya (Durian dan Weitz 1993).
Busa sangat diperlukan dalam beberapa proses industri, misalnya industri makanan, kosmetik, pasta gigi, dan sabun (Durian dan Weitz 1993).
Kesetimbangan Hidrofil-Lipofil (HLB,
Hydrophile-Lypophile Balance)
Sistem HLB pertama kali ditemukan oleh William C. Griffin. Nilai HLB merupakan polaritas relatif yang dimiliki oleh molekul surfaktan yang disebabkan oleh gugus hidrofil dan lipofilnya. Dengan ciri ganda tersebut, surfaktan akan bertindak sebagai jembatan antara dua zat tidak larut satu sama lain. Griffin membagi surfaktan dalam skala 1 sampai 20 (Holmberg et al. 2003).
Tabel 1 Pengaruh HLB pada kelarutan surfaktan dalam air
Kelarutan
dalam air Nilai HLB Aplikasi
Tidak mampu terdispersi dalam air Kemampuan mendispersi kurang baik Dispersi seperti susu;tidak stabil Dispersi seperti susu;stabil Tembus cahaya Untuk larutan jernih Larutan jernih 0 2 4 6 8 10 12 14 16 18 Pengemulsi w/o Wetting agent Detergen Pengemulsi o/w Solubilizer Sumber: Adamson (1982)
Nilai HLB bergantung pada nisbah antara gugus hidrofil dan gugus lipofil dari molekul surfaktan. Nilai HLB yang diperoleh dapat digunakan sebagai acuan dalam meramalkan sifat-sifat dari surfaktan. Berdasarkan Tabel 1 diketahui bahwa jika nilai HLB yang diperoleh rendah, maka akan terdispersi dalam medium minyak (tidak mampu terdispersi dalam air), mempunyai stabilitas pembusaan dan daya detergensi yang rendah. Begitu pula sebaliknya, jika nilai HLB tinggi maka terdispersi dalam medium air, mempunyai stabilitas pembusaan dan daya detergensi yang tinggi (Adamson 1982).
Daya Detergensi
Detergensi adalah proses perpindahan atau pengangkatan kotoran dari serat kain yang meliputi interaksi antara surfaktan, kotoran, dan permukaan kain. Pemilihan jenis surfaktan merupakan salah satu kunci formulasi sebagai bahan pembersih. Surfaktan yang dahulu biasa digunakan adalah sabun Na-asam lemak dan K-asam lemak yang diperoleh dari reaksi saponifikasi trigliserida. Namun, saat ini surfaktan yang digunakan adalah hasil dari proses sintesis, seperti alkohol etoksilat, alkil sulfat, dan alkil eter sulfat (Holmberg et al. 2003).
Kotoran yang melekat pada kain beragam sehingga mekanisme pemindahan atau pengangkatannya beragam pula bergantung pada jenis komponen kotoran. Kotoran dapat berasal dari produk berlemak, seperti minyak sayur, santan, mentega, dan lain-lain. Surfaktan memainkan peranan dalam memindahkan kotoran berlemak dibantu oleh enzim hidrolitik yang ditambahkan dalam formula detergen. Enzim tersebut berfungsi menghidrolisis senyawa-senyawa, seperti trigliserida, protein, dan pati (Holmberg et al. 2003).
Beberapa noda atau zat warna, seperti teh dan darah tidak dapat dipindahkan dari permukaan serat kain meskipun dengan menggabungkan kerja surfaktan dan enzim hidrolitik secara optimal sehingga agen pemutih lebih efektif memindahkan zat warna atau noda tersebut dari permukaan serat kain dengan cara mengubah zat warna tersebut menjadi produk yang tidak berwarna (Holmberg et al. 2003).
Menurut Lynn (1993), faktor-faktor yang memengaruhi daya detergensi adalah konsentrasi surfaktan, struktur surfaktan, komposisi pengotor, dan jumlah pengotor.
4
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah akuades, ester glukosa stearat dan ester glukosa oleat (hasil sintesis yang dilakukan oleh Sari 2006 dan Nugraha 2006), xilena, piridina, benzena, aseton, dan larutan sulfat-kromat.
Alat-alat yang digunakan adalah buret, tensiometer du Nouy model 20 Cole-Parmer,
ultrasonic homogenizer model T8.10
IKA-WERKE, neraca analitik, piknometer, aerator AP−3000, pH meter HM−205 DKK–TOA Corporation, turbidimeter model 2100P HACH, water pass, dan peralatan kaca.
Metode Penelitian
Penentuan Nilai HLB (Gupta et al. 1983 di dalam Kuang et al. 2000). HLB dari
surfaktan ditentukan menggunakan metode bilangan air (water number method). Larutan surfaktan yang mengandung 1 g surfaktan dalam 25 mL campuran piridina dan benzena 95:5 (v/v) dititrasi dengan akuades sampai kekeruhan permanen. Nilai HLB dari sampel surfaktan diperoleh dengan interpolasi pada kurva kalibrasi.
Pengukuran Tegangan Permukaan Metode Du Nouy (ASTM D_1331 2000). Peralatan
dan wadah sampel yang digunakan harus dibersihkan terlebih dulu dengan larutan asam sulfat-kromat dan dibilas dengan akuades, lalu dikeringkan. Cincin platinum yang digunakan pada alat tensiometer du Nouy mempunyai
mean circumference = 5.945.
Posisi alat diatur agar horizontal dengan
water pass dan diletakkan pada tempat yang
bebas dari gangguan, seperti getaran, angin, sinar matahari, dan panas. Larutan surfaktan dengan ragam konsentrasi 0.0000–0.0100% (b/v), dimasukkan ke dalam gelas kimia dan diletakkan di atas dudukan pada tensiometer. Suhu cairan diukur dan dicatat. Selanjutnya cincin platinum dicelupkan ke dalam sampel tersebut (lingkaran logam tercelup ±3 mm di bawah permukaan cincin). Skala vernier tensiometer diatur pada posisi nol dan jarum penunjuk harus berada pada posisi berhimpit dengan garis pada kaca. Selanjutnya kawat torsi diputar perlahan-lahan sampai film cairan tepat putus. Saat film cairan tepat putus, skala dibaca dan dicatat sebagai nilai tegangan permukaan.
Pengukuran Tegangan Antarmuka
(ASTM_D, 1331 2000). Metode penentuan tegangan antarmuka hampir sama dengan pengukuran tegangan permukaaan. Pengukuran tegangan antarmuka menggunakan dua cairan yang berbeda tingkat kepolarannya, yaitu larutan surfaktan dengan ragam konsentrasi 0.0000−0.0040% (b/v) dan xilena (1:1). Larutan surfaktan terlebih dahulu dimasukkan ke dalam wadah sampel, kemudian dicelupkan cincin platinum ke dalamnya (lingkaran logam tercelup ±3 mm di bawah permukaan cairan), setelah itu secara hati-hati larutan xilena ditambahkan di atas larutan surfaktan sehingga sistem terdiri atas dua lapisan. Kontak antara cincin dan larutan xilena sebelum pengukuran harus dihindari. Setelah tegangan antarmuka mencapai ekuilibrium, yaitu benar-benar terbentuk dua lapisan terpisah yang sangat jelas, pengukuran selanjutnya dilakukan dengan cara yang sama dengan pengukuran tegangan permukaan.
Penentuan Kestabilan Emulsi (Modifikasi ASTM 2000). Kestabilan emulsi diukur untuk
jenis emulsi O/W (minyak dalam air) dan W/O (air dalam minyak) antara larutan surfaktan dengan xilena. Larutan surfaktan yang akan diukur mempunyai konsentrasi 0.0010−0.0040% (b/v). Kestabilan jenis emulsi O/W diukur dengan cara sebanyak 9.5 mL larutan surfaktan dimasukkan ke dalam tabung reaksi khusus, kemudian dicampur dengan 0.5 mL xilena. Campuran dikocok selama 5 menit menggunakan ultrasonic
homogenizer. Tinggi emulsi awal diukur.
Emulsi dibiarkan selama 24 jam. Setelah 24 jam, tinggi emulsi yang tersisa diukur. Kestabilan emulsi jenis W/O diukur dengan cara sebanyak 9.5 mL xilena dimasukkan ke dalam tabung reaksi khusus, kemudian ditambah dengan 0.5 mL larutan surfaktan. Campuran dikocok selama 5 menit menggunakan ultrasonic homogenizer.
Lamanya pemisahan fase antara xilena dan larutan surfaktan diukur.
Stabilitas Pembusaan (Modifikasi Hui 1996 di dalam Martini 2003). Uji pembusaan
dimaksudkan untuk mengetahui kemampuan surfaktan dalam menghasilkan busa. Uji ini dilakukan dengan cara sebanyak 3 mL larutan surfaktan dengan ragam konsentrasi 0.0010– 0.0040% (b/v) dimasukkan ke dalam tabung reaksi, lalu dikocok menggunakan aerator selama 1 menit. Waktu terbentuknya busa diukur sebagai lama pembusaan.
5
Daya Detergensi (Lynn 1996 di dalam Martini 2003). Uji detergensi dilakukan
untuk mengetahui kemampuan surfaktan membersihkan kotoran pada suatu kain menggunakan turbidimeter. Kekeruhan yang diperoleh merupakan hasil kelarutan kotoran dalam air. Larutan surfaktan yang digunakan mempunyai ragam konsentrasi 0.0010−0.0040% (b/v).
Uji detergensi dilakukan dengan cara masing-masing larutan surfaktan diukur kekeruhannya dan dicatat sebagai nilai T1. Kain putih berbentuk bujur sangkar dengan luas 25 cm2 direndam dalam 100 mL akuades
selama 30 menit. Setelah itu kain diangkat, kemudian akuades hasil rendaman diukur kekeruhannya dan dicatat sebagai nilai T2. Kain putih dengan jenis dan ukuran yang sama direndam dalam larutan pengotor bumbu rendang dengan konsentrasi 5% (b/v) selama 30 menit. Setelah itu kain ditiriskan selama 30 menit, kemudian kain direndam dalam larutan surfaktan sebanyak 100 mL selama 30 menit. Setelah 30 menit kain diangkat. Kekeruhan larutan surfaktan diukur setelah perendaman dan dicatat sebagai nilai T3.
Pengukuran pH. Pengukuran pH dilakukan
dengan menggunakan pH meter yang telah dikalibrasi dengan buffer pH 4 dan 7. Elektroda dibilas dengan akuades dan dikeringkan dengan tisu. Sampel dimasukkan ke dalam gelas piala kemudian pH sampel diukur.
HASIL DAN PEMBAHASAN
Tegangan Permukaan dan Konsentrasi Misel Kritis (KMK)
Pengukuran tegangan permukaan menggunakan metode cincin du Nouy. Prinsip metode cincin du Nouy adalah gaya yang diperlukan untuk menarik cincin platina sebanding dengan tegangan permukaannya. Pengukuran tegangan permukaan sangat penting dilakukan untuk memperoleh nilai konsentrasi misel kritis (KMK) dari masing-masing ester glukosa. Nilai KMK diperoleh dari perpotongan dua garis pada kurva tegangan permukaan masing-masing ester.
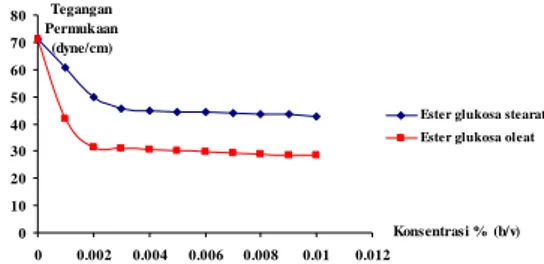
Berdasarkan Gambar 2 diperoleh informasi bahwa ragam konsentrasi larutan surfaktan yang digunakan untuk mengukur tegangan permukaan cukup rendah. Hal ini berarti bahwa larutan surfaktan yang diukur mampu menurunkan tegangan permukaan pada konsentrasi yang sangat rendah. Pada
Gambar tersebut terlihat mula-mula terjadi penurunan tegangan permukaan yang cukup besar, yaitu pada konsentrasi 0.0010% b/v dan 0.0020% (b/v). Hal ini disebabkan karena molekul-molekul surfaktan teradsorpsi di permukaan dan antarmuka larutan-dinding wadah. Jika konsentrasi larutan surfaktan ditingkatkan, maka sebagian molekul surfaktan membentuk misel. Kenaikan konsentrasi surfaktan akan meningkatkan jumlah misel. Konsentrasi ketika surfaktan membentuk misel disebut konsentrasi misel kritis (KMK). Misel adalah agregat-agregat molekul surfaktan di badan cairan yang terbentuk karena permukaan telah jenuh oleh molekul-molekul surfaktan. Pada kondisi di bawah nilai KMK, molekul-molekul surfaktan teradsorpsi sempurna di permukaan dan antarmuka larutan-dinding wadah. Saat kondisi tepat pada nilai KMK larutan menjadi hampir jenuh, molekul-molekul surfaktan hanya sedikit yang teradsorpsi. Setelah melewati KMK surfaktan tidak mampu lagi teradsorpsi pada permukaan dan antarmuka larutan-dinding wadah karena larutan telah jenuh sehingga surfaktan tidak mampu menurunkan tegangan permukaan. Berdasarkan Gambar 2 diperoleh nilai KMK ester glukosa stearat, yaitu 0.0024% (b/v), sedangkan nilai KMK ester glukosa oleat adalah 0.0013% (b/v). Seharusnya nilai KMK ester glukosa oleat lebih besar dibandingkan ester glukosa stearat. Hal ini disebabkan oleh kedua ester tersebut tidak murni karena ditinjau dari kisaran titik lelehnya yang lebar, yaitu 96−114° (Sari 2006) untuk ester glukosa stearat dan 98−110° (Nugraha 2006) untuk ester glukosa oleat. Nilai KMK masing-masing ester glukosa dijadikan sebagai dasar pencirian sifat-sifat ester sebagai pengemulsi, detergen, dan pembusa. Gambar 2 juga menjelaskan bahwa ester glukosa oleat menurunkan tegangan permukaan lebih besar dibandingkan ester glukosa stearat (Lampiran 1). Hal ini disebabkan oleh adanya ikatan rangkap dua pada rantai alkil asam lemak ester glukosa oleat mengakibatkan dimensi molekul ester glukosa oleat lebih ramping dibandingkan ester glukosa stearat sehingga jumlah molekul ester glukosa oleat lebih banyak teradsorpsi dibandingkan ester glukosa stearat. Penurunan tegangan permukaan maksimum yang dicapai oleh ester glukosa stearat dan ester glukosa oleat berturut-turut adalah 42.64 dyne/cm dan 28.36 dyne/cm.
6 0 10 20 30 40 50 60 70 80 0 0.002 0.004 0.006 0.008 0.01 0.012 Konsentrasi % (b/v) Tegangan Permukaan (dyne/cm)
Ester glukosa stearat Ester glukosa oleat
Gambar 2 Tegangan permukaan ester glukosa stearat dan ester glukosa oleat.
Tegangan Antarmuka
Gambar 3 menunjukkan bahwa penurunan tegangan antarmuka bergantung pada konsentrasi surfaktan. Semakin besar konsentrasi surfaktan semakin besar pula penurunan tegangan antarmuka. Penurunan tegangan antarmuka terjadi karena daerah antarmuka air-xilena mengadsorpsi molekul-molekul surfaktan.
Penurunan tegangan antarmuka ester glukosa oleat lebih besar dibandingkan dengan ester glukosa stearat (Lampiran 2). Hal ini disebabkan oleh adanya ikatan rangkap dua pada rantai alkil asam lemak ester glukosa oleat mengakibatkan dimensi molekul ester glukosa oleat lebih ramping dibandingkan ester glukosa stearat sehingga jumlah molekul ester glukosa oleat lebih banyak teradsorpsi pada antarmuka air-xilena dibandingkan ester glukosa stearat. Penurunan tegangan antarmuka maksimum yang dicapai oleh ester glukosa stearat dan ester glukosa oleat terjadi pada konsentrasi 0.0040% (b/v) berturut-turut adalah 27.11 dyne/cm dan 15.14 dyne/cm. 0 10 20 30 40 50 60 0 0.001 0.002 0.003 0.004 0.005 Konsentrasi % (b/v) Tegangan Antarmuka (dyne/cm)
Ester glukosa stearat Ester glukosa oleat
Gambar 3 Tegangan antarmuka ester glukosa stearat dan ester glukosa oleat.
Nilai HLB
Nilai HLB dari ester glukosa oleat adalah 3.85, sedangkan nilai HLB dari ester glukosa stearat adalah 7.25. Nilai HLB yang diperoleh merupakan hasil interpolasi pada kurva
kalibrasi dengan persamaan y = 0.2551x – 3.5487 (Lampiran 3).
Jenis ikatan pada rantai alkil asam lemak ester glukosa berpengaruh terhadap nilai HLB. Asam oleat merupakan asam lemak dengan panjang rantai C18 dan mempunyai satu ikatan rangkap dua, sedangkan asam stearat juga dengan panjang rantai C18, tidak memiliki ikatan rangkap dua. Elektron π pada ikatan rangkap dua asam oleat menyebabkan gugus hidrofil molekul ester glukosa oleat lebih besar dibandingkan gugus hidrofil molekul ester glukosa stearat sehingga nilai HLB ester glukosa oleat lebih besar daripada ester glukosa stearat. Namun, pada penelitian ini diperoleh sebaliknya. Nilai HLB dari ester glukosa oleat lebih kecil dibandingkan ester glukosa stearat. Hal ini disebabkan oleh kedua ester glukosa tersebut tidak murni karena ditinjau dari kisaran titik lelehnya yang lebar, yaitu 96−114° (Sari 2006) untuk ester glukosa stearat dan 98−110° (Nugraha 2006) untuk ester glukosa oleat. Berdasarkan Adamson (1982) maka ester glukosa stearat cocok digunakan sebagai wetting agent, sedangkan ester glukosa oleat cocok digunakan sebagai pengemulsi W/O.
Nilai HLB ini ditentukan dengan metode titrimetri menggunakan benzena dan piridina sebagai pelarut dari surfaktan dan titrat, sedangkan titrannya adalah akuades. Gugus hidrofil surfaktan berinteraksi dengan molekul akuades yang bersifat polar dan pasangan elektron bebas atom nitrogen molekul piridina yang semipolar, sedangkan gugus lipofil surfaktan berinteraksi dengan cincin aromatik dari benzena dan piridina yang bersifat nonpolar. Kekeruhan yang dihasilkan merupakan indikator titik akhir titrasi. Kekeruhan disebabkan oleh molekul-molekul ester glukosa yang membentuk misel karena permukaan telah jenuh tertutupi oleh molekul-molekul surfaktan.
Kestabilan Emulsi
Stabilitas emulsi diukur menggunakan dua larutan yang berbeda polaritasnya. Emulsi yang diukur adalah emulsi jenis O/W dan W/O. Stabilitas emulsi diukur menggunakan larutan surfaktan dengan ragam konsentrasi 0.0010−0.0040% (b/v). Surfaktan mempunyai peranan menstabilkan emulsi. Molekul-molekul surfaktan dalam emulsi membungkus atau mengelilingi molekul-molekul fase terdispersi untuk mencegah molekul-molekul fase terdispersi bergabung membentuk molekul-molekul yang lebih besar. Jika terjadi
7
penggabungan molekul-molekul fase terdispersi maka emulsi menjadi tidak stabil. Semakin besar konsentrasi surfaktan yang digunakan semakin besar pula jumlah molekul yang membungkus fase terdispersi sehingga stabilitas emulsi semakin meningkat.
Hasil pengukuran stabilitas emulsi jenis O/W dapat dilihat pada Gambar 4. Stabilitas emulsi O/W dari ester glukosa stearat dan ester glukosa oleat cukup rendah. Gambar tersebut juga menunjukkan bahwa ester glukosa stearat mempunyai kestabilan emulsi O/W lebih baik dibandingkan dengan ester glukosa oleat. Seharusnya ester glukosa oleat mempunyai stabilitas emulsi O/W lebih baik dibandingkan ester glukosa stearat karena elektron π pada ikatan rangkap dua rantai alkil asam oleat meningkatkan kepolaran dan kelarutan ester glukosa oleat dalam air. Stabilitas emulsi O/W ester glukosa stearat mencapai maksimum pada konsentrasi 0.0040% (b/v), yaitu 13.64%, sedangkan kestabilan emulsi O/W ester glukosa oleat maksimum juga dicapai pada konsentrasi 0.0040 (b/v), yaitu 12.00 %.
Gambar 5 menjelaskan bahwa emulsi W/O dari ester glukosa stearat dan ester glukosa oleat hanya dapat bertahan dalam hitungan menit. Berdasarkan gambar tersebut diketahui bahwa ester glukosa oleat mempunyai stabilitas emulsi W/O lebih baik dibandingkan ester ester glukosa stearat. Seharusnya ester glukosa stearat lebih menstabilkan emulsi W/O karena ester glukosa stearat tidak memiliki ikatan rangkap dua yang kaya elektron π dibandingkan ester glukosa oleat. Elektron-elektron π mengakibatkan sifat kepolaran dan kelarutan dalam pelarut polar bertambah sehingga ester glukosa oleat lebih larut dalam air dibandingkan ester glukosa stearat. Stabilitas emulsi W/O ester glukosa stearat dan ester glukosa oleat mencapai maksimum pada konsentrasi 0.0040% (b/v) berturut-turut adalah 65 menit dan 90 menit (Lampiran 4). 0 2 4 6 8 10 12 14 16 0 0.001 0.002 0.003 0.004 0.005 Konsentrasi % (b/v) Stabilitas Emulsi (% )
Ester glukosa stearat Ester glukosa oleat
Gambar 4 Stabilitas emulsi O/W ester glukosa stearat dan ester glukosa oleat. 0 10 20 30 40 50 60 70 80 90 100 0 0.001 0.002 0.003 0.004 0.005 Konse ntrasi (% b/v) Stabi li tas Emulsi
(me ni t)
Ester glukosa stearat Ester glukosa oleat
Gambar 5 Stabilitas emulsi W/O ester glukosa stearat dan glukosa oleat.
Banyak faktor yang menyebabkan emulsi tidak stabil, seperti pembentukan krim (creaming) yang terjadi jika fase terdispersi dan medium pendispersi mempunyai densitas yang berbeda, flokulasi (pengelompokkan) terjadi jika molekul-molekul fase terdispersi berkelompok karena adanya interaksi antarmolekul dan jarak antarmolekulnya berdekatan, dan koalesensi terjadi jika film tipis molekul pendispersi terputus karena adanya dua molekul fase terdispersi yang bergabung. Namun pada penelitian ini, destabilisasi emulsi terjadi karena ester glukosa stearat dan ester glukosa oleat yang digunakan tidak murni ditinjau dari kisaran titik leleh yang lebar dari kedua ester, yaitu 96−114° (Sari 2006) untuk ester glukosa stearat dan 98−110° (Nugraha 2006) untuk ester glukosa oleat.
Stabilitas Pembusaan
Stabilitas pembusaan merupakan uji untuk mengetahui kemampuan surfaktan dalam menghasilkan busa. Busa yang dihasilkan surfaktan bergantung pada struktur dan konsentrasi surfaktan dan tidak dipengaruhi oleh pembentukan misel (Durian dan Weitz 1993). Berdasarkan hasil penelitian, diketahui bahwa busa yang dihasilkan oleh ester glukosa stearat dan ester glukosa oleat relatif sedikit. Hal ini disebabkan oleh gugus hidrofil yang bulky dari kedua ester glukosa menyebabkan adsorpsi di permukaan tidak tersusun secara baik. Berdasarkan Gambar 6 diketahui bahwa stabilitas pembusaan meningkat sebanding dengan konsentrasi surfaktan.
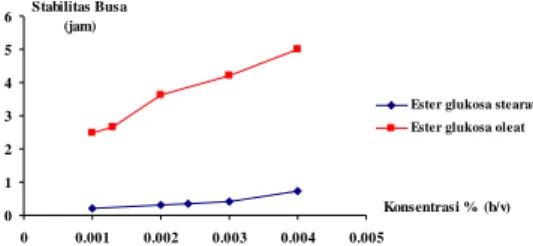
Gambar 6 juga menunjukkan stabilitas pembusaan ester glukosa stearat dan ester glukosa oleat. Ester glukosa oleat memiliki stabilitas pembusaan lebih baik daripada ester glukosa stearat. Hal ini disebabkan oleh adanya ikatan rangkap dua pada rantai alkil
8
asam lemak ester glukosa oleat mengakibatkan dimensi molekul ester glukosa oleat lebih ramping dibandingkan ester glukosa stearat sehingga jumlah molekul ester glukosa oleat lebih banyak teradsorpsi pada daerah antarmuka air-gas. Ester glukosa stearat dan ester glukosa oleat mencapai stabilitas pembusaan maksimum pada konsentrasi 0.0040% (b/v), yaitu berturut-turut 43.54 menit dan 4.59 jam (Lampiran 5).
0 1 2 3 4 5 6 0 0.001 0.002 0.003 0.004 0.005 Konsentrasi % (b/v) Stabilitas Busa (jam)
Ester glukosa stearat Ester glukosa oleat
Gambar 6 Stabilitas pembusaan ester glukosa stearat dan ester glukosa oleat.
Daya Detergensi
Daya detergensi surfaktan cenderung meningkat berbanding lurus dengan peningkatan konsentrasi surfaktan. Hal ini disebabkan oleh peningkatan konsentrasi surfaktan mengakibatkan peningkatan pembentukan misel. Misel yang terbentuk berfungsi membungkus kotoran yang terlepas dari permukaan kain dan memindahkannya ke dalam air.
Gambar 7 dan 8 menunjukkan daya detergensi dari ester glukosa stearat dan ester glukosa oleat. Daya detergensi ester glukosa oleat lebih baik dibandingkan ester glukosa stearat. Hal ini disebabkan oleh adanya ikatan rangkap dua pada rantai alkil asam lemak ester glukosa oleat mengakibatkan dimensi molekul-molekul misel ester glukosa oleat lebih ramping dibandingkan ester glukosa stearat sehingga jumlah molekul ester glukosa oleat lebih banyak teradsorpsi. Kekeruhan air yang terjadi disebabkan oleh kotoran yang terlepas dari permukaan kain. Kekeruhan tersebut berbanding lurus dengan daya detergensi. Daya detergensi ester glukosa oleat dan ester glukosa stearat mencapai maksimum pada konsentrasi 0.0040% (b/v) berturut-turut adalah 3.41 NTU dan 5.93 NTU (Lampiran 6). 0 1 2 3 4 5 6 7 8 9 0 0.001 0.002 0.003 0.004 0.005 Konsentrasi % (b/v) Daya Detergensi (NTU) Detergen komersial Ester glukosa stearat
Gambar 7 Daya detergensi ester glukosa stearat. 0 1 2 3 4 5 6 7 8 9 0 0.001 0.002 0.003 0.004 0.005 Konse ntrasi % (b/v) Daya Detergensi (NTU) Detergen komersial Ester glukosa oleat
Gambar 8 Daya detergensi ester glukosa oleat.
pH
Tabel 2 menunjukkan nilai pH dari ester glukosa stearat dan ester glukosa oleat. Berdasarkan tabel tersebut, dapat diketahui bahwa kedua ester memiliki nilai pH yang relatif netral sehingga dapat diaplikasikan pada produk-produk perawatan diri, seperti kosmetik, pasta gigi, detergen, dan lain-lain karena tidak menimbulkan efek negatif terhadap kulit.
Tabel 2 pH Ester glukosa
Jenis sampel pH
Ester glukosa stearat 6.40 Ester glukosa oleat 6.86
SIMPULAN DAN SARAN
Simpulan
Nilai KMK ester glukosa stearat adalah 0.0024% (b/v), sedangkan nilai KMK ester glukosa oleat adalah 0.0013% (b/v). Penurunan tegangan antarmuka maksimum yang dicapai oleh ester glukosa stearat dan ester glukosa oleat berturut-turut adalah sebesar 27.11 dyne/cm dan 15.14 dyne/cm. Stabilitas emulsi O/W terbaik dicapai oleh ester glukosa stearat, yaitu 13.64%. Stabilitas emulsi W/O terbaik dicapai oleh ester glukosa
9
oleat, yaitu 90 menit. Daya detergensi terbaik dan stabilitas busa terbaik dicapai oleh ester glukosa oleat berturut-turut adalah 5.93 NTU dan 4.59 jam. Nilai pH ester glukosa stearat dan ester glukosa oleat berturut-turut adalah 6.40 dan 6.86.
Saran
Perlu dilakukan proses permurnian lebih lanjut terhadap produk hasil sintesis ester glukosa stearat dan ester glukosa oleat. Perlu juga dilakukan uji wetting agent terutama ester glukosa stearat dan uji toksisitas pada kedua ester apabila digunakan sebagai zat aditif pada industri.
DAFTAR PUSTAKA
Adamson WA. 1982. Physical Chemistry of
Surfaces. Canada: J Willey.
Akoh CC, Swanson BG. 1990. Carbohydrate
Fatty Acid Esters. New York: Marcell
Dekker.
ASTM D_1331. 2000. Standard Test Methods Surface and Interfacial Tension of Surface Active Agents and Emulsions. Annual Book of ASTM Standards, Volume 15. Philadelphia: Easton MD.
Cahn A, Lynn LJ. 1983. Surfactant and Detersive systems. Di dalam Kirk-Othmer
Encyclopedia of Chemical Technology. Ed
ke-3. Volume 22. Canada: J Willey. Durian DJ, Weitz DA. 1993. Foams. Di dalam
Kirk-Othmer Encyclopedia of Chemical Technology. Ed ke-4. Volume 2. Canada: J
Willey.
Flider FJ. 2001. Commercial Consideration and markets for naturally derived biodegradable surfactants. Inform. 12(12):1161-1164.
Friberg ES, Jones S. 1993. Emulsions. Di dalam Kirk-Othmer Encyclopedia of
Chemical Technology. Ed ke-4. Volume 9.
Canada: J Willey.
Gervasio GC. 1996. Bailey’s Industrial Oils
and Fats Products. New York: J Willey.
Holmberg K, Jonsson B, Kronberg B, Lindman B. 2003. Polymers in Aqueous
Solution. Ed ke-2. Chichester: J Willey.
Jaya HS. 2005. Profil Stabilitas emulsi fraksi ringan minyak bumi dalam air dengan penambahan surfaktan nonionik [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Kuang D, Obaje OJ, Ali AM. 2000. Synthesis and characterization of acetylated glucose fatty esters from palm and palm kernel oil fatty methyl esters. J of Oil Palm Res 12(2):14-19.
Lynn LJ. 1993. Detergency. Di dalam
Kirk-Othmer Encyclopedia of Chemical Technology. Ed ke-4. Volume 7. Canada: J
Willey.
Martini Y. 2003. Kajian pengaruh jenis dan konsentrasi katalis pada proses produksi surfaktan sukrosa ester dari metil ester minyak inti sawit [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Nugraha A. 2006. Sintesis ester glukosa oleat dari glukosa pentaasetat dan metil oleat [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Obaje OJ, penemu; URAH Resources. 2005. Trans-acidolysis process for the preparation of Carbohydrate Fatty-Acid Esters. US Patent 6,846,916.
Sari I. 2006. Sintesis ester glukosa stearat melalui reaksi interesterifikasi dengan metode bebas pelarut [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sawyert CN, McCarty PL. 1978. Chemistry
for Environmental Engineering. Ed ke-3.
Singapura: McGraw-Hill.
Swern D. 1997. Bailey’s Industrial Oil and
Fat Products. Ed ke-4. Volume 2. New
11
Lampiran 1 Penentuan tegangan permukaan
Penentuan tegangan permukaan ester glukosa stearat
Konsentrasi % (b/v)
Densitas (g/ml)
Tegangan Permukaan Terukur (dyne/cm) Prerata (dyne/cm) Fr γ = P × Fr (dyne/cm) 0.0000 1.0050 75.90; 76.00; 76.10; 76.10; 75.90 76.00 0.9369 71.20 0.0010 1.0051 65.40; 65.30; 65.30; 65.40; 65.40 65.36 0.9264 60.55 0.0020 1.0051 54.40; 54.40; 54.40; 54.40; 54.40 54.40 0.9150 49.78 0.0030 1.0051 50.10; 50.00; 50.10; 50.20; 50.20 50.12 0.9103 45.62 0.0040 1.0052 49.40; 49.40; 49.40; 49.30; 49.30 49.36 0.9094 44.90 0.0050 1.0053 49.00; 49.00; 49.00; 49.00; 49.00 49.00 0.9090 44.54 0.0060 1.0053 48.90; 48.90; 48.80; 48.80; 48.90 48.86 0.9089 44.41 0.0070 1.0053 48.50; 48.50; 48.40; 48.50; 48.50 48.48 0.9084 44.04 0.0080 1.0052 48.00; 48.10; 48.10; 48.10; 48.10 48.08 0.9080 43.66 0.0090 1.0052 47.90; 47.90; 47.80; 47.80; 47.80 47.84 0.9078 43.43 0.0100 1.0052 47.00; 47.10; 47.00; 47.00; 47.00 47.02 0.9068 42.64
Penentuan tegangan permukaan ester glukosa oleat
Konsentrasi
% (b/v) Densitas (g/mL) Tegangan Permukaan Terukur (dyne/cm) (dyne/cm) Prerata Fr (dyne/cm) γ = P × Fr 0.0000 1.0050 75.90; 76.00; 76.10; 76.10; 75.90 76.00 0.9369 71.20 0.0010 1.0050 46.10; 46.10; 46.10; 46.10; 46.10 46.10 0.9058 41.76 0.0020 1.0050 35.10; 35.10; 35.10; 35.10; 35.10 35.10 0.8929 31.34 0.0030 1.0050 34.70; 34.70; 34.70; 34.70; 34.70 34.70 0.8924 30.97 0.0040 1.0052 34.10; 34.10; 34.10; 34.10; 34.10 34.10 0.8917 30.41 0.0050 1.0051 33.70; 33.70; 33.70; 33.70; 33.70 33.70 0.8912 30.03 0.0060 1.0050 33.30; 33.20; 33.30; 33.20; 33.30 33.26 0.8906 29.62 0.0070 1.0051 32.90; 32.80; 32.90; 32.90; 32.80 32.86 0.8901 29.25 0.0080 1.0052 32.50; 32.40; 32.50; 32.40; 32.40 32.44 0.8896 28.86 0.0090 1.0052 32.00; 32.10; 32.10; 32.00; 32.00 32.04 0.8891 28.50 0.0100 1.0052 31.90; 31.90; 31.90; 31.90; 31.90 31.90 0.8809 28.36 Mean circumference (C) = 5.945 R/r = 53.2561920 T = 28 °C d = Densitas udara = 0.0012 g/mL D = Densitas sampel
P = Rerata tegangan permukaan terukur Fr = Faktor koreksi alat
γ = tegangan permukaan terkoreksi Contoh Perhitungan
• Tegangan permukaan air
R r 679 . 1 04534 . 0 ) ( C P 0.01452 0.7250 Fr 2 + − − + = d D 53.2561920 679 . 1 04534 . 0 ) 0012 . 0 0050 . 1 ( 5.945 76.00 0.01452 0.7250 Fr 2 + − − × + = = 0.9369
12
Lanjutan lampiran 1 γ = P × Fr
= 76.00 dyne/cm × 0.9369 = 71.20 dyne/cm
• Tegangan permukaan larutan ester glukosa stearat 0.0010% (b/v)
R r 679 . 1 04534 . 0 ) ( C P 0.01452 0.7250 Fr 2 + − − + = d D 53.2561920 679 . 1 04534 . 0 ) 0012 . 0 0051 . 1 ( 5.945 65.40 0.01452 0.7250 Fr 2 + − − × + = = 0.9264 γ = P × Fr = 65.40 dyne/cm × 0.9264 = 60.55 dyne/cm
13
Lampiran 2 Penentuan tegangan antarmuka ester glukosa stearat dan ester glukosa oleat
Jenis Konsentrasi % (b/v) Tegangan Antarmuka Terukur (dyne/cm) (dyne/cm) Prerata Fr (dyne/cm) γ = P × Fr
air 0.0000 45.50; 45.30; 45.00; 44.90; 45.70 45.28 1.1286 51.10 0.0010 34.30; 34.70; 34.70; 34.70; 34.30 34.56 1.0821 37.40 0.0020 32.50; 32.50; 32.30; 32.40; 32.40 32.42 1.0721 34.76 1 0.0024 29.10; 29.10; 29.10; 29.40; 29.40 29.22 1.0566 30.87 0.0030 28.10; 28.10; 28.00; 28.10; 28.00 28.06 1.0507 29.48 0.0040 26.00; 26.00; 26.10; 26.20; 26.00 26.06 1.0404 27.11 0.0010 20.60; 20.50; 20.60; 20.50; 20.60 20.56 1.0105 20.78 0.0013 18.50; 18.40; 18.50; 18.50; 18.40 18.46 0.9981 18.78 2 0.0020 17.00; 17.00; 17.10; 17.00; 17.10 17.04 0.9894 16.86 0.0030 16.40; 16.40; 16.40; 16.40; 16.30 16.38 0.9853 16.14 0.0040 15.40; 15.50; 15.50; 15.50; 15.40 15.46 0.9792 15.14
Keterangan: 1 Ester glukosa stearat; 2 Ester glukosa oleat
Mean circumference (C) = 5.945 R/r = 53.2561920
T = 28 °C
d = densitas xilena = 0.8802 g/mL D = densitas sampel
P = Rerata tegangan antarmuka yang terukur Fr = Faktor koreksi
γ = tegangan antarmuka terkoreksi
Contoh Perhitungan tegangan antarmuka ester glukosa stearat 0.0010% (b/v) R r 679 . 1 04534 . 0 ) ( C P 0.01452 0.7250 Fr 2 + − − + = d D 53.2561920 679 . 1 04534 . 0 ) 8802 . 0 0050 . 1 ( 5.945 34.56 0.01452 0.7250 Fr 2 + − − × + = = 1.0821 γ = P × Fr = 34.56 dyne/cm × 1.0821 = 37.40 dyne/cm
14
Lampiran 3 Penentuan nilai HLB
Volume Piridina = 23.75 mL
Volume Benzena = 1.25 mL
Penentuan kurva standar HLB
Jenis Surfaktan V akuades terpakai (mL) HLB Perubahan Warna
Tween-80 (PA) 69.4 15.0 Kuning muda menjadi keruh
Tween-20 (PA) 81.9 16.7 Kuning muda menjadi keruh
GMS 29.6 3.8 Tidak berwarna menjadi putih
Berdasarkan pada tabel diatas, dibuat persamaan garis, volume akuades yang terpakai sebagai sumbu x, sedangkan nilai HLB pada sumbu y, sehingga diperoleh persamaan garis y = 0.2551x − 3.5487. Nilai HLB dari ester glukosa oleat dan ester glukosa stearat diperoleh dengan menginterpolasi kurva kalibrasi di bawah ini (Jaya 2005).
y = 0.2551x - 3.5487 R2 = 0.9881 0 2 4 6 8 10 12 14 16 18 20 0 10 20 30 40 50 60 70 80 90 V akuades terpakai (ml) HL B
Penentuan HLB ester glukosa stearat
Ulangan Bobot
(g)
V akuades terpakai
(mL) HLB Perubahan Warna
1 1.0004 42.25 7.20 Tidak berwarna menjadi putih keruh
2 1.0013 42.50 7.30 Tidak berwarna menjadi putih keruh
Rerata 7.25
Penentuan HLB ester glukosa oleat
Ulangan Bobot
(g)
V akuades terpakai
(mL) HLB Perubahan Warna
1 1.0006 29.25 3.90 Tidak berwarna menjadi putih keruh
2 1.0006 29.00 3.80 Tidak berwarna menjadi putih keruh
Rerata 3.85
Contoh Perhitungan HLB ester glukosa stearat Persamaan garis y = 0.2551x − 3.5487 = 0.2551 (42.25) – 3.5487 = 7.20
15
Lampiran 4 Penentuan kestabilan emulsi Stabilitas emulsi O/W ester glukosa stearat
Ulangan I Ulangan II Konsentrasi % (b/v) Tinggi awal (cm) Tinggi akhir (cm) Stabilitas emulsi (%) Tinggi awal (cm) Tinggi akhir (cm) Stabilitas emulsi (%) Rerata stabilitas emulsi (%) 0.0010 3.50 0.30 8.57 3.40 0.30 8.82 8.70 0.0020 3.30 0.35 10.61 3.30 0.35 10.61 10.61 0.0024 2.70 0.35 12.96 2.60 0.35 13.46 13.21 0.0030 2.70 0.30 11.11 2.60 0.35 13.46 12.29 0.0040 3.30 0.45 13.64 3.30 0.40 13.64 13.64
Stabilitas emulsi O/W ester glukosa oleat
Ulangan I Ulangan II Konsentrasi % (b/v) Tinggi awal (cm) Tinggi akhir (cm) Stabilitas emulsi (%) Tinggi awal (cm) Tinggi akhir (cm) Stabilitas emulsi (%) Rerata stabilitas emulsi (%) 0.0010 3.30 0.10 3.03 3.30 0.10 3.03 3.03 0.0013 3.30 0.15 4.55 3.30 0.15 4.55 4.55 0.0020 3.30 0.20 6.06 3.30 0.20 6.06 6.06 0.0030 3.30 0.30 9.09 3.30 0.30 9.09 9.09 0.0040 2.50 0.30 12.00 2.50 0.30 12.00 12.00 Contoh perhitungan stabilitas emulsi O/W ester glukosa stearat 0.0010% (b/v)
%
100
awal
tinggi
akhir
tinggi
emulsi
Stabilitas
=
×
100% 30 . 3 30 . 0 × = = 8.57 %Stabilitas emulsi W/O ester glukosa stearat dan ester glukosa oleat
Stabilitas Emulsi (menit) Jenis Sampel Konsentrasi % (b/v)
Ulangan I Ulangan II Stabilitas Emulsi Rerata (menit) 0.0010 40.00 40.00 40.00 0.0020 43.00 43.00 43.00 0.0024 48.00 48.00 48.00 0.0030 53.00 53.00 53.00
Ester glukosa stearat
0.0040 65.00 65.00 65.00
0.0010 38.00 39.00 38.50
0.0013 48.00 48.00 48.00
0.0020 52.00 52.00 52.00
0.0030 61.00 61.00 61.00
Ester glukosa oleat
16
Lampiran 5 Penentuan stabilitas pembusaan Stabilitas pembusaan ester glukosa stearat
Lama Pembusaan (menit) Konsentrasi % (b/v) Ulangan I Ulangan II Lama Pembusaan (menit) 0.0010 11.59 12.00 11.59 0.0020 18.47 18.50 18.49 0.0024 21.24 21.26 21.25 0.0030 23.58 24.00 23.59 0.0040 43.50 43.58 43.54
Stabilitas pembusaan ester glukosa oleat
Lama Pembusaan (jam) Konsentrasi % (b/v) Ulangan I Ulangan II Lama Pembusaan (jam) 0.0010 2.28 2.29 2.28 0.0013 2.39 2.40 2.39 0.0020 3.37 3.38 3.37 0.0030 4.10 4.13 4.12 0.0040 4.59 5.00 4.59
17
Lampiran 6 Penentuan daya detergensi Daya detergensi ester glukosa stearat
Konsentrasi % (b/v) Ulangan Turbiditas T1 (NTU) Turbiditas T3 (NTU) Turbiditas Sampel (NTU) 1 0.74 2.03 2 0.74 2.03 0.0010 Rerata 0.74 2.03 1.17 1 0.31 1.44 2 0.31 1.44 0.0020 Rerata 0.31 1.44 0.58 1 1.16 2.88 2 1.16 2.88 0.0024 Rerata 1.16 2.88 2.02 1 0.33 2.29 2 0.33 2.29 0.0030 Rerata 0.33 2.27 1.43 1 0.41 4.26 2 0.41 4.27 0.0040 Rerata 0.41 4.27 3.41
Daya detergensi ester glukosa oleat
Konsentrasi % (b/v) Ulangan Turbiditas T1 (NTU) Turbiditas T3 (NTU) Turbiditas Sampel (NTU) 1 0.71 2.67 2 0.71 2.68 0.0010 Rerata 0.71 2.68 1.82 1 0.71 3.02 2 0.71 3.01 0.0013 Rerata 0.71 3.02 2.16 1 0.31 3.87 2 0.31 3.87 0.0020 Rerata 0.31 3.87 3.01 1 0.31 5.30 2 0.31 5.32 0.0030 Rerata 0.31 5.31 4.45 1 0.40 6.79 2 0.40 6.79 0.0040 Rerata 0.40 6.79 5.93 Turbiditas akuades
Ulangan Turbiditas (T2) (NTU) 1 0.86 2 0.86 Rerata 0.86
Contoh perhitungan penentuan daya detergensi ester glukosa stearat 0.0010% (b/v) OD (Original Dirt) = T2 – T1
= 0.86 – 0.74 = 0.12 NTU
18
Lanjutan lampiran 6
Daya detergensi = T3 – OD – T1 = 2.03 – 0.12 – 0.74 = 1.17 NTU
Daya detergensi detergen komersial
Konsentrasi
% (b/v) Ulangan Turbiditas T1 (NTU) Turbiditas T3 (NTU) Turbiditas Sampel (NTU) 1 0.26 2.86 2 0.26 2.87 0.0010 Rerata 0.26 2.87 2.01 1 0.26 3.43 2 0.26 3.42 0.0013 Rerata 0.26 3.43 2.57 1 0.37 4.15 2 0.37 4.16 0.0020 Rerata 0.37 4.15 3.30 1 0.42 4.54 2 0.42 4.55 0.0024 Rerata 0.42 4.54 3.69 1 0.80 6.36 2 0.80 6.36 0.0030 Rerata 0.80 6.36 5.62 1 0.91 7.80 2 0.91 7.80 0.0040 Rerata 0.91 7.80 6.94