III. IDENTIFIKASI DAN KARAKTERISASI BEBERAPA VIRUS
YANG MENGINFEKSI TANAMAN ANGGREK DI PULAU JAWA
ABSTRAK
IRWAN LAKANI. Identifikasi dan Karakterisasi Beberapa Virus yang Menginfeksi Tanaman Anggrek di Pulau Jawa. Dibimbing oleh GEDE
SUASTIKA, NURHAJATI MATJJIK, dan TRI ASMIRA DAMAYANTI.
Hasil survei pada beberapa lokasi sentra pembibitan/pengembangan pertanaman anggrek, di Jawa Timur (Malang, Surabaya), Jawa Tengah (Magelang), Jawa Barat (Kebun Raya-Bogor, Gunung Sindur-Bogor, Cianjur, Lembang) dan Jakarta (Taman Anggrek Indonesia Permai/TAIP) berdasarkan gejala, uji serologi, RT-PCR dan perunutan DNA menunjukkan terdeteksinya beberapa jenis virus. Gejala yang ditemukan pada daun dan bunga bervariasi berupa ringspot (bercak cincin), mosaik, nekrosis, malformasi daun, klorosis, dan
gejala masing-masing virus sulit dibedakan satu sama lainnya. RT-PCR menggunakan primer universal CMV subgrup IB, Potyvirus, dan Tospovirus
berhasil mengamplifikasi DNA berukuran 382 bp dan 327 bp pada semua sampel uji dan tidak terdeteksi Tospovirus. Deteksi serologi menggunakan antiserum
spesifik CymMV dan ORSV serta RT-PCR menggunakan primer spesifik gen CP virus berhasil mendeteksi keduanya. Analisis nukleotida enam isolat CymMV yang berasal dari Gunung Sindur-Bogor, Kebun Raya-Bogor, Lembang Bandung (Jawa Barat), Magelang (Jawa Tengah) dan Surabaya, Malang (Jawa Timur) menunjukkan homologi sekuen sebesar 96,2-98,8% antar isolat, dan homologi berdasarkan urutan asam amino berkisar 97,3-99,5% terhadap 10 isolat dari beberapa negara lain. Analisis pohon filogenetika menggunakan software MEGA
4.0 berdasarkan asam amino keenam isolat CymMV, menunjukkan terbentuknya tiga kelompok berbeda untuk masing-masing isolat. Hasil analisis nukleotida gen CP ORSV isolat Gunung Sindur-Bogor, Kebun Raya-Bogor, Cipanas-Cianjur, dan Jakarta menunjukkan homologi berkisar 94,9-100% antar isolat, sedangkan analisis berdasarkan urutan asam amino antara isolat Pulau Jawa tersebut dengan 11 sekuen pada GeneBank diperoleh homologi berkisar 92,4–100%.
Analisis pohon filogenetika berdasarkan asam amino menunjukkan keempat isolat ORSV Pulau Jawa membentuk satu kelompok yang sama. Untuk ORSV dilakukan uji penularan terhadap beberapa jenis tanaman indikator yang menunjukkan ORSV mampu menginfeksi semua jenis tanaman indikator dengan kejadian penyakit 60-100%. Deteksi serologi daun tanaman bergejala dan yang tidak bergejala menunjukkan sampel tanaman positif bereaksi terhadap antiserum ORSV.
III. IDENTIFICATION AND CHARACTERIZATION OF SEVERAL
PLANT VIRUSES INFECTING ORCHIDS IN JAVA ISLAND
IRWAN LAKANI. Identification and Characterization of Several Plant Viruses Infecting Orchids in Java Island. Supervised by GEDE SUASTIKA,
NURHAJATI MATJJIK, dan TRI ASMIRA DAMAYANTI.
The survey results at several locations of orchid central nursery in East Java (Malang, Surabaya), Central Java (Magelang), West Java (Kebun Raya-Bogor, Gunung sindur-Raya-Bogor, Cianjur, Lembang) and Jakarta (Taman Anggrek Indonesia Permai/ TAIP) based on symptoms, serological test, RT-PCR and DNA sequence were positively detected several viruses. Symptoms are found in the leaves and flowers varied like ringspot, mosaic, necrosis, leaf malformation, and chlorosis and are difficult to distinguish each other. RT-PCR using universal primers of CMV subgroup IB, Potyvirus and Tospovirus succesfully amplified
DNA sized 382 bp and 327 bp in all tested samples, while Tospovirus
undetecteble. Serological detection using CymMV and ORSV specific antiserum and RT-PCR using specific primer for CP gene successfully amplified both DNAs. Nucleotide sequences analysis of the six CymMV isolates from Gunung Sindur- Bogor, Kebun Raya-Bogor, Lembang Bandung (West Java), Magelang (Central Java) and Surabaya, Malang (East Java) are showed sequence homology ranging from 96.2-98,8% and homology based on amino acid ranging from 97.3 to 99.5% with 10 isolates from several countries. The phylogenetic analysis using MEGA 4.0 software based on amino acid of the six isolates formed three different groups of each isolate. The nucleotide analysis of CP gene of ORSV isolates from Gunung Sindur-Bogor, Kebun Raya-Bogor, Cipanas-Cianjur, and Jakarta showed homology ranging from 94.9 to 100%, and homology based on amino acid ranging from 94.9 to 100% with 11 isolates from several countries. Phylogenetic analysis based on amino acids of four ORSV Java isolates formed one group. Transmission test of ORSV to several species of indicators plant showed that ORSV was able to infect all species of indicator plants with disease incidence 60-100%. Serological detection of symptomatic and asymptomatic leaves showed positive reacted positively against ORSV antiserum.
PENDAHULUAN
Tanaman anggrek (Orchidaceae) merupakan tanaman yang memiliki
jenis terbanyak dan paling bervariasi diantara tanaman hias lainnya.
Orchidaceae terdiri dari lebih 25.000 spesies yang termasuk dalam ± 900 genus.
Anggrek dapat tumbuh secara alami pada kisaran habitat yang luas dari daerah sub tropis sampai daerah beriklim tropis di dunia (Navalinskiene 2005).
Virus tanaman merupakan salah satu masalah dalam budidaya dan pengembangan tanaman anggrek. Beberapa laporan menyatakan bahwa tanaman anggrek dapat diinfeksi oleh lebih dari 50 jenis virus (Zettler et al. 1990;
Chang et al. 2005). Dua jenis virus penting pada tanaman anggrek yang banyak
diteliti adalah Odontoglossum ringspot virus (ORSV) dan Cymbidium mosaic virus (CymMV). Selain itu beberapa laporan menyebutkan tiga virus lainnya
yang menginfeksi anggrek di beberapa negara yaitu Cucumber mosaic virus
(CMV), Potyvirus dan Tospovirus.
Diantara virus yang menginfeksi anggrek, ORSV merupakan salah satu virus yang dominan menyerang pertanaman anggrek di dunia. Laporan dari beberapa negara menunjukkan bahwa virus ini menyebabkan kerugian secara ekonomi di Florida, Taiwan, India, New Zealand, dan beberapa negara lain (Jensen & Gold 1951; Lawson & Brannigan 1986; Zettler et al. 1990; Chang
2008).
ORSV telah dilaporkan dapat menginfeksi 31 genus anggrek (Zaitlin 1976; Inouye 2001). ORSV pertama kali diisolasi dan dikarakterisasi dari spesies anggrek Odontoglossum grande yang memperlihatkan gejala bercak cincin
(ringspot) pada daun. ORSV juga menyebabkan gejala mosaik bergaris atau
bercak, belang berbentuk berlian (diamond mottle), atau bercak cincin pada
daun, warna bunga pecah (color breaking) pada jenis Odontoglossum, Cymbidium, Vanilla, Epidendrum, Encyclia, Oncidium, Phalaenopsis dan
beberapa genus anggrek lainnya (Burnett 1965; Corbett 1967). Warna bunga pecah ditandai dengan variasi warna pada bunga, warna normal pada petal dan sepal diselingi oleh bagian warna yang lebih terang atau redup tidak beraturan (Burnett 1965). Selain itu ORSV dapat menyebabkan nekrosis coklat bergaris dan malformasi serta distorsi pada rangkaian bunga Cattleya (Afieri et al. 1991;
Virus ini tidak dapat ditularkan oleh vektor serangga (Namba & Ishii 1971) namun dapat ditularkan secara mekanis dan dapat bertahan lama pada media pot (Ajjikuttira et al. 2002). Penularan secara mekanis pada tanaman indikator Chenopodium amaranticolor, C. Quinoa, dan Gomphrena globosa menyebabkan
gejala lesio lokal sedangkan pada Tetragonia expansa gejala awalnya lesio lokal
kemudian berkembang menjadi menguning (Navalienskiene et al. 2005).
Selain ORSV, virus lain yang banyak menginfeksi pertanaman anggrek di dunia adalah CymMV. CymMV pertama kali dideskripsi oleh Jensen yang mengamati gejala mosaik dan bercak bergaris nekrosis pada anggrek
Cymbidium (Jensen 1951). Virus ini menyebar di beberapa negara di dunia pada
berbagai jenis anggrek (Moles et al. 2007). Infeksi CymMV menyebabkan
kerugian secara ekonomis karena menurunkan kualitas bunga (Chia et al. 1992).
CymMV menginfeksi beberapa genus anggrek seperti Cattleya, Dendrobium, Epidendrum, Laelia, Phaleonopsis dan Vanda. Infeksi CymMV pada jenis
tanaman anggerk tersebut menyebabkan penurunan vigor tanaman dan kualitas bunga (Lawson & Hsu 1995)
Tanaka et al. (1997) melaporkan bahwa beberapa jenis anggrek di
Thailand terinfeksi CymMV dengan kejadian penyakit sebesar 67% pada anggrek
Cymbidium, 45.5% pada Cattleya, 65.7% pada Dendrobium, 35% pada Oncidium, 25% pada Phalaenopsis, dan 51% pada Vanda. Khalimi (2008)
melaporkan, berdasarkan hasil ELISA terhadap 107 sampel bergejala yang dikumpulkan dari 3 lokasi survei (Gunung Sindur-Bogor, Segunung, Kebun Raya), bahwa sebanyak 62,62% sampel anggrek yang terdeteksi dinfeksi oleh CymMV. Kejadian penyakit CymMV tertinggi terjadi pada lokasi pengambilan sampel di Gunung Sindur-Bogor (64,0%).
Tanaman anggrek yang terinfeksi CymMV selalu memperlihatkan gejala ukuran bunga lebih kecil, kualitas jelek, dan bentuk bunga yang cacat sebagaimana gejala pada daun, sehingga menyebabkan kehilangan nilai ekonomi yang tinggi (Seoh et al. 1998). Gejala infeksi CymMV lain di lapangan
berupa mosaik, klorosis dan nekrosis pada daun dan bunga (Sherpa et al.
2006a).
CymMV dapat ditularkan secara mekanis dan melalui bahan perbanyakan vegetatif tanaman, tetapi tidak dapat ditularkan melalui biji dan oleh serangga (Ryu et al. 1995). CymMV dapat ditularkan melalui kontak langsung antara
yang digunakan selama perawatan dan panen bunga di lapangan (Wisler 1989; Lawson & Hsu 1995).
Belum banyak penelitian yang melaporkan CMV pada tanaman anggrek. Pengamatan biologis dilakukan pada tanaman anggrek Phalaenopsis yang
terinfeksi CMV di Taiwan menggunakan pewarnaan azure A. Pada jaringan yang
terinfeksi terlihat bentuk sudut dan berbagai variasi ukuran badan inklusi. Inklusi tersebut berupa agregasi kristal virus yang terlihat jauh lebih berlimpah di bagian mesofil dari pada bagian sel-sel epidermis. Inklusi ini juga terjadi berlimpah dalam sel floem daun dewasa dan terbatas pada daun yang baru muncul. Identitas virus tersebut dikonfirmasi dengan mikroskop elektron imunofluoresensi
yang dimodifikasi pada sectioning tipis dan diberi label elektron immunogold (Ko
1988).
Virus lain yang menginfeksi anggrek yaitu Potyvirus. Potyvirus pada
anggrek menyebabkan bercak klorosis pada daun Phalaenopsis yang diamati di
Taiwan. Virus diisolasi dari daun anggrek Phalaenopsis sakit dan ditularkan
pada Chenopodium quinoa dan Nicotiana benthamiana. Virus bereaksi dengan
antibodi monoklonal terhadap kelompok Potyvirus. Pengamatan pada sap dan
hasil purifikasi terlihat partikel berbentuk filamen dengan ukuran panjang sekitar 12-15 × 750-800 nm dan badan inklusi berbentuk pinwheel diamati pada sel yang
terinfeksi. (Zheng et al. 2008). Hasil identifikasi, isolasi, inokulasi kembali,
karakterisasi serologi dan molekuler terhadap Potyvirus tersebut diberi nama Phalaenopsis chlorotic spot virus (PhCSV) (Chen et al. 2006).
Deteksi terhadap ORSV telah dilakukan sejak tahun 1951, pada awalnya virus ini disebut sebagai Tobacco mosaic virus strain Orchid (Orchid TMV)
berdasarkan sifat-sifat awal yang diidentifikasi (Thomson & Smirk 1967). ORSV mudah dibedakan dari TMV dan Tobamovirus lainnya dengan kemajuan metode
identifikasi, berdasarkan kisaran inang, serologi, dan sekuen nukleotida pada bagian terminal 3’ (Isomura et al. 1990; Isomura et al. 1991).
Berbagai metode deteksi juga dikembangkan untuk mendeteksi secara sensitif terhadap CymMV dan ORSV. Metode yang dikembangkan antara lain
slot-blot hybridization assay (Sherpa et al. 2006a) dan Capillary zone electrophoresis dan Immuno-capillary zone electrophoresis (I-CZE) (Eun &
Wong 1999).
Metode deteksi lain yang umum dilakukan untuk deteksi ORSV dan CymMV adalah reverse transcription-polymerase chain reaction (RT-PCR) yang
berhasil dilakukan oleh Ryu et al. (1995) dan imonocapture-PCR juga berhasil
dikembangkan oleh Barry et al. (1996). Teknik RT-PCR berhasil dilakukan untuk
mendeteksi ORSV yang menginfeksi tanaman anggrek di Singapura menggunakan sepasang primer yang mengamplifikasi full lenght coat protein
(ORF5) pada posisi 5721-6197 (Ajjikuttira et al. 2005). Teknik deteksi lainnya
adalah menggunakan digoxigenin (DIG)-labeled cRNA probes (Hu & Wong
1998), dan simultan touchdown (TD) RT-PCR dengan pasangan primer tunggal
(Seoh et al. 1998) serta molecular beacons yang dapat mendeteksi secara
bersamaan dua virus ORSV dan CymMV (Eun & Wong 1999).
Adanya virus-virus tersebut pada beberapa negara di Asia, penting artinya bagi pengusahaan anggrek di Indonesia karena kedekatan lokasi dan aktivitas masuk keluarnya bibit anggrek. Sistem perdagangan terbuka memungkinkan virus tanaman masuk melalui kegiatan impor bahan tanaman. Saat ini, Indonesia masih mengimpor bibit anggrek dalam bentuk botolan dan kompot dari beberapa negara seperti Thailand, Singapura dan Taiwan. Selain melalui importir bibit, tanaman anggrek juga masuk melalui para penggemar anggrek. Oleh karena itu perlu dilakukan kajian yang mendeteksi dan mengidentifikasi beberapa virus yang menginfeksi tanaman anggrek di Indonesia, khususnya di Pulau Jawa.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui beberapa virus yang menginfeksi tanaman anggrek di Pulau Jawa yaitu :
1. CMV dan Potyvirus, sebarannya dan mengidentifikasi dengan RT-PCR.
2. CymMV; sebarannya, mengidentifikasi karakter molekuler dengan teknik serologi, RT-PCR dan analisis sekuen beberapa isolat CymMV.
3. ORSV; sebarannya, mengidentifikasi karakter biologi melalui uji penularan, karakter molekuler melalui teknik serologi, RT-PCR dan analisis sekuen isolat ORSV yang ada pada pertanaman anggrek di Indonesia.
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian ini dilakukan dari Bulan Juli 2008 sampai Desember 2009, di Rumah Kasa dan di Laboratorium Virologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor.
Pengumpulan Sampel Tanaman Anggrek yang Terinfeksi
Survei dilakukan untuk mengumpulkan tanaman yang bergejala khas infeksi virus. Survei dan pengambilan contoh tanaman (sampel) anggrek dilakukan di kebun petani/pengusaha anggrek di Jawa Barat (Gunung Sindur-Bogor, Kebun Raya-Sindur-Bogor, Balai Penelitian Tanaman Hias Segunung Cipanas-Cianjur, Lembang-Bandung), Jawa Tengah (Magelang), Jawa Timur (Surabaya, Malang) dan DKI Jakarta (Taman Anggrek Indonesia Permai,TAIP). Survei
dilakukan untuk mengamati gejala pada tanaman anggrek, mengetahui pengaruh infeksi terhadap anggrek, variasi gejala yang muncul pada jenis tanaman anggrek berbeda serta kejadian penyakit pada beberapa lokasi.
Deteksi dan Identifikasi Virus pada Anggrek Serologi
ORSV dan CymMV dideteksi secara serologi dari sampel tanaman hasil survei dan hasil uji penularan pada tanaman indikator. Teknik direct double antibody sandwich-enzyme linked immunoabsorbent assay (DAS-ELISA)
digunakan sesuai prosedur yang dikemukakan oleh pembuat antiserum. Antiserum yang digunakan adalah antiserum spesifik CymMV dan ORSV (DSMZ, Jerman). Analisis secara kuantitatif hasil ELISA ditentukan menggunakan ELISA reader pada panjang gelombang 405 nm. Pengujian dinyatakan positif jika nilai
absorban 1,5x nilai kontrol negatif (tanaman sehat).
Deteksi dengan RT-PCR
Ekstraksi total RNA. Ekstraksi RNA total dilakukan pada sampel tanaman yang dipilih. RNA total diperoleh dari 0,1 g daun bergejala yang digerus dengan nitrogen cair dan diekstraksi menggunakan kit isolasi RNA total (RNAeasy Plant Mini Kit) sesuai prosedur pembuatnya (Qiagen Inc., Chatsworth, CA, USA). Total
Sintesis cDNA. RNA total yang diperoleh digunakan sebagai template
untuk sintesis first strand complementary DNA (cDNA) pada mesin PCR.
Komposisi reagen reaksi RT (reverse transcription) dengan total volume 10 μl
(Tabel 3.1). Total RNA yang diperoleh ditambahkan reagen RT sampai mencapai volume total 10 μl kemudian diamplifikasi menggunakan mesin PCR
Automated Thermal Cycler (GeneAmp 2400; Perkin-Elmer Corp., Norwalk, CT)
yang diprogram untuk satu siklus pada 25 oC selama 5 menit, 42 oC selama 60
menit, dan 70 oC selama 15 menit. Hasil RT tersebut kemudian disimpan pada
suhu -20 oC sampai siap digunakan untuk reaksi RT-PCR.
RT-PCR. Reagen PCR terdiri dari cDNA, PCR mix (Go taq green,
Promega), sepasang primer dan ddH2O (Tabel 3.2). Reaksi PCR diamplifikasi
dengan menggunakan sepasang primer yang mengamplifikasi gen CP untuk masing-masing virus (Tabel 3.3). Amplifikasi dilakukan menggunakan mesin PCR Automated Thermal Cycler dengan kondisi PCR berbeda untuk
masing-masing virus (Tabel 3.4).
Tabel 3.1 Komposisi reagen untuk reaksi reverse trancription (RT)
No. Reagent Vol (µl) Konsentrasi
1. Sampel RNA ORSV 2,00
2. Bufer RT 10x 1,00 1x
3. M-MuLV (200U/ μl) 0,50 100 unit
4. 10 mM dNTP 1,00 2,00 mM 5. 10 μM oligo-dT 1,00 1,00 μM 6. Rnase I (40U/ul) 0,50 2,00 unit
7. dd H2O 4,00
Total 10,00
Tabel 3.2 Komposisi reagen untuk reaksi PCR
No Reagen Volume (µl) Konsentrasi akhir
1 Go taq green (Promega) 12,5 1 x
2 cDNA 2,0 < 250 ng
3 Primer forward 10 µM 1,0 1,0 µM
4 Primer reverse 10 µM 1,0 1,0 µM
5 ddH2O 8,5 N.A
Tabel 3.3 Sekuen primer yang digunakan untuk deteksi virus pada anggrek
No Primer Nama Sekuen primer Produk PCR (bp)
Referensi
1 CMV-IF 5´-ACCGCGGGTCTTATTATGGT–3’ 382 Aramburu et al.
(2007) CMV-IR 5´-ACGGATTCAAACTGGGAGCA-3’ 2 Potyvirus (MJ1)(f) 5’-TGGTHTGGTGYATHGARAAYGG-3’ 327 Marie-Jeanne et al. (2000) Potyvirus (MJ2)(r) 5’-TGCTGCKGCYTTCATYTG-3’ 3 Tospovirus (gL3637)
5’-CCTTAACAGTDGAAACAT-3’ 800 Chu et al.
(2001) Tospovirus (gL4435c) 5’-CATDGCRCAAGARTGRTARACAGA-3’ 4 CymMV-CPF
5´-CGGGATCCATGGGAGAGTCCACTCCA-3’ 672 Sherpa et al.
(2007) CymMV-CPR 5´-GGAATTCTCAGTAGGGGGTCCAGGC-3’ 5 ORSV- CP-f
5’-GCTCTAGAATGTCTTACACTATTACAGACC-3’ 477 Ajjikuttira et al.
(2005) ORSV-
CP-r
5’- TCCCCCGGGTTAGGAAGAGGTCCAAGTAAG- 3’
Tabel 3.4 Kondisi PCR untuk deteksi virus pada anggrek
No Primer Kondisi PCR
1 CMV-IF & CMV-IR 93,5 oC 3 menit; 93,5 oC, 45 detik; 55 oC, 45 detik; 72 oC, 1 menit ekstensi 72 oC, 5 menit. (35 siklus)
2 MJ1 (f) & MJ2 (r) 94 oC 3 menit; 94 oC, 30 detik; 50 oC, 1 menit; 72 oC, 1 menit ekstensi 72 oC, 10 menit. (45 siklus)
3 gL3637 & gL4435c 93 oC 5 menit; 93 oC, 1 menit; 50 oC, 1 menit; 72 oC, 2 menit ekstensi 72 oC, 5 menit. (35 siklus)
4 CymMV-CPF &
CymMV-CPR 95
oC 5 menit; 95 oC, 30 detik; 50 oC, 45 detik; 72 oC, 1 menit ekstensi 72 oC, 10 menit. (35 siklus)
5 ORSV-CP-f &
ORSV-CP-r 95
oC 5 menit; 95 oC, 30 detik; 50 oC, 45 detik; 72 oC, 1 menit ekstensi 72 oC, 10 menit. (35 siklus)
Visualisasi DNA. DNA virus hasil amplifikasi dielektroforesis menggunakan gel agarose 1,2% (w/v) (dalam TBE 0,5 X) yang mengandung
Ethidium bromide (0,5 mg/10 ml). Penanda DNA yang digunakan adalah ladder
100 bp dan 1 Kb (Fermentas), sebanyak 8 µl yang dicampurkan dengan 2 µl 5x
loading buffer. Elektroforesis dilakukan pada tegangan 70 V DC selama 60
menit. Hasil elektroforesis divisualisasi dibawah transilluminator ultraviolet dan
Analisis Sekuen Nukleotida dan Asam Amino Gen CP ORSV dan CymMV
Perunutan DNA. Sampel DNA hasil RT-PCR digunakan untuk sekuen nukleotida. Sekuen nukleotida ORSV sampel Gunung Sindur-Bogor dilakukan di Laboratorium Charoen-Phokphan Indonesia, Jakarta, sedangkan untuk sampel
Kebun Raya-Bogor, Cipanas-Cianjur dan TAIP-Jakarta dilakukan di Laboratorium
Genetica Science di Singapura. Sekuen nukleotida untuk semua sampel
CymMV dilakukan di laboratorium Macrogen Inc Seoul, Korea Selatan.
Analisis Filogenetika. Sekuen gen CP dianalisis untuk mengetahui tingkat homologi dengan gen CP dari virus yang sama yang telah di deposit pada
GeneBank menggunakan software Wu-Blastn (www.ebi.ac.uk). Alignment
selanjutnya dilakukan dengan membandingkan homologi isolat ORSV Gunung Sindur-Bogor, Kabun Raya Bogor, Cipanas-Cianjur dan dengan sekuen gen CP 11 isolat ORSV dari beberapa negara dan satu isolat TMV sebagai pembanding diluar grup (outgroup) (Tabel 3.5). Alignment seluruh isolat CymMV Pulau Jawa
dilakukan dengan membandingkan homologinya terhadap 10 isolat CymMV dari beberapa negara dan satu isolat Potato Virus X (PVX) sebagai pembanding outgroup (Tabel 3.6). Matriks identitas nukleotida dan asam amino diperoleh
menggunakan software BioEdit (Hall 1999).
Pohon filogenetika dikonstruksi menggunakan software MEGA versi 4.0
(Tamura et al. 2007), dengan metode neighbour-joining menggunakan bootstrap
1000 kali pengulangan. Gambar alignment dihasilkan dengan menggunakan
program GeneDoc versi 2.7.000 (Nicholas & Nicholas 1997).
Tabel 3.5 Isolat ORSV dari beberapa negara dan TMV pada GeneBank yang
dibandingkan dengan enam isolat ORSV asal Indonesia
No. Isolat Kode aksesi Aksesor*
1. Brazil AF515606 Rivas et al. 2000
2. Hangzhou (China) AM398154 Shi & Xu 2006
3. Yunan (China) AM055643 Li et al. 2005
4. Taiwan AF406775 Ajjikuttira et al. 2005
5. India AJ564563 Sherpa et al. 2005
6. Korea Selatan EU683879 Chung 2008.
7. Jerman AJ429093 Letschert et al. 2005
8. Florida (USA) U89894 Hilf & Dawson, 1993
9. Singapura AF455273 Ajjikuttira et al. 2004
10. Jepang X55295 Isomura et al. 1991
11. Thailand AY376394 Srifah 2003
12. TMV Yunan AF516913 Ding et al. 2002
* Aksesor merupakan peneliti yang mendaftarkan sekuen Isolat ORSV hasil penelitiannya ke GeneBank
Tabel 3.6 Isolat CymMV dari beberapa negara dan PVX pada GeneBank yang
dibandingkan dengan enam isolat CymMV asal Indonesia
No. Isolat Kode aksesi Aksesor*
1. China Phalaenopsis FJ356061 Pan et al. 2008
2. China Cymbidium DQ067883 Zhang & Chen 2005
3. Hawaii EF125180 Vaughan et al. 2008
4. India 1 Cymbidium EU499362 Pooja et al; 2010
5. India 2 Cattleya sp. AJ698947 Sherpa 2006b
6. Jepang AB197937 Tanno & Itoh 2005
7. Korea Selatan AB541562 Choi et al. 2010
8. Perancis AM236028 Moles et al. 2007
9. Singapura AF405719 Ajjikuttira et al. 2005
10. Taiwan AY571289 Wang & Lin 2004
11. PVX PVU19790 Wang et al. 1991/1995
* Aksesor merupakan peneliti yang mendaftarkan sekuen Isolat ORSV hasil penelitiannya ke GeneBank.
Respon Pada Tanaman Indikator
Perbanyakan sumber inokulum. Untuk mendapatkan virus murni dari tanaman anggrek yang bergejala dilakukan isolasi pada tanaman indikator
Datura stramonium. Tanaman bergejala diperoleh dari tanaman anggrek asal
Gunung Sindur-Bogor. Tanaman anggrek yang positif terinfeksi ORSV berdasarkan hasil ELISA digerus dalam larutan bufer fosfat 0,05 M pH 7,0 (29.1 ml 0.1 M NaOH, 50 ml 0.1 M KH2PO4) dengan perbandingan 1 : 5 (0.1 gram per
500 μl larutan bufer fosfat (1:5 b/v) menggunakan mortar dan pistil steril. Daun tanaman D. stramonium yang akan diinokulasi dilukai dengan karborundum 600
mesh dengan menaburkannya pada permukaan daun, kemudian cairan perasan (sap) dari tanaman sakit dioleskan pada permukaan daun dengan cotton bud,
dilakukan searah tulang daun. Setiap tanaman diinokulasi pada 2 helai daun termuda yang telah membuka penuh. Setelah pengolesan inokulum, permukaan daun dibilas dengan aquades untuk membuang sisa karborundum yang masih melekat pada permukaan daun tanaman uji. Pengamatan gejala dan waktu inkubasi dilakukan sampai 30 hari setelah inokulasi.
D. stramonium akan menunjukkan gejala lesio lokal pada 3–21 hari
setelah diinokulasi virus. Satu lesio tersebut kemudian diinokulasikan lagi ke tanaman D. stramonium secara mekanis dan hal ini dilakukan secara berulang
sampai tiga kali untuk mendapatkan virus murni. Lesio lokal diakhir inokulasi ke tiga kemudian diinokulasi ke tanaman Nicotiana benthamiana untuk
memperbanyak virus. Tanaman N. benthamiana yang bergejala digunakan
sebagai inokulum virus untuk uji penularan ORSV pada tanaman indikator.
Penularan pada tanaman indikator. Tanaman uji yang digunakan sebagai tanaman indikator adalah D. stramonium, N. tabacum cv. Xanthi, N. benthamiana, Chenopodium amaranticolor, C. quinoa, Gomphrena globosa, Cassia occidentalis, dan vanili (Vanilla planifolia). Tanaman indikator
ditumbuhkan dari benih yang ditanam dalam pot-pot kecil (diameter sekitar 15 cm) dengan media tanah + pupuk kandang (1:1) dan dipelihara dalam rumah kaca kedap serangga sampai siap diinokulasi.
Daun-daun tanaman indikator diinokulasi dengan sap N. benthamiana
yang terinfeksi ORSV. Sap disiapkan dengan menggerus daun N. benthamiana
hasil perbanyakan inokulum dalam 500 mM bufer fosfat pH 7,2 (1:5 b/v) dengan mortar. Sap dioleskan dengan cotton bud di atas permukaan daun tanaman
indikator yang telah terlebih dahulu ditaburi Carborundum. Tanaman indikator
yang telah diinokulasi dipelihara sebaik-baiknya dalam rumah kasa kedap serangga dan waktu inkubasi diamati setiap hari sampai muncul gejala.
HASIL DAN PEMBAHASAN
Hasil
Sebaran Virus
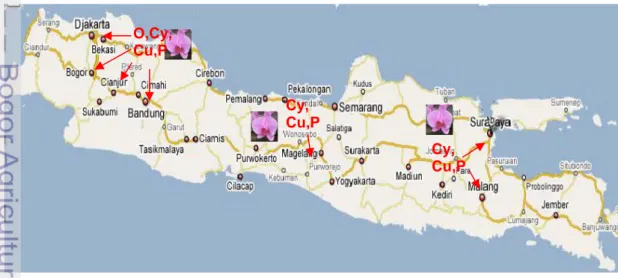
Hasil pengamatan pada beberapa lokasi sentra pengembangan anggrek di Jawa Timur (Surabaya dan Malang), Jawa Tengah (Magelang), Jawa Barat (Gunung Sindur-Bogor, Kebun Raya-Bogor, Balai Penelitian Tanaman Hias Cipanas-Cianjur, Lembang-Bandung), dan DKI Jakarta (Taman Anggrek Indonesia Permai/TAIP) dideteksi secara serologi adanya CymMV dan ORSV. Namun, ORSV hanya ditemukan di Bogor Cianjur dan Jakarta, sedangkan CymMV ditemukan hampir di semua lokasi survei (Gambar 3.1). Di lokasi Gunung Sindur-Bogor, Kebun Raya-Bogor dan Cipanas-Cianjur ditemukan tanaman anggrek Dendrobium yang terinfeksi ganda oleh kedua jenis virus
tersebut.
Sampel tanaman yang diambil dari berbagai lokasi menunjukkan keempat virus menginfeksi beberapa jenis tanaman anggrek. Jenis anggrek yang diinfeksi meliputi jenis anggrek spesies/klon (Cymbidium purpureum, Oncydium golden shower, Phalaenopsis Klon) maupun hibrida (D. burana Jade X D.nindii). Pada
pengamatan di lokasi pengambilan sampel tanaman terlihat bahwa tanaman yang terinfeksi diletakkan secara berdekatan dengan tanaman sehat sehingga ada kemungkinan terjadinya penularan virus ke tanaman sehat secara mekanis. Tanaman yang terinfeksi dapat menyebar ke berbagai daerah lain di Indonesia mengingat anggrek pada lokasi yang diamati diperjualbelikan antar pulau.
Gambar 3.1 Sebaran sampel anggrek yang terinfeksi ORSV (O), CymMV (Cy), CMV (C) dan Potyvirus (P) di Pulau Jawa.
O,Cy, Cu,P Cy, Cu,P Cy, Cu,P
Gejala Infeksi Virus pada Anggrek
Gejala yang ditimbulkan oleh ORSV dan CymMV di lapangan bervariasi berdasarkan jenis anggrek yang diinfeksi. Variasi gejala ini dapat pula disebabkan oleh adanya infeksi campuran dengan CMV dan Potyvirus.
Gejala yang teramati pada enam lokasi pangambilan sampel tanaman menunjukkan adanya variasi, tergantung jenis anggrek yang diinfeksi. Variasi gejala yang muncul berupa nekrosis pada bagian bawah permukaan daun, mosaik dan belang. Pada anggrek Cymbidium sp. asal Surabaya menunjukkan
gejala nekrosis pada bagian bawah permukaan daun, sedangkan pada anggrek
Phalaenopsis di lokasi penangkaran Malang ditemukan gejala mosaik dan
belang. Pengamatan pada lokasi petani dan penangkaran anggrek di Magelang, Lembang dan Kebun Raya-Bogor menunjukkan kemiripan gejala pada jenis C. purpureum dan C. murasaki. Gejala yang teramati berupa mosaik klorosis
dengan pinggiran yang jelas, permukaan daun tidak rata serta bercak nekrosis berbentuk bintik–bintik atau garis berwarna hitam pada daun tua. Di lokasi petani anggrek Gunung Sindur-Bogor, Anggrek Dendrobium sp. menunjukkan gejala
mosaik dan mottle dengan pinggiran yang tidak tegas, ditemukan pula anggrek
dengan daun malformasi (Gambar 3.2). Gejala lainnya yang disebabkan CymMV yang muncul di lapangan pada tanaman anggrek yang disurvei menunjukkan adanya variasi seperti nekrosis dan mosaik pada jenis anggrek yang berbeda, mosaik merata pada permukaan daun, konsentris, nekrosis pada bagian belakang daun dan bentuk daun abnormal. Pada bunga ditemukan adanya gejala nekrosis. Umumnya gejala CymMV pada jenis anggrek Cymbidium dari
semua lokasi sama berupa mosaik dan nekrosis yang serta permukaan daun tidak rata (Gambar 3.3).
Pada jenis anggrek Oncydium gejala terlihat bercak nekrosis merata di
atas dan bawah permukaan daun (Gambar 3.4 A,B). Gejala infeksi pada jenis anggrek yang sama (Dendrobium) terlihat berbeda pada lokasi yang berbeda,
pada Dendrobium di lokasi Gunung Sindur-Bogor terlihat mosaik yang jelas dan
mosaik menguning (Gambar 3.4 C,D) sedangkan di lokasi Malang mosaik tersamar dan permukaan tidak rata (Gambar 3.4 E,F).
Gambar 3.2 Variasi gejala infeksi CymMV pada tanaman anggrek di beberapa lokasi pengamatan : (A) Nekrosis pada anggrek Oncydium sp., Surabaya; (B) Mosaik pada anggrek Phalaenopsis, Malang; (C) Mosaik pada anggrek C.
purpureum, Magelang; (D) mosaik pada anggrek Dendrobium sp., Gunung
Sindur-Bogor; (E) mosaik pada anggrek C. murasaki, Kebun Raya-Bogor; dan (F) Mosaik pada anggrek C. purpureum, Lembang;
Gambar 3.3 Gejala CymMV pada anggrek Cymbidium, (1) mosaik; (2) nekrosis; dan (3) nekrosis dengan permukaan tidak rata, pada sampel daun anggrek dari beberapa lokasi, (A) Kebun Raya-Bogor; (B) Lembang-Bandung; (C) Magelang. B A C E D F 1A 2A 3A 1B 2B 3B 1C 2C 3C
Gambar 3.4 Perbandingan gejala pada tanaman anggrek yang terinfeksi CymMV: (A,B) nekrosis pada daun anggrek Oncydium; (C,D)
mosaik jelas pada anggrek Dendrobium Gunung Sindur; (E)
mosaik tersamar pada anggrek Dendrobium Malang; (F) mosaik
dengan permukaan tidak rata pada anggrek Dendrobium Malang.
Pada anggrek Dendrobium yang terinfeksi ORSV di semua lokasi
pengamatan, gejala yang tampak yaitu bercak klorosis dengan pola konsentris pada permukaan daun, sedangkan pada sisi bawah daun terlihat nekrosis yang bersambungan. Gejala lainnya berupa malformasi pada daun serta nekrosis pada bunga anggrek yang terinfeksi lebih berat (Gambar 3.5 A-E). Deteksi serologi pada sampel tanaman anggrek yang tidak bergejala menunjukkan positif terinfeksi ORSV (Gambar 3.5 F). Gejala pada tanaman yang terinfeksi ganda terlihat lebih berupa tanaman menjadi kerdil dan rangkaian bunga tidak berkembang sehingga ukurannya menjadi pendek. (Gambar 3.6).
A B
C D
Gambar 3.5 Gejala pada tanaman anggrek Dendrobium yang terinfeksi ORSV:
(A,B) mosaik; (C) nekrosis merata pada permukaan daun; (D) daun abnormal; (E) nekrosis pada bunga; (F) tanpa gejala.
Gambar 3.6 Gejala pada tanaman anggrek Dendrobium yang terinfeksi ganda
CymMV dan ORSV: (A) rangkaian bunga pendek; (B) tanaman kerdil
A B
C D
E F
Identifikasi dan Karakterisasi Molekular Virus Anggrek Uji Serologi
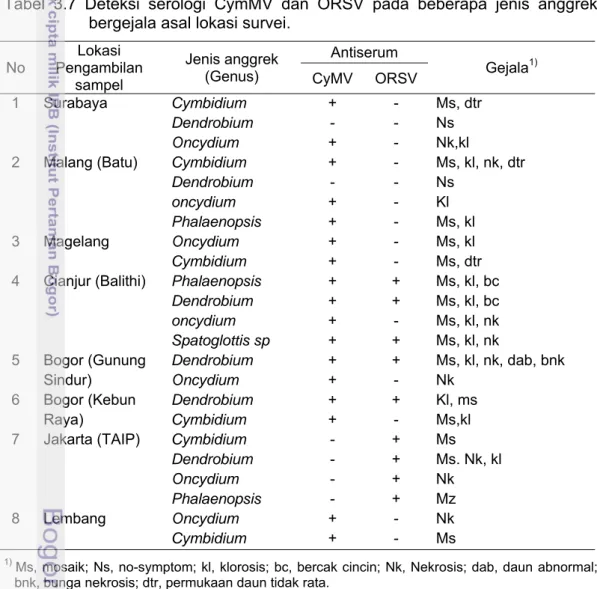
Sampel yang dikumpulkan dari beberapa lokasi menunjukkan reaksi positif terhadap antiserum spesifik CymMV dan ORSV. Beberapa sampel menunjukkan hanya positif CymMV saja, ORSV saja ataupun positif terhadap kedua antiserum (Tabel 3.7). Hal ini menunjukkan bahwa ORSV dan CymMV telah ada dan menyebar luas di berbagai jenis anggrek dan lokasi di Pulau Jawa. Tabel 3.7 Deteksi serologi CymMV dan ORSV pada beberapa jenis anggrek
bergejala asal lokasi survei.
No Pengambilan Lokasi sampel Jenis anggrek (Genus) Antiserum Gejala1) CyMV ORSV 1 Surabaya Cymbidium + - Ms, dtr Dendrobium - - Ns Oncydium + - Nk,kl
2 Malang (Batu) Cymbidium + - Ms, kl, nk, dtr
Dendrobium - - Ns
oncydium + - Kl
Phalaenopsis + - Ms, kl
3 Magelang Oncydium + - Ms, kl
Cymbidium + - Ms, dtr
4 Cianjur (Balithi) Phalaenopsis + + Ms, kl, bc
Dendrobium + + Ms, kl, bc oncydium + - Ms, kl, nk Spatoglottis sp + + Ms, kl, nk 5 Bogor (Gunung Sindur) Dendrobium + + Ms, kl, nk, dab, bnk Oncydium + - Nk 6 Bogor (Kebun Raya) Dendrobium + + Kl, ms Cymbidium + - Ms,kl
7 Jakarta (TAIP) Cymbidium - + Ms
Dendrobium - + Ms. Nk, kl
Oncydium - + Nk
Phalaenopsis - + Mz
8 Lembang Oncydium + - Nk
Cymbidium + - Ms
1) Ms, mosaik; Ns, no-symptom; kl, klorosis; bc, bercak cincin; Nk, Nekrosis; dab, daun abnormal;
bnk, bunga nekrosis; dtr, permukaan daun tidak rata.
Hasil konfirmasi menggunakan antiserum CymMV terhadap sampel beberapa jenis anggrek berbeda dengan variasi gejala dari berbagai lokasi menunjukkan nilai absorban ELISA (NAE) yang bervariasi dari 2-8 kali kontrol negatif (Tabel 3.8). Hasil deteksi ELISA terhadap sampel tanaman bergejala dari lokasi Kebun Raya-Bogor menunjukkan positif bereaksi dengan antiserum
ORSV dan dan CymMV dengan kejadian penyakit 20% dan 80% dari sampel yang diuji (10 tanaman).
Tabel 3.8 Perbandingan hasil ELISA CymMV pada sampel anggrek yang dikumpulkan dari beberapa lokasi survei.
No Lokasi Jenis anggrek Gejala dominan NAE*
1 Magelang Cymbidium purpureum Mosaik, daun cembung, 1,502
2 Surabaya Oncydium sp Nekrosis, khlorosis 1,387**
3 Lembang Cymbidium purpureum Mosaik, daun
cembung, nekrosis
0,685
4 Bogor (Gunung Sindur) Dendrobium sp Mosaik, mottle, 0,572
5 Malang (Batu) Phalaenopsis Klon 237E Mosaik, mottle 0,442
6 Bogor (Kebun Raya) Cymbidium Murasaki Mosaik, khlorosis,
nekrosis 0,384
* NAE = Nilai Absorban ELISA; kontrol negatif (KN) 0,171; ** NAE merupakan rata-rata dari 3 tanaman sampel kecuali C. murasaki hanya satu tanaman.
RT-PCR
Hasil deteksi RT-PCR terhadap sampel dari berbagai lokasi di Pulau Jawa menunjukkan seluruh sampel teridentifikasi CymMV, CMV dan Potyvirus,
sedangkan sampel Jawa Barat (kecuali Lembang) dan Jakarta teridentifikasi ORSV. Belum ditemukan sampel yang positif teridentifikasi adanya Tospovirus
(Tabel 3.9)
Tabel 3.9 Rekapitulasi hasil deteksi RT-PCR virus anggrek dari lokasi survei.
No Asal Lokasi RT-PCR
CMV Potyvirus Tospovirus CymMV ORSV
1 Surabaya + + - + - 2 Malang (Batu) + + - + - 3 Magelang + + - + - 4 Bogor (Gunung Sindur) + + - + + 5 Bogor (Kebun Raya) + + - + + 6 Lembang + + - + - 7 Cianjur (Balithi) + + - td + 8 Jakarta (TAIP) + + - - +
meng teram CMV hasil angg Ga Poty teram bahw Ga 3 3 CMV. H ggunakan mplifikasi D V merupaka deteksi ini grek. ambar 3.7 t s Potyviru yvirus terha mplifikasiny wa Potyvirus ambar 3.8 82 bp 327 bp Hasil deteks primer u NA berukur an virus um i menjadi in Hasil visual lajur (1) Iso Cipanas-Cia tanaman te sehat, (7) Is (10) Isolat M us. Hasil adap semua a DNA ber s juga umum Hasil visua sampel laj (3) Isolat Kontrol po (7) Isolat L Isolat Mala 1 2 1 2 si RT-PCR universal u ran 382 bp mum yang d nformasi ba isasi pita DN lat TAIP-Jak anjur, (4) Iso embakau te solat Lemba Malang, (M) amplifikasi a sampel rukuran 327 m ditemuka alisasi pita D jur (1) Isolat Cipanas-C ositif tanama Lembang, ( ang, (M) Ma 3 4 3 4 pada sam untuk CM (Gambar 3. ditemukan aru terdetek NA CMV pad karta, (2) Is olat Gunung erinfeksi CM ang, (8) Isol Marker 100 i RT-PCR tanaman d 7 bp (Gam an pada sem DNA Potyvir t TAIP-Jaka ianjur, (4) an nilam, (6 8) Isolat Ma arker 100 bp 5 M 5 M mpel tanama V subgru .7). Hal ini pada angg ksinya CMV da gel agaro olat Kebun g Sindur-Bo MV, (6) Kon at Magelang bp. mengguna dari lokasi mbar 3.8). mua sampe rus pada ge arta, (2) Isol Isolat Gunu 6) Kontrol n agelang, (9) . M 6 6 7 an dari lok b IB me i menunjukk rek di Indo V pada berb ose 1,2% TB Raya-Bogo ogor, (5) Ko ntrol negati g, (9) Isolat kan primer survei me Hal ini me l anggrek. el agarose at Kebun R ung Sindur-negatif tanam ) Isolat Sura 7 8 8 9 kasi survei enunjukkan kan bahwa onesia dan bagai jenis BE; sampel r, (3) Isolat ntrol positif if tanaman t Surabaya, r universal enunjukkan enunjukkan 1,2% TBE; Raya-Bogor, -Bogor, (5) man sehat, abaya, (10) 9 10 10
To Tospoviru positif me 3.9). Hal i pada tana Gambar 3 Cy lokasi ya Kebun Ra (Gambar 3 Gambar 672 bp 800 bp ospovirus. us menunju engamplifika ni menunju aman anggr 3.9 Hasil v sampe Klon D Bogor, Isolat L Malang ymMV. DN ng berbed aya, Lemba 3.10). 3.10 Has sam Mag Bog terin kb ( 1 M 1 Hasil d kkan bahw asi DNA be ukkan bahw rek di Indon visualisasi p el lajur (M) M DNA TSWV (5) Isolat C Lembang, (8 g. NA hasil a a (Surabay ang) menun il visualisas mpel lajur no gelang, (4) I gor, (6) Isola nfeksi CymM (Fermentas) 2 1 2 3 eteksi RT-wa tidak ad erukuran 80 wa Tospovir esia, teruta pita DNA To Marker 100b V, (3) Isolat Cipanas-Cian 8) Isolat Ma amplifikasi R ya, Malang njukkan uku si pita DNA o. (1) Isolat Isolat Gunun at Lembang MV, (8) Kont ). 3 4 3 4 5 PCR meng da satu sa 00 bp, kecu rus kemung ama di Pulau ospovirus pa bp (1) Kontr TAIP-Jaka njur, (6) Isol agelang, (9) RT-PCR ke g, Magelan uran DNA y CymMV pa Surabaya, ng Sindur-B , (7) Kontro trol negatif t 5 5 6 ggunakan p ampel pun uali kontrol kinan belum u Jawa.
ada gel aga rol negatif, ( rta, (4) Iso at Gunung S ) Isolat Sura eenam isol ng, Gunung yang sama
ada gel aga (2) Isolat M ogor, (5) Iso ol positif tan tanaman seh 6 M 7 8 primer univ yang terde positif (Ga m terdeteks arose 1,2% (2) Kontrol p lat Kebun R Sindur-Bogo abaya, (10) lat CymMV g Sindur-B a yaitu ± 67 arose 1,2% Malang, (3) olat Kebun R aman Temb hat, (M) ma 7 9 10 versal eteksi ambar si ada TBE; positif Raya-or, (7) Isolat V dari Bogor, 72 bp TBE; Isolat Raya-bakau rker 1 8
gen DNA posit Gamb Cym Anal yang serta Hasi mem align Deng wala meng nukle (data seku Perb terse ORSV. CP terhada A berukuran tif ORSV be bar 3.11 Ha K ta Is J Deteksi MV dan OR lisis Runut Hasil peru g mengkode a asam am l alignmen mperlihatkan nment asam gan demikia upun triplet Alignmen ggunakan eotida gen a tidak dita uen dari ne bandingan n ebut didapa 477 b Deteksi mo ap sampel n ± 500 bp erdasarkan asil visualisa Kontrol positi anaman seh solat Kebun akarta. dan karakte RSV. tan Nukleot unutan DNA e 223 asam mino yang d t nukleotid n ada 99 p m amino me an ada 9 a t kodonnya nt keenam softwarwe CP CymM ampilkan). egara berbe nukleotida atkan homo bp 1 olekuler den tanaman a p. RT-PCR uji serologi
asi DNA gen f tanaman T at; (M) Mark Raya-Bogo erisasi virus tida dan As A gen CP m amino. A ditemukan da antara s posisi basa enunjukkan asam amino berbeda (L isolat CymM Wu.Blast2 V lainnya Berdasark eda untuk p sesama ke ologi sekuen 2 M ngan RT-PC asal lokasi R hanya di (Tabel 3.11 n CP ORSV Tembakau te ker 100 bp; ( or; (5) Isolat s yang lebi sam Amino CymMV d Ada beberap berdasarka sesama iso yang tidak n hanya 30 o yang men Lampiran 1.1 MV dengan 2 (www.EB memiliki tin an 50 seku perbanding eenam gen n sebesar 3 4 CR menggu survei berh ilakukan te 1). V pada gel a erinfeksi OR (3) isolat Gu t Cipanas-C h mendalam o Gen CP C diperoleh uk pa perbeda an sekuen olat CymM k sama uru asam ami ngkode asa 1 dan 1.2). n data yang BI.ac.uk) te ngkat homo uen gen C an terhada n CP CymM 96,2-98,5% 5 6 unakan prim hasil meng rhadap sam agarose 1,2% RSV; (2) Kon unung Sindu ianjur; (6) Is m dilakukan CymMV kuran 672 aan urutan DNA yang MV asal Pu utannya, na ino yang tid am amino y ada pada erhadap 5 ologi berkisa CP tersebut ap isolat Pu MV asal Pu %, sedangka mer spesifik amplifikasi mpel yang % TBE; (1) ntrol negatif r-Bogor; (4) solat TAIP-n terhadap nukleotida nukleotida diperoleh. ulau Jawa amun hasil dak sama. yang sama GeneBank 50 sekuen ar 93-95% t dipilih 10 ulau Jawa. ulau Jawa an dengan
isolat asal negara lain sebesar 95,8-98,8% (Tabel 3.10). Perbandingan isolat Pulau Jawa dengan isolat asal negara lain terlihat bahwa umumnya isolat Pulau Jawa memiliki similaritas 95,8-97,3% dengan isolat China Phal (Phalaenopsis)
kecuali isolat Malang yang memiliki similaritas terendah dengan isolat India 1. Similaritas tertinggi isolat Pulau Jawa umumnya dengan Isolat Jepang, Hawai dan Singapura (97,1-98,8%).
Perbandingan berdasarkan sekuen asam amino antar isolat Pulau Jawa menunjukkan homologi sebesar 98,6%-99,5%, sedangkan perbandingan terhadap sepuluh isolat dari negara lain memiliki homologi sebesar 97,3-99,5% (Tabel 3.11). Alignment antar sesama isolat asal Jawa menunjukkan similaritas
tertinggi (99,5%) yaitu antara CymMV isolat Magelang dengan isolat Surabaya. Perbandingan asam amino antara isolat Pulau Jawa dengan isolat negara lain umumnya menunjukkan bahwa isolat Pulau Jawa memiliki similaritas terendah (97,3-98,6%) dengan isolat China Phal dan China Cym (Cymbidium) kecuali
isolat Surabaya terendah dengan kedua isolat tersebut ditambah isolat India 1,
serta isolat Malang terendah hanya dengan isolat Perancis. Similaritas asam
amino tertinggi (99,1-100) yaitu antara isolat Gunung Sindur-Bogor, Magelang, Malang, Surabaya dengan isolat Jepang dan Korea Selatan, sedangkan isolat Kebun Raya dan Lembang tertinggi dengan isolat India 1. Hal ini menunjukkan kedekatan isolat Pulau Jawa dengan isolat dari ketiga negara tersebut.
Secara umum hasil perbandingan sekuen gen CP menunjukkan bahwa isolat CymMV asal Jawa masih merupakan strain yang sama dengan isolat lainnya di beberapa negara yang dibandingkan.
Alignment berdasarkan urutan nukleotida menunjukkan adanya mutasi
titik pada keenam isolat CymMV yang berbeda dengan 10 isolat lainnya yang dibandingkan. Mutasi terbanyak terjadi pada isolat CymMV Surabaya sedangkan yang terkecil terjadi pada isolat Magelang (Tabel 3.12, Lampiran 1.2). Walaupun isolat CymMV Surabaya yang mengalami mutasi terbanyak ternyata sekuen asam aminonya sama dengan isolat CymMV dari negara lainnya. Dengan demikian isolat CymMV Surabaya tidak mengalami perubahan komposisi asam amino meskipun mengalami mutasi nukleotida.
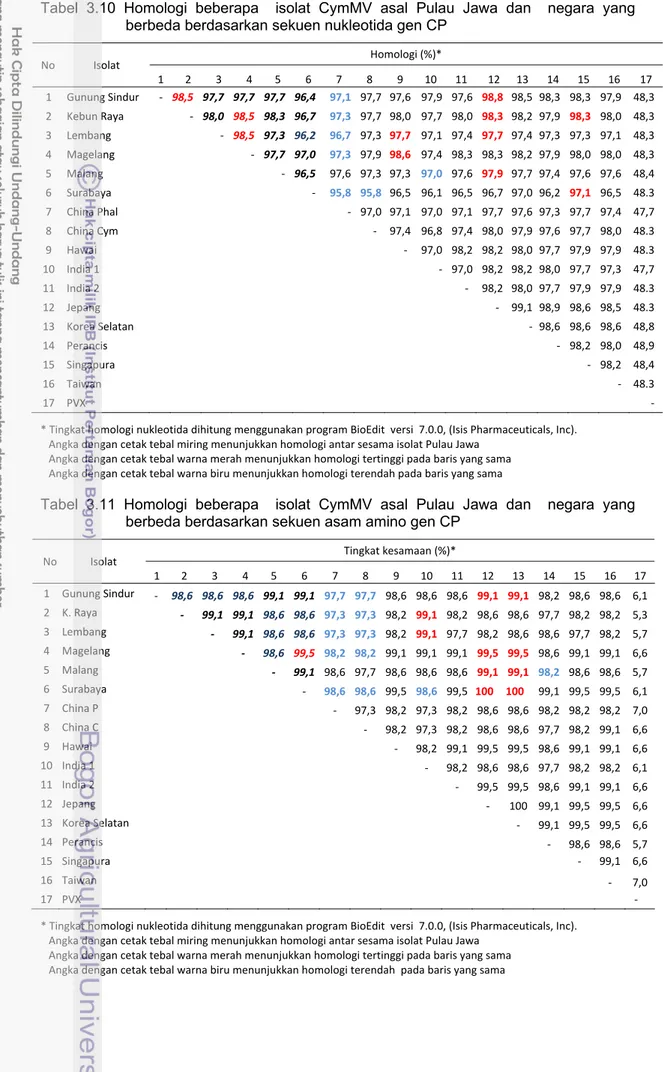
Tabel 3.10 Homologi beberapa isolat CymMV asal Pulau Jawa dan negara yang berbeda berdasarkan sekuen nukleotida gen CP
No Isolat Homologi (%)* 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 1 Gunung Sindur ‐ 98,5 97,7 97,7 97,7 96,4 97,1 97,7 97,6 97,9 97,6 98,8 98,5 98,3 98,3 97,9 48,3 2 Kebun Raya ‐ 98,0 98,5 98,3 96,7 97,3 97,7 98,0 97,7 98,0 98,3 98,2 97,9 98,3 98,0 48,3 3 Lembang ‐ 98,5 97,3 96,2 96,7 97,3 97,7 97,1 97,4 97,7 97,4 97,3 97,3 97,1 48,3 4 Magelang ‐ 97,7 97,0 97,3 97,9 98,6 97,4 98,3 98,3 98,2 97,9 98,0 98,0 48,3 5 Malang ‐ 96,5 97,6 97,3 97,3 97,0 97,6 97,9 97,7 97,4 97,6 97,6 48,4 6 Surabaya ‐ 95,8 95,8 96,5 96,1 96,5 96,7 97,0 96,2 97,1 96,5 48.3 7 China Phal ‐ 97,0 97,1 97,0 97,1 97,7 97,6 97,3 97,7 97,4 47,7 8 China Cym ‐ 97,4 96,8 97,4 98,0 97,9 97,6 97,7 98,0 48.3 9 Hawai ‐ 97,0 98,2 98,2 98,0 97,7 97,9 97,9 48.3 10 India 1 ‐ 97,0 98,2 98,2 98,0 97,7 97,3 47,7 11 India 2 ‐ 98,2 98,0 97,7 97,9 97,9 48.3 12 Jepang ‐ 99,1 98,9 98,6 98,5 48.3 13 Korea Selatan ‐ 98,6 98,6 98,6 48,8 14 Perancis ‐ 98,2 98,0 48,9 15 Singapura ‐ 98,2 48,4 16 Taiwan ‐ 48.3 17 PVX ‐
* Tingkat homologi nukleotida dihitung menggunakan program BioEdit versi 7.0.0, (Isis Pharmaceuticals, Inc). Angka dengan cetak tebal miring menunjukkan homologi antar sesama isolat Pulau Jawa
Angka dengan cetak tebal warna merah menunjukkan homologi tertinggi pada baris yang sama Angka dengan cetak tebal warna biru menunjukkan homologi terendah pada baris yang sama
Tabel 3.11 Homologi beberapa isolat CymMV asal Pulau Jawa dan negara yang berbeda berdasarkan sekuen asam amino gen CP
No Isolat Tingkat kesamaan (%)*
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 1 Gunung Sindur ‐ 98,6 98,6 98,6 99,1 99,1 97,7 97,7 98,6 98,6 98,6 99,1 99,1 98,2 98,6 98,6 6,1 2 K. Raya ‐ 99,1 99,1 98,6 98,6 97,3 97,3 98,2 99,1 98,2 98,6 98,6 97,7 98,2 98,2 5,3 3 Lembang ‐ 99,1 98,6 98,6 97,3 97,3 98,2 99,1 97,7 98,2 98,6 98,6 97,7 98,2 5,7 4 Magelang ‐ 98,6 99,5 98,2 98,2 99,1 99,1 99,1 99,5 99,5 98,6 99,1 99,1 6,6 5 Malang ‐ 99,1 98,6 97,7 98,6 98,6 98,6 99,1 99,1 98,2 98,6 98,6 5,7 6 Surabaya ‐ 98,6 98,6 99,5 98,6 99,5 100 100 99,1 99,5 99,5 6,1 7 China P ‐ 97,3 98,2 97,3 98,2 98,6 98,6 98,2 98,2 98,2 7,0 8 China C ‐ 98,2 97,3 98,2 98,6 98,6 97,7 98,2 99,1 6,6 9 Hawai ‐ 98,2 99,1 99,5 99,5 98,6 99,1 99,1 6,6 10 India 1 ‐ 98,2 98,6 98,6 97,7 98,2 98,2 6,1 11 India 2 ‐ 99,5 99,5 98,6 99,1 99,1 6,6 12 Jepang ‐ 100 99,1 99,5 99,5 6,6 13 Korea Selatan ‐ 99,1 99,5 99,5 6,6 14 Perancis ‐ 98,6 98,6 5,7 15 Singapura ‐ 99,1 6,6 16 Taiwan ‐ 7,0 17 PVX ‐
* Tingkat homologi nukleotida dihitung menggunakan program BioEdit versi 7.0.0, (Isis Pharmaceuticals, Inc). Angka dengan cetak tebal miring menunjukkan homologi antar sesama isolat Pulau Jawa
Angka dengan cetak tebal warna merah menunjukkan homologi tertinggi pada baris yang sama Angka dengan cetak tebal warna biru menunjukkan homologi terendah pada baris yang sama
Tabel 3.12 Mutasi titik yang terjadi pada enam isolat CymMV asal Pulau Jawa yang dibandingkan dengan 10 isolat CymMV dari beberapa negara lain Asal isolat
CymMV Jumlah mutasi Urutan mutasi titik ke-
Gunung Sindur- Bogor
10 C63A*, A130G, C177T, A/T183C, T210C, T255C,
C321T, A576G, C656G, T665C Kebun
Raya-Bogor 8 C10T, C/T183A, C210T, C348T, A576G, A595C, C656G, T665G
Lembang 12 C10T, T87C, A/T183C, C210T, C255T, C312T, C381T,
G480C, T513C, G531C, C656G, T665C
Magelang 7 C10T, T87C, C/T183A, C255T, C312T, C381T, C481T
Malang 9 C/T183A, C312T, C348T, C370T, C499A, G538A,
C603G, C656G, T665G
Surabaya 13 A129G, A/C183T, G185A, C196T, C255T, C321T,
C348T, C387T, T468C, C481T, G486A, G531C, C603G
C = Cytosin, A = Adenin, T = Timin, G = Guanin
* C63A, dibaca mutasi pada basa ke-63 dari basa Cytosin menjadi Adenin, dst
Tabel 3.13 Perbedaan posisi asam amino pada gen CP enam isolat CymMV asal Pulau Jawa dengan 10 isolat CymMV dari beberapa negara lain.
Huruf dengan cetak tebal menunjukkan perbedaan dengan asam amino lainnya dalam kolom yang sama.
Pro = Proline, Ser = Serine, ala = alanine, val = valine, thr = threonine, ile = isoleusine, phe = phenilalanine, lys = Lysine, gln = Glutamine, asn = Asparagine, his=histidine, gly = glycine.
Isolat CymMV Posisi asam amino pada gen CP
4 9 14 19 59 87 91 138 167 199 219
Gunung Sindur-Bogor pro ala ala thr ala phe lys ala gln asn gly
Kebun Raya-Bogor ser ala ala thr ala phe lys ala gln his gly
Lembang ser ala ala thr ala phe lys ala gln asn gly
Magelang ser ala ala thr ala phe lys ala gln asn ala
Malang pro ala ala thr ala phe lys ala lys asn gly
Surabaya pro ala ala thr ala phe lys ala gln asn ala
China P FJ356061 pro val ala ile ala phe lys ala lys asn ala
China C DQ067883 pro ala thr thr ala phe lys ala gln asn ala
Hawai EF125180 pro ala ala thr ala ser lys ala gln asn gly
India 1 EU499362 ser ala ala thr ala phe lys ser gln asn ala
India 2 AJ698947 pro ala ala thr ala phe lys ala gln asn ala
Jepang AB197937 pro ala ala thr ala phe lys ala gln asn ala
Kor.Sel AB541562 pro ala ala thr ala phe lys ala gln asn ala
Perancis AM236028 pro thr ala thr thr phe lys ala gln asn ala
Singapura AF405719 pro ala ala thr ala phe gln ala gln asn ala
Hasil sekuen asam amino ke-16 isolat CymMV berdasarkan terjemahan nukleotida menunjukkan terdapat 11 asam amino yang tidak sama urutannya. Jika dilihat pada enam isolat CymMV asal Pulau Jawa ternyata hanya empat asam amino yang tidak sama dengan isolat lainnya. Asam amino yang tidak sama yaitu Pro4Ser (Isolat Kebun Raya-Bogor, Lembang, Magelang), Gln167Lys (Isolat Malang), Asn199His (Isolat Kebun Raya-Bogor), dan Ala219Gly (Isolat Gunung Sindur-Bogor, Kebun Raya-Bogor, Lembang, Magelang) (Tabel 3.13).
Analisis Filogenetika
Analisis filogenetika nukleotida gen CP CymMV isolat Pulau Jawa terhadap isolat dari negara lain dengan PVX sebagai outgroup menunjukkan terbentuknya
tiga kelompok/cluster. Keenam isolat CymMV asal Pulau Jawa terpisah satu
sama lain ke dalam cluster yang berbeda. CymMV isolat Gunung Sindur-Bogor
berkelompok dengan Isolat dari Jepang, Perancis dan Korea Selatan. CymMV isolat Lembang, Magelang dan Kebun Raya, berkelompok bersama dengan CymMV isolat Hawaii dan India 2, CymMV isolat Malang berkelompok dengan isolat CymMV Phalaenopsis China, sedangkan CymMV isolat Cymbidium China
membentuk sub kelompok dengan isolat Taiwan. Isolat CymMV Surabaya dan isolat Cattleya India terpisah di luar dua kelompok tersebut. Sebagai pembanding
di luar kelompok (outgroup) digunakan PVX (Gambar 3.12a)
Pohon filogenetika berdasarkan sekuen nukleotida keenam isolat Indonesia menunjukkan perbedaan kelompok dibandingkan dengan filogenetika asam amino. Kelompok pertama yaitu isolat CymMV Gunung Sindur-Bogor menyatu dengan tiga isolat asal Indonesia lainnya yaitu isolat Lembang, Magelang dan Kebun Raya serta isolat CymMV India 2. Isolat CymMV Surabaya yang awalnya terpisah berdasarkan nukleotida, membentuk kelompok dengan tujuh isolat CymMV asal negara lain (Jepang, Korea Selatan, Hawaii, India 2, Singapura, China Cymbidium, Taiwan). Isolat CymMV Malang memiliki kekerabatan dengan
isolat CymMV China Phalaenopsis, sedangkan isolat Perancis berada di luar
Gambar 3.12 Pohon filogenetika CymMV berdasarkan sekuen nukleotida (a) dan sekuen asam amino (b) gen CP isolat CymMV asal Pulau Jawa. Pohon filogenetika dibuat dengan metode neighbour-joining menggunakan
software MEGA versi 4.0 (Tamura et al. 2007). PVX digunakan sebagai
pembanding out group.
Analisis Runutan Nukleotida dan Asam Amino Gen CP ORSV
Analisis kekerabatan sekuen DNA gen CP ORSV asal Bogor dibandingkan dengan 50 sekuen gen CP ORSV pada GeneBank menunjukkan
hubungan yang dekat dengan tingkat kesamaan/homologi yang tinggi (98-99%) (data tidak ditampilkan). Sedangkan hasil alignment dengan 11 sekuen terpilih
dari GeneBank yang dianalisis dengan menggunakan program BioEdit versi
7.0.0 (Isis Pharmaceuticals, Inc) menunjukkan homologi berkisar 94,9-100%. CymMVGSindurIna AB197937Japan AM236028FranceTahiti AB541562SouthKorea CymMVKRayaIna CymMVLembangIna CymMVMagelangIna EF125180Hawai AJ698947India2 CymMVMalangIna FJ356061ChinaPal DQ067883ChinaCym AY571289Taiwan AF405719Singapore EU499362IndiaCat CymMVSurabayaIna PVU19790PVX 69 59 70 85 68 57 59 51 85 624 71 624 CymMVGSindurIna CymMVKRayaIna CymMVLembangIna EU499362IndiaCat CymMVMagelangIna CymMVSurabayaIna AB197937Japan AB541562SouthKorea EF125180Hawai AJ698947India2 AF405719Singapore DQ067883ChinaCym AY571289Taiwan CymMVMalangIna FJ356061ChinaPal AM236028FranceTahiti PVU19790PVX 68 68 58 78 99 70 (b)
(a) G.SindurJepang AB197937 Bogor AB693982 PerancisAM236028 Korea Sel.AB541562
Kebun Raya‐Bogor AB693983 Lembang‐Bandung AB693984 Magelang AB693985 Hawaii EF125180 India 2 AJ698947 Malang AB693986 China Phal FJ356061 China Cym DQ067883 Taiwan AY571289 Singapura AF405719 India1 EU499362 Surabaya AB693987 PVX PVU19790
G. Sindur Bogor AB693982 Kebun Raya‐Bogor AB693983 Lembang‐Bandung AB693984 India1 EU499362 Magelang AB693985 Surabaya AB693987 Jepang AB197937 Korea Sel.AB541562 Hawaii EF125180 India2 AJ698947 Singapura AF405719 China Cym DQ067883 Taiwan AY571289 Malang AB693986 China Phal FJ356061 PerancisAM236028 PVX PVU19790
Persentase tingkat kesamaan nukleotida ORSV tertinggi (100%) yaitu antara isolat Cipanas-Cianjur dengan isolat Gunung Sindur-Bogor. Perbandingan nukleotida isolat TAIP-Jakarta, Cipanas-Cianjur dan Gunung Sindur-Bogor dengan 11 isolat asal negara lain terlihat bahwa tiga isolat tersebut memiliki similaritas 96,8%-99,1% dengan isolat Thailand. Demikian halnya tiga isolat tersebut juga memiliki similaritas tertinggi (97,4%-99,7%) dengan isolat Taiwan, Brazil, India, Hangzhou, Korea Selatan dan Florida. Hal berbeda terlihat antara isolat Kebun Raya-Bogor yang memiliki similaritas yang lebih rendah dengan isolat Singapura, Jerman, Yunani dan Jepang, serta memiliki similaritas yang tinggi dengan isolat Thailand. Tingginya tingkat homologi antar gen CP ORSV isolat Bogor, Cipanas dan TAIP-Jakarta (94,9-100%) menunjukkan bahwa ORSV isolat Pulau Jawa merupakan strain yang sama dengan isolat ORSV yang pernah dilaporkan sebelumnya.
Homologi berdasarkan sekuen asam amino antar isolat Pulau Jawa antara 92,4-100%, sedangkan antara isolat Pulau Jawa dengan 11 sekuen pada
GeneBank diperoleh homologi berkisar 94,3–99,3%. Homologi antara isolat
Cipanas-Cianjur dan Gunung Sindur-Bogor mencapai 100% yang menunjukkan asal isolat yang sama. Perbandingan asam amino antara isolat TAIP-Jakarta, Cipanas-Cianjur dan Gunung Sindur-Bogor dengan 11 isolat asal negara lain terlihat bahwa ketiga isolat tersebut memiliki similaritas 94,9%-98,7% dengan isolat Singapura, Jerman dan Jepang. Ketiga isolat tersebut memiliki similaritas yang tinggi dengan delapan isolat lainnya (95,5%-99,3%).
Perbandingan dengan Tobacco mosaic virus (TMV) dari Yunnan
menunjukkan homologi nukleotida dan asam amino yang rendah yaitu masing-masing hanya 64,9%-66,5% dan 67,0%-70,8% (Tabel 3.14 dan 3.15). Hal ini menunjukkan bahwa ORSV berhubungan jauh dengan TMV walaupun masih dalam genus yang sama.
Tabel 3.14 Homologi nukleotida gen CP ORSV isolat Pulau Jawa dengan isolat-isolat dari beberapa negara lain
No Isolat Homologi (%) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 1 TAIP_jakarta ‐ 97,6 94,9 97,6 97,4 97,2 97,4 97,2 97,4 97,2 97,4 96,8 97,4 97,4 97,0 64,9 2 Cipanas_cnjr ‐ 97,2 100 99,7 99,5 99,7 99,5 99,7 99,5 99,7 99,1 99,7 99,7 99,3 66,3 3 G.sindur_bgr 97,2 99,7 99,5 99,7 99,5 99,7 99,5 99,7 99,1 99,7 99,7 99,3 66,3 4 K.raya_bgr ‐ 97,0 96,8 97,0 96,8 97,0 96,8 97,0 97,6 97,0 97,0 96,866,1 5 Taiwan ‐ 99,7 100 99,7 100 99,7 100 99,3 100 100 99,5 66,5 6 Singapura ‐ 99,7 99,5 99,7 99,5 99,7 99,1 99,7 99,7 99,3 66,5 7 Brazil ‐ 99,7 100 99,7 100 99,3 100 100 99,5 66,5 8 Jerman ‐ 99,7 99,5 99,7 99,1 99,7 99,7 99,3 66,3 9 India ‐ 99,7 100 99,3 100 100 99,5 66,5 10 Yunnan ‐ 99,7 99,1 99,7 99,7 99,3 66,5 11 Hangzhou ‐ 99,3 100 100 99,5 66,5 12 Thailand ‐ 99,3 99,3 98,9 66,3 13 Korea Selatan ‐ 100 99,5 66,5 14 Florida ‐ 99,5 66,5 15 Jepang ‐ 66,3 16 TMVYunnan ‐
* Tingkat homologi nukleotida dihitung menggunakan program BioEdit versi 7.0.0, (Isis Pharmaceuticals, Inc). Angka dengan cetak tebal miring menunjukkan homologi antar sesama isolat Pulau Jawa
Angka dengan cetak tebal warna merah menunjukkan homologi tertinggi pada baris yang sama Angka dengan cetak tebal warna biru menunjukkan homologi terendah pada baris yang sama
Tabel 3.15 Homologi asam amino gen CP-ORSV isolat Bogor dengan isolat-isolat dari beberapa negara lain
No Isolat Homologi (%) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 1 TAIP_jakarta ‐ 96,2 92,4 96,2 95,5 94,9 95,5 94,9 95,5 95,5 95,5 95,5 95,5 95,5 94,967,0 2 Cipanas_cnjr ‐ 95,5 100 99,3 98,7 99,3 98,7 99,3 99,3 99,3 99,3 99,3 99,3 98,770,1 3 G.sindur_bgr 95,5 99,3 98,7 99,3 98,7 99,3 99,3 99,3 99,3 99,3 99,3 98,770,1 4 K.raya_bgr ‐ 94,9 94,3 94,9 94,3 94,9 94,9 94,9 94,9 94,9 94,9 95,568,3 5 Taiwan ‐ 99,3 100 99,3 100 100 100 100 100 100 99,3 70,8 6 Singapura ‐ 99,3 98,7 99,3 99,3 99,3 99,3 99,3 99,3 98,7 70,8 7 Brazil ‐ 99,3 100 100 100 100 100 100 99,3 70,8 8 Jerman ‐ 99,3 99,3 99,3 99,3 99,3 99,3 98,7 70,1 9 India ‐ 100 100 100 100 100 99,3 70,8 10 Yunnan ‐ 100 100 100 100 99,3 70,8 11 Hangzhou ‐ 100 100 100 99,3 70,8 12 Thailand ‐ 100 100 99,3 70,8 13 KorSel ‐ 100 99,3 70,8 14 Florida ‐ 99,3 70,8 15 Jepang ‐ 70,8 16 TMVYunnan ‐
* Tingkat homologi nukleotida dihitung menggunakan program BioEdit versi 7.0.0, (Isis Pharmaceuticals, Inc). Angka dengan cetak tebal miring menunjukkan homologi antar sesama isolat Pulau Jawa
Angka dengan cetak tebal warna merah menunjukkan homologi tertinggi pada baris yang sama Angka dengan cetak tebal warna biru menunjukkan homologi terendah pada baris yang sama
Alignment berdasarkan urutan nukleotida menunjukkan adanya mutasi
titik (point mutation) pada keempat isolat ORSV yang berbeda dengan 11 isolat
Raya-Bogor, sedangkan yang paling sedikit terjadi pada isolat Gunung Sindur-Bogor dan Cipanas-Cianjur (Tabel 3.16).
Mutasi titik yang terjadi pada keempat isolat ORSV menyebabkan perubahan asam amino pada beberapa titik. Mutasi nukleotida pada isolat TAIP- Jakarta dan Kebun Raya-Bogor tidak seluruhnya menyebabkan mutasi asam amino (Lampiran 2.1 dan 2.2). Pada isolat TAIP-Jakarta mutasi tidak bermakna di posisi nukleotida ke- 94 dan 475, Sedangkan isolat Kebun Raya-Bogor, mutasi tidak bermakna yaitu pada posisi nukleotida ke-38, 114, 198, 310, 336, 375, 377, 399 dan 420. Pada ORSV isolat Gunung Sindur Bogor dan isolat Cipanas-Cianjur ditemukan mutasi titik dari basa C ke T pada nukleotida ke-5 di N-terminal gen coat protein. Mutasi titik ini menyebabkan perubahan pada
komposisi asam amino. Asam amino yang berubah yaitu asam amino ke-2 dari
serine menjadi phenylalanine (Tabel 3.17, lampiran 2.2).
Tabel 3.16 Mutasi titik yang terjadi pada enam isolat ORSV asal Pulau Jawa yang dibandingkan dengan 10 isolat ORSV dari beberapa negara lain
Isolat Jumlah mutasi Urutan mutasi titik ke-
Gunung Sindur-Bogor 1 C5T*
Cipanas-Cianjur 1 C5T
TAIP-Jakarta 12 C5T, G33A, G34A, T40C, T41C, G44A,
G49A, G55A, C56A, G58C, C94T, T475A.
Kebun Raya-Bogor 13 C5T, C35G, A38T, A76C, A114C, C198T,
A310G, T336C, A375T, C377T, G379T, C399T, T420C
Keterangan : C = Cytosin, A = Adenin, T = Timin, G = Guanin
* C5T, dibaca mutasi pada basa ke-5 dari basa Cytosin menjadi Timin, dst
Tabel 3.17 Perbedaan asam amino pada gen CP empat isolat ORSV asal Pulau Jawa dengan 11 isolat ORSV dari beberapa negara lain.
Huruf dengan cetak tebal menunjukkan perbedaan dengan asam amino lainnya dalam kolom yang sama. Phe= phenylalanine, Ser = Serine, ala = alanine,Pro = Proline, gly= glycine, thr = threonine, leu= leusine, asn = Asparagine, his= histidine, arg = arginine.
Isolat Posisi asam amino pada gen CP
2 12 14 15 17 19 20 26 125 126 127
Gunung Sindur Bogor phe ala leu ser ala ala asp ala arg ser ala
Kebun Raya-Bogor phe gly leu ser ala ala asp his ser phe ser
Cipanas-Cianjur phe ala leu ser ala ala asp ala arg ser ala
TAIP-Jakarta phe thr pro asn thr asn his ala arg ser ala
Konsensus 11 Isolat luar negeri
Analisis Filogenetika ORSV
Hasil analisis kekerabatan yang digambarkan dalam pohon filogenetika berdasarkan sekuen nukleotida dan asam amino. TMV digunakan sebagai pembanding di luar grup (Gambar 3.11). Berdasarkan analisis filogenetika, ORSV isolat-isolat Pulau Jawa sangat dekat kekerabatannya dan berada dalam satu kelompok berdasarkan homologi nukleotida dan asam amino. Secara keseluruhan antar semua isolat membentuk tiga kelompok (cluster) dalam pohon
filogenetika. Jika dibandingkan antara pohon filogenetika nukleotida dan asam amino hanya sedikit perbedaan yaitu pada isolat Kebun Raya-Bogor. Hal ini kemungkinan karena adanya mutasi nukleotida pada isolat Kebun Raya-Bogor, namun mutasi tersebut tidak bermakna karena filogenetika asam amino menempatkan isolat Kebun Raya-Bogor pada kelompok yang sama (kelompok pertama). Kelompok kedua berdasarkan asam amino yaitu ORSV isolat Brazil, China (Yunan), Taiwan, India, Korea Selatan, Jerman, Thailand, Florida dan China (Hangzou). Kelompok ketiga yaitu ORSV isolat Jepang dan Singapura lebih jauh dari isolat Indonesia. Walaupun membentuk tiga cluster, namun
kekerabatan antar isolat masih sangat dekat. Hal ini terlihat pada pohon filogenetika tersebut hanya membentuk sub grup (Gambar 3.13 a dan b).
Berdasarkan bukti ini menunjukkan bahwa ORSV menyebar dari satu negara ke negara lain secara langsung melalui bahan perbanyakan tanaman terinfeksi yang terjadi melalui aktivitas ekspor/impor. Perbedaan asal benua (Asia, Eropa dan Amerika) tidak memperlihatkan perbedaan nukleotida dan asam amino yang berarti hal ini menunjukkan virus ini relatif stabil dalam berbagai kondisi lingkungan.
Gambar 3.13 Pohon filogenetika ORSV berdasarkan nukleotida (a) dan asam amino (b) gen coat protein ORSV isolat Pulau Jawa. Analisis menggunakan software
MEGA versi 4.0 (Tamura et al. 2007). TMV digunakan sebagai
pembanding out group
Respon Tanaman Indikator terhadap Infeksi ORSV
Uji penularan ke tanaman indikator menunjukkan bahwa ORSV dapat menginfeksi hampir semua tanaman indikator yang diuji (Tabel 3.18). Gejala yang ditimbulkan pada sebagian besar tanaman indikator berupa lesio lokal, sedangkan pada tanaman Cassia occidentalis awalnya berupa lesio lokal namun
selanjutnya gejala berubah menjadi mosaik sistemik pada daun-daun yang tidak diinokulasi. Pada tanaman indikator N. tabacum v. xanthi gejala yang ditunjukkan
ORSV khas berbentuk cincin dengan lingkaran yang besar (Gambar 3.12). BRAZIL AF515606
INDIA CAD92094 GERMANY CAD22090 TAIWAN AF406775 SOUTHKOREA ACF74370 USA fLORIDA AAB53796 CHINA HANGZOU CAL38760 cHINA yUNNAN CAJ20839 SINGAPORE AAQ04716 JAPAN CAA39007 INDONESIA TAIPJAK INDONESIA CIPANAS INDONESIA G.SINDUR THAILAND AAQ88335 INDONESIA K.RAYA TMVYunnan(China) AF516913 86 64 64 50 TMVChina(Yunnan) AAM64218 Indonesia Cipanas Indonesia G.SINDUR Indonesia TAIPJak Indonesia KRaya Brazil AF515606 China(Yunnan) CAJ20839 Taiwan AF406775 India CAD92094 Korsel ACF74370 Germany CAD22090 Thailand AAQ88335 USA(Florida) AAB53796 China(Hangzou) CAL38760 Japan CAA39007 Singapore AAQ04716 83 74 70 70 70 74 83 100 100 100 100 100 100 (b) TMV Yunnan AF516913 Cipanas_Cianjur AB693991
G. Sindur Bogor AB693988
TAIP Jakarta AB693990
Kebun Raya‐Bogor AB693989
Brazil AF515606
Yunnan AM055643
Taiwan AF406775
India AF406775
Korea Sel. EU683879
Jerman AJ429093 Thailand AY376394 Florida U89894 Hangzhou AM398154 Jepang X55295 Singapura AF455273
(a) BrazilIndia AF406775AF515606
Jerman AJ429093
Taiwan AF406775
Korea Sel. EU683879
Florida U89894
Hangzhou AM398154
Yunnan AM055643
Singapura AF455273
Jepang X55295
TAIP JakartaAB693990
Cipanas_Cianjur AB693991
G. Sindur Bogor AB693988
Thailand AY376394
Kebun Raya‐Bogor AB693989
Sedangkan pada tanaman N. benthamiana gejala yang muncul berupa mosaik
dan terlihat lingkaran berbentuk cincin sangat kecil. Pengamatan visual pada tanaman vanili menunjukkan gejala mosaik dan hasil ELISA positif terinfeksi ORSV (Gambar 3.14 I).
Gambar 3.14 Gejala penularan ORSV pada tanaman indikator: (A) Datura stramonium;
(B) N. benthamiana; (C) N. tabacum; (D) N. tabacum v. xanthi;
(E) C. amaranticolor; (F) C. quinoa; (G) G. globos; (H) C. ocidentalis;
(I) Vanili.
Tabel 3.18 Hasil uji penularan & NAE ORSV pada beberapa tanaman indikator
Tanaman Indikator Kejadian penyakit Masa inkubasi (hari) Gejala NAE*
Solanaceae
D. stramonium 10/10 6 – 7 lesio nekrosis (l) 0,715
N. tabacum 10/10 6 – 7 lesio nekrosis (l) 0,758
N.benthamiana 10/10 5 – 6 mosaik cincin (s) 1,080
N.tabacum v.xanthi 10/10 5 – 7 bercak cincin (l) 0,655
Chenopodiaceae
C. amaranticolor 10/10 6 – 7 lesio nekrosis (l) 0,709
C. Quinoa 10/10 3 – 4 lesio nekrosis (l) 0,811
G. globosa 6/10 6 – 8 lesio nekrosis 0,396
Leguminoseae
Cassia ocidentalis 8/10 5 Lesio nekrosis (l),
mosaik (s) 0,378
Orchidaceae
V. planifolia 8/10 td mosaik (s) 1,190
Keterangan : NAE = Nilai Absorban ELISA, > 1,5 kali NAE kontrol negatif (0,206); td=masa inkubasi tidak dapat ditentukan l = lokal, s = sistemik
A B C
D FE
I H