LAPORAN AKHIR
LAPORAN AKHIR
PRAKTIKUM LABORATORIUM LINGKUNGAN
PRAKTIKUM LABORATORIUM LINGKUNGAN
PENETAPAN KADAR C- ORGANIK
PENETAPAN KADAR C- ORGANIK
OLEH: OLEH: NAMA
NAMA : : DESI DESI RATNA RATNA KOMALAKOMALA NO.BP
NO.BP : : 09109410140910941014 HARI/TGL PRAK
HARI/TGL PRAKTIKUM TIKUM : RABU/1 JUNI : RABU/1 JUNI 20112011 KELOMPOK
KELOMPOK : : I I (SATU)(SATU) REKAN
REKAN KERJA KERJA : : 1. 1. JULIANTO JULIANTO (0910941004)(0910941004) 2.
2. ALDILLA ALDILLA AFIANI AFIANI ALDA ALDA (0910942019)(0910942019) 3.
3. RAHMI RAHMI (0910942022)(0910942022) 4.
4. WILDA WILDA UTAMI UTAMI NURHUDA NURHUDA (0910942032)(0910942032) 5.
5. ADRIAN ADRIAN ERMANDA ERMANDA (0910942041)(0910942041) 6.
6. RAHMI RAHMI PRATIWI PRATIWI (0910942045)(0910942045)
ASISTEN: ASISTEN: INDRIYANI ZULFA INDRIYANI ZULFA AJENG YANAROSANTI AJENG YANAROSANTI
LABORATORIUM BUANGAN PADAT
LABORATORIUM BUANGAN PADAT
JURUSAN TEKNIK LINGKUNGAN
JURUSAN TEKNIK LINGKUNGAN
FAKULTAS TEKNIK
FAKULTAS TEKNIK
UNIVERSITAS ANDALAS
UNIVERSITAS ANDALAS
PADANG
PADANG
2011
2011
BAB I
PENDAHULUAN
1.1 Tujuan Praktikum
Adapun tujuan dilakukannya praktikum ini adalah untuk menentukan kadar C organik dari suatu sampel sampah.
1.2 Metoda Percobaan
Metoda yang digunakan dalam praktikum ini adalah metoda spektrofotometri.
1.3 Prinsip Percobaan
Karbon sebagai senyawa organik akan mereduksi Cr 6+ yang berwarna jingga menjadi Cr 3+ yang berwarna hijau dalam suasana asam. Intensitas warna hijau yang terbentuk setara dengan kadar karbon dan dapat diukur dengan spektrofotometer pada panjang gelombang 561 nm.
BAB II
TINJAUAN PUSTAKA
Kandungan bahan organik pada masing-masing horizon merupakan petunjuk besarnya akumulasi bahan organik dalam keadaan lingkungan yang berbeda. Komponen bahan organik yang penting adalah C dan N. Kandungan bahan organik ditentukan secara tidak langsung yaitu dengan mengalikan kadar C dengan suatu faktor yang umumnya sebagai berikut: kandungan bahan organik = C x 1,724. Bila jumlah C organik dalam tanah dapat diketahui maka kandungan bahan organik tanah juga dapat dihitung. Kandungan bahan organik merupakan
salah satu indicator tingkat kesuburan tanah (Fandicka, 2011).
Bahan organik adalah bahan dari tanah yang merupakan suatu sistem kompleks dan dinamis yang bersumber dari sisa tanaman atau binatang yang terdapat dalam tanah yang terus menerus mengalami perubahan bentuk karena dipengaruhi faktor biologi, kimia dan fisika. Menurut Stevenson (1994), bahan organik tanah adalah semua senyawa organik yang terdapat dalam tanah, termasuk serasah, fraksi bahan organik ringan, biomassa mikroorganisme, bahan organik terlarut di dalam
air, dan bahan organik yang stabil atau humus (Anonim A, 2010). Manfaat bahan organik (Fandicka, 2011):
1. Menambah keasaman / kebasaan tanah; 2. Mempengaruhi warna tanah;
3. Mempengaruhi cirri fisik tanah (mempengaruhi tekstur dan struktur); 4. Menambah kemampuan tanah untuk mengikat / menahan unsur hara; 5. Sumber unsur hara N, P, S, unsur mikro dan lain-lain.
Pengaruh bahan organik tanah terhadap sifat tanah (Fandicka, 2011): 1. Menurunkan plastisitas;
2. Memperbaiki struktur tanah sehingga menjadi lebih remah;
3. Meningkatkan daya menahan air sehingga drainase tidak berlebihan, kelembapan dan temperatur tanah menjadi stabil;
5. Terhadap kimia tanah bahan organik sebagai sumber nutrisi tanah/sumber unsur hara dan terjadi kapasitas pertukaran kation yang tinggi;
6. Terhadap biologi tanah sebagai suplai energi untuk bahan organisme tanah.
C organik penting untuk mikroorganisme tidak hanya sebagai unsur hara, tetapi juga sebagai pengkondisi sifat fisik tanah yang mempengaruhi karakteristik
agregat dan air tanah. Seringkali ada hubungan langsung antara persentase C organik total dan karbon dari biomassa mikroba yang ditemukan dalam tanah pada zona iklim yang sama. C organik juga berhubungan dengan aktivitas enzim tanah. Di perkebunan teh Gambung, C organik tanah juga digunakan untuk menentukan dosis asam-asam organik dan apabila ditambahkan ke dalam tanah akan meningkatkan kandungan senyawa organik dalam tanah yang dicirikan dengan meningkatnya kadar C organik tanah (Darliana, 2009).
Tanaman mengambil unsur karbon berupa CO2 dari udara bebas (atmosfer).
Kegiatan ini dilakukan oleh organ tanaman yang memiliki klorofil, umunya bagian tanaman yang berwarna hijau dan terdapat di atas tanah. Klorofil mampu manyerap energi cahaya (terutama sinar matahari) dan mengubahnya menjadi energi kimia. Energi tersebut digunakan untuk menghasilkan CO2 menjadi
senyawa organik termasuk karbohidrat (Fauzi, 2008).
Kadar CO2 dalam atmosfer relatif stabil, yakni 0,03% volume atau 0,57 mg/l
udara. Tanpa adanya CO2 di udara, maka kehidupan tanaman akan terhenti. Kalau
kehidupan tanaman terhenti, maka kehidupan makhluk hidup lain termasuk manusia dan hewan mungkin juga terhenti (Fauzi, 2008).
Menurut Konova (1996), sumber utama CO2 di alam berasal dari dekomposisi
bahan organik berupa sisa tanaman ataupun hewan dan dari respirasi invertebrata, bakteri serta fungi. Keperluan seluruh tanaman yang hidup diperkirakan sekitar 80 x 109 ton karbon pertahun. Dengan persediaan CO2 dalam udara sebesar 0,03%
volume, maka CO2 tersebut akan habis diserap tanaman dalam waktu beberapa
dekade saja. Berkat adanya daur yang menghasilkan CO2 maka kadar gas tersebut
Di udara terbuka terdapat 0,03% CO2, sedangkan di tempat yang banyak
tanamannya terdapat CO2 yang lebih besar dari 0,03%. Landegardh (1924)
menyatakan bahwa (Mulyani, 1999):
1. Pada permukaan tanah terdapat sekitar 0,053-0,28%; 2. Di atas daun terdapat sekitar 0,04-0,067%;
3. Satu meter di atas permukaan tanah terdapat sekitar 0,07%.
Pembuatan kompos (composting ) dapat dijadikan jalan keluar dalam mengelola limbah. Kompos sangat berguna dalam memanfaatkan sampah organik (berasal dari benda hidup) menjadi material yang dapat menyuburkan tanah (pupuk kompos). Prinsip pembuatan kompos merupakan pencampuran bahan organik dengan mikroorganisme sebagai aktivator. Mikroorganisme tersebut dapat diperoleh dari berbagai sumber. Mikroorganisme tersebut berfungsi dalam menjaga keseimbangan karbon (C) dan nitrogen (N) yang merupakan faktor penentu keberhasilan pembuatan kompos (Anonim B, 2007).
Pemberian kompos dapat memperbaiki struktur tanah. Pada tanah pasiran, pemberian kompos dapat meningkatkan daya ikat partikel tanah sehingga strukturnya menjadi lemah. Kompos dapat meningkatkan kapasitas menahan air, aktivitas mikroorganisme di dalam tanah dan kesediaan unsur hara tanah. Tetapi penggunaan kompos yang mutunya rendah dapat mengakibatkan kerusakan tanaman C/N yang terlalu tinggi atau karena ammonia yang dihasilkannya. Jika C/N kompos yang diberikan ke dalam tanah terlalu tinggi mengakibatkan tanaman kekeurangan nitrogen (ISW, 2010).
Faktor-faktor yang mempengaruhi proses pengomposan salah satunya adalah rasio C/N. Rasio C/N adalah salah satu parameter penting untuk mengetahui kualitas kompos. Rasio ini digunakan untuk mengetahui apakah kompos sudah cukup ‘matang’ atau belum. Rasio C/N ini juga diat ur di dalam SNI ataupun KepMenTan tentang kualitas kompos. Di dalam SNI rasio C/N kompos yang diijinkan adalah 10 – 20, sedangkan di dalam KepMenTan rasio C/N kompos yang diijinkan berkisar antara 20. Rasio C/N yang efektif untuk proses pengomposan berkisar antara 30: 1 hingga 40:1. Mikroba memecah senyawa C sebagai sumber energi dan menggunakan N untuk sintesis protein. Pada rasio C/N
di antara 30 s/d 40 mikroba mendapatkan cukup C untuk energi dan N untuk sintesis protein. Apabila rasio C/N terlalu tinggi, mikroba akan kekurangan N untuk sintesis protein sehingga dekomposisi berjalan lambat (Anonim C, 2009).
BAB III
PROSEDUR PERCOBAAN
3.1 Alat dan Bahan 3.1.1 Alat 1. Neraca analitik; 2. Oven; 3. Desikator; 4. Labu ukur 100 ml; 5. Gelas ukur 10 ml; 6. Pipet takar 5 ml; 7. Bola hisap; 8. Spatula; 9. Cawan penguap; 10. Lumpang dan alu; 11. Kuvet spektro; 12. Spektrofotometer. 3.1.2 Bahan 1. H2SO4 pekat 2. Kalium Dikromat 1 N; 3. Larutan standar 5000 ppm C. 3.2 Cara Kerja
3.2.1 Menghitung Kadar Air
1. Sampel sampah digerus hingga halus;
2. Cawan kosong dipanaskan pada oven di suhu 105 oC selama 1 jam, setelah itu masukkan dalam desikator selama 15 menit, ditimbang dengan neraca analitik;
3. Masukkan sampel yang sudah digerus tadi ke dalam cawan, lalu ditimbang;
4. Cawan yang berisi sampel tersebut dipanaskan di dalam oven pada suhu 105 oC selama 1 jam, setelah itu masukkan ke dalam desikator selama 15 menit, lalu ditimbang.
3.2.1 Menghitung Kadar C-Organik
1. Ditimbang 1000 mg sampel sampah, masukkan ke dalam labu ukur 100 ml;
2. Ditambahkan 5 ml Kalium Dikromat 1 N, lalu dikocok;
3. Ditambahkan 7,5 ml H2SO4 pekat, dikocok lalu diamkan selama 30 menit.
Lalu diencerkan dengan aquades, dibiarkan dingin dan diimpitkan;
4. Kesokkan harinya diukur absorbansi larutan jernih menggunakan spektrofotometer pada panjang gelombang 561 nm;
5. Sebagai pembanding, dibuat larutan standar dengan konsentrasi 0, 100, 200, 300, dan 500 ppm dengan cara mengencerkan larutan induk 5000 ppm di dalam labu ukur 100 ml;
6. Lakukan hal yang sama pada blangko.
3.3. Perhitungan 3.3.1 Kadar Air (%) % Kadar Air = 100% (a) kosong cawan berat (b) isi cawan berat (x) C 105 isi cawan berat (b) isi cawan berat o 3.3.2 Kadar C-Organik (%)
% Kadar C-Organik = ppm kurva x 0,1 x fk Dimana:
Ppm kurva = kadar contoh yang didapat dari kurva hubungan antara kadar deret standar dengan pembacaan setelah dikoreksi blanko 100 = konversi ke %
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Tabel 4.1 Berat Cawan
Praktikum Berat (gr)
Cawan kosong 55,489
Cawan + sampel sebelum dipanaskan 63,388 Cawan + sampel setelah dipanaskan 61,545
Tabel 4.2 Larutan Standar
No Konsentrasi (ppm) Absorban 1 0 0 2 100 0,200 3 200 0,360 4 300 0,557 500 0,582
Tabel 4.3 Larutan Sampel
Konsentrasi Absorban
x 0,170
4.1.1 Pembuatan larutan standar a. Larutan standar konsentrasi 0 ppm
V1
M1 = V2
M2V1
5000 ppm = 100 ml
0 ppmV1 = 0 ml (blangko)
b. Larutan standar konsentrasi 100 ppm V1
M1 = V2
M2V1
5000 ppm = 100 ml
100 ppmV1 = 2 ml
c. Larutan standar konsentrasi 200 ppm V1
M1 = V2
M2V1 = 4 ml
d. Larutan standar konsentrasi 300 ppm V1
M1 = V2
M2V1
5000 ppm = 100 ml
300 ppmV1 = 6 ml
e. Larutan standar konsentrasi 500 ppm V1
M1 = V2
M2V1
5000 ppm = 100 ml
500 ppmV1 = 10 ml
4.1.2 Pembuatan kurva larutan standar
No xi yi xi.yi xi2 1. 0 0 0 0 2. 100 0,200 20 10000 3. 200 0,360 72 40000 4. 300 0,557 167,1 90000 5. 500 0,582 291 250000
∑ xi = 1100 ∑ yi= 1,699 ∑ xi.yi = 550,1 ∑ xi2= 390000
Rumus Regresi Linear Kurva y = a + bx Keterangan: y = Nilai absorban x = Konsentrasi larutan (ppm) a =
Σy
i
Σx
i 2 −
Σx
i
Σx
iy
i
n
Σx
i2−
Σxi
2 b =(
nΣxiyi) −
Σxi
Σy
i
n
Σx
i2−
Σxi
2Masukkan nilai x dan y ke dalam persamaan agar didapat nilai a dan b:
a =
1,699
390000 −
1100
550,1
5
390000 −
1100
2b =
5 ( 550,1 −
1100
1,699
5
390000 −
1100
2b = 0,0012
Jadi, persamaan regresi linear kurvanya adalah: y = 0,0777 + 0,0012x
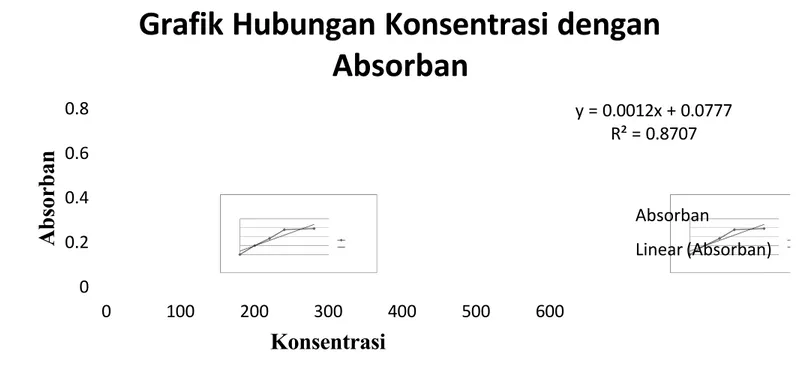
Berikut grafik hubungan konsentrasi terhadap absorban yang telah dilakukan:
Dari perhitungan rumus regresi linear dan kurva kalibrasi yang telah dibuat, didapatkan persamaan y = 0,0777 + 0,0012x, maka dapat dihitung konsentrasi untuk sampel dengan absorbannya = 0,170, yaitu:
y = 0,0777 + 0,0012x 0,170 = 0,0777 + 0,0012x 0,0012x = 0,170-0,0777 x = 0,0923/0,0012 x = 76,9 x 10 x = 769 ppm % Kadar air = 100% (a) kosong cawan Berat -(b) awal isi cawan Berat (c) akhir isi cawan Berat (b) awal isi cawan Berat = 100% gr 55,489 -gr 65,388 gr 61,545 gr 65,388 y = 0.0012x + 0.0777 R² = 0.8707 0 0.2 0.4 0.6 0.8 0 100 200 300 400 500 600 A b s o r b a n Konsentrasi
Grafik Hubungan Konsentrasi dengan
Absorban
Absorban
= 38,8 % Faktor koreksi = air Kadar % 100 100
= 38,8 -100 100 = 1,63Kadar C-Organik (%) = ppm kurva x 0,01 x fk = 769 ppm x 0,01 x 1,63 = 12,53%
4.2 Pembahasan
Pada praktikum kali ini praktikan bersama rekan kerja melakukan praktikum mengenai penentuan kadar C organik dari sampel domestik dengan komposisi sampah yaitu sampah organik berupa sisa makanan (risoles). Sampel ini diambil dari salah satu rumah praktikan yaitu di Pemondokan Cemara.
Setelah melakukan praktikum selama 2 hari didapatkan hasil perhitungan konsentrasi dari C organik pada sampel sebesar 76,9 ppm. Karena pada sampel dilakukan pengenceran sebanyak 10 kali, maka nilai konsentrasi tersebut dikalikan 10 sehingga konsentrasinya menjadi 769 ppm. Pengenceran pada sampel dilakukan karena saat pengukuran dengan spektrofotometer nilai absorban sampel tidak terbaca secara pasti (error ). Setelah pengenceran diperoleh nilai absorbansinya sebesar 0,170. Berdasarkan tabel larutan standar nilai absorbansi sampel terletak pada konsentrasi 0 dan 100 ppm.
Setelah nilai konsentrasi (ppm kurva) dan faktor koreksi diketahui, maka diperoleh nilai kadar C organik pada sampel sebesar 12,53%. Berdasarkan SNI-19-7030-2004 mengenai Spesifikasi Kompos dari Sampah Organik Domestik, persentase kadar C organik standar kualitas kompos yang diperbolehkan adalah
antara 9,8-32%. Kemudian berdasarkan PerMenTan nomor 28 tahun 2009 tentang Pupuk Organik, Pupuk Hayati dan Pembenah Tanah ditetapkan bahwa persentase kadar C organik untuk pupuk organik adalah > 12 %. Dari kedua peraturan tersebut dapat dikatakan bahwa kadar C organik pada sampel yang diuji masih berada di dalam range yang masih diperbolehkan untuk pengomposan.
Dalam tinjauan pustaka dijelaskan bahwa pengukuran kadar C organik bertujuan untuk mencari rasio C/N dalam pengomposan. Namun karena dalam praktikum sampel hanya digunakan untuk mencari kadar C organik tanpa mencari kadar N, maka nilai rasio C/N tidak dapat ditentukan, sehingga tidak dapat diketahui kualitas sampel untuk menghasilkan kompos yang baik.
BAB V
PENUTUP
5.1 Kesimpulan
Berdasarkan hasil dan pembahasan dari bab sebelumnya, dapat praktikan simpulkan sebagai berikut:
1. Persentase kadar C organik pada sampel uji adalah 12,53%. Berdasarkan SNI 19-7030-2004 dan PerMenTan nomor 28 tahun 2009, nilai kadar C organik pada sampel uji masih berada di dalam range yang masih diperbolehkan untuk pengomposan;
2. Dalam praktikum, praktikan hanya menghitung nilai kadar C organik saja tanpa menghitung nilai N pada sampel, sehingga nilai rasio C/N untuk pengomposan tidak dapat diketahui.
5.2 Saran
Adapun saran yang dapat praktikan berikan setelah melakukan praktikum C-organik adalah:
1. Memahami objek praktikumnya pada saat praktikum; 2. Teliti dalam melakukan praktikum;
3. Mempersiapkan segala sesuatunya yang berhubungan dengan praktikum sebelum praktikum dimulai;
4. Berhati – hatilah dalam menggunakan alat – alat praktikum;
5. Bersihkan semua alat dengan aquades, agar tidak timbul reaksi-reaksi yang tidak diinginkan;
6. Sebaiknya alat-alat yang akan digunakan dicek terlebih dahulu apakah masih dalam kondisi yang baik untuk digunakan.
DAFTAR PUSTAKA
Afandi, R. 2002. Ilmu Kesuburan Tanah. Yogyakarta: Kanisus
Anonim A. 2010. Sampah Kota yang Mengandung Karbon Organik . http://damandiri.or.id. Tanggal akses: 31 Mei 2011
Anonim B. 2007. Pemanfaatan Sampah Organik Sebagai Bahan Dasar Kompos . http://journal-iptek.blogspot.com/2007/04/pemanfaatan-sampah-organik-sebagai.html. Tanggal akses: 31 Mei 2011
Anonim C. 2009. C/N Rasio. http://wetrywriter.blogspot.com/2009/07/cn-rasio.html. Tanggal akses: 31 Mei 2011
Darliana. 2009. Pengaruh Jenis Bokashi Terhadap C Organik . http://p4tkipa.org. Tanggal akses: 31 Mei 2011
Fandicka. 2011. Penetapan C Organik dan Kebutuhan Kapur Dalam Tanah .
http://fandicka.blogspot.com/2011/03/28/penetapan-c-organik-dan-kebutuhan-kapur.html. Tanngal akses: 30 Mei 2011
Fauzi, Ahmad. 2008. Analisa Kadar Unsur Hara Karbon Organik dan Nitrogen di Dalam Tanah Perkebunan Kelapa Sawit Bengkalis Riau . Tugas Akhir . USU, Medan
ISW. 2010. Pemanfaatan Kompos Sampah Pasar Untuk Budidaya Sawit Organik . http://bitra.or.id. Tanggal akses: 31 Mei 2011