PENETAPAN KADAR FORMALDEHIDA
DALAM ASAP CAIR (LIQUID SMOKE) DENGAN METODE SPEKTROFOTOMETRI VISIBEL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh: William Salim NIM : 038114127
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
Ad Maiorem Dei Gloriam
Hadapi Kesulitan, Terobos Hambatan, Ciptakan Nilai
Stan Shih
Chairman & CEO ACER GroupDedicated to:
Grandma Khow Sai Tian
Pappy Faisal Salim and Mommy Yuliana
KATA PENGANTAR
Puji syukur kepada Yesus Kristus, atas berkat dan perlindungan-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul “Penetapan Kadar Formaldehida dalam Asap Cair (Liquid Smoke) dengan Metode Spektrofotometri Visibel”. Skripsi ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm.) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta. Pada kesempatan ini, penulis ingin mengucapkan terima kasih kepada:
1. Rita Suhadi, M.Si., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma ( USD ) Yogyakarta.
2. Dra. M. M. Yetty Tjandrawati, M.Si. selaku dosen pembimbing yang telah memberikan motivasi dan diskusi.
3. Drs. Sulasmono, Apt. selaku dosen penguji yang telah memberikan diskusi, kritik, dan saran.
4. Dr. Sabikis, Apt. selaku dosen penguji yang telah memberikan diskusi, kritik, dan saran.
5. Segenap staf edukatif dan staf tata usaha Fakultas Farmasi USD Yogyakarta, yang telah membantu dan memberikan fasilitas selama penulis menempuh studi.
7. Si Kou, Sa Pek, Tua Pek, Tong Ku, Ji Em, Ji Kou, Soi Kou, Si Ie, Soi Ie, beserta keluarga atas dukungan dan doanya.
8. Bapak Tarsisius Suhardiyono beserta keluarga, atas tumpangannya selama 4 tahun.
9. Yosephine yang selalu menemaniku.
10.Hartono dan Adhy Gondez atas segala bantuannya.
11.Teman-teman seperjuangan dari Pontianak (Winarto, Widyono, Manto dan lainnya) dan para sahabat karib (Agustino, Edy GF, dan lainnya) atas persahabatannya.
12.Teman-teman kelas C angkatan 2003, teman-teman kelompok F angkatan 2003 dan teman-teman tim basket Farmasi USD Yogyakarta, atas persahabatan dan kekompakannya.
13.Teman-teman Tasura 52 atas persahabatan dan kebersamaannya..
14.Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah banyak membantu penulis. Dalam hal ini, penulis mohon maaf.
Penulis menyadari bahwa masih banyak kekurangan dalam penyusunan skripsi ini, penulis memohon kritik dan saran yang sifatnya membangun. Penulis memiliki harapan yang sangat besar, semoga laporan ini dapat bermanfaat bagi pembaca.
Yogyakarta, Mei 2007
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, Mei 2007 Penulis
DAFTAR ISI
Hal HALAMAN JUDUL ……… HALAMAN PERSETUJUAN PEMBIMBING ……….. HALAMAN PENGESAHAN ……….. HALAMAN PERSEMBAHAN ……….. KATA PENGANTAR ………. PERNYATAAN KEASLIAN KARYA ………...……... DAFTAR ISI ………
A. Latar Belakang Penelitian ...………... 1. Rumusan Masalah ……...…..………... 2. Keaslian Penelitian ………...………. 3. Manfaat Penelitian ………..………. B. Tujuan Penelitian ………... BAB II PENELAAHAN PUSTAKA
B. Formaldehida .……...……….
1. Sifat ………...……….
2. Produksi ………...….………...
3. Kegunaan ….……….
4. Pengaruh terhadap badan ………. C. Bahan Tambahan Makanan ………..………..
1. Pengertian bahan tambahan makanan ………... 2. Bahan pengawet kimia ………. D. Isolasi Formaldehida ……..………….………... E. Identifikasi Kualitatif Formaldehida …... 1. Uji dengan asam kromotropat ………. 2. Uji dengan Hehner-Fulton ………... 3. Uji dengan FeCl3 ………..
4. Uji dengan reagen Nash …...……… F. Uji Kuantitatif Formaldehida ...…...
1. Metode iodometri ………
2. Metode spektrofotometri …...………..
G. Spektrofotometri ………
H. Peraturan Perundang-Undangan ………. 1. Undang-Undang Republik Indonesia Nomor 23 Tahun 1992 ………. 2. Undang-Undang Republik Indonesia Nomor 7 Tahun 1996 tentang
Pangan ………. 3. Peraturan Menteri Kesehatan Republik Indonesia Nomor
472/Menkes/Per/V/1996 tentang Pengamanan Bahan Berbahaya bagi Kesehatan ... 4. Peraturan Menteri Kesehatan Republik Indonesia Nomor
1168/Menkes/Per/X/1999 ... 5. Undang-Undang Perlindungan Konsumen ... 6. Peraturan Pemerintah Republik Indonesia Nomor 28 tahun 2004
tentang Keamanan, Mutu dan Gizi Pangan ...
I. Hipotesis ……….
BAB III METODE PENELITIAN
A. Jenis dan Rancangan Penelitian ………. B. Variabel Penelitian dan Definisi Operasional ……… C. Alat Penelitian ………...……….
D. Bahan Penelitian ………
E. Jalan Penelitian ………... 1. Pembuatan reagen asam kromotropat …...……….. 2. Pembuatan larutan stock formaldehida ……… 3. Pembuatan seri larutan baku formaldehida …... 4. Optimasi metode penetapan kadar formaldehida secara
spektrofotometri visibel ... 5. Penetapan kadar formaldehida dalam sampel ...
BAB IV HASIL DAN PEMBAHASAN
A. Optimasi Metode Penetapan Kadar Formaldehida Secara Spektrofotometri Visibel ... 1. Penetapan operating time ………. 2. Penetapan panjang gelombang absorbansi maksimal (λmaks) …...
3. Penetapan kurva baku ….………. 4. Validitas metode ………... B. Penetapan Kadar Formaldehida dalam Asap Cair ...………...
1. Preparasi sampel asap cair ... 2. Isolasi formaldehida dari asap cair ... 3. Proses preparasi larutan pereaksi ... 4. Reaksi pembentukan warna formaldehida yang direaksikan dengan
pereaksi kromotropat ... 5. Penetapan kadar formaldehida ... C. Perbandingan Kadar …...………. BAB V KESIMPULAN DAN SARAN
DAFTAR TABEL
Tabel I. Data pengukuran absorbansi kurva baku ... Tabel II. Data perhitungan recovery dan kesalahan sistemik ... Tabel III. Data perhitungan kesalahan acak ... Tabel IV. Hasil pengukuran dan perhitungan kadar formaldehida secara
spektrofotometri visibel ... Tabel V. Hasil analisis dengan Paired Samples T-test ……….. Tabel VI. Data penetapan kurva baku ………. Tabel VII. Data kurva baku yang dipakai ………. Tabel VIII.Data perhitungan recovery, kesalahan sistemik, dan kesalahan
acak ………. Tabel IX. Hasil perhitungan recovery, kesalahan sistemik, dan kesalahan
acak ………. Tabel X. Kadar asap cair A (dua kali destilasi disertai penyaringan) dengan
faktor pengenceran : 100 ml / 3 ml ... Tabel XI. Kadar asap cair B (satu kali destilasi) dengan faktor pengenceran :
100 ml / 3 ml ... Tabel XII. Data yang dimasukkan dalam analisis Paired Samples T-test ……
DAFTAR GAMBAR
Gambar 1. Struktur formaldehida ... Gambar 2. Reaksi kesetimbangan formaldehida ... Gambar 3. Reaksi pembentukan paraformaldehida ... Gambar 4. Reaksi pembentukan warna dari asam kromotropat dengan
formaldehida ... Gambar 5. Rumus bangun 1,8-dihidroksinaftalena-3,6-disulfonat …... Gambar 6. Rumus bangun 1,8-dihidroksinaftalena-3,6-dinatrium sulfonat
dihidrat ... Gambar 7. Interaksi radiasi elektromagnetik dengan bahan-bahan ... Gambar 8. Diagram spektrofotometer ………... Gambar 9. Kurva hubungan antara absorbansi dan waktu ... Gambar 10. Spektrogram panjang gelombang absorbansi maksimal ... Gambar 11. Kurva hubungan antara absorbansi dan konsentrasi ... Gambar 12. Reaksi antara formaldehida dengan air dengan katalis asam ... Gambar 13. Reaksi oksidasi pereaksi kromotropat ... Gambar 14. Reaksi I antara formaldehida dengan pereaksi kromotropat
dengan katalis asam ... Gambar 15. Reaksi II antara formaldehida dengan pereaksi kromotropat
dengan katalis asam ... Gambar 16. Perbandingan hasil reaksi I dan II …...……….. Gambar 17. Spektrogram panjang gelombang absorbansi maksimal reaksi
antara formaldehida dari asap cair dengan pereaksi kromotropat. Gambar 18. Reaksi oksidasi menghasilkan senyawa para quinoidal ……….. Gambar 19. Gugus kromofor dalam struktur formaldehida dengan pereaksi
kromotropat ……….. Gambar 20. Spektrogram operating time ………. Gambar 21. Spektrogram λmaks pada konsentrasi 6,66 μg/ml ...
Gambar 22. Spektrogram λmaks pada konsentrasi 7,77 μg/ml ...
Gambar 23. Spektrogram λmaks pada konsentrasi 8,88 μg/ml ...
Gambar 24. Kurva baku replikasi I ……….. Gambar 25. Kurva baku replikasi II ……… Gambar 26. Kurva baku replikasi III ………... Gambar 27. Tampilan data untuk perhitungan recovery, kesalahan sistemik
dan kesalahan acak ………... Gambar 28. Contoh kurva absorbansi asap cair A (dua kali destilasi disertai
penyaringan) ……….. Gambar 29. Contoh kurva absorbansi asap cair A (dua kali destilasi disertai
penyaringan) dan tampilan data replikasi V dan VI ………. Gambar 30. Contoh kurva absorbansi asap cair B (satu kali destilasi) ………
DAFTAR LAMPIRAN
Lampiran 1. Pembuatan larutan stock formaldehida dan seri larutan baku formaldehida ... Lampiran 2. Penetapan operating time …... Lampiran 3. Penetapan panjang gelombang absorbansi maksimal (λmaks) …
Lampiran 4. Penetapan kurva baku ……... Lampiran 5. Data perhitungan recovery, kesalahan sistemik, dan kesalahan
acak ... Lampiran 6. Contoh cara perhitungan recovery, kesalahan sistemik dan
kesalahan acak ... Lampiran 7. Hasil perhitungan recovery, kesalahan sistemik, dan kesalahan
acak ………... Lampiran 8. Kadar asap cair A (dua kali destilasi disertai penyaringan)
dengan faktor pengenceran : 100 ml / 3 ml …...… Lampiran 9. Kadar asap cair B (satu kali destilasi) dengan faktor
pengenceran : 100 ml / 3 ml ……….. Lampiran 10. Data yang dimasukkan dalam analisis Paired Samples T-test .. Lampiran 11. Artikel yang menyatakan bahwa asap cair murah dan aman ....
INTISARI
Formalin adalah larutan 37% gas formaldehida dalam air yang digunakan untuk pengawetan mayat dan dilarang digunakan dalam makanan. Saat ini ditemukan asap cair sebagai pengawet makanan, yang dinyatakan lebih murah dan lebih aman dibandingkan formalin. Diduga terdapat kandungan formaldehida dalam asap cair. Penetapan kadar formaldehida dalam asap cair dapat dilakukan dengan spektrofotometri visibel yang sebelumnya dilakukan isolasi formaldehida dengan cara destilasi. Penelitian ini bertujuan untuk menetapkan kadar formaldehida dan membandingkan kadar formaldehida pada kedua jenis asap cair.
Penelitian ini termasuk penelitian non-eksperimental analitik. Formaldehida hasil isolasi asap cair direaksikan dengan pereaksi kromotropat selanjutnya diukur serapannya dengan spektrofotometer visibel dan kadarnya dihitung dengan menggunakan persamaan kurva baku yang diperoleh yaitu y = 0,04901 x + 0,0518. Data yang diperoleh dianalisis dengan Paired Samples T-test dengan taraf kepercayaan 95%.
Hasil penelitian menunjukkan rata-rata kadar formaldehida dalam asap cair dua kali destilasi disertai penyaringan (264,26 ± 4,75) μg/ml sedangkan untuk asap cair satu kali destilasi (317,57 ± 1,26) μg/ml. Dari analisis T-test didapatkan nilai signifikansi 0,00 < 0,05, maka dapat disimpulkan bahwa terdapat perbedaan yang bermakna antara rata-rata kadar formaldehida dalam dua jenis asap cair.
ABSTRACT
Formalin is 37% formaldehyde solution in water which used as corpse preservative and forbidden as food addition. Now, liquid smoke had been invented as food addition which claimed cheaper and more safety than formalin. It is guessed, there is formaldehyde content in liquid smoke. Formaldehyde assay in liquid smoke is carried out using visible spectrophotometric prior to formaldehyde isolation using distillation. This research’s purpose to assay formaldehyde content and compare formaldehyde content from the two kind of liquid smoke.
This research is categorized in analytical non-experimental. Formaldehyde as isolation result is reacted with chromotropic reagent then measured its reserve with visible spectrophotometer and the contents is calculated using curve equation standard which is y = 0.04901 x + 0.0518. Data then analyzed with Paired Samples T-test in confidence level 95%.
The result show that average formaldehyde content in liquid smoke distilled twice with refining is (264.26 ± 4.75) μg/ml while in liquid smoke distilled once is (317.57 ± 1.26) μg/ml. From the T-test is find out the significant value 0.00 < 0.05, so it is concluded that there is significant meaning in average formaldehyde content from the two kind of liquid smoke.
BAB I PENGANTAR
A. Latar Belakang Penelitian
Hasil pengujian Badan Pengawas Obat dan Makanan (BPOM) Republik
Indonesia yang dilaporkan pada tanggal 9 Januari 2006 cukup mencengangkan.
Pasalnya 77,78 persen sampling tahu di Jakarta mengandung formalin. Kemudian
di Yogyakarta, dari sampling yang diambil ternyata 64 persen produk mie basah
mengandung formalin. Artinya, Yogyakarta merupakan daerah yang cukup rawan
dan potensial dari peredaran mie yang mengandung formalin (Anonim, 2006 b).
Formalin merupakan salah satu dari tiga ratus empat puluh delapan bahan
berbahaya yang tercantum dalam lampiran 1 Peraturan Menteri Kesehatan
Republik Indonesia Nomor 472/Menkes/Per/V/1996 tentang Pengamanan Bahan
Berbahaya bagi Kesehatan (Anonim, 1996 a). Formalin adalah larutan 37% gas
formaldehida dalam air yang digunakan untuk pengawetan mayat. Berdasarkan
Peraturan Menteri Kesehatan Republik Indonesia Nomor
1168/Menkes/Per/X/1999, dicantumkan bahwa formalin (formaldehida) termasuk
salah satu dari 10 bahan pengawet yang dilarang penggunaannya dalam makanan
(Anonim, 1999 a).
Keracunan formaldehida dapat terjadi akibat dari konsumsi formaldehida
dengan kadar tinggi yang digunakan sebagai pengawet dalam makanan,
contohnya mie basah. Jenis makanan ini merupakan makanan yang banyak
dikonsumsi oleh masyarakat. Ketidaktahuan masyarakat akan kemungkinan
adanya formaldehida dalam makanan dapat menjadi sebab terjadinya keracunan
formaldehida. Kalau terpapar formaldehida dalam jumlah banyak, misalnya
terminum, bisa menyebabkan kematian. Dalam tubuh manusia, formaldehida
dikonversi menjadi asam formiat yang meningkatkan keasaman darah, tarikan
nafas menjadi pendek dan sering, hipotermia, koma, atau kematian (Anonim,
2006 a).
Saat ini ditemukan pengawet alami sebagai alternatif pengganti formalin
yang harganya lebih murah dan aman yaitu asap cair (liquid smoke). Untuk
pengawetan produk makanan, asap cair tidak terkenal seperti formalin. Jika
formalin bisa membuat makanan bertahan sangat lama dengan kondisi terlihat
segar serta tidak berpengaruh pada cita rasa. Sedangkan asap cair tetap memiliki
rasa dan bau seperti asap meskipun dari segi kesehatan lebih baik dibandingkan
dengan formalin. Pengembang penelitian asap cair sendiri terus berkembang
diantaranya dengan pembuatan tepung asap yang juga bisa digunakan sebagai
bahan pengawet makanan (Anonim, 2006 b).
Asap cair bisa menjadi bahan pengawet karena mengandung senyawa
fenolik rantai panjang dan aldehida yang dapat membunuh bakteri pembusuk.
Seperti yang telah dilaporkan menyatakan bahwa pirolisis tempurung kelapa
menghasilkan asap cair dengan kandungan senyawa fenol sebesar 4,13%, karbonil
11,3% dan asam-asam lemah 10,2%. Asap cair yang dipasarkan terdiri dari dua
pengolahan yaitu asap cair destilasi dua kali disertai penyaringan dan asap cair
destilasi satu kali. Harga asap cair destilasi dua kali disertai penyaringan adalah
Rp. 56.000 dalam jerigen lima liter sedangkan asap cair destilasi satu kali adalah
Rp. 36.000 dalam jerigen lima liter. Jika dibandingkan dengan harga formalin
dipertimbangkan dari segi ongkos produksi dan kadar formaldehida yang
dihasilkan.
Diduga terdapat kandungan formaldehida pada keseluruhan kandungan
karbonil dalam asap cair tersebut. Apabila terdapat kandungan formaldehida maka
pengawet asap cair tidak bisa digunakan sebagai pengawet pengganti formalin
karena bahaya penggunaan asap cair sama seperti pada penggunaan formaldehida.
Oleh karena itu, penelitian ini bertujuan untuk menetapkan kadar formaldehida
dalam asap cair dengan metode spektrofotometri visibel serta melihat perbedaan
kadar formaldehida pada kedua jenis asap cair yang dipasarkan yaitu asap cair
dengan destilasi dua kali disertai penyaringan dan asap cair dengan destilasi satu
kali.
1. Rumusan masalah
Berdasarkan latar belakang tersebut muncul permasalahan sebagai
berikut:
a. apakah terdapat formaldehida dalam asap cair?
b. berapakah kadar formaldehida dalam asap cair?
c. apakah terdapat perbedaan kadar formaldehida pada kedua jenis asap cair?
2. Keaslian penelitian
Sejauh penelusuran pustaka yang telah dilakukan, penelitian tentang
penetapan kadar formaldehida dalam asap cair dengan metode
spektrofotometri visibel belum pernah dilakukan. Adapun penelitian yang
sudah pernah dilakukan yaitu oleh Sulistianto (2001) tentang pengaruh cara
(2002) tentang isolasi dan identifikasi formalin sebagai pengawet dalam tahu
yang beredar di kota Yogyakarta.
3. Manfaat penelitian a. Manfaat teoritis
1. Penelitian ini diharapkan dapat bermanfaat sebagai sumber informasi
tentang ada tidaknya formaldehida dalam asap cair.
2. Penelitian ini diharapkan dapat bermanfaat sebagai sumber informasi
tentang berapakah kadar formaldehida dalam asap cair.
3. Penelitian ini diharapkan dapat bermanfaat sebagai sumber informasi
tentang ada tidaknya perbedaan kadar formaldehida pada kedua jenis
asap cair.
b. Manfaat metodologis
Penelitian ini diharapkan dapat bermanfaat sebagai acuan penetapan
kadar formaldehida dalam pengawet makanan alami lainnya
B. Tujuan Penelitian
1. Untuk menguji adanya formaldehida dalam asap cair.
2. Untuk menetapkan kadar formaldehida dalam asap cair dengan metode
spektrofotometri visibel.
3. Untuk membuktikan adanya perbedaan kadar formaldehida pada kedua jenis
BAB II
PENELAAHAN PUSTAKA
A. Asap Cair (Liquid Smoke)
Asap diartikan sebagai suatu suspensi partikel-partikel padat dan cair dalam medium gas (Buell dan Girard, 1992). Asap cair merupakan campuran larutan dari dispersi asap kayu dalam air yang dibuat dengan mengkondensasikan asap hasil pirolisis kayu. Cara yang paling umum digunakan untuk menghasilkan asap pada pengasapan makanan adalah dengan membakar serbuk gergaji kayu keras dalam suatu tempat yang disebut alat pembangkit asap, kemudian asap tersebut dialirkan ke rumah asap dalam kondisi sirkulasi udara dan temperatur yang terkontrol (Setiadji, 2006).
Produksi asap cair merupakan hasil pembakaran yang tidak sempurna yang melibatkan reaksi dekomposisi karena pengaruh panas, polimerisasi, dan kondensasi (Buell dan Girard, 1992). Penggunaan berbagai jenis kayu sebagai bahan bakar pengasapan telah banyak dilaporkan. Pembuatan bandeng asap di daerah Sidoarjo, menggunakan berbagai jenis kayu sebagai bahan bakar seperti kayu bakau, serbuk gergaji kayu jati, ampas tebu, dan kayu bekas kotak kemasan. Namun untuk menghasilkan asap yang baik, pada waktu pembakaran sebaiknya menggunakan jenis kayu keras seperti kayu bakau, serbuk atau serutan kayu jati dan tempurung kelapa, sehingga diperoleh ikan asap yang baik (Setiadji, 2006). Asap yang dihasilkan dari pembakaran kayu keras akan berbeda komposisinya dengan asap yang dihasilkan dari pembakaran kayu lunak. Pada umumnya kayu keras akan menghasilkan aroma yang lebih unggul, lebih kaya kandungan
aromatik dan lebih banyak mengandung senyawa asam dibandingkan kayu lunak (Buell dan Girard, 1992).
Pembuatan asap cair menurut Dr. Bambang Setiadji, M.Sc. sangat sederhana. Tempurung kelapa dipanaskan dalam tungku pirolisis berdiameter 1,5 m. Bagian atas tungku ditutup dan diberi pipa saluran untuk mengumpulkan asap. Kemudian, asap yang terkumpul dalam drum besar diberi alat pendingin dan kumparan yang menghasilkan embun. Dari kondensasi tersebut jadilah cairan asap cair. Agar cairan tidak terlalu hitam, perlu didestilasi sehingga lebih jernih (Anonim, 2006 d).
Asap cair memiliki kemampuan untuk mengawetkan bahan makanan karena adanya senyawa asam-asam lemah, fenolat dan karbonil. Seperti yang telah dilaporkan bahwa pirolisis tempurung kelapa menghasilkan asap cair dengan kandungan senyawa fenol sebesar 4,13%, karbonil 11,3% dan asam-asam lemah 10,2%. Di Amerika Serikat, pengolahan daging menggunakan asap cair yang telah mengalami pengendapan dan penyaringan untuk memisahkan senyawa “tar”. Pasar internasional untuk produk asap cair ini meliputi Amerika, Eropa, Afrika, Australia, dan Amerika Selatan. Asap cair ini telah diaplikasikan pada pengawetan daging, termasuk daging unggas, kudapan daging, ikan salmon dan kudapan lainnya. Asap cair juga digunakan untuk menambah citarasa pada saus, sup, sayuran kaleng, bumbu, dan campuran rempah-rempah (Setiadji, 2006).
Senyawa-senyawa yang terkandung dalam asap cair berasal dari hasil pirolisis selulosa dan lignin. Senyawa-senyawa hasil pirolisis selulosa meliputi: asam asetat, asam formiat, maltol, methylcyclopentenolone, ethylcyclo
Sedangkan senyawa-senyawa hasil pirolisis lignin meliputi: fenol, cresol,
guaiacol, 4-methylguaiacol, 4-ethylguaiacol, 4-propylguaiacol, pyrocatechol,
vanillin, 4-(2-propio)vanillone, 4-(1-propio)vanillone, asetovanillone, 2,4,5-tri
methylbenzaldehyde, 4-hydroxyacetophenone, eugenol, isoeugenol, syringol,
4-methylsyringol, 4-ethylsyringol, 4-propylsyringol, 4-acetosyringol,
syringaldehyde (Anonim, 2006 e).
Asap cair sudah umum digunakan untuk menggantikan pengasapan tradisional dan sudah diproduksi secara komersial. Komponen asap terutama berfungsi untuk memberi cita rasa dan warna yang diinginkan pada produk asapan, dan berperan dalam pengawetan dengan bertindak sebagai antibakteri dan antioksidan. Asap telah diketahui memiliki sifat antioksidan dan antimikroba disamping sifat-sifat lain misalnya merubah tekstur pada produk olahan (daging, ikan) dan merubah kualitas nutrisi pada produk olahan. Antioksidan dan antimikroba terutama diperoleh dari senyawa-senyawa fenol yang merupakan salah satu komponen aktif dalam asap selain keton, aldehida, asam karboksilat, alkohol, dan furan (Setiadji, 2006).
Antioksidan adalah zat yang dapat menunda atau memperlambat kecepatan oksidasi terhadap zat-zat yang dapat mengalami autooksidasi. Fenol juga memiliki sifat sebagai pembentuk cita rasa pada produk pengasapan. Senyawa golongan fenol yang terdapat pada asap merupakan hasil peruraian termal dari komponen lignin dalam kayu (Buell dan Girard, 1992).
diperhatikan warna produk yang dihasilkan, karena ada beberapa produk yang menghendaki warna coklat, sementara beberapa produk lainnya tidak menghendaki terbentuknya warna coklat. Selain memiliki segi-segi keuntungan, proses pengasapan dapat menyebabkan bahan pangan mengandung zat-zat yang bersifat karsinogen yang tidak dikehendaki, dan telah banyak dilakukan usaha untuk mengeliminasi kandungan senyawa tersebut dalam produk pengasapan (Setiadji, 2006).
Menurut Setiadji (2006) asap cair memiliki banyak manfaat dan telah digunakan pada berbagai industri, antara lain :
1. Industri pangan
Asap cair ini mempunyai kegunaan yang sangat besar sebagai pemberi rasa dan aroma yang spesifik, juga sebagai pengawet karena sifat antimikroba dan antioksidannya. Dengan tersedianya asap cair maka proses pengasapan tradisional dengan menggunakan asap secara langsung yang mengandung banyak kelemahan seperti pencemaran lingkungan, proses tidak dapat dikendalikan, kualitas yang tidak konsisten serta timbulnya bahaya kebakaran, yang semuanya tersebut dapat dihindari. Juga digunakan untuk
food processing seperti tahu, mie basah, bakso dan lain-lain.
2. Industri perkebunan
3. Industri kayu
Kayu yang diolesi dengan asap cair mempunyai ketahanan terhadap serangan rayap daripada kayu yang tanpa diolesi asap cair.
B. Formaldehida
Formaldehida awalnya disintesis oleh kimiawan Rusia Alexander Butlerov tahun 1859, tapi diidentifikasi oleh Hoffman tahun 1867 (Anonim, 2006 a). Senyawa kimia formaldehida yang merupakan nama lain metanal; oksometana; oksimetilen; metilen oksida; formiat aldehida merupakan gas yang tidak berwarna yang rumus kimianya H2CO. Berat molekul: 30,03;
terdiri dari unsur C: 39,99%; H: 6,73%; O: 53,29%. Titik didih pada kondisi normal adalah 19,5oC. Larutan formaldehida dikenal juga sebagai formalin; formol; morbicid; veracur. Formalin mengandung ± 37% gas formaldehida dalam air merupakan cairan yang tidak berwarna dan berbau tajam. Kerapatan jenis: 1,081-1,085; titik didih pada kondisi normal: 96oC; indeks bias: 1,3746; menyala pada temperatur 60oC (140oF); pH: 2,8-4,0; dapat campur dengan air, alkohol, eter dan aseton (Budavari et al., 1989).
H C H
O
Gambar 1. Struktur formaldehida
1. Sifat
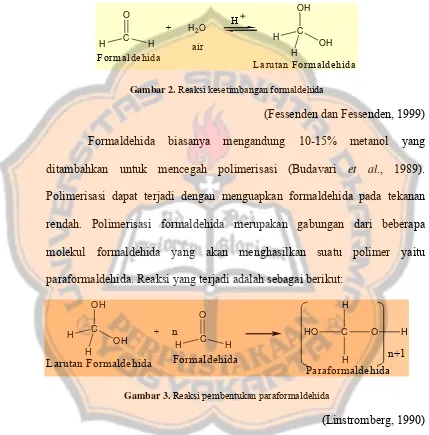
aldehida yang lain, karena gugus karbonilnya mempunyai muatan positif yang cukup besar akibat dari tidak terdapatnya gugus alkil untuk membantu menyebarkan muatan positif. Reaksi kesetimbangan yang terjadi adalah:
H C H
Gambar 2. Reaksi kesetimbangan formaldehida
(Fessenden dan Fessenden, 1999) Formaldehida biasanya mengandung 10-15% metanol yang ditambahkan untuk mencegah polimerisasi (Budavari et al., 1989). Polimerisasi dapat terjadi dengan menguapkan formaldehida pada tekanan rendah. Polimerisasi formaldehida merupakan gabungan dari beberapa molekul formaldehida yang akan menghasilkan suatu polimer yaitu paraformaldehida. Reaksi yang terjadi adalah sebagai berikut:
H C
Gambar 3. Reaksi pembentukan paraformaldehida
2. Produksi
Sumber formaldehida dapat dibagi menjadi dua, dibuat dan alamiah. Formaldehida buatan, dapat diproduksi dalam skala industri yaitu dengan cara mengoksidasi metanol, tetapi secara alamiah formaldehida terdapat juga di alam yang berasal dari hasil proses biologi atau pembakaran bahan-bahan organik, misalnya bahan bakar minyak atau rokok (Anonim, 2001).
Formaldehida bisa dihasilkan dari membakar bahan yang mengandung karbon. Dalam atmosfer bumi, formaldehida dihasilkan dari aksi cahaya matahari dan oksigen terhadap metana dan hidrokarbon lain yang ada di atmosfer. Formaldehida dalam kadar kecil juga dihasilkan sebagai metabolit kebanyakan organisme, termasuk manusia (Anonim, 2006 a).
Secara industri, formaldehida dibuat dari oksidasi katalitik metanol. Katalis yang paling sering dipakai adalah logam perak atau campuran oksida besi dan molibdenum serta vanadium. Dalam sistem oksida besi yang lebih sering dipakai (proses Formox), reaksi metanol dan oksigen terjadi pada 250°C dan menghasilkan formaldehida, berdasarkan persamaan kimia :
2 CH OH3 + O2→ 2 H2CO + 2 H O2
Katalis yang menggunakan perak biasanya dijalankan dalam hawa yang lebih panas, kira-kira 650°C. Dalam keadaan ini, akan ada dua reaksi kimia sekaligus yang menghasilkan formaldehida: satu seperti yang di atas, sedangkan satu lagi adalah reaksi dehidrogenasi :
CH OH3 → H2CO + H2
3. Kegunaan
Formaldehida efektif membunuh kuman, jamur, dan virus tetapi kerjanya lambat. Formaldehida dengan kadar 0,5% memerlukan waktu 6-12 jam untuk membunuh kuman dan 2-4 hari untuk membunuh spora. Efektivitas formaldehida akan menurun bila terdapat zat organik, misalnya protein (Anonim, 1995 a).
Kadar larutan formaldehida berbeda-beda sesuai tujuan penggunaannya. Larutan formaldehida 8% dalam air digunakan untuk sterilisasi alat-alat hemodialisis, endoskopi dan alat-alat kedokteran lainnya karena memiliki sifat korosif. Larutan formaldehida 8% dalam larutan alkohol 70% digunakan untuk sterilisasi sputum pasien tuberkolosis. Kadar formaldehida 37% (formalin) digunakan untuk mengawetkan mayat dan spesimen penelitian (Anonim, 1995 a).
Formaldehida yang digunakan pada kulit yang tidak terluka dapat memperkeras lapisan epidermis, membuat kencang, agak putih dan memberikan efek anastesi lokal. Larutan formaldehida 3% dalam air telah digunakan untuk pengobatan kutil di telapak tangan dan kaki. Biang keringat pada kaki dapat diobati dengan pengolesan 1 bagian larutan formaldehida 3% dalam 3 bagian gliserin atau 5-10 bagian alkohol namun pemakaiannya sebaiknya tidak terlalu lama untuk menghindari terjadinya iritasi (Martindale, 1996).
permanen, misalnya yang dipakai untuk kayu lapis/tripleks atau karpet (Anonim, 2006 a).
Untuk mensintesis bahan-bahan kimia, formaldehida misalnya dipakai untuk produksi alkohol polifungsional seperti pentaeritritol, yang dipakai untuk membuat bahan peledak. Turunan formaldehida yang lain adalah metilen difenil diisosianat, komponen penting dalam cat dan busa poliuretan, serta heksametilen tetramina, yang dipakai dalam resin fenol-formaldehida untuk membuat RDX (bahan peledak). Sebagai formalin, larutan senyawa kimia ini sering digunakan sebagai disinfektan, insektisida, serta bahan baku pabrik-pabrik resin plastik dan bahan peledak (Anonim, 2006 a). 4. Pengaruh terhadap badan.
Formaldehida sangat mengiritasi membran mukosa. Uap formaldehida yang terhirup dapat menyebabkan iritasi berat pada saluran pernapasan yang pada akhirnya menyebabkan bronkitis dan pneumonia. Konsentrasi di udara yang mencapai 2-3 ppm dapat menyebabkan iritasi ringan pada membran mukosa dan pada konsentrasi 10-20 ppm dalam waktu singkat dapat meyebabkan iritasi kuat. Bahaya efek buruk yang pernah dilaporkan sebagai akibat dari bebasnya uap formaldehida dari proses penyabunan sintetik. Beberapa akibat fatal yang pernah dilaporkan, contohnya 30 ml larutan formaldehida yang tertelan dapat berakibat fatal bagi orang dewasa. Konsentrasi maksimal uap formaldehida yang diijinkan di udara adalah 5 ppm (Clarke, 1971).
mual, sakit perut yang akut disertai muntah-muntah, mencret berdarah, timbulnya depresi susunan saraf, atau gangguan peredaran darah (Winarno dan Rahayu, 1994).
Tertelannya formaldehida pada dosis sangat tinggi dapat mengakibatkan ulcer (luka) yang menimbulkan rasa sangat perih pada lambung, konvulsi (kejang-kejang), haematuri (kencing darah), dan
haematomesis (muntah darah), vertigo, hilang kesadaran, bahkan gagal ginjal.
Kematian dapat terjadi akibat dari tertelannya 30 ml formaldehida. Jika pasien dapat bertahan selama 48 jam setelah tertelannya formaldehida, maka tindakan penyembuhan dapat dilakukan. Gas formaldehida dapat menyebabkan iritasi pada mata, hidung, dan saluran pernapasan bagian atas yang selanjutnya dapat mengakibatkan batuk, hilangnya nafsu makan, kejang, dan radang paru-paru (Martindale, 1996).
Dalam tubuh manusia, formaldehida dikonversi menjadi asam formiat yang meningkatkan keasaman darah, tarikan nafas menjadi pendek dan sering, hipotermia, koma, atau kematian. Formaldehida juga bisa menimbulkan terikatnya DNA oleh protein, sehingga mengganggu ekspresi genetik yang normal. Binatang percobaan yang menghisap formaldehida terus-menerus terserang kanker dalam hidung dan tenggorokannya (Anonim, 2006 a).
C. Bahan Tambahan Makanan 1. Pengertian bahan tambahan makanan
(Anonim, 2004). Sedangkan bahan tambahan makanan dalam pengertian khusus adalah senyawa kimia yang sengaja dimasukkan ke dalam makanan untuk membantu proses pembuatan, bertindak sebagai pengganti atau memperbaiki kualitas makanan yang bertujuan untuk mengawetkan makanan atau untuk membuatnya lebih menarik (deMan, 1989).
Penggunaan zat tambahan dalam makanan mempunyai fungsi yang beragam. Zat tambahan dapat membantu kestabilan pada penyimpanan makanan seperti membuat awet dan menarik dari tempat awal produksi sampai tempat pemasaran. Bahan pangan membutuhkan zat tambahan karena bahan pangan dapat rusak akibat pengaruh dari faktor lingkungan, misalnya perubahan temperatur, oksidasi, dan pencemaran mikroorganisme (Buckle et al., 1987).
Bahan tambahan mempunyai lima kegunaan, yaitu sebagai bahan yang ditambahkan untuk memelihara konsistensi produk (sebagai emulgator, stabilisator, pengembang, anti kempal), membuat makanan tetap dalam tekstur yang baik, meningkatkan atau menjaga nilai gizi (vitamin dan mineral), mempertahankan makanan tetap awet (contohnya pengawet dan antioksidan), mengontrol keasaman atau kebasaan (contohnya ragi dan bahan-bahan untuk memodifikasi keasaman atau kebasaan makanan), mempertinggi aroma, dan memperkuat warna yang dikehendaki dengan bumbu-bumbu dan aroma alami (Lu, 1995).
2. Bahan pengawet kimia
dalam bahan pangan atau ada di dalam bahan pangan sebagai akibat dari perlakuan pra-pengolahan atau penyimpanan. Untuk penyesuaian dengan penggunaannya dalam pengolahan secara baik, penggunaan bahan-bahan pengawet ini seharusnya tidak menimbulkan penipuan, menurunkan nilai gizi dari bahan pangan, dan tidak memungkinkan pertumbuhan organisme-organisme yang menimbulkan keracunan bahan pangan. National Health and
Medical Research Council menyebutkan bahwa bahan-bahan pengawet kimia
yang digunakan dalam makanan antara lain: asam benzoat, sulfit, metabisulfit, nisin, asam askorbat, propionat atau garam-garamnya dan setiap peroksida (Buckle et al., 1987).
D. Isolasi Formaldehida
Isolasi formaldehida dalam asap cair dilakukan dengan cara destilasi. Destilasi adalah proses penguapan kemudian pengembunan dari suatu cairan pada titik didihnya. Proses pemanasan akan menyebabkan senyawa kimia menguap. Uap terbentuk akan bergerak melalui condenser sehingga akan terjadi pengembunan dimana uap akan berubah menjadi bentuk cairan (Solomon, 1987).
akan menguap dan uapnya akan mengalir melalui tabung pendingin dan akan berubah menjadi cairan (Hendrickson, Cram, dan Hammond, 1970).
E. Identifikasi Kualitatif Formaldehida
Identifikasi kualitatif formaldehida bertujuan untuk membuktikan ada tidaknya kandungan formaldehida dalam suatu bahan, terutama dalam bahan makanan. Bila terdapat kandungan formaldehida, bahan tersebut akan bereaksi positif terhadap salah satu uji berikut ini:
1. Uji dengan asam kromotropat
Uji kualitatif formaldehida dalam makanan melibatkan reaksi dengan asam kromotropat. Formaldehida dengan adanya asam kromotropat dipanaskan dengan asam sulfat pekat, maka dalam beberapa menit akan terjadi pewarnaan violet atau ungu. Reaksi yang terjadi:
HO3S SO3H
Gambar 4. Reaksi pembentukan warna dari asam kromotropat dengan formaldehida (Schunack, Mayer, dan Haake, 1990). Reaksi asam kromotropat mengikuti prinsip kondensasi senyawa fenol dengan formaldehida membentuk senyawa berwarna (Dibenzo[C,H]Xanten). Pewarnaan disebabkan terbentuknya ion karbonium-oksonium yang stabil karena mesomeri (Schunack, Mayer, dan Haake, 1990).
C16H8O8S2; berat molekul: 296,26; terdiri dari unsur C: 37,5%; H: 2,52%; O:
39,96%; S: 20,02%.
OH OH
HO3S SO3H
Gambar 5. Rumus bangun 1,8-dihidroksinaftalena-3,6-disulfonat
Sediaan yang biasa digunakan merupakan garam natrium dihidrat: C10H6Na2O8S2.2H2O, berbentuk jarum atau daun dan berwarna putih
kecoklatan, sangat larut dalam air dan digunakan sebagai pereaksi (Budavari
et al., 1989).
OH OH
NaO3S SO3Na
H2O
. 2
Gambar 6. Rumus bangun 1,8-dihidroksinaftalena-3,6-dinatrium sulfonat dihidrat
2. Uji dengan Hehner-Fulton
Uji ini menggunakan pereaksi asam sulfat dan susu bebas aldehida. Ke dalam 5 ml destilat ditambahkan 6 ml asam sulfat dingin sambil didinginkan. Dari campuran ini diambil 5 ml, kemudian dimasukkan ke dalam tabung reaksi kemudian tambahkan 1 ml susu yang bebas aldehida secara perlahan-lahan sambil didinginkan, lalu tambahkan 0,5 ml larutan yang teroksidasi dan aduk. Larutan teroksidasi dibuat dengan mencampurkan asam sulfat dengan air dan brom sama banyak dalam keadaan dingin. Adanya formaldehida melalui uji ini ditandai dengan terbentuknya warna merah muda keunguan. Uji ini biasa dilakukan pada produk susu cair (Helrich, 1990). 3. Uji dengan FeCl3
Uji ini dilakukan terhadap produk susu cair dengan melibatkan pemisahan oleh asam asetat dan eter, reaksi dengan asam sulfat dan FeCl3.
Adanya formaldehida ditandai dengan terbentuknya warna merah lembahyung (Anonim, 1992 b).
4. Uji dengan reagen Nash.
Uji ini sering dilakukan terhadap produk sirup. Reagen Nash dibuat dengan cara mencampurkan 150 g Amonium Asetat (CH3COONH4), 3 ml
Asam Asetat (CH3COOH), dan 2 ml Asetil Aseton ke dalam 200-300 ml air
F. Uji Kuantitatif Formaldehida 1. Metode iodometri
Metode iodometri dilakukan dengan cara mengoksidasi formaldehida menjadi asam formiat dalam asam dan kemudian mentitrasi kembali iodium yang tidak terpakai dengan natrium tiosulfat (Schunack, Mayer, dan Haake, 1990).
2. Metode spektrofotometri
Penentuan kadar formaldehida secara spektrofotometri dapat dilakukan dengan mereaksikan formaldehida dengan asam kromotropat atau reagen Nash dan diukur serapannya dengan metode spektrofotometri pada panjang gelombang absorbansi maksimalnya (Helrich, 1990).
G. Spektrofotometri
Prinsip spektroskopi didasarkan adanya interaksi dari energi radiasi elektromagnetik dengan zat kimia. Dengan mengetahui interaksi yang terjadi, dikembangkan teknik-teknik analisis kimia yang memanfaatkan sifat-sifat dari interaksi tersebut. Dalam analisis kimia peristiwa absorbsi merupakan dasar dari cara spektroskopi karena proses absorbsi bersifat unik atau spesifik untuk setiap zat kimia (aplikasi kualitatif). Disamping itu adalah kenyataan bahwa banyaknya absorbsi berbanding lurus dengan banyaknya zat kimia (Sudarmaji, Haryono, dan Suhardi, 1989).
(1 nm = 10-7 cm). Baik radiasi UV maupun radiasi cahaya tampak berenergi lebih tinggi daripada radiasi inframerah. Absorbsi cahaya UV atau cahaya tampak mengakibatkan transisi elektronik, yaitu promosi elektron-elektron dari orbital keadaan dasar berenergi rendah ke orbital keadaan tereksitasi berenergi lebih tinggi (Fessenden dan Fessenden, 1999).
Panjang gelombang cahaya ultraviolet atau cahaya tampak bergantung pada mudahnya promosi elektron. Molekul-molekul yang memerlukan lebih banyak energi untuk promosi elektron, akan menyerap pada panjang gelombang yang lebih pendek. Molekul yang memerlukan energi lebih sedikit akan menyerap pada panjang gelombang yang lebih panjang. Senyawa akan menyerap cahaya dalam daerah tampak (yakni senyawa berwarna) mempunyai elektron yang lebih mudah dipromosikan daripada senyawa yang menyerap pada panjang gelombang UV yang lebih pendek (Fessenden dan Fessenden, 1999).
Absorbsi pada 100 nm (UV) → 750 nm (tampak) Makin mudahnya transisi elektron
Warna merupakan hasil dari suatu perangkat kompleks dari respon faali maupun psikologis terhadap panjang gelombang cahaya antara 400 sampai 750 nm, yang jatuh pada suatu jala (retina) mata. Jika semua panjang gelombang cahaya tampak mengenai jala, akan diterima (dirasakan) warna putih; jika tidak satupun yang mengenai selaput jala, akan dirasakan warna hitam atau kegelapan. Jika panjang gelombang dengan rentang (range) sempit jatuh pada selaput jala, akan diamati warna-warna individu (Fessenden dan Fessenden, 1999).
yang ekstensif menyerap cahaya dengan panjang gelombang tertentu. Apa yang tampak bukanlah warna yang diserap melainkan komplemennya yang dipantulkan. Suatu warna komplementer yang kadang-kadang disebut warna pengurangan (substraksi), merupakan hasil pengurangan beberapa panjang gelombang tampak dari dalam spektrum visual keseluruhan (Fessenden dan Fessenden, 1999).
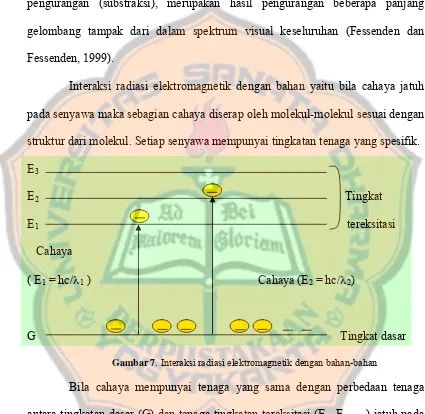
Interaksi radiasi elektromagnetik dengan bahan yaitu bila cahaya jatuh pada senyawa maka sebagian cahaya diserap oleh molekul-molekul sesuai dengan struktur dari molekul. Setiap senyawa mempunyai tingkatan tenaga yang spesifik. E3
E2 Tingkat
E1 tereksitasi
Cahaya
( E1 = hc/λ1 ) Cahaya (E2 = hc/λ2)
G Tingkat dasar
Gambar 7. Interaksi radiasi elektromagnetik dengan bahan-bahan
Bila cahaya mempunyai tenaga yang sama dengan perbedaan tenaga antara tingkatan dasar (G) dan tenaga tingkatan tereksitasi (E1, E2, …) jatuh pada
Karena perbedaan tenaga antar tingkat dasar dan tingkat tereksitasi spesifik untuk tiap-tiap bahan atau senyawa, maka frekuensi yang diserap juga tertentu. Gambar hubungan intensitas radiasi (absorbsi) sebagai fungsi panjang gelombang atau frekuensi dikenal sebagai spektrum serapan. Serapan cahaya oleh molekul dalam daerah tampak tergantung pada struktur elektronik dari molekul (Sastrohamidjojo, 2001).
Instrumen yang digunakan untuk mempelajari serapan atau emisi radiasi elektromagnetik sebagai fungsi dari panjang gelombang yaitu spektrometer atau spektrofotometer. Komponen-komponen pokok dari spektrofotometer meliputi: (1) sumber tenaga radiasi yang stabil, (2) sistem yang terdiri dari lensa-lensa, cermin, celah-celah, dan lain-lain, (3) monokromator untuk mengubah radiasi menjadi komponen-komponen panjang gelombang tunggal, (4) tempat cuplikan yang transparan, dan (5) detektor radiasi yang dihubungkan dengan sistem meter atau pencatat. Diagram sederhana dari spektrofotometer adalah sebagai berikut:
Gambar 8. Diagram spektrofotometer
(Sastrohamidjojo, 2001)
Undang-Undang Republik Indonesia Nomor 23 tanggal 17 September 1992 tentang Kesehatan yang berhubungan dengan penelitian ini adalah pada Bagian Keempat tentang Pengamanan Makanan dan Minuman, yaitu pasal 21 ayat (1), dan (3) yang menyatakan :
(1) Pengamanan makanan dan minuman diselenggarakan untuk melindungi masyarakat dari makanan dan minuman yang tidak memenuhi ketentuan mengenai standar dan atau persyaratan kesehatan.
(3) Makanan dan minuman yang tidak memenuhi ketentuan standar dan atau persyaratan kesehatan dan atau membahayakan kesehatan sebagaimana dimaksud dalam ayat (1) dilarang untuk diedarkan, ditarik dari peredaran, dan disita untuk dimusnahkan sesuai dengan ketentuan peraturan perundang-undangan yang berlaku (Anonim, 1992 a).
Pasal 80 ayat (4) butir a menyatakan : (4) Barangsiapa dengan sengaja :
a. mengedarkan makanan dan atau minuman yang tidak memenuhi standar dan atau persyaratan dan atau membahayakan kesehatan sebagaimana dimaksud dalam Pasal 21 ayat (3);
dipidana dengan pidana penjara paling lama 15 (lima belas) tahun dan pidana denda paling banyak Rp. 300.000.000,00 (tiga ratus juta rupiah) (Anonim, 1992 a).
Penjelasan pasal 21 ayat (3) menerangkan bahwa ”makanan dan minuman yang diproduksi masyarakat seperti industri rumah tangga adalah pengrajin makanan dan minuman yang masih dalam taraf pembinaan, belum dikenakan sanksi pidana sebagaimana ditentukan dalam Undang-Undang ini” (Anonim, 1992 a).
2. Undang-Undang Republik Indonesia Nomor 7 Tahun 1996 tentang Pangan Pada pasal 3 dijelaskan tujuan pengaturan, pembinaan, dan pengawasan pangan adalah:
a. tersedianya pangan yang memenuhi persyaratan keamanan, mutu dan gizi bagi kepentingan kesehatan manusia;
c. terwujudnya tingkat kecukupan pangan dengan harga yang wajar dan terjangkau sesuai kebutuhan masyarakat (Anonim, 1996 b).
3. Peraturan Menteri Kesehatan Republik Indonesia Nomor 472/Menkes/Per/V/1996 tentang Pengamanan Bahan Berbahaya bagi Kesehatan
Di dalam pasal 1 ayat (1), dicantumkan bahwa:
(1) Bahan berbahaya adalah zat, bahan kimia dan biologi, baik dalam bentuk tunggal maupun campuran yang dapat membahayakan kesehatan dan lingkungan hidup secara langsung atau tidak langsung, yang mempunyai sifat racun, karsinogenik, teratogenik, mutagenik, korosif, dan iritasi. Sedangkan dalam pasal 7 ayat (1), dicantumkan bahwa:
(1) Kasus terhadap importir bahan berbahaya berupa boraks, formalin, merkuri, metanil yellow, rodamin B, dan sianida dan garamnya, harus segera melaporkan pemasukan atau penerimaannya kepada Direktur Jenderal selambat-lambatnya 2 (dua) minggu setelah penerimaan barang sesuai dengan contoh formulir laporan pada lampiran V.
Formalin (formaldehida) merupakan salah satu dari tiga ratus empat puluh delapan bahan berbahaya yang tercantum dalam lampiran 1 peraturan tersebut (Anonim, 1996 a).
4. Peraturan Menteri Kesehatan Republik Indonesia Nomor 1168/Menkes/Per/X/1999
Peraturan Menteri Kesehatan Republik Indonesia Nomor 1168/Menkes/Per/X/1999 tentang Perubahan atas Peraturan Menteri Kesehatan Nomor 722/Menkes/Per/IX/1988 tentang Bahan Tambahan Makanan dicantumkan bahwa formalin (formaldehida) termasuk salah satu dari 10 bahan tambahan makanan yang dilarang penggunaannya dalam makanan.
(2) Menambah angka 10 baru pada lampiran II, Peraturan Menteri Kesehatan Nomor 722/Menkes/Per/IX/1988 sehingga selengkapnya menjadi sebagaimana terlampir dalam lampiran II.
Sepuluh bahan tambahan makanan yang dilarang yang tercantum dalam lampiran II adalah: asam borat dan senyawanya, asam salisilat dan garamnya, dietilpirokarbonat ( DEPC ), dulsin, kalium klorat, kloramfenikol, minyak nabati yang dibrominasi, nitrofurazon, formalin, dan kalium bromat (Anonim, 1999 b).
5. Undang-Undang Perlindungan Konsumen
Undang-Undang Republik Indonesia Nomor 8 tahun 1999 tanggal 20 April 1999 tentang Perlindungan Konsumen yang berhubungan dengan penelitian ini antara lain adalah :
a. Hak dan Kewajiban konsumen, yaitu pasal 4 huruf a, c, dan e yang menyatakan :
Hak konsumen adalah :
a. hak atas kenyamanan, keamanan, dan keselamatan dalam mengkonsumsi barang dan/atau jasa;
c. hak atas informasi yang benar, jelas dan jujur mengenai kondisi dan jaminan barang dan/atau jasa;
e. hak untuk mendapatkan advokasi, perlindungan dan upaya penyelesaian sengketa perlindungan konsumen secara patut (Anonim, 1999 c).
b. Perbuatan yang dilarang bagi pelaku usaha, yaitu pasal 8 ayat (1) huruf a dan ayat (4) yang menyatakan :
(1) Pelaku usaha dilarang memproduksi dan/atau memperdagangkan barang dan/atau jasa yang :
a. tidak memenuhi atau tidak sesuai dengan standar yang dipersyaratkan dan ketentuan peraturan perundang-undangan.
c. Tanggung jawab pelaku usaha, yaitu pasal 19 ayat (1), ayat (2), dan ayat (3) yang menyatakan :
(1) Pelaku usaha bertanggung jawab memberikan ganti rugi atas kerusakan, pencemaran, dan/atau kerugian konsumen akibat mengkonsumsi barang dan/atau jasa yang dihasilkan atau diperdagangkan.
(2) Ganti rugi sebagaimana dimaksud ayat (1) dapat berupa pengembalian uang atau penggantian barang dan/atau jasa yang sejenis atau setara nilainya, atau perawatan kesehatan dan/atau pemberian santunan yang sesuai dengan ketentuan peraturan perundang-undangan yang berlaku. (3) Pemberian ganti rugi yang dilaksanakan dalam tenggang waktu 7
(tujuh) hari setelah tanggal transaksi (Anonim, 1999 c).
d. Sanksi administratif, yaitu pasal 60 ayat (1) dan ayat (2) yang menyatakan: (1) Badan Penyelesaian Sengketa Konsumen berwenang menjatuhkan
sanksi administratif terhadap pelaku usaha yang melanggar Pasal 19 ayat (2) dan ayat (3), Pasal 20, Pasal 25, dan Pasal 26.
(2) Sanksi administratif berupa penetapan ganti rugi paling banyak Rp. 200.000.000,00 (dua ratus juta rupiah) (Anonim, 1999 c).
6. Peraturan Pemerintah Republik Indonesia Nomor 28 tahun 2004 tentang Keamanan, Mutu dan Gizi Pangan
Di dalam pasal 23 huruf c, dicantumkan bahwa : Setiap orang dilarang mengedarkan :
c. pangan yang mengandung bahan yang dilarang digunakan dalam kegiatan atau proses produksi pangan;
Formalin merupakan bahan yang dilarang digunakan dalam kegiatan atau proses produksi pangan (Anonim, 2004).
I. Hipotesis
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini tergolong dalam penelitian non-eksperimental analitik.
B. Variabel dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas
Variabel bebas yaitu variabel yang direncanakan untuk diberi pengaruhnya terhadap variabel tergantung. Variabel bebas dalam penelitian ini adalah jenis pada asap cair yaitu destilasi 2 (dua) kali disertai penyaringan dan destilasi 1 (satu) kali.
b. Variabel tergantung
Variabel tergantung yaitu titik pusat permasalahan yang merupakan kriteria penelitian ini. Variabel tergantung dalam penelitian ini adalah kadar formaldehida dalam asap cair.
c. Variabel terkendali
Variabel terkendali yaitu variabel yang diketahui atau secara teoritis mempunyai pengaruh terhadap variabel tergantung, tetapi dapat dikendalikan. Variabel terkendali dalam penelitian ini adalah:
1) Jenis asap cair. Asap cair yang digunakan adalah asap cair yang diambil dari satu toko.
2) Suhu destilasi pada saat isolasi formaldehida dalam sampel, dikendalikan dengan membatasi suhu destilasi yaitu 103oC.
3) Volume destilat, dikendalikan dengan membatasi volume destilat yaitu 50 ml.
4) Alat yang digunakan yaitu spektrofotometer visibel, dikendalikan dengan cara mengukur validitas metode yang digunakan (%perolehan kembali (recovery), kesalahan sistemik dan kesalahan acak).
d. Variabel tak terkendali
Variabel tak terkendali yaitu variabel yang diketahui atau secara teoritis mempunyai pengaruh terhadap variabel tergantung, dan tidak dapat dikendalikan. Variabel tak terkendali dalam penelitian ini adalah hasil destilat yang masih mengandung senyawa organik selain formaldehida. Hal ini dapat dilihat dari destilat yang masih berwarna kuning jernih. 2. Definisi operasional dalam penelitian ini adalah:
a. Jenis asap cair yaitu asap cair A (destilasi dua kali disertai penyaringan) dan asap cair B (destilasi satu kali).
b. Kadar formaldehida dalam asap cair dalam satuan μg/ml.
C. Alat Penelitian
D. Bahan Penelitian
Formaldehida 37%, asam sulfat 97%, asam kromotropat, asam fosfat 85% [p.a. Merck]; aquadest (Fakultas Farmasi USD Yogyakarta), asap cair.
E. Jalan Penelitian 1. Pembuatan reagen asam kromotropat
Larutkan 50 mg asam kromotropat p atau garam natriumnya dalam 100 ml asam sulfat p 75% yang dapat dibuat dengan menambahkan 75 ml asam sulfat p ke dalam 33,3 ml air dengan hati-hati (Anonim, 1995 b).
2. Pembuatan larutan stock formaldehida
Larutan stock dibuat dengan cara memipet 1,0 ml larutan baku formaldehida 37% kemudian diencerkan dengan aquadest sampai volumenya tepat 1000,0 ml sehingga didapat konsentrasi 37 mg / 100 ml.
3. Pembuatan seri larutan baku formaldehida
Seri larutan baku formaldehida dibuat dengan cara memipet 1,5; 1,8; 2,1; 2,4; dan 2,7 ml larutan stock formaldehida kemudian diencerkan dengan aquadest
sampai volumenya tepat 100,0 ml sehingga diperoleh seri konsentrasi larutan baku formaldehida 5,55; 6,66; 7,77; 8,88; dan 9,99 μg/ml.
4. Optimasi metode penetapan kadar formaldehida secara spektrofotometri visibel
a. Penetapan operating time.
kromotropat. Campuran digojog pelan-pelan kemudian dipanaskan dalam penangas air selama 15 menit dan didinginkan. Warna yang terbentuk diukur serapan(absorbansi)nya pada panjang gelombang 478 nm menggunakan spektrofotometer visibel double beam pada menit ke-0 sampai dengan menit ke-30. Operating time didapat dengan melihat rentang waktu yang menunjukkan absorbansi tetap.
b. Penetapan panjang gelombang absorbansi maksimal (λmaks).
Dari seri larutan baku formaldehida dipilih tiga seri larutan baku formaldehida dengan konsentrasi 6,66; 7,77; dan 8,88 μg/ml. Dari larutan tersebut dipipet 1,0 ml dan diperlakukan seperti pada penetapan operating time. Campuran tersebut kemudian didiamkan sesuai operating time yang diperoleh. Setelah itu warna yang terbentuk diukur absorbansinya pada panjang gelombang antara 400 nm sampai 600 nm menggunakan spektrofotometer visibel double beam. Panjang gelombang absorbansi maksimal adalah panjang gelombang dimana terjadi absorbansi terbesar. c. Penetapan kurva baku.
d. Validitas Metode.
1) Penentuan perolehan kembali (recovery)
Dari larutan stock formaldehida dibuat larutan formaldehida dengan konsentrasi 5,55; 6,66; 7,77; 8,88; dan 9,99 μg/ml dengan 3 kali replikasi. Larutan tersebut dipipet 1,0 ml dan diperlakukan seperti pada penetapan operating time. Warna yang terbentuk diukur absorbansinya pada operating time dan panjang gelombang absorbansi maksimal yang diperoleh menggunakan spektrofotometer visibel double beam. Data yang diperoleh dihitung dengan persamaan kurva baku untuk mendapatkan kadar formaldehida dalam larutan. Perolehan kembali diperoleh dengan membandingkan kadar yang diperoleh dengan kadar sebenarnya dikalikan 100%.
Rumus penentuan perolehan kembali,recovery (P):
P = .100%
teoritis Kadar
terukur Kadar
Syarat metode analisis yaitu jika metode tersebut memberikan nilai perolehan kembali (recovery) yang tinggi (90 – 107%) (Harmita, 2004).
2) Kesalahan sistemik
Kesalahan sistemik = 100% - P
Keterangan : P adalah perolehan kembali,recovery (%)
Kesalahan sistemik yang baik yaitu kurang dari 7% (Harmita, 2004). 3) Kesalahan acak
Kesalahan acak (CV) = X SD
.100%
Keterangan : simpangan baku (SD) =
1
Nilai kesalahan acak yang baik yaitu kurang dari 5% (Harmita, 2004). 5. Penetapan kadar formaldehida dalam sampel
a. Penyiapan sampel
1. Pengambilan sampel asap cair dilakukan di sebuah toko di Yogyakarta, yang belum diketahui kadar formaldehidanya.
2. Terdapat 2 jenis sampel yaitu asap cair A (dua kali destilasi disertai penyaringan) dan asap cair B (satu kali destilasi).
b. Isolasi formaldehida dalam sampel
Isolasi formaldehida dalam sampel dimulai dengan memipet 100 ml sampel. Sampel dimasukkan ke dalam labu alas bulat 250 ml dan ditambahkan 2,0 ml asam fosfat 85%. Campuran didestilasi pada suhu 103oC sampai didapatkan destilat sebanyak 50 ml. Destilat kemudian ditambah aquadest sampai 100,0 ml. Dari 100 ml destilat dipipet 3 ml kemudian diencerkan lagi sampai volumenya tepat 100,0 ml dan destilat siap diuji.
c. Uji kualitatif formaldehida dalam sampel
dalam penangas air dan didinginkan. Larutan dinyatakan mengandung formaldehida jika terbentuk warna ungu, dan intensitas warna tersebut tergantung dari jumlah formaldehida yang terkandung (Helrich, 1990). d. Uji kuantitatif formaldehida dalam sampel
Dari hasil uji kualitatif tersebut kemudian ditetapkan absorbansinya pada panjang gelombang absorbansi maksimal dan operating time yang diperoleh menggunakan spektrofotometer visibel double beam. Absorbansi-absorbansi yang diperoleh kemudian digunakan untuk menentukan kadar formaldehida dalam sampel dengan menggunakan persamaan kurva baku y = bx + a dalam satuan μg/ml (Anonim, 1986).
F. Analisis Hasil
BAB IV
HASIL DAN PEMBAHASAN
A. Optimasi Metode Penetapan Kadar Formaldehida Secara
Spektrofotometri Visibel
1. Penetapan operating time
Operating time (OT) adalah jangka waktu yang dibutuhkan oleh suatu
larutan untuk memberikan suatu serapan (absorbansi) yang stabil. Penentuan OT merupakan langkah awal yang harus ditempuh untuk penetapan kadar secara spektrofotometri visibel. Absorbansi yang stabil menunjukkan bahwa reaksi pembentukan warna antara formaldehida dengan pereaksi kromotropat sempurna sehingga absorbansi yang dibaca pada panjang gelombang absorbansi maksimal adalah absorbansi semua formaldehida yang bereaksi dengan pereaksi kromotropat. Menurut Fagnani et al (2002), panjang gelombang absorbansi maksimal untuk reaksi antara formaldehida dengan pereaksi kromotropat adalah pada panjang gelombang 478 nm. Hasil pengukuran sebagai berikut :
Kurva Absorbansi vs Waktu
Gambar 9. Kurva hubungan antara absorbansi dan waktu
Hasil pengukuran OT menunjukkan bahwa absorbansi stabil sejak awal pembacaan (menit ke-0) sampai menit terakhir (menit ke-30). Hal ini berarti pengukuran dari formaldehida yang direaksikan dengan pereaksi kromotropat dapat dilakukan pada rentang waktu tersebut.
2. Penetapan panjang gelombang absorbansi maksimal (λmaks)
Panjang gelombang absorbansi maksimal adalah panjang gelombang dari suatu larutan yang mempunyai absorbansi maksimal. Dalam penelitian ini, panjang gelombang diukur mulai dari 400 nm sampai 600 nm. Panjang gelombang 400 nm sampai 600 nm merupakan panjang gelombang pada daerah visibel dan merupakan daerah absorbansi reaksi antara formaldehida dengan pereaksi kromotropat yang menghasilkan warna visibel. Apabila diukur pada panjang gelombang di bawah 400 nm maka akan memberikan absorbansi pada daerah Ultra Violet (UV) dan senyawa hasil reaksi tidak teridentifikasi.
Kurva Absorbansi vs Panjang Gelombang
0.16
Gambar 10. Spektrogram panjang gelombang absorbansi maksimal
6,66; 7,77; dan 8,88 μg/ml diperoleh dua panjang gelombang absorbansi maksimal pada masing-masing konsentrasi yaitu :
a. Konsentrasi 6,66 μg/ml : 478 dan 573 nm b. Konsentrasi 7,77 μg/ml : 480 dan 574 nm c. Konsentrasi 8,88 μg/ml : 480 dan 573 nm
Panjang gelombang absorbansi maksimal yang dipakai adalah panjang gelombang yang pertama karena formaldehida hasil isolasi pada sampel yang bereaksi dengan pereaksi kromotropat hanya menghasilkan satu panjang gelombang absorbansi maksimal. Panjang gelombang absorbansi maksimal tiga seri konsentrasi larutan baku formaldehida adalah 478; 480; dan 480 nm. Dengan menentukan titik tengah panjang gelombang yang dihasilkan, dapat disimpulkan bahwa maksimal absorbansinya diperoleh pada panjang gelombang 479 nm. Panjang gelombang 479 nm merupakan panjang gelombang absorbansi maksimal formaldehida yang bereaksi dengan pereaksi kromotropat. Besarnya panjang gelombang ini tidak jauh berbeda dari yang tertulis dalam laporan penelitian yang dilakukan oleh Fagnani et al (2002) dengan judul Development of spectrophotometric method for
the analysis of paraformaldehyde in commercial and industrial disinfectants yaitu
3. Penetapan kurva baku
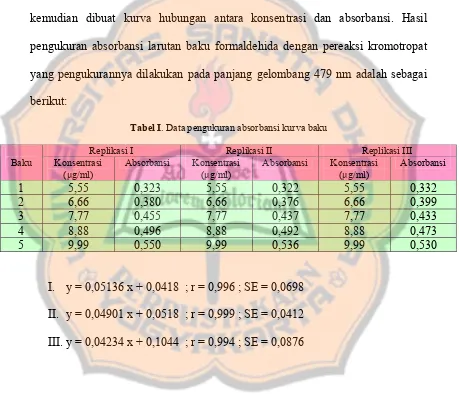
Dalam pembuatan kurva baku diperlukan satu seri larutan baku formaldehida dengan konsentrasi 5,55; 6,66; 7,77; 8,88; dan 9,99 μg/ml. Seri larutan baku formaldehida yang direaksikan dengan pereaksi kromotropat selanjutnya diukur absorbansinya pada panjang gelombang absorbansi maksimal, kemudian dibuat kurva hubungan antara konsentrasi dan absorbansi. Hasil pengukuran absorbansi larutan baku formaldehida dengan pereaksi kromotropat yang pengukurannya dilakukan pada panjang gelombang 479 nm adalah sebagai berikut:
Tabel I. Data pengukuran absorbansi kurva baku
Replikasi I Replikasi II Replikasi III
Baku Konsentrasi
(μg/ml) Absorbansi Konsentrasi (μg/ml) Absorbansi Konsentrasi (μg/ml) Absorbansi
1 5,55 0,323 5,55 0,322 5,55 0,332
2 6,66 0,380 6,66 0,376 6,66 0,399
3 7,77 0,455 7,77 0,437 7,77 0,433
4 8,88 0,496 8,88 0,492 8,88 0,473
5 9,99 0,550 9,99 0,536 9,99 0,530
Kurva Absorbansi vs Konsentrasi
0.3 0.4 0.5 0.6
5.55 6.66 7.77 8.88 9.99
Konsentrasi (μg/ml)
Gambar 11. Kurva hubungan antara absorbansi dan konsentrasi
Dari kurva hubungan antara absorbansi dan konsentrasi ini, dapat dilihat korelasi yang baik antara keduanya dengan garisnya yang linier dimana semakin bertambahnya konsentrasi akan menyebabkan absorbansinya juga meningkat sehingga persamaan garis yang didapat bisa digunakan untuk menghitung kadar formaldehida selanjutnya. Dalam penelitian ini, persamaan garis yang digunakan untuk menghitung kadar formaldehida yaitu y = 0,04901 x + 0,0518, karena nilai koefisien korelasinya (r) dan nilai Standar Error (SE) dari persamaan ini lebih baik dari dua persamaan yang lain. Nilai SE yang diperoleh menunjukkan bahwa sensitivitas dari metode yang digunakan cukup baik, karena nilai SE yang dihasilkan relatif kecil.
4. Validitas metode
kadar suatu zat dalam sampel. Persyaratan yang diharuskan bagi suatu metode analisis adalah jika metode tersebut dapat memberikan nilai recovery yang tinggi (90-107%), kesalahan sistemik kurang dari 7% dan kesalahan acak kurang dari
5%. Recovery menggambarkan akurasi dari suatu metode yang artinya metode
tersebut dapat menghasilkan nilai rata-rata yang sangat dekat dengan nilai sesungguhnya dan recovery ini merupakan tolok ukur efisiensi analisis. Kesalahan sistemik merupakan tolok ukur inakurasi penetapan kadar sedangkan kesalahan acak yang diukur dengan CV (coefficient variacy) merupakan tolok ukur inpresisi suatu analisis yang berarti dalam suatu seri pengukuran atau penetapan kadar dapat diperoleh hasil yang satu sama lain hampir sama. Dari hasil pengukuran, menunjukkan bahwa metode spektrofotometri visibel valid untuk digunakan dalam menetapkan kadar formaldehida, karena sudah memenuhi persyaratan di atas. Data pengukurannya adalah sebagai berikut:
Tabel II. Data perhitungan recovery dan kesalahan sistemik No. Kadar teoritis
(μg/ml) Kadar terukur (μg/ml) Recovery (%) sistemik (%) Kesalahan
Tabel III. Data perhitungan kesalahan acak
B. Penetapan Kadar Formaldehida dalam Asap Cair
1. Preparasi sampel asap cair
Asap cair yang digunakan sebagai sampel berasal dari satu toko, dan sebelum dipipet untuk dianalisis harus dihomogenkan terlebih dahulu agar setiap asap cair mempunyai kesempatan untuk terambil sebagai sampel karena syarat pengambilan sampel harus representatif, jika pengambilan sampel salah (walaupun metode analisisnya tepat dan teliti) maka hasilnya akan keliru. Asap cair setiap perlakuan disiapkan sebanyak lima jerigen dan masing-masing jerigen berisi lima liter. Kelima jerigen tersebut dicampur menjadi satu dalam satu wadah dan kemudian dipipet sebanyak 100,0 ml untuk dianalisis.
2. Isolasi formaldehida dari asap cair
Isolasi formaldehida dimulai dengan memipet 100,0 ml asap cair dan menambahkan 2 ml asam fosfat 85% ke dalam asap cair tersebut. Tujuan menambahkan asam fosfat 85% adalah untuk membuat formaldehida tetap stabil dalam bentuk larutan formaldehida pada saat dipanaskan sewaktu destilasi. Formaldehida memiliki titik didih 19,5oC dan pada suhu ruangan berbentuk gas. Oleh karena itu, formaldehida perlu diubah menjadi larutan formaldehida dengan katalis asam agar tetap stabil pada saat dipanaskan dengan suhu tinggi. Reaksi yang terjadi adalah sebagai berikut:
H C H
Langkah selanjutnya adalah destilasi asap cair. Destilasi merupakan pemisahkan suatu cairan dari suatu senyawa padat atau cairan yang didasari atas perbedaan titik didihnya. Alasan dilakukannya destilasi adalah terdapat banyak kandungan senyawa-senyawa selain formaldehida di dalam asap cair. Kandungan senyawa-senyawa kimia yang dapat diketahui adalah berasal dari hasil pirolisis selulosa dan lignin dari tempurung kelapa. Berikut ini adalah senyawa-senyawa kimia dalam asap cair selain formaldehida beserta titik didihnya yang berasal dari pirolisis selulosa dan lignin menurut http://www.Leffingwell.com/smoke.htm:
¾ Senyawa-senyawa hasil pirolisis selulosa meliputi: asam asetat (122,48oC), asam format (120,41oC), maltol (267,42oC), methylcyclopentenolone
(241,66oC), ethylcyclopentenolone (259,13oC), dimethylcyclopentenolone
(254,16oC), furfural (160,32oC), 5-hydroxymethylfurfural (252,84oC).
¾ Senyawa-senyawa hasil pirolisis lignin meliputi: fenol (170,21oC), cresol (190,98oC), guaiacol (211,61oC), 4-methylguaiacol (232,53oC),
4-ethylguaiacol (248,56oC), 4-propylguaiacol (265,69oC), pyrocatechol
(229,87oC), vanillin (274,48oC), 4-(2-propio)vanillone (265,69oC),
4-(1-propio)vanillone (265,69oC), asetovanillone (281,17oC), 2,4,5-tri
methylbenzaldehyde (239,54oC), 4-hydroxyacetophenone (247,06oC),
eugenol (264,44oC), isoeugenol (270,78oC), syringol (249,24oC),
4-methylsyringol (266,33oC), 4-ethylsyringol (282,51oC), 4-propylsyringol
(297,79oC), 4-acetosyringol (311,52oC), syringaldehyde (309,52oC).
103oC agar semua senyawa formaldehida dan air dapat terdestilasi dan senyawa-senyawa selain formaldehida yang teridentifikasi tidak terdestilasi karena titik didihnya di atas suhu destilasi. Pada hasil optimasi, destilasi 100 ml asap cair pada suhu 103oC akan menghasilkan destilat sebanyak 50 ml. Artinya, setelah destilat mencapai 50 ml, asap cair yang dididihkan tidak menguap lagi sehingga tidak menghasilkan destilat. Hal ini disebabkan titik didih senyawa-senyawa kimia lain dalam asap cair lebih dari 103oC.
3. Proses preparasi larutan pereaksi
Pembuatan larutan pereaksi kromotropat dilakukan dengan melarutkan garam kromotropat ke dalam asam sulfat 75%. Larutan pereaksi kromotropat berwarna kuning muda yang cerah dan harus selalu dibuat baru karena larutan tersebut tidak stabil pada penyimpanan. Hal ini disebabkan karena kromotropat memiliki gugus fenol mudah teroksidasi oleh udara bebas dan cahaya. Reaksi oksidasi yang terjadi adalah sebagai berikut:
NaO3S SO3Na
O H O H
O2
NaO3S S 3Na
O O
kromotropat kromotropat teroksidasi
O
Gambar 13. Reaksi oksidasi pereaksi kromotropat
4. Reaksi pembentukan warna formaldehida yang direaksikan dengan
pereaksi kromotropat
dengan aquadest sampai 100,0 ml, sebanyak 1 ml larutan destilat formaldehida tersebut ditambah 5 ml pereaksi kromotropat kemudian dipanaskan di atas penangas air selama 15 menit dan didinginkan. Pemanasan ini akan mempercepat oksidasi senyawa antara yang terbentuk. Oksidasi ini akan membentuk warna ungu kemerahan yang lebih jelas karena terbentuknya ikatan rangkap terkonjugasi yang lebih panjang.
Warna yang terbentuk dibaca pada spektrofotometer visibel. Besarnya intensitas warna (absorbansi) berbanding lurus dengan banyaknya formaldehida yang terkandung dalam asap cair artinya, semakin besar absorbansinya berarti semakin besar kadar formaldehida yang dikandung.
Terdapat 2 reaksi pembentukan warna antara formaldehida dengan pereaksi kromotropat, yaitu:
a. Reaksi yang pertama adalah reaksi substitusi formaldehida pada posisi orto
pereaksi kromotropat dengan katalis asam sulfat. Reaksinya adalah sebagai berikut:
Gambar 14. Reaksi I antara formaldehida dengan pereaksi kromotropat dengan katalis asam
b. Reaksi yang kedua adalah reaksi substitusi formaldehida pada posisi para
pereaksi kromotropat dengan katalis asam sulfat. Reaksinya adalah sebagai berikut:
Gambar 15. Reaksi II antara formaldehida dengan pereaksi kromotropat dengan katalis asam
(Fagnani et al., 2002) Reaksi ini menghasilkan senyawa para quinoidal yang berwarna ungu. Warna ungu ini dapat dibaca pada panjang gelombang absorbansi maksimal 575 nm.
Berdasarkan data absorbansi baku formaldehida, reaksi antara formaldehida dengan pereaksi kromotropat akan menghasilkan 2 senyawa dengan perbandingan sebagai berikut:
Reaksi substitusi posisi orto pereaksi kromotropat oleh formaldehida menghasilkan senyawa mono-cationic dibenzoxanthylium sebesar 35% sedangkan reaksi substitusi posisi para pereaksi kromotropat oleh formaldehida dengan menghasilkan senyawa para quinoidal sebesar 65% dari total formaldehida yang bereaksi. Berarti, reaksi formaldehida lebih banyak menghasilkan produk substitusi posisi para pada pereaksi kromotropat.
5. Penetapan kadar formaldehida
Penetapan kadar formaldehida dalam asap cair dengan metode spektrofotometri visibel diukur pada panjang gelombang 479 nm. Formaldehida pada hasil isolasi asap cair yang bereaksi dengan pereaksi kromotropat hanya mampu menghasilkan senyawa mono-cationic dibenzoxanthylium yang dapat dibaca pada panjang gelombang absorbansi maksimal 479 nm. Panjang gelombang absorbansi maksimal yang dihasilkan adalah:
Kurva hubungan Absorbansi vs Panjang Gelombang
0.12 0.22 0.32 0.42
400 500 600
Panjang Gelombang (nm)
A
bs
or
bans
i
Gambar 17. Spektrogram panjang gelombang absorbansi maksimal reaksi antara formaldehida