ULTRAVIOLET DAN FOURIER TRANSFORM INFRARED
TAOFIK JASA LESMANA
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2007
PEMBUATAN KOMPOSIT POLIMER-KALSIUM FOSFAT
KARBONAT: SPEKTROSKOPI SERAPAN ATOMIK,
ULTRAVIOLET DAN FOURIER TRANSFORM INFRARED
TAOFIK JASA LESMANA
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2007
ABSTRAK
TAOFIK JASA LESMANA
.
Pembuatan Polimer Kalsium Fosfat Karbonat:
Spektroskopi Serapan Atomik, Ultraviolet dan
Fourier Transform Infrared
.
Dibimbing oleh KIAGUS DAHLAN dan YESSIE WIDYA SARI.
Kalsium fosfat karbonat merupakan mineral penyusun tulang dan gigi.
Kalsium fosfat karbonat, dalam dunia medis digunakan untuk inplantasi
tulang-tulang yang rusak. Kalsium fosfat karbonat yang akan diinplankan harus memiliki
komposisi sesuai dengan komposisi tulang, yaitu mengandung matriks (30% b/b)
dan mineral (70 % b/b). Sifat komponen penyusun komposit tersebut harus
mengikuti metabolisme tubuh, sehingga memberikan syarat
biocompatible
,
biodegradable
,
non toxic
dan
bioactive
. Mineral dibuat dari NaHCO3,
Na2HPO4.2H2O dan CaCl2.2H2O, sedangkan matriks yang digunakan adalah
polyglycolide
, dibuat dari reaksi polimerisasi
sodium chloroacetate
pada suhu
191,5
0C. Telah dilakukan penelitian dalam membuat komposit polimer kalsium
fosfat karbonat melalui metode tetes vakum (1 ml), tetes non vakum (1 ml dan 2
ml) dan perbandingan massa matriks-mineral. Variasi metode dan konsentrasi
yang digunakan menghasilkan kadar fosfat, karbonat, ion Ca dan fosfor yang
berbeda-beda. Komposit yang dihasilkan dengan metode perbandingan massa
mineral-matriks mengandung kadar ion fosfat, karbonat, Ca dan fosfor yang lebih
banyak dari pada metode yang lainnya. Karakterisasi komposit polimer kalsium
fosfat karbonat dengan menggunakan spektrometer FTIR (
Fourier Transform
Infra Red
) bertujuan untuk melihat gugus fosfat dan karbonat pada komposit,
spektrometer AAS digunakan untuk mengukur kadar ion Ca dan Na, sedangkan
spektrometer UV-Vis digunakan untuk melihat kadar ion P.
Kata kunci:
polyglycolide
, kalsium fosfat karbonat,
sodium chloroacetate
, FTIR
dan AAS/UV-Vis.
PEMBUATAN KOMPOSIT POLIMER-KALSIUM FOSFAT
KARBONAT: SPEKTROSKOPI SERAPAN ATOMIK,
ULTRAVIOLET DAN FOURIER TRANSFORM INFRARED
TAOFIK JASA LESMANA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2007
Judul
: Pembuatan Komposit Polimer – Kalsium Fosfat Karbonat:
Spektroskopi Serapan Atomik, Ultraviolet dan
Fourier Transform
Infrared
Nama
: Taofik Jasa Lesmana
NRP
: G 74103009
Menyetujui,
Dr. Kiagus Dahlan
Pembimbing I
Yessie Widya Sari, M.Si
Pembimbing II
Mengetahui :
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP. 131 473 999
PRAKATA
Assalaamu’alaikum Wr. Wb.
Puji syukur hanyalah milik Allah SWT, atas segala izin, rahmat, kekuatan
dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul
”Pembuatan Komposit Polimer – Kalsium Fosfat : Spektroskopi Serapan Atomik,
Ultra Violet Dan
Fourier Transform Infrared”
. Hasil penelitian ini disusun untuk
memenuhi syarat menyelesaikan program pendidikan Sarjana Sains (S.Si) di
Departemen Fisika, Fakultas matematika dan Ilmu pengetahuan Alam. Sholawat
serta salam semoga tetap tercurah kepada Nabi Muhammad SAW beserta
keluarga, sahabat dan umatnya sampai akhir zaman.
Topik ini sangat baik dikembangkan di Indonesia dalam rangka
penyediaan biomaterial untuk meningkatkan kemudahan dalam dunia medis.
Penulis mengucapkan terima kasih kepada
1.
Alloh SWT Rabb seluruh alam
2.
Bapak Dr. Kiagus Dahlan dan Ibu Yessie Widya Sari, M.Si atas waktu yang
telah diberikan untuk membimbing, memotivasi dan memeberikan saran yang
sangat berharga.
3.
Bapak Dr. Irzaman dan Ibu Mersi Kurniati, M.Si selaku dosen penguji yang
banyak memberikan saran yang bermanfaat untuk masa depan.
4.
Ibu/Bapak, Adik, dan keluarga tercinta di rumah yang senantiasa memberikan
do’a dan semangat.
5.
Teman seperjuangan (Priyo P, Mba Arsi dan Pak Jum)
6.
X Bara 3 (Adi P, Adi Y, Kusnadi, Awit, subhi).
7.
7 Soul (Syeikh Tah, D-not, Bang Marwan, Azis, Izhal, Priyo, Alwi dan Om
Rud).
8.
Mr. A. Zaim (my FTIR operator) yang selalu mendorong dan memberi
semangat kepada penulis
9.
Teman Fisika angkatan 38, 39, 41 dan 42.
Semoga hasil penelitian ini dapat bermanfaat.
Wassalaamu’alaikum Wr. Wb
Bogor, Mei 2007
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 20 Nopember 1984 dari
pasangan Bapak Ende Sukandi dan Ibu Ida Hidayah. Penulis merupakan putra
pertama dari dua bersaudara. Penulis menempuh pendidikan di SDN II Rancakole
– Bandung (1991 – 1997), SLTPN 3 Ciparay – Bandung (1997 – 2000), SMUN I
Ciparay – Bandung (2000 – 2003) dan tahun 2003 penulis masuk Ke Departemen
Fisika Institut Pertanian Bogor melalui jalur USMI.
Selama mengikuti perkuliahan, penulis pernah aktif sebagai staff di
Departemen Instrumentasi dan Komunikasi Himpunan Mahasiswa Fisika
(HIMAFI) perioda 2004 – 2005, Kadep Departemen Kerohanian Himpunan
Mahasiswa Fisika (HIMAFI) perioda 2005 – 2006. Penulis pernah menjadi asisten
praktikum Fisika dasar pada tahun 2004 – 2007, asisten paraktikum Biofisika
tahun 2006, asisten Fisika Lanjut tahun 2006 dan asisten Eksperimen Fisika tahun
2007. Penulis juga aktif mengajar Fisika di Bimbingan Belajar mahasiswa PC
(Physics Challenge), Ampuh dan Bintang Pelajar, selain itu juga penulis aktif
dalam beberapa pelatihan seperti pelatihan pembuatan WEB dan Macromedia
Flash MX 2004 dan merakit PC.
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... vii
PENDAHULUAN
Latar Belakang ... 1
Perumusan Masalah ... 1
Tujuan ... 1
Tempat dan Waktu Penelitian ... 1
TINJAUAN PUSTAKA
Matriks Polimer Berpori ... 1
Komposit Polimer-Kalsium Fosfat Karbonat ... 2
Pengaruh Ion Karbonat dalam Kristal Apatit... 3
Identifikasi Senyawa Kalsium Fosfat dengan Spektrometer Infrared... 3
Identifikasi Senyawa kalsium Fosfat dengan Spektrometer UV-Vis... 4
Identifikasi Senyawa Kalsium Fosfat dengan AAS ... 4
BAHAN DAN METODE
Bahan dan Alat... 4
Metode Penelitian
Pembuatan Matriks Polimer... 4
Pembuatan Matriks Polimer Berpori... 4
Presipitasi Polimer Kalsium Fosfat Karbonat... 4
Karakterisasi dengan Spektrometer Infrared... 5
Karakterisasi dengan Spektrometer AAS (
Atomic Absorption
Spetrometry
) dan UV-Vis (
Ultra Violet Visible
) ... 5
HASIL DAN PEMBAHASAN
Polimerisasi
Sodium Chloroacetate
... 6
Analisis Kandungan Ca, Na dan P Menggunakan AAS dan
Spektrometer UV-Vis ... 6
Analisis gugus CO3
2-dan PO4
3-menggunakan spektrometer FTIR .... 9
SIMPULAN ... 16
DAFTAR PUSTAKA ... 16
DAFTAR TABEL
Halaman
1 Polimerisasi
halogenoacetate
... 2
2 Suhu (
oC) dan entalpi reaksi (KJ/mol) pada reaksi polimerisasi ... 2
3 Variasi konsentrasi prekursor... 5
4 Perbandingan konsentrasi untuk setiap metode ... 5
5 Perbandingan bilangan gelombang
Polyglycolide
(PGA)
dengan
sodium chloroacetate
...
7
6 Perubahan massa
Polyglycolide
... 7
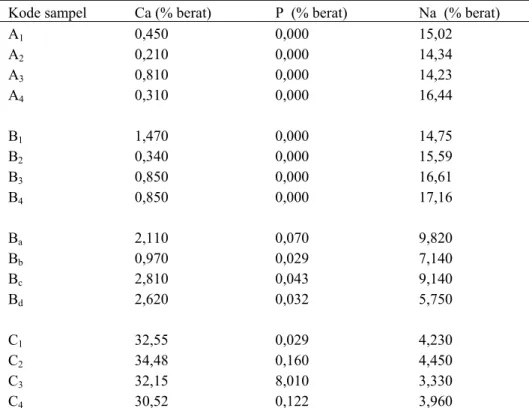
7 Kadar Ca, Na dan P dalam presipitat ... 8
8 Nilai Ca/P... 8
9 Bilangan gelombang spektrum FTIR ... 13
10 Pita serapan fosfat dan karbonat ... ... 15
DAFTAR GAMBAR
Halaman
1 Unit sel dari struktur hidroksiapatit... 3
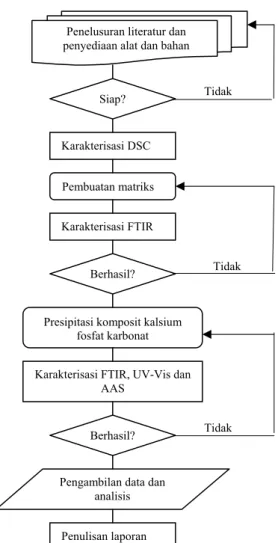
2 Diagram alir penelitian... 6
3 Hasil DSC
sodium chloroacetate
... 7
4 Spektra FTIR
polyglycolide
...
7
5 Spektra FTIR A1, A2, A3 dan A4
... 10
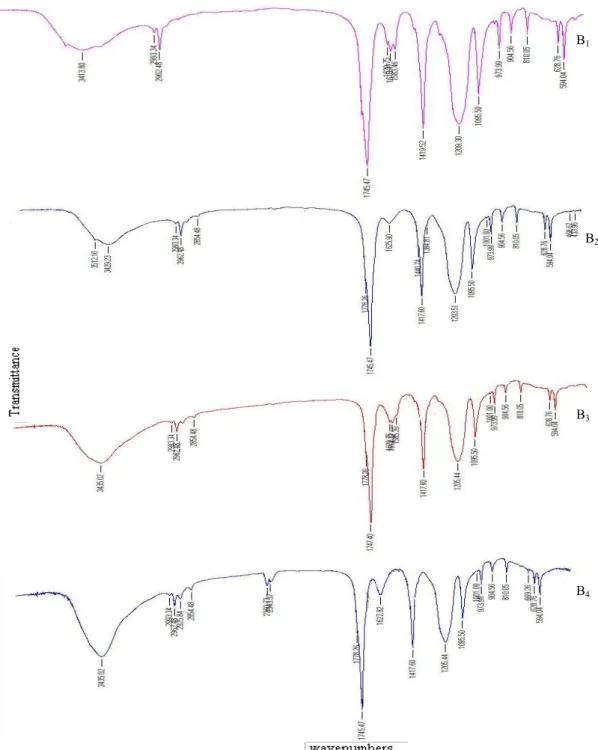
6 Spektra FTIR B1, B2, B3 dan B4
... 11
7 Spektra FTIR Ba, Bb, Bc dan Bd... 12
8 Spektra FTIR C1, C2, C3 dan C4
... 14
9 SEM Sampel B2... 15
10 XRD sampel B2... 15
DAFTAR LAMPIRAN
Halaman
1 Set up percobaan metode tetes vakum dan non vakum... 19
2 Set up percobaan metode perbandingan massa matriks – mineral... 20
3 Massa sampel dan hasil pengukuran AAS/UV-Vis terhadap ion
Ca
2+, P
5+dan Na
+... 21
4 Spektra FTIR sampel A1, A2, A3 dan A4
... 22
5 Spektra FTIR sampel B1, B2, B3 dan B4... 24
6 Spektra FTIR sampel Ba, Bb, Bc dan Bd. ... 26
PENDAHULUAN
Latar Belakang
Secara umum tubuh manusia tersusun oleh jaringan keras dan jaringan lunak. Tulang dan gigi termasuk jaringan keras yang merupakan organ biologi dinamik yang tersusun oleh sel aktif metabiologi yang terintegrasi ke dalam rangka yang kaku[1]. Dalam pertumbuhannya, tulang memerlukan banyak senyawa mineral. Senyawa mineral yang diperlukan untuk pertumbuhan banyak dikonsumsi dari luar tubuh seperti makanan dan susu. Senyawa mineral yang berada di dalam tulang pada umumnya berbentuk senyawa kalsium. Kalsium pada tulang berikatan dengan gugus-gugus diantaranya fosfat, hidroksida, dan karbonat. Senyawa kalsium dalam tulang banyak berikatan dengan fosfat sehingga senyawanya dikenal dengan nama kalsium fosfat[2].
Senyawa kalsium fosfat pada tulang memberikan sifat keras dalam tulang, sehingga senyawa kalsium fosfat sangat penting bagi tulang. Dalam proses kalsifikasi, kalsium fosfat dalam jaringan keras akan semakin dewasa seiring dengan pertambahan umur. Pada usia muda tulang memiliki fasa amorf dalam jumlah yang lebih banyak, menunjukkan bahwa tulang masih tumbuh, sedangkan pada usia mencapai tua, tulang memiliki lebih banyak senyawa kalsium fosfat dalam bentuk kristal[2].
Senyawa kalsium fosfat dalam tulang hadir dalam dua fase, yaitu fase amorf dan fase kristal. Fase kristal senyawa kalsium fosfat yang paling stabil adalah hidroksiapatit (HAP), Ca10(PO4)6(OH)2. Selain gugus fosfat, hidroksida, dan karbonat, di dalam tulang juga terdapat unsur-unsur lain seperti Mg2+, F-, Na+, dan Cl-, kehadiran unsur tersebut akan mengganggu hidroksiapatit.
Adanya kerusakan pada tulang, seperti fraktur akibat kecelakaan dan penyakit, membutuhkan komposit biomaterial antara polimer dan keramik kalsium fosfat yang lebih biokompatibel sebagai substitusi tulang. Polimer yang cocok sebagai material tersebut salah satunya adalah polyglycolide (PGA). Polyglycolide (PGA) merupakan poliester yang
sering digunakan dalam bidang kedokteran yang bersifat biokompatibel, non toxic, dan
mudah terdegredasi di dalam tubuh[3].
Perumusan Masalah
Polimer kalsium fosfat karbonat merupakan biomaterial yang dapat digunakan untuk menggantikan tulang. Biomaterial tersebut dapat mempermudah dalam
pembedahan karena dapat langsung diinplankan ke dalam tubuh tanpa membutuhkan material yang dicangkok dari tulang lain yang sehat.
Biomaterial yang dibutuhkan adalah campuran amorf dan kristal dengan ukuran kecil supaya biomaterial tersebut dapat mengikuti proses metabolisme dalam tubuh. Pada penelitian ini akan dilakukan penambahan gugus karbonat (CO32-) untuk mendapatkan kadar kasium fosfat yang sesuai dengan kondisi fisiologis tubuh. Kadar dan karakteristik senyawa kalsium fosfat karbonat dapat diidentifikasi dengan menggunakan spektrometer AAS, UV-Vis dan FTIR (Fourier Transform Infrared).
Tujuan
1. Membuat matriks polyglycolide berpori
dari sodium chloroacetate dengan proses
reaksi kering.
2. Presipitasi kalsium fosfat karbonat pada
polyglycolide untuk menghasilkan
komposit polimer kalsium fosfat karbonat. 3. Karakterisasi sampel dengan
menggunakan spektrometer FTIR (Fourier Transform Infra Red), AAS
(Atomic Absorption Spectroscopy) dan
UV-Vis (Ultra Violet Visible).
Tempat dan Waktu
Penelitian ini dilaksanakan di Laboratorium Biofisika, Departemen Fisika IPB Kampus IPB Darmaga. Karakterisasi dengan menggunakan spektrometer AAS dan UV-Vis di Laboratorium Terpadu IPB, FTIR dilakukan di pusat penelitian Biofarmaka.
TINJAUAN PUSTAKA
Matriks Polimer Berpori
Matriks polimer berpori merupakan media tempat tumbuh apatit karbonat yang diharapkan dapat membentuk komposit biomaterial dengan kalsium fosfat yang bisa diinplankan langsung ke dalam tulang. Tulang merupakan organ tubuh yang sangat penting dalam menunjang kehidupan, oleh karena itu polimer yang akan menjadi media tempat tumbuh senyawa kalsium fosfat karbonat tersebut harus memenuhi beberapa syarat, yaitu dapat diterima oleh tubuh dan bisa beradaptasi dengan lingkungan biologis[3]. Polimer bertugas sebagai matriks yang keberadaannya dalam tubuh tidak diperlukan selamanya, setelah mineral apatit bersatu di dalam tulang dan membentuk tulang yang sehat, maka polimer tersebut akan hilang. Hal ini
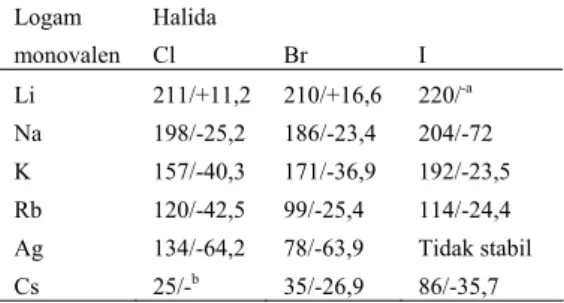
[ OOC CH ] MX n X CH OOC M − → − − − n+ − + 2 2 1 1) Logam Halida monovalen Cl Br I Li 211/+11,2 210/+16,6 220/-a Na 198/-25,2 186/-23,4 204/-72 K 157/-40,3 171/-36,9 192/-23,5 Rb 120/-42,5 99/-25,4 114/-24,4 Ag 134/-64,2 78/-63,9 Tidak stabil Cs
memberikan syarat sifat biodegradable bagi
polimer tersebut[3].
Polyglycolide (PGA) didapatkan dari
reaksi polimerisasi halogenoacetate melaui
reaksi kering. Terdapat berbagai jenis
halogenoacetate di alam yang dapat
menghasilkan polyglycolide dengan pori yang
bervariasi. Pemilihan prekursor dan perlakuan mekanik yang tepat akan menghasilkan ukuran pori rata-rata yang berdiameter 0,3 dan 1,5
μm[4]. 25/-b 35/-26,9 86/-35,7
L
Polyglycolide didapatkan dengan
mengeliminasi logam halida dari
halogenoacetate pada suhu tertentu. Reaksi
eliminasi halogenoacetat adalah:
Halogenoacetate memiliki formula umum
MOOCCH2X dengan M adalah logam monovalen dan X adalah halogen. Untuk mengetahui suhu polimerisasi telah dilakukan beberapa penelitian dengan menggunakan
Differential Scanning Calorimetry(DSC), Thermogravimetry - Differential Thermal Analysis – Mass Spectroscopy (TG-DTA-MS).
Hasil karakterisasi memberikan informasi beberapa halogenoacetate yang dapat
mengalami polimerisasi.
Sodium chloroacetate akan mengalami
polimerisasi pada suhu 1980C (tabel 2). Hasil penelitian menunjukan pada suhu antara 150 0C - 200 0C, struktur
polyglycolide
mencapai sempurna[4]. Diantara beberapa polimer yang ada, polyglycolide (PGA)
merupakan polimer yang lebih biokompatibel dan paling mudah terdegredasi di dalam tubuh dengan air, reaksi enzim dan proses metabolisme tubuh[4].
Komposit Polimer-Kalsium Fosfat Karbonat
Komposit biomaterial polimer-kalsium fosfat karbonat diharapkan dapat mengatasi kekurangan material allograf ataupun autograf
Tabel 1 Polimerisasi halogenoacetate[4]
ogam Halida monovalen Cl Br I Li - - - Na + + - K + + + Rb + + + Ag + + Tidak stabil Cs + + +
NH4 + Tidak dipelajari Tidak dipelajari
Tabel 2 Suhu (oC) dan entalpi reaksi (KJ/mol) pada reaksi polimerisasi [4]
a = Polimerisasi terjadi pada dua titik suhu yaitu 99 0C dan 142 0C
b = Polimerisasi terjadi pada suhu ruang
sebagai subtitusi pada tulang, sehingga dapat mengurangi penderitaan pada pasien. Secara umum penyusun komponen non organik pada tulang adalah kalsium fosfat. Senyawa kalsium fosfat memiliki dua fase, yaitu fase amorf dan kristal. Fase kalsium fosfat yang paling stabil. adalah hidroksiapatit (HAP)[5]. HAP memiliki sifat brittle dan keras untuk dibentuk,
sedangkan polimer bersifat lentur, sehingga polimer sebagai matriks HAP harus memliki sifat sinergis antar keduanya.
Senyawa kalsium fosfat dalam tulang memiliki karakteristik kristalinitas rendah dan non stoikiometri, yang disebabkan oleh kehadiran ion asing seperti Na+, H+, F-, Sr2-,
an Mg
d 2+ yang masuk ke alam kisi kristal atau hanya berada pada permukaan kisi kristal[6]. Kalsium fosfat memiliki satu fase amorf yaitu kalsium fosfat amorf (KAF), dan empat kalsium fosfat berbentuk kristal yaitu: dikalsium fosfat (DKFD, CaHPO4.2H2O), oktakalsium fosfat (OKF, Ca8H2 (PO4).5H2O), trikalsium fosfat (TKF,Ca3(PO4)2) dan hidroksiapatit (HAP, Ca10(PO4)6(OH)2). Hidroksiapatit merupakan kristal paling stabil dibandingkan dengan empat fase yang lain. Hidroksiapatit memiliki struktur heksagonal dengan parameter kisi a = b = 9,42Ao dan
c = 6,88 A0 [5].
Pertumbuhan dan pendewasaan tulang berkaitan erat dengan konversi amorf kalsium fosfat menjadi kristal apatit. Pada proses konversi, pembentukan kristal apatit didahului dengan pembentukan kristal non apatit.
Kehadiran ion karbonat dalam proses konversi tersebut telah diketahui berpengaruh pada morfologi kristal yang terbentuk, yaitu menyebabkan perubahan bentuk dan memperkecil ukuran kristal yang berpengaruh juga pada harga Ca/P.
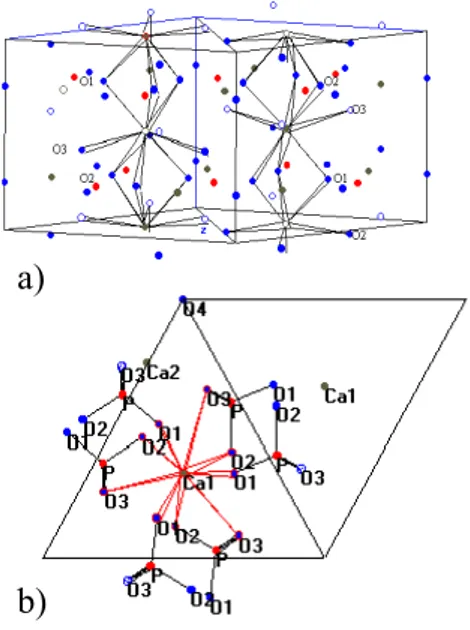
Kristal hidroksiapatit memiliki perbandingan Ca/P sebesar 1,67. Nilai ini bisa dihasilkan jika kondisi pH dan kadar kabonat dalam solusi larutan dapat terkontrol dengan baik[7]. Pada struktur kristal heksagonal senyawa kalsium fosfat stabil (hidroksiapatit), terdapat dua kristal atom kalsium yang berdiri sendiri di dalam unit sel (Gambar 1).
Atom Ca(II) dikelilingi oleh 6 atom O yang dimiliki oleh gugus–gugus PO43- dan satu buah gugus OH-. Atom Ca(I) sedikit mendekati bentuk oktahedral yang dikelilingi oleh 6 atom O. Atom Ca(II) membentuk segitiga normal pada sumbu c. Segitiga Ca(II) menumpuk sepanjang sumbu c, berotasi 600 bersama. Dalam struktur hirdroksiapatit, gugus (OH) -tidak terdapat pada pusat, tatapi bergeser ke bagian atas atau ke bagian bawah dari pusat segitiga. Atom P dikelilingi oleh 4 atom O dan membentuk tetrahedral[8].
Pengaruh Ion Karbonat dalam Kristal Apatit
Kehadiran ion karbonat ke dalam struktur HAP dapat menempati dua posisi, yaitu menggantikan gugus OH- yang akan membentuk apatit karbonat tipe A dan yang lainnya akan menggantikan gugus PO4 3-membentuk apatit karbonat tipe B. Pada umumnya apatit biologi maupun sintesis yang diperoleh pada presipitasi suhu rendah adalah apatit tipe B, sedangkan apatit karbonat tipe A diperoleh dari reaksi padat pada suhu yang tinggi[6]. Hasil SEM, dan XRD menunjukan
bahwa senyawa kalsium fosfat dalam tulang kelinci dan manusia berbentuk plat berdimensi 50-60 dan yang terbesar 320-360 , sedangkan ukuran kristal rata-rata paling kecil terjadi pada saat pembentukan kemudian meningkat saat pendewasaan[9].
0
A A0
Kristal HAP dihasilkan dari presipitasi larutan jenuh kalsium dan fosfat[10]. Kandungan kristal HAP dalam senyawa kalsium fosfat sangat dipengaruhi oleh pH larutan. Kehadiran ion karbonat pada pertumbuhan kristal apatit akan mengganggu proses pertumbuhan kristal kalsium fosfat[11]. Pada proses pertumbuhan senyawa kalsium fosfat di atas matriks organik, mucoza ampela
ayam menunjukan bahwa senyawa kalsium fosfat yang timbul di atas matriks tersebut mempunyai karakteristik yang sesuai dengan kristal HAP dan apatit karbonat[12].
a)
b)
Identifikasi Senyawa Kalsium Fosfat karbonat dengan Spektrometer Infrared
Spektrometer infrared dapat mengidentifikasi kandungan gugus kompleks senyawa kalsium fosfat, tetapi tidak digunakan untuk menentukan unsur-unsur penyusunnya. Gugus fungsi senyawa kalsium fosfat, yaitu PO43-, CO32-, dan OH-. Gugus PO4 3-mempunyai empat mode vibrasi, yaitu: vibrasi
stretching (ν1) dengan bilangan gelombang
sekitar 956 cm-1, vibrasi
bending (ν2) dengan
bilangan gelombang sekitar 430-460 cm-1, vibrasi asimetri stretching (ν3) dengan bilangan
gelombang sekitar 1040-1090 cm-1 dan vibrasi asimetri bending (ν4) dengan bilangan
gelombang sekitar 575-610 cm-1.
Bentuk pita ν3 dan ν4 yang tidak simetri merupakan tanda bahwa senyawa kalsium fosfat tidak seluruhnya dalam bentuk amorf. Spektrum hidroksiapatit dapat diteliti yaitu pada ν4 dalam bentuk belah dengan maksimum 562 cm-1 dan 602 cm-1. Pita absorbsi ν3 mempunyai dua puncak maksimum yaitu pada bilangan gelombang 1090 cm-1 dan 1030 cm-1. Pita ν1 dapat dilihat pada bilangan gelombang 960 cm-1[13].
Pita absorbsi OH- dapat terlihat juga dalam spektrum hidroksiapatit yaitu disekitar 3576 cm-1dan 632 cm-1. Air dapat hadir dalam kristal maupun pada permukaan kristal tersebut. Air di atas permukaan kristal apatit akan hilang dan tidak dapat balik pada pemanasan di bawah suhu 200 0C[14]. Pita serapan energi untuk gugus karbonat dapat diamati pada bilangan gelombang disekitar 1545, 1450, dan 890 cm-1. Kristal apatit tipe B Gambar 1 a) Unit sel dari struktur
hidroksiapatit dan b) Struktur hidroksiapatit tampak atas.
mempunyai daerah bilangan gelombang gelombang disekitar 1465, 1412, 873 cm -1[13].
Identifikasi Senyawa Kalsium Fosfat karbonat dengan Spektrometer UV-Vis
Spektrometer ini memanfaatkan panjang gelombang pada daerah ultraviolet dan cahaya tampak. Panjang gelombang dihasilkan oleh sumber lampu yang mempunyai panjang gelombang khusus, yaitu lampu deuterium, hidrogen, atau tungsen. Spektrometer ini dapat mengukur kadar fosfor dari senyawa kalsium fosfat, dengan menghitung nilai transmitansi dari sinar yang dilewatkan oleh larutan yang ingin diukur kadarnya. Besarnya transmitansi dari larutan akan menunjukan kadar penyusun senyawa tersebut sesuai dengan panjang gelombang yang digunakan[15].
Identifikasi Senyawa Kalsium Fosfat karbonat dengan AAS
Spektrometer AAS untuk menentukan unsur-unsur logam dengan menggunakan prinsip penyerapan energi sinar atom. Energi tersebut berasal dari luar, yaitu lampu hollow cathode. Fenomena AAS dibagi menjadi dua
proses, yaitu produksi atom bebas dari sampel dan serapan radiasi dari sumber luar atom.
Serapan radiasi oleh atom bebas terjadi dari keadaan energi dasar (ground state).
Biasanya transisi terjadi antara keadaan pertama dengan keadaan dasar, dikenal sebagai garis resonansi pertama. Garis resonansi pertama memiliki absortivitas yang paling tinggi. Atom-atom kalsium atau magnesium dalam larutan akan diuapkan dalam api dengan suhu tinggi, yang menyebabkan terurainya ikatan-ikatan kimia di dalam senyawa kalsium fosfat. Atom-atom tersebut akan menyerap sinar dari sumber lampu hollow cathode.
Intensitas awal dan intensitas akhir dari sinar tersebut diukur. Banyaknya sinar yang diserap menunjukkan besarnya konsentrasi logam tersebut dalam larutan.
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan mencakup sodium chloroacetate proanalisis, NaHCO3(s)
proanalisis, Na2HPO4.2H2O(s) proanalisis, CaCl2.2H2O(s) proanalisis, dengan variasi perbandingan konsentrasi terlihat pada tabel 3. Peralatan yang digunakan adalah buret, beaker glasss, statip, pengaduk, crucible (cawan
keramik), alumunium foil, pipet mohr, magnetic strirrer, eksikator, hotplate, neraca
analitik, kertas whatman, furnace, pH meter
digital, buret, termometer digital, bulb, sample holder kaca, mould untuk membuat pelet
matriks standar IR (infra merah), spektrometer AAS (Atomic Absorbtion Spectroscopy), FTIR (Fourier Transform Infrared), dan
spektrometer UV-Vis (Ultraviolet-Visible).
Metode Penelitian
Pembuatan matriks polimer
Sodium chloroacetate terlebih dahulu
dikarakterisasi dengan menggunakan DSC (Differential Scanning Calorimetry) untuk
mengetahui suhu polimerisasi bahan. Serbuk
Sodium chloroacetate ditempatkan pada crucible dan dipanaskan pada furnace dalam
suasana nitrogen sampai suhu polimerisasi. Setelah dipanaskan bahan tersebut digerus dengan dengan mortar.
Pembuatan matriks polimer berpori
Sodium chloroacetate yang telah
dipanaskan digerus dengan mortar kemudian ditekan dengan tekanan standar IR (inframerah) membentuk pelet dengan diameter 13 mm dan tebal 3 mm. NaCl yang bercampur dengan PGA dihilangkan dengan pencucian mengunakan aquades hangat (triplo),
kemudian divakum. Setelah divakum, pelet ditimbang, kemudian dicuci kembali sebanyak 3 kali, divakum, kemudian ditimbang. Proses ini dilakukan sampai massa pelet konstan
Presipitasi komposit polimer-kalsium fosfat karbonat
Metoda tetes vakum
Larutan NaHCO3(l) l ml dan NaHPO4.2H2O(l) 1 ml dicampur dan diteteskan di atas matriks kemudian diikuti CaCl2.2H2O(l) 1 ml. Matriks PGA hasil presipitasi kemudian
divakum pada tekanan 176 mmHg dan dikeringkan menggunakan furnace pada suhu
110 0C selama 10 jam . Metoda tetes non vakum
Terdapat dua volume larutan prekursor yang digunakan 1 ml (Bx) dan 2 ml (By), x = 1, 2, 3 ,4 dan y = a, b, c, d. NaHCO3(l) dicampur dengan larutan Na2HPO4.2H2O(l) dengan perbandingan konsentrasi sesuai dengan tabel 4. Larutan campuran diteteskan di atas matriks
PGA berpori kemudian diikuti dengan
penetesan larutan larutan CaCl2.2H2O(l). Matriks yang telah dipresipitasi dikeringkan dengan furnace pada suhu 110 0C selama 10
M P
C B).
V(
X −
Metode perbandingan massa matriks - mineral
=
[NaHCO3]
M [Na2HPO4.2H2O] M [CaCl2.2H2O] M Larutan kalsium fosfat karbonat dibuat
dengan mencampurkan larutan NaHPO4.2H2O(l) 50ml dan NaHCO3(l) 50 ml dengan variasi konsentrasi sesuai dengan tabel 3 Larutan CaCl2.2H2O 50 ml ditambahkan tetes demi tetes ke dalam larutan sambil diaduk dalam
beaker glass dalam atmosfir N2 dengan
menggunakan magnetic stirrer di atas hotplate
pada suhu 700C. Nilai pH dipertahankan dengan mengunakan amoniak, ketika nilai pH kurang dari 7,4 diteteskan amoniak. Proses ini berakhir setelah CaCl2.2H2O habis. Larutan kalsium fosfat karbonat hasil presipitasi kemudian diendapkan dan disaring menggunakan kertas whatman. Endapan hasil
penyaringan kemudian dikeringkan menggunakan furnace pada suhu 110 0C
selama 10 jam. Komposit dibuat dengan mencampurkan 30 % b/b matriks PGA 70 % b/b kalsium fosfat karbonat. Komposit tersebut kemudian dipress membentuk pellet dengan diameter 13 mm dan tebal 3 mm. NaCl di dalam komposit dihilangkan dengan mencuci komposit memakai aquades hangat (triplo).
Komposit yang telah dicuci kemudian divakum dan ditimbang. Proses ini berakhir sampai massa komposit tetap.
Kararakterisai dengan spektrometer infrared
Dua miligram pelet hasil presifitasi yang sudah kering dicampur dengan 100 mg KBr, dibuat pelet IR (inframerah). Bilangan gelombang yang digunakan adalah 4000 – 400 cm-1.
Karakterisasi dengan AAS (Atomic
Absorption Spectroscopy) dan Spektrometer
UV-Vis (Ultra Violet Visible)
Spektrometer UV-Vis digunakan untuk mengukur fosfor (P), dan AAS digunakan untuk mengukur kadar Ca dan Na. Langkah pertama dalam karakterisasi adalah preparasi sampel. Sampel ditimbang sebanyak 0,1 – 0,3 gram ditambah 3,5 ml asam nitrat pekat (H2NO3) ditambah (HClO4) lalu didiamkan semalam. Sampel didestruksi pada suhu 1000C selama 1 jam, suhu dinaikan menjadi 1500C selama 2 jam, kemudian dinaikan lagi menjadi 2000C selama 1 jam. Sampel didinginkan lalu diencerkan dengan 100 ml air. Sampel dikocok lalu diendapkan 1 malam. Ekstrak jernih di ukur.
Pengukuran Ca dilakukan dengan menambahkan 4,5 ml air ke dalam ekstrak kemudian ditambah CaCl3 lalu dikocok. Setelah
itu kandungan Ca diukur dengan AAS dengan panjang gelombang 422,3 nm - 422,7 nm. Pengukuran PO4, Sebanyak 0,5 ml ekstrak ditambah 4,5 ml air ditambah pereaksi P lalu dikocok dan didiamkan 1,5 jam. Kemudian diukur dengan menggunakan spektrometer UV-Vis dengan panjang gelombang 693 nm. Besarnya konsentrasi masing-masing ion dihitung dengan persamaan:
2) X= konsentrasi ion (ppm) V = Volume larutan (ml) C = Konsentrasi (ppm) B = Konsentrasi blanko P = Pengenceran
M = Massa sampel (gram)
Tabel 3 Variasi konsentrasi prekursor
1 0,50 0,50
1 0,25 0,25
1 0,50 0,84
1 0,25 0,41
Tabel 4 Perbandingan konsentrasi untuk setiap metode
A = Metoda tetes vakum B = Metoda tetes non vakum
C = Metoda perbandingan massa matriks dan mineral
Kon
(M) sentrasi prekursor Kode sampel [Ca] : [PO4] : [CO3] A B C
Bx By 0,50 : 0,50 : 1 A1 B1 Ba C1 0, 0, 0, 25 : 0,25 : 1 A2 B2 Bb C2 84 : 0,50: 1 A3 B3 Bc C3 42 : 0,25 : 1 A4 B4 Bd C4
Gambar 2 Diagram alir penelitian.
HASIL DAN PEMBAHASAN
Polimerisasi sodium chloroacetate
Sodium chlorocetate merupakan salah satu halogenoacetate yang dapat mengalami
polimerisasi ketika dipanaskan. Suhu polimerisasi sodium chloroacetate diketahui
dengan menggunakan differential scanning calorimentry (DSC).
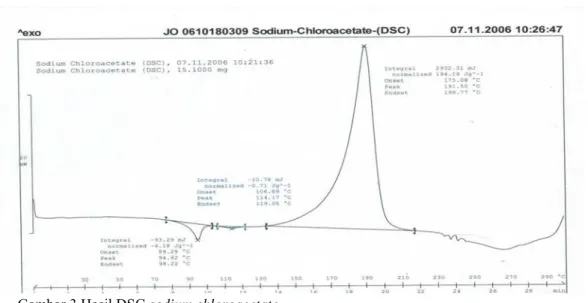
Hasil DSC menunjukkan suhu polimersasi sodium chloroacetate yang digunakan sebesar 191,5 0C (gambar 3). Puncak eksoterm pada suhu 191,5 0C merupakan tanda bahwa
sodium chloroacetate mengalami reaksi polimerisasi.
Polimer yang terbentuk dari hasil reaksi polimerisasi adalah polyglycolide (PGA) dan
hasil reaksi sampingnya adalah garam (NaCl). Hasil FTIR (gambar 4) menunjukkan bahwa polyglycolide (PGA) terbentuk ketika
sodium chloroacetate dipanaskan pada suhu 191,5 0C ditunjukan dengan adanya puncak milik polygycolide (PGA). Tabel 5
memperlihatkan perbandingan bilangan
gelombang milik sodium chloroacetate dengan polyglycolide (PGA).
Penelusuran literatur dan penyediaan alat dan bahan
Siap?
Pembuatan matriks Karakterisasi DSC
Karakterisasi FTIR
Berhasil?
Presipitasi komposit kalsium fosfat karbonat
Karakterisasi FTIR, UV-Vis dan AAS
Berhasil?
Pengambilan data dan analisis
Penulisan laporan
Tidak Tidak
Tidak
Tidak ditemukan pada spektum FTIR bilangan gelombang milik sodium chlroacetate hal ini
menunjukkan bahwa sodium chlroacetate telah
mengalami reaksi polimerisasi membentuk
polyglycolide (PGA) dan NaCl. Polyglycolide
(PGA) berpori (porous polyglycolide)
didapatkan dengan cara mencuci Polyglycolide
menggunakan aquadest
sebanyak tiga kali. NaCl pada PGA akan larut di dalam air dan meninggalkan lubang berupa pori. Tabel 6 menyajikan berat PGA hasil pencucian.
Tabel 6 memperlihatkan bahwa setiap matriks rata-rata massanya berkurang sekitar 0,045 gram atau 1/11 berat awal. Sedikitnya berat NaCl yang larut disebabkan oleh permukaan matriks yang menutupi NaCl bagian dalam sehingga NaCl di bagian dalam matriks sulit untuk larut dan hanya NaCl yang berada pada bagian permukaan matriks saja yang larut di dalam air.
Kelarutan NaCl yang kecil akan menambah kadar Na dalam presipitat. Hasil AAS memperlihatkan rata-rata setiap presipitat masih mengandung kadar Na yang cukup besar ditunjukkan dengan % berat Na dalam presipitat yang lebih besar dari pada Ca dan P (tabel 7).
Kelarutan NaCl dalam air yang kecil akan menghasilkan jumlah dan distribusi pori pada matriks tidak merata. Pembentukan jumlah pori yang sedikit akan menghambat masuknya molekul-molekul prekursor ke dalam matriks. Waktu pencucian yang lama merupakan salah satu cara untuk menghasilkan jumlah pori yang besar, tetapi karena polyglycolide (PGA)
merupakan polimer yang hidrofilik maka
lamanya waktu pencucian akan menyebabkan kerusakan pada struktur matriks.
Analisis kandungan Ca2+, Na+ dan P5+
menggunakan AAS dan spektrometer UV-Vis
Spektrometer AAS digunakan untuk mengidentifikasi kation-kation yang berada pada komposit polimer kalsium fosfat karbonat. Ion – ion tersebut adalah Na+ dan Ca2+, sedangkan spektrometer UV-Vis digunakan untuk mengidentifikasi ion PP
5+. Telah dilakukan tiga metode untuk menghasilkan komposit polimer kalsium fosfat karbonat yaitu: metode tetes vakum (A), (B) metode tetes non vakum (B) dan (C) metode perbandingan massa matriks - mineral (C). Tabel 7 memperlihatkan hasil pengukuran AAS dan UV-Vis terhadap Ca2+, Na+ dan P5+
Gambar 3 Hasil DSC sodium chloroacetate.
Ulangan Massa sampel (gram)
s.a s.b s.c s.d 0 0,50 0,50 0,50 0,50 1 0,49 0,47 0,49 0,49 2 0,47 0,46 0,48 0,48 3 0,46 0,45 0,47 0,47 4 0,46 0,45 0,46 0,46 5 0,46 0,44 0,45 0,46 6 0,46 0,44 0,45 0,46
Tabel 5 Perbandingan bilangan gelombang polyglycolide (PGA) dengan sodium chloroacetat
Gugus Bilangan gelombang (cm-1)
Polyglycolide (PGA)[21] Sodium chlorocetate Polyglycolide (PGA)
Tabel 6 Perubahan massa polyglycolide
Gambar 4 Spektra FTIR polyglycolide.
C – H 2962/2991 3008/2972 2962/2995 C = O dalam ester 1749 1601 1749 = O gugus acetate 1633 1633 O, C – H 1420 1421 1420 OH 1094 1094 975, 904, 809, 628, 594 933, 771, 674, 578. 975, 904, 809, 628, 594 C – O 1249 1210 C CO C –
Tabel 7 Kadar Ca, Na dan P dalam presipitat
Kode sampel Ca (% berat) P (% berat) Na (% berat)
A1 0,450 0,000 15,02 A2 0,210 0,000 14,34 A3 0,810 0,000 14,23 A4 0,310 0,000 16,44 BB1 1,470 0,000 14,75 BB2 0,340 0,000 15,59 BB3 0,850 0,000 16,61 BB4 0,850 0,000 17,16 BBa 2,110 0,070 9,820 BBb 0,970 0,029 7,140 BBc 2,810 0,043 9,140 BBd 2,620 0,032 5,750 C1 32,55 0,029 4,230 C2 34,48 0,160 4,450 C3 32,15 8,010 3,330 C4 30,52 0,122 3,960
Tabel 8 Nilai Ca/P
Kode sampel Jumlah partikel x 1020
Ca P Ca/P A1 6,67 0,000 A2 3,16 0,000 A3 1,22 0,000 A4 4,66 0,000 BB1 22,0 0,000 BB2 5,11 0,000 BB3 12,7 0,000 BB4 12,7 0,000 BBa 31,7 1,40 22,30 BBb 14,6 0,58 25,07 BBc 42,3 0,86 49,00 BBd 39,4 0,64 54,00 C1 1660 2,03 818,4 C2 1760 11,19 157,28 C3 1770 589 3,00 C4 1560 8,30 187,90
Hasil pengukuran spektrometer AAS (tabel 7) terlihat bahwa pada sampel A1 – A4, BB1 - B4 dan Ba – Bd kadar ion terbesar yang
terkandung dalam sampel adalah Na . Sumber Na di dalam sampel berasal dari NaHCO
+ +
3 , Na2HPO4.2H2O dan matriks. Pada metode tetes kadar Na yang terlalu besar pada matriks akan menghambat proses pembentukan komposit polimer kalsium fosfat karbonat, karena saat larutan prekursor diteteskan di atas matriks, Na akan menghambat masuknya Ca dan PO
+ 2+
43- ke dalam pori matriks.
Sampel A1 – A4 merupakan komposit yang dibuat dengan metode tetes vakum dengan tujuan mengeliminasi kadar air dalam presipitat. Perbedaan antara sampel A1 – A4 dengan sampel B1 – B4 terletak pada kadar Ca2+ di dalam presipitat. Kadar Ca2+ dalam A1 – A4 lebih sedikit dibanding dengan B1 – B4, hal ini disebabkan saat preoses vakum, terdapat ion-ion Ca2+ tertarik ke luar tabung vakum (tabel 7).
Kadar P5+ dalam sampel A1 – A4 dan B1 – BB4 adalah nol, hal ini disebabkan oleh kelarutan
P yang cukup besar dalam larutan NaCl saat preparasi sampel uji UV-Vis. Kadar Na yang besar di dalam sampel A
5+
1 – A4 dan B1 – B4 menandakan bahwa masih banyak NaCl di dalam presipitat (tabel 7). Peluang keberadaan P dalam presipitat dapat diperbesar dengan meningkatkan volume prekursor P . Volume prekursor yang digunakan pada sampel B
5+
5+
a – Bd adalah lebih besar dibandingkan dengan sampel A1 – A4 dan B1 – B4, sehingga peluang kadar P dalam presipitat B5+ a – Bd lebih besar dari pada A1 – A4 dan B1 – B4 (tabel 7).
Rasio konsentrasi CO32- terhadap konsentrasi PO43- dapat mempengaruhi kadar P5+ dalam presipitat. Semakin besar perbedaan konsentrasi CO32- terhadap konsentrasi PO43-, maka semakin banyak PO43- yang digantikan oleh CO32-. Rasio konsentrasi CO32- tehadap PO43- pada sampel Ba lebih kecil dari pada sampel Bb sehingga kadar PP
5+ dalam sampel B lebih sedikit dibandingkan dengan sampel B , hal yang sama terjadi juga pada sampel B dan
Bd 3 b a c B, rasio konsentrasi CO 2- terhadap PO43- sampel Bc , sehingga kadar P
lebih kecil dibanding dengan sampel BdB
5+ dalam sampel B lebih kecil dibanding sampel B (tabel 7). c d
Rasio konsentrasi prekursor Ca2+ dan P
P
5+ pada sampel B dan B adalah sama tetapi tidak menghasilkan nilai Ca/P yang sama, hal ini terjadi karena adanya pengaruh karbonat yang dapat mengantikan gugus fosfat dalam presipitat. Pengaruh ion karbonat juga telihat pada sampel Bc dan B , meskipun perbandingan Ca/P telah dikondisikan sebesar
1,67 namun tetap nilai Ca/P hasil presipitasi berbeda (tabel 8).
a b
d
Kadar Ca2+ dan P5+ pada sampel C1 – C4 (tabel 7) bervariasi sesuai dengan variasi konsentrasi setiap prekursor. Sampel C1, C2 dan C4 memiliki nilai Ca/P yang sangat besar dari pada sampel . Nilai Ca/P yang besar pada sampel C1, C2 dan C4 dapat disebabkan larutnya PO43- pada saat pencucian komposit dalam air untuk menghilangkan NaCl dari presipitat, hal ini disebabkan PO43- memiliki kelarutan yang cukup besar di dalam larutan yang mengandung garam[22]. Sampel C3 menghasilkan nilai Ca/P sebesar 3,1 hal ini terjadi karena selain dikondisikan konsentrasi prekursor mendekati Ca/P = 1,6 juga disebabkan oleh kandungan Na dalam sampel yang paling kecil dibanding dengan semua sampel. Komposit polimer kalsium fosfat karbonat yang terbentuk pada sampel C3 bersifat amorf dan memilki karakter apatit karbonat tipe B, karena nilai Ca/P nya lebih dari 1,67.
Analisis gugus CO32- dan PO4
3-menggunakan spektrometer FTIR
Hasil spektra FTIR (gambar 5) tidak menunjukkan puncak milik gugus CO32-
dan
PO43- pada setiap sampel. Puncak yang muncul didominasi oleh puncak gugus-gugus yang dimiliki oleh polyglycolide dan hidroksil. Polyglycolide terletak pada bilangangelombang : 2992/2961 cm-1 (C-H), 1744 cm-1 (C=O), 1096 cm-1 (C-OH), 1420 cm-1 (COO,C-O), 1229 cm-1 (C-O), 1630 cm-1 (C=O), (974, 904, 808, 628 dan 594) cm-1. Hidroksil (O-H) terletak pada bilangan gelombang (3600-3200) cm-1. Gugus PO43-
dan
CO32- tidak ditemukan pada spektra FTIR. Faktor penyebabnya antara lain:1. Jumlah pori pada matriks sangat kecil dan penyebarannya tidak merata, sehingga menyebabkan molekul pembentuk HAP terhambat untuk masuk ke dalam pori-pori matriks.
2. Jumlah pori yang sedikit menyebabkan pertumbuhan HAP terjadi di atas permukaan matriks , sehingga pada saat divakum banyak molekul-molekul HAP yang tertarik oleh udara ke luar tabung vakum.
3. Distribusi pori yang tidak merata menyebabkan pertumbuhan HAP di dalam matriks tidak homogen, sehingga sample yang diambil untuk uji optik (FTIR) kemungkinan bukan bagian matriks yang ditumbuhi oleh HAP.
Sampel A1, A2, A3 dan A4 (gambar 5) memiliki pola spektrum FTIR dengan bilangan
gelombang yang sama. Hal ini menunjukkan bahwa variasi konsentrasi prekursor yang digunakan tidak menimbulkan pengaruh yang
signifikan terhadap pertumbuhan apatit karbonat di atas matriks.
A1
A2
A3
A4
Hasil spektra FTIR komposit menunjukkan PO43- tidak ditemukan pada sampel B1 – B4 kecuali pada sampel B2 terdapat vibrasi bending (ν2) milik PO43- pada bilangan gelombang (433,6 – 468,6) cm-1. Intensitas ν2 PO43- pada sampel B2 menunjukkan rendahnya kadar PO43- pada sampel, hal ini sesuai dengan hasil UV-Vis (tabel 7).
Secara umum bilangan gelombang yang muncul pada sampel B1 – BB4 sama dengan
bilangan gelombang yang ada pada komposit
dengan metode tetes vakum (A1-A4). Bentuk spektra dan bilangan gelombang yang sama antara metode tetes vakum (A1-A4) dengan metode tetes non vakum (B1B – B4) disebabkan
oleh konsentrasi dan volume prekursor yang digunakan pada ke dua metode ini sama. Spektra FTIR komposit menunjukkan baik CO32- dan PO43- tidak ditemukan pada sampel BBa - Bd kecuali pada sampel Ba terdapat vibrasi
bending (ν2) milik PO43- pada bilangan gelombang ( 435,89 cm ). -1
B4
B3
B2
B1
Ba
Bd Bc Bb Tabel 9 menunjukkan bahwa hampir semua
bilangan gelombang yang muncul didominasi oleh bilangan gelombang milik gugus
polyglycolide (PGA), kecuali pada bilangan
gelombang di sekitar 1417 – 1420 cm-1 memungkinkan dapat dimiliki oleh gugus (COO, C-H) dan CO32-. Hal ini disebabkan gugus CO32- memiliki spektra di sekitar bilangan 1412 – 1475 cm-1. Kadar COO, C-H yang besar dalam presipitat memungkinkan
spektra FTIR COO, C-H menutupi spektra FTIR CO32-. Tidak adanya gugus fosfat pada spektra FTIR menunjukkan bahwa pembentukan komposit polimer kalsium fosfat karbonat dengan metode tetes vakum dan tetes non vakum tidak terjadi secara merata ke seluruh bagian martiks.
Tabel 9 Bilangan gelombang spektrum FTIR
Kode sampel Gugus Bilangan gelombang (cm-1)
A1
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH) (3429-3512), (2993/2961), (2885), (1745), (1626), (1417), (1203), (1095), (974, 904, 810, 628, 594) A2
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (C=O), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH) (3429-3512), (2992/2961), (2885), (1745), (1626), (1585) (1417), (1203), (1095), (974, 904, 810, 628, 594) A3
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (C=O), (COO,C-H / CO32-),
(C-O dalam ester), (C-OH) (3435), (2993/2961), (2885), (1745), (1629), (1585) (1419), (1205), (1094), (973, 903, 809,, 628, 594). A4
O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (C=O), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH) (3437), (2993/2961), (2885), (1747), (1629), (1585) (1419), (1211), (1094), (973, 903, 809,, 628, 594). B1
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (C=O), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH) (3414), (2993/2961), (2885), (1745), (1629), (1585) (1419), (1209), (1094), (973, 903, 809,, 628, 594). B2
(O-H), (C-H), CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH,), (ν2) PO4
3-(3433 -3512), (2993/2961), (2885), (1747), 1625), (1417), (1203), (1094), (973), 903, 810, 628, 594, (433,9 – 468.6)
B3
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH) (3435), (2992/2961), (2885), (1747), (1624), (1419), (1205), (1094), (973, 904, 809, 712, 628, 594) B4
(O-H), (C-H), (CH2), (PH), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH) (3435), (2992/2961), (2925, 2885),(2360-234,37), (1747), (1624), (1419), (1202), (1094), (973, 903, 809, 669, 628, 594) Ba
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-), (C-H)
(C-O dalam ester), (C-OH), ((ν2) PO43-)
(3448), (2992/2961), (2885, 2985), (1747), (1629), (1417), (1384), (1211), (1094), (973, 903, 809, 628, 594), (435,89) Bb
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH) (3436), (2992/2961), (2885), (1745), (1629), (1417), (1203), (1095), (974, 904, 810, 628, 594) Bc
(O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH)
(3431-3510), (2993/2961), (2985, 2885), (1745), (1627), (1419), (1203), (1095), (973, 904, 810, 628, 594) Bd (O-H), (C-H), (CH2), (C=O gugus ester),
(C=O ujung gugus asetat), (COO,C-H/ CO32-),
(C-O dalam ester), (C-OH)
(3435), (2992/2962), (2925 - 2885), (1745), (1629), (1419), (1203), (1094), (973, 904, 810, 628, 594)
Sampel C1 - C4 dibuat dengan mencampurkan 30 % b/b matriks dan 70 % b/b mineral. Hasil spektra FTIR (gambar 8) menunjukkan bahwa semua sampel memiliki gugus fosfat dan karbonat. Bilangan gelombang fosfat dan karbonat setiap sampel disajikan pada tabel 10.
Pola spektra FTIR menunjukkan bahwa pita serapan fosfat ν3 sampel C2 lebih asimetri dibandingkan dengan pita serapan fosfat ν3
sampel C1 dan daya belah pita serapan fosfat ν4 sampel C2 lebih besar dari pada sampel C1, hal ini menunjukkan bahwa sampel C2 lebih kristal dari pada sampel C1. Sifat kristal sampel C2 disebabkan oleh sedikitnya gugus fosfat yang digantikan oleh gugus karbonat. Bilangan gelombang 1215,08 cm-1 muncul pada sampel C2 berasal dari polyglycolide yaitu milik C – O.
C1
C4
C2
C3
Pita serapan fosfat ν3 sampel C3 lebih asimetri dibanding pita serapan fosfat ν3 sampel C4 dan daya belah pita serapan ν4 sampel C3 lebih besar dari pada sampel C4, hal ini menunjukkan bahwa sampel C3 lebih kristal dibanding dengan sampel C4. Derajat kekeristalan C3 lebih besar dibanding sampel C4 disebabkan oleh rasio konsentrasi karbonat terhadap fosfat sampel C3 lebih kecil dari pada sampel C4, sehingga lebih sedikit gugus fosfat pada sampel C3 yang digantikan oleh gugus karbonat Pada sampel C3 bilangan gelombang 1215,8 cm -1 muncul berasal dari gugus C – O milik polyglycolide.
Pita serapan (ν2) dan (ν3) karbonat disekitar 871,77 cm-1 dan 1465,8 cm-1 pada sampel (gambar 14) memperlihatkan bahwa pada peresipitat yang terbentuk adalah apatit karbonat tipe B. Semua hasil karakterisasi AAS/UV-Vis dan FTIR menunjukkan bahwa pembentukan komposit polimer kalsium fosfat karbonat melalui metode tetes vakum, tetes non vakum dan metode perbandingan massa matriks-mineral kurang menghasilkan bentuk yang optimal. Hambatan utama dalam membentuk komposit melalui metode tetes vakum dan tetes non vakum adalah sedikitnya
jumlah pori yang terbentuk pada matriks, sehingga menyebabkan proses penumbuhan apatit karbonat dalam matriks tidak merata ke seluruh bagian atau hanya sebagian kecil saja dari bagian matriks yang ditumbuhi oleh apatit karbonat.
Jumlah cuplikan yang diambil pada saat analisis AAS/UV-Vis dan FTIR hanya sebagian kecil dari presipitat yang ada, hal ini memungkinkan bagian yang diambil untuk dianalisis bukan bagian yang ditumbuhi oleh apatit karbonat. SEM (scanning electron microscopy) dan XRD (X-ray difraction)
merupakan alat untuk menganalisis struktur bahan. Bagian bahan yang dianalisis oleh SEM dan XRD adalah seluruh bagian bahan.
Hasil SEM (gambar 9) sampel B2 menunjukkan terdapat apatit karbonat yang diperlihatkan dengan hadirnya campuran amorf dan kristal-kristal kecil yang tajam. Hal ini didukung oleh hasil spektra FTIR yaitu terdapat vibrasi bending ν2 pada bilangan gelombang fosfat (435,9 cm-1 – 459,03 cm-1). Hasil XRD sampel B2 memperlihatkan bahwa apatit karbonat tumbuh terdapat pada pada 2θ = 31,959 dengan ukuran kristal pada bidang (002) sebesar 21,11 nm (gambar 10).
Tabel 10 Pita serapan fosfat dan karbonat
Kode sampel Pita serapan fosfat (cm-1) Pita serapan karbonat (cm-1)
ν
2ν
3ν
4ν
2ν
3 C1 420,46 1035,71 565 871,77 1465,8 459,03 1095,5 603,7 C2 470 1033,78 565,11 871,77 1473,3 1095,57 603,7 C3 435,9 1035,71 567,04 871,77 1473,53 466,75 603,68 C4 468,67 1035,71 871,77 871,77 1473,53 605,61Gambar 9 Hasil SEM sampel B2. Gambar 10 Hasil XRD sampel B2.
Hambatan pada metode perbandingan massa matriks-mineral terletak pada saat pencucian presipitat untuk menghilangkan NaCl. Proses pencucian akan melarutkan NaCl dari presipitat, sehingga aquadest yang
digunakan pada saat pencucian berubah menjadi larutan garam (NaCl). Larutan garam yang terbentuk berfungsi sebagai pelarut bagi fosfat, sehingga menyebabkan kadar fosfat dalam presipitat akan berkurang. Kelemahan dari metode tersebut menyebabkan kadar fosfat yang terdeteksi oleh alat sangat kecil.
SIMPULAN
Berdasarkan hasil DSC, sodium chloroacetate mengalami polimerisasi pada
suhu 191,5 0C dan hasil FTIR juga menunjukkan bahwa tidak ada bilangan gelombang milik sodium sodium chloroacetate. Preparasi sampel untuk uji
UV-Vis mempengaruhi kadar P5+ dalam presipitat. Jumlah pori yang sedikit dan distribusinya yang tidak merata menyebabkan pertumbuhan apatit karbonat di dalam matriks tidak homogen. Kecilnya cuplikan sampel yang diambil untuk uji FTIR menyebabkan pola spektra FTIR gugus fosfat dan karbonat sulit ditemukan. Hasil FTIR menunjukan bahwa, komposit yang dibuat dengan perbandingan massa menghasilkan HAP tipe B ditunjukkan oleh bilangan gelombang gugus karbonat disekitar
ν
2 = 871, 7 cm-1 danν
3 = 1465,8 cm-1.DAFTAR PUSTAKA
[1] Kalfas, Ian H., M.D., F.A.C.S. 2001.
Principles of bone healing. Neurosurg.
Focus. Vol 10.April.
[2] Hidayat, Y. 2004. Karakterisasi senyawa kalsium fosfat karbonat menggunakan AAS (Atomic Absorption spectroscopy), Spektroskopi UV-VIS dan FTIR (Fourier Transform Infrared).
Skripsi S1 Departemen Fisika FMIPA IPB ( Pembimbing K. Dahlan, dan D. S. Soejoko), Bogor
[3] Rezwan K., Q.Z. Chen., J.J. Blaker., Aldo Roberto Boccaccini. 2006.
Biodegradable and bioactive porous polymer inorganiccomposite Scaffolds for Bone tissue Engineering. Biomterials
27. 3413-3431.
[
4] Epple, M,. and O. Herzberg. 1997.Polyglycolide with controlled porosity:
and improved biomaterial. J. Master.
Chem. 7(6), 1037-1042.
[5] Elliott, J. C. 1973. The Problem of composition on structure of the material components of the hard tissue, Clin
Orthop Rel Res 93:313-345.
[6] Bigi, A.,E. Foresti, R. Gregorini, A. Ripamonti, n. Noveri, anf J. S. Shah. 1992. The Role of magnesium on the structure of biological apatite, Calc.
Tiss. Int. 50:439 – 444.
[7] Neuman, W. F., and B. J. Mulryan. 1971. Syntetic hydroxyapatite crystals IV. magnesium incorpororation, Calc.
Tiss. Res. 7, 133-138.
[8] Aoki, Hideki. 1991. Scienceand medical applications of hydroxiapatite, JAAS.
Japan crystals III.. the carbonat system, Calc. Tiss. Res. 7, 133-138.
[9] Riyani, E. 2004. Karakterisasi Senyawa Kalsium Fosfat Hasil Presipitasi Menggunakan XRD (X-ray Diffraction) dan SEM (Scanning Elektron Microscope). Skripsi S1 Departemen
Fisika FMIPA IPB ( Pembimbing A. Maddu, dan D. S. Soejoko), Bogor. [10] Soejoko, D. S., and Sri Wahyuni. 2002.
Spektroskopi inframerah senyawa kalsium fofat hasil presipitasi, Makara
seri sains, Vol. 6 No. #, 117-120.
[11] Siti Ahmiarti Sa. Dan D.S. Soejoko.
Pengaruh ion karbonat dalam proses presipitasi Senyawa kalsium fosfat,
Makara Seri Sains, Vol. 6, No. 2, 2002, 55-58.
[12] Notonegoro, H. A. 2003. Analisis Hasil Spektroskopi Inframerah dan difraksi Sinar X pertumbuhan kristal apatit Pada mucoza ampela ayam, Sekripsi S1
Jurusan Fisika FMIPA UI (Pembimbing D. S. Soejoko), Depok.
[13] Rey, C., V. Renugopalakrishnan, M. Simizu, B. Collins, and Melvin J. Glimcher. 1991. a Resulation-enchanced fourier transform infrared spectroscopy study of environment of The CO3-2 Ion in The Mineral Phase of enamel during its Formations and Maturations, Calc.
Tiss. Int. 49:259-268.
[14] Hanson Bob. 2005. 15000000:1 Model of hydroxyapatite http://www. stofal
.edu. people hansonrmo/apatite/mo.html {30 mar 2005}.
[15] Willard HM, Merritt Lynne LJr, Dean John A, Settle Frank AJr. 1998.
Callifornia: Wadsoworth, Inc. Hlm. 118-148, 243-249.
[16] Schwarz, K., and M. Epple. 1998.
Biomimetic crystalization of apatite in a porous polymer martix. Chem. Eur. J. 4.
No. 10.
[17] Sieder, M., Simon J. Kitchin., Kenneth D.M., Harris., Ana L. C. Lagoa., Herminio P Diongo., Manunel E. Minas da Piedde., and Matthias Epple. 2001.
Porous Poly(D,L-lactida) and poly(D,L-lactida-co-glycolide) produced by thermal salt elimination from halogenocarboxylates. J. Chem Soc.,
Daltons Trans., 3140-3148.
[18] Baig, A. A., J.L. Fox, Z. Wang, W. I. Higuchi, C. Miller, A. M. Barry, M. Otsuka. 1999. Metastable equilibrium solubulity behavior of bone material, Calc. Tiss. Int. 64:329 – 339.
[19] Neuman, W. F., and B. J. Mulryan. 1971. Syntetic hydroxyapatite
[20] Saptari, S. A. 1999. Karbonat sebagai inhibitor dalam pembentukan pidroksiapatite hasil presipitasi, Skripsi
S1 Jurusan Fisika UI (Pembimbing D. S. Soejoko), Depok.
[21] Epple, M and O. Herzberg. Porous Polyglycolide, calc. Tiss, Res 43:
83 – 88, 1998.
Lampiran 1
Set up
percobaan metode tetes vakum dan non vakum
Lampiran 2
Set up
percobaan metode perbandingan massa matriks – mineral
Beaker
glass
Na2HPO4.2H2O 50 ml +
Lampiran 3 Massa sampel dan hasil pengukuran AAS/UV-Vis terhadap ion Ca
2+,
P
P5+
dan Na
+Kode sampel Massa (gram) Konsentrasi ion (ppm)
Ca2+ P5+ Na+ Blanko 1,120 0,000 0,000 A1 0,2846 6,000 0,0002 0,346 6,100 0,338 A2 0,2846 3,660 0,0002 0,348 3,660 0,348 A3 0,2846 6,400 0,0000 0,369 6,380 0,367 A4 0,2846 4,310 -0,0001 0,349 4,310 0,343 Blanko 1,120 0,000 0,000 BB1 0,2846 9,840 0,0002 0,353 9,840 0,348 BB2 0,2846 5,700 -0,0001 0,394 8,660 0,399 BB3 0,2846 5,700 0,0000 0,361 5,750 0,361 BB4 0,2846 10,82 -0,0001 0,391 10,82 0,392 Blanko 0,100 0,000 0,060 BBa 0,100 1,810 0,0529 0,218 1,810 0,0529 0,218 BBb 0,100 0,890 0,0206 0,182 0,890 0,0206 0,182 BBc 0,100 2,400 0,0319 0,211 2,400 0,0320 0,211 BBd 0,100 2,240 0,0229 0,154 2,240 0,0229 0,154 Blanko 0,00 0,0000 0,122 C1 0,3464 4,820 0,1510 0,707 4,820 0,1490 0,709 C2 0,3484 5,090 0,8520 0,742 5,140 0,8520 0,741 C3 0,3663 5,030 2,2140 0,610 5,030 2,2700 0,609 C4 0,3391 4,470 0,6140 0,663 4,470 0,6140 0,656