PERBANDINGAN AKTIVITAS ANTIBAKTERI AIR SEDUHAN
CACING TANAH DENGAN AIR SEDUHAN KAPSUL BUBUK
CACING TANAH (
Lumbricus rubellus
) TERHADAP
PERTUMBUHAN BAKTERI
Escherichia coli
.
KARYA TULIS ILMIAH
Diajukan Sebagai Salah Satu Syarat Untuk Menyelesaikan Pendidikan Diploma III Farmasi
Oleh
MUHAMMAD FAUZAN
1410121221029
AKADEMI FARMASI DWI FARMA
BUKITTINGGI
KATA PENGANTAR
Dengan menyebut nama Allah SWT yang Maha Pengasih lagi Maha
penyayang, saya panjatkan puja dan puji syukur atas kehadiran-Nya, yang telah
melimpahkan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan
penelitian dan penulisan Karya Tulis Ilmiah dengan judul ”PERBANDINGAN
AKTIVITAS ANTIBAKTERI AIR SEDUHAN CACING TANAH DENGAN
AIR SEDUHAN KAPSUL BUBUK CACING TANAH (Lumbricus rubellus)
TERHADAP PERTUMBUHAN BAKTERI Escherichia coli. yang merupakan
salah satu syarat untuk menyelesaikan pendidikan Diploma III Farmasi di Akademi
Farmasi Dwi Farma Bukittinggi.
Pada kesempatan ini penulis ingin menyampaikan ucapan terimakasih kepada:
1. Ibu Dra. ‘Ainun Naim, M.Farm, Apt selaku Direktur Akademi Farmasi Dwi
Farma Bukittinggi.
2. Bapak Budi Setiawan, M.Farm, Apt selaku pembimbing I yang telah
meluangkan waktu, tenaga, pikiran dan dengan penuh kesabaran memberikan
masukan, bimbingan, dorongan dan arahan sehingga penulis dapat
menyelesaikan penelitian dan penulisan Karya Tulis Ilmiah.
3. Ibu Zulfisa, S.Si, M.Farm selaku pembimbing II yang telah meluangkan
waktu, tenaga, pikiran dan dengan penuh kesabaran memberikan masukan,
bimbingan, dan arahan selama penelitian dan penulisan, sehingga penulis
dapat menyelesaikan penelitian dan penulisan Karya Tulis Ilmiah.
4. Bapak Arfiandi, S.Si, M.Farm, Apt selaku kepala laboratorium mikrobiologi
yang telah memberikan izin untuk pemakaian labor dan alat-alatnya, sehingga
v
5. Bapak dan Ibu Dosen beserta Karyawan Akademi Farmasi Dwi Farma
Bukittinggi yang telah memberikan masukan dalam penelitian dan penulisan
Karya Tulis Ilmiah.
6. Orang tua dan keluarga yang selalu memberi semangat, dukungan dan doa
dalam menyelesaikan penelitian dan penulisan Karya Tulis Ilmiah.
7. Teman – teman seperjuangan dan semua pihak yang telah membantu dalam
penelitian dan penulisan Karya Tulis Ilmiah.
Semoga budi baik yang telah diberikan mendapat balasan yang setimpal dari
Allah SWT. Penulis menyadari bahwa Karya Tulis Ilmiah ini masih banyak terdapat
kekurangan dikarenakan keterbatasan ilmu pengetahuan penulis sendiri, untuk itu
penulis mengharapkan saran dan kritikan yang bersifat membangun dari semua pihak
demi kesempurnaan Karya Tulis Ilmiah. Terimakasih untuk semua yang telah
membantu penulisan semoga selalu diberkati oleh Allah SWT. Semoga Karya Tulis
Ilmiah ini memberikan manfaat bagi kita semua. Amiin.
Bukittinggi, Juli 2017
vi
Akademi Farmasi Dwi Farma Bukittinggi Karya Tulis Ilmiah, Juli 2017 MUHAMMAD FAUZAN
ABSTRAK
Perbandingan Aktivitas Antibakteri Air Seduhan Cacing Tanah Dengan Air Seduhan Kapsul Bubuk Cacing Tanah (Lumbricus rubellus) Terhadap
Pertumbuhan Bakteri Escherichia coli
Xii + 19 Halaman + Daftar Pustaka + Lampiran
Telah dilakukan penelitian Perbandingan Aktivitas Antibakteri Air Seduhan Cacing Tanah Dengan Air Seduhan Kapsul Bubuk Cacing Tanah (Lumbricus rubellus) Terhadap Pertumbuhan Bakteri Escherichia coli dengan metoda dilusi cair menggunakan seri konsentrasi 32; 24; 16; 8 %. Hasil penelitian menunjukan bahwa untuk bakteri Escherichia coli pada air seduhan cacing tanah dapat dihambat pada konsentrasi 16 %, sedangkan pada air seduhan kapsul bubuk cacing tanah dihambat pada konsentrasi 24 %. Dapat disimpulkan bahwa air seduhan cacing tanah dan air kapsul bubuk cacing tanah memiliki efek yang berbeda dalam menghambat pertumbuhan bakteri Escherichia coli.
vii
DAFTAR LAMPIRAN xi
DAFTAR TABEL xii
DAFTAR GAMBAR xiii
1. PENDAHULUAN
1.1. Latar Belakang 1
1.2. Perumusan Masalah 2
1.3. Tujuan Penelitian 2
1.4. Manfaat Penelitian 2
II. TINJAUAN PUSTAKA 3
2.1 Tinjauan Biologi Cacing Tanah 3
2.1.1 Klasifikasi Cacing Tanah 3
2.1.2 Marfologi Cacing Tanah 3
2.2 Escherichia coli 4
2.2.1 Klasifikasi Escherichia coli 4
2.2.2 Morfologi Escherichia coli 5
2.3 Sterilisasi 6
2.4 Fase Pertumbuhan Mikroorganisme 7
2.5 Media 8
2.6 Metode Dilusi 9
2.7 Standar Mc. Farland 9
viii
III. METODOLOGI PENELITIAN 11
3.1 Waktu dan Tempat Penelitian 11
3.2 Alat dan Bahan 11
3.2.1 Alat 11
3.2.2 Bahan 11
3.3. Sampel dan Teknik Sampel 12
3.3.1 Pengambilan Sampel 12
3.3.2 Pembuatan sampel uji (Lumbricus rubellus) kering 12
3.3.3 Pengolahan Sampel 13
3.4 Sterilisasi 14
3.5 Peremajaan Bakteri 14
3.6 Pembuatan Larutan Mc. Farland 0,5 14
3.7 Pembuatan Suspensi Bakteri 15
3.8 Pembuatan Nutrient Broth 15
3.9 Pembuatan Konsentrasi Air Seduhan Cacing Tanah 15
3.10 Pembuatan Konsentrasi Air Seduhan Kapsul Bubuk Cacing Tanah 16
3.11 Teknik Pengumpulan Data 17
3.12 Teknik Analisa Data 17
ix DAFTAR PUSTAKA
x
DAFTAR LAMPIRAN
Lampiran Halaman
1. Skema Pengolahan Sampel Air Seduhan Cacing Tanah 23
2. Skema Pengolahan Sampel Air Seduhan Kapsul Bubuk Cacing Tanah 24
3. Skema Peremajaan Bakteri Escherichia coli menggunakan Nutrient Agar 25
4. Skema Kerja Pembuatan Mc.Farland 0,5 26
5. Skema Kerja Konsentrasi Hambat Minimum Air Seduhan Cacing Tanah 27
6. Skema Konsentrasi Hambat Minimum Air Seduhan kapsul Bubuk
Cacing Tanah(Lumbricus rubellus) 28
7. Pengamatan Konsentrasi Hambat Minimum (KHM) Air Seduhan Cacing
Tanah (Lumbricus rubellus) 29
8. Pengamatan Konsentrasi Hambat Minimum (KHM) Air Seduhan
xi
DAFTAR TABEL
Tabel Halaman
I. Tabel Pengamatan Konsentrasi Hambat Minimum Air Seduhan cacing tanah
(Lumbricus rubellus) 29
II. Tabel Pengamatan Konsentrasi Hambat Minimum Air Seduhan Kapsul
xii
DAFTAR GAMBAR
Gambar Halaman
1. Kurva Pertumbuhan Mikroorganisme 8
2. Skema pengolahan sampel Air Rebusan Cacing Tanah
(Lumbricus rubellus) 23
3. Skema Pengolahan Sampel Air Larutan Kapsul Bubuk Cacing Tanah
(Lumbricus rubellus) 24
4. Skema kerja peremajaan bakteri. 25
5. Skema kerja pembuatan Mc.Farland 0,5 26
6. Skema Kerja Konsentrasi Hambat Minimum (KHM) Air Seduhan Cacing
Tanah ( Lumbricus rubellus) 27
7. Skema Kerja Konsentrasi Hambat Minimum (KHM) Air Seduhan Kapsul
Bubuk Cacing Tanah 28
8. Tabel Pengamatan Konsentrasi Hambat Minimum (KHM) Air Seduhan
Cacing Tanah ( Lumbricus rubellus) 29
9. Tabel Pengamatan Konsentrasi Hambat Minimum (KHM) Air Seduhan
Kapsul Bubuk Cacing Tanah (Lumbricus rubellus) 30
10.Hasil Uji Dilusi Tabung Air Seduhan Cacing Tanah Terhadap Bakteri
Escherichia coli 31
11.Hasil Uji Dilusi Tabung Air Seduhan Kapsul Bubuk Cacing Tanah Terhadap
1
I. PENDAHULUAN
1.1 Latar Belakang Masalah
Diare merupakan salah satu masalah kesehatan yang paling sering terjadi pada
anak-anak diberbagai Negara termasuk Indonesia. Diperkirakan lebih dari 1,3 miliar
kasus dan diperkirakan 3,2 juta kematian per tahun pada balita disebabkan oleh diare.
Tingginya angka kejadian diare akibat infeksi bakteri Escherichia coli yang disertai
dengan kasus resistensi bakteri. Masyaraka mengupayakan mencari Pengobatan
alternatif sebagai antibakteri. (Widoyono, 2008) Penelitian mengenai zat yang
berkhasiat sebagai antibakteri selalu dilakukan untuk menemukan produk antibiotik
dengan harga yang terjangkau. Pemanfaatan bahan alam sebagai obat tradisional di
Indonesia mengalami peningkatan dengan adanya isu kembali ke alam, selain itu
antibiotik yang beredar di pasaran relatif harganya mahal dan menyebabkan
menurunnya daya beli masyarakat (Ilham, 1999).
Salah satu obat tradisional yang dapat dimanfaatkan sebagai obat anti diare
adalah cacing tanah, cacing tanah yang digunakan adalah jenis (Lumbricus rubellus).
Senyawa kimia yang terdapat pada cacing tanah yaitu lumbricin, lumbricin
merupakan zat bioaktif mikroba baru yang di isolasi dari cacing tanah, senyawa ini
diduga memiliki aktivitas antibakteri. (cho, dkk. 19985)
Berdasarkan penelitian sebelumnya menyatakan bahwa air rebusan cacing tanah
menggunakan metoda cetak lobang didapatkan zona hambat pertumbuhan bakteri
pada konsentrasi terkecil yaitu 20%. Sehingga peneliti tertarik untuk melakukan
penelitian tentang perbandingan aktivitas antibakteri air seduhan cacing tanah dengan
2
1.2. Rumusan Masalah
Berdasarkan latar belakang masalah diatas, maka rumusan masalah dari
penelitian ini adalah :
1. Berapakah Konsentrasi hambat minimum (KHM) dari air seduhan cacing
tanah dan air seduhan kapsul bubuk cacing tanah (Lumbricus rubellus).
2. Membandingkan mana yang lebih efektif dalam menghambat pertumbuhan
bakteri Escherichia coli antara air seduhan cacing tanah dengan air seduhan
bubuk kapsul cacing tanah.
1.3. Tujuan Penelitian
Untuk mengetahui seberapa besar konsentrasi hambat minimum (KHM)air
seduhan cacing tanah (Lumbricus rubellus) dan air seduhan kapsul bubuk cacing
tanah (Lubricus rubellus) serta menentukan mana yang lebih efektif dalam
menghambat pertumbuhan bakteri Esherichia coli.
1.4. Manfaat Penelitian.
1. Untuk memberikan informasi kepada masyarakat tentang manfaat air seduhan
cacing tanah (Lumbricus rubellus) sebagai obat alternatif dalam terapi
penyembuhan diare.
2. Manfaat bagi peneliti sendiri agar dapat mengaplikasikan ilmu yang di
3
II. TINJAUAN PUSTAKA
2.1 Tinjauan Biologi Cacing Tanah (Lumbricus rubellus)
2.1.1 Klasifikasi Cacing Tanah
Kingdom : Animalia
Filum : Annelida.
Kelas : Oligochaeta.
Ordo : Torriselae.
Family : Lumbricidae.
Genus : Lumbricus.
Spesies : Lumbricus rubellus.
(Kastawi, dkk, 2001)
2.1.2 Morfologi Cacing Tanah (Lumbricus rubellus)
Cacing tanah yang termasuk phylum annelida, tubuhnya bersegmen-segmen.
Hidup dalam tanah yang lembab dan umumnya hidup bebas. Tubuhnya juga tertutup
kutikula yang merupakan hasil sekresi dari epidermis, sudah mempunyai, sistem
cardiovaskular dan sudah ada rongga tubuh (coelom). (Kastawi, dkk, 2001).
Cacing tanah (Lumbricus rubellus) mempunyai bentuk tubuh pipih. Jumlah
cincin yana yang melingkari tubuhnya (segmen) yang dimiliki sekitar 90-195 buah
4
rubellus merupakan cacing yang berukuran relatif kecil dengan panjang sekitar 4-6
cm, bagian punggungnya berwarna merah coklat atau merah violet. Selain itu cacing
ini juga memiliki warna pelangi dan pada umumnya Lumbricus rubellus akan
mencapai usia dewasa pada umur 179 hari, sedangkan umurnya sampai 2,5 tahun
(Dewangga, 2009).
2.2 Escherichia coli
2.2.1 Klasifikasi
Kingdom : Bacteria.
Devisi : Proteobacteria.
Ordo : Enterobacteriales
Famili : Enterobacteriaceae.
Genus : Eschericha
5
2.2.2 Morfologi Escherichia coli
Escherichia coli merupakan bakteri batang gram negatif, tidak berkapsul,
umumnya mempunyai fibria dan bersifat motil. Sel Escherichia coli mempunyai
ukuran panjang 2,0-6,0 mm dan lebar 1,1-1,5 mm, tersusun tunggal. Bakteri ini
tumbuh pada suhu antara 10-40 °C, dengan suhu optimum 37ºC. pH optimum untuk
pertumbuhan adalah pada 7,0-7,5, pH minimum pada pH 9,0 (Anonim, 2007).
Esherichia coli termasuk ke dalam golongan bakteri gram negatif, sifat dari
bakteri ini yang membedakan dengan Bakteri lainnya adalah susunan dinding selnya.
Dinding sel bakteri gram positif berlapis tunggal dengan kandungan lipid 1-4%,
sedang pada bakteri gram negatif dinding selnya berlapis tiga yang terdiri dari
lipoprotein, membran luar fosfolipid dan lipopolisakarida, dan kandungan lipid pada
dinding sel berkisar antara 11-22%. Escherichia coli dapat bertahan hingga suhu
60ºC selama 30 menit (Collier, L., 1998).
2.3 Sterilisasi
Sterilisasi adalah menghilangkan semua bentuk kehidupan baik bentuk patogen,
non patogen, vegetatif, maupun non vegetatif dari suatu objek atau material. Hal
tersebut dicapai melalui cara penghilangan secara fisik semua organisme hidup,
misalnya penyaringan atau pembunuhan organisme dengan panas atau dengan cara
6 Sterilisasi dapat dilakukan dengan cara berikut :
1. Pemanasan basah
Teknik sterilisasi ini menggunakan uap air yang disertai dengan tekanan
yang dilakukan dengan alat yang disebut autoklaf.
2. Pemanasan kering
Cara ini dilakukan dengan cara pembakaran, cara ini biasa dipergunakan
untuk mensterilkan alat penanaman kuman (sangkelit atau ose) yaitu
dengan membakarnya hingga pijar.
3. Sterilisasi dengan panas udara
Alat-alat yang akan disterilan dengan cara ini, ditempatkan didalam oven
dimana suhunya dapat mencapai 160-180ºC selama 1-2 jam.
4. Penyaringan
Penyaringan dilakukan untuk mensterilkan substansi yang peka terhadap
7
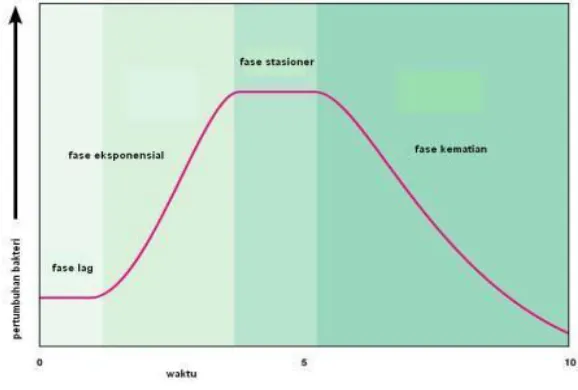
2.4Fase Pertumbuhan Mikroorganisme
Fase petumbuhan mikroorganisme dapat dibagi menjadi 4 :
1. Fase lag
Merupakan fase adaptasi yaitu fase penyesuain mikroorganisme pada
suatu lingkungan baru. Ciri fase lag adalah tidak adanya peningkatan
jumlah sel yang ada hanyalah peningkatan ukuran sel.
2. Fase log/Pertumbuhan eksponensial
Fase dimana mikroorganisme tumbuh dan membela pada kecepatan
maksimum, tergantung pada genetika mikroorganisme, sifat media
dan kondisi pertumbuhan.
3. Fase stasioner.
Pada fase ini pertumbuhan mikroorganisme terhenti dan terjadi
keseimbangan antar jumlah sel yang membelah dan jumlah sel yang
mati. Pada fase ini akan terjadi akumulasi produk buangan yang
toksik.
4. Fase penurunan populasi/fase kematian.
Pada fase kematian jumlah sel yang mati akan meningkat. Faktor
penyebabnya adalah ketidak seimbangan nutrisi dan akumulasi
8
Gambar 1. Kurva Pertumbuhan Mikroorganisme (Anonim, 2007)
2.5 Media
Media adalah suatu substrat untuk menumbuhkan dan mengembang biakan
mikroba. Sedangkan media itu sendiri sebelum digunakan harus dalam keadaan
steril, artinya tidak ditumbuhi oleh mikroba lain yang tidak diharapkan. (Suriawiria,
Unus, 1985)
Contoh media :
Nutrient Broth (NB)
Ektrak daging 3 gram
Pepton 5 gram
Aqua dest 1000 ml
9
Konsentrasi minimum suatu agen anti mikroba untuk dapat menghambat
pertumbuhan mikroorganisme. Pada metoda ini digunakan agen antimikroba dari
kadar terendah hingga tertinggi dan di tanamkan pada media cair yang telah di
tumbuhi mikroorganisme. Metoda ini mengukur MIC (Minimum Inhibitior
Concentration) atau KHM (Konsentrasi Hambat Minimum), cara yang digunakan
adalah membuat seri pengenceran agen antimikroba pada medium cair yang di
tambahkan dengan mikroba uji. Selanjutnya tabung di inkubasi di suhu 37ºC selama
18-24 jam dan di amati kekeruhan pada tabung (Pratiwi, 2008).
2.7 Standar Mc. Farland 0,5
Mc.Farland adalah penyetaraan konsentrasi mikroba dengan menggunakan
BaCl2 1% dan H2SO4 1%. Standar kekeruhan Mc.Farland ini dimaksudkan untuk
menggantikan perhitungan bakteri satu per satu dan untuk memperkirakan kepadatan
10 Berikut skala Mc.Farland
Skala Mc.Farland BaCl2 1%(ml) H2SO4 1% (ml) Cfu (x106/ml)
0,5 0,05 9,95 <300
Standar Mc.Farland tersedia di pasaran (Sutton, 2011)
2.8. Hipotesa
Hipotesa dari penelitian ini adalah air seduhan bubuk cacing tanah dan air
seduhan kapsul bubuk cacing tanah (Lumbricus rubellus) mempunyai aktivitas dalam
11
III. METODOLOGI PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan Maret sampai Juli 2017 di Labotorium
Mikrobiologi Akademi Farmasi Dwi Farma Bukittinggi.
3.2 Alat dan Bahan
3.2.1 Alat
Erlenmeyer, tabung reaksi, inkubator, lampu spiritus, gelas ukur, timbangan
digital, corong, batang pengaduk, jarum ose, autoklaf, pipet tetes, oven, pinset,
kapas, lumpang, stamfer, thermometer, kertas perkamen, kerta saring wathman,
kertas label, gunting,lemari aseptis, botol vial, spatel, rak tabung reaksi.
3.2.2 Bahan
Nutrien Agar (NA), Nutrient Broth (NB), Air Seduhan Cacing Tanah
(Lumbricus rubellus), Kapsul Bubuk Cacing Tanah (Lumbricus rubellus), aqua dest,
12
3.3 Sampel dan Teknik Sampel
3.3.1 Pengambilan Sampel
Sampel yang digunakan dalam penelitian ini adalah Cacing Tanah (Lumbricus
rubellus) kering dan Kapsul Bubuk Cacing Tanah (obat jadi) yang di peroleh dari
daerah Situjuh, Kabupaten Lima Puluh Kota Provinsi Sumatra Barat secara Simple
Random Sampling.
3.3.2 Pembuatan sampel uji (Lumbricus rubellus) kering
1. Pencucian I
Proses ini merupakan tahap awal yang bertujuan untuk membersihkan cacing
dari sisa-sisa tanah yang menempel di tubuh cacing.
2. Perebusan
Tahap selanjutnya adalah perebusan dimana proses ini adalah untuk
menghilangkan lendir dari cacing,
3. Pemotongan
Pemotongan disini bertujuan untuk mengeluarkan isi perut cacing biasanya di
cincang dengan panjang 3 cm.
4. Pencucian II
Setelah cacing di potong-potongdan agar lebih mudah untuk mengeluarkan isi
13
dalam air, tentunya akan lebih efektif jika kita mengaduk-aduknya dalam
larutan tersebut.
5. Pengeringan cacing tanah
Pengeringan adalah proses untuk mengurangi kadar air dalam tubuh cacing,
Proses ini dapat dilakukan dengan oven 40°C atau dengan cara tradisional
dengan cara menjemurnya dibawah terik matahari secara langsung.
6. Tepung cacing tanah.
Selanjutnya cacing tanah yang sudah kering dihaluskan dengan lumpang
hingga menjadi bubuk halus.
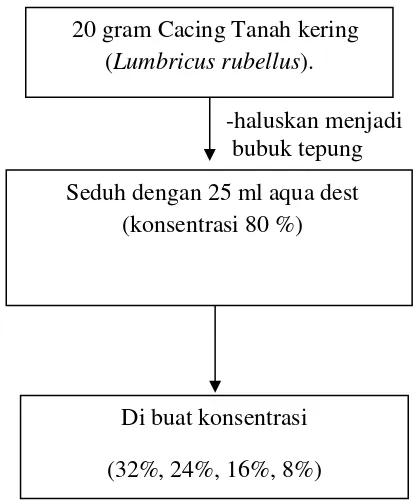
3.3.3 Pengolahan Sampel
Cacing tanah kering yang sudah dijadikan bubuk ditimbang sebanyak 20
gram, panaskan aqua dest hingga 90-98˚C. Seduh bubuk cacing tanah dengan aqua
dest yang telah dipanaskan, kemudian saring dan tambahkan aqua dest hingga 25 ml
sampai didapatkan konsentrsi 80%. Sedangkan untuk pengolahan kapsul cacing
14
3.4 Sterilisasi
Alat di cuci bersih terlebih dahulu dan di keringkan, pipet tetes di bungkus
dengan perkamen. Alat-alat bermulut seperti tabung reaksi di tutup dengan kapas
yang telah dilapisi dengan kain kasa, lalu bungkus dengan perkamen, lakukan
sterilisasi dengan autoklaf pada suhu 121°C selama 15 menit, jarum ose di pijar di
atas nyala lampu spiritus, meja dan lemari aseptis di sterilkan dengan cara di
bersihkan terlebih dahulu kemudian di semprot dengan etanol 70 %.
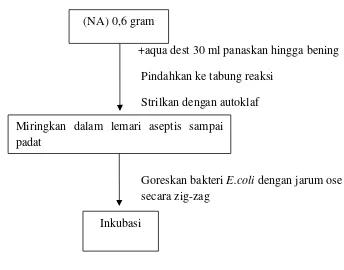
3.5 Peremajaan Bakteri Escherichia coli
Timbang Nutrient Agar (NA) 0,6 gram, tambahkan aqua dest ad 30 ml aduk
hingga larut dalam erlenmeyer, lalu panaskan hingga mendidih dan bening, masukan
ke tabung reaksi yang telah di kalibrasi 10 ml. Tutup padat tabung reaksi dan kapas
yang telah dilapisi dengan kain kasa kemudian sterilkan dengan autoklaf. Setelah di
sterilkan miringkan tabung reaksi di dalam lemari aseptis yang telah di semprot
etanol 70 %, tunggu sampai agar memadat, setelah padat oleskan bakteri Escherichia
coli menggunakan jarum ose, inkubasi selama 24 jam pada suhu 37°C dalam
inkubator.
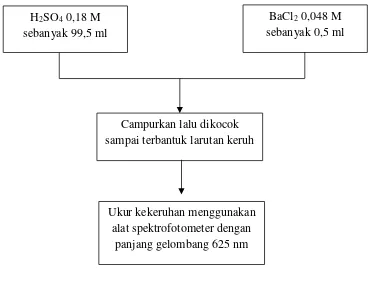
3.6 Pembuatan larutan Mc.Farland 0,5
Larutan H2SO4 1% sebanyak 99,5 ml dicampurkan dengan BaCl2 1% sebanyak
0,5 ml dalam labu ukur. Kemudian di kocok sampai terbentuk larutan yang keruh.
Kekeruhan ini dipakai sebagai standart kekeruhan suspense bakteri uji (BD BBL,
2010). Ukur kekeruhan dengan alat spektrofotometer dengan panjang gelombang
15
3.7 Pembuatan Suspensi Bakteri
Bakteri yang telah diremajakan dalam media agar, di ambil dengan jarum ose
yang telah di sterilkan, kemudian di suspensikan dengan 10 ml larutan NaCl
fisiologis steril dalam botol vial, kemudian di inkubasi 1-2 jam pada suhu 37°C.
Suspensi bakteri disamakan dengan standar Mc.Farland 0,5 dengan penambahan
NaCl fisiologis, ukur kekeruhan dengan menggunakan alat spektrofotometer dengan
absorban 0,08-0,1 panjang gelombang 600-625 nm.
3.8 Pembuatan Nutrient Broth
Timbang1,2 gram Nutrient Broth (NB) masukan ke Erlenmeyer tambahkan aqua
dest hingga 150 ml untuk 2 kali pengulangan (duplo). Panaskan hingga bening
dengan sesekali aduk, setelah bening pindahkan ke tabung reaksi yang
masing-masing telah di kalibrasi 5 ml dan tutup dengan kapas yang telah di balut dengan
kain kasa sterilkan dengan autoklaf.
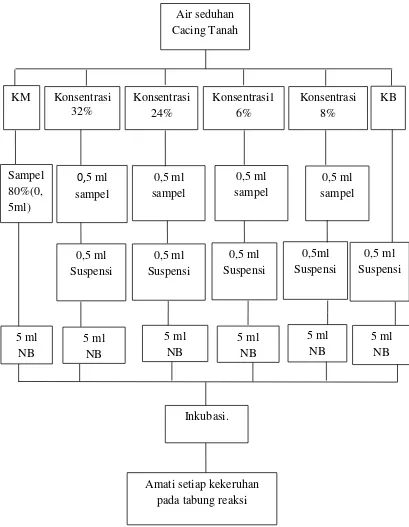
3.9 Pembuatan Konsentrasi air seduhan Cacing Tanah (Lumbricus rubellus)
Dari konsentrasi air rebusan cacing tanah 80% dilakukan pengenceran sebagai
berikut :
a. Konsentrasi 32%
Ambil larutan 80 % sebanyak 6ml, di tambahkan aqua dest ad 15 ml.
b. Konsentrasi 24%
16
c. Konsentrasi 16%
Ambil larutan 80% sebanyak 3 ml, di tambahkan aqua dest ad 15 ml.
d. Konsentrasi 8%
Ambil larutan 80% sebanyak 1,5 ml, di tambahkan aqua dest ad 15 ml
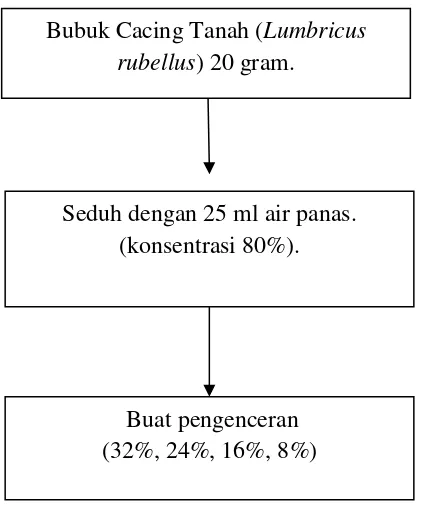
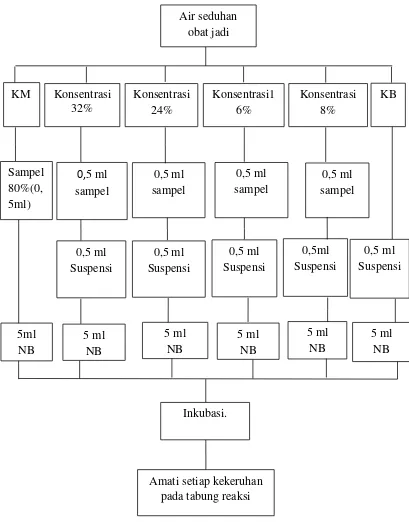
3.10 Pembuatan Konsentrasi air seduhan kapsul bubuk cacing tanah
(Lumbricus rubellus)
Dari konsentrasi air rebusan cacing tanah 80% dilakukan pengenceran sebagai
berikut :
1. Konsentrasi 32%
Ambil larutan 80% sebanyak 6 ml, di tambahkan aqua dest ad 15 ml.
2. Konsentrasi 24%
Ambil larutan 80% sebanyak 4,5ml, di tambahkan aqua dest ad 15 ml.
3. Konsentrasi 16%
Ambil larutan 80% sebanyak 3 ml, di tambahkan aqua dest ad 15 ml.
4. Konsentrasi 8%
17
3.11 Teknik Pengumpulan Data
Metode yang di gunakan dalam penelitian ini adalah metode dilusi tabung
dengan cara :
1. Siapkan 6 tabung reaksi untuk 1 sampel, beri label 1a-6a.
2. Pada tabung reaksi dengan label 1a kontrol media (Km) dan dengan
label 6a dan kontrol bakteri (Kb).
3. Tabung reaksi 2-5a untuk sampel dengan pengenceran yang berbeda.
4. Tambahkan 5 ml media Nutrient Broth ke seluruh tabung reaksi.
5. Dan tambahkan suspensi bakteri ke dalam tabung 2-6a sebanyak 0,5
ml.
6. Pada deretan tabung 2-5 masukan air seduhan cacing tanah dengan
hasil pengenceran yaitu 32%,24%,16% dan 8% masing-masing
sebanyak 0,5 ml.Tabung 1a diisi dari konsetrasi induk 80% sebanyak
1 ml
7. Seluruh tabung reaksi di inkubasi dalam inkubator selama 18-24 jam pada
suhu 37°C.
8. Kemudian amati kekeruhan pada setiap konsentrasi pada tabung reaksi
3.12 TeknikAnalisa Data
Menentukan pada konsentrasi berapa air seduhan cacing tanah dan air seduhan
bubuk kapsul cacing tanah (Lumbricus rubellus) dapat menghambat pertumbuhan
18
IV. HASIL DAN PEMBAHASAN
4.1 Hasil
Dari penelitian yang dilakukan maka didapatkan hasil sebagai berikut :
1. Air seduhan cacing tanah dan air seduhan kapsul cacing tanah memiliki efek
yang berbeda dalam menghambat petumbuhan bakteri Escherichia coli.
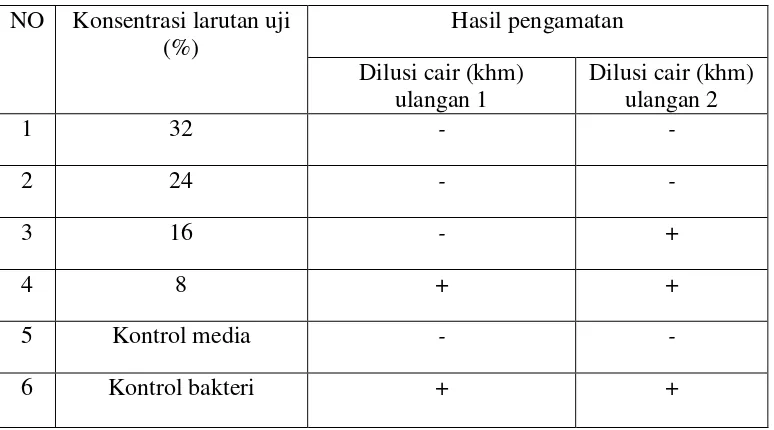
2. Konsentrasi hambat minimum (KHM) dari air seduhan cacing tanah yaitu
pada konsentrasi 16 %, sedangkan pada air seduhan kapsul cacing tanah
berada pada konsentrasi 24%.
4.2 Pembahasan
Pada penelitian ini sampel yang digunakan adalah cacing tanah jenis Lumbricus
rubellus dan kapsul bubuk cacing tanah yang didapatkan di daerah Situjuah,
Kabupaten Lima Puluh Kota Propinsi Sumatera Barat. Cacing tanah dipilih sebagai
antibakteri karena cacing tanah memiliki zat antimikroba yang dapat menghambat
pertumbuhan bakteri gram positif maupun negative (broad spectrum). (Khairumah
dan Khairul, 2009)
Dalam penelitian ini dilakukan pembiakan bakteri yang dimaksudkan untuk
memudahkan pemeriksaan yang akan dilakukan didalam Labotorium Mikrobiologi,
sehingga jika sewaktu-waktu kita memelukan bakteri untuk suatu percobaan maka
bakteri tersebut telah tersedia. Media yang digunakan untuk menumbuhkan bakteri
19
menggunakan media Nutrien Agar untuk menumbuhkan bakteri, karena Nutrien
Agar sudah memiliki nutrsi yang cukup untuk pertumbuhan bakteri.
Sebelum melakukan pembiakan bakteri, kita harus melakukan pengujian
kekeruhan suspensi bakteri yang akan dibiakan. Pengujian kekeruhan ini dilakukan
menggunakan standar Mc.Farland yang diuji dengan menggunakan alat
spektrofotometer UV-Vis. Kekeruhan ini diukur dengan panjang gelombang 625 nm
dan di peroleh absorbannya 0,091. Larutan yang telah dibuat disimpan dalam botol
gelap yang di lapisi dengan alumunium foil pada suhu kamar, larutan ini harus
dikocok terlebih dahulu sebelum dipakai. Dari hasil pengujian tersebut kekeruhan
Mc.Farland 0,5 sebanding dengan jumlah bakteri 1,5 x 108 sel/ml (Dalynn
Biological, 2014)
Selanjutnya kita melakukan pengujian untuk konsentrasi hambat minimum
(KHM) digunakan media Nutrient Broth. Pengujian aktifitas antibakteri air seduhan
cacing tanah dilakukan dengan cara dilusi tabung yang bertujuan untuk mengetahui
pada konsantrasi terkecil berapa sampel mampu menghambat bakteri. Penilian KHM
dengan menggunakan metode dilusi dinilai berdasarkan tingkat kekeruhan pada
setiap tabung setelah melalui masa inkubasi selama 18-24 jam dengan terbentuknya
warna jernih pada larutan. (Dzen, 2003)
Pada penelitian ini didapatkan konsentrasi hambat minimum air seduhan cacing
tanah terhadap bakteri Escherichia coli adalah pada konsentrasi 16% dan pada air
20
air seduhan cacing tanah murni lebih efektif dalam menghambat pertumbuhan
21
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Dari hasil penelitian yang dilakukan dapat disimpulkan bahwa air seduhan
cacing tanah (Lumbricus rubellus) lebih efektif dalam menghambat
pertumbuhan bakteri Escherichia coli.
2. Konsentrasi hambat minimum air seduhan cacing tanah pada konsentrasi 16%
sedangkan konsentrasi hambat minimum air seduhan kapsul cacing tanah
pada konsentrasi 24%
5.2 Saran
Disarankan untuk peneliti selanjutnya untuk melakukan pengujian uji KBM air
seduhan cacing tanah Lumbricu srubellus terhadap bakteri gram positif maupun
22
DAFTAR PUSTAKA
Agoes, G. (1920). Sediaan Farmasi Steril. Institut Teknologi Bandung.
Anonim, 2007, Ecsherichia coli, http://www.wikipedia.com, diakses
24 November 2016
BD BBL.(2010).Mc.Farland Turbity standart no 0,5.
Cho, J, H., C.B.Park, Y.G. Yoon & S.C.Kim. 1998.Lumbricin I, a novel proline-rich antimicrobial peptide from the earthworm : purification , cDNA cloning and moleculer characterization. Biochim. Biophys. Acta 1408 : 67-76.[Abstr. ].
Collier, L.,1998, Microbiology and Microbial Infections, Edisi 9, 935–939, Oxford University Press, Inc., New York.
Dewangga,A.G.(2009).Pengaruh Penggunaan Tepung Cacing Tanah (Lumbricus
rubellus) Terhadap Kecernaan Bahan Kering dan Bahan Organic Ransum
Domba Local Jantan. Skripsi Fakultas Pertanian Universitas Sebelas Maret
Surakarta : Surabaya.
Dalynn Biologicals. (2014).Mc.Farland standar for in vitro use only.
Himedia, (2011). Technical Nutrient Broth, Nutrient Agar. Mumbai.India.
Ilham, K. 1999. Pengaruh pemberian ekstrak biji pepaya (Carica papaya) terhadap
ginjal dan hati mencit (Mus musculus). Hibah Penelitian Dana Rutin. Biologi FMIPA, Padang: Lembaga Penelitian Universitas Andalas.
Kastawi, Y, Sri E. I. Ibrohim. Masjhudi, dan Sofia E. R. (2001). Common Textbook
Pratiwi , S. T. (2008). Mikrobiologi Farmasi. Erlangga .Yogyakarta.
Suriawina, U. (1985), Pengantar Mikrobiolgi Umum, Angkasa. Bandung.
Syahrurachman, A. 1994. Mikrobiologi Kedokteran, Binarupa Angkasa : Jakarta
Sutton, S. 2011. Measurement of Microbial Cells by Optical Density. Journal Of
Validation Technology XVII
Widoyono, (2008).Penyakit Ttropis, Epidemiologi, penularan, pencegahan dan
23
Lampiran 1. Skema pengolahan sampel Air Seduhan Cacing Tanah
(Lumbricus rubellus)
-haluskan menjadi bubuk tepung
Gambar 2. Skema pengolahan sampel Air Rebusan Cacing Tanah
(Lumbricus rubellus)
20 gram Cacing Tanah kering (Lumbricus rubellus).
Seduh dengan 25 ml aqua dest (konsentrasi 80 %)
Di buat konsentrasi
24
Lampiran 2. Skema pengolahan sampel Air Bubuk Cacing Tanah
(Lumbricus rubellus)
Gambar 3.Skema Pengolahan Sampel Air Larutan Kapsul Bubuk Cacing Tanah (Lumbricus rubellus)
Bubuk Cacing Tanah (Lumbricus
rubellus) 20 gram.
Seduh dengan 25 ml air panas. (konsentrasi 80%).
25
Lampiran 3. Skema Peremajaan Bakteri Escherichia coli Menggunakan Nutrient Agar
+aqua dest 30 ml panaskan hingga bening
Pindahkan ke tabung reaksi
Strilkan dengan autoklaf
Goreskan bakteri E.coli dengan jarum ose secara zig-zag
Gambar 4. Skema kerja peremajaan bakteri.
(NA) 0,6 gram
Miringkan dalam lemari aseptis sampai padat
26
Lampiran 4. Skema kerja pembuatan Mc.Farland 0,5
Gambar 5. Skema kerja pembuatan Mc.Farland 0,5
H2SO4 0,18 M sebanyak 99,5 ml
BaCl2 0,048 M sebanyak 0,5 ml
Campurkan lalu dikocok sampai terbantuk larutan keruh
Ukur kekeruhan menggunakan alat spektrofotometer dengan
27
Lampiran 5. Skema kerja Konsentrasi hambat minimum (KHM) Air Seduhan Cacing Tanah.
28
Lampiran 6. Skema kerja Konsentrasi Hambat Minimum (KHM) Air SeduhanBubuk kapsul Cacing Tanah.
Gambar 7. Skema Kerja Konsentrasi Hambat Minimum (KHM) Air Seduhan Kapsul Bubuk Cacing Tanah
29
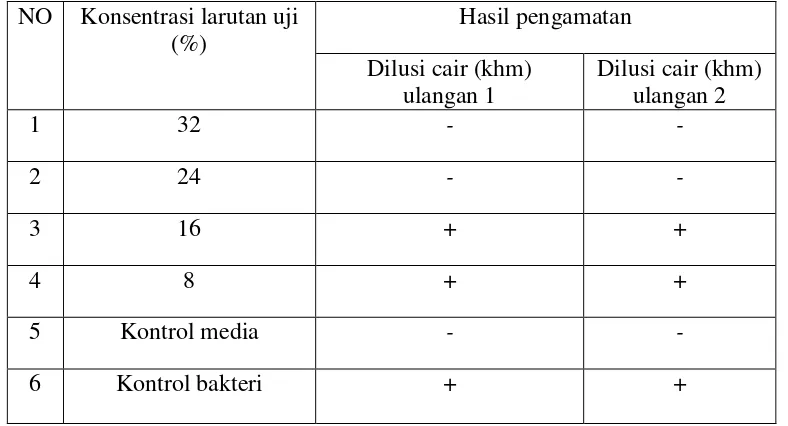
Lampiran 7. Pengamatan Konsentrasi Hambat Minimum (KHM)
Tabel I. Tabel Pengamatan Konsentrasi Hambat Minimum (KHM)
air seduhan cacing tanah Lumbricus rubellus
NO Konsentrasi larutan uji (%)
Gambar 8. Tabel Pengamatan Konsentrasi Hambat Minimum (KHM)
30
Lampiran 8. Pengamatan Konsentrasi Hambat Minimum (KHM)
Tabel II. Tabel Pengamatan Konsentrasi Hambat Minimum (KHM)
Air Seduhan Kapsul BubukCacing Tanah (Lumbricus rubellus)
NO Konsentrasi larutan uji (%)
Gambar 9. Tabel Pengamatan Konsentrasi Hambat Minimum (KHM)
31
Lampiran 9. Hasil Uji Dilusi Tabung Air Seduhan Cacing Tanah Terhadap BakteriEscherichiacoli
Gambar 10. Hasil Uji Dilusi Tabung Air Seduhan Cacing Tanah
32
Lampiran 10. Hasil Uji Dilusi Tabung Air Seduhan Kapsul Cacing Tanah
Terhadap Bakteri Escherichiacoli
Gambar 11. Hasil Uji Dilusi Tabung Air Seduhan Kapsul Bubuk Cacing Tanah