LEMBAR KERJA PRAKTIKUM
Penilaian Pre-test Konsultasi ke-1*)
Konsultasi ke-2*)
Konsultasi ke-3*)
Konsultasi ke-4*)
Nilai Laporan Akhir Pemahaman teori Lulus / Gagal Lulus / Gagal Lulus / Gagal Lulus / Gagal
Kesesuaian skema kerja Lulus / Gagal Lulus / Gagal Lulus / Gagal Lulus / Gagal
Kesesuaian form data pengamatan Lulus / Gagal Lulus / Gagal Lulus / Gagal Lulus / Gagal
Nilai Pre-test 100 90 80 60
Keterangan : *) lingkari salah satu pilihan yang sesuai ** )lingkari salah satu nilai terakhir waktu konsultasi
IDENTIFIKASI OBAT
KELOMPOK 1
NAMA NIM
Edwin Widiantoro I1C015001
Jeremy Tandy Yanuansah I1C015009
Abdillah Hanif Al Faruqi I1C015017
Rezky Oktovision L I1C015025
Faizah Ashlah I1C015033
Novi Amalia Nursyafitri I1C015041
Luvita Nadya Ningrum I1C015049
Nada Subuh Yatitis I1C015053
DOSEN JAGA PRAKTIKUM: Ade Martinus, M.Sc.
LABORATORIUM KIMIA FARMASI
JURUSAN FARMASI
FAKULTAS ILMU-ILMU KESEHATAN
UNIVERSITAS JENDERAL SOEDIRMAN
Hasil
Diteteskan dengan alcohol Ditambah pereaksi parri Dibasakan dengan amoniak Vitamin C
Hasil
Direduksi dengan pereaksi baifoed dan luff Vitamin C
Hasil 1. Organoleptis
2. Kelarutan
3. Flourosensi Dibawah UV
4. Analisis Pendahuluan a. Golongan Karbohidrat
b. Golongan Fenol
c. Golongan Anilin
5. Reaksi Khusus
-Dibentuk serbuk dalam larutan -Dilihat dibawah sinar UV
-Dilarutakan pada NaOH -Dipanaskan
-Ditambahkan larutan FeCl3
-Ditambahkan etanol
-Ditambahkan NaOH + Etanol -Dipanaskan
-Dilihat
-Diraba menggunakan ujung jari -Dibau
-Dirasakan -Dicatat
-Dilarutkan dalam pelarut organic/anorganik
-Ditambahkan 1-2 tetes FeCl3
-Dipanaskan hingga warna menjadi violet
-Ditambahkan etanol dan H2SO4 pekat
-Dididihkan
-Didinginkan&ditambahkan air kedalam tabung reaksi hingga penuh
-Dilarutkan 10mg zat paracetamol kedalam 10ml air -Ditambahkan 1 tetes larutan FeCl3
-Diamati perubahan warna
-Ditambahkan 1ml NaOH 3N -Dipanaskan kemudian didinginkan
-Ditambahkan 1ml asam sulfanilat&beberapa tetes larutan nitrit
-Diamati
Asam Benzoat
10 mg zat dilarutkan dalam 5ml air
Dipanaskan kemudian disaring setelah dingin
Filtrat
Ditambah 4-5 tetes FeCl3
Hasil
Talk dan bolus
Ditambahkan Na bikarbonat, dibakar Ditambahkan HCl hingga larut Ditambahkan NaOH hingga alkalis
Ditambahkan titan yellow/ditambah H2SO4 pekat
Dididihkan kemudian dicuci dengan air Diamati Kristal menggunakan mikroskop
f.
6. Reaksi Penjurusan
Amilum, Gula cair, Gula pasir, Laktosa
Masing-masing ditambahkan Fehling A dan B, Barfoed, dan Luff
Dipanaskan
Diamati perubahan yang terjadi (ada 12 pengamatan)
TABEL PENGAMATAN
A.Uji Organoleptis
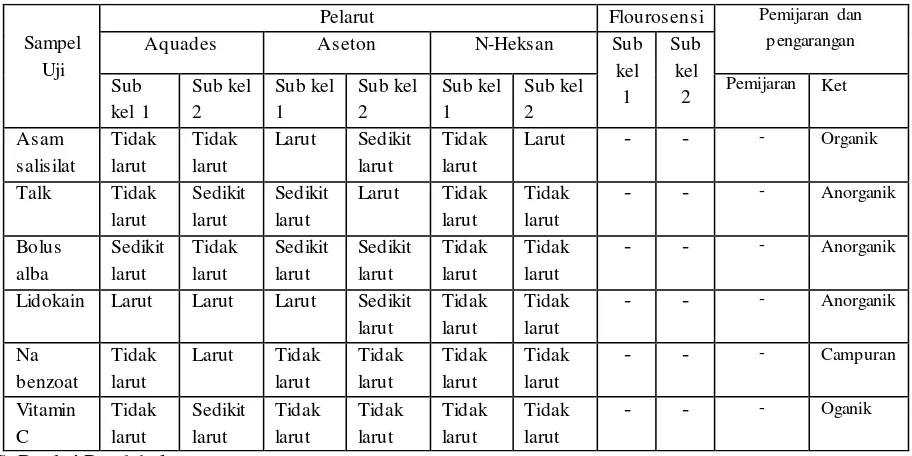
B.Uji Kelarutan, Flourosensi dan Pemijaran Pengarangan
C.Reaksi Pendahuluan
Sampel
Pelarut Flourosensi Pemijaran dan pengarangan
Larut Sedikit larut
Sampel Uji
Analisis Pendahuluan
Gol Karbohidrat [Perub. Warna]
Lidokain Bening putih (-)
Paracetamol Bau
busuk (+)
Bau bususk (+)
D.Reaksi Penjurusan
Sampel Uji
Reagen Fehling A dan B
Barfoed Luff Sebelum Pemanasan
E. Reaksi Khusus
Sampel Uji Hasil Terbentuk Warna
Sub Kel 1 Sub kel 2
As. Salisilat + FeCl3 Ungu Ungu
Paracetamol + Air + FeCl3 Ungu Ungu
Na Benzoat + Air + FeCl3 Putih tulang Coklat kemerahan
Vitamin C + Barfoed Coklat Hitam
Vitamin C + Luff Oren Kuning
Amylum + Yodium Ungu Ungu
Pembahasan
kemungkinan disebabkan praktikan terlalu banyak melarutkan zat tersebut hingga lewat jenuh, sehingga menjadi tidak dapat terlarut. Sedangkan pada asam salisilat, praktikan terlalu banyak memberi pelarut N-heksan, sehingga asam salisilat yang semi polar menjadi larut pada pelarut non polar. Pada uji pengarangan, didapat hasil bahwa vit C, asam salisilat dan amilum merupakan senyawa organik, ditandai dengan terbentuknya arang hitam hasil pembakaran disebabkan senyawa tersebut memiliki atom karbon. Sedangkan pada pemijaran, Na-Benzoat menghasilkan pijaran api berwarna kuning, disebabkan adanya elemen logam dari kation Na+ .
Pengujian ini dilakukan untuk mengetahui senyawa obat yang kita uji termasuk golongan karbohidrat, fenol/salisilat atau termasuk golongan anilin. Adapun senyawa obat yang diuji adalah Bolus Alba, Asam Salisilat, Vitamin C, Lidokain, Talkum, dan Natrium Benzoat. Untuk mengetahui termasuk golongan mana senyawa obat tersebut berikut prosedur pengujian berdasarkan golongannya. Analisis golongan karbohidrat dilakukan dengan cara senyawa menambahkan larutan NaOH, kemudian dipanaskan akan terjadi warna kuning. Setelah dilakukan percobaan, tidak ada senyawa obat yang termasuk dalam golongan karbohidrat. Hal ini sesuai dengan literatur, karena memang tidak ada senyawa obat yang tergolong dalam senyawa obat (Depkes RI, 1995). Analisis golongan fenol/salisilat dilakukan dengan cara menambahkan larutan FeCl3 pada senyawa obat sehingga terjadi warna ungu-bir u. Setelah dilakukan percobaan, senyawa obat yang positif menimbulkan warna tersebut yaitu asam salisilat. Hal ini sesuai dengan literatur asam salisilat termasuk golongan fenol, yakni pada pemeriksaan kualitatif, reaksi besi (III) klorida memberikan warna ungu (Auterhoof dan Kovar, 1987). Terbentuknya senyawa kompleks antara Fe+3 dengan fenol. Fenol memilik i gugus hidroksil yang terikat pada rantai karbon tak jenuh sehingga dapat bereaksi dengan besi (III) klorida (Sudjadi dan Rohman, 2004). Warna ini disebabkan oleh adanya transisi elektronik dari kompleks tersebut. Dimana kompleks ini menunjukkan warna komplementernya karena atom pusatnya memiliki orbital d yang masih belum terisi penuh elektron. Adanya orbital d yang belum terisi penuh ini menyebabkan kemungkinan terjadinya transisi elektronik dari orbital d yang tingkat energinya lebih rendah ke orbital d yang tingkat energinya tinggi. Dan banyaknya pasangan elektron bebas pada senyawa tersebut sehingga dapat membentuk senyawa kompleks. Struktur kompleks ini adalah oktahedral (Banerjee, S., Haldar,B.C., 1950). Adapun reaksi pembentukan senyawa kompleks yaitu
menimbulkan bau busuk yaitu Paracetamol. Sehingga dapat dikatakan paracetamol termasuk senyawa golongan anilin. Hal ini sesuai dengan literatur (Depkes, 1995).
Reaksi penjurusan pada praktikum kali ini menggunakan reagen Fehling A dan B, Barfoed, luff untuk membedakan adanya laktosa dan glukosa serta kandungan gula terduksi monosakarida atau disakarida (Keenan,1986). Sampel yang digunakan yaitu gula pasir, gula cair, amilum, dan laktosa. Masing-masing sampel diuji menggunakan fehling A dan B kemudian dipanaskan. Gula pasir, gula cair dan laktosa menghasilkan warna coklat bata-merah bata yang positif terhadap pereaksi fehling karena ion Cu2+ pada fehling direduksi menjadi ion Cu+ yang dalam suasana basa berubah menjadi warna coklat-merah bata. Amilum dihasilka n endapan biru yang negative terhadap pereaksi fehling karena amilum merupakan polisakarida yang tidak dapat bereaksi positif dengan fehling. Amilum bukan gula pereduksi dan tidak memiliki gugus aldehid dan keton bebas sehingga tidak terjadi oksidasi antara amilum+fehl ing. Uji fehling pada sub kelompok 2 dihasilkan perubahan yang tidak jauh berbeda. Pada uji barfoed gula pasir dan gula cair menghasilkan endapan merah dan warna coklat kemerahan setelah diberi pereaksi barfoed dan dipanaskan hal tersebut sesuai dengan literatur bahwa uji barfoed positif dengan terbentuknya endapan merah. Larutan berfoed akan bereaksi dengan gula monosakarida pereduksi sehingga menghasilkan endapan merah (Sudarmadji,2010). Amilum dan laktosa pada uji barfoed menghasilkan biru tua setelah ditambah pereaksi barfoed dan dipanaskan. Hal tersebut menujukan bahwa amilum dan laktosa bukan gula pereduksi karena tidak ada endapan merah yang dihasilkan. Uji Luff bertujuan untuk menguji adanya gula pereduksi yang memiliki gugus aldehid. Reaksi positif pada uji luff ditandai dengan adanya endapan merah. Senyawa yang positif pada uji luff adalah gula pasir, gula cair dan laktosa. Reaksi yang terjadi adalah :
Reaksi khusus untuk mengidentifikasi parasetamol dengan dilarutkan dalam air dan ditambah FeCl3 menghasilkan warna ungu hasil tersebut sesuai dengan literatur . Warna ungu tersebut dapat muncul karena terbentuknya kompleks antara gugus hidroksil dengan ion besi (Aman, 2012) seperti pada gambar berikut :
susunan elektron pada amilosa. Perbedaan tingkat energi antara amilum dan yodium menyerap cahaya tampak dan membentuk kompleks warna ungu.
Identifikasi vitamin c dengan reagen barfoed menghasilkan warna hitam, hasil tersebut tidak sesuai dengan literature yang menyebutkan bahwa hasil positif reaksi dengan pereaksi barfoed adalah membentuk endapan merah bata. Pada dasarnya reagen barfoed adalah reagen untuk mengidentifikasi karbohirat. Ketika barfoed reagen dicampur dengan larutan monosakarida atau disakarida, dan dipanaskan dalam air panas, mereka bereaksi dan terbentuk endapan kristal . Tembaga asetat yang hadir dalam reagen barfoed ini dikonversi ke oksida tembaga dan memberikan bata endapan merah saat bereaksi dengan monosakarida atau disaccharides (Bucke,1999). struktur yang mirip antara karbohidrat dengan vitamin c yaitu mengandung atom C,H, dan O dapat menjadi alasan pemilihan reagen barfoed ini. Uji kualitatif asam askorbat dengan reagen luff tidak jauh berbeda, reagen tersebut untuk identifikasi adanya gugus aldehid (Bucke,1999). Hasil positif pada reagen luff akan menghasikan warna endapan merah bata. Pada reaksi tersebut terjadi reduksi CuO menjadi Cu2O. Cu2O ini kemudian membentuk endapan merah bata. Dan hasil praktikum ini tidak sesuai literature karena menghasilkan warna kuning padahal seharusnya terjadi warna merah bata karena dalam vitamin c terapat gugus aldehid. Perbedaan hasil kemungkinan karena tanpa proses pemanasan. Asam salisilat yang direaksikan dengan FeCl3 menghasilkan warna violet karena terjadi reaksi gugus fenol yang terdapat pada asam salisilat dengan FeCl3 yang membentuk kompleks dengan ion besi (III) yaitu Fe[Fe(OPh)6] dan hasil percobaan sesuai dengan literatur (Banerjee, S., Haldar,B.C., 1950).Filtrat dari larutan natrium benzoate dalam air yang ditambahkan FeCl3 terdapat endapan coklat. Hal ini sesuai dengan literature yang ada (Depkes RI, 1979)
Kesimpulan
Kesimpulan yang didapatkan dari praktikum kali ini adalah
1. Uji organoleptik, kelarutan, flourosensi, pemijaran dan pengarangan merupakan uji yang dilakukan untuk mengidentifikasi zat berdasarkan sifat fisika dan bukan melalui reaksi 2. Uji pendahuluan bertujuan untuk menentukan golongan senyawa yang diuji karena
setiap golongan memiliki struktur kimia yang berbeda dengan golongan lain
3. Uji penjurusan menggunakan fehling A dan B, barfoed, dan luff digunakan membedakan adanya laktosa dan glukosa serta kandungan gula tereduksi monosakarida atau disakarida 4. Uji reaksi khusus merupakan uji yang spesifik terhadap zat tertentu sehingga prosedur
Daftar Pustaka
Aman,tehseen.2012. Determination of two analgesics (acetyl salicylic acid and
acetaminophen) by a single chromogenic reagent, International Journal of Pharmaceutical Sciences Review and Research p 132.
Auterhoff, H., dan Kovark., 1987, Identifikasi Obat, Bandung, Penerbit ITB.
Awan, 2010, Konsep Dasar Analisis Kualitatif dan Kuantitatif,
http://awanl.blogspot.com/2010/11/konsep-dasar-analisis-kualitatif-dan.html, diakses
pada 23 September 2016
Banerjee, S., Haldar,B.C., 1950, Constitution of ferri-phenol complex in solution, Nature, 165, 1012.
Bucke,Christopher.1999.Carbohydrate Biotechnology Protocol.New Jersey. Humana Press. Diakses dari https://books.google.co.id pada 23 september 2016
Depkes RI, 1979, Farmakope Indonesia Edisi III, Departemen Kesehatan Republik Indonesia, Jakarta.
Depkes RI, 2014, Farmakope Indonesia Edisi Kelima, Jakarta, Departemen Kesehatan Republik Indonesia
Depkes, 1995, Farmakope Indonesia Edisi IV, Jakarta, Departemen Kesehatan Republik Indonesia.
Keenan, Kleinfelter. 1986. Kimia OrganikJilid 2. Jakarta. Erlangga
Sudarmadji, Slamet, 2010. Analisis Bahan Makanan dan Pertanian. Yogyakarta : Liberty Yogyakarta