Sifat, Karakteristik dan Fungsional
DAFTAR ISI
1. Karakteristik Umum ... 2
2. Benzoat Sebagai Bahan Pengawet ... 2
3. Benzoat Sebagai Senyawa Antioksidan dan Agen Anti-Browning ... 5
4. Regulasi dan Metabolisme Benzoat ... 6
5. Daftar Pustaka : ... 8
DAFTAR GAMBAR
Gambar 1. Efek Asam Benzoat Pada Escherichia coli (Bakteriostatik; Aktivitas Bakterisidal) dan Staphylococcus aureus ( Bakteriostatik; Aktivitas bakterisidal) ... 4Gambar 2. Penghambatan Aspergillus niger oleh Asam Benzoat; Asam p-hidroksibenzoat propil ester dan Asam Sorbat ... 4
Gambar 3. Struktur Benzoat dan Senyawa Turunannya ... 5
Gambar 4. Reaksi Pencoklatan Enzimatis ... 6
Gambar 5. Mekanisme Metabolisme Benzoat Dalam Tubuh (Betaria, 2012) ... 7
DAFTAR TABEL
Tabel 1. Kadar Maksimal Benzoat Pada Beberapa Produk Pangan ... 3Tabel 2. Pengaruh pH Pada Disosiasi Asam Benzoat ... 4
Semarang, Maret 2013
1.
Karakteristik Umum
Asam benzoat/ asam benzene karboksilat/ asam phenil karboksilat
(C7H6O2 atau C6H5COOH) merupakan suatu senyawa kimia yang umum
digunakan sebagai bahan pengawet yang dianggap GRAS oleh FDA, dan secara kimia dapat dihasilkan melalui oksidasi fase cair dari toluena (Srour, 1989; WHO, 2000). Asam benzoat memiliki bentuk serbuk kristal padat, tidak berwarna, tidak berbau, sedikit terlarut didalam air, tetapi larut dalam etanol dan sangat mudah larut dalam benzena dan aseton. Asam benzoat, dalam bahan pangan umum digunakan sebagai bahan pengawet. Namun diluar itu, juga dapat dimanfaatkan sebagai penghambat korosi (WHO, 2000). Dalam beberapa penelitian menunjukan bahwa senyawa benzoat dapat ditemukan secara alami pada beberapa jenis tanaman dan juga produk hewani baik dalam bentuk bebas maupun dalam bentuk terikat. Asam benzoat dalam tanaman seperti pada beberapa tanaman berry (±500 mg/kg) seperti cranberry (V.vitis idaea) dan bilberry
(V.macrocarpon) dengan kandungan sebesar 300 – 1300 mg/kg buah ditemukan dalam bentuk
glikosida (Hegnauer, 1996). Selain tanaman berry, Asam benzoat juga teridentifikasi pada beberapa spesies fitofag dan omnivora seperti pada (lagopus mutus) (Hegnauer, 1989).maupun pada muskox jantan (Ovibos moschatus) (Flood et al, 1989)
Natrium benzoat (C7H502Na), merupakan senyawa yang secara kimia
dihasilkan dari reaksi netralisasi asam benzoat dengan natrium hidroksida (NaOH), merupakan salah satu bentuk pengawet benzoat yang sering digunakan untuk menghambat pertumbuhan jamur dan bakteri dengan pKa = 8,0 (Srour, 1989). Secara kimia, natrium benzoat terlarut dalam ethanol, methanol dan etilen glikol dan mempunyai tingkat kelarutan yang lebih
tinggi 200 kali (550 – 630 g/liter pada 20°C) dibandingkan asam benzoat (2,9 g/liter pada 20°C). Kelarutan natrium benzoat dalam air yang tinggi ini kemudian menjadikan natrium benzoat lebih sering digunakan dibandingkan asam benzoat.
2.
Benzoat Sebagai Bahan Pengawet
Di kebanyakan negara, senyawa asam benzoat dan garamnya lebih banyak dimanfaatkan sebagai bahan pengawet makanan. Sebagai bahan pengawet, asam benzoat dan natrium benzoat akan
efektif apabila digunakan pada kisaran pH 2,5 – 4 dan menjadi kurang efektif apabila digunakan pada pH diatas 4,5 (Rahman, 2007). Di USA, asam benzoat dan natrium benzoat merupakan salah satu senyawa yang dikategorikan GRAS (Generally Recognized as Safe) dengan batasan maksimal adalah 0,1%. Untuk masing-masing negara, batasan benzoat yang diizinkan dalam tiap jenis bahan pangan sangat beragam. Berikut tabel batasan benzoat yang diperbolehkan dalam beberapa jenis bahan pangan yang digunakan di India :
Tabel 1. Kadar Maksimal Benzoat Pada Beberapa Produk Pangan
Jenis bahan pangan Kadar maksimal benzoat (ppm)
Anggur non-alkohol, jus buah, air barley (yang digunakan setelah adanya pengenceran)
600
Selai, jelly, buah kaleng 200
Minuman-minuman manis yang siap saji 120
Breewed ginger beer 120
Acar dan chutney 250
Tomat dan produk saus lainnya 750
Caviar 50
Pasta tomat dan puree tomat 750
Sirup dan sharbat 600
Fat spread 1000
(Mahindru, 2000)
Senyawa benzoat sebagai pengawet makanan diketahui dapat mengendalikan pertumbuhan bakteri, khamir maupun kapang. Namun demikian, efektivitas pengendaliannya cenderung lebih tinggi pada khamir dan kapang dibandingkan bakteri (Frazier & Westhoff, 1988). Dalam hal ini, diketahui bahwa kebanyakan khamir dan kapang dapat dihambat sebanyak 0,05% - 0,1% dari jumlah asam yang tidak terdisosiasi, sedangkan bakteri hanya dihambat dalam jumlah yang lebih kecil dibandingkan khamir dan kapang. Oleh karenanya, senyawa benzoat cenderung kurang efektif dalam mengawetkan produk pangan yang potensinya terhadap pertumbuhan bakteri sangat tinggi. Untuk meningkatkan efektifitas dalam menghambat pertumbuhan bakteri, umumnya senyawa benzoat ditambahkan bersama dengan asam sorbat maupun SO2 (Mahindru,
Efektivitas benzoat sebagai pengawet sangat dipengaruhi oleh pH dimana semakin rendah pH maka benzoat akan semakin efektif peranannya sebagai antimikroba karena semakin banyaknya asam yang tidak terdisosiasi. Semakin banyak asam yang tidak terdisosiasi (tidak bermuatan) tersebut maka akan membuat benzoat menjadi semakin mudah terlarut dalam lipid dari membran sel mikroba yang bersifat permeabel terhadap molekul benzoat tersebut. Ketika molekul asam benzoat masuk kedalam sel mikroba tersebut, maka molekul asam benzoat akan terdisosiasi dan menghasilkan sejumlah ion hidrogen (H+) yang menyebabkan penurunan pH pada sel mikroba tersebut, dan sebagai akibatnya aktivitas metabolisme sel akan terganggu dan akhirnya sel mikroba dalam bahan pangan tersebut akan mati (Zentimer, 2007). Gambar 1 dan Gambar 2, menunjukan pengaruh pH terhadap aktivitas benzoat dalam menghambat pertumbuhan Escherichia coli;
Stapylococcus aureus; dan Aspergillus niger
Tabel 2. Pengaruh pH Pada Disosiasi Asam Benzoat pH Asam yang tidak terdisosiasi (%)
3 93,5 4 59,3 5 12,8 6 1,44 7 0,144 (Cahyadi, 2006)
Gambar 1. Efek Asam Benzoat Pada
Escherichia coli ( : Bakteriostatik; :
Aktivitas Bakterisidal) dan Staphylococcus
aureus ( : Bakteriostatik; : Aktivitas
bakterisidal)
Gambar 2. Penghambatan Aspergillus
niger oleh Asam Benzoat ( ); Asam
p-hidroksibenzoat propil ester ( ) dan Asam Sorbat ( )
3.
Benzoat Sebagai Senyawa Antioksidan dan Agen Anti-Browning
Asam benzoat dan senyawa turunannya merupakan salah satu kelompok gugusan senyawa fenolik. Hal tersebut tampak dari keberadaan cincin fenil pada struktur kimia senyawa benzoat dan turunannya (March, 1992; .Natella et al, 1999). Terlepas dari asalnya, keberadaan dari gugusan tersebut menyebabkan senyawa benzoat dapat berperan sebagai senyawa antioksidan, antiviral, antibakterial, antifungal, antimutagenik, maupun insektisidal (Castellano et al, 2012). Keberadaan gugusan hidroksil (OH-) fenolik dalam struktur senyawa benzoat merupakan kunci dalam peranannya sebagai antioksidan. Dalam mekanismenya sebagai anti-radikal, gugus hidroksil (OH-) akan berperan sebagai pendonor elektron terhadap senyawa radikal bebas. Donor elektron terhadap senyawa radikal bebas akan menyebabkan adanya kestabilan muatan dari suatu senyawa radikal (Marcone, 2012).
Asam p-Hidroksibenzoat Asam 3,4-Dihidroksibenzoat Asam Vanillat
Gambar 3. Struktur Benzoat dan Senyawa Turunannya
Sebagai senyawa flavonoid, posisi gugus hidroksil (OH-) dan tingkat hidroksilasi merupakan aspek utama yang menentukan aktivitas antioksidan terhadap suatu senyawa anti-radikal. Pengaruh dari struktur molekul tersebut terhadap aktivitas antioksidan diketahui dalam penelitian Cuvelier et al (1992) yang menunjukan adanya hubungan yang sangat kuat. Dalam kaitannya dengan senyawa benzoat, maka diketahui bahwa derivatif benzoat menunjukan adanya aktivitas antioksidan yang lebih tinggi dibandingkan senyawa asam benzoat itu sendiri. Oleh karenanya dalam peranan sebagai antioksidan, derivatif benzoat lebih banyak dimanfaatkan dibandingkan senyawa asam benzoat (Sroka, 2005). Asam 3,4-dihidroksibenzoat (asam protokatekuat /
protocatechuic acid) merupakan salah satu derivatif benzoat yang memiliki peran penting
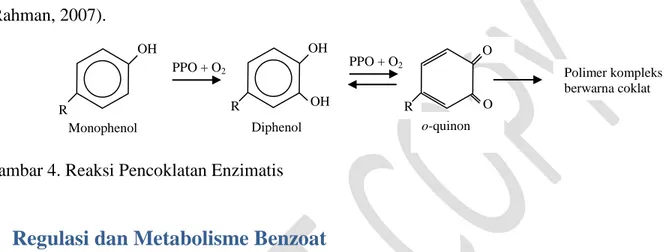
Asam benzoat merupakan salah satu agen yang cukup efektif dalam menghambat pencoklatan dalam kombinasinya dengan asam askorbat. Seperti halnya pada sulfit, kombinasi keduanya menunjukan kemampuan serupa dalam menghambat aktivitas enzim polifenol oksidase (PPO). Enzim ini merupakan enzim yang bertanggung jawab terhadap reaksi pencoklatan, yang muncul ketika senyawa monofenolik dari tanaman ataupun bahan mengalami hidroksilasi menjadi o -difenol dan kemudian menjadi o-quinon dengan adanya pengaruh oksigen dilingkungan (Rahman, 2007).
Gambar 4. Reaksi Pencoklatan Enzimatis
4.
Regulasi dan Metabolisme Benzoat
Di Indonesia, penggunaan asam benzoat dan natrium benzoat diatur dalam BPOM No 36 Tahun 2013 mengenai batas maksimal penggunaan BTP pengawet. Untuk tiap negara, batas maksimal benzoat yang diperbolehkan umumnya berbeda-beda. Dalam hal ini, batasan maksimal benzoat yang boleh ditambahkan dalam bahan adalah sekitar 2000 mg/kg bahan pangan (WHO, 2000). Asam benzoat dari penelitian yang ada, menunjukan tingkat toksisitas akut dalam tubuh yang relatif kecil. Namun, asam benzoat diketahui menyebabkan pseudoallergi (Lahti & Maibach, 1984), menyebabkan iritasi mata (Bayer, 1986), serta sedikit menyebabkan iritasi pada kulit (Bayer, 1978). Sedang untuk natrium benzoat, tidak menunjukan adanya dampak terhadap iritasi kulit dan hanya sedikit menyebabkan iritiasi mata (Bayer, 1977). Namun demikian, dampak asam benzoat dan natrium benzoat terhadap kulit secara umum tergolong langka, karena dari percobaan Brasch et al (1993) terhadap 2045 pasien, hanya 5 pasien saja yang menunjukan reaksi positif dalam uji tempel (patch test).
Dalam beberapa kasus, asam benzoat dan natrium benzoat diketahui menimbulkan beberapa gejala seperti asma dan urtikaria yang diikuti adanya paparan benzoat baik secara oral, dermal maupun melalui pernafasan. Gejala tersebut muncul sesaat setelah terpapar, namun, akan hilang setelah beberapa jam meski terpapar pada dosis yang rendah (Maibach & Johnson, 1975;
R O O OH OH R Monophenol R OH PPO + O2 Diphenol PPO + O2 o-quinon Polimer kompleks berwarna coklat
Clemmensen & Hjorth, 1982; Larmi et al, 1988; Ring, 1989; Gailhofer et al, 1990; Aberer et al, 1992; Lahti et al, 1995; Anderson, 1996; Bindslev-Jensen, 1998; Coverly et al, 1998). Dalam penelitian Wiley & Bigelow (1908), menunjukan adanya dampak seperti sakit kepala, mual, muntah, rasa terbakar dan iritasi pada eksofagus sebagai hasil paparan jangka pendek senyawa benzoat. Sedangkan untuk pengaruh paparan jangka panjang tampak menyebabkan kerusakan pada sistem saraf dan beresiko menimbulkan kanker (Betaria, 2012).
Dalam sejumlah penelitian toksisitas, maka diketahui bahwa LD50 (tikus; oral) senyawa benzoat
adalah sekitar 1,7 – 3,7 g/kg berat badan. Sedangkan berdasarkan penelitian toksisitas pada babi, kucing, anjing dan kelinci menunjukan nilai LD100 adalah 1,4 – 2 g/kg berat badan. 5 mg/kg
berat badan merupakan ADI untuk senyawa benzoat (Belitz et al, 2009; WHO, 2000). Dalam tubuh manusia, tingkat toksisitas secara akut relatif rendah dan tidak menunjukan adanya bahaya akumulasi yang muncul dalam tubuh hingga penggunaan pada dosis 4 g/hari. (WHO, 2000; Lahti & Maibach, 1984). Rendahnya tingkat toksisitas senyawa benzoat dalam tubuh dipengaruhi oleh adanya metabolisme senyawa tersebut didalam tubuh. Dalam hal ini, ketika senyawa benzoat terasup dalam tubuh baik secara oral maupun dermal, maka akan terjadi penyerapan (absorbsi) senyawa benzoat yang sangat cepat dalam gastrointestinal tract, yang kemudian akan dimetabolisme didalam hati melalui adanya konjugasi dengan glisin dan menyebabkan pembentukan asam hippurat yang kemudian akan diekskresikan secara cepat melalui urin (Feldman & Maibach, 1970; US FDA, 1972a; Feillet & Leonard, 1998; WHO, 1996).
Gambar 5. Mekanisme Metabolisme Benzoat Dalam Tubuh (Betaria, 2012) N
C N CH2 COOH + CoA O
CO CoA + AMP PI COCH + ATP + CoA
5.
Daftar Pustaka :
Anonim. (2012). Kandungan Fitokimia Dalam Herbal, Manfaat dan Cara Kerjanya Sebagai Antioksidan dan Perendaman Radikal Bebas (Flavonoid dan Non-Flavonoid Polifenol)
http://mhanafi123.files.wordpress.com/2012/07/fitokimia-dalam-herbal-dan-cara-kerjanya-dalam-mencegah-atau-mengatasi-gangguan-kesehatan.pdf. Diakses pada 23 Juni 2014.
Aberer, W, Kager, B, Ziegler, V, Horak, F. (1992) Schnupfen durch Schneiderkreide — Allergie, Pseudoallergie, Rhinopathie oder Einbildung. Dermatosen Vol 40(6):231–234.
Andersen, K.E; Maibach, H.I; Anjo, M.D. (1980) The Guinea-Pig: an Animal Model for Human Skin Absorption of Hydrocortisone, Testosterone and Benzoic Acid. British journal of dermatology Vol 102:447–453.
Bayer, A.G. (1978). Untersuchung Zur Haut-und Schleimhautver träglichkeit. Wuppertal (Unpublisher Report).
Bayer, A.G. (1986). Benzoesaure DAB8. Prüfung auf primär reizende/ ätzende Wirkung am Kaninchenauge. Wuppertal (unpublished report).
Belitz, H.D; Grosch, W & P, Schieberle. (2009). Food Chemistry 4th Revised and Extended Edition. Springer Science & Bussines Media. Berlin.
Betaria, S. (2012). Pengembangan Sensor Spektrofotometri Untuk Penentuan Natrium Benzoat didalam Minuman Soft Drink. Undergraduate Theses UNIMED. Medan.
Bindslev-Jensen, C (1998) ABC of allergies. Food allergy. British medical journal Vol 316:1299 – 1302.
Brasch, J; Henseler, T; Frosch, P. (1993). Patch Test Reaction to a Preliminary Preservative Series. Dermatosen Vol 41(2):71-76
Cahyadi, S. (2006). Analisis dan Aspek Kesehatan Bahan Tambahan Pangan. PT Bumi Aksara. Jakarta.
Castellano, G; Tena, J & Torrens, F. (2012). Classification of Phenolic Compound by Chemical Structural Indicators and its Relation to Antioxidant Properties of Posidonia Oceania (L) Delile. MATCH Commun.Math.Comput.Chem Vol 67:231-250.
Clemmenson, O & N, Hjorth. (1982). Perioral Contact Urticaria From Sorbic and Benzoic Acid in Salad Dressing. Contact Dermatitis Vol 8:1-6.
Coverly, J; Peters, L; Whittle, E, Basketter, D.A. (1998) Susceptibility to skin stinging, non-immunologic contact urticaria and acute skin irritation; is there a relationship?. Contact dermatitis Vol 38(2):90–95.
Cuvelier, M.E; Richard, H & C, Berset. (1992). Comparison of the Antioxidant Activity of Some Acid Phenols : Structure-Activity Relationship. Biochi.Biotech.Biochem Vol 56:324-325.
Feillet, F; Leonard, J.V. (1998). Alternative Pathway Therapy for Urea Cycle Disorders. Jornal of Inherited Metabolic Desease Suppl Vol 21(1):101-111.
Feldman, R.J; Maibach, H.I. (1970). Absorption of Some Organic Compound Through the Skin in Man. Journal of Investigative Dermatology Vol 54:399-404.
Frazier, W.C & D.C, Westhoff. (1988). Food Microbiology 4th Edition. McGraw Hill. New York. Flood, P.F; Abrams, S.R; Muir, G.D & J.E, Rowell. (1989). Odor of the Muskox. A Preliminary Investigation. Journal of Chemical Ecology Vol 15 : 2207-2217
Hegnauer, R. (1966). Chemotaxonomie der Pflanzen. Basel. Birkhäuser Verlag.
Hegnauer, R. (1989). Chemotaxonomie der Pflanzen. Basel. Birkhäuser Verlag. Pp 415-416 Gailhofer, G; Soyer, H.P; Ludvan, M. (1990). Nahrungsmittelallergien und Pseudoallergien — Mechanismen, Klinik und Diagnostik. Wiener Medizinische Wochenschrift Vol 140:227–232 https://www.academia.edu/5630270/BPOM_No_36_Tahun_2013_Tentang_Batas_Maksimum_P enggunaan_BTP_Pengawet
Kirk & Othmer, 1989.Encyclopedia of chemical technology 4th Ed. Vol 21
Lahti, A & H.I, Maibach. (1948). An Animal Model for Non-Immunological Contact Urticaria. Toxicology and Applied Pharmacology Vol 76:219-224.
Lahti, A; Pylvanen, V; Hannuksela, M. (1995). Immediate Irritant Reaction of Benzoic Acid are Enhanced in Washed Skin Areas. Contact Dermatitis Vol 33: 177-182
Larmi, E; Lahti, A; Hannuksela, M. (1988). Effect of Sorbitan Sesquioleata of Non-immunologic Immediate Contact Reactions to Benzoic Acid. Contact Dermatitis Vol 19:368-371. Lin. H.H; Chen, J.H; Huang, C.C; Wang, C.J. (2007). Apoptotic effect of 3,4-dihydroxybenzoic acid on human gastric carcinoma cells involving JNK/p38 MAPK signaling activation. Int.J.Cancer Vol 120(11):2306-2316.
Maibach, H.I & H.L, Johnson. (1975). Contact Urticaria Syndrome. Archives of Dermatology Vol 111:726-730
March, J. (1992). Advanced Organic Chemistry 4th Edition. Wiley and Sons. New York.
Marcone, M. (2012). Analytical Technique in Food Biochemistry. Dalam Simpson, B.K; Leo, M.L; Nollet; Fidel, T; Benjakul, S; Paliyath G & Y.H, Hui. (2012). Food Biochemistry and Food Processing 2nd Edition. John Wiley & Sins. New York.
Mahindru, S.N. (2000). Food Additives : Characteristics, Detection and Estimation. Mc-Graw Hill. New Delhi.
M. Jones and S.A. Fleming in "Organic Chemistry", Norton, 4th ed., 2010, Chapter 6, p. 227- 230,Chapter 16, p. 797-802; Chapter 17 p. 840
Natella, F; Nardini, M; Felice, M.D & C. Scaccini. (1999). Benzoic and Cinnamic Acid Derivative as Antioxidant : Structure-Activity Relation. J.Agric.Food.Chem Vol 47:1453-1459. Rahman, M.S. (2007). Handbook of Food Preservation 2nd Edition. CRC Press. New York. Rasmussen LEL, Hess DL, Haight JD (1990) Chemical analysis of temporal gland secretions collected from an Asian bull elephant during a four-month musth episode. Journal of chemical ecology, 16(7):2167–2181.
Ring J (1989) Arzneimittelunverträglichkeit durch pseudoallergische Reaktionen. Wiener Medizinische Wochenschrift Vol 139:130–134.
Sroka, Z. (2005). Antioxidative and Antiradical Properties of Plant Phenolic. Z.Naturforsch Vol 60:833-843.
Srour, R. (1989). Benzoid Acid : Aromatic Intermediate and Derivatives. Paris.
US FDA. (1972a). GRAS (Generally Recognized as Safe) Food Ingredient : Benzoic Acid and Sodium Benzoate. US Food and Drug Administration. USA.
WHO. (1996). Toxicological Evaluation of Certain Food Additives. World Health Organization. USA.
WHO. (2000). Benzoic Acid and Sodium Benzoate. World Healt Organization. USA.
Wiley HM, Bigelow WD (1908) Influence of benzoic acid and benzoates on digestion and health. Bulletin 84, Part IV. Bureau of Chemistry, US Department of Agriculture [cited in US FDA, 1972a].
Zentimer, S. (2007). Pengaruh Konsentrasi Natrium Benzoat dan Lama Penyimpanan Terhadap Mutu Minuman Sari Buah Sirsak (Annona muricata L) Berkarbonasi. Departemen Teknologi Pertanian Universitas Sumatra Utara. Sumatra Utara.