BAB II
TINJAUAN PUSTAKA
2.1 Keratin pada Bulu Ayam
Keratin merupakan protein struktural yang tidak larut dalam air yang ditemukan pada bulu, rambut, kuku, tanduk dan jaringan epidermal lain yang mengalami pengerasan (Gushterova et al., 2005). Polipeptidanya diikat padat dengan stabilitas yang kuat oleh ikatan hidrogen dan interaksi hidrofobik, serta rantai proteinnya dihubungkan oleh beberapa ikatan disulfida yang memberi stabilitas mekanik tinggi dan tahan terhadap pendegradasi protein lainnya (Kreplak et al., 2004) seperti pepsin, papain, dan tripsin (Werlang & Brandelli, 2005) sehingga sulit didegradasi.
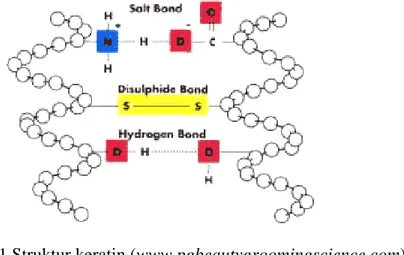
Gambar 2.1 Struktur keratin (www.pgbeautygroomingscience.com)
Keratin berbentuk tiga dimensi yang memiliki lilitan α-heliks atau lipatan β-sheet, dan tersusun atas atom karbon yang berikatan dengan gugus fungsional (gugus amin-NH2 dan gugus karboksil-COOH), atom hidrogen dan gugus R (sulfur) (Brandelli et al., 2010) (Gambar 2.1). Kandungan karbon yang tinggi mengakibatkan keratin dapat bersifat fleksibel dan hidrofobik (Belarmino et al., 2012). Keratin juga tersusun atas 8% jembatan sistein (ikatan disulfida) yang merupakan penghambat enzim proteolitik biasa dalam mendegradasi keratin dan menjadi penentu kekuatan mekanik dari keratin tersebut (Krystyna & Janusz., 2007).
Bulu ayam merupakan salah satu limbah biologi yang kaya protein. Dari hasil pemotongan satu ekor ayam dewasa dihasilkan limbah bulu ayam sekitar 5-7 persen dari berat tubuh totalnya (Gushterova et al., 2005). Kandungan bulu ayam terdiri dari 91% protein keratin, 1% lipid dan 8% air. Keratin pada bulu ayam sebagian besar disusun oleh asam amino sistein, glutamin, prolin dan serin (Saravanan, 2012), sedangkan menurut Gupta et al. (2012), keratin bulu ayam tersusun atas beberapa asam amino seperti glisin, alanin, serin, sistein dan valin, serta sedikit lisin, metionin dan triptofan (Tabel 2.1).
Tabel 2.1 Kandungan asam amino pada bulu ayam
Asam Amino Jumlah Kandungan (%)
Saravanan (2012) Gupta et al. (2012)
Arginin 4,30 6,57 Asam aspartat 6,00 4,76 Glutamin 7,62 9,18 Glisin - 7,57 Theronin 4,00 4,11 Serin 16,00 13,57 Tirosin 1,00 1,85 Leusin 2,62 7,48 Isoleusin 3,32 4,93 Valin 1,61 7,24 Sistein 8,85 2,11 Alanin 3,44 3,66 Fenilalanin 0,86 4,11 Metionin 1,02 0,025 Prolin 12,0 1,01 Asparagin 4,00 - Histidin - 0,016
Keratin pada bulu ayam dapat didegradasi dengan memecah atau memutus ikatan disulfida pada keratin tersebut. Hal ini dapat dilakukan dengan pemanasan tinggi (hidrotermal), perlakuan kimia, serta perlakuan biologis. Perlakuan hidrotermal dilakukan dengan pengaturan suhu dan tekanan yang tinggi, begitu pula perlakuan kimia dilakukan dengan penambahan asam (HCl) dan basa (NaOH) pada konsentrasi tinggi (Cai & Zheng, 2009). Perlakuan biologis dapat dilakukan secara enzimatis dengan menggunakan enzim khusus yaitu keratinase (Brandelli et al., 2010).
2.2 Enzim Keratinase
Keratinase merupakan enzim protease yang dapat digunakan untuk mendegradasi protein keratin dengan baik. Enzim keratinase telah banyak dimanfaatkan dalam bidang industri seperti industri farmasi, pupuk (Brandelli, 2008), bahan tambahan pakan dan lingkungan (Lee et al., 2004), deterjen, lem, dan ikat pinggang (Prakash et
al., 2010), serta perawatan terapi kulit (Kumar et al., 2010).
Enzim dengan nomor kode E.C 3.4.21/24/99 berdasarkan ketentuan dari IUB (Langeveld et al., 2003) memiliki karakteristik biokimia yang berbeda-beda berdasarkan jenis dan sumber isolat, serta medium dan inhibitor yang digunakan. Secara umum, enzim keratinase memiliki berat molekul berkisar antara 20 kDa sampai 60 kDa (Inamdar et al., 2012). Keratinase paling banyak dihasilkan pada keadaan basa atau netral, yaitu berkisar antara pH 7,5 sampai pH 9. Suhu optimum enzim keratinase bervariasi tergantung pada sumber dan asal isolat yang digunakan, yaitu berkisar antara 40 oC sampai 100 oC. Enzim ini juga dapat ditingkatkan maupun dihambat aktivitasnya oleh bahan kimia lain, dimana secara umum Ca2+, Mg2+, dan Mn2+ dapat menstimulasi kerja keratinase, sedangkan Cu2+, Ag+, Hg2+ dan Pb2+ diketahui dapat menghambat kerja dari enzim keratinase (Brandelli et al., 2010).
Secara umum, ada dua tipe katalis pada enzim keratinase yaitu tipe serin dan metaloprotease. Kedua tipe ini dikelompokkan berdasarkan jenis bahan kimia yang menghambat aktivitas enzim tersebut (inhibitor). Aktivitas keratinase yang dihambat oleh EDTA dan 1,10-phenanthroline termasuk kelompok metaloprotease, sedangkan bila dihambat dengan phenylmethylsulfonyl flouride (PMSF) dan benzamidine maka termasuk kelompok serin (Brandelli, 2008). Enzim keratinase yang dihasilkan oleh
Penicillium sp. termasuk pada tipe metaloprotease, karena dihambat kuat oleh EDTA
dan EGTA (El-Gendy, 2010). Begitu juga dengan keratinase yang dihasilkan oleh
Bacillus sp. strain kr 16 (Werlang & Brandelli, 2005) termasuk tipe metaloprotease
karena aktivitas enzimnya dihambat oleh EDTA dan ion Hg+ dan Sn2+. Keratinase yang dihasilkan dari Stenotrophomonas termasuk tipe serin, yang aktivitasnya dihambat oleh phenylmethylsulfonyl flouride (PMSF) (Cao et al., 2009).
2.3 Mikroorganisme Penghasil Enzim Keratinase
Mikroorganisme penghasil enzim keratinase telah banyak dipelajari dan dikarakterisasi oleh banyak peneliti (Tabel 2.2). Enzim keratinase dapat diproduksi dari tiga kelompok mikroorganisme yaitu, bakteri, jamur, dan actinomycetes. Mikroorganisme tersebut dapat diisolasi dari tanah Antartika hingga ke sumber air panas baik pada lingkungan aerobik maupun anaerobik (Brandelli et al., 2010). Tabel 2.2 Karakteristik beberapa mikroorganisme penghasil keratinase
Mikroorganisme BM pH Suhu Tipe Referensi
Bakteri
Stenotrophomonas 35,2 7,8 40 oC Serin Cao et al. (2009)
Bacillus sp. 50-3 27,42 7 37 oC Serin Yue et al. (2011)
B.halodurans PPKS2 ker I ker II 30 60 11 11 60-70 oC 70 oC Serin - Prakash et al. (2010)
Bacillus subtilis 64-69 5-7 40 oC Serin Balaji et al. (2008)
B.subtilis KD-N2 30,5 8,5 55 oC Serin Cai et al. (2008)
Bacillus pumilus 34 9 60 oC Serin Zouari et al. (2010)
Bacillus licheniformis 35 8,5 60 oC Serin Suntornsuk et al.
(2005)
Bacillus pseudofirmus FA
30-01
27,5 8,8-10,3 60 oC Serin Kojima et al. (2006)
Bacillus sp. SCB-3 134 7 40 oC Metalo-protease Lee et al. (2002) Chryseobacterium sp. Kr6 20 - 50-60 oC Metalo-protease Silveira et al. (2010)
B. subtilis PB 100 - 7 30 oC - Zaghloul et al. (2011)
B. subtilis MTCC 9102 - 7 37 oC - Kumar et al. (2010)
Paracoccus sp. WJ-98 - 7,5 37 oC
Metalo-protease
Lee et al. (2004)
Aeromonas hydrophila - 8 45-55 oC
Metalo-protease
Bach et al.(2011)
Serratia marcescens - 6 45-55 oC
Metalo-protease
Bach et al.(2011)
Bacillus sp. Strain - 8-11 45-65 oC
Metalo-protease
Werlang & Brandelli (2005)
Jamur
Myrothecium verrucaria - 9 40 oC Serin Moreira et al. (2007)
Trichophyton
mentagrophytes var.erinacei
38 5,5 50 oC Serin Muhsin & Aubaid (2001) Penicillium sp. Ahm I Ahm II 19 40 7-8 10-11 50 oC 60-65 oC Metalo-protease El-Gendy (2010) Actinomycetes
Domain eukaria yang mampu menghasilkan keratinase adalah jamur. Di lingkungan alami, jamur keratinolitik mendegradasikan keratin untuk memanfaatkan molekul karbon, nitrogen dan sulfur sebagai makanannya dengan mengekskresikan enzim keratinase ke lingkungan. El-Gendy (2010) memperoleh 8 strain Penicillium dengan aktivitas enzim keratinase yang berbeda-beda setelah masa inkubasi 5 hari.
Myrothecium verrucaria diketahui potensial mendegradasi medium bulu ayam
ditambah singkong sebagai substratnya (Gioppo et al., 2009). Tiga belas spesies jamur penghasil enzim keratinase berhasil diisolasi dari limbah bulu ayam oleh Marcondes et al. (2008) dan diketahui bahwa ada 4 spesies yang aktivitas keratinolitiknya paling tinggi yaitu Alternaria tenuissima, Acremonium hyalinulum,
Curvularia brachyspora, dan Beauveria bassiana.
Domain bakteri merupakan penghasil keratinase yang paling banyak diteliti dan paling beragam dalam memiliki kemampuan mendegradasi keratin. Sebagai contoh, Bacillus halodurans PPKS2 banyak digunakan dalam industri deterjen dan ikat pinggang karena kemampuan toleransi dan stabilitasnya terhadap suhu dan pH tinggi pada proses pemutihan (Prakash et al., 2010). Bacillus strain kr16 (Werlang & Brandelli, 2005) potensial dalam industri ikat pinggang karena strain ini mampu mendegradasi tepung bulu ayam secara sempurna. Cai & Zheng (2009) berhasil mengisolasi Bacillus subtilis KD-N2 yang mampu mendegradasi kolagen dan dermis rambut sehingga sangat potensial diaplikasikan pada bidang nutrisi makanan dan pendegradasi rambut.
Keratinase juga dihasilkan dari kelompok Actinomycetes. Beberapa
Streptomyces berhasil diisolasi dari beberapa jenis tanah dan mampu mendegradasi
berbagai substrat keratin seperti rambut, wol, dan bulu (Brandelli et al., 2010). Al-Zarban et al. (2002) berhasil mengisolasi Saccharomonaspora halophila dan
Nocardiopsis halotolerans yang dapat menggunakan sumber karbon dan nitrogen
pada substrat keratin dengan konsentrasi garam tinggi, sehingga potensial digunakan pada bidang bioteknologi pendegradasi keratin di air laut.