OLIMPIADE SAINS NASIONAL 2012
Jakarta
2- 7 September 2012
Bidang Kimia
SOAL
Ujian Praktikum
Waktu: 240 menit
Kementerian Pendidikan Nasional dan Kebudayaan
Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah
Direktorat Pembinaan Sekolah Menengah Atas
2012
Hak Cipta
Instruksi
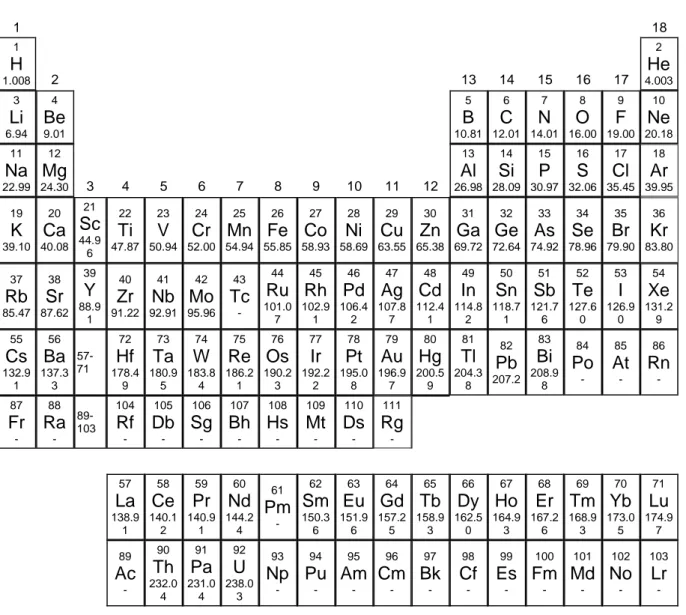
Disediakan Tabel Periodik Unsur.
Ujian praktikum ini terdiri atas 2 soal dengan total 7 halaman.
Anda memiliki waktu 4 jam untuk menyelesaikan percobaan. Masing masing 2 jam untuk
Soal 1 dan 2.
Anda memiliki waktu 15 menit untuk membaca soal ujian yang diberikan pada ujian praktikum ini sebelum memulai percobaan.
Setelah menyelesaikan tugas yang diberikan, selesaikan hasil praktikum Anda dan jawablah pertanyaan di lembar jawaban yang diberikan.
Soal dan lembar jawaban harus anda tinggalkan di meja kerja Anda.
Sebelum melanjutkan ke soal kedua, anda akan memperoleh waktu istirahat selama 30 menit
Mulailah hanya ketika perintah MULAI diberikan. Anda harus segera menghentikan pekerjaan Anda ketika perintah BERHENTI diumumkan. Keterlambatan hingga 5 menit akan menggagalkan ujian praktikum Anda. Setelah perintah BERHENTI diberikan,
tunggulah di tempat Anda bekerja. Petugas lab akan mengecek tempat kerja Anda.
Anda harus mengikuti aturan keselamatan yang berlaku dalam OSN. Ketika ada di laboratorium, Anda harus menggunakan jas lab dan kacamata pelindung yang tersedia kacamata pribadi yang terbukti melindungi mata Anda.Gunakan filler pipet
karet yang tersedia. Anda harus menggunakan sarung tangan ketika bekerja dengan
bahan kimia.
Anda hanya boleh menerima SATU KALI PERINGATAN saja dari petugas laboratorium. Jika Anda melanggar aturan keselamatan pada peringatan yang kedua kalinya Anda
akan dikeluarkan dari laboratorium dengan nilai nol untuk seluruh ujian praktikum. Jangan ragu untuk bertanya kepada petugas lab jika ada pertanyaan yang berhubungan
dengan aturan keselamatan atau jika Anda perlu meninggalkan ruangan.
Anda hanya diperbolehkan bekerja di tempat yang dialokasikan untuk Anda saja. Gunakan hanya pulpen yang disediakan untuk menuliskan jawaban, jangan gunakan
pensil.
Semua hasil harus dituliskan di dalam tempat yang disediakan pada lembar jawaban. Semua yang dituliskan di luar itu tidak akan dinilai. Gunakan bagian belakang kertas jika Anda perlukan untuk corat-coret.
Tabel Periodik dengan Massa Atom Relatif
1 18 1H
1.008 2 13 14 15 16 17 2He
4.003 3Li
6.94 4Be
9.01 5B
10.81 6C
12.01 7N
14.01 8O
16.00 9F
19.00 10Ne
20.18 11Na
22.99 12Mg
24.30 3 4 5 6 7 8 9 10 11 12 13Al
26.98 14Si
28.09 15P
30.97 16S
32.06 17Cl
35.45 18Ar
39.95 19K
39.10 20Ca
40.08 21Sc
44.9 6 22Ti
47.87 23V
50.94 24Cr
52.00 25Mn
54.94 26Fe
55.85 27Co
58.93 28Ni
58.69 29Cu
63.55 30Zn
65.38 31Ga
69.72 32Ge
72.64 33As
74.92 34Se
78.96 35Br
79.90 36Kr
83.80 37Rb
85.47 38Sr
87.62 39Y
88.9 1 40Zr
91.22 41Nb
92.91 42Mo
95.96 43Tc
-44Ru
101.0 7 45Rh
102.9 1 46Pd
106.4 2 47Ag
107.8 7 48Cd
112.4 1 49In
114.8 2 50Sn
118.7 1 51Sb
121.7 6 52Te
127.6 0 53I
126.9 0 54Xe
131.2 9 55Cs
132.9 1 56Ba
137.3 3 57-71 72Hf
178.4 9 73Ta
180.9 5 74W
183.8 4 75Re
186.2 1 76Os
190.2 3 77Ir
192.2 2 78Pt
195.0 8 79Au
196.9 7 80Hg
200.5 9 81Tl
204.3 8 82Pb
207.2 83Bi
208.9 8 84Po
-85At
-86Rn
-87Fr
-88Ra
- 89-103 104Rf
-105Db
-106Sg
-107Bh
-108Hs
-109Mt
-110Ds
-111Rg
-57La
138.9 1 58Ce
140.1 2 59Pr
140.9 1 60Nd
144.2 4 61Pm
-62Sm
150.3 6 63Eu
151.9 6 64Gd
157.2 5 65Tb
158.9 3 66Dy
162.5 0 67Ho
164.9 3 68Er
167.2 6 69Tm
168.9 3 70Yb
173.0 5 71Lu
174.9 7 89Ac
-90Th
232.0 4 91Pa
231.0 4 92U
238.0 3 93Np
-94Pu
-95Am
-96Cm
-97Bk
-98Cf
-99Es
-100Fm
-101Md
-102No
-103Lr
-SOAL 1
Titrasi Asam Basa
1 2 3 4 5 6 Soal 1 22 %
4 6 6 8 8 2 34
Pendahuluan
Menurut Arrhenius, Asam adalah suatu zat yang larut dalam air menghasilkan ion H+ sedangkan basa adalah suatu zat yang larut dalam air menghasilkan OH. Asam bereaksi dengan basa menghasilkan air.
Asam klorida (HCl) adalah gas pada suhu ruang yang dapat larut dalam air menghasilkan larutan asam klorida. Kelarutan maksimum HCl dalam air adalah 37 % massa, namun HCl yang digunakan di laboratorium umumnya cukup encer agar aman terhadap lingkungan. Untuk menentukan konsentrasi asam klorida pada suatu sampel, digunakan cara titrasi dengan basa yang stabil seperti boraks dan natrium karbonat. Boraks memiliki rumus kimia Na2B4O7 sedangkan natrium karbonat memiliki rumus kimia Na2CO3. Setiap mol basa
tersebut dalam air dapat menghasilkan maksimum 2 mol ion OH. Reaksi HCl dengan kedua basa tersebut menghasilkan produk yang berpengaruh pada pH larutan final, karena itu pemilihan indikator yang tepat dapat menghasilkan data yang lebih akurat. Pada percobaan ini anda harus menentukan konsentrasi larutan sampel HCl dengan teliti menggunakan cara titrasi. Anda harus memilih indikator yang paling sesuai untuk kedua reaksi tersebut dan dari hasil yang diperoleh harus dapat disimpulkan berapa konsentrasi HCl yang paling tepat.
Bahan kimia yang diperlukan
Larutan sampel HCl Na2B4O7.10H2O
Na2CO3
Aquades
Phenolphtalein, trayek pH 8-10 Metil Merah, trayek pH 4-6
Alat yang diperlukan
1 Buret 50 mL 1 Labu ukur 100 mL 2 Labu ukur 50 mL
2 Labu Erlenmeyer 100 mL 2 Pipet volumetrik 10 mL
Neraca digital (dipakai bersama)
Catatan : Sebelum anda melakukan titrasi, tuliskan persamaan kimia yang terjadi, kemudian tentukan indikator yang paling tepat untuk digunakan pada titrasi tersebut. Kesalahan memilih indikator dapat berakibat hasil analisis tidak tepat.
Prosedur Kerja
1. Diberikan sampel larutan HCl dalam labu ukur 100 mL, jangan lupa mengencerkan larutan sampel tersebut sampai tanda batas dan homogenkan.
2. Masukkan larutan HCl encer tersebut dalam buret, kemudian tanda bataskan.
3. Masukkan padatan boraks yang telah diberikan (perhatian: catat massa boraks + bungkusnya pada lembar jawaban) ke dalam gelas kimia 100 mL, larutkan padatan boraks dengan 15 mL aquades, aduk hingga larut.
4. Timbang kembali bungkus boraks tersebut, catat massa bungkus dalam lembar jawaban.
5. Masukkan larutan boraks ke dalam labu ukur 50 mL menggunakan corong kecil, bila masih ada boraks yang belum larut, tambahkan aquades sampai semua boraks larut sempurna.
6. Setelah larutan boraks masuk semua ke dalam labu ukur, tambahkan aquades hingga tanda batas.
7. Pipet 10 mL larutan boraks, masukkan ke dalam labu Erlenmeyer 100 mL dan tambahkan indikator yang sesuai.
8. Titrasi larutan boraks tersebut dengan larutan HCl sampai tepat mencapai titik akhir titrasi.
9. Catat pada lembar jawaban volume pemakaian larutan HCl yang digunakan.
10. Ulangi prosedur pekerjaan itu sampai diyakini volume yang tepat untuk titrasi tersebut.
11. Prosedur di atas dapat digunakan pula untuk titrasi larutan HCl dengan natrium karbonat.
12. Buatlah larutan natrium karbonat 0,1 N dalam labu ukur 50 mL.
Catatan: Hitung massa natrium karbonat yang harus anda timbang.
13. Titrasi 10 mL larutan natrium karbonat dengan HCl menggunakan indikator yang sesuai, catat volume HCl yang digunakan pada lembar jawaban.
14. Hitung konsentrasi asam klorida yang diberikan dalam satuan molaritas (mol/L), berdasarkan hasil titrasi anda dengan larutan natrium karbonat.
Referensi:
SOAL 2
Sintesis “Hijau” Senyawa Turunan Nitro Aromatik
1 2 3 4 5 6 7 8 Soal 2 18%
1 2 4 4 6 6 6 4 33
Pendahuluan
Reaksi nitrasi senyawa aromatik merupakan reaksi penting dalam pembuatan senyawa-senyawa nitro-aromatik yang banyak dibutuhkan sebagai bahan baku dalam pembuatan zat warna, obat-obatan/farmasi, parfum, kosmetika dan plastik. Namun selama ini proses reaksi nitrasi aromatik relatif tidak efektif, disamping penggunaan asam sulfat dan asam nitrat pekat yang korosif dan oksidatif.
Dalam percobaan ini dilakukan reaksi nitrasi terhadap senyawa aromatik, yaitu Naftalena, menggunakan katalis asam fasa padat, yaitu silica sulfuric acid ( SSA), yang relatif efisien dan dapat dipakai ulang, sehingga memenuhi tiga aspek “Green Chemistry”, yaitu:
(1) mengatasi masalah yang berhubungan dengan polusi, toksisitas dan proses yang rumit dengan cara mengurangi penggunaan asam sulfat pekat dan asam nitrat pekat serta katalis logam berat lainnya;
(2) efisiensi proses dilihat dari segi hemat biaya, sederhana dalam pengerjaan, dan rendah polutan sehingga ramah lingkungan;
(3) Menghasilkan produk dengan rendemen tinggi dan mengurangi produk samping.
Bahan kimia yang diperlukan
Naftalena 0,13 g
SSA (silica sulfuric acid) 0,6 g Natriun nitrat, NaNO3 0,09 g
SiO2basah 60% (w/w) dalam air 0,5 g
Diklorometana, CH2Cl2– 10 mL
Pelat KLT Silika gel G60 F234– 1 buah
Eluen untuk KLT: etil asetat:n-heksana = 3:7 – 5 mL
n-heksana – 1 pipet tetes
Alat yang diperlukan
Mortar dan alu keramik, 1 buah
Wadah pengembang KLT (gelas kimia 200 mL), 1 buah
Kaca arloji, 1 buah (untuk penimbangan dan untuk menutup wadah pengembang) Pengaduk kaca, 1 buah
Prosedur Kerja
1. Masukkan campuran dari 0,6 g silica sulfuric acid (SSA), 0,09 g natrium nitrat, 0,13 g (1 mmol) naftalena dan 0,5 g SiO2 basah (60% w/w dalam air) ke dalam
mortar, lakukan penggerusan selama± 15 menit.
Catatan: semua zat ditimbang menggunakan kertas timbang yang telah disediakan
di dekat timbangan kecuali untuk SiO2basah ditimbang menggunakan kaca arloji.
2. Setelah reaksi selesai, tambahkan 10 mL diklorometana (CH2Cl2) ke dalam
campuran reaksi, aduk selama± 1 menit.
3. Saring menggunakan corong biasa dan tampung filtratnya pada cawan penguapan yang telah diketahui bobotnya.
Catatan: sebelum penimbangan, cawan penguapan tersebut harus dipanaskan
terlebih dahulu selama 10 menit di atas pemanas yang telah disediakan, dinginkan, lalu timbang.
4. Panaskan cawan penguapan berisi filtrat di atas pemanas selama 5 menit agar pelarut diklorometana menguap, lalu angkat cawan tersebut dan biarkan di udara hingga terbentuk kristal produk.
5. Timbang kembali cawan penguapan dan hitung rendemennya.
6. Lakukan proses KLT (Kromatografi Lapis Tipis) terhadap senyawa awal dan produk reaksi dengan cara sebagai berikut:
a. Larutkan kristal produk reaksi yang ada dalam cawan penguapan dengan 1 pipet tetes penuh n-heksana.
b. Dalam botol vial 5 mL, larutkan pula sedikit naftalena dengan 1 pipet tetes n-heksana.
c. Ke dalam gelas kimia 200 mL untuk wadah pengembang KLT, masukkan kertas saring berbentuk persegi panjang yang telah disediakan sehingga menempati ketinggian yang hampir sama dengan ketinggian gelas tersebut. Hal ini dilakukan untuk menjenuhkan wadah pengembang dengan uap pelarut.
d. Tambahkan 5 mL pelarut/eluen untuk KLT (etil asetat:n-heksana = 3:7) ke dalam gelas kimia tersebut untuk membasahi kertas saring. Tutup gelas tersebut dengan kaca arloji.
e. Gunakan pipa kapiler yang tersedia untuk menotolkan sampel naftalena dan larutan produk pada garis tanda awal pelat KLT.
f. Lakukan proses KLT di dalam gelas bertutup kaca arloji hingga hampir mencapai batas atas pelat (± 5 mm dari ujung atas pelat KLT).
g. Beri tanda batas akhir pelarut dan amati noda pada KLT menggunakan lampu UV yang disediakan, tandai noda-noda yang teramati pada pelat KLT menggunakan pensil.
h. Keringkan plat KLT di udara dan tempelkan pada lembar jawaban. Salin juga hasil KLT di tempat yang disediakan pada lembar jawaban.
i. Hitung nilai Rfnaftalena dan produk sintesis.
Referensi:
Zolfigol, M. A., Mirjalili, B.F., Bamoniri, A., Zarchi, M.A.K., Zarei, A., Khazdhooz, L., dan Noei, J., (2004): Nitration of Aromatic Compounds on Silica Sulfuric Acid, Bull. Korean Chem. Soc., 25, No. 9., 1414-1416.
Zolfigol, M. A., Madrakian, E., dan Ghaemi, E., (2002): Silica Sulfuric Acid/NaNO2 as a Novel
Heterogeneous System for the Nitration of Phenols under Mild Conditions, Molecules, 7, 734-742.