SKRIPSI
PERBANDINGAN EFEKTIFITAS PEMBERIAN PERASAN RIMPANG TEMULAWAK (Curcuma xanthorriza, Roxb) DENGAN MEBENDAZOL
TERHADAP VIABILITAS TELUR CACING Ascaridia galli SECARA IN VITRO
Oleh:
INDAH TRI SUSANTI SURABAYA − JAWA TIMUR
FAKULTAS KEDOKTERAN HEWAN UNIVERSITAS AIRLANGGA
PERBANDINGAN EFEKTIFITAS PEMBERIAN PERASAN RIMPANG TEMULAWAK (Curcuma xanthorriza, Roxb) DENGAN MEBENDAZOL
TERHADAP VIABILITAS TELUR CACING Ascaridia galli SECARA IN VITRO
Skripsi sebagai salah satu syarat guna memperoleh gelar
Sarjana Kedokteran Hewan
pada
Fakultas Kedokteran Hewan Universitas Airlangga
Oleh:
INDAH TRI SUSANTI
NIM. 060112940
Menyetujui
Komisi Pembimbing,
Dr. M. Zainal Arifin, MS., Drh Prof. Dr. Setiawan Koesdarto, MSc., Drh
Setelah mempelajari dan menguji dengan sunguh-sungguh, Kami berpendapat
bahwa tulisan ini ruang lingkup maupun kualitasnya dapat diajukan sebagai
skripsi untuk memperoleh gelar SARJANA KEDOKTERAN HEWAN.
Menyetujui,
Tim Penguji,
Sri Agus Sudjarwo, Ph.D., Drh. Ketua
Tutik Juniastuti, M.Kes., Drh. Ririen Ngesti Wahyuti, M.Kes., Drh.
Sekretaris Anggota
Dr. M. Zainal Arifin, M.S., Drh. Prof. Dr. Setiawan Koesdarto, M.Sc., Drh.
Anggota Anggota
Surabaya, 8 Februari 2006 Fakultas Kedokteran Hewan
Universitas Airlangga Dekan,
PERBANDINGAN EFEKTIFITAS PEMBERIAN PERASAN RIMPANG TEMULAWAK (Curcuma xanthorriza, Roxb) DENGAN MEBENDAZOL
TERHADAP VIABILITAS TELUR CACING
Ascaridia galli SECARA IN VITRO
INDAH TRI SUSANTI
ABSTRAK
Penelitian ini bertujuan untuk mengetahui efektifitas pemberian perasan rimpang temulawak (Curcuma xanthorriza, R) sebagai antelmintik terhadap
viabilitas telur cacing Ascaridia galli secara in vitro.
Sampel yang digunakan untuk penelitianini adalah telur cacing A.galli yang
diperoleh dengan mengumpulkan cacing A.galli dewasa dari usus halus ayam
buras. Rancangan percobaan yang digunakan adalah Rancangan Acak Lengkap (RAL) dengan enam perlakuan yaitu perendaman telur A.galli dalam larutan
NaCL fisiologis (P0), perendaman telur cacing A.galli dalam perasan rimpang
temulawak 2% (P1), perendaman telur cacing A.galli dalam perasan rimpang
temulawak 3% (P2), perendaman telur cacing A.galli dalam perasan rimpang
temulawak 4% (P3), perendaman telur cacing A.galli dalam perasan rimpang
temulawak 5% (P4), perendaman telur cacing A.galli dalam larutan mebendazol
(P5). Masing masing perlakuan terdiri dari empat ulangan, dengan pengamatan
hasil dilakukan setiap hari mulai hari pertama sampai hari ke-10 perendaman. Peubah yang diamati adalah kerusakan sel telur cacing A.galli atau tidak
adanya perkembangan sel telur cacing A.galli. Data disajikan dalam bentuk
persentase dan ditransformasikan ke dalam Arcsin √persentase (%). Data dianalisis dengan uji F dan dilanjutkan dengan Uji Jarak Berganda Duncan untuk mengetahui perlakuan yang terbaik.
Hasil penelitian menunjukkan hasil terbaik pada perlakuan perendaman telur cacing A.galli dalam larutan mebendazol (P5) yang tidak berbeda nyata dengan
perasan rimpang temulawak 5% (P4) yang merupakan hasil terbaik kedua.
Perlakuan perendaman telur A.galli dalam perasan rimpang temulawak 4% (P3)
dapat merusak telur A.galli dan merupakan hasil terbaik ketiga. Perlakuan yang
lain dapat pula merusak telur cacing A.galli dengan hasil terendah pada
KATA PENGANTAR
Puji syukur yang tak terhingga penulis panjatkan kehadirat Allah SWT berkat
rahmat dan hidayah-NYA serta shalawat serta salam bagi junjungan kita Nabi
Muhammad SAW sehingga penelitian dan penulisan skripsi dengan judul
"Perbandingan Efektifitas Pemberian Perasan Rimpang Temulawak (Curcuma
xanthorriza, R) dengan Mebendazol terhadap Viabilitas Telur Cacing Ascaridia
galli secara in vitro" dapat terselesaikan dengan baik.
Penulis menyadari bahwa keberhasilan penelitian hingga penulisan skripsi
tidak lepas dari bantuan dan dukungan dari semua pihak. Dengan rasa hormat,
penulis menyampaikan ucapan terima kasih dan penghargaan kepada :
Prof. Dr. Ismudiono, MS., Drh selaku Dekan Fakultas Kedokteran
Hewan Universitas Airlangga.
Dr. M. Zainal Arifin, MS., Drh selaku Dosen Pembimbing pertama dan
Prof. Dr. Setiawan Koesdarto, MSc., Drh selaku Dosen Pembimbing
kedua yang telah bersedia meluangkan waktu, tenaga dan pikirannya
untuk memberikan bimbingan dan pengarahan selama pelaksanaan
penelitian dan penulisan skripsi ini.
Sri Agus Sudjarwo, Ph.D., Drh, Tutiek Juniastuti, M.Kes., Drh dan
Ririen Ngesti Wahyuti, M.Kes., Drh selaku Tim penguji yang telah
memberikan saran dan masukan yang sangat berguna bagi penyelesian
Keluarga besar Yayasan Tunas Paratama Bhakti yang telah
memberikan bimbingan, bantuan moril dan materiil sejak Sekolah
Dasar hingga Perguruan Tinggi.
Ibunda Sri Asih dan Ayahanda Miselan Alm. serta Kakak-kakakku
Mas Koko dan Mas Aris tercinta, atas segala bantuan, dorongan
semangat dan doa restu yang diberikan selama pendidikan sampai
berakhir.
Andi Kristian Maranatha Purba yang telah meluangkan waktu, doa,
dukungan dan kesabarannya mulai penelitian hingga selesainya
penulisan skripsi ini.
Acie’, Dido, Irma, Novia, Diana, Alitha, Uwi’, Mb.Dahlia, Pi 5,
teman-teman angkatan 2001 dan Asrama AABU, serta semua pihak
yang tidak dapat penulis sebutkan satu persatu yang telah memberikan
bantuan, baik secara langsung maupun tidak langsung hingga
terselesaikannya skripsi ini.
Akhirnya penulis menyadari bahwa penulisan skripsi ini masih jauh dari
sempurna. Semua kritik dan saran sangat penulis harapkan demi kesempurnaan
skripsi ini. Penulis berharap semoga skripsi ini dapat bermanfaat bagi
perkembangan dunia Kedokteran Hewan pada khususnya dan ilmu pengetahuan
pada umumnya.
Surabaya, Januari 2006
DAFTAR ISI
Halaman
DAFTAR TABEL ……… ix
DAFTAR GAMBAR ……… xi
DAFTAR LAMPIRAN ……….. xii
BAB I PENDAHULUAN………... 1
1.1 Latar Belakang ……… 1
1.2 Perumusan Masalah ……… 3
1.3 Landasan Teori ………... 4
1.4 Tujuan Penelitian ………... 4
1.5 Manfaat Penelitian ………. 4
1.6 Hipotesis Penelitian ……… 5
BAB II TINJAUAN PUSTAKA ……… 6
2.1 Temulawak(Curcuma xanthorriza, R) ……….. 6
2.1.1 Sistematika Temulawak ………... 6
2.1.2 Nama Daerah dan Ekologi Penyebaran …….. 6
2.1.3 Morfologi Tanaman Temulawak ………. 7
2.1.4 Ciri-ciri Rimpang Temulawak ……….. 8
2.1.5 Kandungan Rimpang Temulawak ……… 8
2.1.6 Kegunaan dan Pemanfaatan Temulawak …….. 9
2.2 Ascaridiasis ………...… 9
2.2.1 Klasifikasi Ascaridia galli ……… 10
2.2.2 Habitat dan Morfologi ………... 10
2.2.3 Telur Ascaridia galli ………. 11
2.2.4 Siklus Hidup ……….. 11
2.2.5 Patogenesis dan Gejala Klinis Infeksi Ascaridia galli ……… 13
2.2.6 Daya Tahan Ayam terhadap Infeksi Ascaridia galli………. 14
2.2.7 Pengendalian Infeksi Ascaridia galli ………… 15
2.3Mebendazol ……….. 15
BAB III MATERI DAN METODE PENELITIAN ... 17
3.1 Tempat dan Waktu Penelitian ……….. 17
3.2 Materi Penelitian ……….. 17
3.2.1 Sampel Penelitian ……….. 17
3.2.2 Bahan Penelitian ……… 17
3.2.3 Alat-alat Penelitian ……… 17
3.3 Metode Penelitian ………. 18
3.3.1 Penentuan Rentang Konsentrasi Perasan Rimpang Temulawak ………. 18
3.3.2 Pembuatan Perasan Rimpang Temulawak …… 19
3.3.4 Penentuan Karakteristik Telur Cacing
yang Rusak ……….... 20
3.3.5 Prosedur Penelitian ………. 20
3.3.6 Peubah yang Diamati ………... 21
3.3.7 Rancangan Percobaan dan Analisis Data ……… 22
BAB IV HASIL PENELITIAN ………24
BAB V PEMBAHASAN ……….. 29
BAB VI KESIMPULAN DAN SARAN ………... 33
6.1 Kesimpulan ……….. 33
6.2 Saran ………. 33
RINGKASAN ………. 34
DAFTAR PUSTAKA ………. 36
DAFTAR TABEL
Tabel Halaman
1. Persentase Rata-rata dan Standar Deviasi Kerusakan Telur Cacing A.galli pada berbagai Perlakuan Sebelum
Transformasi ... 24
2. Persentase Rata-rata dan Standar Deviasi Kerusakan Telur Cacing A.galli pada berbagai Perlakuan Sesudah
Transformasi ………. 25
3. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-1 ……….. 39 4. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 39
5. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-2 ………... 40 6. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 40
7. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-3 ………... 41 8. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 41
9. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-4 ………... 42 10. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
11. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-5 ………... 43 12. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 43
13. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-6 ………... 44 14. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 44
15. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-7 ………... 45 16. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 45
17. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-8 ………... 46 18. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 46
19. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-9 ………... 47 20. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
Duncan ………. 47
21. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan
Telur A.galli pada Perendaman Hari ke-10 ………. 48 22. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang
Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda
DAFTAR GAMBAR
Gambar Halaman 2 Tanaman Temulawak (Curcuma xanthorriza, R) dan
Rimpang Temulawak ………... 7
3 Bagan Alir Penelitian ……….. 23
4.1 Grafik Persentase Kerusakan Telur Cacing Ascaridia galli dalam Berbagai Perlakuan Pada Perendaman Hari ke-1 sampai Hari ke-10 ………... 27
4.2 Telur Cacing Ascaridia galli dalam Larutan NaCl Fisiologis
yang Mengalami Perkembangan ……… 28
DAFTAR LAMPIRAN
Lampiran Halaman 1. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-1 ……… 39 2. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-2 ……… 40 3. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-3 ……… 41 4. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-4 ……… 42 5. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-5 ……… 43 6. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-6 ……… 44 7. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-7 ……… 45 8. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-8 ……… 46 9. Analisis Statistik Kerusakan Telur Cacing A.galli dari
berbagai Perlakuan pada Perendaman Hari ke-9 ……… 47
10. Analisis Statistik Kerusakan Telur Cacing A.galli dari
BAB I
PENDAHULUAN
1.1 Latar Belakang Penelitian
Peningkatan pendapatan penduduk dan bertambahnya pengertian masyarakat
terhadap peranan gizi bagi kesehatan saat ini meningkatkan kebutuhan masyarakat
akan protein hewani. Bagi peternak, untuk mengimbangi pemenuhan kebutuhan
tersebut adalah dengan meningkatkan produksi dan kesehatan ternak. Salah satu
faktor yang penting adalah usaha penanggulangan penyakit. Beberapa jenis
penyakit yang disebabkan oleh cacing dinilai cukup merugikan, meskipun jarang
menimbulkan kematian namun bersifat kronik, antara lain dapat mengakibatkan
penurunan bobot badan dan terhambatnya pertumbuhan.
Di Indonesia, tingkat kejadian penyakit oleh parasit cacing cukup tinggi.
Kondisi lingkungan Indonesia yang beriklim tropis dengan temperatur dan
kelembaban tinggi merupakan lingkungan yang sangat baik dan menguntungkan
untuk perkembangan cacing terutama yang memerlukan tanah untuk penularannya
(Tjitra, 1991). Infeksi cacing yang sering menyerang ternak ayam dan cukup
banyak menimbulkan kerugian adalah Ascaridiasis yang disebabkan oleh
Ascaridiagalli (Soulsby, 1986).
Upaya pengendalian infeksi cacing dengan obat cacing yang ada di pasaran
sampai saat ini hasilnya belum optimal, karena obat cacing umumnya terbukti
mampu membunuh cacing dewasa, namun belum tentu secara optimal mampu
cacing yang mati akibat obat cacing belum tentu membuat telur yang berada bebas
dalam usus halus induk semang mati dan kemungkinan besar masih efektif
sebagai sumber penular pada unggas lainnya (Oka, 2003). Saat ini telah banyak
obat sintetik yang berkhasiat untuk pengobatan penyakit cacing dan telah beredar
di pasaran diantaranya adalah mebendazol, yang merupakan benzimidazol sintetik
yang mempunyai aktifitas antelmintik berspektrum luas dan insiden efek samping
yang rendah (Katzung, 1994). Namun keadaan sosial masyarakat yang umumnya
masih relatif rendah, maka pemakaian obat sintetik masih mengalami banyak
hambatan, diantaranya harga yang relatif mahal dan kesulitan dalam
mendapatkannya.
Pengobatan tradisional merupakan budaya yang tetap digunakan oleh
masyarakat dari berbagai tingkatan ekonomi di seluruh dunia, dalam upaya
menyembuhkan penyakit dan menjaga kesehatan diri dan hewan peliharaannya.
Dewasa ini pemanfaatan tanaman obat semakin digalakkan, karena selain
memberikan alternatif atas kebutuhan obat yang mudah diperoleh, murah
harganya dan berkhasiat juga dapat sekaligus memanfaatkan bahan yang tersedia
di alam terutama di lingkungan peternak. Hal ini menguntungkan bagi masyarakat
peternak di Indonesia, yang mayoritas tinggal di desa. Di Indonesia terdapat
kurang lebih 40.000 jenis tumbuhan, dan baru sekitar 1000 jenis tumbuhan
(2,5 %) yang sudah dimanfaatkan sebagai tanaman obat (Sumarni, 1994).
Beberapa tanaman obat yang dipergunakan sebagai obat cacing antara lain
rimpang temulawak (Curcuma xanthorriza, R). Mulyaningsih (1989) yang dikutip
mematikan cacing tambang pada anjing secara in vitro. Subekti (1990)
menyatakan bahwa perasan temulawak dapat menurunkan jumlah Egg Per Gram
(EPG) pada ayam yang terinfeksi cacing A.galli. Wibawa (1992) juga menyatakan
dalam penelitiannya bahwa jika ditinjau dari segi efektifitasnya perasan rimpang
temulawak dengan konsentrasi 100% dan 50% cukup efektif mematikan cacing
Haemonchus spp. Di dalam rimpang temulawak terdapat suatu zat yang
berkhasiat sebagai antelmintik yaitu minyak atsiri dan kurkumin. Berdasarkan
manfaatnya sebagai obat cacing, perlu dilakukan pengkajian lebih lanjut mengenai
pengaruh pemberian perasan rimpang temulawak terhadap viabilitas telur cacing
A.galli secara in vitro dibandingkan dengan mebendazol sebagai kontrol obat.
1.2 Perumusan Masalah
Berdasarkan latar belakang, maka dirumuskan permasalahan sebagai berikut:
1. Berapa besar konsentrasi efektif dari berbagai tingkatan konsentrasi perasan
rimpang temulawak yang dapat mempengaruhi viabilitas telur cacing
A.galli dibandingkan dengan mebendazol secara in vitro?
2. Hari ke berapa berbagai tingkatan konsentrasi perasan rimpang
temulawak sudah dapat mempengaruhi viabilitas telur cacing A.galli
dibandingkan dengan mebendazol secara in vitro?
1.3 Landasan Teori
Alternatif pengobatan Ascaridiasis dengan obat tradisional diperlukan untuk
satu bahan antelmintik yang berasal dari dari tumbuh-tumbuhan yang dapat
dipakai untuk memberantas infeksi cacing adalah rimpang temulawak (Subekti,
1990). Rimpang temulawak selain kaya akan zat pati juga mengandung kurkumin
dan minyak atsiri yang mempunyai kegunaan antara lain sebagai bahan antiseptik,
analgesik, sedatif maupun obat cacing {Guenter (1988) yang dikutip Setiawan
(1994).
1.4 Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Mengetahui konsentrasi efektif dari berbagai tingkatan konsentrasi
perasan rimpang temulawak yang dapat mempengaruhi viabilitas telur
cacing A.galli dibandingkan dengan mebendazol secara in vitro.
2. Mengetahui hari ke berapa berbagai tingkatan konsentrasi perasan
rimpang temulawak sudah dapat mempengaruhi viabilitas telur cacing
A.galli dibandingkan dengan mebendazol secara in vitro.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi kepada
masyarakat tentang manfaat rimpang temulawak sebagai salah satu obat
alternatif untuk mencegah dan membasmi cacing A.galli beserta telurnya dalam
upaya peningkatan kesehatan ternak ayam untuk menghasilkan produksi yang
1.6 Hipotesis Penelitian
Hipotesis yang diajukan dalam penelitian ini adalah :
1. Terdapat perbedaan efektifitas dari berbagai tingkatan konsentrasi perasan
rimpang temulawak terhadap viabilitas telur cacing A.galli dibandingkan
dengan mebendazol secara in vitro.
2. Terdapat perbedaan waktu dari berbagai tingkatan konsentrasi perasan
rimpang temulawak terhadap viabilitas telur cacing A.galli dibandingkan
BAB II
TINJAUAN PUSTAKA
2.1 Temulawak (Curcuma xanthorriza, Roxb)
Temulawak diperkenalkan pertama kali oleh Roxburg pada tahun 1810 dengan
nama Curcuma xanthorriza. Tanaman ini mudah dibedakan dari temu-temu lain,
karena mempunyai induk rimpang terbesar diantara familinya (IPTEKnet, 2002).
2.1.1 Sistematika Temulawak
Sistematika tanaman temulawak menurut Backer dan Bakhuizen (1968) yang
dikutip oleh Wibawa (1992) adalah sebagai berikut:
Filum : Spermatophyta
Sub Filum : Angiospermae
Kelas : Monocotyledonae
Ordo : Zingiberales
Famili : Zingiberaceae
Genus : Curcuma
Spesies : Curcuma xanthorriza, Roxb
2.1.2 Nama Daerah dan Ekologi Penyebaran
Temulawak merupakan tanaman asli Indonesia, kemudian menyebar ke
Malaysia, Thailand, Birma, India, Philipina. Di Indonesia, tanaman ini dapat
termasuk Bali. Di pulau Jawa, temulawak dapat tumbuh liar di hutan jati maupun
dibudidayakan di padang alang-alang dan tegalan. Nama daerah dari temulawak
antara lain: temu lawak (Melayu), koneng gede (Sunda), temulawak (Jawa), temu
labak (Madura) (IPTEKnet, 2002).
2.1.3 Morfologi Tanaman Temulawak
Temulawak termasuk tanaman tahunan merumpun, tanaman ini berbatang
semu dan habitusnya dapat mencapai ketinggian 2-2,5 meter. Tiap rumpun
tanaman terdiri atas beberapa tanaman (anakan) dan tiap tanaman memiliki 2-9
helai daun. Daun tanaman temulawak bentuknya panjang dan agak lebar. Lamina
daun dan seluruh ibu tulang daun bergaris hitam, tiap helai daun melekat pada
tangkai daun yang posisinya saling menutupi secara teratur (IPTEKnet, 2002).
A B Gambar 2. A. Tanaman Temulawak (Curcuma xanthorriza, R)
2.1.4 Ciri-ciri Rimpang Temulawak
Rimpang temulawak berukuran paling besar diantara rimpang-rimpang dari
semua jenis Curcuma. Bentuk rimpang membulat dan dari luar berwarna kuning
tua atau coklat kemerahan. Induk rimpang bercabang-cabang banyak dan kuat.
Anak rimpang beraneka ragam dan umumnya berwarna lebih muda dibandingkan
dengan rimpang induk. Bidang irisan berwarna jingga kecoklatan, melengkung
tidak beraturan dan sering ada tonjolan melingkar pada batas antara silinder pusat
dengan korteks. Zat warna kuning kecoklatan rasanya pahit tajam (IPTEKnet,
2002).
2.1.5 Kandungan Rimpang Temulawak
Rimpang temulawak segar mengandung 75 persen air, minyak atsiri, lemak,
zat warna (pigmen), resin, selulose, pentosa, pati, mineral, zat penyebab rasa pahit
dan beberapa kandungan senyawa kimia antara lain berupa fellandrean dan
tumerol (minyak menguap), kemudian kamfer, glukosida, foluymetik karbinol dan
kurkumin (IPTEKnet, 2002). Efek farmako yang ditimbulkan antara lain: anti
sembelit, tonikum, diuretik, fungstatik dan bakteriostatik (Anonimus, 2005).
2.1.5.1 Tinjauan tentang Minyak Atsiri
Minyak Atsiri mengandung flavonoida yang berkhasiat menyembuhkan
radang, minyak atsiri juga membunuh mikroba (Anonimus, 2005). Malingre
temulawak (Curcuma xanthorriza, R) yang terdiri dari: p-tolimetilkarbinol, alfa
zingiberen, sikloisoprenmirsen, kurlon, turmeron, ar-tumeron,
tetrahidro-p-asetil-toluol, santonizol dan isofuranogermaliren.
Berdasarkan gejala yang ditimbulkan oleh cacing diduga cara kerja minyak
atsiri adalah dengan menghambat hantaran neuromuskuler, yaitu dengan
mendepolarisasikan motor and plate, disertai eksitasi pada cacing, kemudian
mencegah repolarisasi sehingga menyebabkan depolarisasi terus menerus, yang
akhirnya terjadi paralisa otot cacing lalu mati (Setiawan, 1994).
2.1.6 Kegunaan dan Pemanfaatan Temulawak
Sebagai obat tradisional, rimpang temulawak banyak digunakan untuk
pengobatan kejang-kejang, malaria, diare, asma, meningkatkan nafsu makan,
produksi ASI, radang ginjal, peluruh batu empedu dan cacing tambang. Selain itu
temulawak juga dapat digunakan sebagai obat flu burung (IPTEKnet, 2002).
2.2 Ascaridiasis
Ascaridiasis adalah salah satu penyakit cacing yang menyerang bangsa unggas
dan menyebabkan kerugian ekonomi yang tinggi. Penyakit ini disebabkan oleh
cacing Ascaridia galli yang berinduk semang pada ayam, kalkun, burung dara, itik
dan angsa. Selain A.galli ditemukan beberapa spesies lain yang berinduk semang
pada berbagai jenis unggas diantaranya A.dissimilis yang berinduk semang pada
ditemukan pada burung puyuh, A.bonasae yang berinduk semang pada sejenis
ayam hutan dan A.numidae yang ditemukan pada burung merak. Infeksi A.galli
dapat menyerang ternak ayam pada semua umur terutama ayam umur 1-3 bulan
(Soulsby, 1986).
2.2.1 Klasifikasi Ascaridia galli
Nama lain dari A.galli adalah A.perspicillum atau A.lineata. Cacing ini disebut
juga Heterakis lineata atau Heterakis inplexa (Schrank, 1780; yang dikutip oleh
Hofstad et al. 1984).
Soulsby (1986) mengklasifikasikan cacing A.galli secara taksonomi dengan
sistematika sebagai berikut :
Filum : Nemathelmintes
Kelas : Nematoda
Sub kelas : Phasinidia, Chitwood dan Chitwood (1933)
Ordo : Ascaridida, Skrjabin dan Schula (1940)
Sub ordo : Ascaridata, Skrjabin (1915)
Super famili : Ascaridoedea, Railliet dan Henry (1915)
Famili : Ascaridea, Daird (1953)
Genus : Ascaridia
2.2.2 Habitat dan Morfologi
Ascaridia galli merupakan cacing Nematoda unggas yang cukup besar. Bentuk
tubuhnya gilig dengan warna putih kekuningan yang rata. Mempunyai tiga bibir
besar dan esofagusnya tidak mempunyai bulbus posterior (Soulsby, 1986). A.galli
menyerang usus halus unggas dan kadang-kadang bisa ditemukan pada esofagus,
tembolok, ventrikulus dan saluran telur (Hofstad etal, 1984). Populasi cacing
A.galli di dalam usus halus ayam lebih banyak betina daripada jantan (Suweta
dkk, 1980).
Cacing jantan berukuran panjang 30-80 mm dan diameter 0,5-1,2 mm. Cacing
ini mempunyai ciri precloacal sucker berbentuk sirkuler dengan kutikula yang
tebal. Mempunyai papila-papila pada tepi tubuh posterior. Bagian ekor
mempunyai lapisan yang halus dan memiliki 10 pasang papila yang pendek dan
tebal. Spikula sama panjang berukuran 1-2,4 mm. Sedangkan cacing betina
berukuran panjang 60-120 mm dengan diameter 0,9-1,8 mm. Vulva terdapat pada
bagian anterior tubuh (Levine, 1990).
2.2.3 Telur Ascaridia galli
Telur berbentuk oval berukuran 75-80 x 45-50 µm berselubung halus
dan tidak bersegmen ketika dikeluarkan. Pada tempat lembab, bersuhu
32,2-38,8 °C dan terhindar dari sinar matahari, telur cacing akan mengalami
optimal, telur cacing dapat bertahan hidup selama 249 hari dan telur yang infektif
dapat bertahan sampai 3 bulan (Urquhart et al, 1987).
2.2.4 Sikus Hidup
Siklus hidup Ascaridia pada ayam berlangsung 35 hari (Akoso, 1998). Siklus
hidup cacing ini tidak membutuhkan induk semang perantara. Penularan cacing
tersebut biasanya melalui pakan, air minum, litter atau bahan lain yang tercemar
oleh feses yang mengandung telur infektif. Telur A.galli dikeluarkan
bersama-sama feses induk semang dan berkembang menjadi stadium infektif di tempat
terbuka dalam waktu 10 hari atau lebih. Temperatur yang cukup tinggi serta
kelembaban dan kadar oksigen yang tinggi mempercepat perkembangan larva
stadium kedua yang sangat resisten terhadap kondisi yang tidak menguntungkan
akan mampu bertahan hidup lebih dari 3 bulan di lingkungan yang teduh
(Urquhart et al, 1987).
Infeksi terjadi karena telur infektif tertelan bersama pakan atau minuman,
selain itu dapat melalui cacing tanah yang menelan telur A.galli, kemudian cacing
tersebut termakan ayam. Telur cacing termakan oleh induk semang akan menetas
dan berkembang menjadi larva stadium ke tiga di dalam usus halus ayam pada
hari ke delapan setelah infeksi, kemudian larva hidup bebas di dalam usus halus.
Pada hari ke 9-10 larva stadium ke tiga menembus mukosa usus halus dan
berkembang menjadi larva stadium ke empat pada hari ke 14-15 setelah infeksi
(Subekti dkk, 2002). Hari ke 17-18 cacing muda akan keluar dari mukosa menuju
Levine, 1990). Cacing dewasa mulai bertelur pada hari ke 100 dan telur-telur
cacing dikeluarkan bersama feses dari induk semang. Seekor cacing dewasa
mampu bertelur lebih kurang 250.000 butir setiap hari (Dunn, 1978).
2.2.5 Patogenesis dan Gejala Klinis Infeksi Ascaridia galli
Penetrasi larva pada mukosa usus akan mengakibatkan kerusakan dinding usus
dan perdarahan usus sehingga ayam akan mengalami anemia dan diare. Cacing
dewasa dalam usus halus akan memakan isi usus dan merusak mukosa usus.
Pada infeksi berat akan menyebabkan penyumbatan lumen usus sehingga
mengganggu peristaltik usus dan mengakibatkan perforasi usus serta dapat
mengakibatkan kematian dari induk semangnya (Soulsby, 1986).
Gejala klinis yang terlihat pada ayam yang menderita Ascaridiasis adalah
nafsu makan menurun, lemah, bulu rontok dan kusam, sayap terkulai serta
mengakibatkan penurunan produksi dan berat badan (Ramadan, 1991).
Soulsby (1986) mengemukakan bahwa gejala klinis yang biasanya tampak
pada ayam yang terinfeksi cacing A.galli adalah: 1) pada ayam-ayam muda
mengakibatkan terjadinya anemia, diare dan menurunnya nafsu makan yang
diakibatkan toksin yang dihasilkan oleh cacing serta rasa haus yang berlebihan; 2)
pada ayam yang sedang berproduksi menyebabkan penurunan produksi telur
sampai berhenti sama sekali, bulu rontok, kusam, kepucatan dan sayap terkulai,
3) pada infeksi yang berat dapat menyebabkan kematian. Sedangkan gejala
patologis pada ayam yang menderita ascaridiasis adalah lesi yang meliputi
perdarahan dan enteritis, yang terjadi akibat adanya penetrasi larva cacing pada
mukosa duodenum. Ayam yang terinfeksi A.galli dalam jumlah besar akan
terjadi kekurangan darah, menurunnya gula darah, peningkatan asam urat,
pengecilan glandula thymus, pertumbuhan terhambat, kelemahan, kekurusan,
diare dan kadang-kadang terjadi kematian (Tabbu, 2002).
2.2.6 Daya Tahan Ayam terhadap Infeksi Ascaridia galli
Tiap individu ayam mempunyai daya tahan yang berbeda-beda terhadap
infeksi cacing tergantung umur, jenis kelamin, genetika, kondisi gizi ayam dan
jumlah cacing A.galli pada lumen duodenum ayam (Subekti dkk, 2002).
Ayam berumur 3 bulan keatas lebih tahan terhadap infeksi cacing A.galli
dibanding ayam muda (kurang dari 3 bulan), hal ini karena adanya peningkatan
jumlah mukus pada saluran usus halus, peningkatan sel-sel goblet dan sel-sel
leukosit pada mukosa usus ini merupakan perkembangan dari respon tubuh untuk
membentuk ketahanan terhadap perkembangan cacing (Hofstad et al, 1984).
Hewan betina lebih tahan terhadap infeksi cacing Nematoda daripada hewan
jantan. Hal ini karena adanya hormon kelamin betina (estrogen) yang dapat
menstimulir pembentukan lapisan penutup mukosa pada dinding usus,
juga menstimulir Reticulo Endothelial System (RES) yang bertanggung jawab
terhadap pembentukan antibodi {Dobson (1965) yang dikutip Yunus (1994)}.
Soulsby (1986) menyatakan bahwa makanan yang kurang mengandung
vitamin A, vitamin B kompleks, mineral dan protein merupakan faktor
predisposisi infeksi A.galli. Faktor predisposisi yang lain adalah populasi ayam
yang terlalu padat dan litter yang lembab (Tabbu, 2002).
2.2.7 Pengendalian Infeksi Ascaridia galli
Ternak ayam diberikan pakan yang cukup mengandung vitamin A, vitamin B
kompleks, mineral dan diet protein hewan tinggi. Peralatan kandang terutama
tempat pakan dan minum dijaga kebersihannya. Litter kandang dijaga
kebersihannya dan diganti secara periodik. Penggunaan kandang individu
mengurangi infeksi cacing A.galli. Pemberian obat cacing sekali sebulan untuk
mencegahnya (Subekti dkk, 2002). Namun mengingat bahwa lalat dapat bertindak
sebagai vektor mekanik dari telur A.galli, maka pengendalian yang terbaik
terhadap infeksi A.galli adalah kombinasi antara pengobatan preventif dan
manajemen yang optimal, meliputi sanitasi atau desinfeksi ketat dan pembasmian
2.3 Mebendazol
Mebendazol diperkenalkan pertama kali pada tahun 1972 sebagai antelmintik
berspektrum luas untuk cacing Nematoda dan merupakan turunan dari senyawa
benzimidazole sintetik (Anonimus 1995).
Cara kerjanya terhadap cacing adalah: 1) menghambat sintesis mikrotubulus
sehingga parasit mati perlahan-lahan dan dikeluarkan dari usus secara
berangsur-angsur dalam beberapa hari; 2) menghambat glukosa uptake secara irreversibel
sehingga terjadi pengosongan (deplesi) glikogen pada cacing; 3) menghambat
asetilkolinesterase yang menyebabkan terjadinya pemupukan asetilkolin dalam
tubuh cacing sehingga terjadi kekejangan pada tubuh cacing; 4) menurunkan
penyediaan Adenosin Tri Phospat (ATP) untuk hidup cacing mengakibatkan
mobilitas lemah dan cacing akan mati (Katzung, 1994).
Mebendazol dapat menimbulkan sterilitas pada telur cacing Trichuris
trichuria, cacing tambang dan Ascaris sehingga telur cacing gagal berkembang
(Anonimus, 1995).
Mebendazol tidak menyebabkan efek toksik sistemik sehingga aman diberikan
pada penderita dengan anemia maupun malnutrisi. Efek samping terhadap
pemakaian mebendazol hampir tidak ada, hanya kadang-kadang penderita
ascariasis berat terjadi mual, muntah dan nyeri perut. Di pasaran mebendazol
tersedia dalam bentuk tablet dan sirup dengan nama dagang Antelmox®, Vermon®,
Vermoran®, Vermox®. Untuk terapi larva migrans, mebendazol dapat dicobakan
BAB III
MATERI DAN METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Helmintologi Fakultas Kedokteran
Hewan Universitas Airlangga Surabaya. Penelitian dimulai pada tanggal
11 Juli 2005 sampai dengan 14 Agustus 2005.
3.2 Materi Penelitian 3.2.1 Sampel Penelitian
Penelitian ini menggunakan telur cacing A.galli yang diperoleh dengan
mengumpulkan cacing A.galli dewasa dari usus halus segar ayam buras yang
dibeli dari pasar tradisional di Surabaya.
3.2.2 Bahan Penelitian
Bahan-bahan yang digunakan pada penelitian ini terdiri atas rimpang
temulawak, NaCl Fisiologis, Mebendazol sebagai kontrol obat atau pembanding,
Aquades dan Tween 80 sebagai suspensator.
3.2.3 Alat Penelitian
pinset, pipet, gelas Beaker, alat pengaduk, gelas ukur, timbangan, inkubator,
termometer, penyaring, sarung tangan dan mikroskop.
3.3 Metode Penelitian
Penelitian ini dibagi menjadi dua tahap yang meliputi penelitian pendahuluan
dan penelitian sesungguhnya.
Penelitian pendahuluan adalah menentukan rentang konsetrasi perasan
rimpang temulawak yang akan digunakan pada penelitian sesungguhnya, serta
menentukan bagaimana karakteristik telur yang dikatakan rusak.
Penelitian sesungguhnya dilakukan secara in vitro dengan menggunakan
berbagai konsentrasi perasan rimpang temulawak (Curcumaxanthorriza, R) yang
telah ditentukan pada tahap pendahuluan dan dibandingkan dengan obat jadi
mebendazol yang memiliki nama dagang Vermox500 (Janssen, Pharmaceutica)
sebagai antelmintik terhadap viabilitas telur cacing A.galli.
3.3.1 Penentuan Rentang Konsentrasi Perasan Rimpang Temulawak
Dilakukan uji pendahuluan untuk mengetahui rentang perasan rimpang
temulawak yang akan digunakan dalam penelitian sesungguhnya. Uji pendahuluan
dilakukan dengan prinsip:
1. Menggunakan seri dosis dengan pengenceran berkelipatan ganda
3. Dosis diatur sedemikian rupa sehingga memberikan efek dari 0% sampai
100% (Depkes RI, 1979; dikutip Sujoni 2002).
Menurut Thomson (1995) dalam Sujoni (2002), untuk memperoleh
penyebaran data yang baik perlu ditentukan faktor penyebaran dosis yang
menyebabkan kematian 0% sampai 100%. Faktor penyebaran selanjutnya dapat
digunakan untuk menentukan interval dosis yang akan digunakan pada tahap
penelitian sesungguhnya.
3.3.2 Pembuatan Perasan Rimpang Temulawak
Rimpang temulawak segar dicuci dengan air hingga bersih, kemudian
diangin-anginkan hingga kering kurang lebih selama 3 jam, ditimbang baru diparut. Hasil
parutan diperas dan disaring dengan kertas saring, sehingga didapatkan sari
temulawak dengan konsentrasi 100%. Pada penelitian ini dari hasil penimbangan
90 gram temulawak didapatkan 100 ml perasan.
Pada penelitian ini konsentrasi perasan rimpang temulawak yang digunakan
adalah 2%, 3%, 4% dan 5%. Cara membuat perasan rimpang temulawak 2%
adalah sebagai berikut: Sari temulawak dengan konsentrasi 100%, diambil dengan
pipet sebanyak 2 ml dan dimasukkan dalam gelas Beaker kemudian ditambahkan
NaCl fiologis ad 100 ml. Setelah itu diaduk sampai rata. Cara yang sama
dilakukan pula pada konsentrasi yang lain sehingga diperoleh konsentrasi larutan
3.3.3 Penyiapan Telur cacing Ascaridia galli
Cacing A.galli diperoleh dari usus halus segar ayam buras yang menderita
Ascaridiasis. Cacing-cacing tersebut dikumpulkan dalam cawan petri yang
berisi NaCl fisiologis, kemudian di inkubasi pada suhu 37˚C. Setelah 4 jam
inkubasi, telur cacing dipanen. Telur-telur cacing selanjutnya disimpan di
dalam lemari es (4°C) untuk menghambat perkembangan telur, setelah itu dibagi
dalam 24 cawan petri kecil masing-masing sebanyak 100 butir, kemudian baru
diberikan perlakuan. Cara penghitungan telur sebanyak 100 butir sebelumnya
dilakukan percobaan pada penelitian pendahuluan sebanyak 3-4 kali dengan
menghitung jumlah telur dari satu tetes suspensi telur dalam cawan petri kecil dan
dihitung di bawah mikroskop dalam satu lapang pandang.
3.3.4 Penentuan Karakteristik Telur Cacing yang Rusak
Uji pendahuluan dilakukan untuk mengetahui sampai berapa lama sel telur
cacing A.galli mampu berkembang dan bertahan hidup dalam berbagai perlakuan,
serta untuk menentukan kerusakan struktur telur cacing karena pengaruh
masing-masing perlakuan. Gambaran kerusakan telur cacing dapat meliputi kerusakan
dinding sel, kretinasi, piknosis, karyoreksis atau cytolisis. Parameter ini yang
3.3.5 Prosedur Penelitian
Pada penelitian ini volume tiap-tiap perlakuan pada cawan petri adalah 10 ml.
Setiap cawan petri berisi 100 butir telur cacing A.galli. Ulangan yang dilakukan
pada masing-masing perlakuan sebanyak 4 kali. Penelitian ini dibagi menjadi
enam macam perlakuan, yaitu :
Perlakuan I (P0) : Perendaman telur cacing dalam 10 ml larutan NaCl
fisiologis.
Perlakuan II (P1) : Perendaman telur cacing dalam 10 ml perasan rimpang
temulawak dengan konsentrasi 2%.
Perlakuan III (P2) : Perendaman telur cacing dalam 10 ml perasan rimpang
temulawak dengan konsentrasi 3%.
Perlakuan IV (P3) : Perendaman telur cacing dalam 10 ml perasan rimpang
temulawak dengan konsentrasi 4%.
Perlakuan V (P4) : Perendaman telur cacing dalam 10 ml perasan rimpang
temulawak dengan konsentrasi 5%.
Perlakuan VI (P5) : Perendaman dalam 10 ml larutan mebendazol.
Pembuatan larutan mebendazol sebagai kontrol obat pembanding adalah
dengan menggerus tablet Vermox 500 mg hingga halus, kemudian disuspensikan
dalam NaCl fisiologis 100 ml dan diberikan Tween 80 sebanyak 1% (dari volume
100 ml) sebagai suspensator. Konsentrasi mebendazol yang digunakan adalah
NaCl fisiologis ad 100 ml. Masing-masing media diaduk dengan batang pengaduk
kaca sampai merata.
Inkubasi masing-masing perlakuan dalam inkubator dengan suhu 37ºC.
Pengamatan dilakukan untuk mencatat persentase telur cacing yang rusak atau
yang tidak mengalami perkembangan dan dilakukan pada hari pertama
perendaman sampai telur menjadi infektif (10 hari).
3.3.6 Peubah yang Diamati
Banyaknya telur cacing yang rusak dihitung setiap kali pengamatan (hari
pertama sampai 10 hari perendaman). Pemeriksaan telur cacing yang rusak atau
tidak mengalami perkembangan dilakukan dengan cara pengamatan telur-telur
tersebut di bawah mikroskop dengan perbesaran 100x, setiap hari.
3.3.7 Rancangan Percobaan dan Analisis Data
Rancangan penelitian yang digunakan adalah Rancangan Acak Lengkap
(RAL) dengan enam perlakuan dan empat ulangan untuk masing-masing
perlakuan. Data yang diperoleh dianalisis dengan Analisis Varian (Anava)
berdasarkan Uji F. Apabila terdapat pengaruh yang nyata dilanjutkan dengan Uji
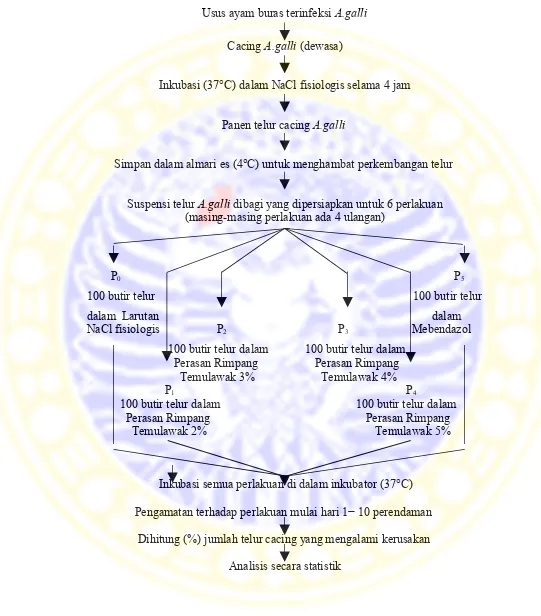
Usus ayam buras terinfeksi A.galli
Cacing A.galli (dewasa)
Inkubasi (37°C) dalam NaCl fisiologis selama 4 jam
Panen telur cacing A.galli
Simpan dalam almari es (4°C) untuk menghambat perkembangan telur
Suspensi telur A.galli dibagi yang dipersiapkan untuk 6 perlakuan
(masing-masing perlakuan ada 4 ulangan)
Inkubasi semua perlakuan di dalam inkubator (37°C)
Pengamatan terhadap perlakuan mulai hari 1− 10 perendaman
Dihitung (%) jumlah telur cacing yang mengalami kerusakan
Analisis secara statistik
BAB IV
HASIL PENELITIAN
Hasil penelitian mengenai Perbandingan efektifitas pemberian perasan
Rimpang Temulawak (Curcuma xanthorriza, R) dengan Mebendazol terhadap
viabilitas Telur Cacing Ascaridia galli secara in vitro diperoleh hasil seperti pada
Tabel 1.
Hasil persentase kerusakan telur cacing tersebut menunjukkan sebaran yang
tidak normal karena terdapat data di bawah 30% dan di atas 70% maka data
tersebut harus ditransformasikan untuk memperoleh sebaran yang normal
(Kusriningrum, 1989). Hasil transformasi selengkapnya tercantum pada Lampiran
1-10, sedangkan Tabel 1 dan Tabel 2 menunjukkan persentase rata-rata kerusakan
telur cacing A.galli sebelum dan sesudah transformasi beserta standar deviasinya
(% ± SD).
Tabel 1. Persentase Rata-rata dan Standar Deviasi Kerusakan Telur Cacing A.galli Pada Berbagai Perlakuan Sebelum Transformasi (% ± SD)
Superskrip yang berbeda pada baris yang sama menunjukkan perbedaan yang nyata (p<0,05)
Tabel 2. Persentase Rata-rata dan Standar Deviasi Kerusakan Telur Cacing A.galli pada berbagai Perlakuan Sesudah Transformasi (% ± SD)
Pada Tabel 1 perendaman dalam NaCl fisiologis (P0), rata-rata kerusakan telur
cacing A.galli tertinggi (11,25%) terdapat pada hari ke-10. Perendaman telur
cacing A.galli dalam perasan rimpang temulawak 2% (P1), rata-rata kerusakan
paling tinggi (52,50%) terdapat pada hari ke-10. Rata-rata kerusakan telur cacing
A.galli dalam perasan rimpang temulawak 3% (P2) tertinggi (56%) juga terdapat
pada hari ke-10. Perendaman dalam perasan rimpang temulawak 4% (P3),
rata-rata kerusakan telur cacing A.galli tertinggi (70,75%) pada hari ke-10.
Perendaman telur cacing A.galli dalam perasan rimpang temulawak 5% (P4),
rata-rata kerusakan paling tinggi (76%) terdapat pada hari ke-10. Rata-rata-rata kerusakan
telur cacing A.galli dalam perendaman dengan larutan mebendazol (P5) yang
tertinggi (79%) juga terdapat pada hari ke-10.
Tabel 1 menunjukkan bahwa pada pengamatan hari ke-1, hasil terbaik
ditunjukkan pada perendaman telur cacing dalam perasan rimpang temulawak 5%
(P4) yang tidak berbeda nyata dengan perlakuan perendaman dalam perasan
temulawak 4% (P3) (p≥0,05). Pada hari ke-2 perendaman, jumlah telur cacing
yang rusak tertinggi masih terdapat pada perasan rimpang temulawak 5%
(P4) namun berbeda nyata dengan perlakuan perasan rimpang temulawak 4% (P3),
3% (P2), 2% (P1), mebendazol (P5) dan NaCl fisiologis (P0). Pada hari ke-3 sampai
ke-6 jumlah telur cacing yang rusak terbanyak adalah perasan rimpang temulawak
5% (P4) kemudian perasan rimpang temulawak 4% (P3) dan disusul mebendazol
Perendaman selama 7 hari, hasil tertinggi pada perendaman dalam perasan
rimpang temulawak 5% (P4), namun berbeda nyata dengan perendaman dalam
larutan mebendazol (P5) sebagai hasil tertinggi kedua.
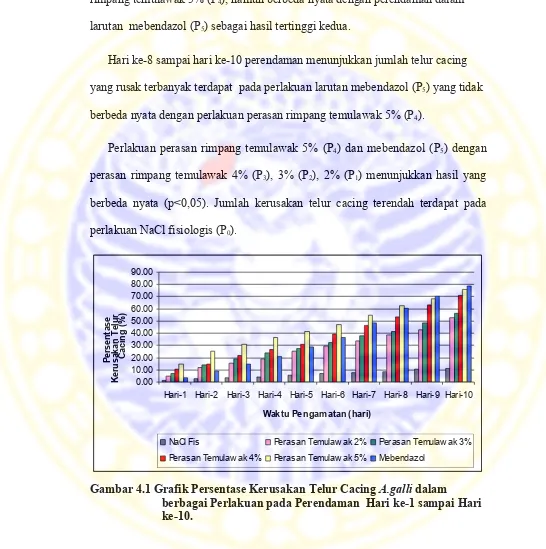
Hari ke-8 sampai hari ke-10 perendaman menunjukkan jumlah telur cacing
yang rusak terbanyak terdapat pada perlakuan larutan mebendazol (P5) yang tidak
berbeda nyata dengan perlakuan perasan rimpang temulawak 5% (P4).
Perlakuan perasan rimpang temulawak 5% (P4) dan mebendazol (P5) dengan
perasan rimpang temulawak 4% (P3), 3% (P2), 2% (P1) menunjukkan hasil yang
berbeda nyata (p<0,05). Jumlah kerusakan telur cacing terendah terdapat pada
perlakuan NaCl fisiologis (P0).
0.00
Hari-1 Hari-2 Hari-3 Hari-4 Hari-5 Hari-6 Hari-7 Hari-8 Hari-9 Hari-10
Waktu Pengam atan (hari)
NaCl Fis Perasan Temulaw ak 2% Perasan Temulaw ak 3%
Perasan Temulaw ak 4% Perasan Temulaw ak 5% Mebendazol
Gambar 4.1 Grafik Persentase Kerusakan Telur Cacing A.galli dalam
berbagai Perlakuan pada Perendaman Hari ke-1 sampai Hari ke-10.
Gambar-gambar hasil pengamatan telur cacing A.galli pada berbagai macam
A B
Gambar 4.2 Telur Cacing A.galli pada Larutan NaCl Fisiologis yang Mengalami Perkembangan, perbesaran 100x
Keterangan:
A. Perkembangan telur pada stadium 16 sel B. Perkembangan telur pada stadium morula
C D
Gambar 4.3 Telur Cacing A.galli dalam berbagai Perlakuan yang Tidak Mengalami Perkembangan atau Rusak setelah Perendaman, perbesaran 100x
Keterangan:
BAB V PEMBAHASAN
Pada penelitian ini digunakan rimpang temulawak sebagai medium untuk
perendaman pada telur cacing A.galli yang dilakukan secara in vitro. Selanjutnya
dilakukan penghitungan terhadap kerusakan telur cacing A.galli akibat
perendaman dengan medium perasan tesebut. Sel telur yang mengalami kerusakan
akibat perlakuan menunjukkan tanda perubahan bentuk struktur lapisan membran
dalam, kretinasi dinding telur, pelarutan sel (cytolisis) dan pecahnya dinding telur.
Hasil analisis statistik menunjukkan bahwa perasan rimpang temulawak
mempunyai efek yang nyata terhadap viabilitas telur cacing A.galli secara in vitro.
Semakin tinggi konsentrasi perasan rimpang temulawak yang diberikan semakin
besar pula jumlah telur A.galli yang mengalami kerusakan. Hal ini membuktikan
perasan rimpang temulawak mempunyai daya antelmintik yang semakin tinggi
dengan bertambah besarnya konsentrasi yang diberikan. Perasan rimpang
temulawak 5% merupakan konsentrasi perasan rimpang temulawak terbaik yang
sebanding dengan mebendazol dalam merusak telur cacing A.galli sedangkan
perasan rimpang temulawak 4% merupakan konsentrasi perasan rimpang
temulawak terbaik kedua (Tabel. 1 dan 2). Pada penelitian ini digunakan
mebendazol sebagai pembanding untuk mengetahui konsentrasi perasan rimpang
temulawak yang paling efektif dalam mempengaruhi viabilitas telur cacing A.galli
Daya antelmintik perasan rimpang temulawak diduga terdapat pada zat yang
terkandung dalam rimpang temulawak yakni minyak atsiri. Hal ini sesuai
pendapat Guenter (1988) yang dikutip oleh Setiawan (1994) bahwa rimpang
temulawak mengandung kurkumin dan minyak atsiri yang mempunyai kegunaan
antara lain sebagai antiseptik, analgesik, sedatif, maupun obat cacing
(antelmintik).
Dari hasil pengamatan kerusakan telur cacing A.galli yang terbanyak adalah
perubahan bentuk struktur lapisan membran dalam dengan tanda-tanda pelarutan
sel (cytolisis). Sel telur dan struktur lapisan membran dalam mengalami
pengkerutan dan kemudian larut pada keesokan harinya. Telur yang tidak berisi
sel (kosong) dan berdinding tipis pada keesokan harinya semakin melebar dan
hilang atau larut pada hari berikutnya, seperti terdapat kebocoran pada dinding sel
telur cacing A.galli. Dari hasil pengamatan diduga kerusakan membran sel telur
cacing tersebut yang menyebabkan kematian sel. Kerusakan membran sel
menyebabkan ion anorganik esensial, nukleotida, koenzim, dan asam amino
merembes ke luar sel. Kerusakan tersebut juga menyebabkan hambatan masuknya
materi esensial yang dibutuhkan sel, kemudian terjadi kematian sel (Volk dan
Wheeler, 1988).
Diduga permeabilitas selektif membran sel telur cacing A.galli terganggu karena
pengaruh pemberian perasan rimpang temulawak. Kandungan flavonoida minyak
atsiri yang merupakan derivat fenol bekerja mendenaturasi protein dan merusak
membran sitoplasma sel telur yang terdiri dari protein dan lemak sehingga terjadi
kemudian mengganggu fungsi membran mitokondria sebagai alat pengangkutan
elektron dan enzim. Organel sel seperti mitokondria merupakan organ yang
mensuplai lebih dari 95% energi sel. Energi pada sel digunakan untuk proses
transportasi, pertumbuhan dan pembelahan. Masuknya fenol dalam mitokondria
akan menyebabkan terdenaturasinya ensim-ensim reaksi pernafasan pada
membran mitokondria. Kejadian tersebut mengakibatkan berkurangnya energi
untuk proses pembelahan dan perkembangan sel telur cacing A.galli menjadi
terhambat, sehingga akhirnya embrio tidak terbentuk {Guyton (1991); Ganong
(1991) yang dikutip oleh Novianto (2002)}
Efektifitas mebendazol sebagai antelmintik yang berspektrum luas adalah
menyebabkan kerusakan struktur sub-seluler dan menghambat sekresi
asetilkolinesterase cacing. Obat ini juga menghambat ambilan glukosa secara
ireversibel. Sehingga terjadi pengosongan (deplesi) glikogen pada cacing,
sehingga cacing akan mati perlahan-lahan (Katzung, 1994).
Digunakan larutan NaCl fisiologis dalam penelitian ini dengan maksud untuk
menyetarakan kondisi telur cacing dalam cairan tubuh hewan tanpa pemberian
makanan. Ion natrium sangat diperlukan oleh makhluk hidup, fungsi utamanya
dalam tubuh adalah mempertahankan tekanan osmotik cairan tubuh, yang
berlebihan.
Pada media NaCl fisiologis beberapa telur cacing A.galli dapat bertahan hidup dan
mengalami perkembangan hingga terbentuk larva pada hari ke enam, hal ini
menunjukkan bahwa NaCl fisiologis adalah media yang sesuai bagi
pembanding. Meskipun telah terjadi kerusakan telur cacing A.galli dalam kontrol
NaCl fisiologis pada hari pertama namun kerusakan tersebut menunjukkan hasil
yang sangat berbeda nyata dengan perlakuan perasan rimpang temulawak 2%
sebagai konsentrasi terendah dalam penelitian tersebut, hal ini menunjukkan
bahwa kerusakan memang disebabkan oleh perlakuan dengan perasan rimpang
temulawak. Kerusakan telur cacing A.galli dalam kontrol NaCl fisiologis tersebut
mungkin disebabkan kelalaian peneliti dalam menjaga kelembaban saat proses
penyiapan telur cacing A.galli dan menjaga suhu inkubator agar tetap stabil.
Sesuai dengan pendapat Levine (1990) bahwa salah satu faktor yang
mempengaruhi perkembangan telur infektif adalah suhu dan kelembaban.
Ditinjau dari efektitasnya, perasan rimpang temulawak dengan konsentrasi 5%
mempunyai kemampuan yang optimal dalam mempengaruhi kerusakan sel telur
cacing A.galli sebesar (76%) yang sebanding dengan mebendazol (79%). Hal ini
membuktikan bahwa perasan rimpang temulawak mempunyai daya antelmintik
yang baik terhadap viabilitas telur cacing A.galli secara in vitro.
BAB VI
KESIMPULAN DAN SARAN
6.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan, maka disimpulkan:
1. Pemberian perasan rimpang temulawak konsentrasi 5% (hari ke-8
sampai dengan hari ke-10 perendaman) mempunyai efektifitas terhadap
viabilitas telur cacing A.galli yang sebanding dengan mebendazol secara
in vitro.
2. Kerusakan telur cacing A.galli yang direndam dalam berbagai perlakuan
sudah ditemukan sejak pengamatan hari pertama, namun peningkatan
jumlah kerusakan telur cacing A.galli dalam berbagai perlakuan
mengalami perbedaan setiap harinya.
6.2 Saran
Saran yang dapat diajukan adalah:
1. Perlu dilakukan penelitian lebih lanjut mengenai bahan aktif dalam
rimpang temulawak yang mampu merusak telur cacing A.galli, sehingga
dapat digunakan untuk keperluan pengobatan pada telur cacing dari genus
yang lain.
Diperlukan rangkaian tentang dosis respon, efek samping, toksisitas, bentuk dan sediaan yang tepat dari rimpang temulawak sehingga dapat meningkatkan efisiensi
RINGKASAN
INDAH TRI SUSANTI. Perbandingan Efektifitas Pemberian Perasan
Rimpang Temulawak (Curcuma xanthorriza, R) dengan Mebendazol terhadap
Viabilitas Telur Cacing Ascaridia galli secara in vitro dibawah bimbingan
Dr. M.Zainal Arifin, MS., drh sebagai dosen pembimbing pertama dan Prof.Dr. Setiawan Koesdarto, MSc., drh sebagai dosen pembimbing kedua.
Penelitian ini bertujuan untuk mengetahui efektifitas perasan rimpang
temulawak sebagai antelmintik terhadap viabilitas telur cacing A.galli. Penelitian
dilakukan selama 5 minggu, dimulai pada tanggal 11 Juli 2005 sampai tanggal 14
Agustus 2005 di Laboratorium Helmintologi Fakultas Kedokteran Hewan
Universitas Airlangga Surabaya.
Sampel dalam penelitian ini adalah telur cacing A.galli yang diperoleh dengan
mengumpulkan cacing A.galli dewasa dari usus halus ayam buras. Cawan petri
masing-masing diberi 100 butir telur cacing A.galli kemudian diberikan
perlakuan, yaitu perasan rimpang temulawak 2%, 3%, 4% dan 5%. Sebagai
kontrol dengan pemberian NaCl fisiologis dan sebagai pembanding menggunakan
larutan mebendazol. Pengamatan terhadap kerusakan telur cacing A.galli
dilakukan setiap hari di bawah mikroskop mulai dari hari pertama sampai hari
Peubah yang diamati adalah kerusakan dinding sel telur cacing A.galli atau
tidak adanya perkembangan sel telur A.galli. Penelitian ini menggunakan
Rancangan Acak Lengkap (RAL) dengan enam perlakuan dan empat ulangan.
Data disajikan dalam bentuk persentase sebelum ditransformasikan, kemudian
dianalisis dengan Analisis Varian menggunakan Uji F dan dilanjutkan dengan Uji
Jarak Berganda Duncan untuk mengetahui perlakuan yang terbaik.
Hasil penelitian menunjukkan bahwa perasan rimpang temulawak sebagai
antelmintik setelah dianalisis dengan Uji F berpengaruh nyata terhadap viabilitas
telur cacing A.galli secara in vitro. Setelah dilanjutkan dengan Uji Jarak Berganda
Duncan menunjukkan bahwa perasan rimpang temulawak dengan konsentrasi 5%
mempunyai nilai efisiensi tertinggi diantara konsentrasi yang lain dan sebanding
dengan mebendazol. Berdasarkan hasil penelitian maka perasan rimpang
DAFTAR PUSTAKA
Akoso, B.T. 1998. Kesehatan Unggas. Penerbit Kanisius. Yogyakarta. 116-120.
Anonimus. 1995. Farmakologi dan Terapi. Edisi IV. Fakultas Kedokteran
Anonimus. 2005. Temulawak. http://www.Aneka Instant/id 17=m.htm
Dunn,A.M. 1978. Veterinary Helminthology 2nd Edition. William Heinemann
Medical Books LTD. London.
Hofstad, M.S.,H.J Barnes, B.W. Calnek, W.N Reid and H.W.Jr Yoder. 1984. Disease of Poultry. 8th Ed.Iowa State University Press.Iowa.USA.
IPTEKnet. 2002. Tanaman Obat Indonesia. Cakrawala IPTEKnet. http://www.iptek.net.id/ind/cakra_obat/tanamanobat.php?id=1
Katzung, B.G. 1994. Farmakologi Dasar dan Klinik – Edisi IV. Penerbit Buku Kedokteran EGC. Jakarta. 844 - 845.
Kusriningrum, R. 1989. Dasar Perancangan dan Percobaan Acak Lengkap. Fakultas Kedokteran Hewan. Universitas Airlangga. Surabaya. 89-142.
Levine, N.D. 1990. Parasitology Veteriner. Gadjah Mada University Press. Yogyakarta.
Novianto, T. 2002. Pengaruh pemberian Perasan Daun Ketepeng Cina (Cassia alata Linn) sebagai Anthelmintika terhadap viabilitas telur cacing Ascaris suum secara in vitro. Skripsi Fakultas Kedokteran Hewan.
Universitas Airlangga. Surabaya.
Oka, I.B.M. 2003. Ovisidal dan Vermisidal Bawang Putih terhadap Telur dan Cacing Ascaridia galli pada Ayam Kampung (Abstr).. Lab.
Parasitologi Fakultas Kedokteran Hewan Universitas Udayana.
Prihandini, A. 2005. Perbandingan Efektifitas Pemberian Infusa Biji Pinang Sirih (Areca catechu L) dengan Mebendazol terhadap Viabilitas Telur Cacing Ascaridia galli secara in vitro, Skripsi Fakultas Kedokteran Hewan .
Universitas Airlangga. Surabaya.
Ramadan, H.H, 1991. Some Phatologicals Biochemical Studies On Experimental Ascariasis in Chichers Exp. Parasitologi 35 (1). (Abstrak).
Retno, F.D. Jahja, J. Suryani, T. 1998. Penyakit-penyakit Penting Pada Ayam. Edisi 4. Penerbit Medion. Bandung
Setiawan, B. 1994. Perbandingan Daya Anthelmintika Minyak Atsiri Rimpang
Temulawak (Curcuma xanthorriza), Temu Ireng (Curcuma
aeruginosa), Temu Giring (Curcuma heyneana) dengan Piperazin
sitrat terhadap cacing Ascaris suum secara in vitro. Skripsi Fakultas
Kedokteran Hewan Universitas Airlangga. Surabaya.
Soulsby, E.J.L. 1986. Helminth, Arthopods and Protozo of Domestic Animal. 7th
Ed. Bailiere Tindall and Cassel. London.
Subekti, S. 1990. Khasiat pemberian Temulawak (Curcuma xanthorriza, R) terhadap Ascariasis pada Ayam. Lembaga Penelitian Universitas Airlangga. Surabaya.
Subekti, S. Koesdarto, S. Mumpuni, S. Puspitawati, H. dan Koesnoto, 2002. Diktat Kuliah Ilmu Penyakit Nematoda Veteriner. Fakultas Kedokteran Hewan. Universitas Airlangga. Surabaya.
Sujoni, 2002. Uji in vitro Ekstrak Buah Pepaya (Carica papaya) terhadap
Mortalitas Cacing Mecistocirrus digitatus. Skripsi Fakultas
Kedokteran Hewan Universitas Airlangga. Surabaya.
Sumarni, S. 1994. Pengujian Manfaat Bahan Alam untuk Pengobatan Cacing Nematoda Usus. Phyto Medika Vol I (IV) : 303-312.
Suweta, I.G.P., I.G.P Putra., I.G Wirat dan A.A.M Ambarwati. 1980. Pengaruh Infestasi 150-950 Telur Cacing A.galli dan Vitamin B-12 terhadap
Performa Ayam Jantan. Risalah (Proceedings) Seminar Penyakit Reproduksi dan Unggas. Institut Pertanian Bogor. Tugu Bogor.
The PoultrySite.com. 2005. The large Roundworm (Ascaridia galli).
http:www.roundworm-large-Ascaridia_Poultry Disease at the PoultrySite_com.htm
Tjitra, E. 1991. Pendidikan penelitian “Soil Transmitted Helminthology di Indonesia”. Cermin Dunia Kedokteran 73: 3-5.
Urquhart, G.M. Armour, J. Duncan, J.L. Dunn, A.M. Jennings, F.W. 1988. Veterinary Parasitology. Departement of Veterinary Parasitology, The Faculty of Veterinary Medicine. The University of Glaskow. Scotland.
Volk, W. A. Wheeler, M.P. 1988. Mikrobiologi Dasar. 5th Edition. Alih Bahasa
Merkham, M.Sc. Penerbit Erlangga.
Wibawa, S.S. 1992. Pengaruh Pemberian Perasan Rimpang Temulawak (Curcuma xanthorriza Roxb) terhadap cacing Haemonchus spp. secara in vitro.
Skripsi Fakultas Kedokteran Hewan. Universitas Airlangga. Surabaya.
Yunus, M. 1994. Efektifitas Interval Pemberian Piperasin Sitrat terhadap
Ascaridia galli pada Ayam Ras Petelur. Lembaga Penelitian
Lampiran 1. Analisis Statistik Kerusakan Telur Cacing A.galli dari berbagai
Jumlah Kuadrat Sisa = 778,2504 – 648,7878 = 129,4626
Kuadrat Tengah Perlakuan = 648,7878 = 129,7575
6 − 1
Kuadrat Tengah Sisa = 129,4626 = 7,1923
6(4−1)
F hitung = 129,7575 = 18,041
7,1923
Tabel 3. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan Telur Cacing A.galli pada Perendaman Hari ke-1
Tabel 4. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda Duncan.
Lampiran 2. Analisis Statistik Kerusakan Telur Cacing A.galli dari berbagai Perlakuan pada Perendaman Hari ke-2
n 5 648,7878 129,7575 18,0411** 2,77 4,25
Sisa 18 129,4626 7,193
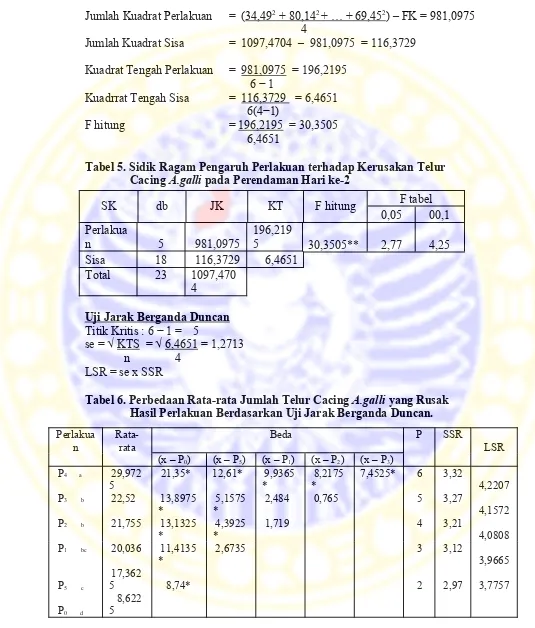
Jumlah Kuadrat Perlakuan = (34,49 2 + 80,14 2 + … + 69,45 2 ) – FK = 981,0975
4
Jumlah Kuadrat Sisa = 1097,4704 – 981,0975 = 116,3729
Kuadrat Tengah Perlakuan = 981,0975 = 196,2195
6 − 1
Kuadrrat Tengah Sisa = 116,3729 = 6,4651
6(4−1)
F hitung = 196,2195 = 30,3505
6,4651
Tabel 5. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan Telur Cacing A.galli pada Perendaman Hari ke-2
Tabel 6. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda Duncan.
Lampiran 3. Analisis Statistik Kerusakan Telur Cacing A.galli dari berbagai
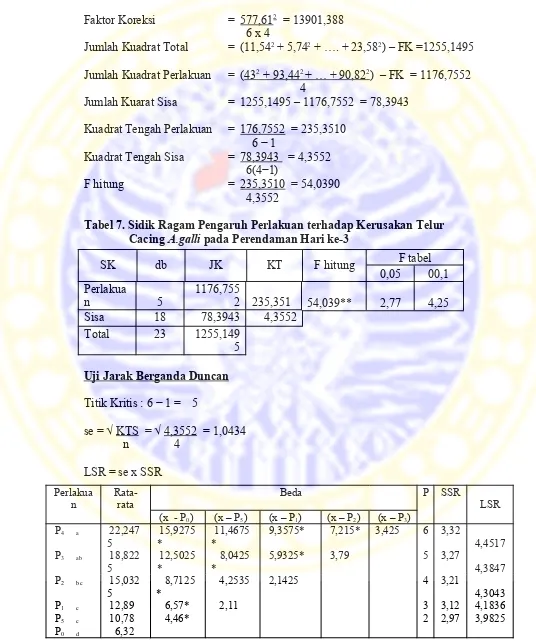
Jumlah Kuarat Sisa = 1255,1495 – 1176,7552 = 78,3943
Kuadrat Tengah Perlakuan = 176,7552 = 235,3510 6 − 1
Kuadrat Tengah Sisa = 78,3943 = 4,3552
6(4−1)
F hitung = 235,3510 = 54,0390
4,3552
Tabel 7. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan Telur Cacing A.galli pada Perendaman Hari ke-3
n 5 1176,7552 235,351 54,039** 2,77 4,25
Sisa 18 78,3943 4,3552
Total 23 1255,149
Tabel 8. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda Duncan.
Lampiran 4. Analisis Statistik Kerusakan Telur Cacing A.galli dari berbagai Perlakuan pada Perendaman Hari ke-4
Faktor Koreksi = 646,912 = 17437,1895
6 x 4
Jumlah Kuadrat Total = (12,922 + 8,132 + …. + 26,562) – FK = 1473,3768
Jumlah Kuadrat Perlakuan = (46,77 2 + 103,32 2 +…+ 108,22 2 )– FK= 1425,7459
4
Jumlah Kuadrat Sisa = 1473,3768 − 1425,7459 = 47,6309
Kuadrat Tengah Perlakuan = 1425,7459 = 285,1492 6 − 1
Kuadrat Tengah Sisa = 47,6309 = 2,6461
6(4−1)
F hitung = 285,1492 = 107,762
2,6461
Tabel 9. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan Telur Cacing A.galli pada Perendaman Hari ke-4
n 5 1425,7459 285,1492 107,7620** 2,77 4,25
se = √ KTS = √ 2,6461 = 0,8133
n 4
LSR = se x SSR
Tabel 10. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda Duncan.
Lampiran 5. Analisis Statistik Kerusakan Telur Cacing A.galli dari berbagai Perlakuan pada Perendaman Hari ke-5
Faktor Koerksi = 725,872 = 21953,,6357
6 x 4
Jumlah Kuadrat Total = (15,342 + 9,982 +….+ 31,952) – FK = 1608,2132
Jumlah Kuadrat Perlakuan = (54,67 2 + 119,98 2 +…+ 128,98 ) – FK=1560,95772
4
Jumlah Kuadrat Sisa = 1608,2132 − 1560,9577 = 47,2555
Kuadrat Tengah Perlakuan = 1560,9577 = 312,1915 6 − 1
Kuadrat Tengah Sisa = 47,2555 = 2,6253
6(4−1)
F hitung = 312,1915 = 118,9165
Tabel 11. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan Telur
Tabel 12. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda Duncan.
Lampiran 6. Analisis Statistik Kerusakan Telur Cacing A.galli dari berbagai Perlakuan pada Perendaman Hari ke-6
Faktor Koreksi = 805,952 = 27064,8084
6 x 4
n 5 1560,9577 312,1915 118,9165** 2,77 4,25
Sisa 18 47,2555 2,6253
Total 23
Jumlah Kuadrat Sisa = 1977,8771 – 1928,1768 = 49,7002
Kuadrat Tengah Perlakuan = 1928,1768 = 385,6353
6 – 1
Kuadrat Tengah Sisa = 49,7002 = 2,7611
6(4–1)
F hitung = 385,6353 = 139,6672
2,7611
Tabel 13. Sidik Ragam Pengaruh Perlakuan terhadap Kerusakan Telur Cacing A.galli pada Perendaman Hari ke-6
Tabel 14. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang Rusak Hasil Perlakuan Berdasarkan Uji Jarak Berganda Duncan.
Faktor Koreksi = 898,82 = 33660,06
6 x 4
Jumlah Kuadrat Total = (16,432 + 14,182 +….+ 43,852) – FK = 2595,8192
Jumlah Kuadrat Perlakuan = (64,5 2 + 142,65 2 +…+ 176,55 ) – FK = 2563,10342
4
Jumlah Kuadrat Sisa = 2595,8192 − 2563,1034 = 32,7158
Kudrat Tengah Perlakuan = 2563,1034 = 512,6206
6 − 1
Kuadrat Tengah Sisa = 32,7158 = 1,8754
6(4−1)
F hitung = 512,6206 = 273,3393
2,7611
Tabel 16. Perbedaan Rata-rata Jumlah Telur Cacing A.galli yang Rusak Hasil PerlakuanBerdasarkan Uji Jarak Berganda Duncan.
Lampiran 8. Analisis Statistik Kerusakan Telur Cacing A.galli dari berbagai Perlakuan pada Perendaman Hari ke-8
Faktor Koreksi = 985,172 = 40439,997
6 x 4
Jumlah Kuadrat Total = (17,462 + 15,342 + ….+ 50,772) – FK = 3470,0095
Jumlah Kuadrat Perlakuan = (67,67 2 + 154 2 + … + 204,94 2 ) – FK = 3428,7941
4
Jumlah Kuadrat Sisa = 3470,0095 − 3428,7941 = 41,2154
Kuadrat Tengah Perlakuan = 3428,7941 = 685,7588
6 − 1
Kuadrat Tengah Sisa = 41,2154 = 2,2897
6(4−1)
F hitung = 685,7588 = 299,4972
2,2897