LAPORAN PRAKTIKUM
KIMIA FARMASI ANALISIS (FA 3211)
PERCOBAAN I
ANALISIS GUGUS FUNGSI
Tanggal Percobaan
: 12 Februari 2015
Tanggal Pengumpulan
: 19 Februari 2015
Disusun oleh:
Stefiani Emasurya Indrajaya (10712038)
Nurinanda Prisky Qomaladewi (10712083)
Asisten:
Putri Dwi Wahyuni (10711025)
LABORATORIUM KIMIA FARMASI ANALISIS
PROGRAM STUDI SAINS DAN TEKNOLOGI FARMASI
SEKOLAH FARMASI
INSTITUT TEKNOLOGI BANDUNG
I. Tujuan Percobaan
1.1Menentukan keberadaan gugus fungsi dari sampel dengan uji analisis gugus fungsi.
II. Prinsip Percobaan
Gugus fungsi adalah kumpulan atom-atom yang berikatan satu sama lain dan memberi peran pada sifat fisikokimia suatu senyawa; seperti kelarutan, keasaman, dan kereaktifan kimia. Gugus fungsi secara umum dianalisis dengan metode kimia dan metode fisikokimia. Analisis metode kimia berarti interaksi kimia antara gugus fungsi dengan pereaksi memberikan warna, bau, endapan, atau kekeruhan yang berbeda untuk masing-masing senyawa. Pereaksi yang digunakan bisa merupakan pereaksi umum dimana memberikan hasil positif dengan beberapa gugus fungsi; atau pereaksi khusus yang hanya memberikan hasil positif untuk gugus fungsi spesifik. Cara yang digunakan dalam metode kimia adalah spot test, dimana sampel dan pereaksi digunakan hanya dalam jumlah 2-3 tetes dalam plat tetes atau tabung reaksi. Analisis kimia biasa disebut dengan uji pendahuluan karena memberikan hasil secara kualitatif. Uji lanjutan atau konfirmasi dilakukan dengan bantuan instrumen khusus dan disebut metode fisikokimia. III. Alat dan Bahan
IV. Metodologi 4.1 Uji Lucas
Sejumlah sampel dimasukkan ke dalam sejumlah peraksi Lucas. Setelah itu, campuran dikocok dan didiamkan. Sampel yang mengandung gugus alkohol sekunder dan tersier akan menghasilkan endapan, sedangkan pada alkohol primer tidak terdapat endapan.
4.2 Uji FeCl3
Sejumlah sampel diteteskan larutan FeCl3, kemudian diamati perubahan warnanya.
4.3 Uji Lieberman
Sejumlah sampel ditambahkan H2SO4 dan NaNO2 (jika sampel mengandung gugus alkohol akan terbentuk warna biru hijau atau biru ungu). Kemudian, campuran diencerkan dengan air, lalu diteteskan NaOH 5%. Terjadi perubahan warna menjadi merah jika sampel mengandung gugus alkohol.
4.4 Uji Pembentukan Hidrazon
Sejumlah sampel ditambahkan 2,4-dinitrofenilhidrazon dan HCl pekat. Jika sampel mengandung gugus karbonil, akan terbentuk endapan jingga coklat.
4.5 Uji Tollens
Sejumlah sampel dimasukkan dalam pereaksi Tollens, terbentuk endapan atau koloidal perak jika sampel mengandung aldehid.
4.6 Uji Kertras Lakmus
Kertas lakmus biru dicelupkan ke dalam sampel. Kertas lakmus akan berubah menjadi merah jika sampel bersifat asam.
4.7 Uji Bikarbonat
Sejumlah sampel ditambahkan larutan NaHCO3 5%. Terbentuk gelembung udara jika sampel mengandung gugus karbonil.
4.8 Uji Fenolftalein
Sejumlah sampel ditambahkan etanol, fenolftalein, dan NaOH 5%. Setelah itu, campuran dipanaskan (warna merah muda hilang saat pemanasan pada sampel yang mengandung gugus ester).
Sejumlah sampel ditambahkan HCl pekat dan NaNO2, kemudian campuran ditambahkan β-Naftol dalan NaOH. Sampel mengandung gugus amina jika terbentuk warna merah atau jingga.
4.10 Uji Baeyer
Sejumlah sampel ditambahkan air dan KMnO4 2%, kemudian campuran dikocok. Sampel mengandung senyawa tidak jenuh jika warna ungu KmNO4 hilang dan terbentuk endapan MnO2.
V. Data dan Pengolahan Data
Jenis Uji Hasil Pengamatan
1. Uji gugus Alkohol Uji Lucas
Kontrol positif : 2-propanol Hasil positif dengan terbentuk kekeruhan setelah waktu cukup lama menunjukkan adanya alkohol sekunder. Kontrol negatif : aseton Hasil negatif tidak terjadi kekeruhan meski telah ditunggu cukup lama karena tidak ada gugus alkohol atau ada gugus alkohol primer. Sampel 18A : hasil negatif tidak terbentuk kekeruhan setelah waktu cukup lama berarti tidak ada gugus alkohol atau ada gugus alkohol primer.
Sampel 18B : hasil negatif tidak terbentuk kekeruhan setelah waktu cukup lama
Hasil negatif dimana seharusnya positif dengan terbentuk warna ungu karena adanya gugus fenol.
Kontrol negatif : -
gugus fenol.
Sampel 18B : hasil negatif tidak terbentuk perubahan warna ungu berarti tidak ada gugus fenol.
Uji Lieberman
Kontrol positif : fenol
Hasil negatif dimana seharusnya positif dengan terbentuk warna merah karena adanya gugus fenol. Kontrol negatif : heksana Hasil negatif tidak terjadi perubahan warna karena tidak ada gugus fenol.
Sampel 18A : hasil negatif tidak terbentuk perubahan warna merah berarti tidak ada gugus fenol.
Sampel 18B : hasil negatif tidak terbentuk perubahan warna merah berarti tidak ada gugus fenol.
3. Uji Gugus Karbonil Uji Hidrazon
Kontrol positif : aseton Hasil positif karena terdapat gugus karbonil dengan terbentuk endapan jingga-coklat.
Kontrol negatif : metanol Hasil negatif tidak terjadi perubahan warna atau endapan karena tidak ada gugus karbonil.
Sampel 18A : hasil negatif tidak terbentuk perubahan warna sama seperti kontrol negatif berarti tidak ada gugus karbonil.
Sampel 18B : hasil positif berarti ada gugus karbonil dengan terbentuk endapan jingga-coklat sama dengan kontrol positif.
Uji Tollens
kehitaman.
Kontrol negatif : heksana Hasil negatif tidak ada perubahan warna atau terbentuknya koloid endapan karena tidak ada gugus karbonil.
Sampel 18A : hasil negatif tidak terjadi perubahan warna sama seperti kontrol negatif berarti tidak ada gugus karbonil.
Sampel 18B : hasil positif berarti ada gugus karbonil dengan terbentuk koloid silver terang.
4. Uji Gugus Karboksil Uji Kertas Lakmus
Kontrol positif : asam asetat Hasil positif karena terdapat gugus karboksil dengan terjadi perubahan kertas lakmus biru menjadi merah. Kontrol negatif : metanol Hasil negatif dimana kertas lakmus biru tidak mengalami perubahan warna.
Sampel 18A : hasil positif dengan terjadi perubahan warna kertas lakmus biru menjadi merah terang dan cepat.
Sampel 18B : hasil positif dengan terjadi perubahan warna kertas lakmus biru menjadi merah.
Uji Bkarbonat
Kontrol positif : asam asetat Hasil positif dengan munculnya gelembung udara sangat banyak menunjukkan adanya gugus karboksil. Kontrol negatif : aseton Hasil negatif tanpa muncul gelembung berarti tidak ada gugus karboksil.
tidak ada gugus karboksil. Sampel 18B : hasil positif dengan muncul gelembung udara meski tidak sebanyak kontrol positif menunjukkan adanya gugus karboksil. 5. Uji Gugus Ester
Uji Fenolftalein
Kontrol positif : etil asetat Hasil positif hilangnya warna merah muda menjadi jernih setelah didiamkan cukup lama dan dipanaskan menunjukkan adanya gugus ester.
Kontrol negatif : aseton Hasil negatif warna merah muda tidak menjadi jernih meski setelah dipanaskan berarti tidak ada gugus ester. Sampel 18A : hasil negatif warna merah muda tidak menghilang menjadi jernih meski telah dipanaskan berarti tidak ada gugus ester. Sampel 18B : hasil positif warna merah muda menghilang menjadi jernih dengan segera berarti ada
Hasil positif terbentuk warna jingga tua berarti ada gugus amina.
Kontrol negatif : air
Hasil negatif tidak terbentuk warna jingga tua berarti tidak ada gugus amina.
Sampel 18A : hasil negatif seperti kontrol negatif berarti tidak ada gugus amina.
Sampel 18B : hasil positif seperti kontrol positif terjadi perubahan warna menjadi jingga tua berarti ada gugus amina.
Uji Baeyer
Kontrol positif : fenol
Hasil positif warna ungu menghilang dan terbentuk endapan berarti terdapat ikatan rangkap karbon dan senyawa bukan jenuh.
Kontrol negatif : aseton Hasil negatif warna ungu tidak menghilang karena ikatan rangkap terjadi antara karbon-oksigen dan bukan karbon-karbon.
Sampel 18A : hasil negatif seperti kontrol negatif berarti senyawa jenuh.
Sampel 18B : hasil positif warna ungu menghilang dan terbentuk endapan seperti kontrol positif berarti terdapat ikatan rangkap karbon-karbon.
Berdasarkan hasil percobaan :
a. Senyawa 18A diidentifikasi sebagai asam dan tidak mengandung gugus fungsi lain.
b. Senyawa 18B diidentifikasi : - Memiliki gugus ester - Memiliki gugus amin - Memiliki gugus karboksil - Memiliki gugus karbonil - Sebagai senyawa asam - Sebagai senyawa tak jenuh VI. Pembahasan
Gambar 1. Struktur air Gambar 2. Struktur sulfanilamide
Terdapat kecocokan dan ketidakcocokan antara hasil percobaan dengan kenyataan pada uji gugus fungsi yang dilakukan dengan prinsip percobaan masing-masing yang disebabkan berbagai faktor dan kondisi.
Berikut beberapa percobaan yang dilakukan, diantaranya: a. Uji Gugus Alkohol
Alkohol adalah senyawa yang mengikat gugus (-OH) dan dapat dibagi menjadi alkohol primer, sekunder, dan tersier. Alkohol primer memiliki rumus umum RCH2-OH sehingga biasanya terletak di ujung rantai karbon. Alkohol sekunder memiliki rumus umum R2CH-OH, sedangkan alkohol tersier R3C-OH. Uji gugus alkohol bisa dilakukan dengan tiga cara sebagai berikut :
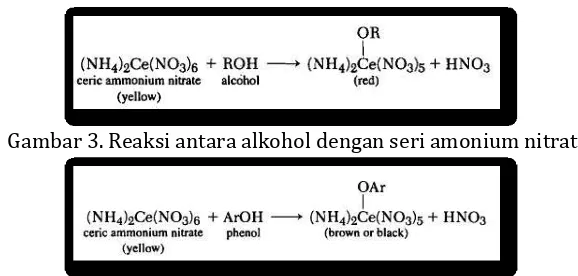
Uji Seri Amonium Nitrat (tidak dilakukan)
Uji ini digunakan untuk membedakan gugus alkohol dengan fenol dari perbedaan warna yang muncul. Pereaksi yang ditambahkan adalah air dan larutan seri ammonium nitrat hingga reaksi kimia yang muncul adalah :
Gambar 3. Reaksi antara alkohol dengan seri amonium nitrat
Gambar 4. Reaksi antara fenol dengan seri amonium nitrat
Pada hasil reaksi dengan alkohol terjadi perubahan warna menjadi merah, sedangkan dengan fenol menjadi hijau-coklat.
Uji ini digunakan untuk membedakan alkohol primer dan alkohol sekunder, dengan alkohol tersier. Pereaksi yang digunakan adalah pereaksi kromat yang merupakan campuran K2Cr2O7 dalam H2SO4 dan menghasilkan warna biru-hijau untuk alkohol primer dan sekunder, sedangkan untuk alkohol tersier tidak akan bereaksi atau terjadi perubahan warna. Prinsip percobaan adalah reaksi redoks, dimana alkohol primer dan sekunder dapat mengalami oksidasi untuk mengimbangi reduksi dari Cr6+ (merah) menjadi Cr3+ (hijau).
Gambar 5. Reaksi kimia pereaksi kromat dengan alkohol primer dan sekunder
Uji Lucas
Uji Lucas dilakukan untuk membedakan alkohol primer, sekunder, dan tersier dengan pereaksi Lucas campuran dari ZnCl2 dan HCl pekat. Reaksi kimia yang terjadi adalah :
Gambar 6. Reaksi alkohol dengan pereaksi Lucas
dilakukan dan senyawa tidak menunjukkan perubahan warna menjadi biru tua-kehijauan, maka bisa dipastikan kedua senyawa tidak memiliki gugus alkohol.
b. Uji Gugus Fenol
Fenol memiliki struktur umum yang serupa dengan akohol, hanya saja gugus fungsi (-OH) menempel pada cincin aromatik. Sifat gugus fungsi pada fenol mudah lepas atau terdeprotonasi ketika ditambahkan dengan basa kuat, dimana sifat inilah yang tidak mungkin dimiliki alkohol.
Uji FeCl3
Uji ini dilakukan untuk mendeteksi adanya gugus fenol dengan hasil reaksi warna ungu. Pereaksi yang digunakan adalah FeCl3 dengan reaksi kimia sebagai berikut :
Gambar 7. Reaksi fenol dengan FeCl3
Dari hasil percobaan tidak didapatkan warna ungu pada sampel A dan B, juga pada kontrol positif dimana seharusnya didapatkan warna ungu. Hal ini bisa dikarenakan pereaksi telah rusak atau adanya kontaminan pada kontrol positif sehingga tidak bisa didapatkan hasil yang sesungguhnya. Bila diasumsikan pereaksi tidak rusak dan pada kontrol positif didominasi kesalahan praktikan, maka sampel A dan B tidak mengandung fenol. Identifikasi tersebut sekaligus menguatkan dugaan bahwa pada uji Lucas tidak ditemukan gugus alkohol. Maka dari dua uji Lucas dan FeCl3 dapat diidentifikasi bahwa kedua sampel tidak memiliki gugus alkohol maupun fenol sehingga sesuai dengan kenyataan struktur sesungguhnya pada sulfanilamid dan air.
Uji Lieberman
Uji Permanganat (tidak dilakukan)
Uji ini dilakukan untuk mengidentifikasi keberadaan gugus fenol dalam suatu senyawa. Dengan menambahkan kalium permanganat, senyawa yang mengandung gugus fenol akan mengalami oksidasi dan kalium permanganat mengalami reduksi menjadi mangan oksida yang memberikan warna coklat.
c. Uji Gugus Karbonil
Gugus karbonil terdiri dari atom karbon yang berikatan rangkap dengan atom oksigen (C=O) dan dikenal secara umum sebagai aldehid atau keton. Aldehid memiliki gugus karbonil pada ujung rantai beserta atom hidrogen, sedangkan keton memiliki gugus karbonil yang terhubung dua atom karbon.
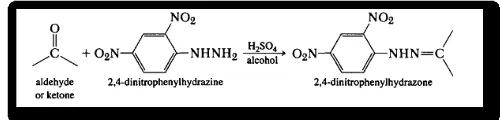
Uji Pembentukan Hidrazon
Uji ini dilakukan untuk mendeteksi adanya gugus karbonil pada senyawa dengan hasil positif terbentuknya endapan jingga-coklat pada (2,4-dinitrofenilhidrazon). Reaksi yang terjadi adalah sebagai berikut :
Gambar 8. Reaksi pembentukan 2,4-dinitrofenilhidrazon
Hasil percobaan pada sampel A tidak menunjukkan adanya perubahan warna ataupun terbentuknya endapan sehingga dapat diidentifikasi tidak memiliki gugus karbonil; sesuai struktur kenyataan pada air tidak memililiki gugus karbonil. Sedangkan hasil percobaan pada sampel B menunjukkan adanya endapan jingga yang menunjukkan adanya karbonil. Hasil ini tidak sesuai dengan kenyataan karena tidak terdapat gugus karbonil pada sulfanilamid. Hal ini disebabkan pipet yang digunakan untuk mengambil sampel B belum bersih dari pengambilan kontrol positif sehingga memengaruhi hasil yang didapatkan.
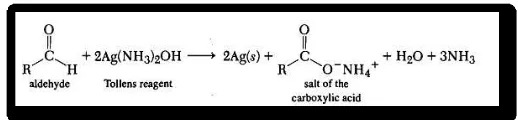
Uji ini dilakukan untuk membedakan aldehid dengan keton dalam sampel dengan pereaksi Tollens yang terdiri dari AgNO3, NaOH, dan NH4OH. Hasil positif uji adalah terbentuk endapan logam atau koloid perak. Pereaksi Tollens hanya positif terhadap gugus aldehid karena dapat mengalami oksidasi untuk logam Ag tereduksi, sedangkan hal tersebut tidak dapat terjadi pada gugus keton. Reaksi kimia yang terjadi adalah :
Gambar 9. Reaksi aldehid dengan reagan Tollens
Dari hasil percobaan pada sampel A, tidak didapatkan endapan perak yang sesuai dengan kenyataan struktur air tidak memiliki gugus aldehid. Sedangkan pada sampel B didapatkan endapan perak terang, dimana seharusnya tidak ada karena struktur sulfanilamid tidak memiliki gugus karbonil. Kesalahan dimungkinkan karena pipet yang terkontaminasi kontrol positif percobaan karbonil telah mencemari sampel sehingga memberikan hasil reaksi yang salah ketika diuji dengan reagen Tollens.
Uji Schiff (tidak dilakukan)
Uji ini dilakukan untuk mengidentifikasi keberadaan gugus aldehid dalam suatu senyawa sekaligus dapat digunakan untuk membedakan keberadaan gugus karbonil (aldehid atau keton) pada suatu senyawa. Penambahan asam klorida dan pereaksi Schiff memberikan warna merah violet untuk senyawa yang mengandung gugus aldehid, sedangkan senyawa dengan gugus keton tidak memberikan perubahan warna setelah penambahan asam klorida dan pereaksi Schiff.
Uji Iodoform (tidak dilakukan)
Pada uji iodoform, senyawa yang mengandung gugus CH3CO- jika ditambahkan NaOH dan larutan iod akan menghasilkan bau yang khas dan membentuk endapan kuning.
Gugus karboksil merupakan gabungan nama antara karbonil (ikatan ganda atom karbon dan atom oksigen) dengan hidroksil (ikatan atom hidrogen dan atom oksigen) sehingga bentuk gugus fungsinya adalah (-COOH). Sifat senyawa yang memiliki gugus karboksil adalah asam, baik kuat maupun lemah.
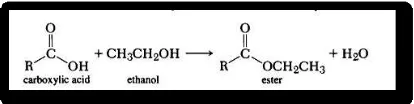
Uji Esterifikasi (tidak dilakukan)
Uji ini dilakukan untuk mendeteksi ada tidaknya asam karboksilat dengan mencium bau ester khas yang muncul dari hasil percobaan. Pereaksi yang digunakan adalah etanol, H2SO4 pekat, dan air. Pemanasan adalah kunci munculnya perubahan aroma wangi ester. Reaksi yang terjadi adalah sebagai berikut :
Gambar 10. Reaksi kimia antara karboksilat dan etanol Uji Kertas Lakmus
Uji kertas lakmus merupakan uji yang paling sederhana dilakukan untuk mengidentifikasi senyawa asam atau basa. Pada percobaan kali ini digunakan kertas lakmus biru sebagai indikator. Perubahan warna yang terjadi pada kertas lakmus disebabkan oleh bahan dasar kertas lakmus (orchein; spesies lumut) yang dapat bereaksi dengan kation pada asam sehingga terjadi perubahan jenis ikatan, posisi, dan delokalisasi. Perubahan-perubahan yang terjadi menyebabkan perubahan penyerapan panjang gelombang yang lebih tinggi sehingga mata menangkap warna kertas lakmus menjadi warna merah. Hal tersebut tidak terjadi pada senyawa basa karena orchein berupa anion sehingga tidak terjadi reaksi apapun pada kertas lakmus.
panjang gelombang yang lebih tinggi sehingga kertas lakmus terlihat berwarna merah. Hal serupa dapat pula terjadi pada sulfanilamid oleh karena sifat basa lemah yang dimiliki dan keelektropositifan hidrogen sehingga hidrogen yang lepas dapat bereaksi dengan orchein, terjadi perubahan penyerapan panjang gelombang yang lebih tinggi sehingga kertas lakmus terlihat berwarna merah.
Uji Bikarbonat
Uji ini dilakukan untuk menentukan keberadaan gugus karboksil pada senyawa. Hasil positif menunjukkan adanya gelembung karbon dioksida yang merupakan hasil sampingan dari reaksi substitusi antara gugus karboksilat dengan NaHCO3.
Gambar 11. Reaksi gugus karboksilat dengan Na-bikarbonat menghasilkan gelembung CO2
Hasil percobaan menunjukkan kedua sampel tidak mengandung gugus karboksil karena gas karbon dioksida tidak terbentuk.
e. Uji Gugus Ester
Ester adalah senyawa organik yang terbentuk ketika salah satu atau lebih atom hidrogen yang ada pada gugus karboksil terlepas dan digantikan gugus organik suatu senyawa yang biasanya berupa alkohol. Senyawa bergugus ester cenderung memiliki aroma khas yang mudah dideteksi ketika terbentuk.
Uji Fenolftalein
Uji fenolftalein dilakukan untuk mengidentifikasi adanya gugus ester dalam senyawa dengan menggunakan fenolftalein sebagai indikator. Dengan adanya senyawa basa dalam suatu larutan, ketika diberikan fenolftalein akan terjadi perubahan warna menjadi merah muda.
mengandung gugus ester. Perubahan warna yang terjadi disebabkan oleh ion natrium pada NaOH berikatan pada gugus karboksilat pada senyawa membentuk ester. Perubahan warna dari merah muda menjadi tidak berwarna terjadi karena NaOH dalam larutan telah bereaksi membentuk ester sehingga indikator PP tidak mengenali adanya NaOH dalam larutan. Perubahan warna yang terjadi pada sulfanilamid terjadi karena sulfanilamid dapat bereaksi pula dengan NaOH sehingga NaOH dalam larutan habis dan tidak dapat dideteksi oleh indikator PP. Pada kontrol negatif (aseton) dan sampel A (air) tidak menunjukkan perubahan warna karena NaOH dalam larutan tidak bereaksi dengan kedua senyawa.
Uji fenolftalein kurang akurat digunakan untuk identifikasi senyawa ester karena perubahan warna pada indikator fenolftalein terjadi oleh hilangnya senyawa NaOH dalam larutan, sedangkan bukan hanya senyawa yang mempunyai gugus ester saja yang dapat berikatan dengan ion natrium dari NaOH.
Uji Asam Hidroksamat (tidak dilakukan)
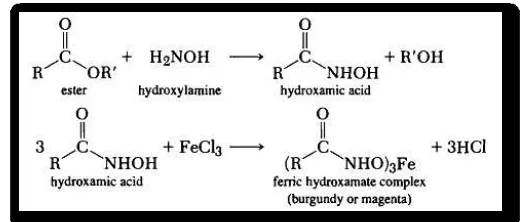
Uji ini dilakukan untuk mendeteksi adanya ester dalam sampel dengan menggunakan pereaksi larutan hidroksilamin HCl dalam etanol, NaOH encer, HCl, dan FeCl3 serta bantuan pemanasan dan pendinginan. Hasil dari uji ini adalah terjadi perubahan warna menjadi merah violet/burgundy/magenta dengan reaksi sebagai berikut :
Gambar 12. Reaksi pembentukan asam hidroksamat dan munculnya warna merah violet
Amina adalah salah satu bentuk senyawa organik dan gugus fungsional yang terdiri dari atom nitrogen berpasangan secara umum dengan hidrogen.
Uji Diazotasi dan Penggabungan
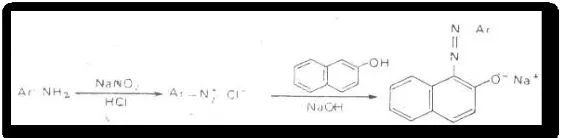
Uji diazotasi menggunakan prinsip pembentukan garam diazonium pada senyawa amin aromatik dengan menggunakan natrium nitrat pada suasana asam serta penambahan senyawa naftol dalam suasana basa. Suasana asam diberikan dengan HCl, sedangkan suasana basa diberikan dengan NaOH. Hasil dari reaksi adalah muncul warna merah atau jingga.
Gambar 13. Reaksi pembentukan garam diazonium
Dari hasil percobaan pada sampel A tidak terjadi perubahan warna berarti tidak ada amin aromatik. Hasil tersebut sesuai kenyataan struktur air tidak memiliki gugus amin. Sedangkan pada sampel B terjadi perubahan warna menjadi jingga yang sama dengan perubahan pada kontrol positif karena kedua senyawa adalah sama memiliki amin aromatik.
Uji p-DAB HCl (tidak dilakukan)
Uji ini dilakukan untuk mengidentifikasi keberadaan amina dalam sampel dengan hasil positif terbentuk endapan kuning sampai jingga. Pereaksi yang digunakan adalah HCl encer dan p-DAB HCl. Reaksi yag terjadi adalah :
Gambar 14. Reaksi gugus amin dengan pereaksi p-DAB HCl
Uji Korek Api (tidak dilakukan)
sampel yang akan mengubah warna batang korek api yang dimasukkan dalam larutan menjadi kuning-jingga.
Uji Karbilamin (tidak dilakukan)
Uji ini menggunakan pereaksi NaOH, etanol, CHCl3 untuk kemudian identifikasi dengan menggunakan bau isonitril yang tercium dan bersifat racun kuat. Reaksi kimia yang terjadi adalah :
Gambar 15. Reaksi amin dengan kloroform dan NaOH
g. Uji Senyawa Tak Jenuh
Uji Adisi Brom (tidak dilakukan)
Uji ini dilakukan untuk mengidentifikasi adanya senyawa tak jenuh dengan melihat perubahan warna ketika senyawa uji ditambahkan larutan jenuh brom (dari coklat menjadi pucat atau tidak berwarna). Perubahan warna yang terjadi disebabkan oleh putusnya ikatan bromida yang kemudian beraksi dengan ikatan rangkap pada senyawa.
Uji Baeyer
Uji Baeyer adalah uji yang dilakukan untuk identifikasi senyawa tak jenuh pada suatu senyawa dengan prinsip reaksi adisi dengan kalium permanganat, dimana hasil samping reaksi adisi yang terjadi antara senyawa tak jenuh dengan kalium permanganat berupa endapan mangan oksida berwarna coklat.
VII. Kesimpulan
7.1Senyawa A diidentifikasi merupakan senyawa asam dan tidak ada gugus fungsi di dalamnya. Senyawa A merupakan air, dimana sifat keasambasaannya netral dan tidak mengandung gugus fungsi di dalamnya, sedangkan senyawa B diidentifikasi merupakan senyawa asam, memiliki gugus ester, amin, karboksil, karbonil, dan memiliki ikatan C rangkap. Senyawa B merupakan sulfanilamid, dimana sifat keasambasaannya basa, memiliki gugus amin dan memiliki ikatan C rangkap.
VIII. Daftar Pustaka
Fessenden dan Fessenden . 2003 . Kimia Organik . Jilid 1 . Jakarta : Erlangga , halaman 259-302.
Furniss, Brian S. 1989 . Vogel’s Textbook of Practical Organic Chemistry . 5th ed . London : Thames Polytechnic , halaman 517-691.
Solomon, Graham T.W. dan Craig B.Fryhle . 2001 . Organic Chemistry . Edisi 8 . New York : John Willey & Sons Inc , halaman 74-77.
http://www.chemistry.mtu.edu/pages/courses/organic/manuals/226/QA/Q
AofROH&C=C.htm (diakses pada 15.02.15 pukul 14:24 WIB).
http://chemwiki.ucdavis.edu/?title=Organic_Chemistry/Aldehydes_and_Keto
nes/Reactions_of_Aldehydes_%26_Ketones/Tollens%E2%80%99_Test
(diakses pada 15.02.15 pukul 14:45 WIB).
http://www2.plymouth.ac.uk/science/wembury/nutrient/nitrogen.htm