Penyelesaian kuantum atom seperti Hidrogen telah dapat memprediksi:
Pendahuluan: motivasi/review pokok bahasan 2
Energi ionisasi golongan 1 lebih kecil dari golongan 7, artinya golongan 1 lebih mudah melepaskan elektron dari pada golongan 7, tetapi energi ionisasi dari atas ke bawah makin besar tidak sesuai eksp.
Struktur
Molekul:Teori Orbital Molekul
Oleh: Dr. Parsaoran Siahaan
Atom 6C Sifat Energi ionisasi/eV 122,0 n=2→n=∞ Semi-logam Atom 1H 3Li 11Na Sifat Energi ionisasi/eV 13,6 n=1→n=∞ 30,6 n=2→n=∞ 183,0 n=3→n=∞ Elektropositip/non-logam Atom 9F 17Cl Sifat Energi ionisasi/eV 275,0 n=2→n=∞ 437,0 n=3→n=∞ Elektronegatip/non-logam
Pendahuluan: motivasi/review pokok bahasan 2
Energi hasil perhitungan perbaikan dengan memperhitungkan interaksi elektron dengan komputasi metode HF/SCF:
Atom 1H 3Li 11Na Sifat
Energi ionisasi pertama/ kJmol-1 1308,11 n=1→n=∞ 514,17 n=2→n=∞ 478,23 n=3→n=∞ Elektropositip/non-logam
Energi ionisasi golongan 1 dari atas ke bawah makin kecil, hasil ini sesuai dengan eksperimen.
Telah diketahui bahwa molekul dapat bersifat non polar, polar dan ion.
Bagaimana menjelaskan dan memprediksi sifat-sifat molekul non polar, polar dan ion dengan mekanika kuantum?
Pendahuluan: motivasi/review pokok bahasan 2
Hδ+2Oδ- Nδ-Hδ+3 Hδ+Clδ- Sifat
Momen dipol μǂ0 μǂ0 μǂ0 polar
Molekul >diatomik Cδ+ Oδ-2 Cδ-Hδ+4 Cδ-6Hδ+6 Sifat
Momen dipol μ=0 μ=0 μ=0 Non polar
Molekul ionik Na+Cl- Mg2+Cl
-2 Ca2+Cl-2 Sifat
Momen dipol - - - Ion
Molekul diatomik H2 O2 Cl2 Sifat
1. Bagaimana menjelaskan terbentuknya molekul H2?
H
2
Sebelum menerapkam metode penyelesaian kuantum atom seperti Hidrogen untuk menjelaskan dan memprediksi sifat-sifat dan kereaktifan molekul, berikut diajukan beberapa pertanyaan :
Pendahuluan: motivasi/review pokok bahasan 2
2. Bagaimana menjelaskan terbentuknya molekul H2+?
H
2
+
3. Bagaimana menjelaskan kereaktifan molekul fenol sebagai pengarah orto, meta, dan para?
OH
fenol
OH COOHorto
OH COOHmeta
OH COOHpara
H O H
sp
3H
O H
sp
34. Bagaimana menjelaskan bentuk molekul H2O?
Bentuk?
H O H H O H H O H H O H H O H H O H H O H H O H5. Bagaimana menjelaskan interaksi antarmolekul berdasarkan sifat-sifat molekul H2O?
H
N
H
H
sp
3H
N
H
H
sp
3Bentuk?
H N H H N H H N H H N H H N H H N H H N H H N H H N H H H H H H6. Bagaimana dengan bentuk molekul NH3?
7. Bagaimana menjelaskan interaksi antarmolekul berdasarkan sifat-sifat molekul NH3?
CaPO4
3-PO43- TCP:Ca
3(PO4)2
8. Bagaimana dengan bentuk molekul kalsium fosfat?
HA:Ca5(PO4)3OH 9. Bagaimana dengan bentuk molekul glukosa?
C6H12O6
10. Bagaimana dengan bentuk molekul dimer glukosa? C12H22O11
11. Bagaimana dengan bentuk molekul metanol dan etanol?
12. Bagaimana dengan bentuk molekul eter? CH3OH C2H5OH
CH3OCH3
13. Bagaimana dengan bentuk molekul segmen dimer, trimer dan tetramer kitin?
14. Bagaimana dengan bentuk molekul segmen dimer, trimer dan tetramer kitosan?
15. Bagaimana dengan bentuk molekul segmen tetramer dan oktamer selulosa?
16. Bagaimana dengan bentuk molekul segmen tetramer dan oktamer pati?
17. Bagaimana dengan bentuk molekul zeolit?
Pendahuluan: motivasi/review pokok bahasan 2
Makin banyak pertanyaan yang dapat anda tuliskan adalah menunjukkan tingkat rasa ingin tahu (curiosity) anda.
Marilah kita mempelajari bagaimana menjelaskan sifat-sifat molekul zeolit.
Molekul:
Molekul adalah partikel yang terdiri dari atom-atom dengan
bagian inti atom yang bermuatan positip dikelilingi oleh
elektron bermuatan negatip.
Kekuatan yang mengikat elektron dan inti pada molekul agar
menjadi satu kesatuan yang
stabil adalah energi
potensial tarik menarik antara muatan positip dan
negatip dikurangi energi tolak menolak antara muatan
positip-muatan positip dan antara muatan
negatip-muatan negatip.
Kekuatan energi tarik menarik sangat kuat pada jarak
tertentu sehingga menghasilkan molekul yang sangat
stabil dan disebut energi ikatan kovalen.
Masalahnya adalah bagaimana menjelaskan energi ikatan
molekul dengan
kuantum
?
Struktur elektron molekul dapat digambarkan dengan
dua
teori mekanika kuantum
:
1. teori ikatan valensi (VB).
2. teori orbital molekul (OM).
Teori ikatan valensi: pemakaian elektron bersama.
Teori ini dapat menjelaskan:
1. ikatan σ dan π.
2. promosi.
3. hibridisasi.
Teori orbital molekul (perluasan konsep orbital atom)
:
fungsi gelombang menyebar pada seluruh atom dalam
molekul.
Kebanyakan perhitungan struktur molekul dengan komputasi
menggunakan teori OM.
Sifat-sifat ikatan kimia antara atom-atom pada molekul
yang dapat ditentukan:
1. kekuatan.
2. jumlah.
3. susunan 3-dimensi.
Penggambaran ikatan kimia dengan
mekanika kuantum
untuk
molekul kompleks telah dapat dilakukan saat ini dengan
menggunakan komputer, kebanyakan memakai teori OM
.
Mekanika kuantum dapat digunakan menjelaskan:
1. Ikatan kovalen (G.N. Lewis, 1916, sebelum mekanika
kuantum): sharing sepasang elektron antara dua atom
bertetanga yang
sama
dan
berbeda
.
2. Ikatan ion: tarik-menarik Coulomb antara ion-ion
bermuatan berbeda.
Aproksimasi Born-Oppenheimer
Semua
teori struktur molekul
membuat simplifikasi.
Persamaan Schrodinger hanya dapat diselesaikan secara
eksak untuk atom hidrogen.
Hal ini
tidak mungkin untuk molekul
, karena molekul paling
sederhana pun sudah terdiri atas tiga partikel:
1. Inti A.
2. Inti B.
3. Satu elektron.
Digunakan aproksimasi Born-Oppenheimer: inti jauh lebih
besar dari elektron, sehingga bergerak relatif lebih
lebih lambat.
Dengan demikian elektron diperlakukan bergerak dalam
medan inti yang diam atau stasioner.
Jadi jarak inti adalah tertentu, dan persamaan Schrodinger
adalah untuk fungsi gelombang elektron yang bergerak.
Aproksimasi Born-Oppenheimer sangat baik untuk molekul
keadaan ground-statate (dasar), perhitungan untuk H
2menyarankan kecepatan inti dan elektron 1:1000 pm.
Validitas aproksimasi berkuruang untuk
molekul poliatomik
keadaan tereksitasi
dan
ion keadaan dasar
.
Kedua spesi ini (keadaan tereksitasi dan ion) sangat penting
pada
spektroskopi fotoelektron
dan
spektroskopi massa
.
Aproksimasi Born-Oppenheimer memilih jarak antar inti
molekul diatomik, R
1, dan kemudian menyelesaikan
persamaan Schrodingernya.
Perhitungan diulang untuk jarak inti lain, R
2, R
3, dst., dan
akhirnya diperoleh energi molekul pada berbagai
panjang ikatan
; dapat dilakukan untuk poliatomik.
Selanjutnya, dapat diperoleh energi molekul pada berbagai
sudut ikatan
.
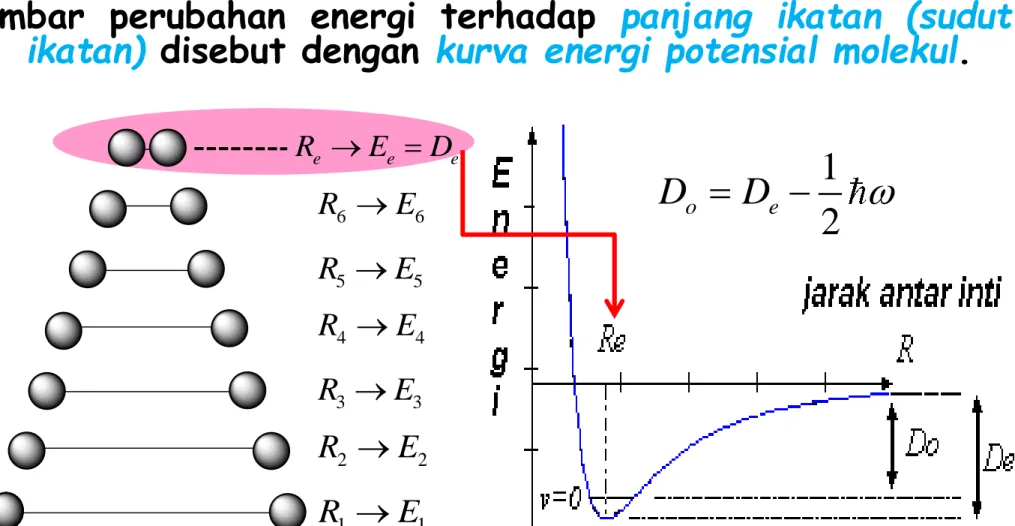
Gambar perubahan energi terhadap
panjang ikatan (sudut
ikatan)
disebut dengan
kurva energi potensial molekul
.
1 1
R
E
2 2R
E
3 3R
E
4 4R
E
5 5R
E
6 6R
E
e e e R E D1
2
o eD
D
Aproksimasi Born-Oppenheimer
Teori Ikatan Valensi (VB)
Teori ikatan valensi adalah teori mekanika kuantum ikatan kimia yang pertama dikembangkan dan banyak digunakan dalam ilmu kimia untuk menjelaskan dan mendeskripsikan:
1. sifat-sifat senyawa organik. 2. reaksi senyawa organik
Teori ini memperkenalkan konsep atau bahasa kimia: 1. spin berpasangan.
2. overlap orbital. 3. ikatan σ dan π. 4. promosi elektron. 5. hibridisasi orbital.
Pada teori VB, ikatan terbentuk bila elektron dalam orbital suatu atom memasangkan spinnya dengan elektron dalam orbital atom lain.
Untuk memahami mengapa pasangan spin elektron menghasilkan ikatan, dapat dijelaskan dari fungsi gelombang kedua elektron yang membentuk ikatan. Misalnya untuk molekul H2.
Fungsi gelombang elektron (dalam ruang/spatial) pada masing-masing kedua atom H yang terpisah, jika elektron 1 pada atom A dan elektron 2 pada atom B, adalah:
Disingkat:
Secara skematik, pembentukan H2:
1 1 H sAr
A H sBr
B
1
2
A
B
Jika kedua atom H sangat dekat, tidak mungkin lagi dapat dibedakan apakah elektron 1 pada A atau elektron 2.
Jadi ada kemungkinan elektron 2 pada A dan elektron 1 pada B:
Bila keduanya mempunyai kemungkinan yang sama, menurut mekanika kuantum sistem dapat digambarkan sebagai superposisi kedua fungsi gelombang melalui kombinasi linier:
Kombinasi dengan energi lebih rendah adalah dengan tanda + (positip, sehingga fungsi gelombang ikatan molekul H2 adalah:
Distribusi elektron yang dihasilkan oleh persamaan ini disebut ikatan σ.
2
1
A B
1
2
2
1
A B A B
1
2
2
1
A B A B
Bagaimana menjelaskan molekul N2?
Konfigurasi elektron valensi masing-masing atom N: 2s22p
x12py12pz1.
Bila sumbu molekul N2 adalah sumbu z, maka orbital pz saling sejajar dan orbital px dan py adalah saling tegak lurus.
Overlap orbital p
z-p
zdisebut
ikatan-σ
,
orbital p
x-p
xdan p
y-p
ydisebut
orbital-π
.
Sumbu-z Sumbu-x atau sumbu-yp
yp
yp
zp
z Sumbu-z overlapTeori Ikatan Valensi (VB): Poliatomik
Bagaimana menjelaskan molekul H2O, NH3, dan CH4?
Caranya sama, yaitu tentukan konfigurasi elektron valensi masing-masing atom.
Molekul H2O akan menghasilkan sudut 90o. Eksperimen adalah 104,5o
Molekul NH2 akan menghasilkan sudut 90o. Eksperimen adalah 107o
Molekul CH4 tidak dapat dijelaskan oleh teori VB.
Molekul CH4 diatasi dengan konsep promosi, yaitu eksitasi elektron ke orbital energi lebih tinggi. Namun demikian pada CH4 terdapat 3 ikatan σ satu jenis dan ikatan σ keempat dari tipe lain.
Selanjutnya molekul CH4 diatasi dengan mengenalkan konsep hibridisasi,
seperti sp3.
Perlu teori lain yaitu Orbital Molekul untuk mengatasi kelemahan teori VB.
Aproksimasi Orbital Molekul (OM)
Pada teori OM, elektron tersebar pada seluruh molekul, tetapi tidak hanya pada ikatan tertentu (VB).
Pada struktur atom telah diuraikan hasil penyelesaian persamaan Schrodinger atom hidrogenik (berelektron tunggal), bahwa fungsi gelombang disebut orbital atom.
Menurut teori klasik, pembentukan molekul melalui interaksi antara atom-atom terjadi karena interaksi antara elektron bermuatan negatip dengan inti bermuatan positip.
Elektron adalah berasal dari kedua atom yang berinteraksi sehingga disebut pemakaian elektron bersama.
Menurut teori kuantum, elektron digambarkan sebagai fungsi gelombang. Oleh karena itu, pembentukan molekul dari atom-atomnya adalah penggabungan atau penjumlahan fungsi gelombang atau orbital atom
Istilah penjumlahan fungsi gelombang disebut sebagai superposisi.
Persamaan gelombang penjumlahan atau superposisi orbital-orital atom disebut orbital molekul.
Penggambaran molekul dengan penjumlahan orbital atom-atomnya menjadi orbital molekul disebut sebagai pendekatan atau aproksimasi orbital molekul, atau LCAO-MO.
Sifat-sifat molekul dapat dihitung dengan menggunakan persamaan Schrodinger, menggunakan hamiltonian dan orbital molekul untuk molekul tersebut.
Fungsi gelombang yang digunakan adalah orbital molekul hasil superposisi orbital atom, sedangkan hamiltonian adalah penjumlahan operator energi kinetik inti, energi kinetik elektron, energi potensial interaksi inti dengan elektron, interaksi inti dengan inti. Kekompleksan persamaan Scrodinger pada molekul tergantung pada
jumlah inti dan elektron yang terdapat pada molekul.
Semakin besar molekul atau semakin banyak jumlah atom dan elektron semakin banyak suku yang terdapat dalam persamaan Schrodinger.
Persamaan Schrodinger sebagai persamaan diferensial dengan suku banyak akan sulit diselesaikan secara analitik.
Oleh karena itu, meskipun persamaan ini kita ketahui tetapi bila tidak dapat diselesaikan maka sifat molekul tetap tidak dapat diketahui. Hal inilah yang menyebabkan materi kuliah berkaitan dengan persamaan
Schrodinger kurang disukai oleh mahasiswa atau dosen, dan cenderung diabaikan dalam metode analisis penelitian.
Sementara itu, persamaan Schrodinger adalah persamaan dasar untuk mengungkap sifat-sifat molekul.
Sebelum perkembangan kimia komputasi, persamaan Schrodinger hanya dapat diselesaikan untuk molekul paling sederhana yaitu molekul H2+.
Metode penyelesaian molekul H2+ menjadi landasan untuk molekul besar
dengan komputasi kimia, dan dengan perkembangan komputasi telah banyak sifat-sifat molekul besar dapat diprediksi.
Skema penggambaran molekul H2+: elektron kedua atom mengikat
inti, interaksi elektron-inti sebagai fungsi jarak r dan inti-inti fungsi jarak R; keadaan sebenarnya: kerapatan elektron sebagai suatu kebolehjadian.
Metode LCAO-MO pada molekul H2+ yang hanya terdiri dari dua atom,
orbital molekul dapat ditulis dengan.
Atau:
dengan OM adalah orbital molekul H2+,
OA1 dan OA2 adalah orbital 2
atom H, C1 dan C2 adalah konstanta menyatakan kontribusi masing-masing orbital atom H pada orbital molekul.
Hamiltonian molekul H2+,adalah penjumlahan energi kinetik dua inti atom
H bermasssa mH, satu elektron bermassa me, energi potensial interaksi elektron dengan dua inti atom H, dan energi potensial interaksi inti dengan inti, dituliskan dengan:
1 1 2 2 OM
c
OAc
OA
2 a Ha b Hb Hc
c
2 2 2 2 2 2 2 2 2ˆ
2
Ha Ha2
Hb Hb2
e e A Be
e
e
H
m
m
m
R
r
r
Sesuai dengan,
Maka:
Hamiltonian untuk molekul H2 dapat ditulis dengan,
H
E
2 2 2 2 2 2 2 2 22
Ha Ha2
Hb Hb2
e e A B a Ha b Hb a Ha b Hbe
e
e
c
c
m
m
m
R
r
r
E c
c
2 2 2 2 2 2 2 2 2 1 1 1 1 2 2 2 2 2 2 2 2 2 12ˆ
2
2
2
2
Ha Hb e Ha Hb e A B e e A Be
e
e
H
m
m
m
R
r
r
e
e
e
m
r
r
r
Menambah satu elektron ke dalam H2+ untuk menghasilkan H
2 telah
menambah 4 suku pada hamiltonian H2.
Persamaan Schrodinger di atas sulit diselesaikan secara analitik.
Bila persamaan Schrodinger diselesaikan tanpa melibatkan parameter hasil eksperimen disebut metode ab initio.
Bila satu atau lebih suku diganti dengan parameter eksperimen disebut
metode semi-empiris.
Metode yang sering digunakan untuk menyelesaikan Schrodinger adalah
metode variasi dan metode HF-SCF (Hartree Fock - Self
Consistent Field).
Metode Variasi: molekul diatomik
Penerapan metode variasi pada molekul AB yang terbentuk dari atom A dan B adalah diawali dengan pembentukan fungsi gelombang AB yaitu:
Untuk menyingkat penulisan diganti dengan sehingga dapat ditulis,
Fungsi gelombang harus ternormalisasi dengan kondisi,
Energi molekul dihitung dengan,
ABc
AA
c
BB
A Bc
A
c
B
*1
d
* *H d
E
d
Energi E adalah energi perhitungan yang tergantung pada konstanta cA dan cB karena fungsi gelombang atom telah diketahui.
Energi E perhitungan adalah lebih kecil dari harga energi sebenarnya, sehingga berlaku kondisi turunan pertama E terhadap cA adalah:
dan cB Dapat ditulis,
0
AE
c
B0
E
c
2 2 2 2 2 2 2 22
2
A B A B A B A B A Bd
c
A
c
B
d
c
A d
c
B d
c c
A
B d
c
c
c c S
* S
A B dS: integral Overlap
Dengan, Sehingga:
2 2 2 2 2 2 A B A B A B A B A A B B A B H d c A c B H c A c B d c A H A d c B H B d c c A H B d c c c c
AA H
A d
BB H
B d
A H
B d
2 2 2 22
2
A A B B A B A B A Bc
c
c c
E
c
c
c c S
α: integral Coulomb
β: integral Resonansi
Turunan pertama E terhadap cA adalah:
Dan terhadap cB adalah:
diperoleh dua persamaan linier dengan dua perubah cA dan cB yaitu,
atau:
2 22
0
2
A A A B B A A B A Bc
c E
c
c SE
E
c
c
c
c c S
2 2 2 0 2 B B B A A B A B A B c c E c c SE E c c c c c S
c
A
A
c E c
A
B
2
c SE
B
0
c
B
B
c E c
B
A
2
c SE
A
0
A
E c
A
ES c
B
0
ES c
A
B
E c
B
0
Kedua persamaan dua variabel terhadap cA dan cB adalah persamaan sekular yang dapat diselesaikan dengan determinan:
Dan hasil determinannya adalah:
Menghasilkan:
0
A BE
ES
ES
E
E
ES
1
E
S
Kesimpulan:Penerapan metode variasi pada persamaan energi, yang mengandung satu persamaan gelombang, ternyata dapat menghasilkan dua tingkat energi E- dan E+.
Metode variasi dapat menyelesaikan persamaan energi tetapi masih mempunyai α dan β, yang mengandung fungsi gelombang .
1
E
S
Setiap energi mempunyai fungsi gelombang sendiri, sehingga penyesaian persamaan juga harus menghasilkan dua fungsi gelombang yaitu untuk tingkat energi E- dan E+.
Fungsi gelombang pertama diperoleh untuk E+ sebagai berikut:
Diperlukan manipulasi matematik:
Sehingga diperoleh: 2 2 2 2 2 2 2 2 2 1 A B A B A B A B A B A B c c c c c c c c E c c c c S
2 2 2 1 1 A B A B c c c c E S
2 2
1 1 2 1 1 1 1 A B A B c c c c S S 2 21
1
A Bc
c
S
dan1
2
1
A Bc c
S
Bila harga cA=cB diperoleh:
Persamaan gelombang untuk tingkat energi E+ adalah:
Dengan cara yang sama untuk E-, diperoleh:
1
2 1
Ac
S
1 2 1 B c S dan
1
2 1
A
B
S
1
2 1
A
B
S
Metode variasi menghasilkan dua keadaan energi dengan persamaan gelombang yang berbeda, masing-masing disebut keadaan atau orbital bonding dan antibonding.