TINJAUAN PUSTAKA
Kakao
Pohon kakao (Theobroma cacao L) diperkirakan mula-mula tumbuh di daerah Amazon utara sampai ke Amerika Tengah. Mungkin sampai ke Chiapas, bagian paling selatan Meksiko. Orang-orang Olmec memanfaatkan pohon dan mungkin juga membuat coklat di sepanjang pantai teluk di selatan Meksiko sekitar 1000 tahun SM. Peradaban pertama yang mendiami daerah Mesoamerika itu mengenal pohon “kakawa” yang buahnya dikonsumsi sebagai minuman. Bagi suku Aztec biji kokoa merupakan “makanan para dewa” (theobroma, dari bahasa Yunani).
Klasifikasi ilmiah kakao antara lain: dunia : Plantae
divisi : Spermatophyta sub divisi : Angiospermae kelas : Dicotyledoneae sub kelas : Dialypetaleae
bangsa : Malvales suku : Sterculiaceae marga : Theobroma Gambar 1 Buah kakao jenis : theobroma cacao L
Kakao adalah biji yang diperoleh dari pohon kakao, Theobroma cacao L, dengan ketinggian pohon 6-12 meter. Tanaman ini dapat tumbuh dengan baik pada area 30-300 meter, pada suhu sedang yaitu berkisar 18-30 ºC dan membutuhkan kelembaban udara yang cukup dengan curah hujan 1-5 liter/ m2 per tahun (Weisburger 2001).
Rasa asli biji coklat sebenarnya pahit akibat kandungan alkaloid, tetapi setelah melalui rekayasa proses dapat dihasilkan coklat sebagai makanan yang disukai oleh siapapun. Biji coklat mengandung lemak 31%, karbohidrat 14% dan protein 9%. Protein coklat kaya akan asam amino triptofan, fenilalanin, dan tirosin. Meski coklat mengandung lemak tinggi namun relatif tidak mudah tengik
karena coklat juga mengandung polifenol (6%) yang berfungsi sebagai antioksidan pencegah ketengikan.
Tabel 1 Kandungan total polifenol produk kakao Produk Kakao Jumlah polifenol total (g /100 g)
Bubuk cokelat 2,00
Cokelat batangan 0,84
Susu cokelat 0,50
Sumber: Wollgast dan Anklam (2000)
Indonesia merupakan negara ketiga penghasil kakao terbesar di dunia setelah Pantai Gading dan Ghana. Ada dua jenis kakao yang umum dikenal di Indonesia, yaitu kakao mulia atau edel kakao (fine/ flavour cocoa) yang berasal dari varietas criollo dengan buah berwarna merah dan kakao lindak (bulk cocoa) berasal dari varietas forestero dan trinitro dengan warna buah hijau. Kakao lindak merupakan kakao kualitas kedua dan digunakan sebagai bahan komplementer dalam mengolah kakao mulia. Meskipun termasuk kualitas kedua dan digunakan sebagai bahan komplementer, jenis kakao lindak mendominasi seluruh perkebunan di Indonesia (Direktorat Jenderal Bina Produksi Perkebunan, 2004). Hal ini disebabkan karena jenis kakao ini relatif lebih tahan terhadap hama dan penyakit, dan tingkat produksinya lebih tinggi dibanding kakao mulia (Zairisman 2006, Siregar et al 2007).
Kualitas dari produk olahan kakao yang dihasilkan sangat tergantung kepada kualitas biji kakao dan proses pengolahan. Salah satu faktor yang sangat menentukan adalah proses fermentasi biji kakao sebelum diolah. Cita rasa coklat yang baik dapat diperolah bila kakao tersebut difermentasi dengan baik. Berdasarkan Direktorat Jenderal Bina Produksi Perkebunan (2004) kakao Indonesia khususnya yang dihasilkan oleh rakyat, di pasaran Internasional dihargai paling rendah, karena didominasi oleh biji-biji tanpa fermentasi. Namun demikian proses fermentasi itu sendiri menyebabkan kandungan senyawa kimia dalam biji kakao menjadi berubah, terutama senyawa flavonoid yang dapat memberikan efek positif untuk kesehatan. Berdasarkan penelitian Misnawi dan Selamat (2003) kandungan polifenol dalam biji kakao menurun sampai 50% selama proses fermentasi.
Menurut Wollgast dan Anklam (2000), kandungan polifenol total dalam produk kakao berbeda-beda. Terdapat berbagai macam produk olahan dari biji kakao yaitu chocolate liquor (pasta kakao), cocoa powder (bubuk coklat), cocoa butter (mentega kakao) dan dark chocolate. Dark chocolate mengandung 15% chocolate liquor dan 60% cocoa butter, gula dan adiktif. Sedangkan cocoa powder (bubuk coklat) dibuat dengan menghilangkan cocoa butter dari chocolate liquor (Vinson et al. 1999). Produk olahan kakao ini digunakan untuk berbagai jenis olahan makanan, industri farmasi dan industri kosmetik. Bubuk kakao banyak digunakan sebagai bahan pembuat roti, es krim, permen dan juga untuk minuman. Cocoa butter banyak digunakan untuk industri makanan, kosmetik dan farmasi (Pusat Penelitian Kopi dan Kakao 2004).
Bubuk kakao bebas lemak dari biji kakao non fermentasi sebagai sumber flavonoid merupakan usaha yang sedang dirintis di Pusat Penelitian Kopi dan Kakao Indonesia di Jember. Bubuk kakao bebas lemak tersebut adalah produk kakao yang berbentuk bubuk yang diperoleh dari pasta kakao setelah dihilangkan lemaknya. Bubuk kakao bebas lemak dibuat melalui proses sebagai berikut : biji kakao basah dicuci bersih dan dioven pada suhu 50ºC sampai kadar air 7,5%. Selanjutnya kulit ari dipisahkan, keping biji yang diperoleh dihaluskan dengan blender (penghancur biji). Pasta kakao yang diperolah kemudian dipisahkan lemaknya (defatting) dalam soxhlet apparatus menggunakan pelarut petroleum benzene (titik didih 40-60ºC). Bubuk kakao yang diperoleh kemudian dihaluskan sampai kehalusan <40 mesh dan kemudian disimpan dalam kemasan yang kedap udara (Misnawi 2005). Berdasarkan penelitian Misnawi et al (2003) dikemukakan bahwa dalam bubuk kakao bebas lemak dari biji kakao non fermentasi terdapat 120-180 g/kg polifenol. Bubuk kakao bebas lemak dari verietas bulk masak berdasarkan penelitian Zairisman (2006) mengandung total fenol sebesar 4,43 gr/ 100 gr. Kandungan polifenol kakao juga sangat tergantung pada proses pengolahan dan produk akhir. Hasil penelitian Misnawi et al. (2002b) juga mendapatkan bahwa aktifitas antioksidan polifenol biji kakao masih tetap tinggi walaupun telah dipanaskan sampai suhu 140ºC selama 45 menit.
y p a k p C d a b y j 2 p d d p 2 f Rasa yang dimilik pigmen pew akibat oksid komponen l pengawet da Flavon C6-C3-C6 d dan reaksi k aktivitas an bioflavonoid yang merup jenuh yang 2000). Flavo phenylbenzo dasarnya, ya dari dua cin piran atau p 2000). Hal i flavonoid ad a pahit yang kinya yaitu warna alami, dasi. Adanya lemaknya se ari luar. noid merupa dan berperan kelat pada l ntioksidanny d. Kompone akan senyaw merupakan onoid memi opyrones (ph
aitu tiga cin ncin benzena piron dengan ini dipertega dalah rangka G Flavon g terdapat pa flavonoid. senyawa pe a flavonoid d ehingga men akan kelomp n dalam mek logam (Hall ya di dala en antioksida wa reaktif y penyusun m iliki berat henylchromo ncin utama y a (A dan B) n ikatan gan as lagi oleh aian cincin ka Gambar 2 St noid pada k ada kakao b Flavonoid m emberi cita r dalam kakao ngurangi ke ok senyawa kanisme don l 2001). Fla am tubuh an ini dapat yang dapat b membran, RN molekul ren ones) denga yang saling yang dihubu nda yang dis Miean dan arbon C6C3 truktur kimia kakao berkaitan den memainkan
rasa dan pel o dapat menc ebutuhan aka a yang memp nor hidrogen avonoid umu sehingga menetralisir bereaksi den NA dan DNA ndah, dan p an berbagai melekat. Str ungkan mela sebut cincin Mohamed C6. a flavonoid ngan kompo peran pentin lindung dari cegah keten an penamba punyai ciri k n, penangkap umnya dike sering jug r reaktivitas ngan asam le A (Hammer pada dasarn variasi pad ruktur dasar alui cincin h n ”C” (Midd (2001) bahw onen kimia ng sebagai kerusakan gikan pada ahan bahan konfigurasi pan radikal enal karena ga disebut dari ROS, emak tidak rstone et al nya adalah da struktur r ini terdiri heterosiklik dleton et al wa struktur
Flavonoid yang terpenting yang ditemukan dalam kakao adalah flavanol yang terdiri dari monomer katekin dan epikatekin dan oligomer procianidin (CIC 2001).
Gambar 3 Struktur kimia katekin, epikatekin dan prosianidin pada kakao (Andersen dan Markham, 2006)
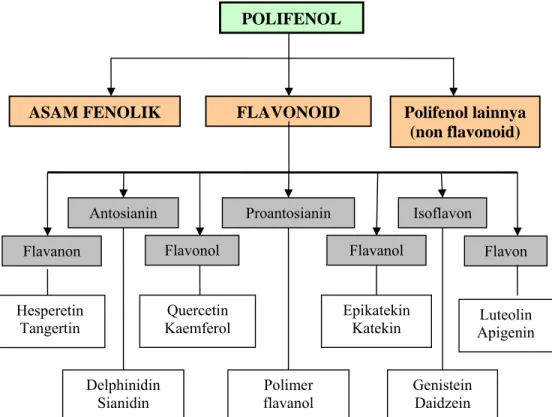
Flavonoid yang merupakan salah satu sub kelas dari polifenol mempunyai 7 kelas utama yaitu antochyanin, proantochyanin, isoflavone, flavanone, flavonol, flavanol, dan flavone.
FLAVONOID Flavanon Flavon Luteolin Apigenin Antosianin Delphinidin Sianidin Flavonol Quercetin Kaemferol Proantosianin Flavanol Epikatekin Katekin Isoflavon Genistein Daidzein Polimer flavanol
ASAM FENOLIK Polifenol lainnya
(non flavonoid) Hesperetin Tangertin POLIFENOL R1=H, R2=OH=(+)-catekin Prosianidin R1=OH, R2=H=(-)epikatekin
Kakao mengandung senyawa flavonoid golongan flavanol, yang memberikan efek yang menguntungkan bagi tubuh. Selain itu juga bisa mengurangi resiko mortalitas dan morbiditas kardiovaskuler, kanker dan osteoporosis dan bisa mencegah penyakit neurodegeneratif serta diabetes militus (Grassi et al 2006). Murphy et al (2003) menyatakan bahwa mengkonsumsi flavonoid dan prosianidin secara teratur dapat meningkatkan konsentrasi epikatekin dan katekin di dalam plasma tetapi tidak menyebabkan oksidasi, dan juga dapat mengurangi agregasi dan aktivasi platelet penyebab peradangan. Prosianidin kakao bermanfaat dalam modulasi respon imun dan inflamasi pada mamalia. Selain itu, prosianidin kakao dari kakao cair ataupun kering bisa terdapat dalam makanan, suplemen dan obat-obatan untuk modulasi produk gen sitokin dan kadar protein dan memberikan efek menguntungkan pada penderita penyakit asma, peradangan akibat virus atau resiko peradangan virus (Schmitz et al 2001). Prosianidin yang dikombinasikan dengan L-arginin meningkatkan pengaruh fisiologis dalam memproduksi nitrat oksida pada mamalia yang mencerna produk itu. Efeknya antara lain menurunkan tekanan darah, ketahanan terhadap penyakit kardiovaskuler dan aktivitas antikanker (Cheuvaux et al 1999).
Pada manusia, bioavailabilitas flavonoid berkisar antara 1-26 %. Pada tubuh kita flavonoid akan bersikulasi dalam plasma, terdapat sebagai glukoronida, methyl dan sulfat konjugat atau kombinasi dari ketiganya yang merupakan hasil reaksi enzim fase I dan fase II (Grassi et al 2006).
Antioksidan
Antioksidan adalah zat yang mampu memperlambat atau mencegah proses oksidasi (Schuler, 1990). Menurut Gutteridge dan Halliwell (1996), antioksidan adalah suatu substansi yang menghentikan atau menghambat kerusakan oksidatif terhadap suatu molekul target. Sementara itu menurut Cillard et al (1980) dan Schluler (1990) antioksidan adalah zat dengan kadar lebih rendah dari zat yang mudah teroksidasi, secara nyata mampu memperlambat oksidasi zat tersebut. Sebaliknya pada kadar tinggi zat antioksidan bersifat peroksidan atau meningkatkan oksidasi. Antioksidan biologis adalah zat yang mampu melindungi
sistem biologis dari kerusakan akibat kelebihan oksidasi (Krinsky 1992). Antioksidan primer adalah zat yang dapat bereaksi dengan radikal bebas atau mengubahnya menjadi produk yang stabil, sedangkan antioksidan sekunder atau antioksidan preventif dapat mengurangi laju awal reaksi rantai atau tahap inisiasi reaksi oksidasi.
Ada 2 macam antioksidan yaitu antioksidan primer dan sekunder (Winarno, 1997), yaitu :
1. Antioksidan Primer
Antioksidan primer adalah suatu zat yang dapat menghentikan reaksi berantai pembentukan radikal yang melepaskan hidrogen. Zat-zat yang termasuk golongan ini dapat berasal dari alam seperti tokoferol, lesitin, fosfatida, dan asam askorbat serta antioksidan buatan seperti BHA (Butylated hydroxyanisole), BHT (Butylated hydroxytoluene), dan PG (Propylgallate).
2. Antioksidan Sekunder
Antioksidan sekunder adalah suatu zat yang dapat mencegah kerja prooksidan sehingga dapat digolongkan sebagai sinergi. Beberapa asam organik tertentu dapat mengikat logam-logam (sequestran), misalnya satu molekul asam sitrat akan mengikat prooksidan Fe seperti sering dilakukan pada minyak kacang kedelai. EDTA (Etilendiamin tetra asetat) adalah sequestran logam yang sering digunakan dalam minyak salad.
Mekanisme kerja antioksidan dapat melalui beberapa cara, antara lain yang dilaporkan oleh Charpentier dan Cateora (1996) adalah: 1) menghambat terbentuknya radikal bebas, 2) menjadi perantara dalam netralisasi radikal bebas yang telah terbentuk (scavenger), 3) menurunkan kemampuan radikal bebas dalam reaksi oksidasi, dan 4) menghambat enzim oksidatif, misalnya sitokrom P-450. Penghambatan reaksi radikal bebas akan melidungi hepatosit normal dari kerusakan dan mengoptimalkan lingkungan bagi sel-sel hati untuk bergenerasi. Menurut Shahidi (1997), antioksidan diketahui bekerja pada berbagai tahapan oksidasi molekul lemak, yaitu dengan cara menurunkan kadar oksigen, menangkap singlet oksigen, pencegahan tahap inisiasi reaksi rantai melalui penangkapan radikal hidroksil, pengikatan ion logam katalisator, dekomposisi
produk utama menjadi senyawa non radikal dan pemutusan reaksi rantai untuk mencegah kelanjutan penarikan elektron dari substrat. Antioksidan dapat berasal dari bahan alami dan sintetik. Sumber antioksidan alami telah banyak dilaporkan berasal dari tanaman.
Menurut Papas (1999), enzim-enzim antioksidan seperti katalase, glutathion peroksidase, superokside dismutase, dan peroksidase merupakan lini pertama dari sistem pertahanan tubuh yang menahan pembentukan radikal bebas. Pada lini pertahanan kedua, antioksidan yang menangkap radikal seperti vitamin C, vitamin E, karotenoid dan flavonoid berfungsi untuk menghambat rantai inisiasi dan atau memecah rantai propagasi. Lini pertahanan ketiga dipegang oleh enzim fosfolipase, protease, transferase, dan DNA repair enzyme yang berfungsi untuk memperbaiki kerusakan membran. Lini terakhir dari sistem pertahanan tubuh adalah proses adaptasi, dimana tubuh akan memproduksi enzim antioksidan yang sesuai untuk ditransfer ke sisi tertentu pada waktu dan konsentrasi yang tepat.
Penelitian tentang antioksidan pada tanaman telah banyak dilakukan. Chipault et al (1952) menguji aktivitas antioksidan dari 32 jenis rempah-rempah dan Puspita-Nienaber et al (1992) menguji aktivitas antioksidan dari 23 jenis ekstrak rempah-rempah asal Indonesia. Nakatani (1997) meringkas hasil penelitian tentang aktivitas antioksidan senyawa fenolik dari berbagai tanaman, antara lain: rosmaridifenol, rosmarikuinon, epirosmanol, dan isorosmanol dari rosemary; karnosol dari sage; asam hidroksibenzoat dan hidroksinamat dari oregano; thymol dan karvarol dari thyme; kapsaicin dan hidrokapcaisin dari cabe; sesamol dan lignan dari wijen; katekin dari teh hijau; dan kurkuminoid dari kunyit. Zhu et al (2005) menyatakan bahwa katekin, epikatekin, yang diisolasi dari kakao dapat mengurangi kerentanan eritrosit terhadap radikal bebas penyebab hemolisis.
Radikal bebas dan kerusakan sel
Radikal bebas dapat menyebabkan stres oksidatif. Stress oksidatif merupakan keadaan ketidakseimbangan antara reaktif oxygen species (ROS) / reaktif nitrogen species (RNS) dan antioksidan (Halliwell & Gutteridge 2001).
Jika radikal bebas berada dalam jumlah berlebihan dan jumlah antioksidan seluler tetap atau lebih sedikit maka kelebihannya tidak bisa dinetralkan dan berakibat pada kerusakan sel (Langseth 1995; Palmer & Paulson 1997). Kerusakan sel merupakan gangguan atau perubahan yang dapat mengurangi viabilitas dan fungsi essensial sel (Kehrer 1993). Stress oksidatif dapat menyebabkan kematian sel secara apoptosis dan nekrosis. Menurut Zitouni et al (2005), radikal bebas juga dapat mengganggu endotelium dan memacu terjadinya kerusakan membran, sebagai contohnya akan meningkatkan ekresi albumin urin dan memacu diabetes.
Reaksi tidak terkendali radikal bebas terhadap komponen sel seperti asam lemak tidak jenuh ganda (PUFA), heksosa, pentosa, asam amino dan komponen DNA menghasilkan beberapa produk seperti : Malonaldehida atau MDA, diena terkonjugasi, dikarbonil dan asam 15-hidroperoksi-5,8,4,13 eikosatetraenoik (15-HPETE). MDA merupakan melekul dialdehid yang mempunyai tiga atom karbon dan bersifat reaktif (Rice-Evan et al. 1991; Zaden et al. 1995). 1,1,3,3-tetraetoksipropan merupakan prekusor malondialdehid sehingga sebagai larutan standar dapat digunakan larutan tetraektoksipropan.
Malonaldehida atau MDA (C3H4O2) merupakan salah satu hasil peroksidasi asam lemak tidak jenuh (ALTJ) terutama asam arakhidonat (Bird dan Draper, 1984; Frankel dan Neff, 1983). Malonaldehida atau MDA dijumpai juga sebagai produk samping biosintesis prostaglandin. Pengukuran MDA telah digunakan sebagai indeks tidak langsung kerusakan oksidatif yang disebabkan oleh peroksidasi lipida (Auroma 1997).
Peningkatan kadar Malonaldehida dapat ditekan dengan pemberian antioksidan seperti vitamin C, A, dan E dan beberapa komponen bioaktif (Cho et al. 2000; Palloza et al. 2000; Kris-Ethon & Keen 2002) yang secara keseluruhan dapat menekan proses peroksidasi lipid.
Senyawa-senyawa yang menjadi target ROS atau radikal bebas adalah molekul-molekul seluler dan ektraseluler antara lain: protein, asam lemak tidak jenuh ganda, glikoprotein, lipoprotein dan bahan-bahan penyusun DNA seperti karbohidrat dan basa purin.
Di bawah ini disajikan beberapa jenis radikal bebas dan ROS yang berperan pada kerusakan sel.
Tabel 2 Jenis-jenis Reaktif Oxygen Species dan radikal bebas yang berperan pada kerusakan sel
Radikal bebas Lambang Non radikal Lambang Hidrosil Superoksida Nitrit oksida Lipid peroksida OH* O2* NO* LOO* Hidrogen peroksida Singlet oksigen Asam hipoklorida Ozon H2O2 1O 2 HOCl O3 (Halliwell & Gutteridge 1999).
Berdasarkan hasil penelitian, radikal bebas dan ROS dalam tubuh makhluk hidup berasal dari :
1. Pada organisme aerob, 95% oksigen dalam sel direduksi menjadi air oleh rantai pernafasan pada mitokondria, proses reduksi ini melibatkan 4 elektron dan 2 proton. Kebocoran elektron diperkirakan mencapai 1-5%, elektron yang bocor ini bereaksi dengan oksigen membentuk radikal superoksida (O2*), hidrogen peroksida (H2O2) dan radikal hidroksil (OH*) (Lehninger, 1993). 2. Reduksi O2 menjadi superoksida pada fagositosis. Fagositosis merupakan salah
satu sistem pertahanan humoral dalam melawan infeksi atau bahan asing yang masuk kedalam tubuh. Dengan bantuan NADPH-oksidase, netrofil dan makrofag (Haliwell & Gutteridge 1999).
3. Peristiwa iskemi yaitu deplesi ATP akibat kekurangan oksigen dimana terjadi pemecahan ATP menjadi AMP, adenosine dan hipoxantin. Hipoxantin diubah oleh xantin oksidase, menjadi asam urat dan radikal bebas seperti: superoksida, hidrosil dan hydrogen peroksida (Greenwald 1985; Haliwell & Gutteridge 1999).
4. Reaksi Fenton dan Haber-weiss, melalui reaksi oksidasi-reduksi yang dikatalis oleh Fe+2 dan Fe+3. Fe+2 dan Fe+3 berasal dari hemoglobin dan mioglobin (Greenwald 1985; Zakaria 1996; Haliwell & Gutteridge 1999).
5. Radikal bebas juga dihasilkan dari reaksi metabolisme eicosanoidi yaitu metabolisme asam arakhidonat melalui mekanisme prostaglandin atau
leukotrin. Perubahan ini menghasilkan ROS (Rise-Evan et al. 1991; Haliwell 1994).
6. Secara alamiah sel-sel tubuh baik sel normal ataupun sel kanker melakukan apoptosis yaitu program bunuh diri. Apoptosis menjadi penting karena jika jumlahnya menjadi berlebihan maka akan memicu kelainan. Pada saat sel melakukan apoptosis maka semua isi sel akan keluar (Roitt 1991; Haliwell & Gutteridge 1999).
Sistem pertahanan tubuh nonenzimatik
Sistem pertahanan tubuh nonenzimatik terhadap serangan radikal bebas melibatkan vitamin C, vitamin E dan komponen-komponen bioaktif. Pertahanan nonenzimatik terhadap radikal bebas dibagi atas 2 kelompok besar yaitu : sistem pertahanan preventif dan pemutusan rantai reaksi radikal bebas (Nabet 1996).
Sistem pertahanan tubuh enzimatik
Sistem Pertahanan Tubuh Enzimatik terhadap radikal bebas melibatkan : enzim superoksida dismutase (SOD), katalase dan glutation peroksidase (GSH-Px) (Halliwell et al. 1992; Schmidl et al, 2000).
a. Superoksida dismutase (SOD)
Superoksida dismutase adalah metaloenzim yang mengkatalis dismutasi radikal anion superoksida menjadi hydrogen peroksida dan oksigen. SOD tidak stabil terhadap panas, cukup stabil pada kondisi basa. SOD masih mempunyai aktivasi walaupun disimpan selama 5 tahun pada suhu 5 0C (http:/www. Orthington-biochem.com). Untuk aktivitasnya SOD membutuhkan logam seperti Zn, Cu, dan Mn sebagai kofaktor (Mc Cord & Fridovich 1969).
Aktivitas SOD dihambat oleh sianida dan H2O2, oleh karena SOD dihambat oleh H2O2 maka dalam kerjanya SOD sangat membutuhkan katalase (Rice-Evan et al. 1991; Haliwell & Gutteridge 1999). Aktivitas SOD (U/g jaringan) tertinggi ditemukan didalam hati. SOD juga ditemukan pada kelenjar adrenalin, ginjal, darah, limfa, pankreas, otak, paru-paru, lambung, usus, ovarium, dan timus (Haliwell and Gutteridge 1999).
Aktivitas SOD diukur berdasarkan pengukuran aktivitas enzim secara tidak langsung, salah satunya dengan metode yang dikembangkan oleh Misra dan Fridovich (1997). Metode ini berdasarkan kepada kemampuan penghambatan autooksidasi epinefrin menjadi adenokrom oleh SOD. Perubahan epinefrin menjadi adenokrom menimbulkan warna coklat, makin besar kadar SOD sampel maka makin besar penghambatan dan makin kurang intensitas warna. Warna coklat dideteksi secara spektrofotometri.
b. Enzim Glutation Peroksidase
Glutation Peroksidase merupakan selonoprotein sebagai active site, terdiri dari 4 sub unit protein yang dapat mengkatalis reaksi reduksi H2O2 menjadi senyawa organik hidroperoksida (ROOH) (Rice-Evan et al. 1991; Haliwell 1994). Glutation peroksidase menggunakan glutation tereduksi (GSH) sebagai substrat. Glutation Peroksidase mereduksi hidroperoksida dan pada saat yang sama glutation tereduksi mengalami oksidasi. Pada manusia, aktivitas glutation peroksidase sebanding dengan konsentrasi selenium (Se) plasma.
Glutation Tereduksi
Glutation (L-γ-glutamil-cysteinyl-glisin) merupakan tripeptida yang mengandung gugus sulfuhidril (-SH). Glutation merupakan salah satu sistem antioksidan, terutama berpartisipasi dalam penghancuran H2O2 dan peroksida organik (Greenwald 1985). Ada dua jenis glutation yaitu glutation tereduksi dan glutation teroksidasi. Glutation banyak ditemukan dalam sitosol hati. Keberadaan GSH di dalam sel sangat diperlukan sebagi substrat glutation peroksidase dan sebagai senyawa konjugat detoksifikasi xenobiotik pada reaksi enzim fase II (Hodgoson & Levi 2000).
c. Enzim katalase
Katalase merupakan enzim yang mengkatalis reaksi pemecahan senyawa hidrogen peroksida menjadi oksigen dan air.
2H2O2 Katalase H2O + O2
Katalase ditemukan pada hewan dan tumbuhan tingkat tinggi. Katalase pada mamalia disusun oleh 4 sub unit protein. Tiap unit terdiri dari satu gugus hem dengan inti ion ferri sebagai active site. Aktivitas katalase dihambat oleh senyawa
azida, sianida dan HOCl tapi meningkat dengan meningkatnya akumulasi H2O2 (Haliwell & Gutteridge 1999).
Pada manusia, katalase ditemukan di dalam darah, ginjal, limfa, pankreas, otak, jantung, paru-paru, adipose, kelenjar adrenal dan konsentrasi tertinggi terdapat pada hati (± 1400 U/mg protein) ( Halliwell 1994) bersama-sama dengan glutation peroksida (Greenwald 1985). Pada organ dan jaringan ini katalase ditemukan di dalam peroksisom, mitokondria, dan retikulum endoplasma. Hidrogen peroksida di dalam tubuh melalui dua mekanisme yaitu:
1. Pemecahan oleh katalase membentuk air dan molekul oksigen 2H2O2 Katalase H2O + O2
2. Pemecahan oleh glutation peroksidase dengan bantuan substrat glutation GSH- + H2O2 GSH-Px GS + H2O
Salah satu metode penentuan aktivitas katalase adalah metode kalorimetri yang dikembangkan oleh Sinha (1972). Metode ini menggunakan zat warna bikromat sebagai indikator dimana ion bikromat dalam suasana asam dapat direduksi oleh H2O2menjadi kromat. Perubahan warna yang muncul dibaca secara spektrofotometri pada panjang gelombang 570 nm. Satu unit aktivitas katalase adalah banyaknya H2O2 yang dipakai oleh katalase permenit.
Metabolisme xenobiotik dan detoksifikasi senyawa beracun
Toksikologi dapat didefenisikan sebagai cabang ilmu yang mempelajari tentang zat-zat yang beracun. Namun pengertian ini terus berkembang seiring dengan semakin kompleksnya kehidupan sosial masyarakat. Selanjutnya toksikologi tidak hanya dikaitkan dengan zat-zat yang beracun tetapi juga mempelajari tentang pendeteksian, keberadaan, efek dan regulasi dari senyawa toksik (Hodgoson & Levi, 2000). Toksikologi berhubungan erat dengan cabang farmakologi/ farmasi. Hal ini bisa dijadikan dasar pengetahuan tentang metabolisme senyawa asing atau yang lebih dikenal dengan xenobiotik (Murray et al. 1999). Xenobiotik merupakan senyawa asing yang masuk ke dalam tubuh kita
dan bukan merupakan komponen gizi. Xenobiotik ini dikeluarkan oleh tubuh kita melalui proses detoksifikasi (Hodgoson & Levi, 2000).
Toksikologi pangan berhubungan erat dengan keamanan pangan karena makhluk hidup tidak lepas dari makanan. Berbagai macam makanan ternyata tidak sepenuhnya bebas dari zat kimia toksik atau xenobiotik yang berada pada makanan sebagai zat tambahan makanan, pencemar makanan ataupun zat toksik alamiah. Contoh xenobiotik pangan antara lain alkohol, flavon (zat toksik alamiah), BHA (antioksidan pangan), benzopiren yang terdapat pada daging panggang dan lain sebagainya (Donatus 2001).
Timbulnya pengaruh bahaya atau efek toksik racun atas makhluk hidup terjadi melalui beberapa proses. Pertama kali makhluk hidup menerima racun, berikutnya mengalami absorbsi, distribusi racun atau metabolitnya ke tempat aksi yaitu sel sasaran atau reseptor yang ada dalam makhluk hidup. Di dalam aksi ini, kemudian terjadi reaksi antara racun atau metabolitnya ke tempat aksi sel sasaran atau reseptor, dan berbagai peristiwa biokimia dan biofisika berikutnya, akhirnya timbul pengaruh berbahaya atau efek toksik dengan wujud dan sifat tertentu. Jadi toksisitas suatu senyawa ditentukan oleh keberadaan yang meliputi kadar dan lama tinggal senyawa itu atau metabolitnya di tempat aksinya dan keefektifan antar aksinya (mekanisme aksi). Reaksi yang berlangsung juga tergantung pada kondisi makhluk hidup (Donatus 2001).
Metabolisme senyawa beracun dapat didefenisikan sebagai perubahan hayati atau biotransformasi zat kimia toksik menjadi suatu metabolit yang secara kimia berbeda dengan zat kimia induknya, dalam diri makhluk hidup. Hal ini mengandung arti bahwa pertama, di dalam tubuh zat kimia toksik tersebut mungkin mengalami perubahan struktur molekul melalui mekanisme tertentu. Kedua, perubahan bentuk struktur tersebut akan mengakibatkan perubahan sifat-sifat fisika-kimia yang berbeda dengan zat induk. Ketiga, bentuk ubahannya yang disebut bentuk metabolit yang memilki sifat fisika kimia yang berbeda dengan zat induk. Keempat, akibat perubahan sifat fisika-kimia tersebut menyebabkan metabolit memiliki kelarutan dalam air atau lipid, aktivitas dengan jaringan atau tempat aksi dan aktivitas intrinsik yang berbeda dengan zat induknya. Kelima,
hasil bersih berbagai perubahan biokimia tersebut adalah perubahan ketoksikan zat induk, sehingga respon toksik makhluk hidup terhadap racun juga akan berubah (Donatus 2001).
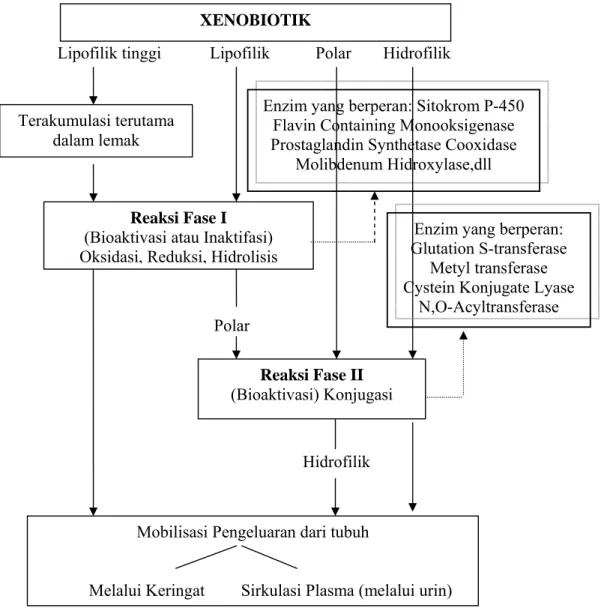
Beberapa langkah biotransformasi xenobiotik dalam tubuh terlihat pada gambar berikut:
Lipofilik tinggi Lipofilik Polar Hidrofilik
Polar
Hidrofilik
Gambar 5 Biotransformasi xenobiotik di tubuh (Blaauboer 1996)
Hodgoson & Levi (2000) menyebutkan bahwa mekanisme pergerakan bahan toksik melewati membran-membran khususnya pada awal masukan, merupakan hal yang kurang menjadi perhatian dengan baik, meskipun sesungguhnya telah
XENOBIOTIK
Terakumulasi terutama dalam lemak
Reaksi Fase I (Bioaktivasi atau Inaktifasi) Oksidasi, Reduksi, Hidrolisis
Reaksi Fase II (Bioaktivasi) Konjugasi
Mobilisasi Pengeluaran dari tubuh
Melalui Keringat Sirkulasi Plasma (melalui urin)
Enzim yang berperan: Sitokrom P-450 Flavin Containing Monooksigenase Prostaglandin Synthetase Cooxidase
Molibdenum Hidroxylase,dll
Enzim yang berperan: Glutation S-transferase
Metyl transferase Cystein Konjugate Lyase
dilakukan pada masalah khusus obat-obatan. Terdapat 4 mekanisme pokok yang memungkinkan bahan toksik untuk melintasi membran.
1. Transpor pasif. Mekanisme ini mendominasi hampir semua bahan toksik. Pengangkutan pasif melibatkan pergerakan campuran-campuran melewati membran-membran lipid oleh difusi sederhana dengan koefisien pembagi air/ lipid yang sebagian besar menentukan tingkat pergerakan. Campuran-campuran dalam bentuk yang telah diionisasi tidak menggerakan dengan sangat cepat oleh difusi melalui membran untuk beberapa alasan. Pertama, bentuk yang telah diionisasi cenderung memiliki daya larut lipid rendah, sebuah faktor yang sangat penting untuk difusi membran. Kedua, memungkinkan terjadinya interaksi ion antara xenobiotik, lipid, dan protein dalam membran.
2. Filtrasi. Seringkali pori-pori dalam membran memperbolehkan masuknya dengan berat molekul kurang dari 100 dalton. Molekul-molekul yang lebih besar, bagaimanapun juga, dikeluarkan kecuali dalam banyak jaringan-jaringan yang penyerapannya tinggi, seperti ginjal dan hati. Karena kebanyakan bahan toksik relatif bermolekul sangat besar, jalan kecil ini seringkali memiliki arti penting mekanisme penyerapan yang terbatas. Filtrasi umumnya memiliki arti yang sangat penting dalam pembuangan bahan toksik, khususnya ginjal.
3. Transpor khusus. Sejumlah sistem pengangkutan khusus, terutama sekali pada bidang gastro intestinal, membantu dalam pengangkutan campuran endogen melalui membran. Proses tersebut dapat membutuhkan energi dan memungkinkan senyawa untuk melewati gradien konsentrasi (transpor aktif) atau mungkin tidak memerlukan energi dan tidak dapat menggerakkan senyawa melewati sebuah tanjakan/ gradien (pengangkutan yang difasilitasi). Meskipun hasilnya bisa jadi berbeda, mekanisme ini agak mirip dan telah didiskusikan bersama. Pada kedua masalah ini, protein pembawa yang bergabung dengan bahan toksik telah diketahui. Protein ini membantu pergerakan bahan toksik dari satu sisi membran ke yang lain, dan di lain sisi, bahan kimia berpisah dari protein, yang kemudian bebas untuk mengambil
molekul bahan toksik yang lain. Penetrasi seperti itu lebih cepat daripada difusi sederhana dan dalam hal pengangkutan aktif, dapat diproses di luar titik yang berkonsentrasi sama pada kedua sisi membrannya.
Mekanisme ini mungkin menjadi penting dan relatif jarang terjadi dalam bahan toksik yang memiliki bahan kimia atau struktur menyerupai bahan kimia endogen yang berprinsip pada mekanisme pengangkutan khusus untuk pengambilan fisiologi normal dan itu dapat menggunakan sistem yang sama. Sebagai contoh, 5-fluorouracil diangkut oleh sistem pengangkutan timidin. Timah dapat dipindahkan secara cepat dengan sistem pengangkutan yang dilibatkan secara normal pada pengambilan kalsium. Sebagai mekanisme penyerapan, sistem pengangkutan khusus ini banyak dimuat pada penyerapan gastro intestinal. Mekanisme ini menjadi lebih besar perannya dalam pembuangan bahan racun, bagaimanapun juga pengangkutan khusus penting pada pemindahan xenobiotik dan metabolitnya. Sifat penting dari pengangkutan khusus adalah mereka memperbolehkan pergerakan senyawa dengan daya larut lipid lebih rendah, hal ini menyangkut senyawa-senyawa yang biasanya diharapkan untuk bergerak sangat lambat melewati membran lipid yang sangat tinggi. Kebanyakan sistem pengangkutan aktif dihubungkan ke energi yang menghasilkan enzim (misalnya ATPase), dan kedua sistem pengangkutan aktif dan difasilitasi memperlihatkan sifat saturasi (dengan kata lain, saturasi dari ketersediaan protein pembawa oleh molekul bahan toksik). Dengan begitu, kinetik/ ilmu gerak dari sistem pengangkutan khusus dapat dijelaskan lebih baik lagi dengan menggunakan model kinetik enzim Michaelis-Menton.
4. Endositosis. Pinositosis (untuk cairan) dan pagositosis (untuk padat) adalah proses pengangkutan yang dikhususkan pada permukaan membran atau pengaliran disekeliling bahan kimia yang memungkinkan transfer yang lebih cepat melalui membran. Hanya pada pemisahan kejadian seperti penyerapan dari karagen (mol wt ~40.000) dalam usus memiliki mekanisme ini yang telah ditemukan menjadi penting pada masukan awal. Setelah di dalam tubuh,
bagaimanapun juga endositosis adalah mekanisme yang sedikit umum dan penelanan senyawa di dalam paru-paru adalah umum (pagositosis paru-paru)
Berlangsungnya metabolisme senyawa asing di dalam tubuh, dapat terjadi di dalam hati, ginjal, usus, kulit, kelenjar kelamin, plasenta serta darah. Meskipun hati merupakan organ utama dalam sistem biotransformasi, tetapi metabolisme senyawa xenobiotik juga dapat berlangsung pada jaringan-jaringan di luar hati, misalnya saja darah (Krovat et al. 2000). Setelah toksikan masuk ke dalam sirkulasi darah, maka toksikan tersebut akan didistribusikan atau disebar ke seluruh jaringan tubuh manusia (Donatus 2001). Menurut Hodgoson dan Levi (2000), cairan tubuh memegang peranan penting dalam pendistribusian toksikan dalam tubuh yang telah diabsorpsi.
Metabolisme seyawa xenobiotik terdiri dari dua fase. Pada fase satu, toksikan bersifat lipofilik akan ditransformasikan oleh enzim-enzim fase satu (monoksigenase) menjadi senyawa-senyawa metabolit yang bersifat polarreaktif grup. Pada fase dua, metabolit yang terbentuk akan dikonjugasikan oleh enzim-enzim fase dua (konjugasi) sehingga dihasilkan senyawa yang bersifat hidrofilik dan mudah diekresikan ke luar tubuh. Namun jika metabolisme senyawa xenobiotik menghasilkan produk yang reaktif, maka akan menimbulkan efek toksik bagi tubuh (Hodgoson & Levi, 2000).
A. Reaksi fase satu
Reaksi-reaksi fase satu meliputi monooksigenasi mikrosom, oksidasi mitokondria dan sitosol, kooksidasi dalam reaksi sintesis prostaglandin, reduksi, hidrolisis dan hidrasi epoksida. Semua reaksi pada fase satu menghasilkan metabolit atau merubah toksikan menjadi lebih polar sehingga dapat dikonjugasi dalam reaksi-reaksi fase dua dan mudah diekresikan baik secara langsung maupun tidak langsung setelah mengalami reaksi fase satu (Hodgoson & Levi, 2000). Lebih lanjut, Donatus (2001) menjelaskan bahwa fungsi utama reaksi metabolisme fase I adalah mengubah struktur senyawa asing melalui proses oksidasi, reduksi atau hidrolisis, guna memasukkan gugus fungsional yang sesuai bagi reaksi konjugasi fase II.
Enzim yang berperan penting dan terlibat paling dominan pada reaksi fase I adalah enzim monoksigenase Sitokrom P-450. Berdasarkan percobaan yang dilakukan oleh Omura dan Sato (1964), maka mereka mendefenisikan Sitokrom P-450 sebagai suatu protein heme yang mengandung satu molekul besi-protoporfirin IX sebagai gugus prostetik atau gugus aktifnya. Nama sitokrom P-450 diperoleh dari kenyataan bahwa sitokrom memberikan satu spektra resapan maksimum pada panjang gelombang 450 nm, bila tereduksi dan terkompleks dengan karbon monoksida. Sifat ini khas diperantarai oleh adanya gugus tiolat sebagai suatu ligan protein heme itu. Menurut Donatus (2001) Sitokrom P-450 menunjukkan selektivitas yang luas terhadap aneka ragam substrat. Keadaan ini disebabkan oleh adanya aneka ragam isoenzim sitokrom tersebut, yang satu dengan yang lainnya berbeda dalam struktur rantai polipeptida dan kekhasan reaksi yang dikatalisirnya.
Induksi terhadap metabolisme fase I, terutama yang dikatalisir oleh sitokrom P-450 mikrosomal memilki arti penting karena sistem ini sering membentuk metabolit perantara yang reaktif atau toksik (Donatus, 2001). Beberapa produk yang dibentuk oleh enzim ini berimplikasi pada penyebab penyakit kanker atau karsinogenik (Shimada et al, 1996). Intermediet yang terdapat dalam aktivasi dioksigen merupakan awal terbentuknya superoksida atau peroksida. Mekanisme aktivasi dioksigen diketahui sebagai tahap terakhir dari katalisis P-450, yang dimulai dengan reduksi komplek dioksigen (Benson et al, 1997).
Ada dua hal penting yang berhubungan dengan fungsi enzim sitokrom P-450, yang pertama adalah enzim ini memiliki jalur yang kritis dan spesifik dalam metabolisme senyawa-senyawa kimia endogenus. Kedua, Proses enzim ini merupakan pokok dari produk-produk alami, bahkan saat ini ditambah dengan bahan-bahan kimia seperti obat-obatan dan xenobiotik lainnya dalam senyawa-senyawa non selektif (Guengerich 1991). P-450 dan komponennya bisa ditemukan di kulit, mukus, paru-paru, gastrointestinal. Selain organ-organ tersebut juga telah banyak dilakukan penelitian tentang keberadaan P-450, diantaranya di hati, ginjal, plasenta, testis serta pada darah (Hodgoson & Levi, 2000).
B. Reaksi fase dua
Pada reaksi fase dua, senyawa yang terhidroksilasi atau senyawa lainnya yang diproduksi dalam fase satu, diubah oleh enzim yang spesifik menjadi berbagai metabolit polar lewat konjugasi dengan asam glukuronat, sulfat, asetat, glutation atau asam amino tertentu lewat metilasi. Reaksi konjugasi ini membuat molekul lebih bersifat dapat larut dalam air sehingga akhirnya dapat diekresikan ke dalam urin dan empedu (Murray et al. 1999).
Reaksi fase dua lebih dikenal dengan reaksi konjugasi, menyangkut penambahan gugus polar ke senyawa asing. Reaksi fase dua merupakan reaksi biosintetik, maka dibutuhkan energi sehingga reaksi dapat berlangsung. Reaksi penting pada fase II adalah reaksi konjugasi glutation karena sering terlibat dalam penghilangan zat atau metabolit perantara yang reaktif, yakni yang bersifat elektrofil. Berlangsungnya reaksi ini dikatalisir oleh enzim glutation S-transferase (Donatus 2001).
Glutation S-transferase merupakan suatu famili enzim yang mengkatalisir tahap awal pembentukan N-asetilsisteina (asam merkapturat) yang terutama terdapat dalam sitosol testis, hati, ginjal, usus, kelenjar adrenal (Donatus 2001). Enzim ini berperan dalam binding, transport dan detoksifikasi komponen endogenus maupun eksogenus. Glutation S-transferase ditemukan dalam jumlah yang besar pada hati, tetapi juga terdapat pada aliran darah terlebih lagi jika hati mengalami kerusakan (Mulder et al 1999).
Sejumlah xenobiotik elektrofilik yang berpotensi beracun akan terkonjugasi dengan glutation nukleofilik dalam reaksi berikut:
R + GSHO R – S - G
Dimana R adalah xenobiotik elektrofilik. Jika xenobiotik yang potensial beracun tidak terkonjugasi maka molekulnya akan berada dalam keadaan bebas yang membentuk ikatan kovalen dengan DNA, RNA atau protein sel dengan demikian dapat mengakibatkan kerusakan sel yang serius (Murray et al. 1999).
Induksi enzim detoksifikasi glutation S-transferase merupakan mekanisme pertahanan terhadap kanker. Prinsipnya peningkatan enzim glutation S-transferase
dapat mereduksi karsinogenesis melalui penguatan pembuangan elektrofil reaktif (Kirlin et al. 1999). Analisis yang digunakan dengan menggunakan prinsip bahwa GSH dapat berkonjugasi dengan 1-kloro-2,4-dinitrobenzene (CDNB) dengan adanya katalis enzim glutation S-transferase dan menghasilkan produk dapat diukur secara spektrofotometri (Habig et al. 1974).
Metabolisme Senyawa Bioaktif
Metabolisme senyawa bioaktif seperti senyawa flavonoid dalam tubuh dipengaruhi oleh struktur kimia dan perlunya molekul itu mengalami konjugasi. Meskipun bioavailabilitas flavonoid bervariasi antara flavonoid tipe satu dan yang lain, mulai dari antosianin yang sangat sedikit diserap dan isoflavon yang dengan mudah diserap, jalur dalam mekanisme absorbsi pada umumnya sama untuk semua flavonoid. Perubahan melalui jalur metabolisme ditentukan oleh spesifitas dan aktivitas transporter, spesifitas dan aktivitas metabolisme dan stabilitas flavonoid (Meskin et al, 2004).
Senyawa flavonoid dalam tanaman biasanya dalam bentuk glikosida. Glikosida flavonoid yang diasup tubuh mencapai usus halus melalui jalur pencernaan. Senyawa flavanol seperti katekin dan proanthosianin oligomer sebagian besar tidak terglikosolasi harus dideglikolasi. Deglikosilasi dapat terjadi pada beberapa tempat dalam duodenum dan jejenum dalam lumen intestinal, brush border atau hidrolase intraseluler setelah terjadinya transport flavonoid ke dalam enterosit. Deglikosilasi adalah perlakuan awal sebelum konjugasi oleh enzim yang terdapat dalam usus dan transport sampai serosol atau sisi mukosal. Hal yang sama juga berlaku untuk isoflavon, aglikonnya dapat diserap dalam usus halus. Tahap awal proses absorbsi untuk flavonoid terglikosilasi dan isoflavon adalah deglikosilasi oleh lactase phlorizin hydrolase (LPH) yang merupakan enzim yang terletak dalam bagian brush border dari usus halus yang bertanggung jawab dalam hidrolisis laktosa (Meskin et al 2004).
Hasil dari reaksi deglikosilasi adalah aglikon bebas yang dapat berdifusi ke dalam sel-sel epitel secara pasif atau secara difusi fasilitatif. Reaksi deglikosilasi ini adalah reaksi yang spesifik dan memiliki aktivitas yang besar. Reaksi
selanjutnya yang terjadinya adalah penyerapan atau absorbsi. Penyerapan glikosida flavonoid tidak dipengaruhi oleh perlakuan awal menggunakan β-glukosidase dari mikroba diduga karena enzim LPH dalam usus halus mengakatalis reaksi yang sama. Absorbsi aglikon dalam lumen tergantung pada keberadaan komponen-komponen lain dan juga karena kelarutan atau koefisien partisi dari flavonoid. Mekanisme absorbsi alternatif yang terjadi melibatkan transpor glikosida flavonoid ke dalam enterosit dalam bentuk serapan melalui fungsi transporter gula. Kedua jalur absorbsi menaikkan jumlah aglikon intaraseluler transient yang ditemukan dalam jaringan usus halus tikus setelah reaksi fusi in vitro dengan glukosida quarcetin atau isoflavon (Meskin et al, 2004).
Reaksi yang terjadi selanjutnya adalah konjugasi. Usus memiliki kapasitas konjugasi tertentu termasuk oleh glukoronosyl transferase atau UGTs dan glutation transferase. Absorbsi di usus halus menentukan transfer flavonoid dari mukosa usus sampai darah (Kuhnle et al 2000 dalam Setiawan 2006). Ditemukan bahwa quercetin, katekin dan genistein sebagian besar adalah dalam bentuk glukoronidase. Enzim-enzim yang mengkatalis reaksi konjugasi di dalam usus dan hati adalah UGT1A1 dan 1A8. Sebagian kecil flavonoid seperti katekin galloylasi dan isoflavon melewati konjugasi usus namun hanya dalam keadaan, dosis dan waktu tertentu (Meskin et al, 2004).
Pada reaksi glukoronidasi selama absorbsi, beberapa flavonoid mengalami metabolisme lebih lanjut. Pada tahap ini residu glukoronida dikeluarkan dan diganti dengan sulfat. Reaksi sulfitasi ini pada umumnya terjadi di liver. Hati menerima flavonoid dari darah termasuk darah dari usus halus pada awal metabolisme. Berdasarkan percobaan perfusi secara invitro dan invivo pada tikus, flavonoid dari usus halus terutama glukoronida yang mencapai liver secara keseluruhan terkonjugasi. Semua flavonoid yang telah terkonjugasi kemudian disalurkan ke dalam empedu dan kembali ke usus halus tanpa mengalami dekonjugasi lagi dan kemudian dikirim ke kolon serta diikuti deglukoronidasi atau sulfatasi oleh mikroba dalam ileum atau kolon dan terjadi reabsorbsi flavonoid dalam tikus enterohepatik (Meskin et al, 2004).
Darah menyalurkan flavonoid ke jaringan-jaringan tubuh. Apabila terdapat dalam plasma aglikon memasuki jaringan perifer dengan difusi pasif atau terfasilitasi. Konjugat glukoronida perlu disalurkan ke dalam jaringan perifer karena senyawa tersebut bersifat hidrofilik dan berdifusi melewati membran dengan lambat. Untuk dekonjugasi dalam jaringan, banyak sel memiliki aktivitas β-Glukoronidase dalam fraksi lisosom dan lumen dalam retikulum endoplasma. Dalam hati, enzim ini aktif terhadap quarcetin glukoronida. Tahap terakhir dari metabolisme senyawa flavonoid adalah ekresi yang merupakan ekresi di ginjal. Meskipun demikian kandungan flavonoid karena pembentukan deglikosilasi flavonoid juga terjadi di kolon oleh mikroba (Meskin et al, 2004).
Komponen darah
Menurut Koolman dan Rohm (1996), darah menyusun sekitar 8% dari masa tubuh manusia. Darah merupakan suatu jaringan bersifat cair yang terdiri atas sel-sel darah dan plasma sebagai mediumnya. Plasma darah bersifat homogen dan alkali lemah serta terdiri dari garam organik, protein, lemak, hormon, vitamin, enzim serta zat-zat nutrisi lainnya. Sel-sel darah mamalia terdiri dari sel darah merah atau eritrosit, keping darah atau trombosit, dan sel darah putih atau leukosit (Hartono 1989).
Darah mempunyai berbagai fungsi di dalam tubuh manusia. Darah merupakan alat transpor, mempertahankan lingkungan dalam tubuh agar terjaga konstan (homeostasis) dan berperan penting pada pertahanan tubuh terhadap benda-benda asing.
Eritrosit
Eritrosit adalah suatu sel yang berisi hemoglobin dan membawa oksigen dari paru-paru ke seluruh tubuh disebut juga sel darah merah (red blood cell/RBC). Di dalam tubuh manusia dalam keadaan diam sekitar 250 ml oksigen dikonsumsi dan 200 ml karbondioksida diproduksi setiap menit, selama latihan jumlah ini meningkat sepuluh kali lipat (Anonim 2006). Warna kemerah-merahan disebabkan oleh kandungan hemoglobin. Eritrosit berbentuk bikonkaf yang
meningkatkan area permukaan sel sehingga memudahkan difusi oksigen dan karbon dioksida. Bentuk ini dipertahankan oleh suatu sitoskeleton yang terdiri atas beberapa protein. Eritrosit sangat fleksibel dan dapat berubah bentuk saat mengalir di dalam kapiler. Eritrosit yang belum matang disebut retikulosit, secara normal terdapat 1-2% dari jumlah sel darah merah di dalam darah. Garis tengah eritrosit manusia adalah 6-8 µm, jauh lebih kecil dibanding hampir seluruh sel manusia. Eritrosit mengandung sekitar 270 juta molekul hemoglobin dengan masing-masing membawa empat kelompok heme (Anonim 2006). Dalam rangka mengikat oksigen, besi yang terdapat pada heme yang mengisi separuh jumlah hemoglobin harus dijaga dalam bentuk tereduksi disamping sebagai agen oksidasi endogen dan eksogen (Anonim 2006).
Plasma darah
Plasma adalah suatu larutan encer yang terdiri atas elektrolit, zat-zat makanan, metabolit, protein, vitamin, elemen pelacak dan hormon. Plasma mengandung banyak sekali ion, molekul anorganik, organik yang sedang diangkut ke berbagai bagian tubuh atau membantu transpor zat-zat lain. Volume plasma normal adalah sekitar 5 % berat badan atau secara kasar 3500 ml (berat badan 70 kg). Plasma akan menggumpal jika didiamkan dan hanya akan bertahan cair jika ditambah antikoagulan (Ganong 2000).
Protein membentuk bagian terbesar komponen yang tidak mudah menguap di dalam plasma darah. Konsentrasinya berkisar antara 60 dan 80 g/L. Dengan demikian sekitar 4 % dari seluruh protein tubuh adalah protein plasma. Di dalam plasma terdapat sekitar 100 protein yang berbeda (Koolman dan Rohm, 2001).