2 Tinjauan Pusaka
2.1 Polimer
Polimer adalah molekul besar yang terbentuk dari pengulangan unit yang kecil dan sederhana. Unit ulang dari polimer biasanya sama atau hampir sama dengan monomernya. Polimer yang terbentuk bisa lurus, membentuk cabang, dan membentuk ikatan silang.3 Panjang rantai suatu polimer ditentukan melalui jumlah unit ulang dalam rantai, biasanya dinyatakan dengan derajat polimerisasi (DP). Polimer yang memiliki nilai DP rendah biasa disebut sebagai oligomer. Polimer disebut juga sebagai makromolekul karena ukuran molekulnya yang besar, lebih besar dari molekul-molekul organik lain yang lebih sederhana.
Proses polimerisasi (sintesis polimer) oleh Flory (1953) dan Carothers (Mark 1940) dibagi menjadi dua kelompok besar, yaitu polimerisasi kondensasi (step-reaction polymerization) dan polimerisasi adisi (chain-reaction polymerization).3 Polimerisasi kondensasi merupakan polimerisasi bertahap, didasarkan pada reaksi antara dua pusat aktif sehingga terbentuk senyawa baru dan hasil samping. Bila molekul pereaksi memiliki dua gugus fungsi atau lebih, reaksi dapat berjalan lebih lanjut membentuk rantai polimer yang panjang.4
Polimerisasi adisi didasarkan pada pemutusan ikatan rangkap pada substrat. Pada polimerisasi adisi biasanya terjadi reaksi rantai dimana radikal bebas atau ion terlibat di dalamnya.5 Radikal bebas dapat terbentuk dari dekomposisi senyawa yang kurang stabil, atau biasa disebut sebagai inisiator. Polimerisasi ionik, polimerisasi radikal, dan polimerisasi Ziegler-Natta termasuk kedalam polimerisasi adisi.
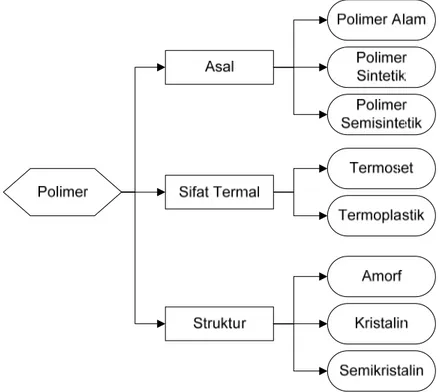
Berdasarkan asalnya, polimer dibagi menjadi tiga macam yaitu polimer alam, polimer sintetik, dan polimer semisintetik (Gambar 2.1). Polimer alam merupakan polimer yang terbentuk di alam seperti protein dan polisakarida. Polimer alam biasanya dapat terdegradasi dengan mudah (biodegradable polymer). Polimer sintetik merupakan polimer buatan, hasil sintesis manusia. Polimer sintetik ini dibagi menjadi tiga golongan, yaitu serat, plastik, dan elastomer. Polimer
4 semisintetik adalah polimer hasil sintesis manusia, tetapi bahan dasarnya berasal dari polimer alam. Contoh polimer semisintetik adalah selulosa asetat yang berasal dari selulosa.4
Gambar 2. 1 Klasifikasi polimer
Berdasarkan sifat termalnya, polimer dibagi menjadi polimer termoplastik dan polimer termoset. Polimer termoplastik merupakan polimer yang dapat meleleh saat dipanaskan, sehingga lebih mudah dibentuk. Polimer jenis ini dapat didaur ulang, tetapi suhu pemakaian maksimumnya lebih rendah dari suhu lelehnya. Sedangkan polimer termoset merupakan polimer yang tidak meleleh saat dipanaskan, karena terbentuknya ikatan silang pada saat pemanasan pertama. Polimer jenis ini sulit mengalami daur ulang, tetapi suhu pemakaian maksimumnya bisa lebih tinggi dari suhu pembuatan polimer tersebut.4
Berdasarkan strukturnya, polimer dibagai menjadi tiga macam, yaitu polimer kristalin, polimer amorf, dan polimer semikristalin. Polimer kristalin adalah polimer yang susunan rantainya teratur, disebabkan oleh adanya ikatan antar rantai yang kuat. Polimer amorf adalah polimer yang susunan rantainya acak karena tidak adanya antaraksi antar rantai yang kuat. Sedangkan polimer semikristalin adalah polimer yang memiliki bagian kristalin dan amorf (Gambar 2.2). Biasanya polimer memiliki struktur semikristalin, dan derajat kristalinitasnya dapat ditentukan dengan menggunakan analisis difraksi sinar-X.4
5
Gambar 2. 2 Struktur polimer
2.2 Polistiren
Stiren berhasil diekstrak pertama kali pada tahun 1831 oleh M. Bonastre. Kemudian pada tahun 1845, AW Hofmann dan J Blyth berhasil mendapatkan padatan (metastiren) dari stiren dengan cara memanaskan stiren tanpa kehadiran oksigen. Kemudian beberapa penilitian pada awal 1900 dilakukan untuk membuat polimer dari stiren, tapi belum membuahkan hasil.6 Beberapa tahun kemudian, seorang ahli kimia Jerman, Hermann Staudinger, menemukan bahwa pemanasan stiren mengawali reaksi rantai yang menghasilkan makromolekul (polimer). Senyawa ini kemudian diberi nama polistiren. Polistiren dikembangkan secara komersial pertama kali pada tahun 1930 oleh suatu perusahaan dari Jerman yang bernama I.G. Farben yang dipelopori oleh Professor Katz.6
2.2.1 Sintesis Polistiren
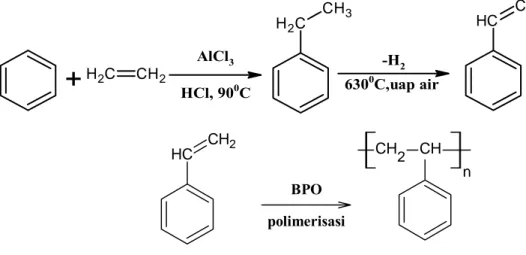
Polistiren berasal dari monomer stiren (vinilbenzene). Stiren dapat disintesis dari benzene dan etilen dengan bantuan katalis aluminium klorida, pada suhu 900C. Dari proses ini akan dihasilkan etil benzene yang kemudian didehidrogenasi sehingga terbentuk stiren (Gambar 2.3).3
6 HC CH2 H2C CH3 -H2 6300C,uap air C H2 CH2
+
AlCl3 HCl, 900C HC CH2 BPO polimerisasi n CH 2 CHGambar 2. 3 Reaksi polimerisasi polistiren
Proses polimerisasi stiren dapat dilakukan melalui polimerisasi adisi dengan radikal bebas, kationik, anionik, maupun Ziegler-Natta. Metode sintesis yang paling sering digunakan adalah polimerisasi adisi secara radikal bebas dengan menggunakan benzoil peroksida (BPO) sebagai inisiator. Reaksi polimerisasi ini terdiri dari tiga tahap, yaitu tahap inisiasi, tahap propagasi, dan tahap terminasi (Gambar 2.4).4
Tahap Inisiasi : O O O O Panas O O O Benzoil Peroksida + O + H H H O O R CH H2C R Tahap Propagasi : dst + H H H H2C CH R R H2C CH CH2 CH
7 Tahap Terminasi :
R-R
R
O O atau atauR + R
CH CH2 R nGambar 2. 4 Mekanisme reaksi polimerisasi polistiren
2.2.2 Struktur dan Sifat Polistiren
Berdasarkan stereokimianya, polistiren dapat dibagi menjadi tiga macam5, yaitu :
a. Polistiren isotaktik adalah polistiren yang semua gugus fenilnya berada pada satu arah yang sama terhadap bidang rantai utama. Karena keteraturan yang tinggi, biasanya polimer jenis ini bersifat kristalin.
b. Polistiren sindiotaktik adalah polistiren yang gugus fenilnya berada pada arah yang bergantian terhadap bidang rantai utama.
c. Polistiren ataktik adalah polistiren yang gugus fenilnya tidak mempunyai keteraturan (acak) terhadap bidang rantai utama. Strukturnya bersifat amorf dan biasanya tidak memiliki titik leleh (Tm).
8 Polistiren merupakan suatu polimer termoplastik yang bersifat transparan, mudah diwarnai, mudah difabrikasi, dan mudah disintesis. Polistiren dapat dilunakkan pada suhu sekitar 100°C. Seperti polimer lainnya, polistiren cenderung bersifat inert, memiliki ketahanan terhadap alkali, asam halida, dan senyawa oksidator/reduktor lainnya. Penyinaran dalam waktu lama oleh sinar UV, oksigen, atau ozon mempengaruhi kekuatan dan ketahanan dari polimer tersebut.7
2.2.3 Aplikasi Polistiren
Polistiren yang dijual secara komersial biasanya merupakan polimer linier, bersifat ataktik dan amorf. Polistiren seperti ini banyak digunakan untuk bahan pengemas, mainan, dan peralatan rumah tangga. Polistiren isotaktik atau sindiotaktik dapat juga diproduksi, akan tetapi kurang diminati karena sifatnya lebih kristalin, mahal, dan lebih susah untuk diproses. Polistiren tipe isotaktik atau sindiotaktik banyak digunakan untuk peralatan medis karena lebih tahan terhadap panas (dapat disterilisasi).
Polistiren yang paling luas dikenal adalah styrofoam. Selain polistiren, pada styrofoam terdapat zat-zat aditif yang ditambahkan. Seng dan senyawa butadiena ditambahkan agar polistiren kehilangan sifat jernihnya dan berubah warna menjadi putih susu. Untuk kelenturannya, ditambahkan dioktilptalat (DOP), butil hidroksi toluena, atau n-butil stearat. Plastik busa yang mudah terurai menjadi struktur sel-sel kecil merupakan hasil proses peniupan dengan menggunakan gas chlorofluorocarbon (CFC). Hasilnya adalah styrofoam seperti yang kita pergunakan saat ini.8
2.3 Poli-δ-Valerolakton (PVL)
PVL merupakan senyawa lakton yang termasuk ke dalam golongan poliester. PVL dapat disintesis dari monomer δ-valerolakton, suatu senyawa ester siklik yang dapat diperoleh dari hasil kondensasi alkohol dengan asam karboksilat.
O O distanoksan polimerisasi O O n Gambar 2. 6 Polimerisasi PVL
9 PVL dapat disintesis dengan cara polimerisasi pembukaan cincin dari monomer δ-valerolakton dengan menggunakan katalis distanoksan (Gambar 2.6). Senyawa δ-valerolakton dapat terpolimerisasi secara spontan dalam temperatur kamar, walaupun dengan massa molekul yang rendah. Polimer yang dihasilkan tersebut ternyata larut dalam pelarut organik dan bersifat asam.9 Madeleine Aubin melakukan penelitian tentang blending antara PVL dengan PVC, dan diketahui bahwa blending antar kedua polimer tersebut bersifat miscible. Interaksi terjadi antara gugus karbonil pada PVL dengan hidrogen alfa pada PVC. Terjadinya poliblend yang homogen dan miscible dapat dilihat dari hasil analisis DSC yang menunjukkan adanya satu temperatur transisi gelas, yaitu pada suhu 260K. Selain itu, karena tidak ditemukan adanya transisi pelelehan, maka blending tersebut dipastikan bersifat amorf.10
Penelitian Madeleine Aubin juga menyebutkan bahwa temperatur transisi gelas PVL adalah 206K dan titik lelehnya adalah 332K. Jika dibandingkan dengan polikaprolakton (PCL), kedua polimer tersebut memiliki nilai titik leleh dan temperatur transisi gelas yang hampir sama. Ditemukan juga bahwa perbedaan jumlah gugus metilen pada PVL dan PCL (4 dan 5) ternyata tidak terlalu berpengaruh terhadap sifat-sifat intrinsik dari keduanya. PVL diperkirakan memiliki sifat-sifat intrinsik yang sama dengan PCL.10
2.4 Distanoksan
Senyawa golongan distanoksan memiliki beberapa karakteristik, yaitu dapat membentuk dimer baik dalam keadaan padat maupun larutannya (Gambar 2.7). Dimerisasi distanoksan terjadi akibat adanya ikatan Sn-O-Sn dan faktor penting lain yaitu terikatnya satu unsur yang sangat elektronegatif , misalnya oksigen atau unsur-unsur halogen pada tiap atom Sn.1
OH Sn O Sn O Sn OH Sn Cl Cl C4H9 C4H9 C4H9 C4H9 C4H9 C4H9 C4H9 C4H9
10 Sebagian besar senyawa-senyawa distanoksan tidak larut dalam air, namun mempunyai kelarutan yang tinggi dalam pelarut organik termasuk hidrokarbon alifatik. Hanya sedikit penelitian yang meneliti tentang kereaktifan dan aplikasi sintesis distanoksan. Distanoksan dapat mengkatalisis sintesis uretan dari isosianat dan alkohol dengan kereaktifan lebih tinggi dari katalis Sn umum lainnya.1
Distanoksan juga dapat digunakan sebagai katalis dalam reaksi polimerisasi pembukaan cincin senyawa lakton menghasilkan suatu poliester dengan massa molekul relatif besar. Pembukaan cincin yang terjadi bisa melalui pemutusan ikatan antara karbon karbonil dengan oksigen dari lakton, atau pemutusan ikatan antara karbon non-karbonil dengan oksigen dari lakton.
2.5 Benzoil Peroksida (BPO)
Benzoil peroksida (BPO) merupakan senyawa kimia yang tergolong ke dalam peroksida organik. BPO terdiri dari dua gugus benzoil yang dihubungkan oleh gugus peroksida (Gambar 2.8). BPO biasa digunakan sebagai inisiator radikal. Pemecahan homolitik ikatan lemah oksigen dengan oksigen akan menyebabkan terbentuknya radikal bebas yang akan memicu terjadinya reaksi lanjutan.
Gambar 2. 8 Struktur benzoil peroksida
Pada tahun 1920, Jack Breitbart dari Laboratorium Revlon, mulai mengembangkan BPO untuk mengatasi masalah jerawat.Selain itu, BPO juga digunakan untuk pemutih gigi, disinfektan, pengering, dan agen pembersih.11
BPO dapat disintesis dengan mereaksikan natrium peroksida dengan benzoilklorida, sehingga dihasilkan benzoil peroksida dan natrium klorida.Waktu paruh dari BPO adalah satu jam pada suhu 920C, sedangkan pada suhu 1310C waktu paruhnya adalah satu menit. Berat jenis dari BPO adalah 1,334 g/cm3. Reaksi sintesis BPO adalah sebagai berikut11 :
11
2.6 Kopolimer
Polimerisasi yang menggunakan lebih dari satu jenis monomer disebut dengan kopolimerisasi, dan hasilnya disebut kopolimer. Kopolimerisasi biasanya dilakukan dengan tujuan untuk mendapatkan hasil polimer yang lebih baik. Terdapat empat jenis kopolimer4, yaitu:
a. Kopolimer blok : rantai polimer A berikatan dengan rantai polimer B.
b. Kopolimer bergantian : unit ulang A dan B tersusun secara bergantian dan teratur.
c. Kopolimer acak : unit ulang A dan B terikat secara acak.
d. Kopolimer graft (cangkok) : polimer A menyusun rantai utama, sedangkan polimer B menyusun rantai cabang.
Untuk memperoleh suatu kopolimer blok, biasanya digunakan polimer dengan gugus ujung yang labil, sehingga bisa terpolimerisasi lebih lanjut. Gugus ujung dapat diaktivasi dengan menggunakan panas atau sinar ultraviolet, sehingga terbetuknya radikal. Polimer radikal juga dapat diperoleh melalui mastikasi.
Jika, terdapat dua jenis monomer M1dan M2 yang merupakan sumber radikal M1. dan M2., maka terdapat empat cara penambahan monomer dalam suatu rantai polimer5, yaitu:
• ⎯ → ⎯ + • • ⎯ → ⎯ + • • ⎯ → ⎯ + • • ⎯ → ⎯ + • 2 2 2 1 1 2 2 2 1 1 1 1 22 21 12 11 M M M M M M M M M M M M k k k k (2-1)
Jika konsentrasi-konsentrasi M1• dan M2 • dianggap tetap (keadaan tunak), maka laju adisi
•
1
M ke M2 akan sama dengan laju adisi M2• ke M1, artinya :
[
1][ ]
2 21[
2][ ]
112
M
M
k
M
M
12 Laju pengurangan M1 dan M2 dapat dinyatakan dengan persamaan berikut:
[ ]
[
][ ]
[
][ ]
1 2 21 1 1 11 1 k M M k M M dt M d • + • = − (2-3)[ ]
[
][ ]
[
][ ]
2 2 22 2 1 12 2 k M M k M M dt M d • + • = −Jika didefinisikan bahwa 1 12 11 r kk = dan 21 2 22 r k k = ,
maka kombinasi kedua persamaan laju pengurangan monomer di atas adalah:
[ ]
[ ]
=[ ]
[ ]
⎜⎜⎝⎛[ ] [ ]
[ ] [ ]
++ ⎟⎟⎠⎞ 2 2 1 2 1 1 2 1 2 1 M r M M M r M M M d M d (2-4)Jika r > 1 maka radikal monomer lebih memilih untuk bereaksi dengan monomer sejenis (propagasi). Tetapi jika r < 1, maka kopolimerisasi lebih disukai.5
Jika nilai r1r2 = 1, maka kopolimerisasi dikatakan ideal, artinya kedua jenis radikal memiliki kecenderungan yang sama untuk bereaksi dengan kedua jenis monomer. Jenis kopolimerisasi ini biasanya menghasilkan kopolimer acak. Kopolimerisasi bergantian terjadi jika r1 = r2 = 0 dan d[M1]/ d[M2] = 1. Pada keadaan ini, radikal monomer tidak bereaksi dengan monomer yang
sejenis dengannya. Sedangkan jika r = ∼, maka kopolimer tidak terbentuk (hanya terbentuk homopolimer.4
2.7 Karakterisasi Polimer
Karakterisasi polimer dilakukan untuk mengetahui sifat-sifat dari polimer yang dihasilkan. Dengan melakukan karakterisasi, dapat diketahui sifat fisik maupun kimia dari polimer. Karakterisasi yang dilakukan pada percobaan ini adalah analisis gugus fungsi, analisis kristalinitas, analisis termal, dan analisis kekuatan mekanik.
2.7.1 Analisis Gugus Fungsi
Hampir setiap senyawa yang memiliki ikatan kovalen, apakah senyawa organik atau senyawa anorganik, akan menyerap berbagai frekuensi radiasi elektromagnetik dalam daerah spektrum infra merah. Akan tetapi, ikatan yang dapat menyerap radiasi infra merah hanyalah ikatan yang
13 memiliki momen dipole. Ketika suatu molekul menyerap radiasi infra merah, maka energi yang diserap akan menaikkan amplitudo gerakan vibrasi ikatan dalam molekul dan molekul akan tereksitasi ke tingkat energi yang lebih tinggi. Panjang gelombang dari absorpsi suatu tipe ikatan tertentu bergantung pada macam vibrasi dari ikatan tersebut. Oleh karena itu, masing-masing tipe ikatan akan memiliki nilai yang khas.12
Vibrasi molekul terdiri dari dua macam, yaitu vibrasi ulur/rentangan (stretching) dan vibrasi tekuk/bengkokan (bending). Vibrasi ulur terbagi lagi menjadi dua macam, yaitu vibrasi ulur simetris dan vibrasi ulur asimetris. Sedangkan vibrasi tekuk terbagi menjadi empat, yaitu vibrasi goyang (rocking), vibrasi gunting (scissoring), vibrasi kibasan (wagging), dan vibrasi pelintiran (twisting).12
Analisis gugus fungsi dilakukan dengan menggunakan alat Fourier Transform Infra Red (FTIR). Terdapat tiga kompenen utama dalam spektrofotometer12, yaitu:
a. Sumber radiasi infra merah, yang memancarkan sinar dan mengenai sampel yang dianalisis. b. Monokromator
c. Detektor yang mengubah energi frekuensi serapan menjadi energi listrik yang kemudian dapat terbaca.
Sampel yang digunakan bisa dalam fasa padat, cair, atau gas. Ketiganya memiliki penanganan yang berbeda. Untuk sampel padat, bisa dengan metode Nujol Mull, pellet KBr, atau pembuatan film. Sampel cair dapat disiapkan dengan memasukkannya ke dalam sel khusus atau dengan menggunakan window NaCl seperti Nujol Mull. Sedangkan sampel gas disiapkan dengan memasukkannya ke dalam sel khusus untuk sampel gas12.
2.7.2 Analisis Kristalinitas
Difraksi dapat terjadi ketika radiasi elektromagnetik berinteraksi dengan struktur yang periodik yang jarak pengulangannya sama dengan panjang gelombang radiasi tersebut. Sinar-X memiliki panjang gelombang, dalam orde angstrom, yang kira-kira sama dengan jarak antar atom pada padatan kristalin. Oleh karena itu, sinar-X dapat terdifraksi dalam material kristalin.13
Pada tahun 1912, Maxwell von Laue mengungkapkan bahwa sinar-X dapat dihamburkan oleh atom pada padatan kristalin jika adanya suatu kemiripan dalam jaraknya. Jadi, jika besarnya
14 panjang gelombang dan jarak antar atom kira-kira sama, maka difraksi dapat terjadi. Pola difraksi yang terjadi menggambarkan susunan struktural dari atom yang bersangkutan.
Difraksi sinar-X dalam material padatan dapat dimanfaatkan untuk mengetahui derajat kristalinitas dari suatu polimer. Penentuan derajat kristalinitas polimer dilakukan dengan membandingkan luas kurva fasa kristalin terhadap luas keseluruhan. Fasa kristalin pada difraktogram dinyatakan sebagai luas puncak yang relatif tajam dengan intensitas yang kuat, sedangkan fasa amorf dinyatakan dengan daerah di bawah puncak yang landai dan memiliki intensitas puncak yang kecil. Persamaan yang digunakan untuk menentukan derajat kristalinitas adalah sebagai berikut :
%
100
%
×
+
=
amorf kristalin kristalinI
I
I
x
(2-5)
dengan
%X = derajat kristalinitas
I
kristalin= intensitas fasa kristalin
I
amorf= intensitas fasa amorf
2.7.3 Analisis Termal
Analisis termal dapat dilakukan dengan menggunakan alat thermogravimetric analysis (TGA) dan Differential Thermal Analysis (DTA). Melalui analisis termal, beberapa sifat termal polimer dapat diketahui, diantaranya adalah titik kristalisasi, suhu transisi gelas (Tg), suhu pelelehan (Tm), perubahan kalor (ΔH), suhu dekomposisi dan stabilitas panas.
TGA merupakan suatu teknik analisis yang digunakan untuk menentukan stabilitas termal dari suatu material dengan memperhatikan perubahan berat yang terjadi pada analit yang dipanaskan14. Pengukuran biasanya dilakukan dalam udara terbuka atau dalam gas inert seperti helium atau argon, dan perubahan berat sampel biasanya dicatat sebagai fungsi kenaikan temperatur. Beberapa instrument untuk analisis sifat termal juga mengukur perbedaan suhu antara sampel dengan pembanding setiap suhu tertentu, atau yang biasa disebut DTA14.
Dari kurva TGA, kita dapat melihat temperatur degradasi dari suatu polimer. Dari kurva DTA, kita dapat mengamati berbagai gejala fisik dan kimia yang terjadi pada polimer seperti transisi gelas, pelelehan, degradasi, oksidasi, dan lain-lain. Pengukuran DTA dan TGA secara simultan memungkinkan kita mengamati berbagai gejala endotermik dan eksotermik dari suatu polimer.
15
Gambar 2. 9 Termogram TGA secara umum
2.7.4 Analisis Kekuatan Mekanik
Tujuan dilakukannya analisis sifat mekanik suatu polimer adalah untuk mengetahui seberapa kuat kekuatan mekanik dari suatu polimer. Parameter yang menunjukkan kekuatan mekanik ini berupa kekuatan tarik (tensile strength), regangan (elongation at break), dan Modulus Young. Kekuatan tarik (σ) merupakan besarnya gaya tarik maksimum yang diperlukan saat suatu bahan putus. Kekuatan tarik dapat diperoleh melalui persamaan :
F
A
σ
=
(2-6)
dimana σ = kekuatan tarik (MPa), F = beban pada saat putus (Kgf), A = luas penampang (mm2).
Regangan (ε) menggambarkan perbandingan perpanjangan yang terjadi sebelum polimer tersebut putus terhadap panjang awal. Dapat dinyatakan dalam persamaan :
16 0 0
(
)
ε =
l l
100%
l
−
×
(2-7) dimana ε = % regangan l = panjang akhir (cm) l 0 = panjang awal (cm)Modulus Young (E) merupakan perbandingan antara kekuatan tarik terhadap regangan dan menggambarkan ukuran kekakuan dari suatu material. Persamaan untuk Modulus Young adalah sebagai berikut :
E
σ
ε
=
(2-8)
dimana E = Modulus Young (MPa), ε = % regangan,