BAB 2
TINJAUAN PUSTAKA
2.1. Lemak dan Minyak
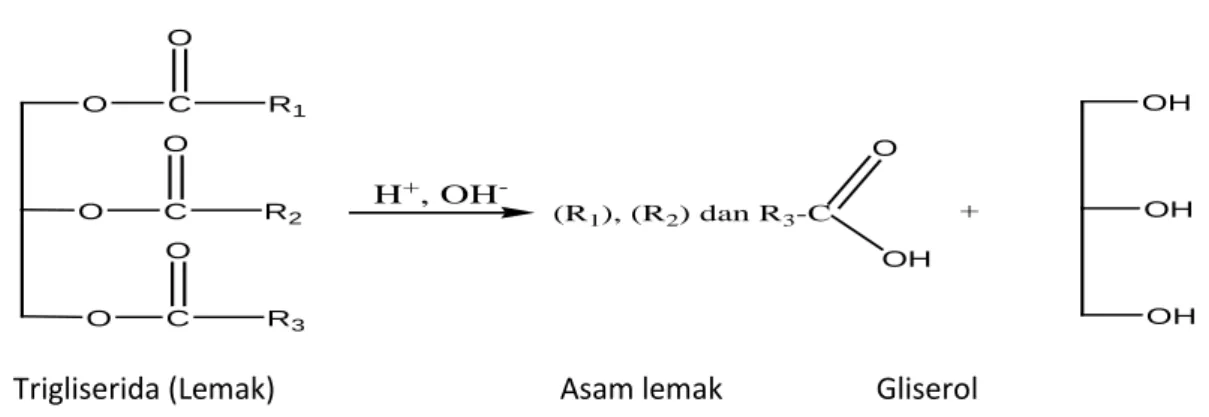
Lemak dan minyak merupakan salah satu kelompok yang termasuk golongan lipida. Satu sifat yang khas dan mencirikan golongan lipida (termasuk lemak dan minyak) adalah daya larutnya dalam pelarut organik (misalnya eter, benzen, chloroform) atau sebaliknya ketidak larutannya dalam pelarut air. Lemak dan minyak secara kimiawi adalah trigliserida yang merupakan bagian terbesar dari kelompok lipida. Trigliserida ini merupakan senyawa hasil kondensasi satu molekul gliserol dengan tiga molekul asam lemak (Sudarmadji dan Haryono, 1989). O O C C O O R1 R2 H+, OH -(R1), (R2) dan R3-C + OH OH OH O C O R3 O OH
Trigliserida (Lemak) Asam lemak Gliserol
Gambar 2.1. Hasil Hidrolisis Trigliserida menjadi Asam Lemak dengan Gliserol (Bahl, 2004).
Lemak dan minyak tidak larut dalam air dan sedikit larut dalam alkohol, terutama minyak dengan berat molekul rendah, kecuali minyak jarak (castor oil). Minyak dan lemak dapat larut sempurna dalam eter, hidrokarbon, benzena, karbon disulfida dan
pelarut-pelarut organik lainnya. Kelarutan minyak atau lemak dalam suatu pelarut-pelarut ditentukan oleh sifat polaritas asam lemaknya. Asam lemak yang bersifat polar cenderung larut dalam pelarut polar, sedangkan asam lemak non polar larut dalam pelarut non polar. Sebagai contoh ialah asam lemak berantai pendek (misalnya asam butirat) pada lemak susu bersifat polar cenderung larut dalam air sedangkan asam lemak berantai karbon panjang tidak larut dalam air. Sifat dan daya kelarutan ini digunakan sebagai dasar praktek pada pengujian-pengujian analitis dan ekstraksi minyak dengan pelarut. Sifat minyak dan lemak yang larut dalam pelarut tertentu dipergunakan dalam pengolahan minyak secara komersil. Daya kelarutan asam asam lemak biasanya lebih tinggi dari komponen gliseridanya dan dapat larut dalam pelarut organik yang bersifat polar dan non polar. Semakin panjang rantai karbon maka minyak dan lemak tersebut semakin sukar larut (Ketaren, 2008).
2.2 Oleokimia
Oleokimia pada dasarnya merupakan cabang ilmu kimia yang mempelajari trigliserida menjadi asam lemak dan gliserin serta turunan asam lemak baik dalam bentuk ester, amida, sulfat, sulfonat, alkohol, alkoksi, maupun sabun. Asam lemak bersama-sama dengan gliserol merupakan penyusun utama minyak nabati atau lemak dan merupakan bahan baku untuk semua lipida pada makhluk hidup. Asam lemak ini mudah dijumpai dalam minyak masak (minyak goreng), margarin atau lemak hewan dan dapat menentukan nilai gizinya. Secara alami, asam lemak bisa berbentuk bebas (karena lemak yang terhidrolisis) maupun yang terikat dari gliserida. Asam lemak merupakan salah satu dasar oleokimia (Tambun, 2006).
Oleokimia merupakan turunan gliserol dengan asam lemak yang berubah dalam bentuk turunannya yang digunakan baik sebagai surfaktan, detergen, polimer, aditif bahan bakar dan sebagainya. Bahan dasar oleokimia seperti gliserol, asam lemak, amina asam lemak dan alkohol dapat diperoleh dengan mengubah lipida baik yang berasal dari hewan maupun tumbuhan menjadi gliserol dan turunan asam lemak. Penggunaan terbesar dari asam lemak adalah dengan mengubahnya menjadi alkohol asam lemak, plastik dan nilon
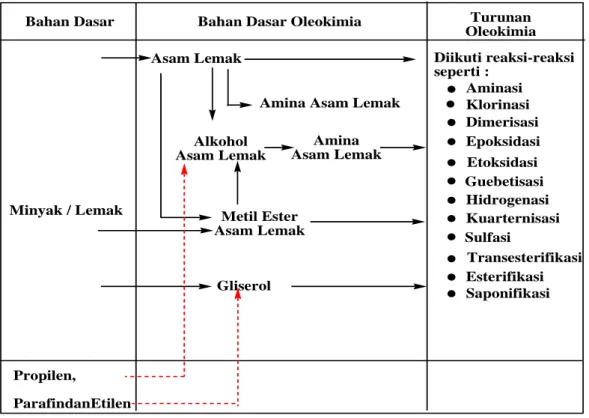
(hampir mencapai 40% dari total penggunaannya). Penggunaan terbesar berikutnya sebesar 30% untuk dijadikan sabun, detergen, kosmetik. Asam lemak juga digunakan sebagai bahan dasar pembuatan resin dan cat sekitar 15% sisanya digunakan dalam industri pembuatan ban, tekstil, kulit kertas, pelumas dan lilin (Richtler and Knaut, 1984). Diagram alur oleokimia dapat digambarkan pada tabel 2.1. dibawah ini!
Tabel 2.1. Diagram Alur Proses Oleokimia dari Bahan Dasar Minyak atau Lemak menjadi Oleokimia dan Turunan Oleokimia
Bahan Dasar Bahan Dasar Oleokimia Turunan Oleokimia
Minyak / Lemak
Asam Lemak Diikuti reaksi-reaksi seperti : Aminasi Klorinasi Dimerisasi Epoksidasi Etoksidasi Guebetisasi Hidrogenasi Kuarternisasi Sulfasi Transesterifikasi Esterifikasi Saponifikasi Amina Asam Lemak
Alkohol Asam Lemak Amina Asam Lemak Metil Ester Asam Lemak Propilen, ParafindanEtilen
Sumber : Richtler and Knaut, 1984 : Alami
: Sintesis
Gliserol
2.3.Asam Lemak dan Turunannya
Asam lemak merupakan asam karboksilat alifatis berantai panjang. Asam yang mempunyai berat molekul yang paling besar didalam molekul gliserida juga merupakan bagian yang
reaktif. Hingga dapat dimengerti bahwa asam lemak mempunyai pengaruh besar terhadap lemak dan minyak. Asam lemak yang menyusun lemak ini dapat dibedakan antara asam lemak jenuh dan tak jenuh. Asam lemak disebut jenuh bila semua atom C dalam rantainya diikat tidak kurang daripada dua atom H, hingga dengan demikian tidak ada ikatan rangkap. Asam-asam lemak jenuh yang telah dapat diidentifikasi sebagai bagian dari lemak mempunyai atom C4 hingga C26. Adapun struktur umum rantai karbon dari asam lemak jenuh adalah sebagai berikut:
R C H H C C H H H H C O OH
Asam-asam lemak yang didalamnya rantai karbonnya mengandung ikatan rangkap. Derajat ketidakjenuhan dari minyak tergantung pada jumlah rata-rata dari ikatan rangkap didalam asam lemak.Pada asam lemak tak jenuh, masih dibedakan antara asam lemak yang mempunyai bentuk “non-conjugated” yaitu ikatan rangkap dalam rantai C selalu dipisahkan oleh dua ikatan tunggal. Bentuk yang lain adalah asam yang “conjugated”, dimana antara atom-atom C tertentu terdapat ikatan tunggal dan ikatan rangkap berganti-ganti.
C
H H R C C C H H O OHRantai karbon dari asam lemak tak jenuh
R C C H H C H H C C C H H H C H C H H C C H C H H C H C C H O OH C R H O OH
Rantai asam lemak yang “non-conjugated” Rantai asam lemak yang (tak terkonjugasi) “conjugated” (terkonjugasi)
Hampir semua asam lemak yang terdapat dalam alam mempunyai jumlah atom karbon yang genap karena asam ini dibiosintesis dari gugus asetil berkarbon dua dalam asetil koenzim A.
dua atom karbon
CH
3C
O SCoA8
asetil koenzim A
banyak tahap
CH
3(CH
2)
14CO
2H
asam palmitat
jumlah atom karbon genap
(Fessenden dan Fessenden, 1986).
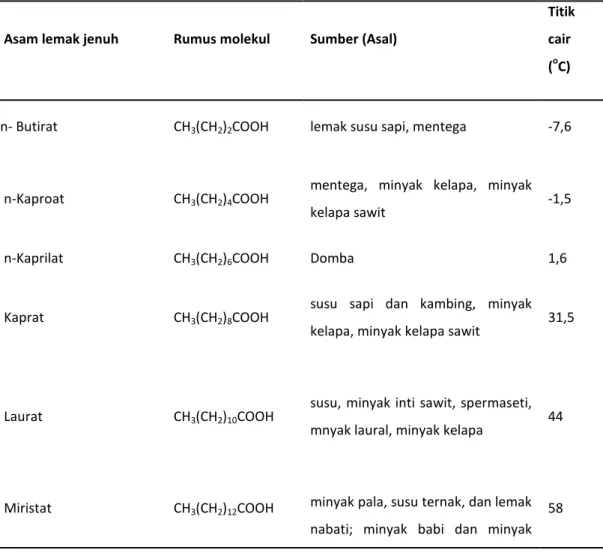
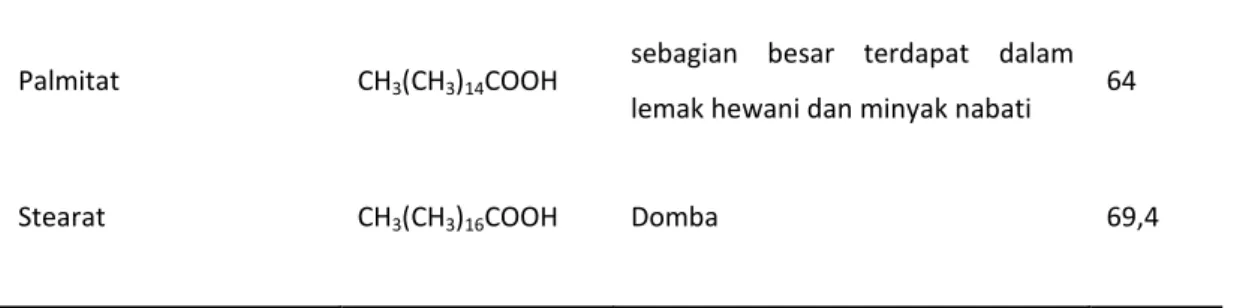
Asam lemak jenuh dan tidak jenuh yang penting, terdapat dalam minyak dan lemak dapat dilihat dalam tabel 2.2 dan 2.3 berikut:
Tabel 2.2. Asam Lemak Jenuh yang Terdapat dalam Lemak dan Minyak
Asam lemak jenuh Rumus molekul Sumber (Asal)
Titik cair (oC)
n- Butirat CH3(CH2)2COOH lemak susu sapi, mentega -7,6
n-Kaproat CH3(CH2)4COOH
mentega, minyak kelapa, minyak
kelapa sawit -1,5
n-Kaprilat CH3(CH2)6COOH Domba 1,6
Kaprat CH3(CH2)8COOH
susu sapi dan kambing, minyak kelapa, minyak kelapa sawit 31,5
Laurat CH3(CH2)10COOH
susu, minyak inti sawit, spermaseti, mnyak laural, minyak kelapa 44
Miristat CH3(CH2)12COOH minyak pala, susu ternak, dan lemak nabati; minyak babi dan minyak
ikan hiu Palmitat CH3(CH3)14COOH
sebagian besar terdapat dalam lemak hewani dan minyak nabati 64
Stearat CH3(CH3)16COOH Domba 69,4
Tabel 2.3. Asam Lemak Tidak Jenuh yang Terdapat dalam Lemak dan Minyak
Asam lemak tak jenuh
Rumus molekul Sumber
(asal) Titik cair (oC) Palmitoleat CH3(CH2)5=CH(CH2)7COOH minyak kacang dan jagung 33 Oleat (Omega 9) CH3(CH2)7CH=CH(CH2)7COOH disebagian besar minyak dan lemak 14 Linoleat (Omega 6) CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH Minyak biji kapas, biji lin, biji poppy -11 Linolenat (Omega 3) CH3CH2CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH Minyak perilla, biji lin -
(Ketaren, 2008).
2.3.1 Asam Laurat
Asam laurat atau disebut juga dengan asam dodekanoat merupakan asam lemak jenuh yang tersusun dari 12 atom karbon. Asam laurat mengandung hidrokarbon non Polar pada bagian ekornya dan gugus karboksilat yang Polar pada bagian kepala sehingga dapat berinteraksi dengan air. Asam laurat merupakan satu diantara tiga asam lemak jenuh yang paling banyak dijumpai daripada asam miristat,asam palmitat dan asam stearat. Asam laurat paling banyak dijumpai pada cinnamon (80-90%),minyak kelapa (40-60%) dan minyak inti sawit(40-50%). Asam laurat banyak digunakan pada pembuatan sabun,sampo,kosmetik dan bahan aktif permukaan lainnya.
Adapun struktur dari asam laurat adalah sebagai berikut.
C
11H
23C
OOH
Gambar 2.2. Struktur Asam Laurat Sifat-sifat asam laurat adalah sebagai berikut:
-rumus molekul : C12H24O2 -Berat molekul : 200,31 gr/mol
-Densitas : 0,869 gr/cm3 - Titik didih : 225 oC -Titik lebur : 44oC - kristal serbuk berwarna putih
- tidak larut dalam air,1 gram larut dalam 1ml alkohol, 2,5 ml dalam propil alkohol dan larut sempurna dalam benzena dan eter (Anonimous,1976).
2.4. Ester
Ester adalah turunan asam karboksilat yang gugus OH dari karboksilnya diganti gugus
OR dari alkohol. Ester mengandung gugus karbonil dan satu ikatan eter dengan karbon
karbonil (Wilbraham dan Matta, 1992).
Rumus Umum
R C
O
O R
Gambar 2.3. Rumus Umum Ester
Ester dapat diperoleh dari asam organik yang di reaksikan dengan alkohol.
Pembentukan air pada reaksi esterifikasi, selalu OH nya berasal dari asam, sebab
reaksi senyawa organik bersifat molekular, meskipun asam karboksilat terionisasi
sedikit, tetapi alkohol tidak terionisasi.
Ester dari asam organik memiliki sifat:
•
Berupa larutan bila massa rumusnya tidak terlalu besar
•
Larutan yang netral, tidak berwarna, lebih mengkilat dibandingkan air dan
berbau harum
•
Senyawa yang massa rumusnya rendah dapat larut dalam air tapi sangat
sedikit, lebih banyak larut dalam alkohol dan eter
•
Titik didih relatif rendah, dibandingkan titik didih asam atau alkohol yang
menyusunnya (Besari dkk, 1982).
Reaksi esterifikasi adalah suatu reaksi antara asam karboksilat dan alkohol membentuk
ester. Turunan asam karboksilat membentuk ester asam karboksilat. Ester asam
karboksilat ialah suatu senyawa yang mengandung gugus –CO
2R dengan R dapat
berupa alkil maupun aril. Esterifikasi dikatalisis asam dan bersifat dapat balik
(Fessenden dan Fessenden ,1986).
Menurut Besari dkk (1982), reaksi esterifikasi dapat dilakukan dengan reaksi-reaksi
berikut ini:
1. Asam karboksilat ditambah dengan alkohol
H3C C
O
OH + C2H5OH H3C C
O
OC2H5 + H2O
Asam asetat etanol etil asetat air
2. Alkil halida ditambah garam dari suatu asam karboksilat
CH3I + AgOC CH3
O
H3C C
O
OCH3 + AgI
Metil Iodida garam argentum metil asetat argentum iodida
3. Anhidrida asam ditambah dengan alkohol
CH3 C O O C O CH3 + C2H5OH CH3 C O OH + CH3 C O OC2H5
Anhidrida asetat etanol asam asetat etil asetat
4. Asil halida ditambah dengan alkohol
H3C C
O
Cl + C2H5OH H3C C
O
OC2H5 + HCl
5. Alkohol ditambah dengan amida
C2H5OH + H3C C O NH2 NH3 + H3C C O OC2H5Etanol amida amoniak etil asetat
Salah satu contoh dari reaksi pembuatan ester adalah reaksi esterifikasi antara
hidroxylethyl albizia benth oil
dengan anhidrida maleat dengan bantuan katalis HCl
menghasilkan
maleanised hydroxyethyl albizia benth oil amide
. Dimana
hidroxyethyl
albizia benth oil
merupakan hasil reaksi dari
albizia benth oil
dengan dietanolamina.
Reaksi esterifikasi dilanjutkan terhadap
maleanised hydroxyethyl albizia benth oil
amide
dengan penambahan anhidrida ftalat yang menghasilkan senyawa
maleanised
albizia benth oil polyesteramide
, seperti reaksi berikut ini : (Akintayo
et al
,2012).
+ O O C C O O R1 R2 O C O R3 HN CH2 CH2 CH2 CH2 OH OH 3 H3C(CH2)3CH2 CH CH CH2 CH CH CH2 (CH2)4 CH2CH2 C O N CH2 CH2 CH2 CH2 OH OH + O O O H3C(CH2)3CH2CH CH CH2CH CHCH2 (CH2)4CH2CH2 C O N CH2CH2 CH2CH2 O OH C COOH O
Albizia Benth Oil dietanolamina
Hidroksietil Albizia Benth Oil Amida (HEABOA) anhidrida maleat HCl Maleanised HEABOA C C O O O anhidrida ftalat + H3C(CH2)3CH2CH CH CH2CH CHCH2 (CH2)4CH2CH2 C O N CH2CH2 CH2CH2 O O C COOH O C O COOH Maleanised albizia benth oil poliesteramida (MA-ABOPEA)
Gambar 2.4. Reaksi pembentukan
maleanised albizia benth oil polyesteramide
2.5. Amida
Amida umumnya dibuat dengan jalan mereaksikan suatu klorida asam dengan amina, amonia, amina monosubstitusi atau amina disubstitusi. Pemberian nama senyawa amida yaitu dengan mengganti akhiran –oat atau –at dari asam karboksilat dengan –amida. Jika atom nitrogen suatu amida berikatan dengan gugus alkil atau aril, maka gugus yang berikatan pada amida ditunjukkan dengan N- (Riswiyanto,2009).
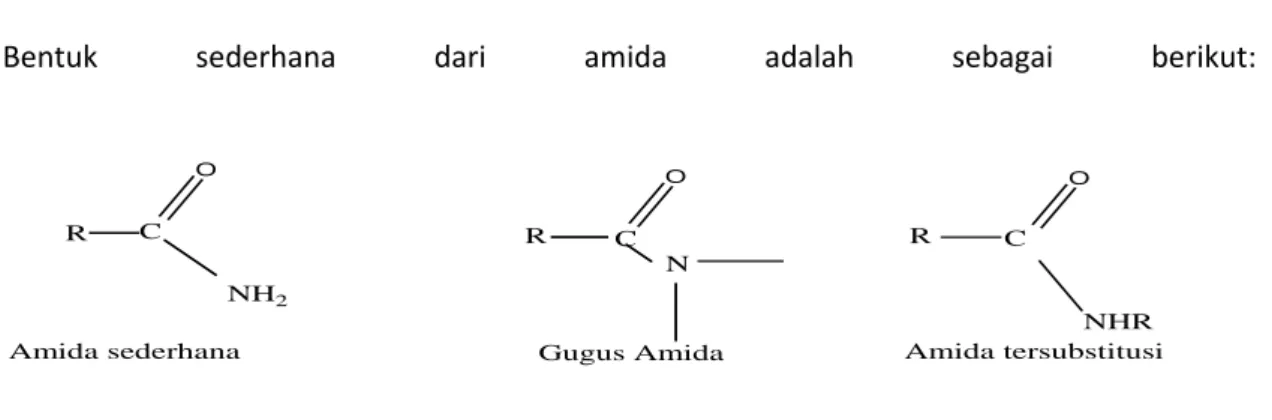
Bentuk sederhana dari amida adalah sebagai berikut:
Amida sederhana C O NH2 C O N Gugus Amida NHR C O Amida tersubstitusi R R R
Gambar 2.5. Bentuk-Bentuk Amida (Fessenden dan Fessenden,1986).
Amida juga dapat dibuat dari reaksi ammonia atau amina dengan turunan asam karboksilat, ester terutama metil ester dan anhidrida asam. Jika ester digunakan sebagai bahan baku, terbentuk alkohol sebagai hasil samping reaksi. Jika digunakan anhidrida, hasil sampingnya adalah asam karboksil (Wilbraham,1992).
Amida siklik mempunyai nama khusus, yaitu diberi akhiran
–laktam
sebagai
pengganti dari gugus lakton yang di dalam cincinnya mengandung atom
nitrogen(Riswiyanto, 2009).
NH H3C NH O O α β γ ε α β−butirolaktam ε−kaprolaktam
Gambar 2.6. Contoh Amida Siklik
2.5.1. Reaksi Amidasi
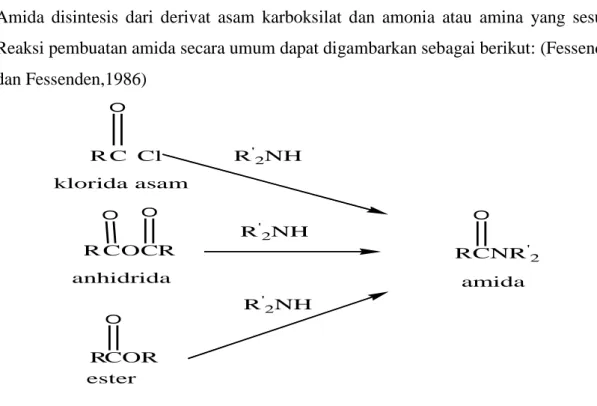
Amida disintesis dari derivat asam karboksilat dan amonia atau amina yang sesuai.
Reaksi pembuatan amida secara umum dapat digambarkan sebagai berikut: (Fessenden
dan Fessenden,1986)
C O Cl R CR O CO R O COR O R CNR'2 O R R'2NH R'2NH R'2NH klorida asam anhidrida ester amidaReaksi antara monoetanolamin dengan metil ester asam lemak untuk
membentuk alkanolamida telah banyak dikembangkan untuk pembuatan Stearamida
(amida asam lemak) yang banyak digunakan dalam kosmetik dan sabun kecantikan
(Urata and Takaishi, 1998).
Apabila senyawa amina direaksikan dengan ester, reaksi akan terjadi pada suhu
tinggi, tetapi sangat lambat sekali apabila dilakukan pada suhu rendah dan tanpa
bantuan katalis basa Lewis seperti NaOCH
3yang lebih kuat dari trietilamin. Reaksi
amidasi antara amina dan ester dengan bantuan katalis NaOCH
pada suhu 100
o-120
oC, sedangkan apabila tidak menggunakan katalismaka reaksi
dapat berlangsung pada suhu 150
o-250
oC (Gabriel, 1984).
Pembuatan amida antara lain :
1. Reaksi asam karboksilat dengan amoniak
HOH CH3 C O OH + NH3 CH3 C OH OH NH2 CH3 C O NH2 +
asam
asetat amoniak
asetamida
air
2. Dalam perdagangan didapat dari garam amoniumnya dipanaskan pada temperatur
100 -200
oC
100-200 oC H2O + CH3 C O ONH4 CH3 C O NH2amonium asetat
asetamida
air
3. Dengan mereaksikan anhidrida asam dengan amoniak
H NH2 + H3C C O NH2 + CH3 C O OH H3C C O O C O H3C
anhidrida asetat
amoniak
asetamida
asam asetat
4. Dengan menghidrolisa senyawa nitril, yakni pada reaksi sebelum terbentuknya asam
karboksilat, terbentuk dahulu amida sebagai salah satu hasil antara.
+ H2O CH3 C CH 3 C O NH2 N
Metil sianida
Air
asetamida
H2O + CH3 C O NH2 CH3 C O OH + NH3
(Besari dkk, 1982)
2.5.2.Etanolamina
Etanolamina (NH2-(CH2)2-OH) merupakan cairan yang higroskopis, kental, berbau amoniak, mampu mengabsorpsi CO2 dan larut dalam air, metanol serta aseton.Etanolamina dikenal juga dengan nama 2-Aminoethanol, Monoethanolamine, Ethylolamine,β-Amino Ethyl alcohol dan β–Hydroxylethylamine. Etanolamina dapat digunakan untuk menghilangkan CO2, H2S dari gas alam ataupun gas lainnya. Etanolamina dapat juga digunakan sebagai sintesis pembuatan surfaktan (Anonimous,1976).
Reaksi dari etilen oksida dengan amonia menghasilkan etanolamina yang digunakan untuk menghilangkan hidrogen sulfida dan karbon dioksida dan gas alam.
H2C CH2
O
NH3 + H2N-CH2-CH2OH
Etanolamina
Gambar 2.7. Reaksi Pembuatan etanolamina (Bailey,1985).
2.5.3.Dietanolamina
Pada umumnya, dietanolamina berbentuk cairan kental, sedikit berbau amoniak dan larut dalam air, metanol, serta aseton. Dietanolamina diproduksi bersamaan dengan monoetanolamina dan trietanolamina melalui amonolisis etilen oksida. Dietanolamina dapat digunakan sebagai emulsifier, dalam pembuatan surfaktan, agen pendispersi, dalam bidang kosmetik dan juga dalam bidang farmasi (Anonimous,1976).
Dietanolamina adalah senyawa yang terdiri dari gugus amina dan dialkohol. Dialkohol menunjukkan adanya dua gugus hidroksil pada molekulnya. Dietanolamina juga dikenal dengan nama bis(hydroxyethyl)amine, diethylolamine, hydroxtdiethylamine, diolamine dan 2,2-iminodiethanol.
H
2C
CH2 ONH
3+
H
2N-CH
2CH
2OH
Dietanolamina
HN-CH
2CH
2OH
CH2CH2OHHOH
2CH
2C-N
CH2CH2OH CH2CH2OHTrietanolamina
Etanolamina
+
+
Amoniak Etilen Oksida
Gambar 2.8. Reaksi pembuatan dietanolamina (Bailey, 1985).
Sifat-sifat dietanolamina adalah sebagai berikut : a. Rumus molekul : C4H11NO2
b. Berat molekul : 105,1364 g/mol c. Densitas : 1,090 g/cm3 d. Titik leleh : 28ºC (1atm) e. Titik didih : 268,8ºC (1atm)
f. Kelarutan : H2O, alcohol, eter
Dietanolamina banyak digunakan dalam produk kosmetik dan detergen karena mampu menciptakan tekstur yang lembut dan foaming agent (Wikipedia,2007).
2.5.4. Alkanolamida
Alkanolamida adalah surfaktan bukan ionik dimana gugus hidroksil yang dimilikinya tidak cukup hidrofilik untuk membuat alkanolamida larut dalam air dengan sendirinya.
Alkanolamida digunakan sebagai bahan pembusa (foom boosting) dalam pembuatan shampoo (Nuryanto,2002).
Untuk membuat senyawa alkanolamida dengan menggunakan dietanolamina melalui reaksi amidasi langsung dengan trigliserida akan menghasilkan senyawa alkanolamida yang memiliki dua gugus hidroksi (poliol) seperti yang telah dilakukan oleh penelitian sebelumnya (Anasri, 2009).
Alkanolamida adalah surfaktan bukan ionik dimana gugus hidroksil yang
dimilikinya tidak cukup hidrofilik untuk membuat alkanolamida larut dalam air
dengan sendirinya. Alkanolamida digunakan sebagai bahan pembusa (
foom boosting
)
dalam pembuatan shampoo.
Jenis alkanolamida yang paling penting adalah dietanolamida. Senyawa
N-etanol alkil amida adalah senyawa yang termasuk dalam golongan asam lemak yang
dapat dimanfaatkan sebagai surfaktan dalam produk detergen, kosmetik dan tekstil.
Senyawa ini dapat dibuat dengan mereaksikan asam lemak sawit destilat dengan
senyawa yang mengandung gugus atom Nitrogen seperti alkanolamina (Nuyanto, dkk,
2002). Sifat kimia dari suatu senyawa alkanolamida sangat bervariasi, tergantung dari
panjang cincin hidrokarbon dan sifat substituen pada atom nitrogen (Bilyk
et al
, 1992).
2.5.5. Monoetanolamida
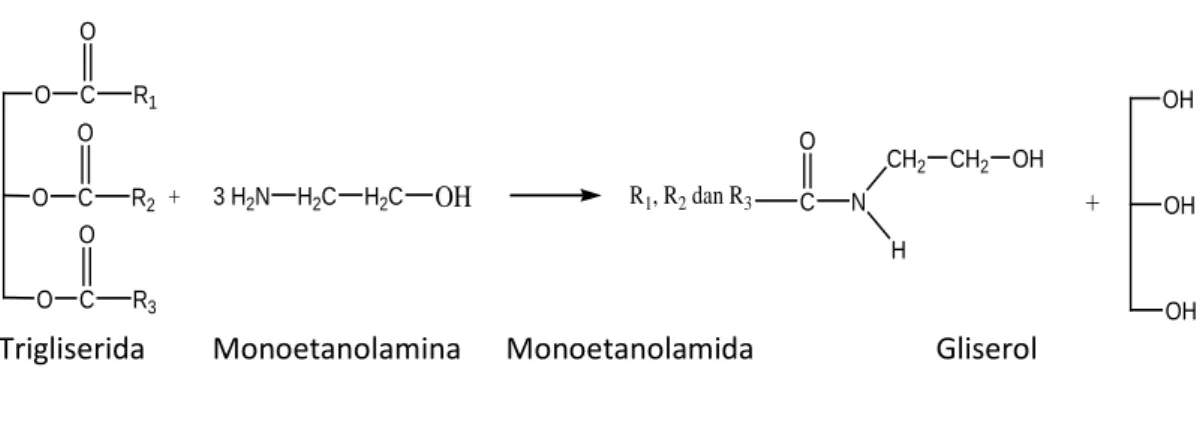
Monoetanolamida asam lemak memiliki banyak kegunaan khususnya dalam detergen dan kosmetik. Fungsi utama dari monoetanolamida adalah sebagai penstabil busa, meningkatkan viskositas dan emulsifier. Secara komersial metil ester asam lemak atau trigliserida dengan monoetanolamina dapat menghasilkan monoetanolamida pada temperatur dan tekanan tetentu seperti gambar 2.3 berikut (Rahman, 2003) :
+ O O C C O O R1 R2 O C O R3 OH OH OH C O N CH2 CH2 OH + H R1, R2 dan R3 OH H2C H2C 3 H2N
Trigliserida Monoetanolamina Monoetanolamida Gliserol
Gambar 2.9. Reaksi Pembentukan Monoletanolamida (Hughes and Lew, 1970)
2.5.6. Dietanolamida
Dietanolamida pertama kali diperoleh dengan mereaksikan dua mol dietanolamina dengan satu mol asam lemak. Senyawa ini diberi nama kritchevsky sesuai dengan nama penemunya. Bahan baku yang digunakan dalam produksi dietanolamida dapat berupa asam lemak, trigliserida atau metil ester. Dietanolamida biasanya diproduksi secara kimia konvensional pada temperature 150oC selama 6-12 jam (Herawan,1999).
Berikut merupakan reaksi pembuatan dietanolamida:
+ O O C C O O R1 R2 O C O R3 OH OH OH C O N CH2 CH2 CH2 CH2 OH OH + R1, R2 dan R3 HN CH2 CH2 CH2 CH2 OH OH 3
trigliserida
dietanolamina
dietanolamida
gliserol
2.6. Anhidrida Asam
Anhidrida asam berasal dari dua asam karboksilat yang melepaskan satu molekul air.
Anhidrida berarti tanpa air. Anhidrida dinamai dengan menambahkan kata anhidrida di
depan nama asamnya. Anhidrida dari asam monokarboksilat berwujud cair, sedangkan
asam dikarboksilat dan asam karboksilat aromatik berwujud padat (Wilbraham dan
Matta, 1992).
CH
3COCCH
3O O
Gambar 2.11. Anhidrida Asam
IUPAC
: anhidrida asam etanoat
Trivial
: anhidrida asam asetat
(Fessenden dan Fessenden, 1986).
Asam anhidrida lebih reaktif dibandingkan dengan ester, tetapi reaksinya
dengan nukleofil kurang reaktif dibandingkan dengan asil halida. Air menghidrolisis
anhidrida kembali menjadi asam. Reaksinya dengan alkohol menghasilkan ester,
sedangkan dengan amonia menghasilkan asam (Hart, 1990).
2.6.1. Tatanama Anhidrida
Anhidrida dinamai dengan menambahkan kata anhidrida di depan nama asamnya.
Salah satu anhidrida asam ialah anhidrida asetat :
H3C C O
O C CH3 O
2.6.2. Pembuatan Anhidrida
Dengan sedikit kekecualian, anhidrida asam tidak dapat dibentuk langsung dari asam
karboksilat induknya, tetapi harus dibuat dari derivat asam karboksilat yang lebih
reaktif. Satu jalur ke anhidrida ialah dari klorida asam dan suatu karboskilat.
R-C-Cl + -O-C-R' R-C-O-C-R' + Cl
-O O O O
suatu klorida asam suatu ion karboksilat suatu anhidrida
Jalur lain pembuatan anhidrida ialah dengan mereaksikan asam karboskilat dan
anhidrida asetat. Suatu reaksi
reversible
terjadi antara suatu asam karboskilat dan
suatu anhidrida. Letak kesetimbangan dapat digeser ke kanan dengan menyuling asam
asetat segera setelah asam ini terbentuk (Fessenden dan Fessenden, 1986).
2.6.3. Reaksi Anhidrida
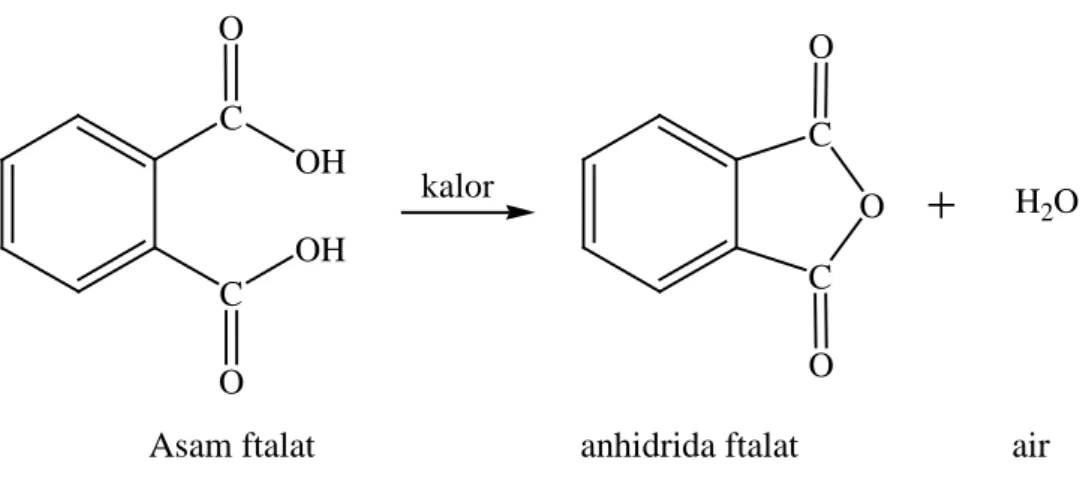
Beberapa asam dikarboksilat tertentu mudah melepas air dalam pemanasan apabila
dapat membentuk cincin beranggota lima atau enam. Misalnya :
H2C H2C OH OH C O C O kalor H2C H2C O C O C O H2O
OH OH C O C O kalor O C O C O H2O
Asam ftalat
anhidrida ftalat
air
Anhidrida asam dari asam monokarboksilat berwujud cair, sedangkan asam
dikarboksilat dan asam karboksilat aromatik berwujud padat (Wilbraham dan Matta,
1992).
Reaksi pembuatan anhidrida asam umumnya berlangsung antara asil klorida
dengan garam dari asam karboksilat. Sifat kimia anhidrida asam sama dengan klorida
asam, namun anhidrida bereaksi sedikit lebih lambat daripada klorida asam. Anhidrida
bereaksi dengan air menghasilkan asam, dengan amina menjadi amida, dengan alkohol
membentuk ester, dan dengan LiAlH
4menghasilkan alkohol primer.
R O R C O C O anhidrida asam R C OH O R C NH2 O R C OR' O R C H O LiAlH4 R C H OH H H2O NH3 R'OH LiAlH4
asam amida ester aldehida alkohol primer
2.6.4 Anhidrida Ftalat
Anhidrida ftalat disebut juga 1,3-
Isobenzofurandione
. Dengan rumus molekul C
8H
4O
3,
berat molekul 148,11 dan titik lebur 130,8
oC. Larut dalam alkohol.
O O
O
Gambar 2.13. Anhidrida Ftalat
(Anonimous, 1967)
2.7.Surfaktan
Surfaktan atau
surface active agent
merupakan senyawa yang dapat menurunkan
tegangan permukaan air. Molekul surfaktan apa saja mengandung suatu ujung
hidrofobik (satu rantai hidrokarbon atau lebih) dan suatu ujung hidrofilik (biasanya,
namun tidak harus, ionik). Jumlah hidrokarbon dari suatu molekul surfaktan harus
mengandung 12 atau lebih atom karbon agar efektif.
O
Ekor hidrofobik
Ekor hidrofilik
Gambar 2.14. Lambang Umum Surfaktan (Fessenden dan Fessenden,1986).
Berdasarkan gugus hidrofiliknya, surfaktan diklasifikasikan menjadi 4 golongan yaitu (Rosen,2004) :