Analisis Densitometrik Protein Reseptor Fertilisasi (ZP3) pada Zona Pelusida
Kambing sebagai Kandidat Bahan Imunokontrasepsi
Densitometric Analysis of Fertilization Receptor Protein (ZP3) on Goat Zona
Pellucida As Candidate of Immunocontraceptive Substance
Imam Mustofa
1), Laba Mahaputra
1), Yoes Prijatna Dachlan
2),
Fedik Abdul Rantam
3), Aucky Hinting
4)1)
Department of Veterinary Reproduction,
3)Department of Veterinary Micobiology
Faculty of Veterinary Medicine,
2)Tropical Disease Center,
4)In Vitro Fertilization
Laboratory of Dr. Soetomo Hospital / Faculty of Medicine, Airlangga University
Abstract
The aim of this study was to confirm the result of SDS-PAGE of goat zona
pellucida protein, and to measure the proportion of it constituents. Goat ovaries
were collected from Surabaya abattoir. Oocyte collected by aspiration of 2 – 5 mm
diameter of follicle. Zona pellucida was collected mechanically by using two
tuberculin syringe followed by three times washing in phosphate buffer saline
(PBS) to avoid debris. Goat’s zona pellucida (gZP) constituents were identified
using sodium dodecyl sulphate poly acryl amide gel electrophoresis (SDS-PAGE)
12 % with high range SDS-PAGE standards and stained with silver.
Densitometric analysis on the gel indicated that each band of gZP1, gZP2, and
gZP3 correlated with the peaks of densitograph. Densitometer curve showed the
composition gZP1, gZP2 and gZP3 were 6.93 %, 29.60 % and 63.47 %
respectively. The results of gel analysis by using SDS-PAGE and densitometry
indicated that isolate protein was originated from the third band (gZP3) of
SDS-PAGE result of goat zona pellucida protein. Densitometric analysis could be use
to get confirmation each band result of SDS-PAGE and to predict the proportion
of goat zona pellucida protein constituents.
Pendahuluan
Zona pelusida adalah glikoprotein yang membungkus oosit atau sel telur. Zona
pelusida mamalia pada umumnya mengandung tiga macam konstituen protein
terglik-osilasi, yaitu Zp1, ZP2, dan Zp3 (Wassarman, 2002). Di antara komponen-komponen
glikoprotein zona pelusida, ZP3 berperan penting dalam proses fertilisasi. Fungsi ZP3
adalah reseptor primer reaksi pengenalan spermatozoa sehingga proses fertilisasi dapat
berberlangsung paripurna (Wassarman et al, 2001). Berdasarkan fungsi tersebut, maka
ZP3 potensial untuk target imunokontrasepsi (Sumitro dan Aulanni’am, 2001).
Penelitian tentang potensi protein zona pelusida-3 kambing (goat zona pellucida-3,
gZP3) sebagai bahan imunokontrasepsi sampai saat ini belum ada pihak lain yang
melakukan. Penelitian sebelumnya menunjukkan bahwa crude protein gZP mencegah
kebuntingan pada hewan coba model. Elektroforesis protein gZP menghasilkan tiga
band
, yaitu gZP1, gZP2, dan gZP3. Protein gZP3 merupakan reseptor fertilisasi pada
zona pelusida kambing. Hal itu dibuktikan bahwa protein gZP3 dikenali oleh membran
plasma spermatozoa kambing (Mustofa dkk., 2004), sedangkan antibodi gZP3 mencegah
fertilisasi in vitro oosit kambing (Mustofa, 2005). Protein gZP3 juga diketahui potensial
sebagai bahan imunokontrasepsi pada hewan model (Mustofa dkk., 2005).
Hasil elektroforesis protein zona pelusida kambing untuk mengisolasi protein
gZP3 tersebut belum dikonfirmasi dengan metode yang lain. Analisis densitometri
merupakan salah satu cara untuk konfirmasi hasil elektroforesis. Hasil analisis
densitometrik terhadap band-band yang ada pada satu lane dalam gel hasil elektroforesis
dapat digunakan untuk konfirmasi keberadaan masing-masing band, dan untuk
kuantifikasi proporsi penyusun protein yang dielektroforesis (Aulanni’am, 2004).
konstituennya. Hasil penelitian ini diharapkan dapat dipakai sebagai dasar untuk
mengeksplorasi protein gZP3 lebih lanjut dalam rangka menemukan peptida asal
protein gZP3 sebagai kandidat bahan imunokontrasepsi untuk wanita.
Metode Penelitian
1. Preparasi Zona Pelusida Kambing
Zona pelusida diperoleh dari aspirasi folikel-folikel yang ada pada permukaan
ovarium kambing asal Rumah Potong Hewan (RPH) Pegirian, Kota Surabaya. Semua
folikel pada ovarium diaspirasi untuk mendapatkan oosit menggunakan alat suntik
yang berisi phosphate buffer saline (PBS, dibuat oleh Sub Laboratorium Fertilisasi In Vitro,
Laoratorium Kebidanan Veteriner Fakultas Kedokteran Hewan Universitas Airlangga).
Sel-sel kumulus yang masih melekat pada oosit dilepaskan dengan cara pemipetan
berulang-ulang, selanjutnya dicuci tiga kali dengan PBS dari petri ke petri. Zona
pelusida diperoleh dengan memecah oosit secara manual dengan pengamatan
mikroskop disecting. Satu ujung jarum tuberkulin menahan satu sisi zona pelusida oosit.
Ujung jarum tuberkulin yang lain ditusukkan pada zona pelusida oosit pada sisi yang
berlawanan dengan gerakan mencongkel untuk mengeluarkan vitelus dari oosit. Zona
pelusida dihisap satu per satu, kemudian dicuci tiga kali dengan PBS dari petri ke petri
untuk menghilangkan debris. Sonikasi dengan Ultrasonic Homogenizer pada frekuensi 25
KHz secara bertahap (2 menit, 2 menit, dan 1 menit) dilakukan untuk fraksinasi protein
zona pelusida (Mustofa dkk., 2004).
2. Elektroforesis Protein Zona Pelusida Kambing
Elektroforesis dilakukan dengan sodium dodecil sulphuric acid - polyacrylamide gel
electrophoresis
(SDS-PAGE) 12 % menggunakan electrophoresis set mini protein gel
(Bio-Rad).
Sampel hasil sonikasi gZP ditambah Naphtol hingga konsentrasinya 0,1 %,
selanjutnya divortex dan didiamkan pada suhu ruang selama 20 menit. Suspensi
sampel zona pelusida kambing diencerkan dengan larutan NaCl fisiologis
dengan perbandingan 1 : 3 kemudian dicampur dengan RSB (reducing sample
buffer
), yaitu Laemli buffer (1:1). Sampel dalam tabung Eppendorf dipanaskan 50
0C selama 3 detik dan selanjutnya dimasukkan ke dalam tiap sumuran
masing-masing 20 l. Marker, High Range SDS-PAGE Standards (Bio-Rad) dengan volume
yang sama juga dimasukkan ke salah satu sumuran. Running elektroforesis
dilakukan dengan arus konstan 40 mA dengan tegangan 125 Volt selama 2,5 jam
atau sampai sampel turun semua di atas dasar gel. Pewarnaan gel dilakukan
dengan silver stain SDS-PAGE Standards (Bio-Rad).
Isolasi gZP3 dilakukan dengan elektroforesis horisontal (Bio-Rad). Eluat
dikonfirmasi kebenarannya (apakah benar band gZP3 yang telah diisolasi) dengan cara
di-running ulang dalam SDS-PAGE. Sebanyak 10 μl isolat (mengandung 2,9 μg gZP3)
diencerkan dalam Laemli buffer 1 : 1. Larutan tersebut selanjutnya dipaparkan pada
sumuran SDS-PAGE 12 % seperti pada proses yang dilakukan sebelumnya.
3. Densitometri
Gel hasil SDS-PAGE gZP dan gel hasil SDS-PAGE ulang protein eluat, diperiksa
dalam Densitometer apparatus pada panjang gelombang 573 nm. Hasil pemeriksaan
dengan Analisis Densitometri (densitograf) diperiksa kesesuaiannya dengan band-band
hasil SDS-PAGE protein zona pelusida kambing dan isolat protein gZP3. Kuantifikasi
proporsi protein pada masing-masing lane dilakukan berdasarkan luas daerah dibawah
kurva densitograf.
Hasil dan Pembahasan
Pada SDS-PAGE protein mengalami elektroforesis dalam deterjen ionik,
sehingga deterjen akan mengikat residu hidrofobik peptida. Protein dalam SDS-PAGE
akan bermigrasi sesuai dengan massa molekul relatifnya dan akan terkonsentrasi pada
band
atau pita pada gel. Protein dengan massa molekul relatif (Mr) yang lebih besar pada
gel SDS-PAGE akan tertahan pada posisi yang lebih tinggi daripada protein dengan Mr
yang lebih rendah (Rantam, 2003).
Apabila glikoprotein zona pelusida (ZP) dipaparkan pada SDS-PAGE, maka
pada umumnya akan terbagi dalam tiga macam protein konstituen, yitu ZP1, ZP2 dan
Zp3 (Carino et al., 2001 ; Carino et al., 2002 ; Mate et al., 2003). Penelitian sebelumnya
menunjukkan bahwa zona pelusida kambing pada SDS-PAGE juga menghasilkan tiga
band.
Sesuai dengan nomenklatur (Hafez, 2000), maka berdasarkan kenaikan massa
molekul relatif (Mr) nya ketiga band tersebut berturut-turut disebut sebagai gZP1, gZP2
dan gZP3 dengan Mr berturut-turut 120,67 ± 6,12 ; 94,38 ± 1,66 dan 82.,5 ± 6,90 kDa
(Gambar 1) (Mustofa dkk., 2004).
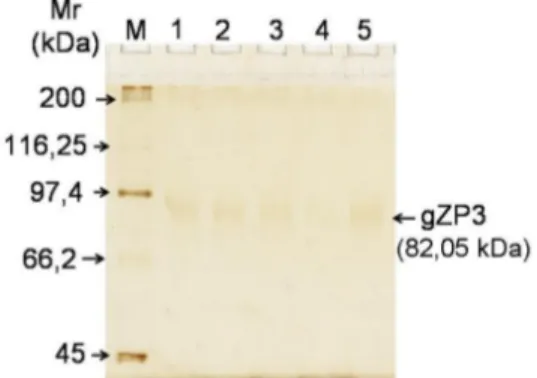
Gambar 1. Gel Hasil Analisis dengan SDS-PAGE 12 % pada Zona Pelusida Kambing dengan Pewarnaan Silver Stain (M : marker, 1, 2 dan 3 : sampel gZP) (Mustofa dkk., 2004).
Sampel hasil elusi protein gZP3 dianalisis dengan SDS-PAGE untuk konfirmasi
apakah protein yang diisolasi benar-benar berasal dari band ketiga gel hasil running
sampel protein gZP (Gambar 2). Lima sampel eluat dalam running ulang semuanya
menghasilkan band tunggal yang terletak di bawah marker posphorilase b (Mr = 97,4 kDa),
sesuai dengan posisi gZP3 pada Gambar 1. Hasil tersebut menunjukkan bahwa protein
yang diisolasi adalah protein gZP3. Pada Gambar 2, band tunggal protein gZP3 hasil
SDS-PAGE kurang jelas, sehingga perlu dikonfirmasi keberadaannya dengan
densitometri.
Gambar 2. Analisis Isolasi Protein gZP3 dengan SDS-PAGE 12 % (M : marker ; 1, 2, 3, 4 dan 5 : sampel gZP3)
Densitometri Gel SDS-PAGE Protein gZP dan gZP3
Pemeriksaan gel hasil SDS-PAGE dengan densitometri dilakukan dengan tujuan
untuk konfirmasi keberadaan band pada masing-masing lane, dan untuk menghitung
proporsi protein dalam satu lane (Aulanni’am, 2004). Suatu band yang menandakan
adanya akumulasi protein pada gel hasil elektroforesis diidentifikasi sebagai oleh suatu
puncak (peak). Masing-masing puncak memiliki karakteristik ketinggian (height) sebagai
intensitas densitograf dan luas daerah di bawah kurva (area) sebagai gambaran kuantitas
protein pada band tersebut. Teknik densitometri dapat digunakan sebagai alat bantu
untuk memisahkan beberapa protein pada adenovirion (Zeineh et al., 1986), untuk
mengetahui konstituen protein pada beberapa spesies jamur (Petrovska et al., 2004), dan
menganalisis kemurnian hasil akhir pemisahan protein (Arvys Protein brochure).
Hasil pemeriksaan dengan Densitometri terhadap lane marker, lane gZP dan
gZP3 diperoleh konfirmasi keberadaan band yang sesuai dengan densitogramnya.
Kesesuaian tersebut ditandai dengan kesamaan letak band dan letak puncak (peak)
densitogram. Kesesuaian terdapat baik pada lane marker, lane sampel gZP (terdiri dari
band
gZP1, gZP2, dan gZP3) maupun lane gel hasil SDS-PAGE ulang isolat gZP3
(Gamba1 3 – 5).
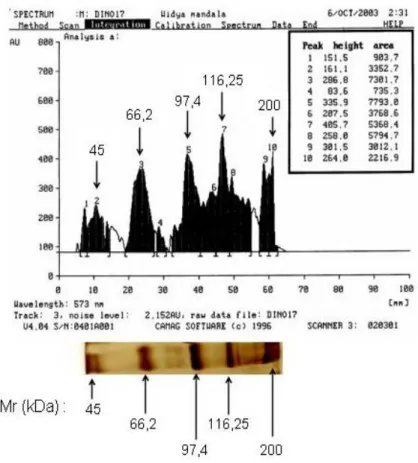
Pada kurva densitograf lane marker (Gambar 3), muncul sepuluh puncak (peak)
kurva, namun ada lima puncak dengan ketinggian dan luas area dominan yang letaknya
sesuai dengan lima band yang ada pada gel hasil SDS-PAGE adalah puncak nomor 2, 3,
5, 7 dan 9. Hasil ini menunjukkan bahwa terdapat kesesuaian antara lane marker
SDS-PAGE dengan analisis densitometrik. Dengan demikian teknik densitometri relevan
digunakan untuk menganalisis gel hasil SDS-PAGE protein suspensi zona pelusida
kambing dan protein gZP3.
Gambar 3. Analisis Marker Hasil SDS-PAGE dengan Densitometri pada Panjang Gelombang 573 nm
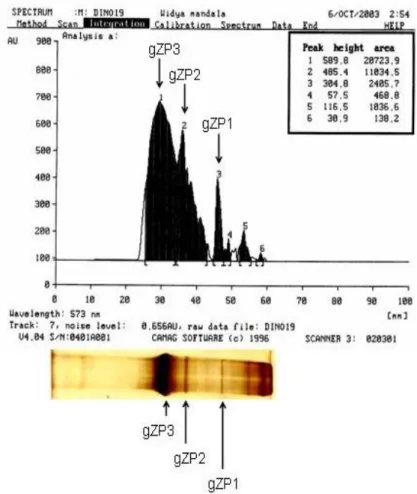
Pada kurva densitograf SDS-PAGE sampel gZP (Gambar 4) muncul enam
puncak. Gambaran kurva yang sesuai dengan band gZP1, gZP2 dan gZP3 adalah puncak
densitograf nomor 3, 2 dan 1, sedangkan puncak 4, 5 dan 6 relatif sangat rendah.
Diantara ketiga puncak tersebut, puncak nomor 1 (gZP3) paling dominan, sedangkan
puncak nomor 3 (gZP1) tampak langsing. Kurva densitograf gZP2 dan gZP3 saling
tumpang tindih (overlapping), namun pada gel ketiga konstituen tampak jelas terpisah.
Gambar 4. Analisis Protein gZP Hasil SDS-PAGE dengan Densitometri pada Panjang Gelombang 573 nm
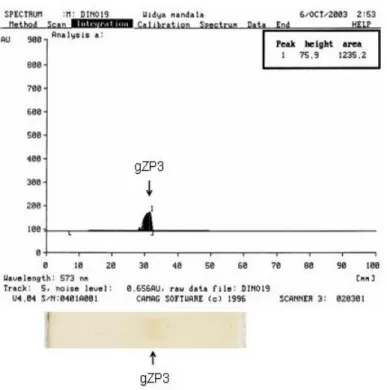
Identifikasi band tunggal hasil SDS-PAGE ulang isolat gZP3 pada Densitometer
juga menghasilkan peak tunggal dengan jarak migrasi protein sejauh 32 mm, sesuai
dengan jarak migrasi protein gZP3 pada gel hasil SDS-PAGE gZP3 maupun gZP. Pada
densitograf tampak kurva tunggal dengan ketinggian 75,9 mm dan luas daerah di
bawah kurva sebesar 12,35 cm
2(Gambar 5).
Gambar 5. Analisis Protein gZP3 Hasil SDS-PAGE Ulang Isolat gZP3 dengan Densitometri pada Panjang Gelombang 573 nm
Proporsi Massa Konstituen Zona Pelusida Kambing
Densitometri juga dapat memberikan analisis kuantitatif protein dalam satu lane
gel hasil elektroforesis. Shawn et al. (1999) membuktikan bahwa analisis densitometri
dapat dipakai untuk menentukan komponen G protein regulated inwardly rectifying K
+(GIRK) secara stokiometrik. Lopez et al. (2005) melakukan kuantifikasi albumin dan
protein-protein lain yang ada pada gambar gel SDS-PAGE serum atau plasma, yang
diwarnai dengan comasie blue.
Pada penelitian ini didapat lima lane pada gel SDS-PAGE dengan tiga band
konstituen zona pelusida yang jelas terbaca. Analisis densitometrik terhadap kelima lane
tersebut menghasilkan nilai luas area di bawah kurva densitograf pada masing-masing
komponen zona pelusida. Rerata proporsi massa (persentase) gZP1, gZP2 dan gZP3
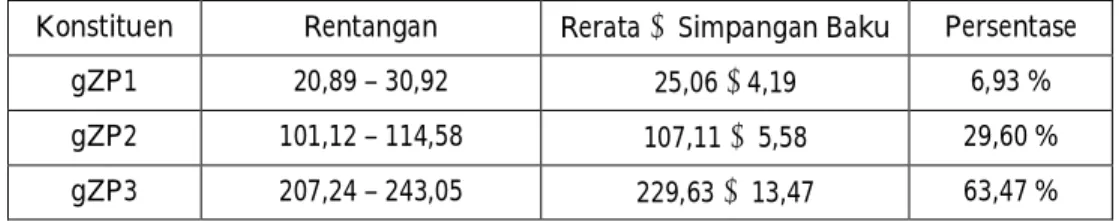
Tabel 1. Rerata, Simpangan Baku dan Persentase Luas Daerah (cm2) Di Bawah Kurva Densitograf Konstituen Zona Pelusida Kambing
Konstituen Rentangan Rerata Simpangan Baku Persentase
gZP1 20,89 – 30,92 25,06 4,19 6,93 %
gZP2 101,12 – 114,58 107,11 5,58 29,60 %
gZP3 207,24 – 243,05 229,63 13,47 63,47 %
Ketebalan band pada gel hasil SDS-PAGE dikuantifikasi dalam bentuk luas
daerah di bawah kurva (area) pada kurva densitograf. Kuantitas tersebut menunjukkan
proporsi kadar protein pada gel (Green, 1997 ; Hemachand et al, 2002). Pada zona
pelusida kambing band paling tebal adalah band gZP3, kemudian diikuti band gZP2 dan
paling tipis band gZP1. Adanya data bahwa band gZP3 adalah yang paling tebal,
menunjukkan bahwa gZP3 mempunyai proporsi massa paling banyak dibandingkan
gZP1 dan gZP2 pada zona pelusida kambing. Konstituen ZP3 mempunyai proporsi
terbesar karena fungsi utama zona pelusida dalam fertilisasi adalah untuk pengenalan
primer spermatozoa terhadap oosit yang selanjutnya menginduksi reaksi akrosom pada
spermatozoa tersebut.
Gambar 6. Diagram Persentase Proporsi Konstituen Protein Zona Pelusida Kambing Berdasarkan Densitometri Gel Hasil SDS-PAGE
gZP1 7% gZP2 30% gZP3 63%