TESIS – SK142502
TURUNAN ISONIAZID: SINTESIS DAN UJI
BIOAKTIVITAS TERHADAP
Mycobacterium
ISONIAZID DERIVATIVES: SYNTHESIS AND
BIOACTIVITY TEST AGAINTS
Mycobacterium
tuberculosis
H
37Rv
M. RIZA GHULAM FAHMI NRP 1415 201 006
SUPERVISOR
Prof. Mardi Santoso, Ph. D
MAGISTER PROGRAM ORGANIC CHEMISTRY
TURUNAN ISONIAZID: SINTESIS DAN UJI BIOAKTIVITAS
TERHADAP
Mycobacterium tuberculosis
H
37Rv
Nama Mahasiswa : M. Riza Ghulam Fahmi
NRP : 1415 201 006
Pembimbing : Prof. Mardi Santoso, Ph. D
ABSTRAK
ISONIAZID DERIVATIVES: SYNTHESIS AND BIOACTIVITY
TEST AGAINTS
Mycobacterium tuberculosis
H
37Rv
By : M. Riza Ghulam Fahmi
Student Identity Number : 1415 201 006
Supervisor : Prof. Mardi Santoso, Ph. D.
ABSTRACT
2-Isonicotinohidrazone-3-(N-4-KATA PENGANTAR
Alhamdulillahirobbil’alamin. Puji syukur penulis panjatkan kepada Allah SWT karena berkat rahmat dan ridho-Nya penulis dapat menyelesaikan naskah tesis yang berjudul “Turunan Isoniazid: Sintesis dan Uji Bioaktivitas terhadap Mycobacterium tuberculosis H37Rv”. Penulis mengucapkan terima kasih kepada pihak-pihak yang telah membantu dan mendukung dalam pengerjaan tesis ini, yaitu:
1. Prof. Mardi Santoso, Ph.D selaku dosen pembimbing dan dosen wali yang telah sabar memberikan arahan dan bimbingan selama proses pengerjaan nasakah tesis ini.
2. Prof. Dr. Didik Prasetyoko, M.Sc selaku Kepala Departemen Kimia yang telah memberikan fasilitas selama penyusunan naskah tesis
3. Bapak dan Ibu dosen yang telah mendidik dan menginspirasi penulis selama menempuh studi di kampus perjuangan ini.
4. Ayah, Ibu, indar dan seluruh keluarga, terima kasih atas doa, dukungan, dan motivasi yang selalu dialirkan sehingga penulis dapat menyelesaikan rancangan tesis ini.
5. Lidya Tumewu dari Lembaga Penyakit Tropis Universitas Airlangga dan Elvira dari Kimia ITB yang telah membantu dalam melakukan analisis menggunakan spektrometer massa dan NMR.
6. Linda Oktabriana dari Laboratorium Mikrobiologi Fakultas Kedokteran UGM yang telah membantu dalam melakukan pengujian anti-tuberkular. 7. Teman-teman mahasiswa Program Magister Departemen Kimia FMIPA
angkatan 2015 dan laboratorium kimia bahan alam dan sintesis (KIBAS) telah menemani penulis dalam pengerjaan rancangan tesis ini.
8. LPPM ITS atas dana penelitian yang diberikan melalui Dana Penelitian Hibah Hibah 903/PKS/ITS2017 ITS 2017.
Penulis menyadari bahwa naskah tesis ini masih terdapat kekurangan, oleh karena itu penulis menerima saran dan kritik yang membangun dari pembaca. Semoga Tesis ini memberikan manfaat bagi penulis dan pembaca.
Surabaya, Juli 2017
DAFTAR ISI
BAB II TINJAUAN PUSTAKA 7
2.1 Isatin (5) 7
2.2 Tuberkulosis 10
2.3 Bakteri Mycobacterium tuberculosis 12
2.4 Kromatografi 15
2.5 Identifikasi Hasil Sintesis 16
2.5.1 Identifikasi Hasil Sintesis Dengan Spektroskopi Inframerah (IR)
16
2.5.3 Identifikasi Hasil Sintesis Dengan Spektroskopi Massa 19
BAB III METODOLOGI PENELITIAN 21
3.1 Alat dan Bahan 21
3.1.1 Alat 21
3.1.2 Bahan 21
3.2 Prosedur 21
3.2.1 Sintesis N-Benzil-5,7-dibromosatin (12b) 21 3.2.2 Sintesis N-4-Bromobenzil-5,7-dibromosatin (12c) 22 3.2.3 Sintesis 2-Isonikotinohidrazon-5,7-dibromoisatin (11a) 22 3.2.4 Sintesis
2-Isonikotinohidrazon-3-(N-benzil)-5,7-dibromoisatin (11b)
23
3.2.5 Sintesis 2-Isonikotinohidrazon-3-(N-4-bromobenzil)-5,7-dibromoisatin (11c)
23
3.2.6 Pengujian Hasil Sintesis (11a-c) terhadap M. tuberculosis Secara in vitro
24
BAB IV HASIL DAN PEMBAHASAN 25
BAB V KESIMPULAN DAN SARAN 47
5.1 Kesimpulan 47
5.2 Saran 47
DAFTAR PUSTAKA 49
DAFTAR GAMBAR
Gambar 1.1 Analisa retrosintesis turunan isoniazid (11a-c) 6 Gambar 2.1 Struktur dinding sel M. tuberculosis 13 Gambar 2.2 Data pergeseran kimia dalam 1H NMR 19 Gambar 2.3 Data pergeseran kimia dalam 13C NMR 19 Gambar 4.1 KLT sintesis N-benzil-5,7-dibromoisatin (12b) 25 Gambar 4.2 KLT N-benzil-5,7-dibromoisatin (12b) hasil sintesis 26 Gambar 4.3 Spektrum 1H-NMR N-benzil-5,7-dibromoisatin (12b) 27 Gambar 4.4 Usulan mekanisme umum reaksi benzilasi 5,7-dibromoisatin (12b-c) 27 Gambar 4.5 KLT sintesis N-4-bromobenzil-5,7-dibromoisatin (12c) 28
Gambar 4.6 KLT N-4-bromobenzil-5,7-dibromoisatin (12c) hasil
sintesis 29
Gambar 4.7 Spektrum (12c) 1H-NMR N-4-bromobenzil-5,7-dibromoisatin 30
Gambar 4.8 Spektrum 13C-NMR N-4-bromobenzil-5,7-dibromoisatin
(12c) 31
Gambar 4.9 KLT sintesis 2-isonikotinohidrazon-5,7-dibromoisatin
(11a) 32
Gambar 4.10 Hasil uji kemurnian 2-isonikotinohidrazon-5,7-dibromoisatin (11a) hasil intesis 32
Gambar 4.15 KLT Sintesis 2-isonikotinohidrazon-(
N-benzil)-5,7-dibromoisatin (11b) 36
Gambar 4.16 KLT 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin
(11b) hasil sintesis 36
Gambar 4.17 Spektrum HRMS 2-isonikotinohidrazon-(
N-benzil)-5,7-dibromoisatin (11b) hasil sintesis 37
Gambar 4.18 Spektrum 1H-NMR 2-isonikotinohidrazon-(
N-benzil)-5,7-dibromoisatin (11b) 38
Gambar 4.19 KLT sintesis 2-isonikotinohidrazon-(
N-4-bromobenzil)-5,7-dibromoisatin (11c) 39
Gambar 4.20 KLT 2-isonikotinohidrazon-(
N-4-bromobenzil)-5,7-dibromoisatin (11c) hasil sintesis 39
Gambar 4.21 Spektrum HRMS 2-isonikotinohidrazon-(
N-4-bromobenzil)-5,7-dibromoisatin (11c) hasil sintesis 40 Gambar 4.22 Spektrum 1H-NMR
2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) 41 Gambar 4.23 Spektrum 13C-NMR
2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) 42 Gambar 4.24 Spektrum dept-135 2-isonikotinohidrazon-(
DAFTAR TABEL
Tabel 1.1 Data bioaktivitas hidrazona dari turunan isatin Bacillus subtilis ATCC6633 (7a-d) terhadap 3
Tabel 1.2 Data aktivitas biologis turunan hidrazona tuberculosis H37Rv (8a-c) terhadap M. 3
Tabel 1.3 Data aktivitas biologis turunan hidrazona bakteri Pseudomonas aeruginosa (10a-f) terhadap 5 Tabel 2.1 Karakteristik serapan IR gugus fungsi 17 Tabel 4.1 Data perbandingan 1H-NMR hasil benzilasi 7,7-dibromoisatin (12b-c) 30
Tabel 4.2 Tabel perbandingan data 1H-NMR turunan isoniazid hasil sintesis (11a-c) 41
DAFTAR LAMPIRAN
LAMPIRAN A SKEMA KERJA 55
A.1 Prosedur Sintesis N-benzil-5,7-dibromoisatin (12b) 55 A.2 Prosedur Sintesis (N-4-bromobenzil)-5,7-dibromoisatin (12c) 56 A.3 Prosedur Sintesis 2-Isonikotinohidrazon-5,7-dibromoisatin (11a) 57 A.4 Prosedur Sintesis 2-Isonikotinohidrazon-3-(dibromoisatin (11b) N-benzil)-5,7- 58
A.5 Prosedur Sintesis 2-Isonikotinohidrazon-3-5-(dibromoisatin (11c) N-4-bromobenzil)-5,7- 59
A.6 Pengujian Hasil Sintesis vitro (11-c) terhadap M. tuberculosis Secara in 60
LAMPIRAN B PERHITUNGAN RENDEMEN 61
B.1 Perhitungan Rendemen Hasil N-benzil-5,7-Dibromoisatin (12b) 61 B.2 Perhitungan Rendemen Hasil (12c) N-4-bromobenzil-5,7-Dibromoisatin 62
B.3 Perhitungan Rendemen Hasil 2-isonikotinohidrazon-5,7-dibromoisatin (11a) 63
B.4 Perhitungan Rendemen Hasil 2-isonikotinohidrazon-(dibromoisatin (11b) N-benzil)-5,7- 64
BAB I
PENDAHULUAN
1.1 Latar Belakang
floroquinolona seperti leflokasin (3) dan oflakasin (4) yang disebut extensively drug-resistant (XDR). WHO melaporkan bahwa pada tahun 2014 penderita MDR-TB di Indonesia berjumlah 1.182 orang. Penyebab utama resistansi adalah mutasi gen secara alami, ketidakpatuhan terapi, dan penggunaan obat yang tidak teratur (Schneider et al., 2005; Marriner et al., 2011). Terlepas dari meningkatnya jumlah resistansi terhadap obat anti-TB, belum ada obat TB baru yang diluncurkan selama empat dekade. Pengembangan senyawa-senyawa baru anti-TB yang aman dan efektif sangat diperlukan untuk menangani penyakit yang diakibatkan M. tuberculosis (Dixit et al., 2006).
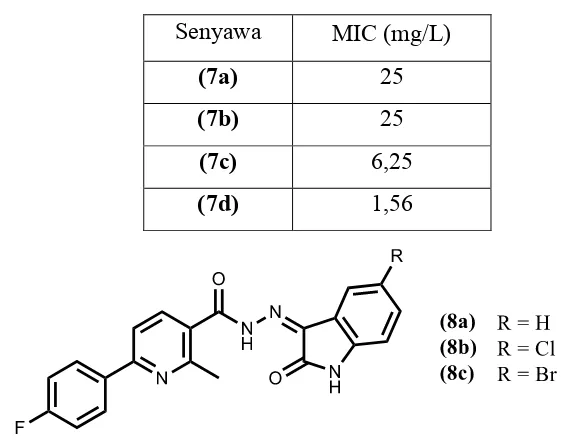
dapat dilihat pada Tabel 1.1. Data menunjukkan isatin (7d) dengan gugus pensubtitusi dibromo pada C-5 dan C-7 lebih aktif daripada isatin (7a-c). Eldehna et al. (2015) melaporkan bahwa hidrazona (8a-c) memiliki aktivitas biologis sebagai antituberkulosis terhadap bakteri M. tuberculosis H37Rv. Hidrazona (8c) dengan gugus pensubtitusi bromo lebih aktif daripada hidrazona (8a-b), sebagaimana dapat dilihat pada Tabel 1.2.
Tabel 1.1 Data bioaktivitas turunan isatin (7a-d) terhadap Bacillus subtilis ATCC6633
Senyawa MIC (mg/L)
(7a) 25
(7b) 25
(7c) 6,25
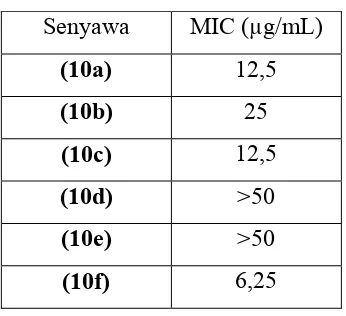
Aboul-Fadl et al. (2015) mendapatkan bahwa hidrazona dari 5-floroisatin (9a-b) memiliki aktivitas terhadap bakteri M. tuberculosis H37Rv, hidrazona dengan gugus
N-benzil (9b) menunjukkan MIC yang lebih rendah (MIC 0,156 µg/mL) daripada senyawa (9a) dengan MIC 5 µg/mL. Tehrani et al. (2016) berhasil mensintesis dan menguji aktivitas biologis hidrazona (10) terhadapa bakteri gram negatif Pseudomonas aeruginosa. Hasil uji sebagaimana dapat dilihat pada Tabel 1.3 menunjukkan bahwa bioaktivitas hidrazona (10f) lebih baik dari pada senyawa lain (10a-e). Hal ini menunjukkan bahwa hidrazon hasil reaksi isatin (5) dengan nukleofil isoniazid
(1) memiliki aktivitas biologis yang lebih baik daripada hidrazon hasil reaksi dengan nukleofil yang lain.
Tabel 1.3 Data bioaktivitas turunan hidrazona (10a-f) terhadap bakteri
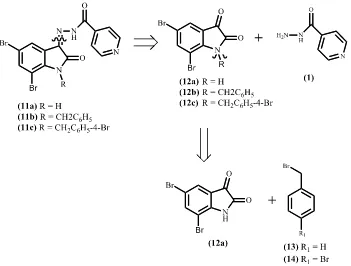
Gambar 1.1. Analisis retrosintesis turunan isoniazid (11a-c) 1.3 Tujuan Penelitian
Penelitian bertujuan untuk mendapatkan (N-benzil)-5,7-dibromoisatin (12b), (N-4-bromobenzil)-5,7-dibromoisatin (12c), turunan isoniazid baru (11a-c), serta mendapatkan data bioaktivitas senyawa (11a-c) terhadap M. tuberculosis. 1.4 Manfaat Penelitian
BAB 2
KAJIAN PUSTAKA DAN DASAR TEORI
2.1 Isatin (5)
Isatin (5) juga dapat diperoleh dengan Metode Stolle yang melibatkan reaksi anilina dengan oksalil klorida (23) menjadi 2-okso-2-(fenilamino)asetil klorida (24) yang selanjutnya diikuti dengan asilasi Friedel-Craft intramolekular menggunakan katalis asam kuat lewis sehingga diperoleh isatin (5) (Beckman, 2005).
2.2 Tuberkulosis
Tuberkulosis (TBC atau TB) adalah penyakit infeksi yang termasuk sepuluh besar sebagai penyebab kematian. Tuberkulosis merupakan penyakit menular yang disebabkan oleh Mycobacterium tuberculosis dengan gejala yang bervariasi, dan dapat mengenai semua organ tubuh dengan lokasi terbanyak pada organ paru-paru (90%) (WHO, 2015; Mansjoer, 2000). Tuberkulosis paru adalah penyakit infeksi yang menyerang pada saluran pernafasan (Smeltzer et al., 2010). Penyakit TB dapat ditularkan melalui udara. Penyakit TB dapat meningkatkan resiko terkena Human Immunodeficiency Virus (HIV) (Wells et al., 2009).
Resistensi obat anti-TB disebabkan bakteri M. tuberculosis telah mengalami kekebalan terhadap obat anti-TB, dan merupakan masalah yang sangat serius. Resistensi terhadap obat anti-TB terdapat dalam bentuk multi-drug resistant tuberculosis (MDR-TB) dan extensively drug-resistant tuberculosis (XDR-TB). MDR-TB merupakan kekebalan bakteri M. tuberculosis terhadap obat lini pertama seperti isoniazid (1) dan rifampisin (2), sedangkan XDR-TB adalah kekebalan bakteri M. tuberculosis terhadap isoniazid (1) dan rifampisin (2) serta salah satu obat lini kedua seperti golongan florokuinolona atau setidaknya salah satu dari obat suntik seperti amikasin (37) (Raviglione, 2010).
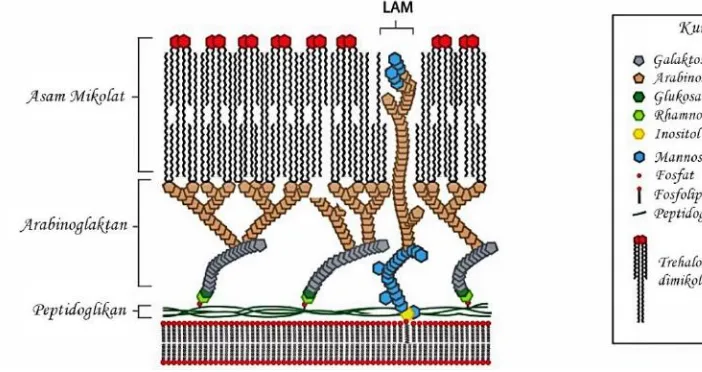
2.3 Bakteri Mycobacterium tuberculosis
Genus mycobacterium termasuk basil gram positif yang menunjukkan karakteristik pewarnaan tahan asam. Dinding sel terdiri dari peptidoglikan dan mirip dengan organisme gram positif lainnya yang banyak mengandung polisakarida dengan rantai bercabang, protein dan lipid (Ryan dan Ray, 2010).
Bakteri M. tuberculosis strain H37 pertama kali didapatkan dari pasien TB pada tahun 1905 oleh Edward R. Baldwin. Strain H37 memiliki dua varian yaitu varian “R” yang menunjukkan tahan terhadap lingkungan dan “S” yang menunjukkan peka terhadap lingkungan. Untuk menunjukkan virulensi atau avirulensi, ditambahkanan huruf (v) atau (a) sehingga menjadi "Rv" dan "Ra". Varian “R” dan “S” diklasifikasikan kedalam gram positif dan acid fast. Varian “S” berbentuk batang padat, kadang-kadang sedikit melengkung dan panjangnya bervariasi dari 2 sampai 5 mikron. Varian “S” sangat stabil pada media alkali. Varian “R” adalah pleomorfik, ukuran bervariasi dari 3 sampai 10 mikron. Varian “R” sangat stabil pada media asam (Steenken et al., 1943; Loerger et al., 2010; Bouwman et al., 2012).
Isoniazid (1) memiliki struktur yang terdiri dari cincin piridin dan gugus hidrazida yang memiliki peranan penting untuk melawan M. tuberculosis. Resistensi isoniazid (1) disebabkan oleh mutasi gen pada oxyR-ahpc, furA, katG, kasA, iniA, iniB, iniC, ndh, dan inhA. Mutasi gen terjadi pada gen katG sebesar 50-95%; gen inhA sebesar 8-43% dan sisanya pada gen lain. Mekanisme kerja isoniazid (1) adalah dengan menghambat biosintesis asam mikolat (Ramaswamy dan Musser, 1998; Zhang dan Yew, 2009).
Gen InhA merupakan gen pengkode enzim enoil reduktase yang berperan dalam biosintesis asam mikolat. Ikatan isoniazid (1) diaktivasi untuk membentuk kompleks terner INH-NADH sehingga menghasilkan penghambatan biosintesis asam mikolat. Gen katG merupakan gen pengkode enzim katalase peroksidase yang digunakan untuk mengaktivasi isoniazid (1). Enzim katalase peroksidase digunakan untuk mengaktivasi isoniazid (1) menjadi isonikotinat asil yang akan menghambat biosintesis asam mikolat dan terganggunya biosintesis asam mikolat mengakibatkan kematian bakteri. Hilangnya aktivitas enzim katalase peroksidase dan mutasi gen katG akan mengakibatkan resistensi isoniazid (1) (Ramaswamy dan Musser, 1998; Da Silva et al., 2011)
yang mengkode subunit β-polimerase asam ribonukleat (RNA) yang mengakibatkan penghambatan inisiasi transkripsi dari mRNA. (Da Silva et al., 2011).
2.4 Kromatografi
KLT dua arah atau dua dimensi digunakan untuk analisis sampel dengan komponen-komponen yang mempunyai sifat kimia dan nilai Rf yang hampir sama. KLT dua dimensi dilakukan dengan cara menotolkan noda plat KLT yang berbentuk persegi empat yang selanjutnya dimasukkan ke dalam chamber yang telah berisi eluen pertama. Plat KLT selanjutnya diputar 90° dan dimasukkan ke dalam chamber yang telah berisi eluen kedua (Rohman, 2007).
2.5 Identifikasi Hasil Sintesis
2.5.1 Identifikasi Hasil Sintesis dengan Spektroskopi Inframerah (IR) Spektroskopi inframerah merupakan suatu metode identifikasi yang digunakan untuk mengetahui gugus fungsi. Identifikasi dengan spektroskopi inframerah didasarkan pada vibrasi internal atom suatu gugus fungsi. Radiasi infra merah yang dilewatkan melalui suatu cuplikan, menyebabkan inti-inti atom yang terikat secara kovalen dapat menyerap energi inframerah dan terjadilah transisi dari tingkat vibrasi dasar (ground state) menuju tingkat vibrasi tereksitasi (excited state). Tipe ikatan bersifat spesifik terhadap serapan panjang gelombang. Hal inilah yang menyebabkan tiap-tiap molekul akan memiliki karakteristik spektrum inframerah pada konsentrasi ukur tertentu, yang dapat dibedakan dari spektrum lain melalui posisi dan intensitas serapan. Ikatan yang mengalami relaksasi melepas foton yang kemudian ditangkap oleh detektor dan diubah menjadi spektrum IR yang merupakan plot jumlah radiasi inframerah yang diteruskan melalui cuplikan sebagai fungsi frekuensi atau panjang gelombang (Bruice, 2004; Silverstein et al., 2005; Solomons dan Fryhle, 2011).
Spektrum IR memberikan informasi tentang panjang gelombang atau bilangan gelombang sebagai sumbu absis x dan intesitas absorpsi atau persen transmitan sebagai sumbu y. Transmitan merupakan perbandingan antara sinar yang diteruskan oleh sampel dengan sinar yang diserap oleh sampel. Sinar inframerah memiliki serapan pada bilangan gelombang 4000 cm-1 sampai 400 cm -1 dari spektrum gelombang elektromagnetik. Inframerah jauh pada bilangan
gelombang berbanding terbalik terhadap frekuensi dan energi. Bilangan gelombang adalah kebalikan dari panjang gelombang. Semakin besar bilangan gelombang semakin tinggi frekuensi gelombang, sehingga menyebabkan semakin tinggi frekuensi penyerapan pada ikatan. Tabel 2.1 dibawah ini memberikan data karakteristik serapan IR gugus fungsi (Bruice, 2004; Silverstein et al., 2005).
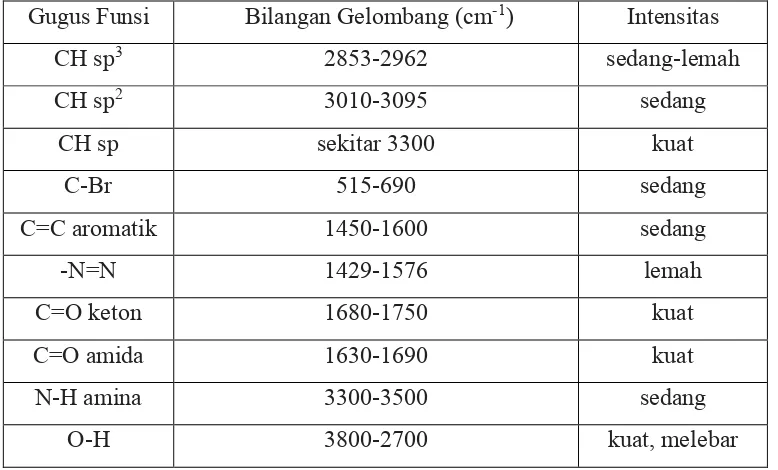
Tabel 2.1 Karakteristik serapan IR gugus fungsi
Gugus Funsi Bilangan Gelombang (cm-1) Intensitas
CH sp3 2853-2962 sedang-lemah
CH sp2 3010-3095 sedang
CH sp sekitar 3300 kuat
C-Br 515-690 sedang
C=C aromatik 1450-1600 sedang
-N=N 1429-1576 lemah
C=O keton 1680-1750 kuat
C=O amida 1630-1690 kuat
N-H amina 3300-3500 sedang
O-H 3800-2700 kuat, melebar
2.5.2 Identifikasi Hasil Sintesis dengan Spektroskopi Resonansi Magnetik Inti
melepaskan foton atau energi. Foton atau energi ditangkap oleh detektor dan diubah menjadi sebuah spektrum (Jacobsen, 2007).
Spektroskopi NMR yang umum digunakan adalah spektroskopi 1H dan 13C NMR. Spektrum NMR berisi informasi tentang pergeseran kimia (chemical shift) yang merupakan perbedaan penyerapan radiasi gelombang radio antara proton atau karbon dengan senyawa pembanding tetrametilsilan (TMS) yang mengakibatkan perbedaan posisi dari proton maupun karbon. Senyawa pembanding yang umum digunakan adalah tetrametilsilan atau (TMS). TMS sulit bereaksi (inert), mudah menguap pada suhu 27 °C, mudah larut dalam pelarut organik, dan memberikan signal singlet tajam. TMS secara umum memiliki proton yang lebih terlindungi (shielding) dari pada proton lain dari senyawa organik, sehingga signal TMS berada pada posisi sebelah kanan spektrum NMR (upfield). Proton yang tidak terlindungi (deshielding) mimiliki signal yang berada di sebelah kiri dari TMS (downfield) (Balci, 2005)
Spektroskopi 1H NMR memberikan informasi tentang jumlah atom hidrogen, jenis atom hidrogen, pembelahan spin-spin, dan pergeseran kimia. Pembelahan spin-spin merupakan akibat dari interaksi spin proton dengan proton tetangga dalam satu lingkungan kimia. Pembelahan dapat mengikuti aturan n+1. Puncak singlet menujukkan proton tersebut tidak memiliki proton tetangga (n=0), dan puncak doublet menunjukkan proton tersebut memiliki proton tetangga satu (n=1). Puncak triplet, multiplet dan seterusnya menujukkan bahwa proton tersebut memiliki tetangga lebih dari 1 (n=2, n=3, dan seterusnya). Intensitas puncak pada spektrum NMR tersebut mengikuti aturan segitiga Pascal dimana puncak doublet memiliki perbandingan 1:1 untuk masing-masing puncak, puncak triplet 1:2:1, puncak kuartet 1:3:3:1, dan seterusnya (Silverstein et al., 2005).
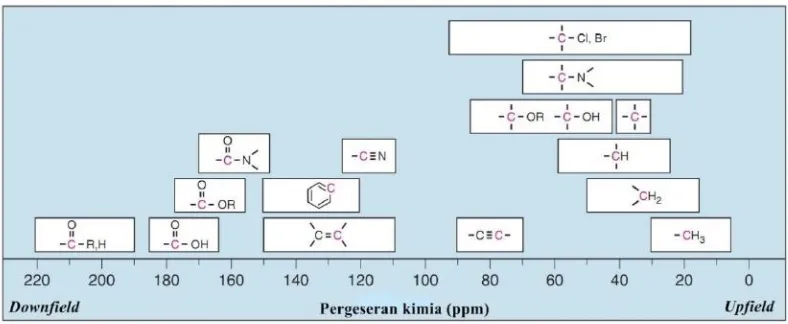
2.2 dan 0-220 ppm untuk 13C NMR sebagaimana dapat dilihat pada Gambar 2.3 (Hoffman, 2004).
Gambar 2.2 Data pergeseran kimia dalam 1H NMR
Gambar 2.3 Data pergeseran kimia dalam 13C NMR 2.5.3 Identifikasi Hasil Sintesis dengan Spektroskopi Massa
horizontal) memberikan informasi tentang massa ion molekul per muatan (m/z) dan pada sumbu y (garis vertikal) memberikan informasi tentang kelimpahan masing-masing ion-ion (abundance) (Silverstein et al., 2005; Solomons dan Fryhle, 2011).
Electrospray ionization (ESI) merupakan salah satu jenis ionisasi pada spectrometer massa. ESI pertama kali dideskripsikan oleh Zeleny pada tahun 1917 sebagai energi potensial listrik yang diterapkan pada pipa kapiler untuk membuat pelarut menjadi tetesan kecil. Penggunaan ESI dengan spektroskopi massa pertama kali dilaporkan oleh Yamashita dan Fenn serta Aleksandrov et al. pada pertengahan tahun 1980. Keuntungan dari ESI adalah dapat dilaksanakan pada tekanan atmosfir, mudah dihubungkan dengan LC atau HPLC untuk molekul dengan berat molekul yang besar dan tidak mudah menguap. Peralatan dasar ESI terdiri dari jarum semprot dengan energi potensial listrik 4-5 kV, ruang desolvasi berupa panas atau berisi udara dan penghubung vakum. Cara kerja spektroskopi massa ESI adalah sampel memasuki sumber ion yang dilingkupi dengan aliran gas nitrogen (nebulizing gas) dan diubah menjadi tetesan berukuran mikro di bawah medan listrik yang tinggi sampai membentuk aerosol yang bermuatan (taylor cone). Aerosol mengalami desolvasi oleh gas pengering berupa gas nitrogen atau panas sampai terbentuk ion bermuatan positif yang selanjutnya mengalami pemisahan berdasarkan rasio massa terhadap muatan (m/z), dan di konversi menjadi spektrum massa oleh detektor. Spektrum massa yang dihasilkan oleh ESI-MS memiliki pola fragmentasi yang sedikit dengan bentuk spektrum yang sederhana. Puncak massa pada spectrum ESI tidak selalu sebagai puncak ion molekul, sebaliknya dalam bentuk ion pseudomolekular seperti M+H, M+Na, M+K, M+Li dan lain-lain. Puncak ion molekul dalam bentuk M+H menunjukkan bahwa M merupakan puncak dari ion molekul ditambah dengan massa atom hidrogen (de Hoffmann dan Stroobant, 2007; Kazakevich dan LoBrutto, 2007).
BAB III
METODOLOGI PENELITIAN
3.1 Alat dan Bahan
3.1.1 Alat
Penelitian menggunakan peralatan laboratorium berupa gelas piala, erlenmeyer, corong, labu alas bundar, labu leher dua, labu leher tiga, pipet tetes, pipet volume, pro pipet, pipet mikro, pengaduk, kertas whatman no. 41, magnetic stirrer, rotatory evaporator, plat KLT, alat refluks, alat ukur titik leleh melting point apparatus Fischer John, neraca analitik, kaca arloji, termometer, pipa kapiler, bejana KLT, lampu UV dengan λ 254 dan 366 nm, corong, corong pisah, spektrometer massa Waters LCT Premier XE, spektrometer NMR Agilent 500 MHz untuk 1H NMR dan 125 MHz untuk 13C.
3.1.2 Bahan
10 menit pada suhu kamar. Campuran selanjutnya ditambahkan benzilbromida (13) (0,065 gram; 0,38 mmol) tetes demi tetes, dan diaduk lebih lanjut pada suhu kamar selama 22 jam (reaksi yang berjalan dipantau dengan KLT). Hasil reaksi ditambah air garam dingin (25 mL) setelah reaksi berjalan tuntas, dan diekstrak dengan diklorometana (3x20 mL). Fasa organik yang diperoleh digabung, dicuci dengan aquades, dikeringkan dengan magnesium sulfat heptahidrat, dan diuapkan dalam rotary evaporator. Hasil pemurnian diuji kemurniannya dengan KLT dan titik leleh. Hasil sintesis yang telah murni ditimbang, dan diidentifikasi dengan spektrometer MS, dan NMR.
3.2.2 Sintesis N-4-Bromobenzil-5,7-dibromosatin (12c)
Sintesis N-4-bromobenzil-5,7-dibromosatin (12c) dilakukan dengan prosedur sintesis N-benzil-5,7-dibromosatin (12b). Larutan 5,7-dibromoisatin (12a) (0,046 gram; 0,15 mmol) dalam pelarut DMF anhidrat (10 mL), ditambahkan natrium hidrida (0,007 gram; 0,30 mmol) dan diaduk selama 10 menit pada suhu kamar. 4-Bromobenzilbromida (14) (0,0375 gram; 0,15 mmol) selanjutnya ditambahkan tetes demi tetes, dan campuran diaduk pada suhu kamar selama 24 jam. Reaksi yang berjalan dipantau dengan KLT. Campuran hasil reaksi ditambah air garam dingin (25 mL) setelah reaksi berjalan tuntas, dan diekstrak dengan diklorometana (3x20 mL). Fasa organik yang diperoleh digabung, dicuci dengan aquades, dikeringkan dengan magnesium sulfat heptahidrat, dan diuapkan dalam rotary evaporator. Hasil pemurnian diuji dengan KLT dan titik leleh. Hasil sintesis yang telah murni ditimbang dan diidentifikasi dengan spektrometer MS, dan NMR. 3.2.3 Sintesis 2-Isonikotinohidrazon-5,7-dibromoisatin (11a)
dicuci dengan etanol dingin dan dikeringkan dalam desikator. Hasil sintesis diuji kemurnian hanya dengan KLT dan pengukuran titik leleh.Hasil sintesis yang telah murni ditimbang, dan diidentifikasi dengan spektrometer MS dan NMR.
3.2.4 Sintesis 2-Isonikotinohidrazon-3-(N-benzil)-5,7-dibromoisatin (11b) Sintesis 2-isonikotinohidrazon-3-(N-benzil)-5,7-dibromoisatin (11b) dilakukan dengan mengikuti prosedur sintesis 2-isonikotinohidrazon-5,7-dibromoisatin (11a). Larutan N-benzil-5,7-dibromoisatin (12b) (0,040 gram; 0,1 mmol) dan isoniazid (1) (0,027 gram; 0,2 mmol) dalam etanol (25 mL) ditambahkan katalis asam sulfat pekat (1 tetes), kemudian direfluks selama 30 menit. Reaksi yang berlangsung dipantau dengan KLT. Hasil reaksi didinginkan setelah reaksi berlangsung tuntas dan diuapkan dalam rotatory evaporator. Hasil reaksi dicuci dengan etanol dingin dan dikeringkan dalam desikator. Hasil sintesis diuji kemurnian hanya dengan KLT dan pengukuran titik leleh.Hasil sintesis yang telah murni ditimbang, dan diidentifikasi dengan spektrometer MS dan NMR. 3.2.5 Sintesis 2-Isonikotinohidrazon-3-(N-4-bromobenzil)-5,7-dibromoisatin
(11c)
3.2.6 Pengujian Hasil Sintesis (11a-c) terhadap M. tuberculosis Secara in vitro
Senyawa hasil sintesis (11a-c) masing-masing disiapkan sebagai larutan stock dengan kosentrasi 10.000 ppm dalam DMSO. Larutan senyawa uji kemudian diencerkan secara berseri dengan kosentrasi 500, 125, dan 31,25 ppm dan dimasukkan dalam tabung screw cap 3 mL. Beberapa tabung screw cap 3 mL disiapkan sebagai senyawa kontrol, kontrol positif (+), kontrol media, kontrol pelarut, dan kontrol antibiotik.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Sintesis N-Benzil-5,7-dibromosatin (12b)
Hasil sintesis selanjutnya diuji kemurniannya dengan KLT (Gambar 4.2) yang menunjukkan bahwa padatan hasil reaksi merupakan senyawa murni, yang ditandai dengan noda tunggal pada masing-masing plat KLT. Uji kemurnian dengan uji titik leleh menunjukkan rentang titik leleh sebesar 85-86 °C yang memperkuat hasil uji kemurnian dengan KLT bahwa hasil sintesis merupakan senyawa murni. Senyawa murni memiliki perbedaan titik leleh sebesar ± 1 °C (Juwita, 2008).
Gambar 4.2 KLT N-benzil-5,7-dibromoisatin (12b) hasil sintesis
Identifikasi padatan hasil sintesis dengan spektrometer NMR (dalam pelarut DMSO-d6) memberikan spektrum 1H-NMR sebagaimana dapat dilihat pada Gambar 4.3, yang sesuai dengan struktur N-benzil-5,7-dibromoisatin (12b). Spektrum 1H-NMR dengan jelas menunjukan sinyal singlet pada pergeseran kimia δ 5,21 ppm yang merupakan sinyaal dua proton gugus metilena yang menunjukkan bahwa gugus benzil telah terikat pada 5,7-dibromoisatin. Spektrum juga menunjukkan dua sinyal singlet pada pergeseran kimia (δ) 7,75 dan 7,95 ppm yang merupakan sinyal dari dua proton unit 5,7-dibromoisatin (12a). Sinyal multiplet pada δ 7,21-7,34 ppm merupakan sinyal dari proton aromatik gugus benzil.
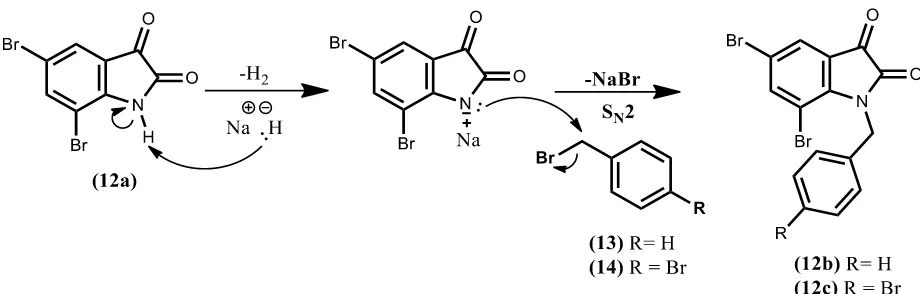
Reaksi 5,7-dibromoisatin (12a) (0,058 gram; 0,19 mmol), natrium hidrida (0,010 gram; 0,38 mmol), dan benzil bromida (13) (0,065 gram; 0,38 mmol) dalam pelarut DMF (15 mL) diperoleh N-benzil-5,7-dibromoisatin (12b) berupa padatan merah dengan massa 0,071 gram atau dengan rendemen 94% (perhitungan rendemen dapat dilihat pada lampiran). Mekanisme pembentukan N-benzil-5,7-dibromoisatin (12b) disarankan berlangsung sebagaimana dapat dilihat pada Gambar 4.4.
Keterangan eluen:
1. kloroform : etil asetat (4:1) 2. diklorometana
3. n-heksana : kloroform (1:1) 4. n-heksana : diklorometana (2:1) 5. n-heksana : kloroform (1:1)
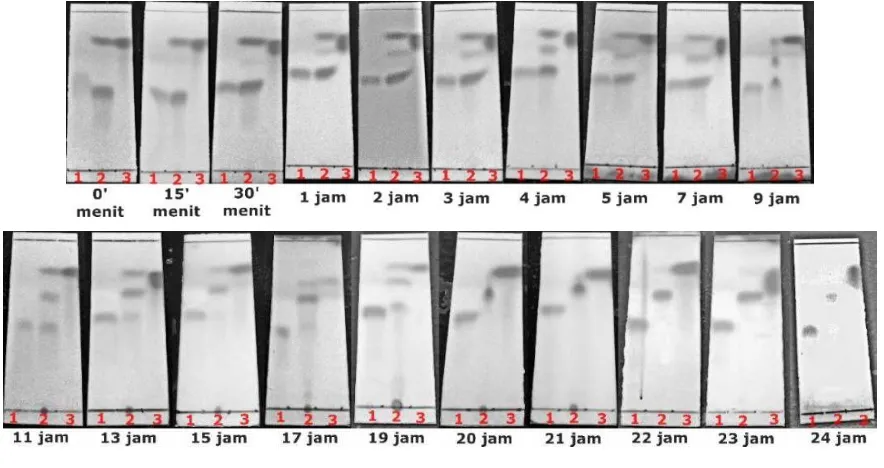
dibromoisatin (12a) dan natrium hidrida dalam DMF anhidrat pada suhu kamar selama 10 menit merupakan tahap pertama. Hasil reaksi pada tahap pertama selanjutnya ditambahkan 4-bromobenzil bromida (14), dan diaduk lebih lanjut pada suhu kamar (reaksi yang berjalan dipantau dengan KLT). Hasil pemantauan reaksi benzilasi 5,7-dibromoisatin (`12a) tahap kedua sebagaimana dapat dilihat pada Gambar 4.5 menunjukkan bahwa hasil reaksi telah terbentuk dalam waktu reaksi 15 menit yang ditandai dengan adanya noda dengan nilai Rf yang berbeda dengan nilai Rf 5,7-dibromoisatin (12a), tetapi masih terdapat 5,7-dibromoisatin (12a) yang belum bereaksi. Hasil pemantauan pada waktu reaksi berlangsung 30 menit sampai19 jam menunjukkan masih terdapat noda pereaksi yang belum bereaksi, sehingga pada jam ke 19 ditambahkan natrium hidrida. Noda hasil reaksi semakin menebal dalam kurun waktu reaksi 20-23 jam dan semakin menipisnya noda 5,7-dibromoisatin (12a), dan reaksi berjalan tuntas pada saat reaksi berlangsung 24 jam. Hasil reaksi selanjutnya ditambah air garam dingin (50 mL), dan diekstrak dengan diklorometana (5x50 mL). Fasa organik yang diperoleh digabung, dikeringkan menggunakan magnesium sulfat heptahidrat, diuapkan pelarutnya menggunakan rotatory evaporator, dan dikeringkan dalam desikator sehingga diperoleh padatan oranye sebanyak 0,068 gram.
Keterangan : 1. 5,7-dibromoisatin (12a) 2. hasil reaksi 3. 4-bromobenzil bromida (14) eluen = n-heksana : etil asetat (2:1)
Gambar 4.6 KLT N-4-bromobenzil-5,7-dibromoisatin (12c) hasil sintesis
Hasil reaksi benzilasi 5,7-dibromoisatin (12c) diuji kemurniannya dengan KLT (Gambar 4.6) yang menunjukkan bahwa padatan hasil reaksi merupakan senyawa murni, yang ditandai dengan adanya noda tunggal pada masing-masing plat KLT. Uji kemurnian dengan uji titik leleh menunjukkan rentang titik leleh sebesar 156-157 °C, yang memperkuat hasil uji kemurnian dengan KLT. Senyawa murni memiliki perbedaan titik leleh sebesar ± 1 °C (Juwita, 2008).
Identifikasi padatan hasil benzilasi 5,7-dibromoisatin (12c) menggunakan spektrometer NMR dalam pelarut DMSO-d6 memberikan spektrum 1H NMR sebagaimana dapat dilihat pada Gambar 4.7. Spektrum 1H NMR dengan jelas menunjukkan signal singlet pada pergeseran kimia (δ) 5,16 ppm yang merupakan signal dua proton gugus metilena. Proton-proton aromatik gugus 4-bromobenzil memberikan dua signal doublet pada (δ) 7,33 ppm dan 7,49 ppm. Proton-proton aromatic unit 5,7-dibromoisatin (12a) memberikan dua sinyal singlet pada (δ) 7,76 dan 7,96 ppm. Spektrum 13C NMR (Gambar 4.8) dengan jelas menunjukkan signal pada δ 55,44 ppm yang merupakan signal karbon metilena, dua karbon karbonil memberikan signal pada δ 181,01 dan 159,69 ppm. Karbon-karbon aromatik memberikan 10 sinyal pada pergeseran kimia 104,62; 116,20; 120,63; 123,39; 126,76; 129,07; 131,77; 137,16; 143,69; dan 146,61 ppm. Perbandingan
Keterangan eluen:
1. kloroform : etil asetat (4:1) 2. diklorometana
3. n-heksana : kloroform (1:1) 4. n-heksana : diklorometana (2:1) 5. n-heksana : kloroform (1:1)
Tabel 4.1 Data perbandingan 1H-NMR hasil benzilasi 7,7-dibromoisatin (12b-c)
Proton (12b) (12c)
Metilena 5,21 (s, 2H) 5,16 (S, 2H)
ArH
7,21-7,34 (m, 5H) 7,75 (s, 1H, isatin ArH) 7,79 (s, 1H, isatin ArH)
7,33 (d, 2H) 7,49 (d, 2H) 7,76 (s, 1H) 7,96 (s, 1H) .
Gambar 4. 8 Spektrum 13C-NMR N-4-bromobenzil-5,7-dibromoisatin (12c)
4.3 Sintesis 2-isonikotinohidrazon-5,7-dibromoisatin (11a)
Gambar 4.9 KLT sintesis 2-isonikotinohidrazon-5,7-dibromoisatin (11a)
Gambar 4.10 KLT uji kemurnian 2-isonikotinohidrazon-5,7-dibromoisatin (11a) hasil intesis Uji kemurnian hasil sintesis dengan KLT lebih lanjut sebagaimana dapat dilihat pada Gambar 4.11 menunjukkan bahwa padatan hasil reaksi merupakan senyawa murni, yang ditandai dengan adanya noda tunggal pada masing-masing plat KLT. Uji kemurnian dengan uji titik leleh menunjukkan rentang titik leleh sebesar 310-311 °C yang memperkuat hasil sintesis sebagai senyawa murni, senyawa murni memiliki perbedaan titik leleh sebesar ± 1 °C (Juwita, 2008).
Gambar 4.11 KLT 2-isonikotinohidrazon-5,7-dibromoisatin (11a) hasil sintesis Keterangan : 1. 5,7-dibromoisatin (12a)
2. hasil reaksi eluen = diklorometana : metanol (20:1) 3. isoniazid (1)
Keterangan : 1. 5,7-dibromoisatin (12a) 2. filtrat
3. hasil reaksi 4. isoniazid (1)
eluen = diklorometana : metanol (20:1)
Keterangan eluen:
1. n-heksana : etil asetat (2:1) 2. diklorometana
3. diklorometana : metanol (1:1) 4. metanol
5. diklorometana : metanol (1:1))
struktur 2-isonikotinohidrazon-5,7-dibromoisatin (11a). Spektrum menunjukan sinyal singlet proton NH hidrazida dan NH isatin masing-masing (δ) 11,84 ppm dan 7,71 ppm. Proton-proton aromatik cincin unit isatin memberikan sinyal singlet pada (δ) 7,72 dan 7,79 ppm. Proton-proton aromatik unit isoniazid memberikan dua signal doublet pada (δ) 8,80 dan 8,89 ppm yang masing-masing mewakili dua proton.
Identifikasi padatan hasil sintesis menggunakan spektroskopi massa resolusi tinggi (HRMS-ESI) memberikan spektrum massa (Gambar 4.12) yang menunjukkan puncak ion [M-H]- yang sekaligus sebagai puncak dasar pada m/z 420,896 sesuai untuk rumus molekul C14H7N4O2Br2, sedangkan massa ion [M-H]- hasil perhitungan sebesar 420,8935.
Gambar 4.12 Spektrum HRMS padatan hasil sintesis 2-isonikotinohidrazon-5,7-dibromoisatin (11a)
Gambar 4.14 Spektrum 1H-NMR 2-isonikotinohidrazon-5,7-dibromoisatin (11a) 4.4 Sintesis 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b)
N-benzil-5,7-pelarutnya. Padatan yang terbentuk dicuci dengan etanol dingin dan dikeringkan dalam desikator sehingga diperoleh padatan berwarna oranye sebanyak 0,041 gram.
Gambar 4.15 KLT Sintesis 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b)
Gambar 4.16 KLT 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b) hasil sintesis Uji kemurnian hasil sintesis dengan KLT sebagaimana dapat dilihat pada Gambar 4.16 menunjukkan bahwa sebagai senyawa murni, yang ditandai dengan adanya noda tunggal pada masing-masing plat KLT. Uji kemurnian dengan uji titik leleh menunjukkan rentang titik leleh 325-326 °C yang memperkuat bahwa hasil sintesis sebagai senyawa murni, senyawa murni memiliki perbedaan titik leleh sebesar ± 1 °C (Juwita, 2008).
Identifikasi padatan hasil sintesis menggunakan spektrometer NMR (dalam pelarut DMSO-d6) memberikan spektrum 1H-NMR sebagaimana dapat dilihat pada Gambar 4.18 yang sesuai dengan struktur 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b). Spektrum menunjukkan sinyal singlet pada (δ) 5,32 ppm yang merupakan sinyal dua proton dari gugus metilena. Proton-proton aromatik memberikan signal multiplet pada (δ) 7,24-7,30 (4H), multiplet pada (δ) 7,79-7,84 (2H), singlet pada pergeseran kimia (δ) 8,87 (1H), dan proton NH hidrazida pada pergeseran kimia (δ) 7,78 (1H) berupa sinyaal singlet.
Keterangan : 1. N-benzil-5,7-dibromoisatin (12b) 2. hasil reaksi
3. isoniazid (1)
eluen = diklorometana : metanol (20:1)
Keterangan eluen:
1. n-heksana : etil asetat (2:1) 2. diklorometana
3. diklorometana : metanol (1:1) 4. metanol
5. diklorometana : metanol (1:1))
sebagai puncak dasar pada m/z 512,9573 untuk molekul dengan rumus molekul C21H15N4O2Br2, yang hampir sama dengan hasil perhitungan sebesar 512,9563.
Gambar 4.17 Spektrum HRMS 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b) hasil sintesis
Gambar 4.18 Spektrum 1H-NMR 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b) 4.5 Sintesis 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c)
mencapai suhu kamar, dan pelarutnya diuapkan. Padatan yang diperoleh dicuci dengan etanol dingin (2x5mL), dan dikeringkan dalam desikator sehingga diperoleh padatan berwarna oranye kecoklatan sebanyak 0,14 gram.
Gambar 4.19 KLT sintesis 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) Uji kemurnian hasil sintesis dengan KLT sebagaimana dapat dilihat pada Gambar 4.20 menunjukkan sebagai senyawa murni, yang ditandai dengan adanya noda tunggal pada masing-masing plat KLT. Uji kemurnian dengan uji titik leleh memberikan rentang titik leleh 227-228°C yang memperkuat hasil sintesis sebagai senyawa murni. Senyawa murni memiliki perbedaan titik leleh sebesar ± 1 °C (Juwita, 2008).
Keterangan : 1. N-4-bromobenzil-5,7-dibromoisatin (12c) 2. hasil reaksi
3. isoniazid (1)
eluen = diklorometana : metanol (20:1)
Keterangan eluen:
1. n-heksana : etil asetat (2:1) 2. diklorometana
molekul yang sekaligus sebagai puncak dasar pada [M+H]+ m/z 590,8667 yang sesuai dengan massa relatif C21H14N4O2Br3 hasil perhitungan sebesar 590,8668.
Gambar 4.21 Spektrum HRMS 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) hasil sintesis
Identifikasi padatan hasil sintesis dengan analisa spektrometer NMR (dalam pelarut DMSO-d6memberikan spektrum 1H-NMR sebagaimana dapat dilihat pada Gambar 4.22 yang sama dengan struktur 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) menunjukkan sinyal singlet pada (δ) 5,27 ppm yang merupakan signal dua proton gugus metilena, proton-proton aromatik memberikan signal-signal pada (δ) 7,47 (1H), 7,76-7,82 (6H), dan 8,78-8,85 (4H). Spektrum 13C NMR (Gambar 4.23) dengan jelas menunjukkan signal karbon metilena pada δ 43,98, dan dua karbon karbonil memberikan signal pada δ 162,02 dan 164,85 ppm. Karbon-karbon aromatik pada pergeseran kimia 104,35; 116,47; 120,85; 122,00; 123,19; 124,87; 129,05; 131,94; 136,73; 138,59; 138,95; 139,61; 139,77; 150,76; dan 151,19. Data hasil analisa 13C NMR diperkuat dengan spektrum Dept 135 (Gambar 4.24) yang menunjukkan bahwa pada pergeseran kimia 43,98 ppm merupakan puncak dari karbon metilena. Karbon-karbon aromatik memberikan δ pada 122,00; 123,19; 129,05; 131,94; 138,95; 150,76; dan 151,19 ppm. Perbandingan data 1 H-NMR dari turunan isoniazid (11a-c) hasil sintesis ditampilakn pada Tabel 4.1 dibawah ini.
Tabel 4.2 Tabel perbandingan data 1H-NMR turunan isoniazid (11a-c) hasil sintesis
Proton (11a) (11b) (11c)
CH2 5,32 (s, 2H) 5,27 (s, 2H)
ArH
7,72 (s, 1H) 7,79 (s, 1H) 8,80 (d, 2H) 8,89 (d, 2H)
7,24-7,30 (m, 4H) 7,79-7,84 (m, 2H)
8,87 (s, 1H),
7,47 (1H), 7,76-7,82 (6H),
8,78-8,85 (4H) NH isatin 7,71 (s, 1H)
4.6 Pengujian Hasil Sintesis (11a-c) terhadap M. tuberculosis Secara in vitro
Pengujian anti-tuberkulosis secara in vitro dilakukan dengan metode dilusi untuk mengetahui minimum inhibitory concentration (MIC) atau kadar hambat minimum (KHM) senyawa uji. Metode dilusi dilakukan dengan cara membuat pengenceran berseri dari sampel uji yang selanjutnya ditambahkan dengan bakteri uji. Sampel uji dengan kosentrasi terkecil yang tanpa adanya pertumbuhan yang ditandai dengan warna jernih pada media uji merupakan KHM. Larutan stock senyawa uji (11a-c) dibuat dengan kosentrasi 1000 ppm disiapkan dengan melarutkan 1 mg dalam 1 mL DMSO. Senyawa uji selanjutnya diencerkan dengan kosentrasi berseri sebesar 100, 10, dan 1 ppm. Selain itu, disiapkan kontrol media, kontrol positif, rifampisin (2) disiapkan sebagai kontrol abiotik, dan DMSO sebagai kontrol pelarut.
44
Tabel 4.3 Hasil pengujian anti-tuberkular senyawa (11a-c) terhadap M. tuberkulosis
Pengujian Kontrol Kontrol Media Kontrol Positif Senyawa Uji
Pengamatan sampel
Tumbuh Tumbuh Tidak (11c) Tidak Tumbuh Tidak Tumbuh Tumbuh II Tumbuh Tidak
Tumbuh Tumbuh Tidak (11c) Tidak Tumbuh Tidak Tumbuh Tumbuh III Tumbuh Tidak
“Halaman ini sengaja dikosongkan”
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Benzilasi 5,7-dibromoisatin (12a) dengan benzil bromida (13) dan 4-bromobenzil bromida (14) masing-masing selama 22 jam dan 24 jam diperoleh benzil-5,7-dibromosatin (12b) dan N-4-bromobenzil-5,7-dibromoisatin (12c) dengan rendemen masing-masing sebesar 94% dan 91%. Turunan isoniazid baru berupa isonikotinohidrazon-5,7-dibromoisatin (11a), 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b), dan 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) masing-masing berhasil disintesis dari reaksi 5,7-dibromoisatin (12a), N-benzil-5,7-dibromosatin (12b) dan N-4-bromobenzil-5,7-dibromoisatin (12c) dengan isoniazid (1) menggunakan katalis asam sulfat. Sintesis turunan isoniazid (11a), (11b) dan (11c) masing-masing membutuhkan waktu selama 240, 30 dan 120 menit dengan rendemen masing-masing sebesar 92%, 81% dan 84%. Hasil uji boaktivitas terhadap M. tuberculosis menujukkan bahwa senyawa 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) merupakan senyawa yang paling aktif dengan nilai KHM 10 ppm.
5.2 Saran
Penelitian lanjutan untuk mengkaji bioaktivitas turunan isoniazid (11c) dengan kosentrasi yang lebih kecil, sehingga dapat diperoleh nilai KHM senyawa (11c) yang lebih maksimal.
“Halaman ini sengaja dikosongkan”
DAFTAR PUSTAKA
Aboul-Fadl, T., Abdel-Hamid, M. K., Youssef A. F. (2015) Schiff bases of indoline-2,3-dione (isatin) derivatives as efficient agents against resistant strains of Mycobacterium tuberculosis. Der Pharma Chem. 7, 217–225. Aboul-Fadl, T., Bin-Jubair F. A. S. (2010) Anti-tubercular activity of isatin
derivatives. Int. J. Res. Pharm. Sci. 1, 113–126.
Aboul-Fadl, T., Bin-Jubair, F. A. S., Aboul-Wafa O. (2010) Schiff bases of indoline-2,3-dione (isatin) derivatives and nalidixic acid carbohydrazide, synthesis, antitubercular activity and pharmacophoric model building. Eur. J. Med. Chem. 45, 4578–4586.
Aboul-Fadl, T., Mohammed, F. A.-H., Hassan E. A.-S. (2003) Synthesis, antitubercular activity and pharmacokinetic studies of some Schiff bases derived from 1-alkylisatin and isonicotinic acid hydrazide (INH). Arch. Pharm. Res. 26, 778–84.
Al-Maamari, K. A. (2013) Isatin Derivatives: Synthesis, Reactivity and Anticorrosion Properties. Thesis, University of Mohammed-V-Agdal, Rabat.
Benkendorff, K., Bremner, J. B., Davis A. R. (2001) Indole derivatives from the egg masses of Muricid molluscs. Molecules 6, 70–78.
Bruice, P. (2004) Organic Chemistry. edisi keempat., Prentice Hall International, Inc, New Jersey.
Chisholm-Burns, M. A., Wells, B. G., Schwinghammer, Terry, L. Malone, P. M., Kolesar, J. M., DiPiro J. T. (2013) Pharmacotheraphy Principles & Practice. 3rd ed., McGraw-Hill Education, New York.
Clay, C. M., Abdallah, H. M., Jordan, C., Knisley, K., Ketcha, D. M. (2012) N-alkylation of isatins utilizing KF/alumina. Arkivoc 4, 317–325.
Dixit, P. P., Patil V. J., Nair, P. S., Jain, S., Sinha, N., Arora S. K. (2006) Synthesis of 1-[3-(4-benzotriazol-1/2-yl-3-fluoro-phenyl)-2-oxo-oxazolidin-5-ylmethyl]-3-substituted-thiourea derivatives as antituberculosis agents. Eur. J. Med. Chem. 41, 423–8.
Eldehna, W., Fares, M., Abdel-Aziz, M., Abdel-Aziz H. (2015) Design, synthesis and antitubercular activity of certain nicotinic acid hydrazides. Molecules 20, 8800–8815.
Feng, L. S., Liu, M. L., Zhang, S., Chai, Y., Wang, B., Zhang, Y. Bin, Lv K., Guan, Y., Guo, H. Y., Xiao C. L. (2011) Synthesis and in vitro antimycobacterial activity of 8-OCH3 ciprofloxacin methylene and ethylene isatin derivatives. Eur. J. Med. Chem. 46, 341–348.
Gritter, R. ., Bobbit, J., Swharting A. E. (1991) Pengantar Kromatografi. Edisi Kedua. 2nd ed., ITB, Bandung.
de Hoffmann, E., Stroobant V. (2007) Mass spectrometry: Principles and applications. edisi ketiga., John Wiley & Sons, Inc, Hoboken, New Jersey.
Hostettmann, K., Hostettmann, M., Marston A. (1995) Cara Kromatografi Preparatif., ITB, Bandung.
Jacobsen, N. E. (2007) NMR Spectroscopy Explained: Simplified Theory, Applications and Examples for Organic Chemistry and Structural Biology., A John Wiley & Sons, Inc, Hoboken, New Jersey.
Johnson, E. L., Stevenson R. (1991) Dasar Kromatografi Cair., Universitas Udayana, Bandung.
Kazakevich, Y., LoBrutto R. (2007) HPLC for Pharmaceutical Scientists., John Wiley & Sons, Inc, Hoboken, New Jersey.
Kristanti, A. N. (2008) Buku Ajar Fitokimia., Airlangga University Press, Surabaya.
Kumar, S. B., Ravinder, M., Kishore, G., Jayathirtha, Rao V., Yogeeswari, P., Sriram, D. (2014) Synthesis, antitubercular and anticancer activity of new Baylis-Hillman adduct-derived N-cinnamyl-substituted isatin derivatives. Med. Chem. Res. 23, 1934–1940.
agents: A Review. Med. Chem. (Los. Angeles). 4, 417–427.
Overman, L. E., Peterson E. A. (2003) Enantioselective synthesis of (-)-idiospermuline. Tetrahedron 59, 6905–6919.
Pahlavani, E., Hadi, K., Rad N. S. (2015) A study on antitubercular and antimicrobial activity of isoniazid derivative. Zahedan J. Res. Med. Sci. 17, 7–10.
Pal, M., Sharma, N. K., Priyanka, Jha, K.K. (2011) Synthetic and biological multiplicity of isatin: a Review. J. Adv. Sci. Res. 2, 35–44.
Raviglione, M. C. (2010) Tuberculosis Fourth Edition The Essentials. edisi keempat. ed. LenfantClaude, New York.
Rehn, S. (2004) Synthesis of indole and oxindole derivatives incorporating pyrrolidino, pyrrolo or imidazolo moieties. Thesis, Karolinska University Perss.
Rohman ,A. (2007) Kimia Farmasi Analisis., Pustaka Pelajar, Yogyakarta. Schneider, E., Moore M., Castro K. G. (2005) Epidemiology of tuberculosis in
the United States. Clin Chest Med 26, 183–95, v.
Sherma, J., Fried B. (2003) Handbook of Thin-Layer Chromatography edited by. edisi ketiga., Marcel Dekker, Inc, New York.
da Silva, J. F. M., Garden, S. J., Pinto A. C. (2001) The chemistry of isatins: a review from 1975 to 1999. J. Braz. Chem. Soc. 12, 273–324.
Silverstein, R. M., Webster, F. X., Kiemle D. J. (2005) Spectrometric identification of organic compounds., John Wiley & Sons, Inc, New York.
Lippincott Williams & Wilkins, Philadelphia.
Solomons, T. W. G., Fryhle C. B. (2011) Organic Chemistry. edisi kesepuluh., John Wiley & Sons, Inc, Hoboken, New Jersey.
Tehrani, K. H. M. E., Maryam, H., Maryam, H., Kobarfard, F., Shohreh M. (2016) Synthesis and antibacterial activity of Schiff bases of 5-substituted isatins. Chinese Chem. Lett. 27, 221–225.
Vine, K. L., Locke, J. M., Ranson, M., Benkendorff, K., Pyne, S. G., Bremner, J. B. (2007a) In vitro cytotoxicity evaluation of some substituted isatin derivatives. Bioorganic Med. Chem. 15, 931–938.
Vine, K. L., Locke, J. M., Ranson, M., Pyne, S. G., Bremner J. B. (2007b) Cytotoxicity and mode of action of some novel n-alkyl-sub isatin. J. Med. Chem. 50, 5109–5117.
Vine, K. L., Matesic, L., Locke, J. M., Danielle S. (2013) Recent highlights in the development of isatin-based anticancer agents. Advance in ANticancer Agents in Medical Chemistry (254–312). Bentham Science, Sharjah UAE.
Wells, B., Dipiro, J., Schwinghammer, T., Dipiro C. (2009) Pharmacotherapy handbook., edisi ketujuh. McGraw-Hill, Inc., New York.
LAMPIRAN A
SKEMA KERJA
A.1 Prosedur Sintesis N-benzil-5,7-dibromoisatin (12b)
- dilarutkan dalam 10 mL DMF
- ditambah NaH (0,010 gram; 0,38 mmol) - diaduk pada suhu ruang selama 10 menit
- ditambah benzil bromida (13) (0,065 gram; 0,38 mmol)
- diaduk selama 22 jam (reaksi yang berjalan dipantau dengan KLT) - ditambah dengan air garam dingin (50 mL)
- diekstrak dengan diklorometana (3X20 mL)
- dikeringkan dengan MgSO4 heptahidrat - disaring
- diuapkan dengan rotatory evaporator
- diuji kemurnia dengan KLT dan titik leleh
- diidentifikasi dengan spektrometer NMR dan massa 5,7-dibromoisatin (12a) (0,058 gram; 0,19 mmol)
Residu Fasa air Fasa organik
Filtrat
A.2 Prosedur Sintesis (N-4-bromobenzil)-5,7-dibromoisatin (12c)
- dilarutkan dalam 10 mL DMF
- ditambah NaH (0,07 gram; 0,30 mmol ) - diaduk pada suhu ruang selama 10 menit
- ditambah 4-bromobenzil bromide (14) (0,0375 gram; 0,15 mmol ) - diaduk selama 24 jam (reaksi yang berjalan dipantau dengan KLT) - ditambah dengan air garam dingin (50 mL)
- diekstrak dengan diklorometana (3X20 mL)
- dikeringkan dengan MgSO4 heptahidrat - disaring
- diuapkan dengan rotatory evaporator
- diuji kemurnia dengan KLT dan titik leleh
- diidentifikasi dengan spektrometer NMR dan massa 5,7-dibromoisatin (12a) (0,046 gram; 0,15 mmol)
mmol)
Residu Fasa air Fasa organik
Filtrat
A.3 Prosedur Sintesis 2-Isonikotinohidrazon-5,7-dibromoisatin (11a)
- dilarutkan dalam 20 mL etanol - ditambah asam sulfat 1 tetes
- direfluks selama 20 menit pada suhu 78 °C
- ditambah isoniazid (1) (0,033 gram; 0,12 mmol) dalam etanol 10 mL - direfluks pada suhu 78 °C selama 4 jam (reaksi yang berjalan dipantau
dengan KLT
- didinginkan dan diuapkan pelarutnya dalam rotatory evaporator - dimurnikan dengan kromatografi kolom
- dicuci dengan etanol dingin (2x5 mL) - dikeringkan dalam desikator
- diuji kemurnian dengan KLT dan titik leleh, dan diidentifikasi dengan spektrometer IR, massa, dan NMR
- diuji antituberkulosis terhadap bakteri Mycobacterium tuberculosis H37Rv
5,7-dibromoisatin (12a) (0,036 gram; 0,12 mmol)
Hasil Sintesis
2-Isonikotinohidrazon-5,7-dibromoisatin (11a) (0,0458 gram; rendemen 91,6%)
A.4 Prosedur Sintesis 2-Isonikotinohidrazon-3-(N-benzil)-5,7-dibromoisatin (11b)
- dilarutkan dalam 20 mL etanol - ditambah asam sulfat 1 tetes
- direfluks selama 20 menit pada suhu 78 °C
- ditambah isoniazid (1) (0,027 gram; 0,2 mmol ) dalam etanol 10 mL - direfluks pada suhu 78 °C selama 30 menit (reaksi yang berjalan
dipantau dengan KLT
- didinginkan dan diuapkan pelarutnya dalam rotatory evaporator - dimurnikan dengan kromatografi kolom
- dicuci dengan etanol dingin (2x5 mL) - dikeringkan dalam desikator
- diuji kemurnian dengan KLT dan titik leleh, dan diidentifikasi dengan spektrometer IR, massa, dan NMR
- diuji antituberkulosis terhadap bakteri Mycobacterium tuberculosis H37Rv
(N-benzil)-5,7-dibromoisatin (12b) (0,040 gram; 0,1 mmol)
Hasil Sintesis
2-Isonikotinohidrazon-3-(N-benzil)-5,7-dibromoisatin (11b) (0,041 gram; rendemen 81%)
A.5 Prosedur Sintesis 2-Isonikotinohidrazon-3-5-(N-4-bromobenzil)-5,7-dibromoisatin (11c)
- dilarutkan dalam 20 mL etanol - ditambah asam sulfat 1 tetes
- direfluks selama 20 menit pada suhu 78 °C
- ditambah isoniazid (1) (0,023 gram; 0,17 mmol ) dalam etanol 10 mL - direfluks pada suhu 78 °C selama 2 jam (reaksi yang berjalan dipantau
dengan KLT
- didinginkan dan diuapkan pelarutnya dalam rotatory evaporator - dimurnikan dengan kromatografi kolom
- dicuci dengan etanol dingin (2x5 mL) - dikeringkan dalam desikator
- diuji kemurnian dengan KLT dan titik leleh, dan diidentifikasi dengan spektrometer IR, massa, dan NMR
- diuji antituberkulosis terhadap bakteri Mycobacterium tuberculosis H37Rv
(N-4-bromobenzil)-5,7-dibromoisatin (12c) (0,040 gram; 0,085 mmol)
Hasil Sintesis
2-Isonikotinohidrazon-3-(N-4-bromobenzil)-5,7-dibromoisatin (11c) (0,042 gram; rendemen 84,4)
A.6 Pengujian Hasil Sintesis (11-c) terhadap M. tuberculosis Secara in vitro
- disiapkan sebagai stock dengan kosentrasi 10.000 ppm dalam DMSO. - diencerkan secara berseri dengan kosentrasi 500, 125, dan 31,25 ppm
dan dimasukkan dalam tabung screw cap 3 mL
- disiapkan beberapa tabung screw cap 3 mL sebagai senyawa kontrol, kontrol positif (+), kontrol media, kontrol pelarut, dan kontrol antibiotik.
- dibuat suspensi bakteri MT 108 CFU/mL dengan cara 1 ose bakteri MT dimasukkan ke dalam tabung crew cap yang berisi 10 glassbeads dan 2 tetes Twen 0,05% steril serta akuades steril
- disiapkan suspensi bakteri MT 106 CFU/mL dalam 80 mL MB DS untuk masing-masing pengujian dibuat dengan cara diambil 0,8 mL suspensi bakteri 108 CFU/mL
- dimasukkan ke dalam media MB DS
- diinkubasi suspensi bakteri 106 CFU/mL yang berisi senyawa uji, kontrol positif, kontrol pelarut, dan kontrol antibiotik
- diinokulasi pada suhu 37 °C selama 10 hari yang selanjutnya pada suhu 37 °C selama 3-4 minggu
- diamati pertumbuhannya
- dilakukan pengulangan tiga kali Senyawa hasil sintesis (11a-c)
LAMPIRAN B
PERHITUNGAN RENDEMEN
B.1. Perhitungan Rendemen Hasil N-benzil-5,7-Dibromoisatin (12b)
Mol N-benzil-5,7-dibromoisatin (12b) teoritis yang terbentuk = 0,19 mmol Massa N-benzil-5,7-dibromoisatin (12b) teoritis yang terbentuk
= 0,19 mmol x 395,0455 g/mol = 0,075 gram Rendemen yang diperoleh = 𝑀𝑎𝑠𝑠𝑎 𝑝𝑟𝑜𝑑𝑢𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑝𝑒𝑟𝑜𝑙𝑒ℎ 𝑀𝑎𝑠𝑠𝑎 𝑡𝑒𝑜𝑟𝑖 𝑦𝑎𝑛𝑔 𝑑𝑖𝑝𝑒𝑟𝑜𝑙𝑒ℎ
B.2. Perhitungan Rendemen Hasil N-4-bromobenzil-5,7-Dibromoisatin (12c)
Mol N-4-bromobenzil-5,7-dibromoisatin (12c) teoritis yang terbentuk = 0,15 mmol
Massa N-4-bromobenzil-5,7-dibromoisatin (12c) teoritis yang terbentuk = 0,15 mmol x 473,9415 g/mol = 0,075 gram
Rendemen yang diperoleh = 𝑀𝑎𝑠𝑠𝑎 𝑝𝑟𝑜𝑑𝑢𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑝𝑒𝑟𝑜𝑙𝑒ℎ 𝑀𝑎𝑠𝑠𝑎 𝑡𝑒𝑜𝑟𝑖 𝑦𝑎𝑛𝑔 𝑑𝑖𝑝𝑒𝑟𝑜𝑙𝑒ℎ = 0,068 𝑔𝑟𝑎𝑚 0,075 𝑔𝑟𝑎𝑚 = 91%
Mol 2-isonikotinohidrazon-5,7-dibromoisatin (11a) teoritis yang terbentuk = 0,12 mmol
Massa 2-isonikotinohidrazon-5,7-dibromoisatin (11a) teoritis yang terbentuk = 0,12 mmol x 424,0469 g/mol = 0,050 gram
Mol 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b) teoritis yang terbentuk
= 0,1 mmol
Massa 2-isonikotinohidrazon-(N-benzil)-5,7-dibromoisatin (11b) teoritis yang terbentuk = 0,1 mmol x 511,9489 g/mol = 0,05 gram
Rendemen yang diperoleh = 𝑀𝑎𝑠𝑠𝑎 𝑝𝑟𝑜𝑑𝑢𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑝𝑒𝑟𝑜𝑙𝑒ℎ 𝑀𝑎𝑠𝑠𝑎 𝑡𝑒𝑜𝑟𝑖 𝑦𝑎𝑛𝑔 𝑑𝑖𝑝𝑒𝑟𝑜𝑙𝑒ℎ = 0,041 𝑔𝑟𝑎𝑚 0,050 𝑔𝑟𝑎𝑚 = 81%
Mol 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) teoritis yang terbentuk = 0,085 mmol
Massa 2-isonikotinohidrazon-(N-4-bromobenzil)-5,7-dibromoisatin (11c) teoritis yang terbentuk = 0,085 mmol x 589,8589 g/mol = 0,050 gram
BIODATA PENULIS
Penulis dilahirkan di Malang, 10 Juni 1993 dengan nama lengkap M. Riza Ghulam Fahmi. Pendidikan formal yang telah ditempuh oleh penulis, yaitu di SDNU Bagorejo 1 Jember, SMPN 3 Peterongan Jombang, dan SMA Darul Ulum 1 Peterongan Jombang. Setelah lulus dari SMA Darul Ulum 1 Peterongan Jombang, penulis melanjutkan pendidikan di jurusan Kimia ITS Surabaya pada tahun 2011 dan terdaftar dengan NRP. 1411 100 127. Di Jurusan Kimia ini, Penulis mengambil bidang minat Kimia Organik dibawah bimbingan Prof. Mardi Santoso, Ph.D dan Arif Fadlan M.Si. Penulis pernah aktif dalam kegiatan sosial yang diadakan oleh Himpunan Mahasiswa Kimia (HIMKA), salah satunya yaitu HIMKA FOR NATION. Latihan Keterampilan Manajemen Mahasiswa (LKMM) yang pernah diikuti penulis selama kuliah di ITS adalah Pra-Tingkat Dasar (Pra-TD). Selain Latihan Keterampilan Manajemen Mahasiswa Pra-Tingkat Dasar (LKMM Pra-TD), penulis juga pernah mengikuti pelatihan Keamanan dan Keselamatan Kerja Laboratorium yang diadakan oleh Jurusan Kimia. Penulis diterima di program magister kimia ITS pada tahun 2015 dengan NRP 1415201006 dan menyelesaikan pendidikan magister selama 24 bulan. Penulis dapat dihubungi melalui
No HP : 085733133017