commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 3
BAB II
LANDASAN TEORI
II.1 Tinjauan Pustaka II.1.a Tulang
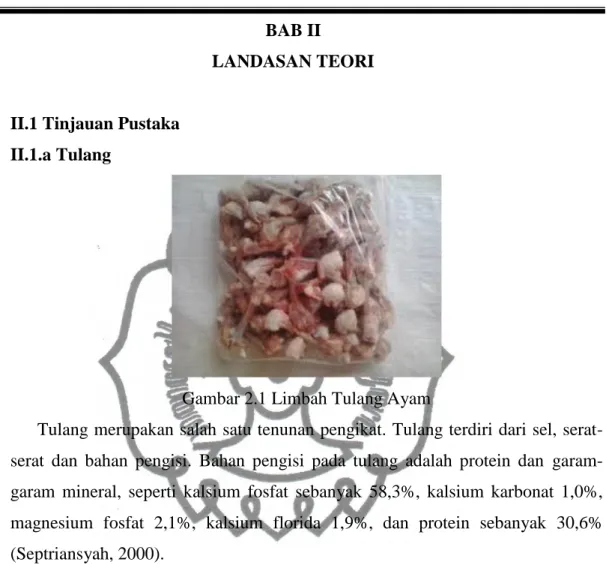
Gambar 2.1 Limbah Tulang Ayam
Tulang merupakan salah satu tenunan pengikat. Tulang terdiri dari sel, serat-serat dan bahan pengisi. Bahan pengisi pada tulang adalah protein dan garam-garam mineral, seperti kalsium fosfat sebanyak 58,3%, kalsium karbonat 1,0%, magnesium fosfat 2,1%, kalsium florida 1,9%, dan protein sebanyak 30,6% (Septriansyah, 2000).
Tulang mengandung kurang lebih 50% air dan 15% sumsum merah dan kuning. Sumsum tulang teridiri dari lemak sebesar 96%. Tulang yang telah diambil lemaknya terdiri dari bahan organik dan garam-garam anorganik dalam perbandingan 1:2. Penghilangan zat organik oleh panas tidak menyebabkan perubahan struktur tulang secara keseluruhan, tetapi akan mengurangi berat tulang (Septriansyah, 2000). Terdapat dua jenis protein dalam tulang, yaitu protein kolagen dan non kolagen. Kandungan kolagen dalam tulang lebih besar dibandingkan non kolagen. Protein kolagen memiliki nilai jual tinggi yang mana digunakan untuk pembuatan kosmetik, bahan dasar pembuatan gelatin dan perekat (Aini, 2011).
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 4
Pemanfaatan protein yang terkandung dalam tulang ayam dapat dilakukan dengan cara ekstraksi. Ekstraksi protein dari tulang ayam merupakan salah satu usaha pemanfaatan limbah industri yang bergerak di bidang pangan. Ekstraksi protein ini diharapkan dapat meningkatkan nilai ekonomis tulang ayam. Ekstraksi adalah proses pemisahan suatu zat dari campurannya dengan menggunakan solvent sebagai tenaga pemisah. Ektraksi protein dari tulang ayam dilakukan melalui padat-cair. Ekstraksi padat cair adalah ekstraksi dimana solute yang akan dipisahkan terdapat dalam padatan menggunakan pelarut yang berupa cairan (Aini, 2010).
Tulang dibedakan menjadi dua yaitu tulang rawan dan tulang keras (tulang sejati) :
Tulang Rawan
Tulang rawan adalah tulang yang berserabut tebal dan matriks yang elastis. Tulang rawan memiliki kandungan kolagen yang tinggi sehingga bersifat kuat dan lentur. Tulang rawan tidak mempunyai saraf dan pembuluh darah. Tulang rawan banyak ditemukan pada bagian ujung tulang keras, hidung, telinga, dan vertebrae (ruas-ruas tulang belakang).
Tulang Sejati
Tulang sejati adalah tulang yang telah mengalami osifikasi (pematangan tulang) sehingga strukturnya lebih keras. Dalam matriksnya kandungan kolagen sangat sedikit, sedangkan bahan anorganik lainnya seperti kalsium, fosfor, bikarbonat, sirat, Mg, Na, dan K sangat banyak didapati.
Komposisi kimia dan fisik tulang dapat dilihat pada Tabel 2.1 dan komposisi tulang ayam kerangka binatang dapat dilihat pada Tabel 2.2
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 5
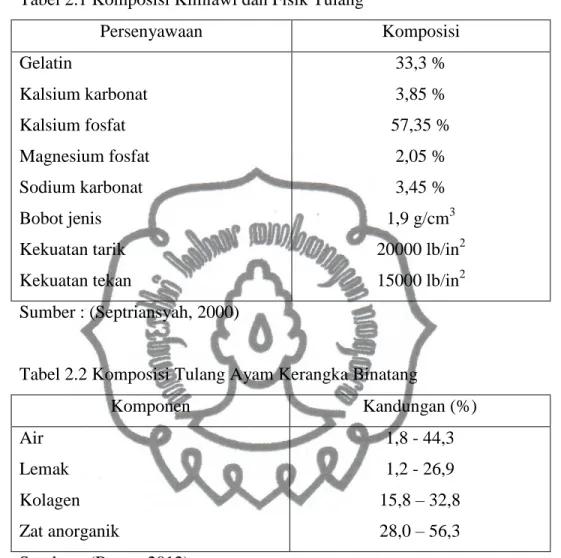
Tabel 2.1 Komposisi Kimiawi dan Fisik Tulang
Persenyawaan Komposisi Gelatin Kalsium karbonat Kalsium fosfat Magnesium fosfat Sodium karbonat Bobot jenis Kekuatan tarik Kekuatan tekan 33,3 % 3,85 % 57,35 % 2,05 % 3,45 % 1,9 g/cm3 20000 lb/in2 15000 lb/in2 Sumber : (Septriansyah, 2000)
Tabel 2.2 Komposisi Tulang Ayam Kerangka Binatang
Komponen Kandungan (%) Air Lemak Kolagen Zat anorganik 1,8 - 44,3 1,2 - 26,9 15,8 – 32,8 28,0 – 56,3 Sumber : (Retno, 2012) II.1.b Kolagen
Bahan baku utama dari gelatin adalah senyawa kolagen. Kolagen ini banyak terdapat pada urat, kulit, tulang rawan dan tulang keras pada hewan. Kolagen merupakan komponen serat utama dari jaringan ikat protein yang paling melimpah yaitu mencapai 20-25% dari total protein (Septriansyah, 2000).
Jaringan kolagen tersusun atas fibril kolagen yang nampak seperti garis-garis melintang. Fibril ini terorganisasi sesuai dengan sistem biologis jaringan tersebut. Kolagen merupakan protein yang mengandung 35% glisin dan sekitar
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 6
11% alanin serta kandungan prolin yang cukup tinggi. Komposisi inilah yang menjadi dasar untuk produksi gelatin (Septriansyah, 2000).
Molekul kolagen tersusun dari kira-kira dua puluh asam amino yang memiliki bentuk agak berbeda bergantungan pada sumber bahan bakunya. Asam amino glisin, prolin dan hidrosiprolin merupakan asam amino utama kolagen (Miskah, 2010).
Molekul dasar pembentukan kolagen disebut tropokolagen yang mempunyai struktur batang dengan BM 300.000, dimana di dalamnya terdapat tiga rantai polipeptida yang sama panjang, bersama-sama membentuk struktur heliks. Tropokolagen akan terdenaturalisasi oleh pemanasan atau perlakuan dengan zat seperti asam, basa, urea, dan potassium permanganate (Miskah, 2010).
Pemanasan kolagen secara bertahap akan menyebabkan struktur rusak dan rantai-rantai akan terpisah. Bobot molekul, bentuk dan konfirmasi larutan kolagen sensitif terhadap perubahan temperatur yang dapat menghancurkan makromolekulnya. Kolagen murni sangat sensitif terhadap reaksi enzim dan kimia. Perlakuan alkali menyebabkan kolagen mengembang dan menyebar. Disamping pelarut alkali, kolagen juga larut dalam pelarut asam (Septriansyah, 2000).
Sifat-sifat kolagen antara lain tidak larut dalam larutan asam maupun alkali, tahan terhadap enzim tripsin dan chimotripsin. Kolagen juga dapat mengkerut apabila dipanaskan. Apabila pemanasan berada pada suhu pengkerutannya yaitu
520C maka kolagen akan berubah menjadi gelatin (Retno, 2012).
II.1.c Gelatin
Gelatin adalah salah satu hidrokoloid yang dapat digunakan sebagai gelling,
bahan pengental (thickner) atau penstabil. Gelatin berbeda dengan hidrokoloid
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 7
pektin, sedangkan gelatin merupakan protein mudah dicerna, mengandung semua asam-asam amino essensial kecuali triptofan (Septriansyah, 2000).
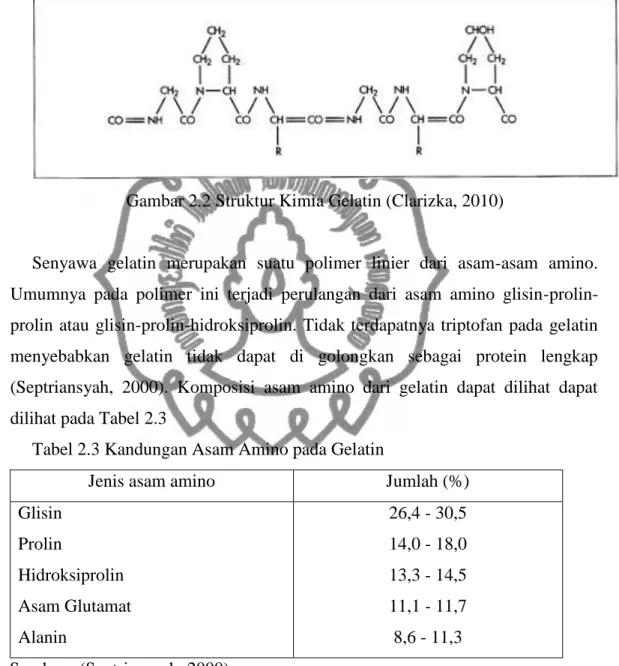
Gambar 2.2 Struktur Kimia Gelatin (Clarizka, 2010)
Senyawa gelatin merupakan suatu polimer linier dari asam-asam amino. Umumnya pada polimer ini terjadi perulangan dari asam amino glisin-prolin-prolin atau glisin-glisin-prolin-prolin-hidroksiglisin-prolin-prolin. Tidak terdapatnya triptofan pada gelatin menyebabkan gelatin tidak dapat di golongkan sebagai protein lengkap (Septriansyah, 2000). Komposisi asam amino dari gelatin dapat dilihat dapat dilihat pada Tabel 2.3
Tabel 2.3 Kandungan Asam Amino pada Gelatin
Jenis asam amino Jumlah (%)
Glisin Prolin Hidroksiprolin Asam Glutamat Alanin 26,4 - 30,5 14,0 - 18,0 13,3 - 14,5 11,1 - 11,7 8,6 - 11,3 Sumber : (Septriansyah, 2000)
Gelatin digunakan dalam pengolahan pangan lebih disebabkan sifat kimia dan fisika gelatin yang khas dari pada nilai gizinya sebagai sumber protein. Dalam indutstri pangan gelatin berfungsi sebagai pembentuk gel, pemantap emulsi, pengental, penjernih, pengikat air, pelapis dan pengemulsi. Gelatin jika direndam
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 8
dalam air akan mengembang dan menjadi lunak berangsur-angsur menyerap air
5-10 kali bobotnya. Gelatin dengan mudah larut pada suhu 71,10C dan cenderung
membentuk gel pada suhu 48,80C. Gelatin mudah larut dalam gliserol, manitol,
sorbitol dan propile, tetapi tidak larut dalam alkohol, aseton dan pelarut nonpolar lainnya (Septriansyah, 2000).
Mekanisme rekasi pembentukan gelatin :
C102H149N31O38 + H2O C102 H151N31O39
Kolagen Gelatin
Faktor-faktor yang mempengaruhi pembentukan gelatin antara lain suhu hidrolisa. Semakin tinggi suhu, maka reaksi akan semakin cepat, tetapi warna gelatin yang dihasilkan semakin gelap karena protein dalam kolagen rusak.
Apabila dijalankan pada suhu lebih dari 950C. maka akan terjadi pemecahan
gelatin. Menurut persamaan Archenius: k=A.e-RT, apabila suhu diperbesar maka nilai k juga akan semakin besar sehingga konversi besar. Jika suhu melebihi
950C, gelatin yang sudah terbentuk mengalami pemecahan menjadi semiglutin
dan hemikolin (Retno, 2012). Reaksinya adalah sebagai berikut :
C102 H151N31O39 + H2O C55 H83N17O22 + C47 H70N14O18
Gelatin Air Semiglutin Hemikolin
Gelatin terbagi menjadi dua tipe berdasarkan perbedaan proses pengolahannya yaitu tipe A dan tipe B dalam pembuatan gelatin tipe A bahan baku diberi perlakuan perendaman dalam larutan asam sehingga proses ini dikenal dengan sebutan proses asam. Sedangkan dalam pembuatan gelatin tipe B, perlakuan yang diaplikasikan adalah perlakuan basa, proses ini disebut sebagai proses alkali (Hariyanto dan Sambudi, 2011).
Bahan baku yang biasanya digunakan pada proses asam adalah tulang dan kulit babi, sedangkan bahan baku yang biasa digunakan pada proses basa adalah
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 9
tulang dan kulit jangat sapi. Secara ekonomis, proses asam lebih disukai dibandingkan proses basa hal ini dikarenakan perendaman yang dilakukan dalam proses asam relatif lebih singkat dibandingkan proses basa (Hariyanto dan Sambudi, 2011). Hidrolisis protein dengan menggunakan alkali dapat menyebabkan degradasi protein, namun tergantung dosis, konsentrasi, suhu dan lama perlakuan. (Mayasaroh, Rusmana, dan Wiradimadja, 2012).
Pada tahap ini perendaman dapat dilakukan dengan larutan asam organik seperti asam asetat, sitrat, fumarat, askorbat, malat suksinat, tartarat dan asam lainnya yang aman. Sedangkan asam anorganik yang biasa digunakan adalah asam klorida, fosfat, dan sulfat. Jenis pelarut alkali yang umum digunakan adalah sodium karbonat, sodium hidroksida, potassium karbonat dan potassium hidroksida (Hariyanto dan Sambudi, 2011).
Nilai rendemen dari suatu pengolahan bahan merupakan parameter yang penting sebagai dasar perhitungan analisis finansial, memperkirakan jumlah bahan baku untuk memproduksi produk dalam jumlah tertentu, dan mengetahui tingkat efisiensi dari suatu proses pengolahan (Fulanah, 2012).
Sifat fisik secara umum dan kandungan unsur-unsur mineral tertentu dalam gelatin dapat digunakan untuk menilai mutu gelatin. Standar mutu gelatin menurut SNI dapat dilihat pada Tabel 2.4 (Septriansyah, 2000).
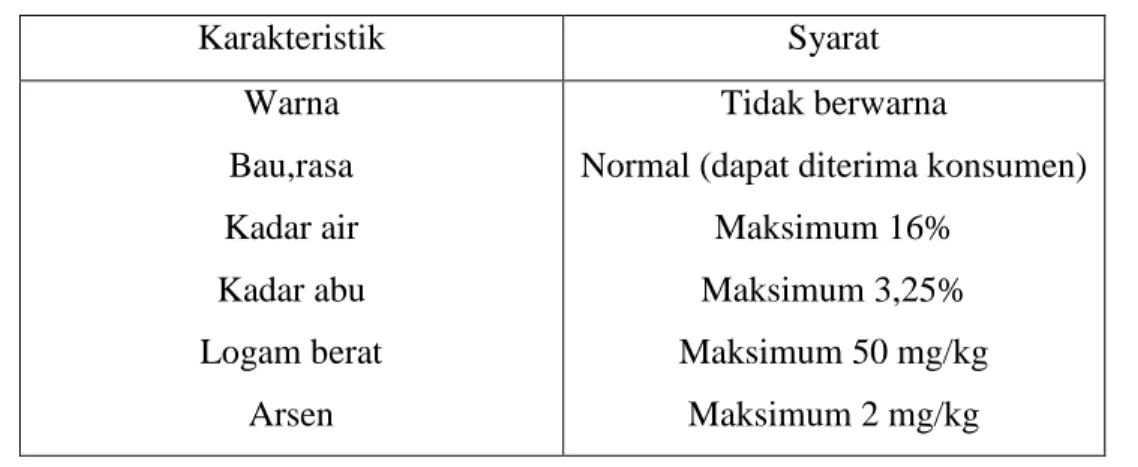
Tabel 2.4 Standar Mutu Gelatin (SNI 06-3735, 1995)
Karakteristik Syarat Warna Bau,rasa Kadar air Kadar abu Logam berat Arsen Tidak berwarna
Normal (dapat diterima konsumen) Maksimum 16%
Maksimum 3,25% Maksimum 50 mg/kg
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 10 Tembaga Seng Sulfit Maksimum 30 mg/kg Maksimum 100 mg/kg Maksimum 1000 mg/kg
II.I.d Aplikasi Gelatin
a. Aplikasi gelatin dalam bahan makanan
Gelatin banyak digunakan karena kemampuannya untuk memekatkan, menstabilkan, mengeraskan dan menghasilkan produk yang baik. Ciri khusus dari gelatin yang tidak dapat diganti dengan bahan lain adalah kemampuan
membentuk thermo-reversible gels dan lebur pada suhu ruangan.
Contoh produk yang mengandung gelatin : 1. Marshmallow, fruit chews, toffee, dan jelly
2. Produk roti dan kue
3. Produk daging : sosis
4. Produk susu : es krim, yoghurt, margarin
5. Produk minuman buah-buahan dan wine
b. Aplikasi gelatin dalam pharmaceutical dan kosmetik
1. Sebagai pengembang plasma darah
2. Kapsul gelatin keras, kapsul lembut untuk obat-obatan dan makanan
suplemen
3. Agen pembentukan dan pembungkus tablet dan pil
4. Bahan campuran lotion, cream dan kosmetik
c. Aplikasi gelatin dalam fotografi
1. Gelatin digunakan sebagai gel penguat untuk pembungkus negatif film,
kertas fotografi dan film sinaran X (X-ray), gel penguat ini berisi pewarna dan bahan yang sensitit terhadap cahaya.
2. Bahan imaging bagi holografi dan pembungkus kertas ink-jet.
commit to user Program Studi Diploma III Teknik Kimia Universitas Sebelas Maret
Surakarta 11
Aplikasi gelatin dapat diklasifikasikan antara lain:
1. Ph : gelatin dengan pH rendah digunakan untuk produk sirup rasa asam, juice,
mayonnaise, krim dan aneka kosmetik. Sedangkan gelatin dengan Ph netral digunakan untuk produk daging, cat, farmasi dan fotografi.
2. Proses perendaman : Gelatin tipe A digunakan untuk produk krim tabir
surya/sunblock, milk cleanser/susu pembersih dll. Sedangkan gelatin tipe B digunakan untuk pembuatan sabun mandi cair, shampoo, shower gel dll
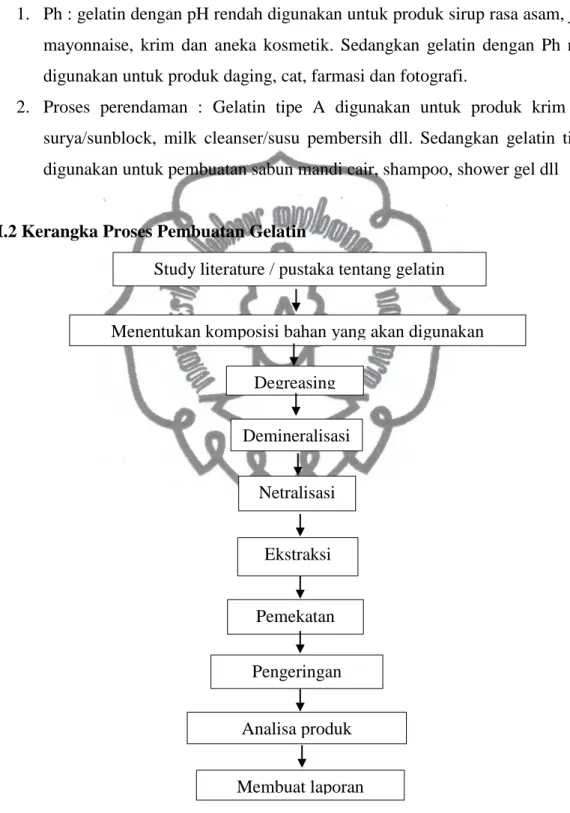
II.2 Kerangka Proses Pembuatan Gelatin
Gambar 2.3 Skema Pelaksanaan Penelitian Study literature / pustaka tentang gelatin
Menentukan komposisi bahan yang akan digunakan Degreasing Analisa produk Membuat laporan Demineralisasi Netralisasi Ekstraksi Pemekatan Pengeringan