LAPORAN PRAKTIKUM ELEKTROANALISIS
PENGUKURAN KONDUKTIVITAS DAN TDS
Dosen Pembimbing : Ibu Endang W , MT
Kelompok 6
Nevy Puspitasari NIM 111431020
Nurul Latipah NIM 111431022
Rizky Permatawati NIM 111431025
Tanggal Percobaan : 21 September 2012
Tanggal Penyerahan : 28 September 2012
POLITEKNIK NEGERI BANDUNG TEKNIK KIMIA - D3 ANALIS KIMIA
Tanggal Percobaan : 21 September 2012
Judul Percobaan : PENGUKURAN KONDUKTIVITAS DAN TDS Pembimbing : Ibu Endang W, MT
Tujuan Percobaan :
1. Dapat melakukan kalibrasi elektroda dan konduktometer secara benar dan tepat 2. Dapat mengukur konduktivitas larutan dengan benar
3. Dapat mengamati perubahan konduktivitas terhadap suhu dan konsentrasi yang berbeda 4. Dapat menentukan TDS dari suatu larutan berdasarkan konduktivitas
Teori Dasar
:
TDS (Total Dissolve Solid) yaitu ukuran zat terlarut (baik itu zat organic maupun anorganic, misalnya : garam, dll) yang terdapat pada sebuah larutan. TDS meter
menggambarkan jumlah zat terlarut dalam Part Per Million (PPM) atau sama dengan milligram per Liter (mg/L). Umumnya berdasarkan definisi diatas seharusnya zat yang terlarut dalam air (larutan) harus dapat melewati saringan yang berdiameter 2 micrometer (2×10-6 meter). TDS meter menggambarkan jumlah zat terlarut dalam ppm atau sama dengan miligram per Liter. Aplikasi yang umum digunakan adalah untuk mengukur kualitas cairan biasanya untuk pengairan, pemeliharaan aquarium, kolam renang, proses kimia, pembuatan air mineral, dll. Setidaknya, kita dapat mengetahui air minum mana yang baik dikonsumsi tubuh, ataupun air murni untuk keperluan kimia (misalnya pembuatan kosmetika, obat-obatan, makanan, dll). Sampai saat ini ada dua metoda yang dapat digunakan untuk mengukur kualitas suatu larutan. Ada pun dua metoda pengukuran TDS (Total Dissolve Solid) tersebut adalah :
1. Gravimetry
2. Electrical Conductivity
HUBUNGAN TDS/PPM DAN EC 1 μS/cm = 1 x 10-6
Hubungan antara konduktivitas dengan TDS yang dikemukakan oleh Victorian Salinity Program and the Murray Darling Basin Commission adalah mikrosiemens per sentimeter (µS/cm pada 25oC) yang ditunjukan sebagai berikut:
TDS (mg/L) = EC (µS/cm pada 25oC) x 0,6
ELECTRICAL CONDUCTIVITY
EC (Electrical Conductivity) atau konduktansi adalah ukuran kemampuan suatu bahan untuk menghantarkan arus listrik. Konduktansi (G) merupakan kebalikan (invers) dari resistansi (R). Setiap bahan mempunyai sifat tertentu yang diungkapkan sebagai hambatan
jenis, , dengan satuan ohm meter. Sifat listrik juga diungkapkan melalui kuantitas,
berbanding terbalik terhadap hambatan, konduktan, G, dengan satuan S (siemen). Sehingga persamaan matematisnya adalah :
G = 1 / R
Sehingga dengan menggunakan Hukum Ohm, maka didapatkan definisi lainnya :
V = I x R
I = G x E
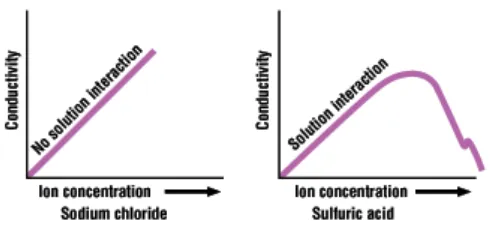
Secara definisi diatas : jika dua plat yang diletakkan dalam suatu larutan diberi beda potensial listrik (normalnya berbentuk sinusioda), maka pada plat tersebut akan mengalir arus listrik. Konduktansi suatu larutan akan sebanding dengan konsentrasi ion-ion dalam larutan tersebut. Namun pada beberapa situasi hal ini tidak berlaku, seperti yang ditunjukkan pada gambar dibawah ini :
Gambar 1 : Hubungan Konduktansi dan Konsetrasi Ion
Konduktansi dipengaruhi pula oleh temperatur. Dalam sebuah metal, konduktansi menurun dengan naiknya temperatur, namun dalam sebuah semikonduktor, konduktansi akan makin besar dengan makin tingginya temperatur.
Persamaan untuk konduktor logam dapat digunakan untuk larutan elektrolit, bila pengukuran dilakukan pada arus dan tegangan bolak-balik. Pengukuran demikian digunakan pada konduktometer, yang terdiri dari wadah dan elektroda platina yang dilapisi platina hitam. Luas permukaan yang dilapisi platina hitam, dinyatakan dengan A dan jarak antara dua elektroda platina. Perbandingan jarak antara dua elektroda platina dengan luas permukaan platina adalah parameter tertentu pada setiap wadah konduktometri dan disebut kapasitas resistif dari wadah konduktometri.
Alat dan Bahan
Alat Bahan Jumlah
Gelas kimia 100 mL 8 buah
Botol semprot 1 buah
Batang pengaduk 1 buah
Ball pipet 1 buah
Gelas ukur 100 mL 1 buah
Pipet ukur 10 mL 1 buah
Sampel air 300 mL
Etanol 200 mL
Sukrosa 2 gram
Larutan NaCl 200 mL
HCl 200 mL
NaOH 200 mL
Aquadest 300 mL
Asam asetat 300 mL
NH4OH 100 mL
KOH 200 mL
Langkah Kerja
A. Kalibrasi elektroda / immersion cell
1. Memasang elektroda pada konduktometer (sesuaikan warna kabel dan socket) 2. Mengatur tombol “cell const” sesuai dengan tetapan sel dari elektroda ( tercantum
pada elektroda).
3. Menggunakan tombol Pt-100 untuk elektroda yang sudah terpasang sensor suhu
4. Mengatur koefisien suhu pada nilai 2,0
5. Menggunakan frekuensi pengukuran 2 kHz dan range pengukuran pada posisi “outo” 6. Mencelupkan elektroda kedalam larutan KCl, mengusahakan sensor suhu tercelup
larutan
7. Menyalakan konduktometer dan tekan tombol “stand by” 8. Menekan tombol “Temp”, dan baca suhu larutan
9. Melihat konduktan dari larutan KCl 0,1 M dan suhu yang terukur
10.Mengatur kembali tombol “cell const”, hingga harga konduktan sesuai dengan nilai pada tabel
11.Bila pada tampilan nilai konduktan sudah sesuai dan tetap, menekan tombol “stand by” dan alat siap untuk digunakan
B. Pengaruh jenis senyawa, jenis pelarut, reaksi kimia terhadap Konduktivitas 1. Menyiapkan larutan/padatan yang akan diukur konduktivitasnya
2. Mencelupkan elektroda dan tekan tombol „meas‟ untuk mengukur konduktivitas larutan uji
C. Pengukuran TDS
1. Menyiapkan sampel air yang akan diukur TDS nya
2. Memastikan konduktometer dan elektroda sudah dikalibrasikan
3. Mencelupkan elektroda ke dalam sampel air, menghilangkan gelembung udara yang
mengelilingi elektroda dengan cara menaik-turunkan elektroda
4. Membaca suhu larutan dan bila tidak pada suhu 25oC, membandingkan dengan nilai dari tabel konduktivitas
5. Mengukur dan membaca konduktivitas dari larutan uji
Data Pecobaan dan Perhitungan
A. Perhitungan persamaan linear penentuan tetapan sel Data nilai konduktivitas larutan KCl 0,1 M
Suhu yang terbaca berdasarkan percobaan kalibrasi = 26,7oC sehingga : Persamaan regeresi linier :
y= 6,758 + 0,245 x y = 6,705 + 0,247 (26,7) y= 13,30
Untuk mengubah nilai konduktivitas menjadi 13,30, maka tetapan sel diubah menjadi sebesar 9,96 x 0,1 = 0,996
B. Pengaruh Konduktivitas terhadap Jenis Senyawa
13. CH3CO2H 0,1 M 0,466
14. NH3 0,1 M 0,651
15. NaCl 0,1 M 10,41
C. Pengaruh jenis pelarut terhadap konduktivitas
Senyawa Konduktivitas (S/cm)
Penggolongan
Tidak mengion Sedikit mengion Mengion sempurna
D. Pengaruh reaksi kimia terhadap konduktivitas
Senyawa Konduktivitas (mS/cm)
Penggolongan
CH3COOH 3% ( dari larutan asam asetat 4 M )
M = =
= 0,39 M
M1.V1 = M2.V2
0,39 . 100 = 0,4. V2
V2= 100x0,39 / 0,4 = 97,5 (membutuhkan air 2,5 mL)
CH3COOH 15% ( dari larutan asam asetat 100% )
%1.V1 = %2.V2
100 . V1 = 15. 100
V1= 1500 / 100 = 15 mL (membutuhkan air 80 mL)
CH3COOH 6 M ( dari larutan asam asetat 100% )
M = =
= 13,17 M
M1.V1 = M2.V2
13,17 . V1 = 6. 100
V1= 600 / 13,17 = 45,56 mL (membutuhkan air 54,45 mL)
E. Perhitungan TDS pada sampel air ledeng
TDS (mg/L) = EC ( µS/cm pada 25oC ) x 0,6 = 0,427 x 0,6
= 0,2562 mg/L
Larutan Konduktivitas (µS/cm) TDS (ppm)
Air ledeng 0,427 0.2562
Air mineral 0,347 0.2082
PEMBAHASAN
Pada praktikum konduktivitas zat ditetapkan dengan mengukur tahanan listrik antara dua elektroda dan membandingkan tahanan ini dengan tahanan suatu larutan potasium klorida
(KCl) pada suhu 25oC. Percobaan ini dilakukan terhadap berbagai bahan berupa larutan maupun zat padat. Dimana setiap bahan diukur konduktivitasnya untuk mengetahui
kemampuannya dalam menghasilkan ion-ion bebas sehingga diketahui sifat bahan dalam
menghantarkan listrik. Elektroda yang digunakan pada percobaan ini adalah menggunakan
elektroda platina. Sebelum dilakukan pengukuran, alat konduktometer terlebih dahulu
dikalibrasi, agar mengurangi kesalahan pembacaan harga konduktan sehingga didapat
ketelitian hasil pengukuran serta untuk menetapkan tetapan sel konduktometer. Pada proses
kalibrasi ini dilakukan dengan mencelupkan elektroda kedalam larutan KCl 0,1M, digunakan
larutan KCl 0,1 M, karena larutan KCl 0,1 M memiliki nilai konduktivitas yang diketahui
pada berbagai suhu, sehingga tetapan sel dapat ditentukan. Pada saat kalibrasi elektroda
kemudian dicelupkan kedalam larutan KCl, dan dipilih tombol Temp ini dimaksudkan untuk
membaca suhu larutan KCl sehingga suhu larutan KCl yang terbaca adalah 26,7oC. Setelah mengetahui suhu larutan KCl maka dilakukan pengukuran nilai konduktivitasnya.
Berdasarkan tabel suhu dan nilai konduktivitas KCl 0,1M, ternyata pada suhu tersebut tidak
terdapat nilai konduktivitas KCl sehingga perhitungan nilai konduktivitas KCl pada suhu
26,7oC dihitung berdasarkan persamaan regeresi linier dengan data yang diambil dari tabel nilai konduktivitas dan suhu KCl dari suhu 25oC-29oC. Dari perhitungan didapat nilai konduktivitas KCl pada suhu 26,7oC adalah sebesar 13,30 sehingga tetapan sel diubah sampai nilai konduktivitas larutan pada suhu tersebut 13,30 sehingga didapat tetapan selnya adalah
0,996 . Pada saat kalibrasi elektroda harus tercelup sampai ruang yang ada didalam elketroda
terisi penuh dengan larutan yang diukur. Hal ini dikarenakan agar pengukuran berlangsung
secara teliti.
Pengaruh Jenis Senyawa terhadap Konduktivitas
Berdasarkan praktikum, hampir semua senyawa memiliki nilai konduktivitas. Hal ini
menunjukan bahwa semua senyawa dapat mengion/terurai menjadi ion-ion. Namun, tidak
semua senyawa mengion secara sempurna. Hal tersebut ditunjukan oleh nilai konduktivitas
yang dihasilkan, apabila nilai konduktivitasnya kecil dapat dikatakan bahwa senyawa tersebut
sedikit mengion sedangkan apabila nilai konduktivitasnya besar dapat dikatakan bahwa
senyawa. Pada percobaan ini tidak dilakukan pengukuran konduktivitas pada senyawa
berbentuk padatan, karena secara otomatis padatan tidak akan menghasilkan nilai
konduktivitas yang benar dan tepat karena pada pengukuran konduktometri adalah mengukur
konduktivitas dari larutan biasanya larutan elektrolit, dimana senyawa tersebut mampu
mengion dalam pelarutnya.
Pada percobaan mengukur konduktivitas air, digunakan 3 jenis sampel air yaitu air
suling, air ledeng dan air mineral. Berdasarkan percobaan konduktivitas air ledeng adalah
yang paling besar diantara yang lainnya sedangkan konduktivitas yang paling kecil adalah
sampel air suling. Sampel air ledeng adalah paling besar karena pada air ledeng masih
memiliki banyak mengandung ion-ion bebas, kemudian pada air mineralpun memiliki
mineral dan ion-ion bebas akan tetapi tidak sebanyak pada air ledeng. Sedangkan air yang
daya hantarnya paling rendah yaitu air suling berasal dari berbagai langkah proses kimia
untuk menghilangkan kandungan mineral-mineral dalam air tersebut itulah sebabnya ion-ion
bebas untuk menghantarkan listrik pada air suling adalah kecil dan sebenarnya sifat air suling
adalah termasuk kedalam golongan senyawa yang tidak mengion.
Selanjutnya dilakukan pengukuran pada etanol 96% sehingga didapat konduktivitas
etanol adalah sedikit mengion karena etanol tergolong larutan organik dan tidak terurai
sempurna, sehingga ion bebas untuk menghantarkan listriknya kecil. Selanjutnya pengukuran
dilakukan pada asam asetat pada 15% dengan konsentraso 3%. Berdasarkan data percobaan
nilai konduktivitas asam asetat 15% lebih tinggi dibanding 3%. Hal ini disebabkan karena
semakin pekat larutan yang dikur maka konsentrasi ion-ion bebasnya lebih besar sehingga
daya hantar listrik yang dihasilkannya pun semakin besar. Nilai konduktivitas asam asetat
yang terukur sesuai dengan teori bahwa larutan yang konsentrasinya lebih tinggi maka akan
memiliki nilai konduktivitas yang lebih besar. Akan tetapi pada asam asetat ini menghasilkan
larutan yang sedikit mengion, hal ini dikarenakan asam asetat tidak terurai sempurna menjadi
ion-ionnya sehingga larutannya sedikit mengion. Kemudian pengukuran dilakukan pada
sukrosa, sukrosa pada tidak dilakukan pengukuran sedangkan sukrosa larutan dilakukan
pengukuran. Berdasarkan percobaan nilai konduktivitas sukrosa adalah besar yaitu 110,7,
seharusnya konduktivitas sukrosa tidak besar atau seharusnya nilai yang dihasilkannya kecil.
Hal ini dikarenakan pada larutan sukrosa tidak terjadi ionisasi yang sempurna, atau ionisasi
yang terjadi adalah kecil karena hanya sedikit ion-ion yang dihasilkan pada larutan ini yang
akan menghantarkan listrik. Ketidaksesuaian ini dapat terjadi karena tidak sempurnanya
pembilasan elektroda oleh aquadest sehingga terdapat sisa larutan pada pengukuran
pengukuran NaCl didapat konduktivitas yang sangat besar hal ini dikarenakan NaCl
merupakan pencampuran antara asam kuat dan basa kuat yang memiliki daya ionisasi tinggi.
NaCl dapat terionisasi sempurna dalam pelarutnya sehingga ion-ion bebasnya banyak yang
dapat menghantarkan listrik. Kemudian untuk HClpun sama karena HCl adalah asam kuat
maka HCl dapat terionisai sempurna dalam pelarutnya sehingga nilai konduktivitasnya besar
dan termasuk pada zat yang mengion sempurna. Pengukuran NaOH dilakukan dan didapat
nilai konduktivitas besar, karena NaOH adalah basa kuat yang dapat terionisasi sempurna
dalam pelarut sehingga nilai konduktivitasnya pun besar, inilah yang mengakibatkan NaOH
adalah zat yang mengion sempurna. Selanjutnya pengukuran dilakukan pada asam asetat
0,1M dan NH4OH 0,1M kedua senyawa ini merupakan asam lemah dan basa lemah dimana
kedua senyawa ini tidak dapat terionisasi sempurna menjadi ion-ionnya sehingga nilai
konduktivitas yang dihasilkannya pun kecil. Kedua senyawa ini digolongkan pada zat yang
sedikit mengion.
Pengaruh Jenis pelarut terhadap konduktivitas
Senyawa yang digunakan adalah KOH, pelarut yang digunakan adalah air dan etanol,
dan 1 jenis KOH berbentuk padatan dan KOH padatan ini tidak dilakukan percobaan.
Pengukuran yang dilakukan hanyalah KOH 1% dan KOH dalam etanol. Dari data percobaan
KOH yang dilarutkan pada air memiliki konduktivitas yang lebih besar dibanding
konduktivitas KOH dalam etanol. Hal ini disebabkan KOH yang dialrutkan dalam air, karena
air lebih bersifat dapat dengan mudah berikatan dengan ion-ion dari senyawa KOH
dibandingkan dengan ikatan pelarut etanol dengan ion-ion dari senyawa KOH. Karena daya
ikat antara ion-ion bebas dengan pelarut akan berpengaruh terhadap mobilitas ion-ion
senyawa dalam larutannya. Selain itu KOH dalam pelarut, KOH akan terionisasi sempurna
menghasilkan ion-ion bebas yang dapat menghantarkan listrik sehingga nilai
konduktivitasnya tinggi. Sedangkan KOH yang dilarutkan pada etanol, KOH tidak akan
terionisasi sempurna atau sedikit terionisasi sehingga menghasilkan nilai konduktivitas yang
lebih kecil.
Pengaruh Reaksi Kimia terhadap Konduktivitas
Pada percobaan ini dilakukan reaksi antara padatan CaCO3 dengan CH3COOH dan
reaksi antara CaCO3 dan HCl. Berdasarkan percobaan reaksi yang terjadi dari dua reaksi
Reaksi CaCO3 dan CH3COOH 6M:
CaCO3(S) + 2CH3COOH(aq) Ca(CH3COO)2(aq) + H2CO3
Reaksi antara CaCO3 dan HCl 6M:
CaCO3(s) + HCl(aq) CaCl2(aq) + H2CO3
Pengaruh reaksi kimia dalam hal ini adalah terletak pada pereaksi yang digunakan yaitu
pereaksi yang memiliki konsentrasi yang pekat (6M). Pada saat CaCO3 direaksikan dengan
CH3COOH 6M atau larutan asam asetat pekat, maka asam asetat yang pekat ini dapat
mendesak CaCO3 yang akan mengakibatkan CaCO3 terurai menjadi ion Ca2+ dan ion CO3
2-sehingga menghasilkan konduktivitas sebesar 5,7. Sedangkan reaksi antara CaCO3 dengan
HCl yang merupakan elektrolit kuat, pereaksi yang digunakan adalah asam kuat yang pekat
sehingga reaksi untuk mendesak CaCO3 menjadi Ca2+ dan CO32- pun lebih besar.
Berdasarkan percobaan konduktivitas pada reaksi ini tidak terbaca, hal ini dikarenakan
konduktivitas yang dihasilkan teralalu besar sehingga tidak dapat terbaca oleh konduktometer.
Berdasarkan percobaan, reaksi antara CaCO3 dengan HCl konduktivitasnya lebih besar dari
reaksi CaCO3 dengan asam asetat, hal ini dikarenakan reaksi anata CaCO3 dengan HCl
merupakan reaksi dengan pereaksi asam kuat yang pekat, nilai konduktivitas HCl sendiripun
sudah sangat besar sehingga bila direaksikan dengan CaCO3 nilai konduktivitasnya akan
lebih besar.
Pengukuran TDS
Pada percobaan ini didapatkan nilai TDS yang tertinggi adalah sampel air ledeng dari
pada air suling atau air mineral. Hal ini dikarenakan pada air ledeng kandungan
mineral/logam/zat terlarut lainnya dalam air ledeng lebih banyak dibanding air mineral yang
telah diolah ataupun dengan air suling yang telah mengalami proses kimia. Sehingga nilai
TDS air ledeng lebih besar diantara yang lainnya yaitu sebesar 0,2562 ppm. Sedangkan untuk
TDS air mineral, air ini telah diolah sehingga kadungan logam atau zat terlarutnya lebih
sedikit sehingga nilai konduktivitasnya lebih kecil dari air ledeng yaitu 0,2082 ppm.
Kemudian untuk nilai TDS air suling, karena air suling telah mengalami proses kimia
sehingga sangat kecil kemungkinan adanya zat terlarutnya, sehingga TDS yang dihasilkannya
KESIMPULAN
Berdasarkan praktikum yang dilakukan, didapat hasil percobaan: 1. Berdasarkan pengaruh jenis senyawa terhadap konduktivitas
a. senyawa atau zat yang mengion sempurna adalah sukrosa,NaCl,HCl, NaOH b. zat yang sedikit mengion adalah adalah air ledeng,air mineral,etanol, asam
asetat, serta NH4OH.
c. zat yang tidak mengion adalah air ledeng.
2. Berdasarkan pengaruh jenis pelarut terhadap konduktivitas
a. senyawa atau zat yang mengion sempurna adalah KOH dalam air b. zat yang sedikit mengion adalah adalah KOH dalam etanol
3. Berdasarkan pengaruh reaksi kimia terhadap konduktivitas
a. Reaksi yang mengion sempurna adalah CaCO3 dengan HCl 6M
b. Reaksi yang sedikit mengion adalah adalah CaCO3 dengan CH3COOH 6M
DAFTAR PUSTAKA
Anonim. “Konduktivitas Termal”, (online),
( http://id.wikipedia.org/wiki/Konduktivitas_termal. diunduh 27 Sepetember 2012 pkl 13.00)
Anonim, 2011. “Konduktivitas”, (online),
(http://ml.scribd.com/doc/52687112/KONDUKTANSI-ELEKTROLIT-KUAT-DAN-LEMAH diunduh 27 September 2012 pkl. 13.21)
Anonim. “Konduktivitas Listrik”, (online),
( http://id.wikipedia.org/wiki/Konduktivitas_listrik. diunduh 27 Sepetember 2012 pkl 13.00)
Annisa, 2012. “ TDS meter”, (online), ( www.airminumisiulang.com/product/12/14/TDS-diunduh 27 September 2012 pkl. 13.14)
Lischer, 2009. “ Larutan Elektrolit”, (online),