DETEKSI GENDARUSIN A DALAM URIN SUBYEK
PRIA SETELAH PEMBERIAN ORAL KAPSUL
EKSTRAK ETANOL DAUN
Justicia gendarussa
Burm. f
WILDAN ALFIAN NOOR
FAKULTAS FARMASI UNIVERSITAS AIRLANGGA
DEPARTEMEN FARMAKOGNOSI DAN FITOKIMIA
DETEKSI GENDARUSIN A DALAM URIN SUBYEK
PRIA SETELAH PEMBERIAN ORAL KAPSUL
EKSTRAK ETANOL DAUN
Justicia gendarussa
Burm. f
WILDAN ALFIAN NOOR
NIM: 050810231
FAKULTAS FARMASI UNIVERSITAS AIRLANGGA
DEPARTEMEN FARMAKOGNOSI DAN FITOKIMIA
iii
Dengan perkembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya dengan judul:
“DETEKSI GENDARUSIN A DALAM URIN SUBYEK PRIA SETELAH PEMBERIAN ORAL KAPSUL EKSTRAK ETANOL DAUN Justicia gendarussa Burm. f”
untuk dipublikasikan atau ditampilkan di internet, digital library Perpustakaan Universitas Airlangga atau media lain untuk kepentingan akademik sebatas sesuasi dengan Undang-Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi skripsi/karya ilmiah ini saya buat dengan sebenarnya.
Surabaya, 28 September 2012
iv Saya yang bertanda tangan di bawah ini, Nama : Wildan Alfian Noor
NIM : 050810231 Fakultas: Farmasi
menyatakan dengan sesungguhnya bahwa hasil tugas akhir yang saya tulis dengan judul:
“DETEKSI GENDARUSIN A DALAM URIN SUBYEK PRIA SETELAH PEMBERIAN ORAL KAPSUL EKSTRAK ETANOL DAUN Justicia gendarussa Burm. f”
adalah benar-benar merupakan hasil karya saya sendiri. Apabila kemudian hari ditemukan bahwa skripsi ini menggunakan dan merupakan hasil plagiarisme, maka saya bersedia menerima sanksi berupa pembatalan kelulusan atau pencabutan gelar yang saya peroleh.
Demikian surat pernyataan ini saya buat untuk dipergunakan dengan semestinya.
Surabaya, 28 September 2012
v
PRIA SETELAH PEMBERIAN ORAL KAPSUL
EKSTRAK ETANOL DAUN Justicia gendarussa Burm. f
SKRIPSI
Dibuat Untuk Memenuhi Syarat Mencapai Gelar Sarjana Farmasi Pada Fakultas Farmasi Universitas Airlangga
2012
Oleh :
WILDAN ALFIAN NOOR NIM. 050810231
Skripsi ini telah disetujui tanggal 4 September 2012 oleh :
Pembimbing Utama Pembimbing Serta
vi
“Bacalah dengan (menyebut) nama Tuhanmu Yang menciptakan, Dia telah menciptakan manusia dari segumpal darah. Bacalah, dan Tuhanmulah Yang Maha Pemurah, Yang mengajar (manusia) dengan perantaran kalam, Dia mengajar kepada manusia apa yang tidak diketahuinya” (QS Al-alaq 1-5). Alhamdullillah, atas perkenan Allah SWT akhirnya saya bisa mnyelesaikan skripsi yang berjudul “DETEKSI GENDARUSIN A DALAM URIN SUBYEK PRIA SETELAH PEMBERIAN ORAL KAPSUL EKSTRAK ETANOL DAUN Justicia gendarussa Burm. f” dengan sebaik-baiknya. Sholawat serta salam tidak henti-hentinya saya ucapkan kepada Rasulullah Muhammad SAW yang menjadi suri tauladan kebaikan yang langkah hidupnya menginspirasi kita semua.
Saya ucapkan terimakasih yang sedalam-dalamnya atas berbagai pihak yang membantu, menyemangati dan memudahkan selama pengerjaan penelitian ini terutama kepada:
1. Dekan Fakultas Farmasi Universitas Airlangga Surabaya Dr. Umi Athijah.,MS.,Apt.
2. Prof. Dr. Bambang Prajogo EW., MS.,Apt sebagai dosen pembimbing utama serta kesempatan yang diberikan kepada saya untuk berpartisipasi dalam tim gendarussa 2012 ini.
3. Dr. Suharjono.,MS.,Apt selaku dosen pembimbing serta yang dengan sabar memberikan masukan dan saran disaat saya mengalami hambatan penelitian ini.
4. Dr.rer.nat. Mulja Hadi Santosa.,Apt da Prof. Dr. Mangestuti Agil.,MS.,Apt selaku dosen penguji yang telah memberikan masukan berharga bagi skripsi saya.
5. Bapak Sriyatno.,S.Pd dan Ibu Nihayatul Mahmudah merupakan kedua orang tua saya yang selalu menyemangati dan mendoakan saya dari rumah.
vii
7. Rekan-rekan seangkatan PPSDMS Nurul Fikri Surabaya yang selalu menyemangati saya dalam menyelesaikan skripsi ini. 8. Teman-teman anggota kontrakan lukim, kanzul, rozikin, zaki,
muslih, dan juga Asset At-taqwa.
9. Teman-teman angkatan 2008 yang paling kompak.
10. Pihak-pihak institusi dari PT Angler Biochemlab yaitu Bapak Suwidji dan Ibu Veronika, laboran lab. MM Bapak Kusairi dan Mas Iwan, KSKR FK UNAIR dr. Dian Pramesti, dan PT Aneka Gas. Trimakasih atas semua kerjasamanya.
Akhir kata semoga Allah SWT membalas kebaikan pihak-pihak yang membantu kelancaran pengerjaan skripsi ini dengan balasan yang setimpal. Amin.
Surabaya, September 2012
viii
SETELAH PEMBERIAN ORAL KAPSUL EKSTRAK ETANOL DAUN Justicia gendarussa Burm. f
Wildan Alfian Noor
Hasil penelitian menunjukkan bahwa dalam fraksi n-butanol daun gandarusa terdapat 12 komponen flavonoid dengan komponen mayor 6,8-di-α-L-arabinopiranosil-4’,5,7-trihidroksiflavon atau 6,8-diarabinosil-apigenin, yang kemudian dikenal dengan gendarusin A, salah satu bahan anti fertilitas dengan aktivitas pencegahan penetrasi spermatozoa in vitro dengan mekanisme penghambatan enzim hialuronidase. Komponen minor adalah 6,8-α-L-arabinopiranosil-4’,5,7-trihidroksi-8-β-D-silopiranosilflavon atau 6-arabinosil-8-silosilapigenin yang kemudian dikenal dengan gendarusin B (Prajogo, 2002).
Penelitian tentang penetapan parameter farmakokinetika gendarusin A dalam urin menggunakan 6 subyek pria dengan metode analisis memakai HPLC (Sihabuddin, 2009) serta tentang deteksi gendarusin A dalam urin pada pria hari ke 72 menggunakan HPLC (Saifullah, 2010), kedua penelitian tersebut secara kuantitatif dapat mendeteksi gendarusin A dalam urin sampel. Dasar dari penelitian tersebut adalah kesamaan waktu retensi antara gendarusin A dalam sampel dengan standar gendarusin A. Hal tersebut menjadi dasar untuk melakukan penelitian lebih lanjut yaitu tentang identifikasi gendarusin A dalam urin dengan metode LC-MS/MS untuk memastikan apakah gendarusin A memang terekskresi dalam urin dalam bentuk utuh. LC-MS/MS memiliki kemampuan yang terpercaya untuk mengidentifikasi gendarusin A dalam sampel urin karena dapat menampilkan data tiga dimensi yaitu sebagai fungsi sinyal terhadap waktu serta spektrum masa dari analit yang akan diidentifikasi.
ix
dahulu digunakan metode HPLC (preliminary). Kondisi HPLC yang digunakan adalah kolom Novapak Waters C-18 3,9 x 150 mm 60 Å, 4 µm, suhu kolom 30o C, kecepatan alir 1 ml/menit, dan detektor DAD UV/Vis. Fase gerak yang digunakan adalah sistem gradien metanol/air dengan waktu analisis 11 menit. Selektivitas yang diperoleh dari analisis gendarusin A dalam blanko urin diperoleh resolusi 2,12 dan faktor selektivitas 1,58.
Selanjutnya digunakan alat LC-MS/MS yang mempunyai sensitivitas lebih tinggi daripada HPLC dengan menggunakan kolom eclipse plus C-18 4,6 x 50 mm 3,5 um, kecepatan alir 1 ml/menit temperatur kolom 50o C, polaritas negatif dan tipe skanning MRM (Multiple Reaction Monitoring). Dilakukan optimasi awal berupa tuning yaitu dengan infusi standar ke dalam MS (Mass Spectrometer) dengan hasil m/z apigenin [M-H]- 269 Da dan gendarusin A [M-H]- 533 Da. MRM terpilih untuk apigenin adalah m/z 268,9/116,8 Da dan m/z 268,9/150,8 Da. MRM terpilih untuk gendarusin A adalah m/z 533/352,9 Da dan m/z 533/382,9 Da. Kromatografi awal dari standar gendarusin A menunjukkan puncak kecil yang muncul yang kemungkinan berasal dari isomer yang masih terikutkan dalam standar gendarusin A. LOD (Limit of Detection) sebesar 1,179 ppb dan LOQ (Limit of Quantification) sebesar 2,009 ppb dari gendarusin A dengan LC-MS/MS.
x
Subject after Oral Ingestion Capsules Ethanol Extract Leaf Justicia gendarussa Burm. f
Wildan Alfian Noor
Justicia gendarussa Burm. f has 12 flavonoid component with major component 6.8-di-α-L-arabinopiranosil-4',5,7-trihidroksiflavon or 6,8-diarabinosilapigenin, which have been known as gendarusin A, one of the anti-fertilities with prevention activities penetration of spermatozoa in vitro with hyaluronidase enzyme inhibition mechanism.
The purpose of this study is to detect of intact C-glycosyl flavonoid, 6,8-diarabinosilapigenin in human urine after oral ingestion capsules from ethanol extract leaves Justicia gendarussa Burm. f. Four healhty subjects, each one given a dosage gandarusa extract 900 mg equal 3.78 mg of gendarusin A from leaves Justicia gendarussa Burm F (2 capsules). For chromatography used HPLC (preliminary study) with Novapak column Waters C-18 3.9 X 150 mm 60 Å, 4 μm, column temperature of 30o C, flow rate of 1 ml / min, and DAD detector UV/Vis. The mobile phase used was a gradient system of methanol / water. Selectivity obtained from the analysis of the blank urine spiked with 6,8-diarabinosilapigenin , resolution 2,12 and selectivity factor 1,58.
The study continued with LC-MS/MS QTRAP using column eclipse plus C-18 4.6 x 50 mm 3.5 um, flow rate 1 ml / min, temperature column 50° C, negative mode and scan type MRM (Multiple Reaction Monitoring). Perform an initial optimization by tuning the standard infusion into the MS (Mass Spectrometer) show apigenin with m/z [M-H]- 269 Da and gendarusin A m/z [M-H]- 533 Da. Chromatography of standard gendarusin A shows a small peak appears, indicating the possibility that it came from isomer from the analyte. LOD 1.179 ppb and LOQ 2.009 ppb from gendarusin A. From 4 subjects with accumulation of 24-hour urine samples found only 1 subject with identification gendarusin A in the form intact with a maximum intensity of 100.0 cps. Urine samples at collection time points showed no detection both gendarusin A and apigenin.
xi
DAFTAR LAMPIRAN………. xviii
DAFTAR SINGKATAN……….. xix
BAB I PENDAHULUAN 1.1 Latar belakang masalah………. 1
1.2 Rumusan masalah ………. 5
1.3 Tujuan penelitian ……….. 6
1.4 Manfaat penelitian ……… 6
BAB II TINJAUAN PUSTAKA 2.1 Tinjauan tentang Justicia gendarussa Burm F…… 7
2.1.1 Klasifikasi ……… 7
2.1.7 Standarisasi ekstrak etanol daun Justicia gendarussa Burm F……… 11
2.2. Tinjauan tentang senyawa flavonoid………. 12
2.2.1 Kegunaan flavonoid……… 13
2.2.2 Struktur dasar flavonoid………. 13
xii
2.3 Tinjauan tentang gendarusin A……… 17
2.4 Penelitian sebelumnya tentang gendarusin A dalam urin………... 19
2.5 Bioavaibilitas, absorpsi, distribusi, dan ekskresi dari flavonoid……… 20
2.6 Tinjauan tentang analisis biotransformasi flavonoid dengan LC-MS/MS………... 23
2.7 Tinjauan tentang urin ……… 27
2.7.1 Validitas data urin……… 28
2.8 Tinjauan tentang LC-MS/MS……… 29
2.8.1 Instrumentasi ……… 31
2.8.2 Sumber ion……… 31
2.8.3 Analiser masa……… 32
2.8.4 CID dan MS/MS……… 33
2.8.5 Kolom kromatografi………. 35
2.9 Metode analisis gendarusin A dalam urin……... 36
BAB III KERANGKA KONSEPTUAL 3.1 Uraian kerangka konseptual……… 37
3.2 Kerangka konseptual……… 40
3.3 Kerangka operasional……….. 41
BAB IV METODE PENELITIAN 4.1 Jenis penelitian……… 42
4.2 Lokasi penelitian……… 42
4.3 Bahan penelitian……… 42
4.3.1 Bahan obat……… 42
xiii
4.8 Optimasi metode (pendahuluan)………... 47
4.8.1 Optimasi standar gendarusin A dan apigenin… 47 4.8.2 Optimasi serapan standard dan blanko urin… 48 4.8.3 Uji selektivitas……….. 48
4.8.4 Penentuan perolehan kembali……….. 49
4.9 Penentuan kondisi LC-MS/MS………. 49
4.9.1 Optimasi kondisi kromatografi……… 49
4.9.2 Fase gerak………. 50
4.9.3 Optimasi kondisi MS……… 50
4.9.4 Penentuan LOD/LOQ……… 50
4.10 Preparasi sampel………. 51
4.11 Pengolahan data……….. 51
BAB V HASIL PENELITIAN 5.1 Pemilihan kondisi HPLC……… 53
5.1.1 Hasil pemilihan panjang gelombang…………. 53
5.1.2 Hasil pemilihan fase gerak……… 54
5.2 Hasil pemilihan metode preparasi urin………. 56
5.3 Hasil optimasi metode kualitatif……… 57
5.3.1 Selektivitas………. 57
5.3.2 Persen rekoveri………. 59
5.4 Hasil optimasi menggunakan LC-MS/MS QTRAP 4000 series………... 60
5.4.1 Hasil tuning awal……….. 60
5.4.2 Hasil pemilihan fase gerak LC-MS/MS……… 62
5.4.3 Perhitungan LOD/LOQ……… 64
5.4.4 Efek matriks………. 65
5.5 Identifikasi metabolit A dalam urin……….. 66
BAB VI PEMBAHASAN……….. 68
BAB VII KESIMPULAN DAN SARAN 7.1 Kesimpulan……… 76
xv
Tabel 4.1 Fase gerak yang digunakan……….… 47 Tabel 5.1 Fase gerak HPLC gendarusin A……….. 54 Tabel 5.2 Rekoveri standar gendarusin A
dalam urin blanko………. 59
xvi
Gambar 2.1 Tanaman Justicia gendarussa Burm. f... 7
Gambar 2.2 Struktur Alkaloid Justicia gendarussa Burm. f... 9
Gambar 2.3 Struktur dasar flavonoid ... 14
Gambar 2.4 Sistem penomoran untuk turunan flavonoid... 14
Gambar 2.5 Beberapa aglikon flavonoid... 15
Gambar 2.6 Struktur molekul gandarusin A ……… 18
Gambar 2.7 Struktur molekul gandarusin B... 18
Gambar 2.8 Skema bioavaibilitas, absorbsi, distribusi, metabolisme dan eksresi dari flavonoid ………... 21
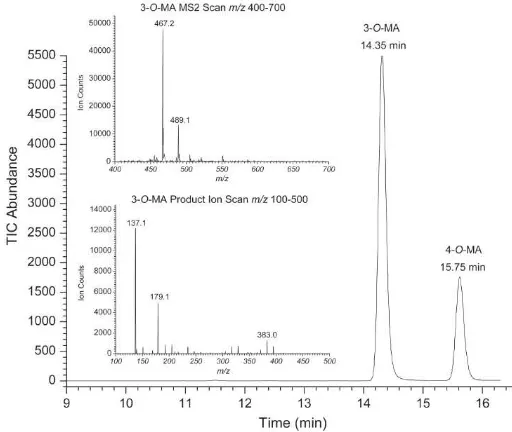
Gambar 2.9 Contoh kromatogram MRM LC-MS/MS dari 3-O-MA dan 4-O-MA……… 25
Gambar 2.10 Contoh kromatogram LC-ESI-MS/MS dari sampel urin setelah konsumsi ekstrak rooibos….. 26
Gambar 2.11 Penerapan berberapa teknik ionisasi LC/MS…… 32
Gambar 2.12 MS/MS dengan spektrometer massa triple-quadrupole……… 34
Gambar 3.1 Skema kerangka konseptual……… 40
Gambar 3.2 Skema kerangka operasional……….. 41
Gambar 5.1 Spektra 2D gendarusin A yang menunjukkan panjang gelombang maksimum pada 340 nm…... 53
xvii
Gambar 5.4 Skema ekstraksi gendarusin A pada sampel urin.... 57 Gambar 5.5 Kromatogram HPLC, blanko urin, gendarusin A
/metanol, gendarusin A dalam urin blanko…….. . 58 Gambar 5.6 Profil LC-MS/MS standar apigenin CE 40……….. 60 Gambar 5.7 Profil LC-MS/MS standar gendarusin A
CE 100 dan CE 50………. 61
Gambar 5.8 Kromatogram LC-MS/MS standar apigenin…….. 62 Gambar 5.9 Kromatogram LC-MS/MS standar gendarusin A. 63 Gambar 5.10 Kromatogram LC-MS/MS pre / post spike
standar gendarusin A dalam urin blanko………… 65 Gambar 5.11 Kromatogram LC-MS/MS identifikasi
gendarusin A dalam urin subyek AST dan BAG.. 66 Gambar 5.12 Kromatogram LC-MS/MS identifikasi
xviii
Lampiran 1 Keterangan Kelaikan Etik………. 83 Lampiran 2 Naskah Penjelasan Untuk Mendapatkan Persetujuan 84 Sukarelawan dan Formulir Persetujuan (Inform Consent) Lampiran 3 Declaration Helsinki……….. 89 Lampiran 4 Karakteristik Subyek……….. 93 Lampiran 5 Kromatogram LC-MS/MS LOD dan LOQ……..…. 94 Lampiran 6 Kromatogram sampel LC-MS/MS
QTRAP 4000 Series………. 97
Lampiran 7 Formula kapsul Ekstrak Etanol
xix
APCI Atmospheric Pressure Chemical Ionization APPI Atmospheric Pressure Photoionization
As Arsen
CBG Cytosolic Β Glucosidase
Cd Cadmium
CE Collision Energy
CID Collision-Induced Dissociation COMT Catechol-O-Methyltransferases CPE Corona Penetration Enzyme CSP Chiral Stationary Phase
Da Dalton
DAD Diode Array Detektor ESI Electrospray Ionization
FT-ICR Fourier Transform-Ion Cyclotron Resonance GC-MS Gas Chromatography-Mass Spectrometry
Hg Hydrargyrum
HPLC High Performance Liquid Chromatography
IVF In Vitro
KB Keluarga Berencana
KSKR Kelompok Studi Kesehatan Reproduksi LC Liquid Chromatography
xx LPH Lactase Phloridizin Hydrolase MRM Multiple Reaction Monitoring MRP Multidrug Resistance Protein
MS Mass Spectrometry
ODS Octadecyl-Silica
Pb Plumbum
P-gp P-Glycoprotein ppb part per billion ppm part per million QTRAP Quadrupole Ion Trap
RP-HPLC Reverse Phase High Performance Liquid Chromatography
Rs Resolution
SD Standart Deviation SULT Sulfotransferases TIC Total Ion Current
tR Retention time
UGTs Uridine-5’-Diphosphatase Glucoronosyl-Transferases
UV Ultra Violet
BAB I PENDAHULUAN
1.1 Latar Belakang Masalah
Daun Justicia gendarusa Burm. f. diketahui mengandung kalium, flavonoid, steroid atau triterpenoid, tannin 0,4% (DepKes RI,1995); alkaloid, amin aromatik, iridoid dan kumarin (Prajogo, 2002). Hasil penelitian menunjukkan bahwa dalam fraksi n-butanol daun gandarusa terdapat 12 komponen flavonoid dengan komponen mayor 6,8-di-α-L-arabinopiranosil-4’,5,7-trihidroksiflavon atau 6,8-diarabinosilapigenin, yang kemudian dikenal dengan gendarusin A, salah satu bahan antifertilitas dengan aktivitas pencegahan penetrasi spermatozoa in vitro dengan mekanisme penghambatan enzim hialuronidase. Komponen minor adalah 6,8-α-L-arabinopiranosil-4’,5,7-trihidroksi-8-β-D-silopiranosilflavon atau 6-arabinosil-8-silosilapigenin yang kemudian dikenal dengan gendarusin B (Prajogo, 2002). Dari hasil studi bioaktivitas dari ekstrak diklorometana dan methanol, daun Justicia gendarusa Burm. f dapat menurunkan motilitas dan viabilitas spermatozoa kelinci, mencit dan manusia secara in vitro dan menghambat spermatogenesis mencit. Fraksi etil asetat dan n-butanol daun
Justicia gendarusa Burm. f dapat menghambat motilitas dan viabilitas spermatozoa secara in vitro, serta pemberian infus dapat menurunkan kadar testosteron serum tikus (Prajogo, 2002).
maka pengembangan industri obat tradisional. Justicia gendarusa Burm. f harus memenuhi serangkaian uji klinik untuk menjamin efikasi, kualitas dan keamanannya. Di tahun 2011 ini dilakukan uji klinik fase tiga dari Justicia gendarusa Burm. f untuk melanjutkan uji klinik fase dua yang sebelumnya telah selesai dilakukan.
Penelitian ini dilakukan untuk mendeteksi senyawa gendarusin A yang telah melewati berbagai kompartmen dalam tubuh manusia yang terekskresi di dalam urin subyek pria setelah pemberian ekstrak etanol daun
Justicia gendarusa Burm. f. Studi juga dapat dipergunakan untuk mengidentifikasi hasil metabolit dari senyawa gendarusin A dalam urin dan sebagai langkah awal untuk menjelaskan proses biotransformasi dalam tubuh manusia dari senyawa gendarusin A yang mempunyai khasiat sebagai antifertilitas bagi pria.
Dari hasil penelitian sebelumnya yang juga menggunakan sampel urin tentang penetapan parameter farmakokinetika gendarusin A dalam urin menggunakan 6 subyek pria dengan metode analisis memakai HPLC (Sihabuddin, 2009) serta penelitian tentang deteksi gendarusin A dalam urin pada pria hari ke 72 menggunakan HPLC (Saifullah, 2010) secara kuantitatif dapat mendeteksi metabolit dalam urin manusia yang mempunyai waktu retensi sama dengan standar gendarusin A. Hal ini menimbulkan pertanyaan apakah gendarusin A terekskresi dalam bentuk utuh di dalam urin manusia.
mengalami perubahan bentuk (biotransformasi) menjadi bentuk metabolit dan terkonjugasi dengan molekul-molekul yang berada di dalam tubuh menjadi bentuk yang lebih polar agar dapat dieliminasi dari tubuh. Studi ilmiah tentang biotransformasi, proses absorbsi, metabolisme dan bioavaibilitas secara in vivo dari senyawa yang terkandung dalam ekstrak etanol daun Justicia gendarusa Burm. f masih belum secara jelas diketahui dan dilakukan. Secara umum dapat diterima bahwa bentuk glikosida dari flavonoid yang terkandung dalam makanan saat dikonsumsi akan terhidrolisis menjadi bentuk free aglycons yang selanjutnya akan berubah menjadi bentuk terkonjugasi dengan sulfat dan glukoronat oleh liver dan permukaan epitel yang lain. Konjugat biologi ini akan mengalami sirkulasi bersama plasma dan terekskresi bersama urin dan feses (Clarke et al.,
2002). Sehingga perlu adanya penelitian tentang deteksi gendarusin A dalam urin manusia untuk memastikan apakah gendarusin A memang terekskresi dalam bentuk utuh di urin atau terkonjugasi dengan senyawa endogen tubuh.
senyawa gendarusin A akan mengalami proses yang sama dalam tubuh karena berasal dari jenis yang sama yaitu C-glycosyl flavonoid.
Ada tiga pendekatan utama untuk mengetahui informasi tentang konjugasi. Pertama adalah untuk melakukan hidrolisis enzimatik secara selektif untuk menghasilkan data dari total sulfat, total glukoronat dan free aglycons, serta menentukan jumlah semua senyawa yang sebenarnya sebagai konsentrasi aglikon. Kedua adalah memisahkan konjugat menjadi fraksi-fraksi dengan langkah-langkah proses kromatografi, melakukan hidrolisis dari fraksi yang terpisah tersebut, dan menentukan jumlah aglikon yang dihasilkan, biasanya menggunakan GC-MS. Ketiga, hal yang mungkin dilakukan adalah dengan mengukur langsung jumlah semua konjugat secara bersamaan, tanpa langkah pengolahan sampel dimana rasio konsentrasi dari konjugat dan aglikon dapat terpengaruh. (Clarke, et al., 2002).
Berdasarkan uraian diatas teknik analisis saat ini yang memenuhi kualifikasi dan kuantifikasi penuh dari deteksi analit dalam matriks biologi adalah LC-MS/MS. Penggunaan mass spectrometry untuk penelitian sejenis telah dilakukan yaitu tentang penentuan jumlah isoflavon glukoronat dalam urin tikus dengan LC-ESI/MS dan ion-trap LC-MS/MS (Doerge et al.,
. Metode LC-MS/MS merupakan gabungan dari dua teknik analisis yaitu liquid chromatography dan mass spectrometers. Liquid chromatography (LC) adalah teknik pemisahan yang fundamental di dalam ilmu science dan terkait dengan kimia. Tidak seperti gas kromatografi, yang tidak dapat digunakan untuk molekul-molekul yang tidak dapat menguap dan tidak stabil terhadap panas. Liquid chromatography (LC) dapat memisahkan banyak komponen organik secara aman, seperti metabolit dari obat dengan molekul yang kecil sampai peptida dan protein. Mass spectrometers (MS) juga dapat menampilkan data secara tiga dimensi. Dengan penambahan kekuatan sinyal juga dapat menampilkan data yang penting seperti berat molekul, struktur molekul, kuantitas dan kemurnian dari sampel. Data dari mass spectra dapat menambah spesifitas yang meningkatkan hasil analisis baik kualitatif maupun kuantitatif. Metode LC-MS/MS tersebut dapat digunakan untuk mendeteksi senyawa gendarusin A dan mengembangkan penelitian sejenis tentang penentuan metabolit dari gendarusin A dalam urin manusia serta senyawa lain yang terkandung di dalam ekstrak etanol daun Justicia gendarussa Burm F.
1.2 Rumusan Masalah
Berdasarkan uraian latar belakang tersebut, maka dapat diambil suatu permasalahan sebagai berikut:
1.3 Tujuan Penelitian
Tujuan umum penelitian ini adalah untuk mendeteksi gendarusin A dalam urin dan menunjang penelitian-penelitian yang lain dalam proses pengembangan Justicia gendarusa Burm. f sebagai kandidat obat kontrasepsi herbal baru bagi pria.
Sedangkan tujuan khusus dari penelitian ini adalah mendeteksi gendarusin A dalam urin subyek pria setelah pemberian kapsul ekstrak etanol daun Justicia gendarusa Burm. f dengan menggunakan metode LC-MS/MS.
1.4 Manfaat Penelitian
Penelitian ini diharapkan dapat bermanfaat untuk:
1. Mendeteksi gendarusin A dalam urin subyek pria setelah pemberian ekstrak etanol daun Justicia gendarusa Burm. f dengan menggunakan LC-MS/MS sebagai bentuk yang tidak berubah. 2. Menambah informasi dan menunjang penelitian-penelitian yang
BAB II
TINJAUAN PUSTAKA
2.1 Tinjauan tentang Justicia gendarussa Burm. f.
Gambar 2.1 Tanaman Justicia gendarussa Burm. f.
2.1.1 Klasifikasi
Klasifikasi (Van Steenis, 1978) Divisi : Spermatophyta Anak Divisi : Angiospermae Kelas : Dicotyledonae Anak Kelas : Sympetalae Bangsa : Schropulariales Suku : Achanthaceae Marga : Justicia
Jenis : Justicia gendarussa Burm.f. Sinonim : Gendarussa vulgaris Nees
Justicia dahona (Buch) Justicia nigricans Lair
2.1.2 Nama Daerah
Aceh : besi-besi
Jawa : gandarusa, handarusa, ghandharusa Bima : gandarisa
Ternate : puli (DepKes RI, 1995)
2.1.3 Morfologi Tanaman
Justicia gendarussa Burm F merupakan tanaman perdu yang tumbuh tegak di hutan atau ditanam sebagai tumbuhan obat atau tanaman pagar. Tanaman ini di Jawa ditemukan tumbuh pada ketinggian 1-500 m dpl. Morfologi lain dari tanaman ini adalah batang yang berkayu, bentuknya segiempat tumpul atau cukup bulat, warnanya ungu (muda) dan coklat muda (tua), tinggi 0,7-2 m, bercabang. Daun tunggal bertangkai pendek (5-8 mm), letak berhadapan, helai daun berbentuk lanset, berlekuk lebar dan tidak dalam, ujung meruncing, pangkal berbentuk baji, pertulangan menyirip, panjang 5-20 cm, lebar 1-3,5 cm, warna hijau tua. Bunga majemuk, tersusun dalam malai, keluar dari ketiak daun atau ujung percabangan, mahkota berbentuk tabung, berbibir dua, putih. Daun pelindung kecil, sempit, runcing dan hampir sama. Buah berbentuk, bulat panjang, berbiji empat, licin. (Dalimartha, 1999 dan Steenis, 1997)
2.1.4 Kandungan Kimia Tanaman
flavonoid adalah 6,8-di-α-l-arabinopiranosil-4’,5,7-trihidroksiflavon atau 6,8-diarabinosilapigenin yang kemudian dikenal dengan gendarusin A, dengan aktivitas pencegahan penetrasi spermatozoa invitro dan salah satu komponen minor adalah 6-α-l-arabinopiranosil-4’,5,7 -trihidroksi-8-B-d-silopiranosilflavon atau 6-arabinosil-8-silosilapigenin yang kemudian dikenal dengan gendarusin B (Prajogo,2002).
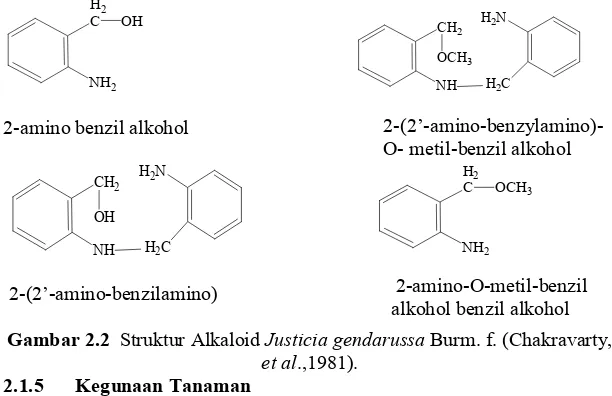
Kandungan alkaloid yang telah diisolasi dari daun Justicia gendarussa Burm. f. antara lain 2-amino benzil alkohol, 2-amino-O-metil benzil alkohol, 2-(2’-amino-benzilamino) benzil alkohol, serta 2-(2’ -amino-benzil)-O-metil-benzil alkohol (Chakravarty & Dastidar, 1982).
NH2
Gambar 2.2 Struktur Alkaloid Justicia gendarussa Burm. f. (Chakravarty,
et al.,1981).
2.1.5 Kegunaan Tanaman
Daun tanaman Justicia gendarussa Burm. f. pada umumnya digunakan sebagai obat penawar racun. Dalam bentuk ramuan tradisional, daun-daun ditumbuk bersama cuka dan merica digunakan untuk sakit kepala 2-(2’-amino-benzylamino)- O- metil-benzil alkohol
akibat pilek dan dengan kapur sirih dan merica untuk encok (rheumatik). Daun gandarusa, adas pulasari dan kapur yang digiling hingga menjadi bubur, digunakan sebagai obat gosok jika merasa sakit atau pegal pada tulang-tulang dan pinggang (Heyne, 1987).
Bagi orang Melayu, daun gandarusa terkenal sebagai obat encok dan sakit pinggang, daun yang ditumbuk bersama merica putih digunakan sebagai obat yang memperlancar datang bulan. Air rebusan daun gandarusa dapat mengeluarkan keringat dan mencegah demam. Di Sulawesi daunnya digunakan seb.agai obat cuci perut. (Heyne, 1987).
Di Irian Jaya, daun dan akar direbus dan diminum setidaknya 2 kali sebulan bagi suami untuk kontrasepsi atau KB. (Moeso dan Agus, 1985).
2.1.6 Bioaktivitas daun Justicia gendarusa Burm. f
fertilisasi (Prajogo dkk, 1998a). Penelitian fraksi diklormetan dan ekstrak metanol ternyata menyebabkan penurunan aktivitas akrosin dan β -glukosidase kelinci dan secara kualitatif menyebabkan sifat inhibitor hialorunidase pada testis sapi (Prajogo dkk, 1998b).
Pemberian fraksi air daun gendarusa pada mencit jantan dengan dosis per oral 26.06 mg/ 20 g BB; 18,39 mg/ 20 g BB; 3,47 mg/ 20 g BB dan 3,13 mg/ 20 g BB atau 1/12, 1/17, 1/90 dan 1/100 LD50 satu kali sehari selama 1,5 kali siklus spermatogenesis menyebabkan hambatan aktivitas enzim hialorunidase pada kumulus ooforus sehingga terjadi hambatan penetrasi spermatozoa pada mencit (Arif, 2005).
Uji toksisitas akut (LD50) dan uji teratogenik ekstrak etanol 60 % daun gendarusa dengan dosis 17,83 g/kg BB, dan fraksi air bebas alkaloid dengan dosis 15,63 g/kg BB pada mencit galur Balb C, termasuk kategori praktis tidak toksik dan tidak menyebabkan efek teratogen (Prajogo dkk, 2008).
2.1.7 Standarisasi ekstrak etanol daun Justicia gendarussa Burm. f.
Penentuan parameter standar umum ekstrak etanol 70 % daun
-Kadar minyak atsiri : 0,59 % + 0,01 -Cemaran logam berat : Hg = 0,000 mg/kg
As = 0,00 mg/kg Pb = 1,673 ppm Cd = 0,184 ppm
Parameter standar umum simplisia daun Justicia gendarusa sama dengan parameter standar umum yang ada di buku Materia Medika Indonesia. Untuk penetapan kadar gendarusin A dalam ekstrak dilakukan menggunakan metode HPLC. Dari penetapan tersebut didapatkan kadar gendarusin A sebesar 0,42 % + 0,01 (Bagus, 2012).
2.2 Tinjauan Tentang Senyawa Flavonoid
2.2.1 Kegunaan Flavonoid
Sebagai pigmen bunga, flavonoid berperan jelas dalam menarik burung dan serangga penyerbuk bunga. Beberapa flavonoid tanpa warna, tetapi flavonoid yang menyerap sinar UV barangkali penting juga dalam mengarahkan serangga. Banyak peranan lain flavonoid pada tanaman yang mengandungnya, diantaranya adalah pengaturan tumbuh, pengaturan fotosintesis, kerja antimikroba dan antivirus, dan kerja terhadap serangga. Beberapa flavonoid, seperti jenis fitoaleksin lain, merupakan komponen abnormal yang hanya dibentuk sebagai tanggapan terhadap infeksi atau luka dan kemudian menghambat fungus yang menyerangnya. Beberapa flavonoid yang dihasilkan oleh tumbuhan polong meng-imbas gen pembintilan dalam bakteria bintil penghambat nitrogen, sementara flavonoid yang lain membalikkan pengaktifan tersebut (Markham, 1988)
Efek flavonoid terhadap bermacam-macam organisme sangat banyak macamnya dan dapat menjelaskan mengapa tumbuhan yang mengandung flavonoid banyak dipakai dalam pengobatan tradisional (Markham, 1988).
2.2.2 Struktur Dasar Flavonoid
O
Gambar 2.3 Struktur dasar flavonoid (Markham, 1988).
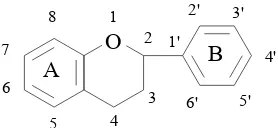
Susunan tersebut dapat menghasilkan tiga jenis struktur, yaitu diarilpropan atau flavonoid, 1,2-diarilpropan atau isoflavon dan 1,3-diarilpropan atau neoflavonoid. Istilah flavonoid dikenal sebagai suatu golongan besar senyawa yang berasal dari kelompok senyawa yang paling umum, yaitu senyawa flavon (Markham, 1988). Sistem penomoran untuk turunan flavonoid sebagai berikut:
Gambar 2.4 Sistem penomoran untuk turunan flavonoid.
2.2.3 Aglikon Flavonoid
Gambar 2.5 Beberapa aglikon flavonoid
2.2.4 Flavonoid O-glikosida
Glukosa adalah gula yang paling umum terlibat. Galaktosa, ramnosa, xilosa arabinosa sering juga terdapat. Sedangkan gula lain yang kadang-kadang dotemukan adalah alosa, manosa, fruktosa, apiosa, asam glukuronat dan galakturonat (Markham, 1988).
2.2.5 Flavonoid C-glikosida
Gugus gula juga dapat terikat pada atom C flavonoid, yaitu pada inti benzena dengan suatu ikatan karbon-karbon yang tahan asam (dibandingkan dengan O-glikosida). Glikosida yang demikian disebut favonoid C-glikosida. Gula yang terikat hanya ditemukan pada atom C nomor 6 dan 8 dalam inti flavonoid. Jenis gula yang terlibat jauh lebih sedikit ketimbang jenis gula pada O-glikosida, biasanya dari jenis glukosa, galaktosa, ramnosa, xilosa dan arabinosa (Markham, 1988).
2.2.6 Sifat dan Kelarutan Flavonoid
2.3 Tinjauan tentang Gendarusin A
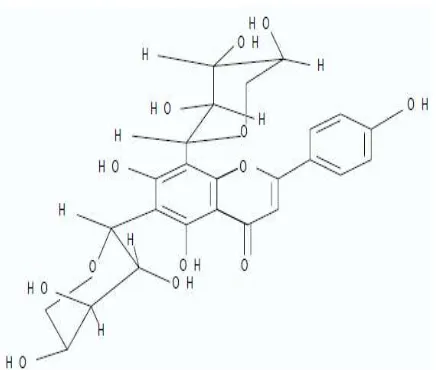
Gendarusin A merupakan komponen mayor yang terkandung dalamtanaman Justicia gendarussa Burm. f. Nama lain dari gendarusin A adalah 6,8-di-α-L-arabinopiranosil-4’,5,7 trihidroksiflavon atau 6,8 -diarabinosilapigenin yang mana senyawa tersebut digolongkan dalam kelompok di-C-glycosyl flavonoids (Markham & andersen, 2006). Selain senyawa tersebut, dalam tanaman Justicia gendarussa Burm. f. Juga terdapat komponen minor yang salah satunya adalah 6-α -l-arabinopiranosil-4’,5,7-trihidroksi-8-β-D-silopiranosilflavon atau 6-arabinosil-8 – silosilapigenin yang kemudian dikenal dengan gendarusin B (Prajogo, 2002).
Hasil isolasi dan purifikasi gendarusin A dari tanaman Justicia gendarussa Burm. f. yang telah dilakukan menunjukkan bahwa gendarusin A memiliki beratmolekul sebesar 535. Pada prosesnya dilakukan analisis dari senyawa mayor 40 mg dengan menggunakan 1H-13C NMR, Varian Unity INOVA 500 MHZ.
Gambar 2.6 Struktur molekul 6,8-di-α-L-arabinopiranosil-4’,5,7 -trihidroksi-flavon atau 6,8-diarabinosil-apigenin dikenal sebagai gandarusin
A (Prajogo, 2002)
Gambar 2.7 Struktur molekul 6-α-L-arabinopiranosil-4’,5,7-trihidroksi-8- β-D-silopiranosilflavon atau 6-arabinosil-8-silosilapigenin dikenal dengan
Berdasarkan penelitian yang telah dilakukan diketahui bahwa gendarusin A mempunyai aktivitas pencegahan penetrasi spermatozoa in vitro. Hal tersebut ditunjukkan dari hasil uji aktivitas in vitro gendarusin A dengan metode IVF. Hasil uji fertilisasi in vitro (IVF) dari komponen major flavonoid murni (gendarusin A) J.gendarussa pada spermatozoa epididimis mencit in vitro menunjukkan hasil yang positif, yakni tidak terjadinya fertilisasi selama 5 jam inkubasi (Prajogo, 2002).
2.4 Penelitian sebelumnya tentang Gendarusin A dalam Urin
Penelitan kedua dilakukan oleh Saifullah tahun 2010 tentang deteksi gendarusin A dalam urin pria fértil pada hari ke-144 setelah pemberian kapsul ekstrak etanol 70% daun Justicia gendarussa Burm F selama 72 hari. Proses spermiogenesis pada pria berlangsung selama 72 hari. Tujuh subyek (n=7) pria diberi perlakuan dengan mengkonsumsi kapsul yang mengandung 450,5 mg ekstrak etanol 70% daun Justicia gendarussa Burm F selama 72 hari. Lalu 72 hari sebelumnya subyek tidak diberi perlakuan, digunakan sebagai masa rekoveri. Penelitian menggunakan metode HPLC dengan kolom Waters Novapak C-18, kondisi fase gerak isokratik metanol: air (30:70), kecepatan alir 1,0 ml/menit, suhu kolom 30 oC, dan panjang gelombang 270 nm. Waktu retensi stándar gendarusin A sekitar 11 menit, LOD 0,0963 ug/ml, dan LOQ 0,3208 ug/ml. Hasil yang diperoleh adalah konsentrasi gendarusin A dalam urin subyek pada hari ke-72 (jam kelima) 37,530-149,625 ug (rata-rata 89,936 + 50,13 ug). Pada hari ke-144 setelah perlakuan tidak terdeteksi senyawa gendarusin A dalam urin (konsentrasi < LOD).
2.5. Bioavaibilitas, Absorbsi, Distribusi, Metabolisme dan Eksresi dari
Flavonoid.
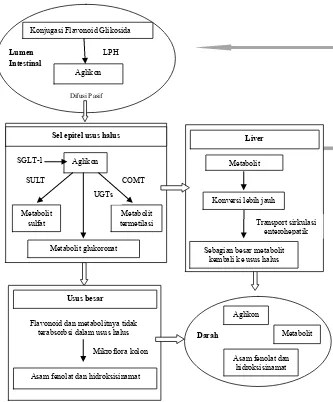
Gambar 2.8. Skema bioavaibilitas, absorbsi, distribusi, metabolisme dan eksresi dari flavonoid (Bageta et al, 2012).
Konjugasi Flavonoid Glikosida
Dari gambar diatas secara singkat dapat dijelaskan mengenai metabolisme flavonoid dari tumbuhan setelah pemberian oral. Flavonoid yang terkonjugasi dengan glikosida akan mengalami hidrolisis oleh Lactase Phloridizin Hydrolase (LPH) di brush border dari sel epitel usus halus menghasilkan aglikon. LPH bekerja pada substrat yang luas dengan spesifikasi pada flavonoid-glukosida dan menghasilkan aglikon yang kemudian menembus sel epitel dengan mekanisme difusi pasif sebagai hasil dari peningkatan lipofilisitas. Hidrolisis alternatif dilakukan oleh cytosolic β
glucosidase (CBG) dengan mekanisme transport aktif menggunakan
sodium-dependent glucose transporter SGLT1 untuk membawa glukosida yang polar ke dalam sel epitel. Sebelum mencapai perjalanan lebih lanjut dalam aliran darah aglikon tersebut mengalami metabolisme membentuk sulfat, glukoronat, dan atau metilasi metabolit dengan masing-masing aksi dari enzim sulfotransferases (SULT), uridine-5’-diphosphatase glucoronosyl-transferases (UGTs), dan catechol-O-methyltransferases
dan hidroksisinamat. Senyawa tersebut kemudian diabsorbsi dan mungkin mengalami metabolisme fase 2 di enterosit dan atau dalam liver sebelum diekskresikan melalui urin dalam jumlah yang besar dimana sebagian besar merupakan kelebihan metabolit flavonoid yang menembus sistem sirkulasi melewati usus halus (Bageta et al, 2012).
Deglikosilasi pada glikosida flavonoid merupakan metabolisme fase I. (Day et al, 2000). Dengan menggunakan usus halus manusia dan ekstrak bebas sel hati untuk mengetahui apakah ada aktivitas glukosidase terhadap glikosida flavonoid. Beberapa tetapi tidak semua glikosida flavonoid dihidrolisa oleh usus halus dan ekstrak hati. Setelah diabsorpsi, flavonoid berikatan dengan albumin dan diangkut ke hati melalui vena porta (Manach et al, 2005).
2.6 Tinjauan Tentang Analisis Biotransformasi Flavonoid Dengan
LC-MS/MS.
secara alami pada sampel urin setelah konsumsi menu dengan rata-rata kandungan isoflavon sebesar 0,5-100 mg/hari selama 11 hari. Tidak perlu dilakukan pretreatment terhadap sampel, selain penambahan standar internal dan penyesuaian pH. Urin disuntikkan langsung ke kolom analitis. Jumlah rata-rata daidzein dan bentuk konjugatnya berada sampai kadar 20% dari nilai terhidrolisis. Konsentrasi dari aglikons bebas hingga 22% dari genistein dan daidzein 18% dari yang diamati. Rata-rata jumlah yang teramati adalah 54% 7-glucuronide, 25% 4’-glucuronide, 13% monosulfat, daidzein bebas 7%, 0,9% sulfoglucuronide, diglucuronide 0,4%, dan disulfat <0,1% (Clarke et al., 2002).
Keberhasilan metode analisis juga ditentukan pula oleh faktor preparasi sampel selain faktor instrumentasi, termasuk proses ekstraksi dan purifikasi. Urin mempunyai kandungan bermacam-macam konjugat, molekul-molekul sisa dalam darah dan senyawa residu tubuh yang siap di ekskresi dengan matriks yang kompleks. Dibutuhkan suatu tahapan yang dapat memisahkan analit dari matriks sampel, termasuk ekstraksi dan purifikasi yang umumnya bertingkat, lama dan membutuhkan waktu yang lama. Dengan metode LC-MS/MS preparasi sampel dan waktu analisis yang lebih singkat, jumlah sampel lebih sedikit, memiliki sensitivitas yang rendah sampai level ppb, mampu menganalisa berbagai macam cemaran, deteksi yang sanagt selektif dengan hasil analisis yang terpercaya (Yuwono, 2009).
)
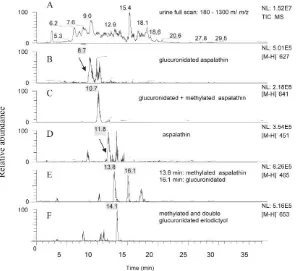
Gambar 2.10 Contoh kromatogram LC-ESI-MS/MS dari sampel urin setelah konsumsi ekstrak rooibos (16,3 % aspalathin) dari subyek babi pada hari ke-7 penelitian. Total Ion Current (TIC) dari sampel urin tanpa treatmen enzimatik (A), ekstrak ion kromatogram dari 6 metabolit (B-F) sebagai berikut: (B) [M-H]- m/z 627 glucuronidated aspalathin, (C) [M-H] -m/z 641 glucuronidated dan methylated aspalathin, (D) [M-H]- m/z 451
2.7 Tinjauan Tentang Urin
Urin atau air seni atau air kencing adalah cairan sisa yang diekskresikan oleh ginjal yang kemudian akan dikeluarkan dari dalam tubuh melalui proses urinasi. Ekskresi urin diperlukan untuk membuang molekul-molekul sisa dalam darah yang disaring oleh ginjal dan untuk menjaga homeostasis cairan tubuh. Urin disaring di dalam ginjal, dibawa melalui ureter menuju kandung kemih, akhirnya dibuang keluar tubuh melalui uretra.
Urin secara kontinyu dibentuk oleh ginjal. Fungsi utama urin adalah untuk membuang zat sisa seperti racun atau obat-obatan dari dalam tubuh. Komposisi urin berubah sepanjang proses reabsorpsi ketika molekul yang penting bagi tubuh, misal glukosa, diserap kembali ke dalam tubuh melalui molekul pembawa.
Umumnya, urin terdiri dari urea dan bahan-bahan organik maupun anorganik lain yang terlarut dalam air. Variasi dalam konsentrasi senyawa-senyawa tersebut dapat terjadi sebagai akibat dari faktor seperti asupan makanan, aktivitas fisik, metabolisme tubuh, fungsi endokrin, dan bahkan posisi tubuh. Urea, sisa produk metabolisme, dihasilkan di hati dari pemecahan protein dan asam amino, terhitung hampir setengah dari total komponen yang terlarut dalam urin. Senyawa organik lain termasuk kreatinin dan asam urat. Komponen anorganik utama yang terlarut yakni klorida, natrium dan kalium.
dipengaruhi oleh asupan makanan. Senyawa-senyawa lain yang ditemukan dalam urin ternasuk hormon, vitamin, dan obat-obatan. Meskipun senyawa-senyawa tersebut bukan merupakan bagian dari filtrat plasma, urin mungkin juga mengandung elemen berbentuk seperti sel, zat warna, kristal, mukus, dan bakteri. Peningkatan dari jumlah elemen bentukan tersebut sering mengindikasi adanya penyakit.
Urin normal memiliki volume sekitar 600-2500 ml dalam 24 jam, rata-rata 1200 ml, dengan pH normal sekitar 4,6-8,0 (rata-rata pH 6,0). Urin segar nampak jernih hingga sedikit berkabut, berwarna kuning pucat-kuning sawo, dan berbau khas (Fischbach, 2000).
2.7.1 Validitas Data Urin
Untuk mendapatkan studi ekskresi kumulatif melalui urin yang valid pada pemberian obat dosis tunggal maka harus dipenuhi kriteria sebagai berikut ( Ritschel, 1986 ):
1. Obat harus diekskresikan melalui ginjal paling sedikit 10% dalam bentuk tidak berubah (utuh).
2. setelah berpuasa semalam, satu jam sebelum percobaan dimulai, subjek diberi minum 400 ml air untuk pengosongan kandung kemih. Kemudian 200 ml air diberikan bersama-sama dengan pemberian obat, diikuti dengan 200 ml setiap selang waktu satu jam selama empat jam berikutnya.
4. Untuk masing-masing sampel urin yang didapat harus dicatat dengan tepat volume dan waktunya.
5. Jika urin tidak langsung dianalisis, maka urin sebanyak 20-25 ml diberikan pengawet sebanyak 0,5-1 ml toluen dan segera dimasukkan lemari es.
6. Semua cuplikan urin setiap waktu harus dikumpulkan, tidak boleh ada yang hilang.
7. Urin harus dikumpulkan sampai semua obat dalam bentuk tidak berubah terekskresi sempurna. Oleh karena itu maka paling sedikit pengambilan sampelnya selama 7-10 kali waktu paruh eliminasinya.
2.8 Tinjauan Tentang LC-MS/MS
Kromatografi adalah teknik pemisahan fisik suatu campuran berdasarkan pada perbedaan migrasi masing-masing analit senyawa pada fase diam dibawah pengaruh fase gerak. Dasar pemisahan kromatografi adalah terjadinya perubahan dari sistem kesetimbangan distribusi statik molekul senyawa ke sistem kesetimbangan distribusi dinamik diantara fase diam dan fase gerak yang berkesinambungan. Karena molekul analit pada kondisi variabel kromatografi tertentu mempunyai tetapan kesetimbangan distribusi dinamik yang khas, maka akan terjadi pola pemisahan yang tetap (Yuwono, 2009)
Kromatografi cair merupakan dasar teknik pemisahan di bidang sains dan terkait dengan kimia. Kromatografi cair dapat dengan aman memisahkan senyawa organik dengan rentang yang sangat luas yaitu mulai dari metabolit obat dengan molekul kecil sampai peptida dan protein.
Detektor umum dari kromatografi cair termasuk indeks refraksi, elektrokimia, fluoresensi, dan ultraviolet-visible (UV-Vis). Beberapa dari detector tersebut memberikan data dua dimensi yaitu data yang menunjukkan kekuatan signal sebagai fungsi atas waktu. Detektorfluorosensi dan diode-array UV-Vis menghasilkan data tiga dimensi yaitu tidak hanya kekuatan signal namun data spectra dari masing-masing poin waktu. Mass spectrometers juga menghasilkan data tiga dimensi. Selain kekuatan signal juga menghasilkan data massa spektral yang dapat memberikan informasi berharga tentang struktur, berat molekul, identifikasi, jumlah, dan kemurnian sampel. Data spektral massa menambahkan spesifitas yang meningkatkan kepercayaan dalam hasil dari analisis baik kualitatif dan kuantitatif. Untuk sebagian besar senyawa yang di analisis dengan spektrometer massa jauh lebih sensitif dan lebih spesifik daripada semua LC detektor lainnya. Hal ini dapat menganalisis senyawa yang tidak memiliki kromofor yang cocok. Hal ini juga dapat mengidentifikasi komponen dalam kromatografi dengan peak yang belum terselesaikan, mengurangi kebutuhan untuk kromatografi yang sempurna.
mengidentifikasi, mengkonfirmasi, dan mengukur senyawa. Beberapa spektrometer massa (mass spectrometers) memiliki kemampuan untuk melakukan beberapa langkah spektrometri massa pada sampel tunggal. Hal tersebut bisa menghasilkan spektrum massa,memilih secara selektif ion tertentu dari spektrum, fragmen ion, dan menghasilkan spektrum massa lainnya serta mengulang seluruh siklus beberapa kali. Spektrometer massa seperti secara harfiah dapat mendekonstruksi molekul kompleks sepotong demi sepotong sampai struktur dapat ditentukan.
2.8.1 Instrumentasi
Spektrometer massa bekerja dengan molekul peng-ion dan kemudian menyortir dan mengidentifikasi ion sesuai dengan massa-muatan (m/z) rasio. Dua komponen kunci dalam proses ini adalah sumber ion yang menghasilkan ion, dan analiser massa, yang menghasilkan berbagai macam ion. Beberapa berbagai jenis sumber ion umumnya digunakan untuk LC/MS. Masing-masing cocok untuk berbagai kelas senyawa. Beberapa yang berbeda jenis dari analiser massa juga digunakan. Masing-masing memiliki keuntungan dan kerugian tergantung pada jenis informasi yang dibutuhkan.
2.8.2 Sumber Ion.
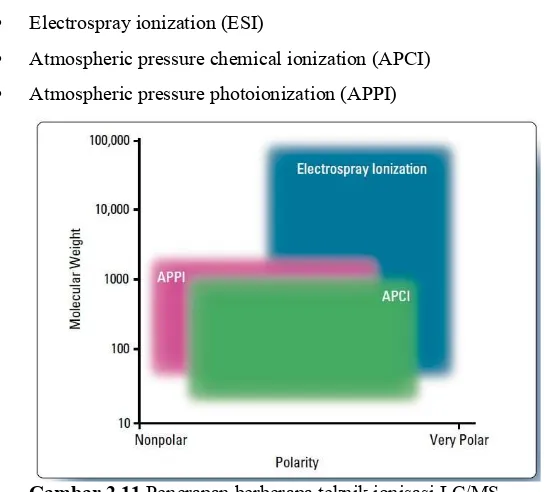
Electrospray ionization (ESI)
Atmospheric pressure chemical ionization (APCI)
Atmospheric pressure photoionization (APPI)
Gambar 2.11 Penerapan berberapa teknik ionisasi LC/MS
2.8.3 Mass Analyzers (Analiser massa).
Meskipun dalam teori apapun jenis analiser massa dapat digunakan untuk LC / MS ada empat jenis:
Quadrupole
Time-of-flight
Ion trap
Fourier transform-ion cyclotron resonance (FT-ICR or FT-MS) paling sering digunakan.
2.8.4 Collision-Induced Dissociationand Multiple-Stage MS
(Disosiasi induksi tabrakan dan tahap-tahap MS)
Teknik atmospheric pressure ionization (API) yang dibahas adalah semua teknik yang relatif lunak. Terutama menghasilkan:
• Molekul ion M+ atau M -• Molekul terprotonasi [M+H]+ • Ion adisi sederhana [M+Na]+
• Ion yang mewakili kehilangan yang sederhana seperti hilangnya air [M+H-H2O]+
Informasi tentang berat molekul yang dihasilkan sangat berharga, namun informasi struktural pelengkap sering dibutuhkan. Untuk memperoleh informasi struktural, ion analit yang terfragmentasi karena bertabrakan dengan molekul netral dalam proses yang dikenal sebagai
collision induced dissociation (CID) atau collisionally activated dissociation (CAD). Tegangan yang diterapkan pada ion analit untuk menambah energi untuk tabrakan dan menciptakan fragmentasi lebih banyak.
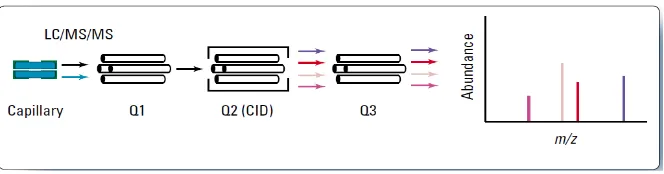
Gambar 2.12 MS/MS dengan spektrometer massa triple-quadrupole. Tahap ketiga (quadrupole atau FPT) maka menghasilkan spektrum yang dihasilkan produk ion. Hal ini juga dapat melakukan pemantauan ion terpilih dari hanya beberapa ion produk ketika mengkuantifikasi senyawa target. Dalam perangkap ion dan FT-ICR spektrometer massa, semua ion kecuali ion prekursor yang diinginkan dikeluarkan dari perangkap. Prekursor ion kemudian diberikan energi dan tabrakan untuk menghasilkan produk ion. Ini adalah teknik yang sangat kuat untuk menentukan struktur molekul.
2.8.5. Kolom Kromatografi
Kolom dengan kinerja yang tinggi yang dapat digunakan secara luas untuk pemisahan sampel merupakan jantung dari modern kromatografi cair.
1. Kolom untuk kiral kromatografi yang digunakan untuk memisahkan senyawa-senyawa kiral (isomer) yang mempunyai kolom packing seperti α-acid glycoprotein, cellulose tris
(3,5-dimethylphenylcarbamate), vancomycin. Kolom yang ter-packing
dengan α-acid glycoprotein merupakan jenis kolom kiral yang dapat memisahkan enansiomer (optis aktif) dan dapat bekerja secara stereoselektif (Corre et al, 1988). Vancomycin pada silica yang berfungsi sebagai sebagai chiral stationary phase (CSP) dapat memisahkan enansiomer dengan fase organik yang polar. (Svensson et al, 2000).
2. Kolom silika C-18 merupakan standar emas yang digunakan untuk RP-HPLC dengan material packing alkil yang lebih pendek C12 dan C8, kolom nitril (medium-polarity) untuk analit polar serta alkil yang lebih panjang seperti kolom C30 untuk obat yang hidrofobik. Octadecyl-silica (ODS) atau C-18 dapat digunakan secara luas untuk pemisahan mulai dari mikroanalisis sampai isolasi skala besar (Holcapek et al, 2008).
2.9 Metode Analisis Gendarusin A dalam Urin
KERANGKA KONSEPTUAL
3.1 Uraian Kerangka Konseptual
Daun Justicia gendarussa Burm. f telah digunakan oleh sebagian rakyat Irian Jaya sebagai obat kontrasepsi pria (Soerjowinoto & Pujorianto, 1985). Dari hasil penelitian diketahui bahwa dalam fraksi n-butanol daun gandarusa terdapat 12 komponen flavonoid dengan komponen mayor 6,8-di-α-L-arabinopiranosil-4’,5,7-trihidroksiflavon, yang kemudian dikenal dengan gendarusin A, salah satu bahan anti fertilitas dengan aktivitas pencegahan penetrasi spermatozoa in vitro dengan mekanisme penghambatan enzim hialuronidase (Prajogo, 2002).
Hasil uji klinik fase I yang dilakukan pada 36 pria normospermatozoa dengan hasil analisis fisik, fungsi dan kimia darah semua kondisi subyek tetap aman dan sehat setelah mendapat perlakuan selama 108 hari. Kemudian penelitian sejenis dilakukan pada uji klinik fase II. Setelah pemberian sediaan ekstrak etanol daun Justicia gendarussa
Burm. f. terhadap 6 subyek pria sehat menunjukkan harga parameter farmakokinetika gendarussin A menunjukkan t1/2 = 2,44-8,53 jam (rata-rata 4,44 + 2,14 jam) dan Kel = 0,08-0,28 jam-1 (rata-rata 0,18 + 0,07 jam). Serta penelitian pemberian kapsul ekstrak etanol 70 % daun Justicia gendarussa
sampel urin maupun sampel plasma masih menggunakan metode HPLC. Obat yang masuk ke dalam tubuh umumnya mengalami proses absorpsi, distribusi, pengikatan untuk sampai di tempat kerja dan menimbulkan efek. Kemudian, dengan atau tanpa biotransformasi, obat diekskresi dari dalam tubuh. Seluruh proses ini disebut proses farmakokinetik (Ganiswara, 1995). Proses farmakokinetik ini sangat kompleks dan sebagian besar obat akan mengalami proses biotransformasi di dalam tubuh manusia.
Pada penelitian ini subyek mendapat sediaan kapsul ekstrak etanol 70 % daun Justicia gendarussa Burm F yang mengandung 0,42% gendarusin A. Masing-masing subyek akan mendapatkan 2 kapsul gandarusa atau setara dengan 900 mg ekstrak daun Justicia gendarussa
Burm F. Setelah pemberian obat, sampel urin dari masing-masing subyek penelitian diambil pada interval waktu 0-24 jam dan dicatat waktu serta volume urin yang tertampung. Data tersebut dapat menggambarkan data kualitatif berupa deteksi gendarusin A yang terakumulasi dalam urin 24 jam setelah konsumsi ekstrak etanol daun Justicia gendarussa Burm F.
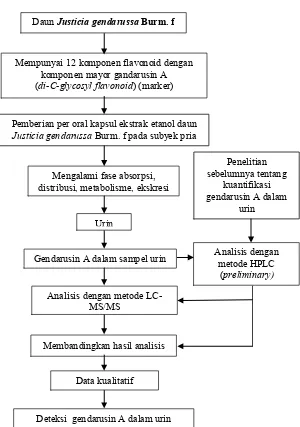
Gambar 3.1 Skema kerangka konseptual. Pemberian per oral kapsul ekstrak etanol daun
Justicia gendarussa Burm. f pada subyek pria Mempunyai 12 komponen flavonoid dengan
komponen mayor gandarusin A (di-C-glycosyl flavonoid) (marker)
Gendarusin A dalam sampel urin
Analisis dengan metode LC-MS/MS
Daun Justicia gendarussa Burm. f
Deteksi gendarusin A dalam urin Mengalami fase absorpsi, distribusi, metabolisme, ekskresi
Urin
Pemberian per oral kapsul ekstrak etanol daun
Justicia gendarussa Burm F
Kepada 4 volunteer pria
Catat waktu dan volume urin tertampung, simpan pada suhu -20 0C
Optimasi preliminary
dengan HPLC 1.Optimasi spektra standar gendarusin A dan apigenin 2.Optimasi serapan blanko urin 3.Optimasi serapan standar dalam
blanko urin
4.Optimasi serapan metabolit gendarusin A sampel
Dianalisis dengan
LC-MS/MS Metode kualitatif:
1. Tuning standar gendarusin A dan apigenin
2. Pemilihan fase gerak 3. LOD/LOQ
4. Identifikasi analit dalam sampel
METODE PENELITIAN
4.1 Jenis Penelitian Eksperimental
4.2 Lokasi Penelitian
a. Pengambilan urin dilakukan di Laboratorium Dasar Bersama
Kampus B Universitas Airlangga Surabaya di bawah pengawasan
Dokter yang bersangkutan.
b. Optimasi serta identifikasi flavonoid dan metabolitnya dalam urin
dilakukan di Laboratorium Analisis Farmasi Universitas Airlangga
dan Laboratorium PT Angler BioChemLab Surabaya.
4.3 Bahan Penelitian 4.3.1 Bahan Obat
Kapsul ekstrak gandarussa (sediaan ekstrak etanol daun Justicia
gendarussa Burm. f. ) dibuat oleh PT. Sido Jodo. Merupakan sediaan kapsul
gandarusa yang mengandung 450,0 mg ekstrak.
4.3.2 Bahan Kimia
Bahan kimia yang dipakai dalam proses analisis adalah:
- Metanol untuk HPLC
- Standar apigenin (Merck SIGMA-ALDRICH Co)
- Senyawa marker gendarusin A Departemen Farmakognosi dan
Fitokimia Fakultas Farmasi Universitas Airlangga.
- Asetonitril
- Aqua for irrigation
4.4 Alat – alat
4.4.1 Treatmen dan Preparasi
- Beaker glass - Venoject
- Tabung reaksi - Apendorf
- Vorteks mixer - Microsyringe
- Sentrifuge -Vial
- Spuit injeksi -Filter holder
- Corong pisah -Ultrasonik
-Neraca analitik - Membran filter nylon 0,2 µm
-Gelas ukur
4.4.2 Instrumen Analisis
Instrumen yang digunakan dalam penelitian ini adalah
LC-MS/MS QTRAP 4000 series agilent Triple Quadrupole dan HPLC
Agilent 1100 dengan spesifikasi:
HPLC Agilent 1100:
- Agilent 1100 Series Diode Array Detektor G1315A
- HPLC Column Novapak Waters C18 3,9 X 150 MM 60 Å, 4 µm
- Guard Column
LC-MS/MS:
- Kolom eclipse plus C-18 4,6 x 50 mm 3,5 um
- Agilent QTRAP 4000 series MS Detector
4.5 Subyek Penelitian
Diperlukan 4 volunteer pria sehat. Jumlah tersebut berdasarkan
penelitian dari Courts dan Williamson tahun 2009 tentang identifikasi
adalah pria maka subyek dipilih pria saja. Subyek dari penelitian ini telah
menjalani proses skreening yaitu melakukan tes kesehatan yang dilakukan
oleh Kelompok Studi Kesehatan Reproduksi (KSKR) Fakultas Kedokteran
Universitas Airlangga. Sebelum penelitian seluruh subyek uji harus
menandatangani lembar pernyataan kesediaan (informed consent).
Penelitian ini dilakukan sesuai dengan ketentuan yang ada di Deklarasi
Helsinki dan disetujui oleh komite etik penelitian Fakultas Kedokteran
Universitas Airlangga.
A. Populasi
4 volunteer pria sehat pria sehat, usia 20 – 40 tahun.
B. Kriteria Inklusi
1. Telah melakukan pemeriksaan laboratorium dan
dinyatakan sehat.
Pemeriksaan laboratorium yaitu glukosa darah puasa dan
2 jam setelah makan, fungsi ginjal (kreatinin dan ureum),
fungsi hati (SGOT, SGPT) bagi subyek yang tidak
memiliki data laboratorium tersebut selama 3 (tiga) bulan
terakhir serta kholesterol total, koleserol-LDL,
trigliserida, kolesterol-HDL, viskositas darah dan agregasi
trombosit
2. Telah bersedia menandatangani informed consent sebelum
Tahap-tahap perlakuan terhadap subyek adalah sebagai berikut:
1. Subyek berjumlah 4 orang, masing-masing diberi sediaan kapsul
gandarusa dengan dosis 900 mg ekstrak (setara dengan 3,78 mg
gendarusin A) daun Justicia gendarussa Burm F (2 kapsul), sekali per
oral setengah jam sesudah makan pagi.
2. Subyek diharuskan puasa selama 8 jam sebelum diberikan kapsul
ekstrak etanol daun Justicia gendarussa Burm. f dan dilakukan
pengambilan urin blanko dari masing masing subyek sebelumnya.
3. Dilakukan karantina terhadap seluruh subyek penelitian selama 24 jam.
4. Setelah pemberian obat, sampel urin dari masing-masing subyek
penelitian diambil pada interval 0-24 jam, dicatat waktu serta volume
urin yang tertampung (Mullen et al, 2008)
5. Subyek disarankan untuk minum air putih sebanyak 250 ml setiap 30
menit setelah minum obat selama 2 jam.
6. Sampel urin dikumpulkan menjadi satu dan terpisahkan masing-masing
subyek serta dicatat waktu dan volume dari masing-masing poin
pengambilan urin.
7. Masing-masing sampel urin diambil menggunakan beaker besar dan
diukur volumenya dengan gelas ukur. Selanjutnya seluruh sampel urin
Sebelum dilakukan analisis dengan menggunakan LC-MS/MS
terlebih dahulu digunakan metode HPLC. Sebelumnya telah dilakukan
penelusuran pustaka untuk menentukan kondisi HPLC yang sesuai untuk
menganalisis gendarusin A dan bentuk aglikonnya yaitu apigenin, sebelum
dilakukan analisis lebih lanjut menggunakan LC-MS/MS.
4.7.1 Pemilihan Panjang Gelombang Maksimum
Instrument yang digunakan dalam analisis gendarusin A dilengkapi
dengan UV-VIS Detektor. Untuk mendapatkan tanggap detektor yang
optimum, analisis dilakukan pada panjang gelombang maksimum ( maks).
Pemilihan maksimum dilakukan dengan cara menginjekkan larutan baku gendarusin A dalam metanol ke dalam kolom HPLC dan dianalisa pada
yang berbeda yaitu pada 270, 254, dan 340 nm.
4.7.2 Optimasi Fase Gerak
Dilakukan pemilihan dan pengaturan perbandingan fase gerak
dengan berbagai komposisi yang memberikan hasil pemisahan terbaik. Fase
gerak yang pernah digunakan untuk analisis gendarusin A adalah fase gerak
metanol dan asam fosfat 0,2% dengan sistem gradien yang memberikan
waktu retensi gendarusin A yang tidak terlalu lama dan menghasilkan peak
gendarusin A yang tidak bertumpukan dengan peak komponen endogen urin
(Sihabuddin, 2009). Untuk optimasi selanjutnya dilakukan pemilihan fase
gerak lagi karena untuk mengindari buffer seperti asam fosfat pada
pemakaian LC-MS/MS. Optimasi fase gerak yang dilakukan dengan sistem
Fase gerak Komposisi fase gerak (% v/v)
Metanol Aquadest for HPLC
30 70
4.8 Optimasi Metode Pendahuluan (preliminary)
Optimasi preliminary dilakukan dengan menggunakan HPLC
untuk mengetahui pemisahan dan recovery dalam urin dari senyawa
gendarusin A. Hasil optimasi tersebut digunakan sebagai dasar analisis
dengan menggunakan metode LC-MS/MS. Optimasi tersebut dipergunakan
untuk melihat komponen matriks yang mempunyai pengaruh di analisis,
mengoptimasi cara ekstraksi, mengoptimasi fase gerak, dan melihat bila ada
interaksi yang terjadi dalam urin.
4.8.1 Optimasi Standar Gendarusin A dan Apigenin.
Membuat larutan baku induk dari standar gendarusin A 64 ppm
dalam 10 ml pelarut methanol dan apigenin 100 ppm 5 ml dalam pelarut
asetonitril dan aquadest. Selanjutnya dilakukan pengenceran dari kadar
tersebut menjadi kadar yang lebih kecil untuk diinjekkan ke dalam kolom
HPLC sebanyak 20 µl. Optimasi standar ini dilakukan untuk melihat waktu
retensi yang optimal untuk standar berdasarkan panjang gelombang dan fase
merupakan senyawa yang polar dan larut dalam metanol sedangkan
apigenin memiliki sifat yang kurang begitu polar dan tidak melarut dalam
metanol. Sehingga perlu adanya optimasi pelarut termasuk fase gerak dan
waktu retensi dari standar tersebut.
4.8.2 Optimasi Serapan Standar dan Blanko Urin
Optimasi serapan blanko urin ini dipergunakan untuk mengetahui
ada atau tidaknya peak yang muncul dari blanko urin yang mengganggu
analit. Blanko urin dipreparasi dengan cara ekstraksi terpilih. Hasil ekstraksi
kemudian diinjekkan ke dalam kolom HPLC. Diamati kromatogram yang
terjadi. Urin blanko ditambahkan larutan standar gendarusin A dengan
konsentrasi tertentu kemudian dipreparasi untuk selanjutnya diinjeksikan ke
dalam kolom HPLC. Diamati kromatogram yang terjadi sehingga diperoleh
prosen rekoveri dan selektivitasnya.
4.8.3 Uji Selektivitas
Uji selektivitas bertujuan untuk mengetahui pemisahan gendarusin
A dengan komponen-komponen lain yang terkandung dalam urin. Dapat
diketahui dengan menentukan resolusi (Rs), yaitu parameter yang
menggambarkan pemisahan kromatogram campuran dua analit yang
mempunyai waktu retensi berbeda. Resolusi ini ditentukan dengan
menginjekkan blanko urin dan larutan gendarusin A yang ditambahkan
dengan konsentrasi tertentu ke dalam kolom HPLC. Resolusi mengukur
perbedaan waktu retensi dari dua macam analit yang dibagi dengan lebar
dasar puncaknya (W). Resolusi dapat dihitung menggunakan rumus :
tR = Waktu yang dibutuhkan solut untuk menempuh jarak sepanjang kolom
W = lebar dasar puncak dan diukur antara titik potong garis singgung pada
kedua sisi puncak dengan poros horizontal.
Untuk mendapatkan pemisahan yang baik, harga resolusi > 1,5.
Apabila dua puncak menghasilkan harga resolusi yang kecil atau bahkan <
1, maka dua puncak tersebut saling berhimpitan (over lapping) (Mulja dan
suharman, 1995).
4.8.4 Penentuan Perolehan Kembali(recovery)
Menentukan kembali konsentrasi gendarusin A dalam urin
(rekoveri) dibuat larutan gendarusin A dalam urin, yaitu urin blanko dan
larutan baku gendarusin A dengan konsentrasi 6,4 dan 25.6 ppm
masing-masing direplikasi sebanyak tiga kali lalu diinjekkan ke dalam kolom HPLC
sebanyak 20 µl. Rekoveri dihitung menggunakan dengan rumus berikut:
Prosen rekoveri yang diperoleh kemudian di rata-rata. Nilai prosen rekoveri
yang memenuhi syarat adalah 80-110 % (Huber, 2004)
4.9 Penentuan Kondisi LC-MS/MS.
4.9.1 Optimasi Kondisi Kromatografi.
Optimasi kondisi kromatografi dilakukan untuk mendapatkan
pemisahan analit yang baik, dengan parameter α dan Rs. Optimasi
dilakukan dengan menggunakan sistem elusi yang terbaik, laju alir dan
temperatur kolom yang menghasilkan pemisahan metabolit dalam urin
optimal.
Fase gerak untuk LC-MS/MS dioptimasi dengan menggunakan
HPLC dan digunakan fase gerak yang sama dengan hasil optimasi tersebut.
4.9.3 Optimasi Kondisi MS
Electrospray Ionization (ESI) LC-MS/MS dioptimasi dengan
kondisi tertentu. Dilakukan tuning dengan infusi standar gendarusin A dan
apigenin ke dalam vakum ionisasi untuk memperoleh spektrum masa dan
kondisi MRM yang optimal. Kriteria identifikasi: analisis dengan
menggunakan MRM (Multiple reaction monitoring) menghasilkan rasio ion
dengan penyimpangan maksimum 20 %.
Optimasi kondisi MS ini dapat memberikan respon yang optimal
dalam analisis metabolit dalam urin. Berupa optimasi drying gas flow,
drying gas temperature, nebulizer gas, Vcap, fragmentor. Analisis metabolit
ekstrak gendarusa menggunakan ion spesifik yang merupakan hasil
fragmentasi MS/MS. Untuk memperoleh ion spesifik dalam analisis
LC-MS/MS dilakukan dengan mode scan tipe: MS2 produk ion. Selanjutnya
dilakukan optimasi collision energy untuk melihat energi yang diperlakukan
untuk menghasilkan product ion dengan jumlah maksimal (Yuwono, 2009).
4.9.3 Penentuan LOD dan LOQ
Penentuan batas deteksi (LOD) dan batas kuantifikasi (LOQ)
bertujuan untuk mengetahui konsentrasi analit terendah yang dapat
dideteksi, sedangkan penentuan batas kuantifikasi bertujuan untuk
mengetahui konsentrasi analit terendah dalam sampel yang dapat ditentukan
dengan presisi dan akurasi yang dapat diterima pada kondisi eksperimen
menghubungkan konsentrasi pada y-intersep ditambah 2,33 dikalikan
standar deviasi dari analisis dalam laboratorium. Sedangkan batas
kuantifikasi (CCβ) dihitung dengan menambah konsentrasi pada batas
deteksi ditambah 1,64 kali standar deviasi dari analisis dalam laboratorium
(Council Directive 96/23/EC Europen Community).
4.10 Preparasi Sampel
1. 2-5 ml urin (pada masing-masing interval dikumpulkan) ditambah
metanol (1:1, v/v), diultrasonikasi selama 15 menit dalam tabung.
2. Sampel kemudian divortex selama 5 menit lalu disentrifuse dengan
kecepatan 4.000 rpm selama 10 menit.
3. Supernatan yang diperoleh dikumpulkan pada tabung yang berbeda,
proses tersebut (tahap 1-2) diulang dua kali.
4. Supenatan tersebut dipekatkan menggunakan gas nitrogen lalu
direkonstitusi kembali dengan metanol 500 ul dan diultrasonikasi
selama 10 menit.
5. Sampel kemudian disentrifuse dengan kecepatan 6.000 rpm selama 10
menit, supernatan disaring menggunakan membran filter nylon 0,2 m
kemudian 20 l supernatant diinjeksikan ke dalam HPLC. (Sihabuddin,
2009)
4.11 Pengolahan Data
Standar gendarusin A dan apigenin dilakukan infusi ke dalam MS
untuk menentukan MRM pada kondisi tuning optimal. Dipilih kelimpahan
maka sampel hasil preparasi diidentifikasi dengan tipe skaning MRM untuk
mencari bentuk gendarusin A dan apigenin yang mungkin muncul dalam
sampel. Konfirmasi identifikasi dari analit yang muncul berdasarkan 2