PENDAHULUAN Latar Belakang
Protein berasal dari bahasa yunani yaitu proteo (Geraldus Mulder 1802), yang bearti yang utama atau yang di dahulukan. Protein merupakan salah satu kelompok bahan makronutrien yang sangat dibutuhkan oleh tubuh makhluk hidup. Berbeda dengan karbohidrat dan lemak, protein berperan lebih penting dalam pembentukan biomolekul daripada sumber energi. Meski pun demikian protein selain berfungsi sebagai zat pembangun dan pengatur juga berfungsi dalam pengganti energy saat kekurangan karbohidrat dengan memecahnya menjadi asam-asam amino. Protein memiliki unsur molekul C, H, O, dan N. namun terkadang beberapa ptein juga megandung unsur S, P, dan Fe.
Sifat protein sangant mudah dalam hal bentuk fisik maupun aktivitas biologis karna protein memiliki molekul yang sangat besar perubahan ini juga biasa disebut dengan Denaturasi. Adapun beberapa factor yang dapat menyebabkan perubahan dari sifat protein yaitu seperti panas, asam, basa, pelarut organik, pH, garam, logam berat, maupun sinar radiasi radioaktif. Selain itu protein juga bersifat ion zwiter karna protein mengandung muatan ion positif maupun negative dan tiap protein memiliki pH tertentu yang biasa disebut dengan pH isoiletrik yang berkisar antara 4 hingga 4,5 dan bermuatan 0.
Protein juga bersifaat amfoter yaitu adanya gugus amino yang bersifat basa dan gugus karboksil yang bersifat asam. ikatan peptida terbentuk karena sifat amfoternya, maka dua molekul asam amino atau lebih dapat bersenyawa satu sama lain dengan melepaskan satu molekul air membentuk ikatan antara gugus karboksil (COOH-) asam amino yang satu dengan gugus amino (-NH2) yang lain disebut dengan ikatan peptida.
Tujuan
TINJAUAN PUSTAKA Susu Murni
Susu adalah cairan yang disekresikan oleh kelenjar ambing, berfungsi utama sebagai nutrisi yang kompleks untuk pertumbuhan dan perkembangan bayi manusia atau hewan yang baru lahir karena zat gizi yang dikandung sangat lengkap dengan perbandingan sempurna seperti karbohidrat, lemak susu, protein dari asam amino, mineral, dan vitamin. Komposisi susu terdiri dari air (87.20%), protein (3.50%), lemak (3.70%), abu (0.70%), bahan kering (12.80%), dan laktosa (4.90%) Badan standarisasi nasional, 2011). Karbohidrat susu sapi terdiri dari laktosa yaitu 5% dan hampir konsisten pada semua breed sapi. Protein susu sebagian besar terdiri dari kasein yaitu 8085%, jika pH susu menurun menjadi 4.6 maka kasein akan berubah menjadi lapisan endapan, bagian cairan endapan tersebut disebut whey. Kandungan lemak pada susu yaitu 3.5-5% dan bervariasi pada setiap breed serta sebagian besar terdiri dari trigliserida (Jay et al. 2005)
Sari Kedelai
Sari kedelai adalah cairan hasil ekstraksi protein biji kedelai dengan menggunakan air panas. Sari kedelai berwarna putih seperti susu dan bergizi tinggi mengandung protein, lemak, karbohidrat, mineral dan vitamin. Dalam pelaksanaan pembutan susu kedelai, teknologinya sangat sederhana, peralatan yang dibutuhkan seadanya dan mudah dipahami (Hartoyo, 2005).
Kandungan protein kedelai dipengaruhi oleh varietas kedelai yang digunakan sebagai bahan, jumlah air yang ditambahkan, jangka waktu dan kondisi penyimpanan, serta perlakuan panas. Semakin banyak jumlah air yang digunakan untuk mengencerkan susu maka akan semakin sedikit kadar protein yang diperoleh (Hartoyo, 2005).
Bubur kedelai disaring dan diperas dengan kain saring rangkap dua. Cairan yang diperoleh disebut sari kedelai (Hartoyo, 2005).
minyak dalam air. Kandungan protein maksimal dalam susu/ sari kedelai adalah 7%. Kandungan protein yang lebih dari angka tersebut akan menyebakan terbentuknya jendalan/gumpalan. Umumnya, kadar protein terlarut dalam susu kedelai berkisar antara 3% sampai 5%. Susu kedelai dengan konsentrasi protein terlarut lebih dari 7% akan menggumpal apabila dipanaskan pada suhu 70oC- 100oC selama lebih dari 10 menit.adapun sifat protein kedelai yang lain adalah akan menggumpal karena pengaruh asam (Suprapti, 2010).
Putih Telur
Albumin atau lazimnya disebut putih telur merupakan protein globular yang tidak rapat atau tersusun dalam aturan tertentu. Molekul air mudah menerobos ke ruang-ruang kosong dalam molekul protein. Protein globular dapat terdispersi dengan baik dalam air atau larutan garam, membentuk koloid, serta terpengaruh oleh asam, alkali dan panas. Albumin atau putih telur tersusun atas empat lapis yaitu bagian tipis luar, bagian kokoh, bagian tipis dalam dan lapisan khalsiferus.
Komposisi putih telur tersusun atas protein sebagai komponen utama. Kandungan lemak yang ada dalam putih telur dapat diabaikan, karena jumlahnya yang sangat sedikit. Kandungan karbohidrat dalam putih telur berupa karbohidrat bebas dan karbohidrat yang terikat dengan protein, sekitar 98% karbohidrat bebas dalam putih telur adalah glukosa. Albumin telur sebagai sumber protein yang murah yang dapat digunakan sebagai pengikat senyawa tanin yang dapat menyebabkan pencoklatan pada ekstrak (Rayner, 2002).
Protein
Protein berasal dari bahasa yunani yaitu proteos, yang bearti yang utama atau yang di dahulukan. Kata ini diperkenalkan oleh ahli kimia Belanda, Geraldus Mulder (1802-1880). Ia berpendapat bahwa protein adalah zat yang paling penting dalam setiap organisme (Ellya, 2010).
dimiliki oleh lemak atau karbohidrat. Molekul protein mengandung pula posfor, belerang dan ada jenis protein yang mengandung unsur logam seperti besi dan tembaga (Budianto, A.K, 2009).
Protein juga merupakan sumber energi tubuh, selain karbohidrat dan lemak,. Jika tubuh kekurangan energi, fungsi protein sebagai pembangun berkurang untuk menyediakan energi (Widodo, 2009).
Ciri-ciri Molekul Protein
1. Berat molekulnya besar, ribuan sampai jutaan sehingga merupakan suatu makro molekul.
2. Umumnya terdiri dari 20 macam asam amino.
3. Terdapat ikatan kimia lain yang menyebabkan terbentuknya lengkungan-lengkungan rantai polipeptida menjadi struktur tiga dimensi protein.
4. Strukturnya tidak stabil terhadap beberapa faktor seperti pH, radiasi, temperatur, medium pelarut organik dan deterjen.
5. Umumnya reaktif dan sangat spesifik, disebabkan terdapatnya gugusan samping yang reaktif dan susunan khas struktur makromolekul (Ellya, 2010).
Penggolongan Protein
Protein merupakan senyawa polipeptida yang tersusun dari berbagai jenis asam amino, sehingga sifat protein juga dapat ditentukan oleh sifat asam amino penyusunnya. Berdasarkan keanekaragaman penyusun struktur protein, maka penggolongan protein dilakukan dengan berbagai kriteria sebagai berikut:
Berdasarkan bentuk morfologisnya protein digolongkan atas dua golongan (Budianto, 2009), yaitu:
1. Protein serabut (fibrous protein) yaitu protein yang berbentuk serabut atau lempengan, terutama disusun oleh polipeptida primer dan sekunder. Contoh protein serabut adalah kolagen yang terdapat pada tulang rawan, miosin pada otot, keratin pada rambut, dan fibrin pada gumpalan darah. 2. Protein bulat (globular protein) yaitu protein yang berbentuk bulat atau
terdapat pada otot, serum, kuning telur; histon terdapat dalam jaringan-jaringan kelenjar timus, pankreas, dan protamin.
Berdasarkan fungsi protein (Almatsier, 2004), yaitu:
1. Penyusun Enzim, protein merupakan bagian terbesar pada enzim.
2. Protein Pengangkut, mampu mengikat, membawa, dan melepaskan molekul protein tertentu, misalnya hemoglobin mengangkut O2 dalam darah, lipoprotein mengangkut lipida dalam darah dan mioglobin mengangkut O2 dalam otot.
3. Protein pembangun, sebagai protein pembangun dan pengganti protein yang rusak pada organel atau jaringan. Contohnya glikoprotein, keratin, kolagen dan elastin.
4. Protein otot, protein yang mengontrol gerak oleh otot, misalnya miosin dalam otot, dinein dalam rambut.
5. Protein pertahanan tubuh, protein ini dikenal dengan imunoglobulin (Ig), dimana merupakan suatu protein khusus yang dapat mengenal, mengikat, dan menghancurkan benda-benda asing yang masuk dalam tubuh seperti virus, bakteri, dan sel asing, misalnya berbagai antibodi, fibrinogen (dalam proses pembentukan darah).
6. Protein hormon, sebagai pembentuk hormon, contohnya insulin.
7. Protein Racun, protein yang bersifat racun, misalnya risin dalam beberapa jenis beras, racun ular.
8. Protein Makanan, protein yang dijadikan sebagai cadangan energi, misalnya albumin, orizenin, dan sebagainya.
Akibat Kekurangan dan Kelebihan Protein
Akibat kekurangan protein
Dapat menyebabkan Kwashioskor, pertama kali diperkenalkan oleh Dr. Cecily Wiliams pada tahun 1993 di Ghana, Afrika. Penyakit ini lebih banyak terdapat pada usia dua hingga tiga tahun yang komposisi gizi makanannya tidak seimbang terutama dalam hal protein (Yuniastuti, 2008).
Gejala penyakit Kwashioskor (Widodo, 2009), adalah sebagai berikut: a. Pertumbuhan terhambat.
b. Otot-otot berkurang dan lemah.
d. Muka bulat seperti bulan (moonface). e. Gangguan psikimotor.
f. Nafsu makan kurang. g. Apatis.
Akibat kelebihan protein
Jika terlalu berlebihan mengkomsumsi protein juga akan sangat membebani kerja ginjal. Protein secara berlebihan tidak menguntungkan tubuh. Makanan yang tinggi proteinnya biasanya tinggi lemak sehingga menyebabkan obesitas.
Macam Sifat Protein 1. Denaturasi
Pada umumnya, protein sangat peka terhadap pengaruh-pengaruh fisik dari zat kimia, maka mudah mengalami perubahan bentuk. Perubahan atau modifikasi pada struktur molekul protein disebut dengan denaturasi. Hal-hal yang menyebabkan terjadinya denaturasi adalah panas, pH, tekanan, aliran listrik, dan adanya bahan kimia seperti urea, alkohol, dan sabun. Temperatur merupakan titik tengah dari proses denaturasi yang disebut dengan melting temperature (Tm) yang pada umumnya protein mempunyai nilai Tm kurang dari 100ºC, apabila diatas suhu Tm, maka protein akan mengalami denaturasi. Protein yang mengalami denaturasi akan menurunkan aktivitas biologinya dan berkurang kelarutannya, sehingga mudah mengendap (Yazid, 2006).
2. Ion zwiter dan pH isoelektrik
Larutan asam amino dalam air mempunyai muatan positif maupun negatif sehingga asam amino disebut ion zwiter. Setiap jenis protein dalam larutan mempunyai pH tertentu yang disebut pH isoelektrik (berkisar 4-4,5). Pada pH isoelektrik molekul protein mempunyai muatan positif dan negatif yang sama, sehingga saling menetralkan atau bermuatan nol. Pada titik isoelektrik, protein akan mengalami pengendapan (koagulasi) paling cepat (Yazid, 2006).
3. Sifat amfoter
protein bermuatan positif, sebaliknya dalam larutan basa gugus karboksilat bereaksi dengan ion OH-, sehingga protein bersifat negatif. Adanya muatan pada molekul protein menyebabkan protein bergerak dibawah pengaruh medan listrik (Yazid, 2006).
Titik Isoelektrik
Titik isoelektrik merupakan titik dimana derajaf keasaman saat ketika kehilanagn muatan oleh reaksi asam dan reaksi basa yang terjadi. Jadi saaat titik isoelektrik terjadi muatannya bernilai 0. Daya reaksi berbagai jenis protein terhadap asam dan basa tidak sama, tergantung dari jumlah dan letak gugus amino dan karboksil dalam molekul
Setiap jenis protein dalam larutan mempunyai pH tertentu yang disebut pH isoelektrik (berkisar 4-4,5). Pada pH isoelektrik molekul protein mempunyai muatan positif dan negatif yang sama, sehingga saling menetralkan atau bermuatan nol. Pada titik isoelektrik, protein akan mengalami pengendapan (koagulasi) paling cepat (Yazid, 2006).
MATERI DAN METODE Materi
Dalam praktikum ini menggunakan berbagai alat dan bahan. Alat-alat yang digunakan pada praktikum ini adalah beaker glass, botol selai, tabung reaksi, rak tabung reaksi, kertas indikator pH, magnetic stirrer, pipet, spoide, kompor dan panci Sedangkan bahan yang digunakan dalam praktikum kali ini yaitu larutan HCl 0,1 N, NaOH 0,1 N, HgCl2 jenuh, formaldehyde 10%, putih telur ayam ras, susu murni, sari kedelai, dan aquades.
Metode
Putih telur dimasukkan dalam tabung reaksi dengan bantuan corong kemudian diamati dan dicatat sifat fisiknya. Tabung reaksi dimasukkan ke dalam air yang mendidih beberapa lama kemudian diamati dan dicatat perubahan yang terjadi. Prosedur yang sama juga dilakukan pada sampel susu murni dan sari kedelai.
Reaksi dengan formaldehyde
Putih telur dimasukkan dalam masing-masing 5 tabung reaksi dengan bantuan corong secukupnyakemudian lakukan pengamatan dan catat sifat fisiknya. Larutan formaldehyde dimasukkan dalam masing-masing 5 tabung reaksi sebanyak 2, 4, 6, 8, dan 10 tetes. Diamati dan dicatat perubahan yang terjadi. Tabung reaksi dimasukkan ke dalam air yang mendidih selama beberapa lama kemudian diamati dan dicatat perubahan yang terjadi. Prosedur yang sama dilakukan pada sampel susu murni dan sari kedelai.
Pengendapan protein dengan logam berat
Putih telur dimasukkan dalam tabung reaksi dengan bantuan corong lalu kemudian diamati dan dicatat sifat fisiknya. Kemudian ditambahkan larutan HgCl2 jenuh sampai terlihat perubahan. Dicatat perubahan tersebut terjadi setelah diteteskan berapa HgCl2. Prosedur yang sama dilakukan pada sampel susu murni dan sari kedelai.
Pengamatan sifat amfoter
HASIL DAN PEMBAHASAN Hasil
Dari praktikum yang telah dilakukan tentang pengujian sifat protein,maka deperoleh hasil :
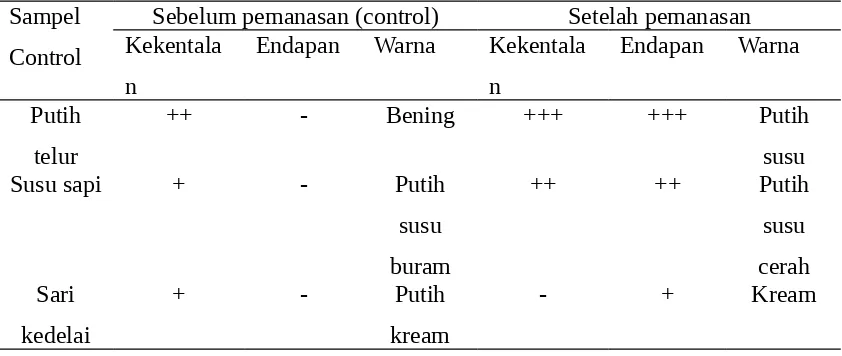
Table 1. Kelarutan Protein Terhadap Pemanasan
Sampel Control
Sebelum pemanasan (control) Setelah pemanasan Kekentala
n
Endapan Warna Kekentala n
Endapan Warna
Putih telur
++ - Bening +++ +++ Putih
susu
Susu sapi + - Putih
susu buram
++ ++ Putih
susu cerah Sari
kedelai
+ - Putih
kream
- + Kream
- : Tidak kental
+ : Kental
++ : Agak Kental
+++ : Sangat Kental
Table 2. Reaksi Dengan Formadehyde
Sampel Sebelum Pemanasan (control) Setelah Pemanasan
2 4 6 8 10 2 4 6 8 10
Telur + ++ +++ ++++ +++++ +++++ ++++ +++ ++ +
Susu kedelai
+ ++ +++ ++++ +++++ +++++ ++++ +++ ++ +
Susu + ++ +++ ++++ +++++ +++++ ++++ +++ ++ +
Table 3. Pengendapan Protein dengan Logam Berat
Sampel Jumlah Tetesan HgCl2 Keterangan
Susu murni 7 +
Kedelai 1 +++
Putih telur 1 ++
Pembahasan
Protein selain merupakan komponen yang sangat penting bagi tubuh, karena berfungsi sebagai zat pembangun dan pengatur, Protein juga merupakan sumber asam- asam amino yang mengandung unsur C, H, O dan N yang tidak dimiliki oleh lemak atau karbohidrat. Molekul protein mengandung pula posfor, belerang dan ada jenis protein yang mengandung unsur logam seperti besi dan tembaga.
Protein memiliki berat molekul yang besar,terdiri berbagai macam asam amino, memiliki strukturnya yang tidak stabil. Sifat protein juga dapat ditentukan oleh sifat asam amino penyusunnya. Berdasarkan fungsi, protein berguna dalam penyusun Enzim,sebagai pengangkut, pembangun,pertahanan tubuh, dan sebagai hormone.
pH, tekanan, aliran listrik, dan adanya bahan kimia seperti urea, alkohol, sabun dan temperature. Selain itu protein juga bersifat Ion zwiter karna protein memiliki muatan ion positif maupun negatif dan mempunyai pH isoelektrik yang berkisar 4-4,5. Protein juga memiliki sifat amfoter yang disebabkan karena adanya gugus amino (-NH2) yang bersifat basa dan gugus karboksil (-COOH) yang bersifat asam yang terdapat pada pada ujung-ujung rantainya.
Pada praktikum ini dilakukan percobaan dengan tiga metode pengamatan, yaitu yang pertama pengujian kelarutan protein terhadap pemanasan (table 1).sampel yang digunakan adalah putih telur susu sapi dan sari kedelai. Pada saat sebelum dipanaskan putih telur dan susu sapimemiliki tingkat kekentalan yang biasa dan agak kental dan tidak memiliki endapan setelah pemanasan diperoleh bahwa terjadinya peningkatan kekentalan dan terdapatnya endapan dengan warna yang berubah lebih terang. Hal ini terjadinya karena denaturasi protein dari putih telur dan susu yang dapat mengubah sifat protein menjadi lebih sukar larut dan makin kental yang disebut koagulasi. Semakin lama waktu pemanasan semakin banyak gumpalan yang terbentuk pada susu dan putih telur karena suhu yang tinggi dapat menyebabkan protein yang terdenaturasi lebih banyak. Sedangkan pada sari kedelai mengalami penurunan kekentalan dan peningkatan endapan setelah pemanasan.. ini karena Protein kedelai yang sebagian besar mengandung globulin tersebut mempunyai titik isoelektrik 4.1- 4.6. Globulin akan mengendap pada pH 4.1 sedangkan protein lainnya seperti proteosa, prolamin, dan albumin bersifat larut dalam air sehingga diperkirakan penurunan kadar protein dalam perebusan disebabkan terlepasnya ikatan struktur protein non-globulin karena panas yang menyebabkan terlarutnya komponen protein tersebut dalam air.
Pada perccobaan dengan pengendapan protein dengan logam berat (table 3). Laruttan yang digunakan untuk campuran pada sampel susu murni, sari kedelai dan putih telor adalah larutan HgCl2 jenuh. Perubahan yang terjadi setelah dilakukan penambahan HgCl2 adalah dengan hasil sari kedelai lebih cepat diketahui adanya logam berat dari susu murni dan putih telor karna sari kedelai sudah terdapat endapan pada tetesan 1. Sedangkan pada susu murni pengendapa baru terjadi pada tetesan ke 7 dan putih telur pada tetesan 1. Ikatan yang terbentuk amat kuat dan akan memutuskan jembatan garam, sehingga protein mengalami denaturasi. Albumin dengan kasein akan mengalami pengendapan karena mengalami titik isolistrik akibat reaksi antara albumin dan kasein (basa sehingga laritan bermuatan negatif) dengan Zn mengakibatkan terjadinya denaturasi dan koagulasi. Warna keruh disebabkan karena terjadi ikatan antara Zn dengan albumin menjadi Zn proteinat, Zn dapat menjenuhkan larutan hingga pH larutan berada di atas pH isolistrik sehingga gumpalan larut kembali.
KESIMPULAN
DAFTAR PUSTAKA
Badan Standarisasi Nasional. 2011. SNI 01-3141-2011 Susu Sapi Segar. BSN: Jakarta.
Jay, et al. 2005. Penetapan kesegaran susu sapi berkualitas. Gadjah mada university press, Yogyakarta.
Suprapti. 2010. Teknologi Tepat Guna Kembang Tahu Dan Susu Kedelai. Kanisius:
Yogyakarta.
Rayner T. 2002. Fining and Clarifying Agent. (terhubung berkala)
http://www.nature.com/onc/journal/v22/n42/full/1206814a.html. Diakses
pada 10 Maret 2014.
Almatsier. 2004. Prinsip Dasar Ilmu Gizi. Jakarta: Gramedia Pustaka Utama.
Budianto. AK. 2009. Pangan, gizi, dan pembangunan Manusia Indonesia. Dasar-Dasar Ilmu Gizi, Malang: UMM pen 1-16.
Yuniastuti. 2008.
http://digilib.unimus.ac.id/files/disk1/125/jtptunimus-gdl-lailiratna-6245-3-babii.pdf. Diakses pada 10 Maret 2014.
http://repository.usu.ac.id/bitstream/123456789/18842/4/Chapter%20II.pdf.
Yazid, E. dan Nurjanti,L. 2006. Penentuan Praktikum Biokimia. Penerbit Andi. Yogyakarta.