kg/jam) 66 (31.565,65 produk Kapasitas kg/jam) (580,4420 produk Kapasitas (X) baku Bahan kg/jam) (1000 baku bahan Basis
LAMPIRAN A
PERHITUNGAN NERACA MASSA
Kapasitas Produk : 250.000 ton/tahun Satuan Operasi : kg/jam
Waktu kerja pertahun : 330 hari Kapasitas produksi perjam :
tahun ton 000 . 250 × hari 330 tahun 1 × jam 24 hari 1 × ton 1 kg 1000 = 31.565,6566 kg/jam
Kemurnian bahan baku : 99,85 % ( PT. Kaltim Methanol Industri ) Kemurnian produk : 99,85 %
Tabel LA.1. Komposisi Metanol
No Nama Dagang Rumus Kimia Kadar
1 Metanol CH3OH 99,85 %
2 Air H2O 0,15%
Total 100 %
Perhitungan neraca massa dilakukan dengan alur maju dimana perhitungan dimulai dari alur bahan baku sampai ke alur produk. Untuk mendapatkan jumlah bahan baku yang masuk pada kapasitas produksi sebanyak 31.565,6566 kg/jam, maka terlebih dahulu digunakan basis bahan baku yang masuk sebanyak 1000 kg/jam. Untuk basis bahan baku 1000 kg/jam dihasilkan dimetil eter sebanyak 580,4420 kg/jam, maka untuk kapasitas produksi 250.000 ton/tahun diperoleh kapasitas bahan baku sebanyak 54.382,1029 kg/jam. Dengan rumus perbandingan:
Bahan baku : kg/jam 580,4420 kg/jam 6 31.565,656
×
1000 kg/jam =54.382,1029 kg/jamFH-01
1
2 LA.1. Fired Heater (FH-01)
Fungsi : Untuk merubah fasa metanol dari fasa cair menjadi fasa gas serta meningkatkan temperatur sampai 250 oC
Gambar LA.1. Diagram alir fired heater (FH-01)
Neraca massa total : F1 = F2 Neraca massa komponen :
a. F1 Metanol = 0,9985 × 54.382,1029 kg/jam = 54.300,5297 kg/jam N1 Metanol = 1696,8916 kmol/jam F2 Metanol = 54.300,5297 kg/jam b. F2 Air = 0,0015 × 54.382,1029 kg/jam = 81,5732 kg/jam N2 Air = 4,5319 kmol/jam F2 Air = 81,5732 kg/jam
Tabel LA.2. Neraca Massa pada Fired Heater (FH - 01) Komponen Masuk (kg/jam) Keluar (kg/jam)
Alur 1 Alur 2 CH3OH 54.300,5297 54.300,5297 H2O 81,5732 81,5732 Total 54.382,1029 54.382,1029 LA.2. Reaktor (R-01) F1 CH3OH (l) 99,85% F2 CH3OH (g) 99,85%
F2 CH3OH 99,85% T = 250oC P = 12 atm F3 CH3OCH3 H2O CH3OH 3 R-01
Fungsi : Sebagai tempat terjadinya reaksi dehidrasi metanol sehingga menghasilkan dimetil eter yang akan dimurnikan pada proses berikutnya.
Gambar LA.2. Diagram alir reaktor (R-01)
Reaksi : 2CH3OH(l) CH3OCH3(g) + H2O(g)
Konversi : 90% terhadap Metanol Neraca massa total : F2 = F3
Nearca massa komponen : a. Metanol BM Metanol = 32 kg/kmol F2 Metanol = 0,9985 × F1 = 0,9985 × 54.382,1029 kg/jam = 54.300,5297 kg/jam N2 Metanol = Metanol BM Metanol F2 = kg/kmol 32 kg/jam 7 54.300,529 = 1696,8916 kmol/jam
Metanol bereaksi = 90 % × 1696,8916 kmol/jam = 1527,2024 kmol/jam
N3 Metanol = 1696,8916 kmol/jam - 1527,2024 kmol/jam = 169,6892 kmol/jam
F3 Metanol = 5430,0530 kg/jam b. Dimetil Eter
BM Dimetil eter = 46 kg/mol
r = -X.N Metanol 2 = 2 -kmol/jam 1696,8916 0,9 - = 763,6012 kmol/jam N3 Dimetil Eter = 0 + r = 763,6012 kmol/jam
F3 Dimetil Eter = 35.125,6552 kg/jam
c. Air F2 Air = 81,5732 kg/jam N2 Air = 4,5318 kmol/jam Air terbentuk = 0 + r = 763,6012 kmol/jam = 13.744,8216 kg/jam
N3 Air = Air masuk + Air yang terbentuk = 4,5318 kmol/jam + 763,6012 kmol/jam = 768,1330 kmol/jam
F3 Air = 13.826,3947 kg/jam
Tabel LA.3. Neraca Massa pada Reaktor (R-01)
Komponen Masuk Keluar
Alur 2 (kg/jam) Alur 3 (kg/jam)
CH3OH 54.300,5297 5430,0530
H2O 81,5732 13.826,3947
CH3OCH3 - 35.125,6552
Total 54.382,1029 54.382,1029
CD-01
Fungsi : Untuk merubah fasa produk reaktor (R – 01) menjadi fasa cairan jenuh pada suhu bubble pointnya.
Gambar LA.3. Diagram alir condensor (CD-01)
Neraca Massa Total untuk Condensor – 01 F3 = F4
Neraca massa komponen : a. Dimetil eter :
N3 Dimetil eter = 763,6012 kmol/jam F3 Dimetil eter = 35.125,6552 kg/jam N4 Dimetil eter = 763,6012 kmol/jam F4 Dimetil eter = 35.125,6552 kg/jam
b. Metanol : N3 Metanol = 169,6892 kmol/jam F3 Metanol = 5430,0530 kg/jam N4 Metanol = 169,6892 kmol/jam F4 Metanol = 5430,0530 kg/jam c. Air : N3 Air = 768,1330 kmol/jam F3 Air = 13.826,3947 kg/jam N4 Air = 768,1330 kmol/jam F4 Air = 13.826,3947 kg/jam
Tabel LA.4. Neraca Massa Condensor (CD – 01) F3 CH3OCH3 H2O CH3OH F4 CH3OCH3 H2O CH3OH 3 4
F5 CH3OCH3 H2O CH3OH F4 CH3OCH3 H2O CH3OH F10 - H2O - CH3OH - CH3OCH3 KD-01
Komponen Masuk Keluar
Alur 3 (kg/jam) Alur 4 (kg/jam)
CH3OH 5430,0530 5430,0530
H2O 13.826,3947 13.826,3947
CH3OCH3 35.125,6552 35.125,6552
Total 54.382,1029 54.382,1029
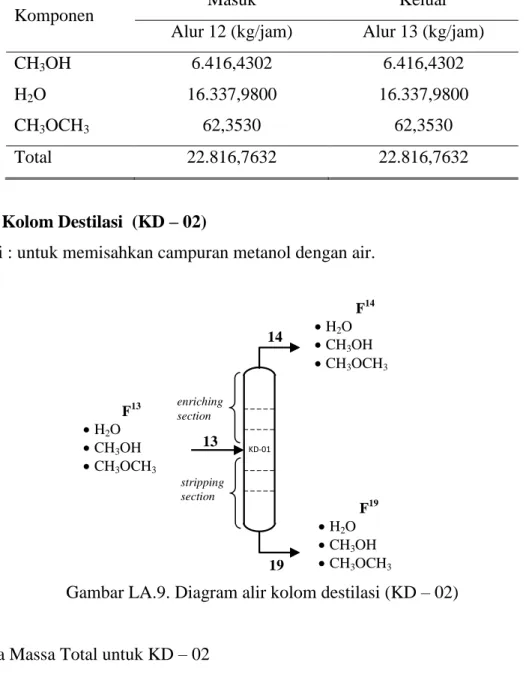
LA.4. Kolom Destilasi (KD – 01)
Fungsi : Untuk memisahkan campuran metanol dan air pada produk bawah dengan dimetil eter sebagai produk atas.
Gambar LA.4. Diagram alir kolom destilasi (KD – 01) Neraca Massa Total untuk KD – 01
F4 = F5 + F10
Tabel LA.5. Komposisi Bahan Masuk Kolom Destilasi (KD – 01) Komponen F (kg/jam) N (kmol/jam) Fraksi mol (xi)
CH3OH 5430,0530 169,6892 0,0997
H2O 13.826,3947 768,1330 0,4515
CH3OCH3 35.125,6552 763,6012 0,4488
Total 54.382,1029 1701,4234 1.0000
Yang diinginkan adalah 99,85% Dimetil Eter keluar dari atas kolom destilasi. 5 10 4 enriching section stripping section
Metode Hengtebeck’s (R.K.Sinnott)
Light key (LK) : Dimetil Eter
Heavy key (HK) : Metanol
Distribusi LK dan HK adalah 99,85% = 0,9985
Diinginkan 99,85 % Dimetil Eter keluar dari atas KD – 01
LK = [x.Dimetil Eter]d
N5 Dimetil Eter = 763,6012 kmol/jam × 99,85 % = 762,4558 kmol/jam
F5 Dimetil Eter = 35.072,9667 kg/jam [x.Dimetil Eter]b
N10 Dimetil Eter = 763,6012 kmol/jam × 0,15 % = 1,1454 kmol/jam
F10 Dimetil Eter = 52,6885 kg/jam
Log (Xd/Xb) = log jam kmol jam kmol / 1,1454 / 762,4558 = 2,8233
Diinginkan 99,5 % Metanol keluar dari bottom KD – 01 LK = [x.Metanol]d N5 Metanol = 169,6892 kmol/jam × 0,15 % = 0,2545 kmol/jam F5 Metanol = 8,1451 kg/jam HK = [x.Metanol]b N10 Metanol = 169,6892 kmol/jam × 99,85 % = 169,4346 kmol/jam F10 Metanol = 5.421,9079 kg/jam Log (Xd/Xb) = log jam kmol jam kmol / 169,4346 / 0,2545 = -2,8233
Diinginkan 99,85 % Air keluar dari bottom KD – 01 LK = [x.Air]d
CD-02 N5 Air = 768,1330 kmol/jam × 0,15 % = 1,1522 kmol/jam F5 Air = 20,7396 kg/jam HK = [x.Air]b N10 Air = 768,1330 kmol/jam × 99,85 % = 766,9808 kmol/jam F10 Air = 13805,6552 kg/jam
Tabel LA. 6. Neraca Massa Kolom Destilasi (KD – 01)
Komponen Input (kg/jam)
Output (kg/jam)
Top Bottom
Alur 4 Alur 5 Alur 10
CH3OCH3 5430,0530 35.072,9667 52,6885 CH3OH 13.826,3947 8,1451 5421,9079 H2O 35.125,6552 20,7396 13.805,6552 Total 54.382,1029 35.101,8514 19.280,2515 54.382,1029 LA.5. Condensor (CD-02)
Fungsi : Untuk merubah fasa produk atas destilasi KD - 01 menjadi fasa cair
Gambar LA.5. Diagram alir condenser (CD-02)
Neraca Massa Total untuk CD – 01 F5 = F6
Neraca massa komponen : a. Dimetil eter :
N5 Dimetil eter = 762,4558 kmol/jam F5 CH3OCH3 (g) H2O(g) CH3OH (g) F6 CH3OCH3 (l) H2O(l) CH3OH (l) 5 6
F5 Dimetil eter = 35.072,9667 kg/jam N6 Dimetil eter = 762,4558 kmol/jam F6 Dimetil eter = 35.072,9667 kg/jam
b. Metanol : N5 Metanol = 0,2545 kmol/jam F5 Metanol = 8,1451 kg/jam N6 Metanol = 0,2545 kmol/jam F6 Metanol = 8,1451 kg/jam c. Air : N5 Air = 1,1522 kmol/jam F5 Air = 20,7396 kg/jam N6 Air = 1,1522 kmol/jam F6 Air = 20,7396 kg/jam
Tabel LA. 6. Neraca Massa Condenser (CD – 02)
Komponen Masuk Keluar
Alur 5 (kg/jam) Alur 6 (kg/jam)
CH3OH 8,1451 8,1451
H2O 20,7396 20,7396
CH3OCH3 35.072,9667 35.072,9667
SP-01
LA.6. Splitter (SP-01)
Fungsi : Untuk membagi aliran destilat yang berasal dari CD - 02 menjadi aliran refluks dan aliran destilat produk
Gambar LA.6. Diagram alir splitter (SP-01)
Refluks Rasio = 0,1008 (Dimian dan Bildea, 2008): Neraca massa total : F7 = F8 + F9
Neraca massa komponen : a. Dimetil eter :
N7 Dimetil eter = 762,4558 kmol/jam F7 Dimetil eter = 35.072,9667 kg/jam
N9 Dimetil eter = 0,1008 × 762,4558 kmol/jam = 76,8174 kmol/jam
F9 Dimetil eter = 3.533,6014 kg/jam
N8 Dimetil eter = 762,4558 kmol/jam - 76,8174 kmol/jam = 685,6384 kmol/jam
F8 Dimetil eter = 31.539,3653 kg/jam
b. Metanol : N7 Metanol = 0,2545 kmol/jam F7 Metanol = 8,1451 kg/jam N9 Metanol = 0,1008 × 0,2545 kmol/jam = 0,0256 kmol/jam F9 Metanol = 0,8206 kg/jam
N8 Metanol = 0,2545 kmol/jam - 0,0256 kmol/jam F7 CH3OCH3 H2O CH3OH F8 CH3OCH3 H2O CH3OH 7 9 8 F9 CH3OCH3 H2O CH3OH
= 0,2289 kmol/jam F8 Metanol = 7,3245 kg/jam c. Air : N7 Air = 1,1522 kmol/jam F7 Air = 20,7396 kg/jam N9 Air = 0,1008 × 1,1522 kmol/jam = 0,1161 kmol/jam F9 Air = 2,0895 kg/jam
N8 Air = 1,1522 kmol/jam - 0,1161 kmol/jam = 1,0361 kmol/jam
F8 Air = 18,6501 kg/jam
Tabel LA.8. Neraca Massa Total Splitter (SP – 01)
Komponen
Input (kg/jam) Output (kg/jam)
Refluks Destilat
Alur 7 Alur 9 Alur 8
CH3OCH3 35.072,9667 3.533,6014 31.539,3653 CH3OH 8,1451 0,8206 7,3245 H2O 20,7396 2,0895 18,6501 Total 35.101,8514 3.536,5115 31.565,3398 35.101,8514 LA.7. Reboiler (RB-01)
RB-101
Fungsi : Untuk menguapkan sebagian campuran produk bottom KD-01
Gambar LA.7. Diagram alir reboiler (RB-01) Keterangan :
V* : Aliran Vapor (Refluks) RB-01 L* : Aliran Feed RB-01
B* : Aliran Bottom Produk RB-01 Kondisi Uap kondenser :
P = 8,0 atm = 810,6 kPa T = 159 oC = 432 oK q =
jumlah mol total cair mol jumlah = 4234 , 1701 1330 , 768 6892 , 169 = 0,5512 Sehingga : B* = 1109,5345 kmol/jam V* = V - ( 1- q ) x F (Geankoplis, 1997) = 763,8625 + ( 1 – 0,5512 ) × 1701,4234 kmol/jam = 0,2613 kmol/jam Neraca Total : L* = B* + V* = 1109,5345 kmol/jam - 0,2613 kmol/jam = 1109,7958 kmol/jam Perhitungan : a. Dimetil eterN10 Dimetil eter = 0,0012 × 1109,7958 kmol/jam
= 1,3558 kmol/jam
F10 Dimetil eter = 62,3676 kg/jam F11 (V*) CH3OCH3 H2O CH3OH F10 (L*) CH3OCH3 H2O CH3OH F12 (B*) H2O CH3OH CH3OCH3 11 10 12
N11 Dimetil eter = 0,0012 × 0,2613 kmol/jam
= 0,2613 kmol/jam
F11 Dimetil eter = 0,0147 kg/jam
N12 Dimetil eter = 0,0012 × 1109,5345 kmol/jam
= 1,3555 kmol/jam
F12 Dimetil eter = 62,3530 kg/jam
b. Metanol N10 Metanol = 0,1807 × 1109,7958 kmol/jam = 200,5607 kmol/jam F10 Metanol = 6417,9415 kg/jam N11 Metanol = 0,1807 × 0,2613 kmol/jam = 0,0472 kmol/jam F11 Metanol = 1,5113 kg/jam N12 Metanol = 0,1807 × 1109,5345 kmol/jam = 200,5134 kmol/jam F12 Metanol = 6416,4302 kg/jam c. Air N10 Air = 0,8181 × 1109,7958 kmol/jam = 907,8793 kmol/jam F10 Air = 16.341,8281 kg/jam N11 Air = 0,8181 × 0,2613 kmol/jam = 0,2138 kmol/jam F11 Air = 3,8481 kg/jam N12 Air = 0,8181 × 937,2995 kmol/jam = 907,6656 kmol/jam F12 Air = 16337,9800 kg/jam
H-01
Komponen Input (kg/jam)
Output (kg/jam)
Refluks Bottom
Alur 10 Alur 11 Alur 12
CH3OCH3 62,3676 0,0147 62,3530 CH3OH 6.417,9415 1,5113 6.416,4302 H2O 16.341,8281 3,8481 16.337,9800 Total 22.822,1373 5,3741 22.816,7632 22.822,1373 LA.8. Heater (H-01)
Fungsi : Untuk meningkatkan temperatur dari produk reboiler (RB-01) pada suhu bubble pointnya.
Gambar LA.8. Diagram alir heater (H-01)
Neraca Massa Total untuk H – 01 F12 = F13
Neraca massa komponen :
a. Dimetil eter :
N12 Dimetil eter = 1,3555 kmol/jam F12 Dimetil eter = 62,3530 kg/jam N13 Dimetil eter = 1,3555 kmol/jam F13 Dimetil eter = 62,3530 kg/jam
b. Metanol : N12 Metanol = 200,5134 kmol/jam F12 Metanol = 6.416,4302 kg/jam F12 CH3OCH3 H2O CH3OH F13 CH3OCH3 H2O CH3OH 12 13
KD-01 N13 Metanol = 200,5134 kmol/jam F13Metanol = 6.416,4302 kg/jam c. Air : N12 Air = 907,6656 kmol/jam F12 Air = 16.337,9800 kg/jam N13 Air = 907,6656 kmol/jam F13 Air = 16.337,9800 kg/jam
Tabel LA.10. Neraca Massa Heater (H – 01)
Komponen Masuk Keluar
Alur 12 (kg/jam) Alur 13 (kg/jam)
CH3OH 6.416,4302 6.416,4302
H2O 16.337,9800 16.337,9800
CH3OCH3 62,3530 62,3530
Total 22.816,7632 22.816,7632
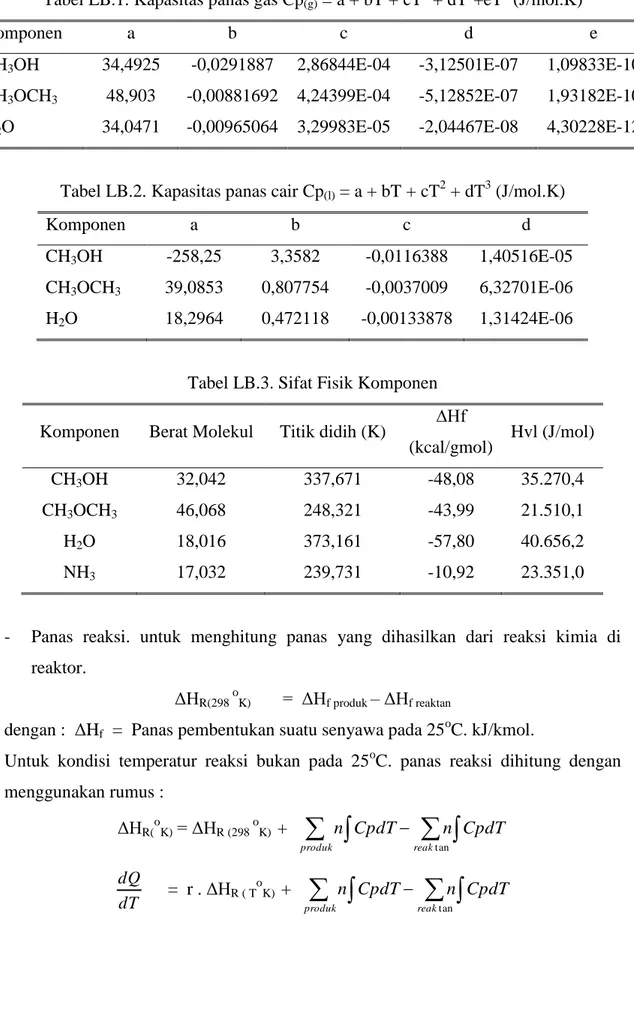
LA.9. Kolom Destilasi (KD – 02)
Fungsi : untuk memisahkan campuran metanol dengan air.
Gambar LA.9. Diagram alir kolom destilasi (KD – 02)
Neraca Massa Total untuk KD – 02
14 F13 H2O CH3OH CH3OCH3 19 13 F14 H2O CH3OH CH3OCH3 F19 H2O CH3OH CH3OCH3 enriching section stripping section
F13 = Umpan (F14 + F19)
Tabel LA.11. Komposisi Umpan Masuk Kolom Destilasi (KD – 02)
Komponen xi N (kmol/jam) F (kg/jam)
CH3OCH3 0.0012 1,3555 62,3530
CH3OH 0.1807 200,5134 6.416,4302
H2O 0.8181 907,6656 16.337,9800
Total 1.0000 1.109,5345 22.816,7632
Yang diinginkan adalah 99,85% Dimetil Eter keluar dari atas kolom destilasi.
Metode Hengstebeck’s (R.K.Sinnott)
Light key (LK) : Metanol
Heavy key (HK) : Air
Distribusi LK dan HK adalah 99,85% = 0,9985 Diinginkan 99,85 % Metanol keluar dari atas KD - 02 LK = [x.Metanol]d N14 Metanol = 200,5134 kmol/jam × 99,85 % = 200,2127 kmol/jam F14 Metanol = 6.406,8056 kg/jam [x.Metanol]b N19 Metanol = 200,5134 kmol/jam × 0,15 % = 0,3008 kmol/jam F19 Metanol = 9,6246 kg/jam Log (Xd/Xb) = log jam kmol jam kmol / 0,3008 / 200,2127 = 2,8233
Diinginkan 99,85 % Air keluar dari bawah KD - 02 HK = [x.Air]b
N14 Air = 907,6656 kmol/jam × 99,85 % = 906,3041 kmol/jam
LK = [x.Air]d
N19 Air = 907,6656 kmol/jam × 0,15 %
= 1,3615 kmol/jam
F19 = 24,5070 kg/jam
Diinginkan 99,85 % Dimetil eter keluar dari atas KD - 02 LK = [x. Dimetil eter]d
N14 Metanol = 1,3555 kmol/jam × 99,85 % = 1,3535 kmol/jam
F14 Dimetil eter = 62,2594 kg/jam [x. Dimetil eter]b
N19 Dimetil eter = 1,3555 kmol/jam × 0,15 %
= 0,3008 kmol/jam
F19 Dimetil eter = 0,0935 kg/jam
Tabel LA. 12. Data Neraca Massa Total Kolom Destilasi (KD – 02)
Komponen Input (kg/jam)
Output (kg/jam)
Top Bottom
Alur 13 Alur 14 Alur 15
CH3OCH3 62,3530 62,2594 0,0935 CH3OH 6.416,4302 6.406,8056 9,6246 H2O 16.337,9800 24,5070 1.6313,4731 Total 22.816,7632 6.493,5720 1.6323,1912 22.816,7632 LA.10. Condensor (CD-03)
CD-03
Fungsi : Untuk merubah fasa produk atas destilasi KD - 02 menjadi fasa cair
Gambar LA.10. Diagram alir condensor (CD-03)
Neraca Massa Total untuk CD – 03 F14 = F15
Neraca massa komponen : a. Dimetil eter :
N14 Dimetil eter = 1,3535 kmol/jam F14 Dimetil eter = 62,2594 kg/jam N15 Dimetil eter = 1,3535 kmol/jam F15 Dimetil eter = 62,2594 kg/jam
b. Metanol : N14 Metanol = 200,2127 kmol/jam F14 Metanol = 6406,8056 kg/jam N15 Metanol = 200,2127 kmol/jam F15 Metanol = 6406,8056 kg/jam c. Air : N14 Air = 1,3615 kmol/jam F14 Air = 24,5070 kg/jam N15 Air = 1,3615 kmol/jam F15 Air = 24,5070 kg/jam
Tabel LA. 13. Neraca Massa Condensor (CD – 03) F14 CH3OCH3 H2O CH3OH F15 CH3OCH3 H2O CH3OH 14 15
SP-01
Komponen Masuk Keluar
Alur 14 (kg/jam) Alur 15 (kg/jam)
CH3OH 6.406,8056 6.406,8056
H2O 24,5070 24,5070
CH3OCH3 62,2594 62,2594
Total 6.493,5720 6.493,5720
LA.11. Splitter (SP-02)
Fungsi : Untuk membagi aliran destilat yang berasal dari CD - 03 menjadi aliran refluks dan aliran destilat
Gambar LA.11. Diagram alir splitter (SP-02)
Refluks Rasio = 0,01
Neraca massa total : F16 = F17 + F18 Neraca massa komponen :
a. Dimetil eter :
N16 Dimetil eter = 1,3535 kmol/jam F16 Dimetil eter = 62,2594 kg/jam
N18 Dimetil eter = 0,01 × 1,3535 kmol/jam = 0,0135 kmol/jam
F18 Dimetil eter = 0,6226 kg/jam
N17 Dimetil eter = 1,3535 kmol/jam - 0,0135 kmol/jam = 1,3399 kmol/jam
F17 Dimetil eter = 61,6368 kg/jam F16 CH3OCH3 H2O CH3OH F18 CH3OCH3 H2O CH3OH 16 17 18 F17 CH3OCH3 H2O CH3OH
b. Metanol : N16 Metanol = 200,2127 kmol/jam F16 Metanol = 6406,8056 kg/jam N18 Metanol = 0,01 × 200,2127 kmol/jam = 2,0021 kmol/jam F18 Metanol = 64,0681 kg/jam
N17 Metanol = 200,2127 kmol/jam - 2,0021 kmol/jam = 198,2105 kmol/jam F17 Metanol = 6342,7375 kg/jam c. Air : N16 Air = 1,3615 kmol/jam F16 Air = 24,5070 kg/jam N18 Air = 0,01 × 1,3615 kmol/jam = 0,0136 kmol/jam F18 Air = 0,2451 kg/jam
N17 Air = 1,3615 kmol/jam - 0,0136 kmol/jam = 1,3479 kmol/jam
F17 Air = 24,2619 kg/jam
Tabel LA.14. Neraca Massa Total Splitter (SP – 02)
Komponen Input (kg/jam)
Output (kg/jam)
Refluks Destilat
Alur 16 Alur 18 Alur 17
CH3OCH3 62,2594 0,6226 61,6368 CH3OH 6406,8056 64,0681 6342,7375 H2O 24,5070 0,2451 24,2619 Total 6493,5720 64,9357 6428,6362 6493,5720 LA.12. Reboiler (RB - 02)
RB-102
Fungsi : Untuk menguapkan sebagian campuran produk bottom KD - 02
Gambar LA.12. Diagram alir reboiler (RB-02) Keterangan :
L* [F19] : Aliran vapor RB-102 V* [F20] : Aliran Refluks RB-102
B* [F21] : Aliran Bottom Produk RB-102 Kondisi Uap kondenser :
P = 8,0 atm = 8,1062 kPa T = 177 oC = 432 oK q =
jumlah mol total cair mol jumlah = 5345 , 1109 6656 , 907 = 0,8181 Sehingga : B* = 911,2722 kmol/jam V* = V - ( 1- q ) x F (Geankoplis, 1997) = 202,9276 + ( 1 – 0,8181 ) × 1109,5345 kmol/jam = 1,0587 kmol/jam Neraca Total : L* = V* + B* = 1,0587 kmol/jam + 911,2722 kmol/jam = 910,2135 kmol/jam Perhitungan : a. Dimetil eter F20 (V*) CH3OCH3 H2O CH3OH F19 (L*) CH3OCH3 H2O CH3OH F21 (B*) CH3OCH3 H2O CH3OH 20 19 21N19 Dimetil eter = (2,2060×10-6) × 910,2135 kmol/jam
= 0,0020 kmol/jam
F19 Dimetil eter = 0,0940 kg/jam
N20 Dimetil eter = (2,22×10-6)× 1,0587 kmol/jam = 2,3504 × 10-6 kmol/jam
F20 Dimetil eter = 0,0001 kg/jam
N21 Dimetil eter = (2,2060×10-6) × 911,2722 kmol/jam
= 0,0020 kmol/jam
F21 Dimetil eter = 0,0939 kg/jam
b. Metanol N19 Metanol = 0,0003 × 910,2135 kmol/jam = 0,3023 kmol/jam F19 Metanol = 9,6742 kg/jam N20 Metanol = 0.0003 × 1,0587 kmol/jam = 0,0004 kmol/jam F20 Metanol = 0,0112 kg/jam N21 Metanol = 0,0003 × 911,2722 kmol/jam = 0,3020 kmol/jam F21 Metanol = 9,6629 kg/jam c. Air N19 Air = 0,9997 × 910,2135 kmol/jam = 910,9678 kmol/jam F19 Air = 16,397,4202 kg/jam N20 Air = 0,9997 × 1,0587 kmol/jam = 1,0583 kmol/jam F20 Air = 19,0501 kg/jam N21 Air = 0,9997 × 911,2722 kmol/jam = 909,9094 kmol/jam F21 Air = 16378,3701 kg/jam
C-01
Tabel LA. 15. Neraca Massa Total Reboiler (RB - 02)
Komponen Input (kg/jam)
Output (kg/jam)
Refluks Bottom
Alur 19 Alur 20 Alur 21
CH3OCH3 0,0940 0,0001 0,0939 CH3OH 9,6742 0,0112 9,6629 H2O 16.397,4202 19,0501 16378,3701 Total 16.407,1884 19,0615 16.388,1269 16.407,1884 LA.13. Cooler (C-01)
Fungsi : Untuk mendinginkan produk bawah reboiler (RB-02)
Gambar LA.13. Diagram alir cooler (C-01) Neraca Massa Total untuk C – 01
F21 = F22
Neraca massa komponen :
a. Dimetil eter :
N21 Dimetil eter = 0,0020 kmol/jam F21 Dimetil eter = 0,0939 kg/jam N22 Dimetil eter = 0,0020 kmol/jam F22 Dimetil eter = 0,0939 kg/jam
b. Metanol : N21 Metanol = 0,3020 kmol/jam F21 Metanol = 9,6629 kg/jam N22 Metanol = 0,3020 kmol/jam F21 CH3OCH3 H2O CH3OH F22 CH3OCH3 H2O CH3OH 21 22
F22 Metanol = 9,6629 kg/jam c. Air : N21 Air = 909,9094 kmol/jam F21 Air = 16378,3701 kg/jam N22 Air = 909,9094 kmol/jam F22 Air = 16378,3701 kg/jam
Tabel LA. 16. Neraca Massa Cooler (C – 01)
Komponen Masuk Keluar
Alur 21 (kg/jam) Alur 22 (kg/jam)
CH3OH 9,6629 9,6629
H2O 16.378,3701 16.378,3701
CH3OCH3 0,0939 0,0939
LAMPIRAN B
PERHITUNGAN NERACA PANAS
Kapasitas : 250.000 ton/tahun Operasi Pabrik : 330 hari/tahun Basis Perhitungan : 1 Jam operasi Temperatur Referensi : 25oC = 298o K Satuan Panas : kilo Joule (kJ)
Panas yang dihitung pada neraca panas ini. meliputi :
- Panas yang dihitung apabila terjadi perubahan temperatur. Q = n.Cp .ΔT
dengan : ΔT = T - To
Q : Panas yang dihasilkan/dikeluarkan. kJ. Cp : Kapasitas panas. kJ/kmol.K.
N : Mol senyawa. kmol.
To : Temperatur referensi. 25oC T : Temperatur senyawa. oC Keterangan :
T T p p o dT C T C .Kapasitas panas cairan
4 4
4 3 3 3 2 2 2 3 2 . o D o C o B o T T T T T T T T T T A dt DT CT T B A o
Kapasitas panas gas
5 5
5 4 4 4 3 3 3 2 2 2 4 3 2 . o E o D o C o B o T T T T T T T T T T T T A dt ET DT CT T B A o
Tabel LB.1. Kapasitas panas gas Cp(g) = a + bT + cT2 + dT3+eT4 (J/mol.K)
Komponen a b c d e
CH3OH 34,4925 -0,0291887 2,86844E-04 -3,12501E-07 1,09833E-10
CH3OCH3 48,903 -0,00881692 4,24399E-04 -5,12852E-07 1,93182E-10
H2O 34,0471 -0,00965064 3,29983E-05 -2,04467E-08 4,30228E-12
Tabel LB.2. Kapasitas panas cair Cp(l) = a + bT + cT2 + dT3 (J/mol.K)
Komponen a b c d
CH3OH -258,25 3,3582 -0,0116388 1,40516E-05
CH3OCH3 39,0853 0,807754 -0,0037009 6,32701E-06
H2O 18,2964 0,472118 -0,00133878 1,31424E-06
Tabel LB.3. Sifat Fisik Komponen Komponen Berat Molekul Titik didih (K) ∆Hf
(kcal/gmol) Hvl (J/mol)
CH3OH 32,042 337,671 -48,08 35.270,4
CH3OCH3 46,068 248,321 -43,99 21.510,1
H2O 18,016 373,161 -57,80 40.656,2
NH3 17,032 239,731 -10,92 23.351,0
- Panas reaksi. untuk menghitung panas yang dihasilkan dari reaksi kimia di reaktor.
ΔHR(298 oK) = ΔHf produk – ΔHf reaktan
dengan : ΔHf = Panas pembentukan suatu senyawa pada 25oC. kJ/kmol.
Untuk kondisi temperatur reaksi bukan pada 25oC. panas reaksi dihitung dengan menggunakan rumus : ΔHR(oK) = ΔHR (298 oK) +
produk reak CpdT n CpdT n tan dT dQ = r . ΔHR ( ToK) +
produk reak CpdT n CpdT n tanFH-01
1
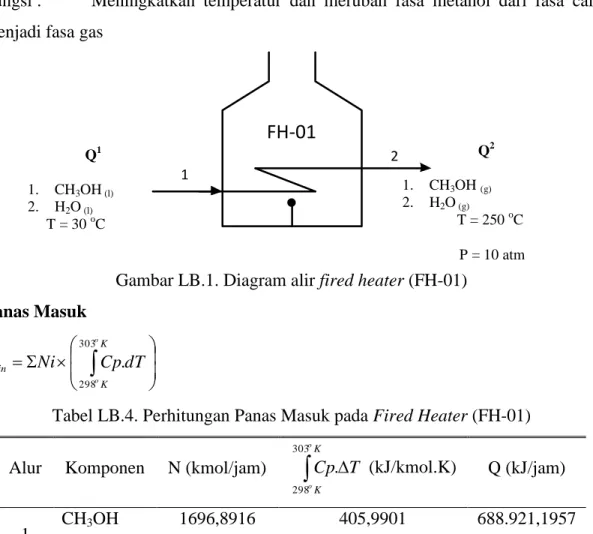
2 LB.1. Fired Heater (FH-01)
Fungsi : Meningkatkan temperatur dan merubah fasa metanol dari fasa cair menjadi fasa gas
Gambar LB.1. Diagram alir fired heater (FH-01) Panas Masuk
K K in o o dT Cp Ni Q 303 298 .Tabel LB.4. Perhitungan Panas Masuk pada Fired Heater (FH-01) Alur Komponen N (kmol/jam)
K K o o T Cp 303 298 . (kJ/kmol.K) Q (kJ/jam) 1 CH3OH 1696,8916 405,9901 688.921,1957 H2O 4,5318 374,6878 1.698,0261 Total 690.619,2218 Panas Keluar
K K out o o dT Cp Ni Q 523 298 .Tabel LB.5. Perhitungan Panas Keluar pada Fired Heater (FH-01) Alur Komponen N (kmol/jam)
K K o o T Cp 523 298 . (kJ/kmol.K) Q (kJ/jam) 2 CH3OH 1.696,8916 11.791,6344 20.009.124,79 H2O 4,5318 7.741,1999 35.081,8945 Total 20.044.206,68 Q2 1. CH3OH (g) 2. H2O (g) T = 250 oC P = 10 atm Q1 1. CH3OH (l) 2. H2O (l) T = 30 oC T = 300 oC
K K in K K out o o o o dT Cp Ni dT Cp Ni dT dQ 303 298 523 298 . . = Q out – Q in = 20.044.206,68 kJ/jam – 690.619,2218 kJ/jam = 19.353.587,46 kJ/jamPanas yang diperlukan = 19.353.587,46 kJ/jam
Fuel Mass Flow = 904,8120 kg/jam (Hysis)
Efficiency = 80 %
Fraction Excess Air = 15 %
Qt = Flow Mass Fuel diperlukan Panas = kg/jam 904,8120 kJ/jam ,46 19.353.587 = 21.389,6218 kg/jam Qn = Efficiency Qt = 80% kg/jam 8 21.389,621 = 26.737,0273 kJ/kg release heat lb/MBtu oil fuel with 8 840 106 t n f x Q G
Fuel Oil Rate, Gf = 22,0090 kg/jam (Walas, 218)
Tabel LB.6. Neraca Panas pada Fired Heater (FH-01) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 690.619,2218 -
Produk - 20.044.206,68
Panas yang diserap 19.353.587,46 - Total 20.044.206,68 20.044.206,68
R-01
LB.2. Reaktor (R-01)
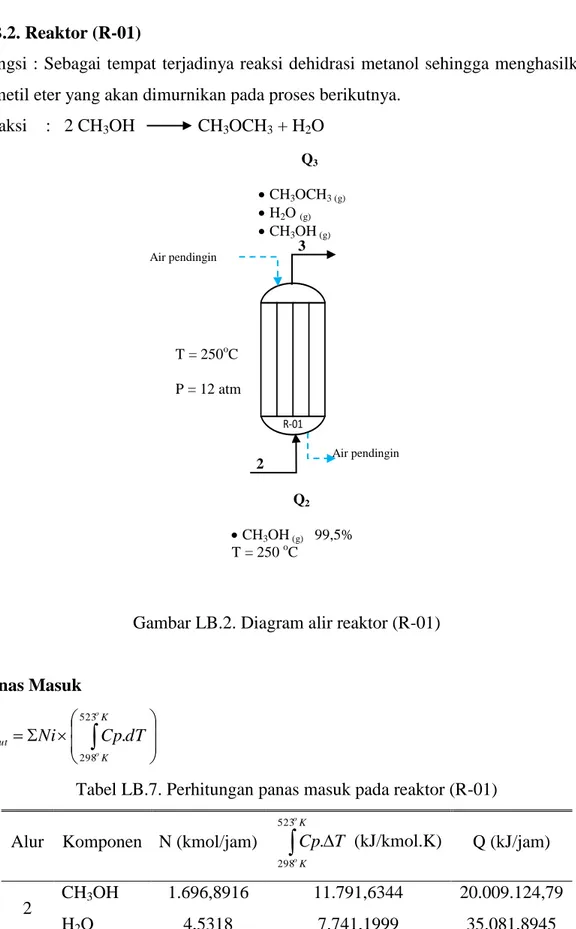
Fungsi : Sebagai tempat terjadinya reaksi dehidrasi metanol sehingga menghasilkan dimetil eter yang akan dimurnikan pada proses berikutnya.
Reaksi : 2 CH3OH CH3OCH3 + H2O
Gambar LB.2. Diagram alir reaktor (R-01)
Panas Masuk
K K out o o dT Cp Ni Q 523 298 .Tabel LB.7. Perhitungan panas masuk pada reaktor (R-01) Alur Komponen N (kmol/jam)
K K o o T Cp 523 298 . (kJ/kmol.K) Q (kJ/jam) 2 CH3OH 1.696,8916 11.791,6344 20.009.124,79 H2O 4,5318 7.741,1999 35.081,8945 Total 20.044.206,68 Panas Keluar T = 250oC P = 12 atm Q2 CH3OH (g) 99,5% T = 250 oC Q3 CH3OCH3 (g) H2O (g) CH3OH (g) T = ? 3 2 Air pendingin Air pendingin T = 40 oC
Perhitungan suhu keluar reaktor dT dQ = r . ΔHR ( oK) +
T C out o dT Cp N 250 . OH CH in OH CH XN r 3 3 = 2 -1696,8916 0,90 - = 763,6012 kmol = 763.601,2 mol/jamPanas standard reaksi
) 25 ( C HR o = HofCH OCH HofHO HofCH 3 2 3 3 = -43,99 + (-57,08) – (-48,08) = -52,99 kcal/gmol
Panas reaksi 250oC dapat dihitung dengan persamaan
) 250 ( C HR o = ΔHR ( 25oC) +
C C out o o dT Cp 250 25 . ) 250 ( C HR o = -52,99 kcal/gmol + [7741,1999 + 19.522,1668 – (2 × 11.791,6344)] cal/gmol= - 49,3099 kcal/gmol (∆HR < 0, reaksi eksoterm)
diasumsikan kapasitas panas konstan, maka
0 = 763.601,1994 × (- 49,3099) + [768,1330 × 7741,1999 + 763,6012 × 19.522,1668 + (2 × 11.791,6344) × 2.000.912,479] × ( T2 – 250 ) T – 250 = 1,6475 T2 = 251,6475 oC = 524,6475 K
64 , 524 298 .dT Cp Ni QoutTabel LB.8. Perhitungan Panas Keluar Pada Reaktor (R-01) Alur Komponen N (kmol/jam)
K K o o T Cp 64 , 524 298 . (kJ/kmol.K) Q (kJ/jam) 3 CH3OH 169,6892 11.892,5668 2.018.039,619 H2O 768,1330 7.799,5740 5.991.110,555 CH3OCH3 763,6012 19.689,5012 15.034.926,72 Total 23.044.076,89
Panas reaksi = r × HR(250oC) = 763,6011994 kmol/jam × ( - 0,0493099) kcal/kmol = -37,6531 kcal/jam = -157,5406 kJ/jam Q = r × o out in R C Q Q H (250 ) = 2.999.712,668 kJ/jam
Air pendingin untuk mengkontrol suhu agar tetap pada 250 oC Kondisi suhu masuk = 25 oC
Kondisi suhu keluar = 40 oC
H(40 oC) = 167,5 kJ/kg (Reklaitis) H(25 oC) = 125,8 kJ/kg (Reklaitis) Mair pendingin = ) H(25 -C) H(40 Q o o C Mair pendingin = 125,8 -167,5 668 2.999.712,
Mair pendingin = 71.935,556 kg/jam
Tabel LB.9. Neraca Panas pada Reaktor (R-01) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 20.044.206,68 Produk - 23.044.076,89 Panas reaksi - -157,5406 Air pendingin 2.999.712,668 - Total 23.043.919,35 23.043.919,35 LB.3. Condensor (CD-01)
CD-01
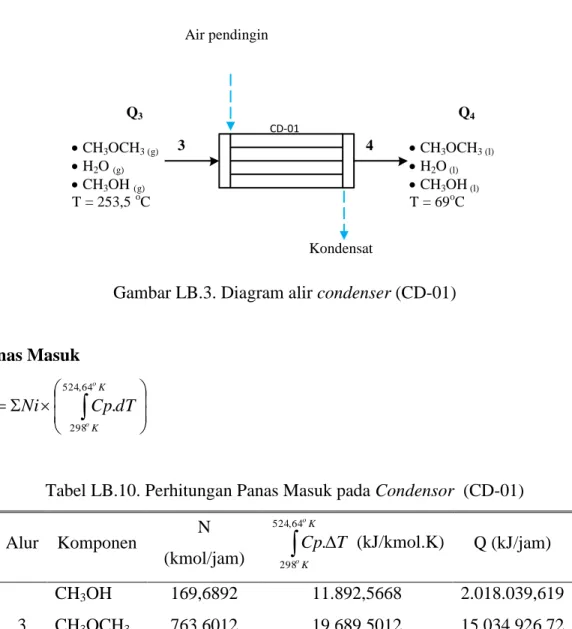
Fungsi : Untuk menurunkan temperatur produk reaktor serta merubah fasa menjadi cairan jenuh agar memudahkan proses pemisahan di kolom destilasi
Gambar LB.3. Diagram alir condenser (CD-01)
Panas Masuk
K K o o dT Cp Ni Q 64 , 524 298 .Tabel LB.10. Perhitungan Panas Masuk pada Condensor (CD-01)
Alur Komponen N (kmol/jam)
K K o o T Cp 64 , 524 298 . (kJ/kmol.K) Q (kJ/jam) 3 CH3OH 169,6892 11.892,5668 2.018.039,619 CH3OCH3 763,6012 19.689,5012 15.034.926,72 H2O 768,1330 7.799,5741 5.991.110,555 Total 23.044.076,89 Panas Keluar
K K o o dT Cp Ni Q 343 298 .Tabel LB.11. Perhitungan Panas Keluar pada Condensor (CD-01) Q3 CH3OCH3 (g) H2O (g) CH3OH (g) T = 253,5 o C P = 12 atm Q4 CH3OCH3 (l) H2O (l) CH3OH (l) T = 69oC Air pendingin T = 25oC Kondensat T = 40oC 3 4
Alur Komponen N (kmol)
K K o o T Cp 343 298 . (kJ/kmol.K) Q(kJ/jam) 4 CH3OH 169,6892 3.844,4873 652.367,806 CH3OCH3 763,6012 5.693,0375 4.347.210,308 H2O 768,1330 3.390,5215 2.604.371,594 Total 7.603.949,707Panas yang diserap ammonia (Q) adalah :
K K in K K out o o o o dT Cp Ni dT Cp Ni dT dQ 524,64 298 343 298 . . Qamonia = Qout - Qin = 7.603.949,707 kJ/jam – 23.044.076,89 kJ/jam = -15.440.127,19 kJ/jamKondisi air pendingin masuk pada T = 25oC ; 1 atm Kondisi air pendingin keluar pada T = 40oC ; 1 atm
H (25 oC) = 125,8 kJ/kg (Reklaitis)
H (40 oC) = 167,5 kJ/kg (Reklaitis)
Maka jumlah air pendingin yang dibutuhkan :
Mammonia = C) (25 H -C) (40 H Q o o = kJ/kg 125,8 -kJ/kg 167,5 kJ/jam ,19 15.440.127 = 370.266,8391 kg/jam
Tabel LB.12. Neraca Panas pada Condensor (CD-01) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 23.044.076,89 -
Produk - 7.603.949,707
Air pendingin - 15.440.127,19
Total 23.044.076,89 23.044.076,89 LB.4. Kolom Destilasi 1 (KD – 01)
KD-01
Fungsi : Untuk memisahkan campuran metanol dan air sebagai produk bawah dengan dimetil eter sebagai produk atas.
Gambar LB.4. Diagram alir kolom destilasi (KD-01)
Kondisi Feed : bubble point Menentukan suhu umpan masuk :
Umpan yang masuk ke kolom destilasi merupakan cairan jenuh. Untuk menentukan suhu umpan, maka dilakukan perhitungan bubble point dengan cara trial suhu umpan hingga syarat ∑ Ki.xi = 1 terpenuhi.
Tabel LB.13 Komposisi Bahan Masuk Kolom Destilasi (KD – 01) Komponen F (kg/jam) N (kmol/jam) Fraksi mol (xi)
CH3OH 5420,3966 169,3874 0,0997 H2O 13.801,8070 766,7671 0,4515 CH3OCH3 52,6738 1,1451 0,4488 Total 54.382,1029 1701,4234 1.0000 Persamaan Antoine : ln Pi = A - C T B , dimana P = kPa, T = oK Kondisi umpan masuk [F4] :
P = 8 atm = 810,6 kPa T = 70 oC = 343 oK 5 Q4 H2O(l) CH3OH (l) CH3OCH3 (l) T = 70oC P = 8 atm 10 4 Q5 H2O(g) CH3OH (g) CH3OCH3 (g) T = 70oC P = 8 atm Q10 H2O(l) CH3OH (l) CH3OCH3 (l) T = 70oC
Tabel LB.14. Nilai Bilangan Antoine
Komponen A B C
CH3OH 16,4948 3.593,39 -35,2249
H2O 16,5392 3.985,44 -38,9974
CH3OCH3 14,3448 2.176,84 -24,6733
Dengan menggunakan persamaan antoine maka diperoleh : Menghitung Tekanan pada Dimetil Eter :
ln PiDME = A - C T B = 14,3448- (-24,6733) 343 2176,84 = 7,5064 Pi = 1819,6813 kPa
Menghitung tekanan pada Metanol : ln PiMetanol = A - C T B = 16,4948 - (-35,2249) 343 3.593,39 = 4,8194 Pi = 123,8937 kPa
Menghitung tekanan pada Air : ln PiAir = A - C T B = 16,5392 - (-38,9974) 343 3.985,44 = 3,4293 Pi = 30,8554 kPa Menghitung nilai Ki
Ki = Pi/P a. Dimetil Eter Ki = 810,6 123,8937 = 0,1528 b. Metanol Ki = 810,6 30,8554 = 0,0381 c. Air Ki = 810,6 1.819,6813 = 2,2449 Menentukan Harga Yi Yi = Ki × Xi a. Dimetil Eter Yi = 0,1528 × 0,0997 = 0,0152 b. Metanol Yi = 0,0381 × 0,4515 = 0,0172 c. Air Yi = 2,2449 × 0,4488 = 1,0075
Berikut data yang diperoleh :
Tabel LB.15. Perhitungan untuk temperatur umpan masuk (bubble point)
Komponen xi Pi P Pi Ki Yi = Ki . xi CH3OCH3 0,0997 123,8937 0,1528 0,0152 CH3OH 0,4515 30,8554 0,0381 0,0172 H2O 0,4488 1.819,6813 2,2449 1,0075 Total 1,0399 Panas Masuk
K K o o dT Cp Ni Q 343 298 .Tabel LB.16. Perhitungan Panas Masuk pada Kolom Destilasi (KD-01) Alur Komponen N (kmol)
K K o o T Cp 343 298 . (kJ/kmol.K) Q(kJ/jam) 4 CH3OH 169,6892 3.844,4873 652.367,806 CH3OCH3 763,6012 5.693,0375 4.347.210,308 H2O 768,1330 3.390,5215 2.604.371,594 Total 7.603.949,707 Panas Keluar
K K o o Hvl dT Cp Ni Q 343 298 .Tabel LB.17. Perhitungan Panas Keluar Destilat Kolom Destilasi (KD-01) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 343 298 . (kJ/kmol.K) Q (kJ/jam) 5 CH3OH 0,2545 35.270,4 2.046,6958 9.498,4597 CH3OCH3 762,4558 - 3.367,5468 2.567.605,6138 H2O 1,1522 40.656,2 1.517,3376 48.592,3316 Total 3.717.829,808
K K o o Hvl dT Cp Ni Q 343 298 .Tabel LB.18. Perhitungan Panas Keluar Bottom Kolom Destilasi (KD-01) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 343 298 . (kJ/kmol.K) Q (kJ/jam) 10 CH3OH 200,5607 - 3.844,4873 771.052,9587 CH3OCH3 1,3559 21.510,1 5.693,0376 36.882,5107 H2O 907,8794 - 3.390,5215 3.078.184,43 Total 3.886.119,899
Panas Refluks Kondensor
K K o o dT Cp Ni Q 315 298 .Tabel LB.19. Perhitungan Panas Refluks Kondensor Alur Komponen N (kmol)
K K o o T Cp 315 298 . (kJ/kmol.K) Q(kJ/jam) 9 CH3OH 0,8206 1398,8626 1147,90665 CH3OCH3 3.533,6014 2060,6975 7.281.683,571 H2O 2,0895 1276,2024 2.666,6249 Total 7.288.164,727
Panas Refluks Reboiler
QRB = Q destilat + Qbottom + Qrefluks kondensor – Qin
= 3.717.829,808 + 3.886.119,899 + 7.288.164,727 – 7.603.949,707 = 7.288.164,727 kJ/jam
Tabel LB. 20 Neraca Energi Total Kolom Destilasi (KD-01)
Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 7.603.949,707 Qdestilat 3.717.829,808
QRB 7.288.164,727 Qbottom 3.886.119,899
- Qkondensor 7.288.164,727
Total 14.892.114,4300 14.892.114,4300
LB.5. Condensor (CD-02)
Fungsi : Mengubah fasa metanol dan air yang berfasa gas menjadi fasa cair dari produk top kolom destilasi
CD-02
Gambar LB.5. Diagram alir Condensor (CD-02)
Perhitungan untuk titik embun (dew point) berdasarkan trial hingga ∑ 1
i i
K y
Berikut adalah data trial terakhir dengan menggunakan suhu 42 oC Tekanan : 8 atm = 810,600 kPa
Temperatur : 42 oC = 315 oK
Berikut adalah trial terakhir yang dilakukan Menentukan harga yi yi = Mol/Total mol yi DME = 0906 , 983 2801 , 981 = 0,9982 yi metanol = 0906 , 983 3276 , 0 = 0,0003 yi air = 0906 , 983 4829 , 1 = 0,0015 Menentukan harga Pi ln Pi DME = A - C T B Q5 CH3OCH3 (g) H2O(g) CH3OH (g) T = 70oC Q6 CH3OCH3 (l) H2O(l) CH3OH (l) T = 42oC 5 6 Air pendingin T = 25oC
Air pendingin bekas T = 40oC
= 14,3448- (-24,6733) 315 2.176,84 Pi = 940,9612 kPa
Menghitung tekanan pada Metanol : ln Pi Metanol = A - C T B = 16,4948 - (-35,2249) 315 3.593,39 Pi = 38,5112 kPa
Menghitung tekanan pada Air : ln Pi Air = A - C T B = 16,5392 - (-38,9974) 343 3.985,44 Pi = 8,1607 kPa Menentukan harga Ki Ki = Pi/P Ki DME = 810,6000 940,9612 = 1,1608 Ki Metanol = 810,6000 38,5112 = 0,0070 Ki Air = 810,6000 8,1607 = 0,0101 Menentukan harga xi xi DME = f K x
= 1,1608 0,9982 = 0,8599 xi Metanol = 0,0475 0,0003 = 0,0070 xi Air = 0,0101 0,0015 = 0,1498
Tabel LB.21. Data trial akhir temperatur titik embun (dew point)
Komponen yi Pi P Pi Ki i i i K y x CH3OCH3 0,9982 940,961 1,1608 0,8599 CH3OH 0,0003 38,5112 0,0475 0,0070 H2O 0,0015 8,1607 0,0101 0,1478 Total 1,0000 1,0167 Panas masuk
K K o o Hvl dT Cp Ni Q 343 298 .Tabel LB.22. Perhitungan Panas Umpan Masuk Condensor (CD-02) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 343 298 . (kJ/kmol.K) Q (kJ/jam) 5 CH3OH 0,2545 35.270,4 2.046,6958 9.498,4597 CH3OCH3 762,4558 - 3.367,5468 2.567.605,6138 H2O 1,1522 40.656,2 1.517,3376 48.592,3316 Total 2.625.696,4051 Panas Keluar
K K o o Hvl dT Cp Ni Q 315 298 .Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 315 298 . (kJ/kmol.K) Q (kJ/jam) 6 CH3OH 0,2545 - 1.398,8626 356,0577 CH3OCH3 762,4558 - 2.060,6975 1.571.190,781 H2O 1,1522 - 1.276,2024 1.470,4398 Total 1.573.017,278Panas yang diserap air (Q) adalah :
K K in K K out o o o o Hvl dT Cp Ni Hvl dT Cp Ni dT dQ 343 298 315 298 . .Qair pendingin = Qout - Qin
= 1.573.017,278 kJ/jam - 2.625.696,4051 kJ/jam = -1.052.679,127 kJ/jam
Kondisi air pendingin masuk pada T = 25oC ; 1 atm Kondisi air pendingin keluar pada T = 40oC ; 1 atm
H (25oC) = 125,8 kJ/kg (Reklaitis)
H (40oC) = 167,5 kJ/kg (Reklaitis)
Maka jumlah air pendingin yang dibutuhkan : Mair pendingin = C) (25 H -C) (40 H Q o o = kJ/kg 125,8 -kJ/kg 208 kJ/jam 127 1.052.679, = 25.244,1038 kg/jam
Tabel LB.24. Neraca Panas pada Condensor (CD-02) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 2.625.696,4051 -
RB-01
Air pendingin - 1.052.679,127
Total 2.625.696,4051 2.625.696,4051
LB.6. Reboiler (RB-01)
Fungsi : Untuk menguapkan kembali dimetil eter yang masih tersisa di bottom kolom destilasi
Gambar LB.6. Reboiler (RB-01)
Perhitungan untuk titik didih (bubble point) berdasarkan trial hingga ∑yi.xi 1
Berikut adalah trial akhir dengan menggunakan temperatur 159 oC
Menentukan harga xi xi = Mol/Total mol xi DME = 6403 , 1206 4741 , 1 = 0,0012 xi metanol = 6403 , 1206 0623 , 218 = 0,1807 xi air = 6403 , 1206 1039 , 987 = 0,8181 Q11 (V) CH3OCH3 (g) H2O(g) CH3OH (g) T= 159 oC Q10 (L) CH3OCH3 (l) H2O(l) CH3OH (l) T = 70oC Q12 (B) CH3OCH3 (l) H2O(l) CH3OH (l) T= 159oC 11 10 12 Steam T=180oC Kondensat T = 180oC P = 10 atm
Menentukan harga Pi ln Pi DME = A - C T B = 4,3448- (-24,6733) 432 2176,84 Pi = 8107,8547 kPa
Menghitung tekanan pada Metanol : ln Pi Metanol = A - C T B = 16,4948 - (-35,2249) 432 3593,39 Pi = 1699,8738 kPa
Menghitung tekanan pada Air : ln Pi Air = A - C T B = 16,5392 - (-38,9974) 432 3985,44 Pi = 600,7617 kPa Menentukan harga Ki KiDME = Pi/P = 810,6000 8107,8547 = 10,0023 KiMetanol = 810,6000 1699,8738 = 2,0971 KiAir = 810,6000 600,7617 = 0,7411
Menentukan harga yi yi = xi × Ki yi DME = 0,0012 × 10,0023 = 0,0122 yi Metanol = 0,1807 × 2,0971 = 0,3790 yi Air = 0,8181 × 0,7411 = 0,6063
Tabel LB.25. Data trial error temperatur titik didih (bubble point) Reboiler
Komponen xi Pi P Pi Ki yi = xi.Ki CH3OCH3 0,0012 8.107,8547 10,0023 0,0122 CH3OH 0,1807 1.699,8738 2,0971 0,3790 H2O 0,8181 600,7617 0,7411 0,6063 Total 1,0000 0,9975 Panas Masuk
K K o o Hvl dT Cp Ni Q 343 298 .Tabel LB.26. Perhitungan Panas Umpan Masuk Reboiler (RB-01) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 343 298 . (kJ/kmol.K) Q (kJ/jam) 10 CH3OH 200,5607 - 3.844,4873 771.052,9587 CH3OCH3 1,3559 21.510,1 5.693,0376 36.882,5107 H2O 907,8794 - 3.390,5215 3.078.184,43 Total 3.886.119,899 Panas Keluar
K K o o Hvl dT Cp Ni Q 432 298 .Tabel LB.27. Perhitungan Panas Refluks Reboiler (RB-01) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 432 298 . (kJ/kmol.K) Q (kJ/jam) 11 CH3OH 0,0472 6.546,6779 309,1829 CH3OCH3 0,0003 10.819,4568 3,4543 H2O 0,2138 40656,2 4.559,2093 9.666,3667 Total 9.979,0039
Tabel LB.28. Perhitungan Panas Keluar Bottom Reboiler (RB-01) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 432 298 . (kJ/kmol.K) Q (kJ/jam) 12 CH3OH 200,5135 - 14.178,6192 2.843.003,771 CH3OCH3 1,3555 - 20.549,7502 57.012,0848 H2O 907,6656 - 10.226,6547 9.282.382,231 Total 12.182.398,09
Panas yang dibutuhkan (Q) adalah :
K K in K K bottom K K refluks o o o o o o Hvl dT Cp Ni Hvl dT Cp Ni Hvl dT Cp Ni dT dQ 343 298 432 298 432 298 . . .Qsteam = (Qrefluks + Qbottom )- Qin
= (9.979,0039 kJ/jam + 12.182.398,09 kJ/jam) - 3.886.119,899 kJ/jam = 8.306.257,191 kJ/jam
Kondisi steam masuk adalah saturated steam pada T = 179,9oC ; 10 atm Kondisi kondensat keluar pada T = 179,9oC ; 10 atm Steam H (179,9 oC) = 2776.2 kJ/kg (Reklaitis) Kondensat H (179,9 oC) = 762,6 kJ/kg (Reklaitis) Maka jumlah steam yang dibutuhkan :
Msteam = C) (179,9 H -C) (179,9 H Q o kondensat o steam
H-01 = kJ/kg 762,6 -kJ/kg 2.776,2 kJ/jam 191 8.306.257, = 4.125,0781 kg/jam
Tabel LB.29. Neraca Panas pada Reboiler (RB-01) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 3.886.119,899 - Refluks - 9.979,0039 Bottom - 12.182.398,09 Steam 8.306.257,191 - Total 12.192.377,09 12.192.377,09 LB.7. Heater (H-01)
Fungsi : Meningkatkan temperatur umpan hingga 165 oC yang akan disuplai ke kolom destilasi 2 sesuai titik didihnya agar lebih memudahkan pemisahan metanol dengan air.
Gambar LB.7. Diagram alir heater (H-01)
Panas Masuk
K K o o dT Cp Ni Q 432 298 .Tabel LB.30. Panas Umpan Masuk pada Heater (H-01) Q12 H2O(l) CH3OH (l) CH3OCH3 (l) T= 159 oC Q13 H2O(l) CH3OH (l) CH3OCH3 (l) T= 165 oC Steam T= 180 oC P = 10 atm Kondensat T= 180 oC
Alur Komponen N (kmol)
K K o o T Cp 432 298 . (kJ/kmol.K) Q (kJ/jam) 12 CH3OH 200,5135 14.178,6192 2.843.003,771 CH3OCH3 1,3555 20.549,7502 27.855,1658 H2O 907,6656 10.226,6547 9.282.382,231 Total 12.153.241,17 Panas Keluar
K K o o dT Cp Ni Q 438 298 .Tabel LB.31. Panas Keluar pada Heater (H-01)
Alur Komponen N (kmol)
K K o o T Cp 438 298 . (kJ/kmol.K) Q (kJ/jam) 13 CH3OH 200,5135 15.119,7958 3.031.722,325 CH3OCH3 1,3555 21.815,5314 29.570,9309 H2O 907,6656 10.697,7572 9.709.985,76 Total 12.771.279,02
Panas yang diberikan steam, Qs :
K K in K K out o o o o dT Cp Ni dT Cp Ni dT dQ 432 298 438 298 . . Qs = Qkeluar – Qmasuk = (12.771.279,02 – 12.153.241,17) kJ /jam = 618.037,8477 kJ/jamKondisi steam masuk adalah saturated steam pada T = 179,9oC ; 10 atm Kondisi kondensat keluar pada T = 179,9oC ; 10 atm Steam H (179,9 oC) = 2676 kJ/kg (Reklaitis) Kondensat H (179,9 oC) = 419,4 kJ/kg (Reklaitis) Maka jumlah steam yang dibutuhkan :
KD-02 Msteam = C) (179,9 H -C) (179,9 H Q o kondensat o steam = kJ/kg 762,6 -kJ/kg 2.776,2 kJ/jam 77 618.037,84 = 306,9318 kg/jam
Tabel LB.32. Neraca Panas pada Heater (H-01) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 12.153.241,17 -
Produk - 12.771.279,02
Steam 618.037,8477 -
Total 12.771.279,02 12.771.279,02
LB.8. Kolom Destilasi 2 (KD – 02)
Fungsi : Untuk memisahkan campuran, dimana air sebagai produk bawah dan metanol sebagai produk atas
Gambar LB.8. Diagram alir kolom destilasi (KD-02) Persamaan Antoine : ln Pi = A - C T B , dimana P = Bar, T = oK
Dengan melakukan perhitungan trial error bubble point untuk mendapatkan suhu titik didih maka didapatkan kondisi umpan masuk KD – 102 :
P = 9,2 atm = 932,19 kPa T = 165 oC = 438 oK 14 Q13 H2O(l) CH3OH (l) CH3OCH3 (l) T = 165 oC 19 13 Q14 H2O(g) CH3OH g) CH3OCH3 (g) T = 136 oC Q19 H2O(l) CH3OH (l) CH3OCH3 (l) T = 177 oC
Tabel LB.33. Nilai Bilangan Antoine
Komponen A B C
CH3OH 16,4948 3593,3900 -35,2249
H2O 16,5392 3985,4400 -38,9974
CH3OCH3 14,3448 2176,8400 -24,6733
Dengan menggunakan persamaan antoine maka diperoleh : Menghitung Tekanan pada DME :
ln PiDME = A - C T B = 14,3448- (-24,6733) 438 2176,84 Pi = 8.761,8916 kPa
Menghitung tekanan pada Metanol : ln PiMetanol = A - C T B = 16,4948 - (-35,2249) 438 3593,39 Pi = 1.945,3957 kPa
Menghitung tekanan pada Air : ln PiAir = A - C T B = 16,5392 - (-38,9974) 438 3985,44 Pi = 699,7294 kPa Menghitung nilai Ki Ki = Pi/P a. Dimetil Eter
Ki = 932,19 8.214,6684 = 9,3993 b. Metanol Ki = 932,19 1.739,0203 = 2,0869 c. Air Ki = 932,19 616,4251 = 0,7506 Menentukan Harga Yi Yi = Ki × Xi a. Dimetil Eter Yi = 9,3993 × 0,0012 = 0,0115 b. Metanol Yi = 2,0869 × 0,1807 = 0,3771 c. Air Yi = 0,7506 × 0,8181 = 0,6141
Berikut data yang diperoleh :
Tabel LB.34. Kondisi Umpan Masuk Kolom Destilasi (KD-02)
Komponen xi Pi P Pi Ki Yi = Ki. xi CH3OCH3 0,0012 8.761,8916 9,3993 0,0115 CH3OH 0,1807 1.945,3957 2,0869 0,3771 H2O 0,8181 699,7294 0,7506 0,6141 Total 1,0000 11.407,0167 1,022 Panas Masuk
K K o o dT Cp Ni Q 438 298 .Tabel LB.35. Panas Masuk Kolom Destilasi (KD-02)
Alur Komponen N (kmol)
K K o o T Cp 438 298 . (kJ/kmol.K) Q (kJ/jam)
13 CH3OH 200,5135 15.119,7958 3.031.722,325 CH3OCH3 1,3555 21.815,5314 29.570,9309 H2O 907,6656 10.697,7572 9.709.985,76 Total 12.771.279,02 Panas Keluar
K K o o Hvl dT Cp Ni Q 409 298 .Tabel LB.36. Perhitungan Panas Keluar Destilat Kolom Destilasi (KD-02) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 409 298 . (kJ/kmol.K) Q (kJ/jam) 14 CH3OH 200,2127 35.270,4 6.872,3779 2.437.518,245 CH3OCH3 1,3535 - 11.359,9203 15.375,2629 H2O 1,3615 - 4.766,5947 6.489,7107 Total 3.010.644,367
K K o o Hvl dT Cp Ni Q 438 298 .Tabel LB. 37. Perhitungan Panas Keluar Bottom Kolom Destilasi (KD-02) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 438 298 . (kJ/kmol.K) Q (kJ/jam) 19 CH3OH 0,3023 35.270,4 15.119,7958 15.233,8579 CH3OCH3 0,0020 21.510,1 21.815,5314 88,5451 H2O 910,9678 - 10.697,7572 9.745.312,25 Total 9.760.634,653
Panas Refluks Kondensor
K K o o dT Cp Ni Q 438 298 .Tabel LB.38. Perhitungan Panas Refluks Kondensor Alur Komponen N (kmol)
K K o o T Cp 438 298 . (kJ/kmol.K) Q(kJ/jam)
CD-03 18 CH3OH 64,0681 10.936,9223 700.707,8316 CH3OCH3 0,6226 16.065,3910 10.002,31245 H2O 0,2451 8.436,5589 2.067,8006 Total 712.777,9446
Panas Refluks Reboiler
QRB = Q destilat + Qbottom + Qrefluks kondensor – Qin
= 3.010.644,367 + 9.760.634,653 + 712.777,9446 – 12.771.279,02 = 712.777,9446 kJ/jam
Tabel LB. 39. Neraca Energi Total Kolom Destilasi (KD-01)
Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 12.771.279,02 Qdestilat 3.010.644,367
QRB 712.777,9446 Qbottom 9.760.634,653
- Qkondensor 712.777,9446
Total 13.484.056,96 13.484.056,96
LB.9. Condensor (CD-03)
Fungsi : Mengkondensasikan air produk dari menara destilasi
Q14 CH3OCH3 (g) H2O(g) CH3OH (g) T = 165 oC 14 15 Air pendingin T = 25oC Q15 CH3OCH3 (l) H2O(l) CH3OH (l) T = 136 oC
Gambar LB.9. Diagram alir condensor (CD-03)
Perhitungan untuk titik embun (dew point) berdasarkan trial hingga ∑ 1
i i
K x
Berikut adalah data trial terakhir dengan menggunakan suhu 136 oC Tekanan : 9,2 atm = 932,19 kPa
Temperatur : 136 oC = 409 oK
Berikut adalah trial terakhir yang dilakukan Menentukan harga xi xi = Mol/Total mol xi DME = 4268 , 171 1434 , 1 = 0,0067 xi metanol = 4268 , 171 1333 , 169 = 0,9866 xi air = 4268 , 171 1502 , 1 = 0,0067 Menentukanharga Pi ln PiDME = A - C T B = 14,3448- (-24,6733) 409 2.176,84 Pi = 5.888,5478 kPa Menghitung tekanan pada Metanol : ln PiMetanol = A - C T B
Air pendingin bekas T = 40oC
= 16,4948 - (-35,2249) 409 3.593,39 Pi = 973,6231 kPa
Menghitung tekanan pada Air : ln PiAir = A - C T B = 16,5392 - (-38,9974) 409 3.985,44 Pi = 319,8385 kPa Menentukan harga Ki Ki = P Pi a. Dimetil Eter Ki = 932,19 5.888,5478 = 6,3269 b. Metanol Ki = 932,19 973,6231 = 1,0444 c. Air Ki = 932,19 319,8385 = 0,3431 Menentukan harga Yi Yi = i i K x Yi DME = 3169 , 6 0067 , 0 = 0,0011 Yi metanol = 0444 , 1 9866 , 0 = 0,9446
Yi air = 3431 , 0 1502 , 1 = 0,0196
Tabel LB.40. Data trial error titik embun (dew point)
Komponen xi Pi P Pi Ki Yi = xi /Ki CH3OCH3 0,0067 5888,5478 6,3169 0,0011 CH3OH 0,9866 973,6231 1,0444 0,9446 H2O 0,0067 319,8385 0,3431 0,0196 Total 1,0000 0,9652 Panas masuk
K K o o Hvl dT Cp Ni Q 438 298 .Tabel LB.41. Perhitungan Panas Umpan Masuk Condensor (CD-03) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 438 298 . (kJ/kmol.K) Q (kJ/jam) 14 CH3OH 200,2127 35.270,4 6.872,3779 8.437.518,245 CH3OCH3 1,3535 - 11.359,9203 15.375,2629 H2O 1,3615 - 4.766,5947 6.489,7107 Total 8.459.383,219 Panas Keluar
409 298 .dT Hvl Cp Ni QTabel LB.42. Perhitungan Panas Keluar Condensor (CD-03) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 409 298 . (kJ/kmol.K) Q (kJ/jam) 15 CH3OH 200,2127 - 10.936,9223 2.189.710,455 CH3OCH3 1,3535 - 16.065,3910 21.743,9566
H2O 1,3615 - 8.436,5589 11.486,3611
Total 2.222.940,773
Panas yang diserap air (Q) adalah :
K K in K K out o o o o Hvl dT Cp Ni Hvl dT Cp Ni dT dQ 438 298 409 298 . .Qair pendingin = Qout - Qin
= 2.222.940,773 kJ/jam – 8.459.383,219 kJ/jam = -6.236.442,446 kJ/jam
Kondisi air pendingin masuk pada T = 25 oC ; 1 atm Kondisi air pendingin keluar pada T = 40 oC ; 1 atm
H (25oC) = 125,8 kJ/kg (Reklaitis)
H (40oC) = 167,5 kJ/kg (Reklaitis)
Maka jumlah air pendingin yang dibutuhkan : Mair pendingin = C) (25 H -C) (40 H Q o o = kJ/kg 125,8 -kJ/kg 167,5 kJ/jam 446 6.236.442, = 149.554,9747 kg/jam
Tabel LB.43. Neraca Panas pada Condenser (CD-03) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 8.404.157,215 -
Produk - 2.093.547,103
Air pendingin - 6.236.442,446
Total 8.404.157,215 8.404.157,215
LB.11. Reboiler (RB-02)
Fungsi : Untuk menguapkan sebagian metanol pada bottom kolom destilasi Q20 (V) CH3OCH3 (g) H2O(g) CH3OH (g) T= 177oC 20 Steam T=180 oC
Gambar LB.10. Diagram alir reboiler (RB-02)
Perhitungan untuk titik didih (bubble point) berdasarkan trial hingga ∑yi.xi 1
Berikut adalah data trial akhir dengan menggunakan temperatur 177 oC
Menentukan harga Yi Yi = Mol/Total mol YiDME = 8727 , 765 0017 , 0 = 2,2196 × 10-6 Yimetanol = 8727 , 765 2541 , 0 = 0,0003 Yi air = 8727 , 765 6169 , 765 = 0,9997 Menentukan harga Pi ln PiDME = A - C T B = 14,3448- (-24,6733) 450 2176,84 Pi = 10165,5293 kPa
Menghitung tekanan pada Metanol : ln PiMetanol = A - C T B Q19 (L) CH3OCH3 (l) H2O(l) CH3OH (l) T = 165oC Q21 (B) H2O(l) CH3OH (l) CH3OCH3 (l) T= 177oC 19 Kondensat T = 180 oC 21
= 16,4948 - (-35,2249) 450 3593,39 Pi = 2518,2864 kPa
Menghitung tekanan pada Air : ln PiAir = A - C T B = 16,5392 - (-38,9974) 450 3985,44 Pi = 936,6663 kPa Menentukan harga Ki KiDME = P Pi = 932,19 10165,5293 = 10,9050 KiMetanol = 932,19 2518,2864 = 2,7015 KiAir = 932,19 936,6663 = 1,0048 Menentukan harga xi xi = Ki × Yi xi DME = 10,9050 × 2,2196 × 10-6 = 2,420 × 10-5 xi Metanol = 2,7015 × 0,0003 = 0,0009 xi Air = 1,0048 × 0,9997 = 1,0045
Komponen Yi Pi P Pi Ki xi = Ki.Yi CH3OCH3 2,2196 × 10-6 10.165,5293 10,9050 2,420 × 10-5 CH3OH 0,0003 2518,2864 2,7015 0,0009 H2O 0,9997 936,6663 1,0048 1,0045 Total 1,0000 1,0048 Panas Masuk
K K o o Hvl dT Cp Ni Q 438 298 .Tabel LB. 45. Perhitungan Panas Umpan Masuk Reboiler (RB-02) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 438 298 . (kJ/kmol.K) Q (kJ/jam) 19 CH3OH 0,3023 35.270,4 15.119,7958 15.233,8579 CH3OCH3 0,0020 21.510,1 21.815,5314 88,5451 H2O 910,9678 - 10.697,7572 9.745.312,25 Total 9.760.634,653 Panas Keluar
K K o o Hvl dT Cp Ni Q 450 298 .Tabel LB.46. Perhitungan Panas Refluks Reboiler (RB-02) Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 450 298 . (kJ/kmol.K) Q (kJ/jam) 20 CH3OH 0,0004 - 7.532,3262 2,6456 CH3OCH3 2,37E-06 - 12.455,1686 0,0296 H2O 1,0583 - 5.182,3349 5.484,6793 Total 5.487,3544
Alur Komponen N (kmol) ∆Hvl
K K o o T Cp 450 298 . (kJ/kmol.K) Q (kJ/jam) 21 CH3OH 0,3020 35.270,4 17.140,153 15.826,2401 CH3OCH3 0,002 21.510,1 24.479,497 93,8803 H2O 910,2135 - 11.646,1568 10.596.948,16 Total 10.612.868,28Panas yang dibutuhkan (Q) adalah :
K K in K K bottom K K refluks o o o o o o Hvl dT Cp Ni Hvl dT Cp Ni Hvl dT Cp Ni dT dQ 438 298 450 298 450 298 . . .Qsteam = (Qrefluks + Qbottom )- Qin
= (5.487,3544 kJ/jam + 10.612.868,28 kJ/jam) – 9.760.634,653 kJ/jam = 857.720,9806 kJ/jam
Kondisi steam masuk adalah super steam pada T = 179,9oC ; 10 atm Kondisi kondensat keluar pada T = 179,9oC ; 10 atm Steam H (179,9oC) = 2676 kJ/kg (Reklaitis) Kondensat H (179,9oC)= 419,4 kJ/kg (Reklaitis)
Maka jumlah steam yang dibutuhkan :
Msteam = C) (179,9 H -C) (179,9 H Q o kondensat o steam = kJ/kg 762,6 -kJ/kg 2.776 kJ/jam 06 857.720,98 = 425,9639 kg/jam
Tabel LB.48. Neraca Panas pada Reboiler (RB-02) Masuk (kJ/jam) Keluar (kJ/jam)
C-01 Umpan 9.760.634,653 - Refluks - 5.487,3544 Bottom - 10.612.868,28 Steam 857.720,9806 - Total 10.618.355,63 10.618.355,63 LB.12. Cooler (C – 01)
Fungsi : Untuk menurunkan temperatur produk dari reboiler (RB-02)
Gambar LB.11. Diagram alir cooler (C-01)
Panas Masuk
K K o o dT Cp Ni Q 450 298 .Tabel LB.49. Perhitungan Panas Masuk pada Cooler (C-01)
Alur Komponen N (kmol)
K K o o T Cp 450 298 . (kJ/kmol.K) Q (kJ/jam) CH3OH 0,30197 17.140,15295 5.175,7549 21 CH3OCH3 0,0021 24.479,4970 49,9709 H2O 909,9095 11.646,1569 10.596.948,16 Total 10.602.173,88 Panas Keluar Q21 CH3OCH3 (l) H2O(l) CH3OH (l) T = 177 oC Q22 CH3OCH3 (l) H2O (l) CH3OH (l) T = 30 oC Air pendingin T = 25oC
Air pendingin bekas T = 40oC
K K o o dT Cp Ni Q 303 298 .Tabel LB.50. Perhitungan Panas Keluar pada Cooler (C-01)
Alur Komponen N (kmol)
K K o o T Cp 303 298 . (kJ/kmol.K) Q (kJ/jam) CH3OH 0,30197 405,9901 122,5955 22 CH3OCH3 0,0021 596,5609 1,2178 H2O 909,9095 374,6878 340.932,0048 Total 341.055,8181
Panas yang diserap air pendingin (Q) adalah :
K K in K K out o o o o dT Cp Ni dT Cp Ni dT dQ 450 298 303 298 . .Qair pendingin = Qout - Qin
= 341.055,8181 kJ/jam – 10.602.173,88 kJ/jam = -10.261.118,07 kJ.jam
Kondisi air pendingin masuk pada T = 25oC ; 1 atm Kondisi air pendingin keluar pada T = 40oC ; 1 atm
H (40oC) = 167,5 kJ/kg (Reklaitis)
H (25oC) = 125,8 kJ/kg (Reklaitis)
Maka jumlah air pendingin yang dibutuhkan : Mair pendingin = C) (25 H -C) (40 H Q o o = kJ/kg 125,8 -kJ/kg 167,5 kJ/kg ,07 10.261.118 = 246.069,9776 kg/jam
Tabel LB.51. Neraca Panas pada Cooler (C-01) Masuk (kJ/jam) Keluar (kJ/jam)
Umpan 10.602.173,88 -
Produk - 341.055,8181
Air pendingin - 10.261.118,07
LAMPIRAN C
PERHITUNGAN SPESIFIKASI ALAT
1. Tangki Penyimpanan Metanol
Fungsi : Menyimpan metanol untuk kebutuhan 30 hari Bahan konstruksi : Carbon Steel SA-285 Grade C
Bentuk : Silinder vertikal dengan alas datar dan tutup ellipsoidal Jenis sambungan : Single welded butt joints
Jumlah : 4 unit
T-102
Gambar LC.1. Tangki Penyimpanan Metanol (T-01) Kondisi operasi :
Tekanan = 1 atm
Temperatur = 30 C
Laju alir massa = 54.382,10289 kg/jam
Densitas = 791,5 kg/m3
Kebutuhan perancangan = 30 hari
Faktor keamanan = 10 % Perhitungan: a. Volume tangki Volume larutan,Vl = 3 / 5 , 791 jam/hari 24 hari 30 kg/jam 939 2.915.716, m kg = 55.256 m3 Terdapat 4 tangki maka =
4 m 55.256 3 = 13.814,19902 m3 Volume tangki, Vs = (13.814 × 0,1) + 24734,75305 m3 = 15.195,61892 m3 T - 01