BAB 2
TINJAUAN PUSTAKA
2.1. Kitosan
Kitosan adalah senyawa polimer alam turunan kitin yang diisolasi dari limbah perikanan, seperti kulit. udang dan cangkang kepiting dengan kandungan kitin antara 65-70 persen. Sumber bahan baku kitosan yang lain di antaranya kalajengking, jamur, cumi, gurita, serangga, laba - laba dan ulat sutera dengan kandungan kitin antara 5-45 persen. Kitosan merupakan bahan kimia multiguna berbentuk serat dan merupakan kopolimer berbentuk lembaran tipis, berwarna putih atau kuning, tidak berbau. Kitosan merupakan produk deasetilasi kitin melalui proses kimia menggunakan basa natrium bidroksida atau proses enzimatis menggunakan enzim chitin deacetylase. Serat ini bersifat tidak dicerna dan tidak diserap tubuh. Sifat menonjol kitosan adalah kemampuan mengabsorpsi lemak hingga 4-5 kali beratnya (Rismana, 2006).
Kitosan adalah senyawa kimia yang berasal dari bahan hayati kitin, suatu senyawa organik yang melimpah di alam ini setelah selulosa. Kitin ini umumnya diperoleh dari kerangka hewan invertebrata dari kelompok Arthopoda sp, Molusca sp, Coelenterata sp,
Annelida sp, Nematoda sp, dan beberapa dari kelompok jamur Selain dari kerangka
hewan invertebrata, juga banyak ditemukan pada bagian insang ikan, trakea, dinding usus dan pada kulit cumi-cumi. Sebagai sumber utamanya ialah cangkang Crustaceae sp, yaitu udang, lobster, kepiting, dan hewan yang bercangkang lainnya, terutama asal laut. Sumber ini diutamakan karena bertujuan untuk memberdayakan limbah udang (Hawab, 2005).
Kitosan adalah produk terdeasetilasi dari kitin yang merupakan biopolimer alami kedua terbanyak di alam setelah selulosa, yang banyak terdapat pada serangga, krustasea, dan fungi (Sanford and Hutchings, 1987). Diperkirakan lebih dari 109-1.010 ton kitosan diproduksi di alam tiap tahun. Sebagai negara maritim, Indonesia sangat berpotensi menghasilkan kitin dan produk turunannya. Limbah cangkang rajungan di Cirebon saja berkisar 10 ton perhari yang berasal dari sekurangnya 20 industri kecil. Kitosan tersebut masih menjadi limbah yang dibuang dan menimbulkan masalah lingkungan. Data statistik menunjukkan negara yang memiliki industri pengolahan kerang menghasilkan sekitar 56.200 ton limbah. Pasar dunia untuk produk turunan kitin menunjukkan bahwa oligomer kitosan adalah produk yang termahal, yaitu senilai $ 60.000/ton.
Kitosan merupakan senyawa turunan kitin, senyawa penyusun rangka luar hewan berkaki banyak seperti kepiting, ketam, udang dan serangga. Kitosan dan kitin termasuk senyawa kelompok polisakarida. Senyawa – senyawa lain yang termasuk kelompok polisakarida yang sudah tidak asing bagi kita adalah pati dan sellulosa. Polisakarida – polisakarida ini berbeda dalam jenis monosakarida penyusunnya dan cara monosakarida – monosakarida berikatan membentuk polisakarida (Rismana, 2006).
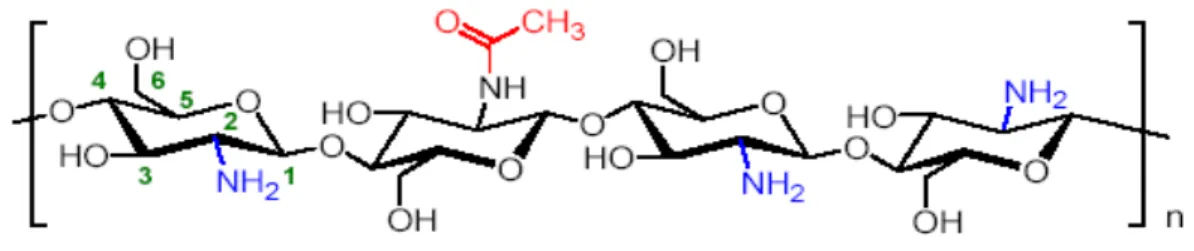
2.1.1. Struktur Kitosan
Kitosan adalah jenis polimer rantai yang tidak linier yang mempunyai rumus umum (C
-6H11O4)n atau disebut sebagai (1,4)-2-Amino-2-Deoksi-β-D-Glukosa, dimana strukturnya
dapat dilihat sebagai berikut :
2.1.2. Sifat – Sifat Kimia dan biologi Kitosan
Sebagian besar polisakarida yang terdapat secara alami seperti sellulosa, dekstran, pektin, asam alginat, agar, karangenan bersifat netral atau asam di alam, sedangkan kitosan merupakan polisakarida yang bersifat basa (Kumar, 2000).
Menurut Rismana (2006) sifat alami kitosan dapat dibagi menjadi dua sifat besar yaitu, sifat kimia dan biologi. Sifat kimia kitosan antara lain :
• Merupakan polimer poliamin berbentuk linear. • Mempunyai gugus amino aktif.
• Mempunyai kemampuan mengikat beberapa logam.
Sifat biologi kitosan antara lain:
• Bersifat biokompatibel artinya sebagai polimer alami sifatnya tidak mempunyai akibat samping, tidak beracun, tidak dapat dicerna, mudah diuraikan oleh mikroba (biodegradable).
• Dapat berikatan dengan sel mamalia dan mikroba secara agresif. • Bersifat hemostatik, fungistatik, spermisidal, antitumor, antikolesterol.
• Bersifat sebagai depresan pada sistem saraf pusat. Berdasarkan kedua sifat tersebut maka kitosan mempunyai sifat fisik khas yaitu mudah dibentuk menjadi spons, larutan, pasta, membran, dan serat. yang sangat bermanfaat.
(Rismana, 2006)
Kitosan dengan bentuk amino bebas tidak selalu larut dalam air pada pH lebih dari 6,5 sehingga memerlukan asam untuk melarutkannya. Kitosan larut dalam asam asetat dam asam formiat encer. Adanya dua gugus hidroksil pada kitin sedangkan kitosan dengan 1 gugus amino dan 2 gugus hidroksil merupakan target dalam modifikasi kimiawi (Hirano, dkk.,1987).
Sifat kation kitosan adalah linier polielektrolit, bermuatan positif, flokulan yang sangat baik, pengkelat ion – ion logam. Sifat biologi kitosan adalah non toksik, polimer alami, sedangkan sifat kimia seperti linier poliamin, gugus amino dan gugus hidroksil yang reaktif. Aplikasi kitosan dalam berbagai bidang tergantung sifat – sifat kationik, biologi dan kimianya (Sandford dan Hutchings, 1987).
2.1.3. Kelarutan Kitosan
Kitosan yang disebut juga dengan β-1,4-2 amino-2-dioksi-D-glukosa merupakan senyawa yang sedikit larut dalam HCl, HNO3, dan H3PO4 dan tidak larut dalam H2SO4. Kitosan
tidak beracun, mudah mengalami biodegradasi dan bersifat polielektrolitik. Disamping itu kitosan dapat dengan mudah berinteraksi dengan zat-zat organik lainnya seperti protein. Oleh karena itu, kitosan relatif lebih banyak digunakan pada berbagai bidang industri terapan dan industri kesehatan. Kitosan tidak larut dalam air, pelarut-pelarut organik, juga tidak larut dalam alkali dan asam-asam mineral pada pH di atas 6,5. Dengan adanya sejumlah asam, maka dapat larut dalam air-metanol, air-etanol, air-aseton, dan campuran lainnya. Kitosan larut dalam asam formiat dan asam asetat dan menurut Peniston dalam 20% asam sitrat juga dapat larut. Asam organik lainnya juga tidak dapat melarutkan kitosan, asam-asam anorganik lainnya pada pH tertentu setelah distirer dan dipanaskan dan asam sitrat juga dapat melarutkan kitosan pada sebagian kecil setelah beberapa waktu akan terbentuk endapan putih yang menyerupai jelly. ( Widodo. A, 2005 )
2.2. Glutaraldehide
Glutaraldehide adalah suatu senyawa organik dengan Rumus Molekul C5H8O2 /
CH2(CH2CHO)2, dengan Massa molar 100.12 g mol−1 dan densitasnya adalah 1.06 g/mL.
Glutaraldehid merupakan salah satu desinfektan yang populer pada kedokteran gigi, baik tunggal maupun dalam bentuk kombinasi.
Aldehid merupakan desinfektan yang kuat. Glutaraldehid 2% dapat dipakai untuk mendesinfeksi alat-alat yang tidak dapat disterilkan, diulas dengan kasa steril kemudian diulas kembali dengan kasa steril yang dibasahi dengan akuades, karena glutaraldehid yang tersisa pada instrumen dapat mengiritasi kulit/mukosa, operator harus memakai masker, kacamata pelindung dan sarung tangan heavy duty. Larutan glutaraldehid 2% efektif terhadap bakteri vegetatif seperti M. tuberculosis, fungi, dan virus akan mati dalam waktu 10-20 menit, sedang spora baru akan mati setelah 10 jam.
http://signaterdadie.wordpress.com/2009/10/08/desinfektan/
2.2.1. Struktur Glutaraldehide
Gambar 2.2. Struktur Glutarakdehide
Dilihat dari strukturnya, glutaraldehida mempunyai 2 gugus aldehida yang reaktif. Gugus aldehide tersebut sangat reaktif terhadap gugus amina pada kitosan sehingga apabila direaksikan, gugus aldehida akan berikatan kovalen dengan gugus amina dan membentuk jembatan yang menghubungkan polimer kitosan yang satu dengan yang lainnnya. Dengan penambahan agen crosslinking ini dipercaya dapat meningkatkan kekuatan mekanik membran.
http://en.wikipedia.org/wiki/Glutaraldehyde
2.3. Logam Tembaga (Cu) 2.3.1. Logam
Logam juga dapat menyebabkan timbulnya suatu bahaya pada makhluk hidup. Hal ini terjadi jika sejumlah logam mencemari lingkungan. Logam-logam tertentu sangat
berbahaya jika ditemukan dalam konsentrasi tinggi dalam lingkungan, karena logam tersebut mempuyai sifat merusak tubuh makhluk hidup. Disamping hal tersebut, beberapa logam sangat diperlukan dalam proses kehidupan makhluk hidup (Darmono,1995).
Logam berat dapat menimbulkan efek gangguan terhadap kesehatan manusia, tergantung pada bagian mana dari logam berat tersebut yang terikat dalam tubuh serta besarnya dosis paparan. Efek toksik dari logam berat mampu menghalangi kerja enzim sehingga mengganggu metabolisme tubuh, menyebabkan alergi, bersifat mutagen, tetratogen, atau karsinogen bagi manusia maupun hewan (Widowati, W. 2008).
2.3.2. Tembaga (Cu)
Tembaga adalah logam merah muda, yang lunak, dapat ditempa dan liat. Ia melebur pada suhu 10380C. Karena potensial elektroda standarnya positif, (+0,34 V untuk pasangan Cu/Cu2+), ia tak larut dalam asam klorida dan asam sulfat encer, meskipun dengan adanya oksigen ia dapat larut sedikit. Asam Nitrat yang sedang pekatnya (8M) dengan mudah melarutkan tembaga. (Widowati, 2008)
Tembaga yang tidak berikatan dengan protein merupakan zat racun. Mengkonsumsi sejumlah kecil tembaga yang tidak berikatan dengan protein dapat menyebabkan mual dan muntah.
Makanan atau minuman yang diasamkan, yang bersentuhan dengan pembuluh, selang atau katup tembaga dalam waktu yang lama, dapat tercemar oleh sejumlah kecil tembaga. Jika sejumlah besar garam tembaga, yang tidak terikat dalam protein, secara tidak sengaja tertelan atau jika pembebatan larutan garam tembaga digunakan untuk mengobati daerah kulit yang terbakar luas, sejumlah tembaga bisa terserap dan merusak ginjal, menghambat pembentuklan air kemih dan menyebabkan anemia karena pecahnya sel-sel darah merah (hemolisis). Keracunan tembaga dapat diobati dengan penisilamin yang dapat mengikat tembaga dan memudahkan pengeluaran/ pembuangannya.
Kekurangan tembaga jarang terjadi pada orang sehat. Ini sering terjadi pada bayi-bayi prematur atau bayi-bayi-bayi-bayi yang sedang dalam masa penyembuhan dari malnutrisi yang berat.Orang-orang yang menerima makanan secara intravena (parenteral) dalam waktu lama juga memiliki resiko menderita kekurangan tembaga. (http://indonesiaindonesia.com)
2.3.3. Efek Toksik Tembaga
Unsur Tembaga (Cu) bisa ditemukan pada berbagai jenis makanan, air dan udara sehingga manusia bisa terpapar Tembaga(Cu) melalui jalur makanan, minuman dan saat bernafas. Tembaga (Cu) merupakan unsur yang dibutuhkan dalam jumlah kecil. Apabila jumlah Tembaga (Cu) telah melampaui batas aman, akan muncul toksisitas. Manusia biasanya terpapar Tembaga (Cu) dari tanah, debu, makanan, serta minuman yang tercemar Tembaga(Cu) yang berasal dari pipa bocor pada penambangan Tembaga (Cu) atau industri yang menghasilkan limbah tembaga (Cu). Kira-kira 75%-99% total intake Tembaga (Cu) berasal dari makanan dan minuman. Setiap hari manusia bisa terpapar Tembaga (Cu) yang antara lain berasal dari peralatan dapur ataupun koin.
Keracunan logam berat bersifat kronis dan dampaknya baru terlihat setelah beberapa tahun. Logam berat bersifat akumulatif didalam tubuh organisme dan konsentrasi mengalami peningkatan (biomagnifikasi) dalam rantai makanan. Biomagnifikasi berhubungan langsung dengan manusi yang menempati posisi top level dalam rantai makanan karena konsentrasi logam berat yang dikandung dalam makanan manusia telah mengalami peningkatan mulai dari komponen tingkat dasar (produsen). Keracunan kronis Tembaga (Cu) dapat mengurangi umur, menimbulkan berbagai masalah reproduksi dan menurunkan fertilitas. (Widowati, 2008)
2.4. Adsorbsi
2.4.1. Pengertian Adsorbsi
Peristiwa penyerapan suatu zat pada permukaan zat lain disebut adsorbsi. Zat yang terserap disebut fase terserap sedangkan zat yang diserap disebut adsorben. Kecuali zat padat, adsorben dapat pula berupa zat cair. Karena itu adsorbsi dapat terjadi antara: zat padat dan zat cair, zat padat dan gas, zat cair dan zat cair, atau gas dan zat cair.
Proses adsorbsi ini disebabkan oleh gaya tarik molekul permukaan adsorben. Adsorbsi berbeda dengan absorbsi, karena pada absorbsi zat yang diserap masuk kedalam absorbens.
Berkat selektivitasnya yang tinggi, proses adsorbsi sangat sesuai untuk memisahkan bahan dengan konsentrasi yang kecil dari campuran yang mengandung bahan lain yang berkonsentrasi tinggi. Adsorbsi digunakan dalam pengolahan air buangan industri, terutama untuk mengurangi komponen-komponen organik misalnya warna, fenol, detergen, zat-zat toksik dan zat-zat organik yang sukar diuraikan
(non-biodeyadable). (Mc. Cabe dkk., 1999)
Kecepatan adsorbsi tidak hanya tergantung pada perbedaan konsentrasi dan pada luas permukaan adsorben, melainkan juga pada suhu, tekanan (untuk gas), ukuran partikel dan porositas adsorben. Juga tergantung pada ukuran molekul bahan yang akan diadsorbsi dan pada viskositas campur yang akan dipisahkan (cairan, gas). Pemilihan proses adsorbsi yang akan digunakan untuk pemisahan disesuaikan dengan kondisi agregasi campuran yang akan dipisahkan (padat, cair, gas), konsentrasi bahan yang akan dipisahkan, adsorben yang paling cocok, metode regenerasi yang diperlukan maupun pertimbangan ekonominya.
Proses adsorbsi meliputi tiga tahap mekanisme yaitu : - Pergerakan molekul adsorbat menuju permukaan adsorben
- Penarikan molekul-molekul adsorbat oleh permukaan aktif membentuk ikatan, yang berlangsung sangat cepat (Metcalf and Eddy, 1979).
2.4.2. Adsorben
Adsorben (untuk adsorbsi fisik) adalah bahan padat dengan luas permukaan dalam yang sangat besar. Permukaan yang luas ini terbentuk karena banyaknya pori yang halus pada padatan tersebut. Biasanya luasnya berada dalam orde 200 - 1000 m2/g adsorben. Diameter pori sebesar 0,0003 – 0,002 µm.
Disamping luas spesifik dan diameter pori, maka kerapatan unggun, distribusi ukuran partikel maupun kekerasannya merupakan data karakterisitik yang penting dari suatu adsorben. Tergantung pada tujuan penggunaannya, adsorben dapat berupa granulat (dengan ukuran butir sebesar beberapa mm) atau serbuk (khusus untuk adsorbsi campuran cair) (Mc.Cabe dkk.,1999)
2.5. Spektrofotometri Serapan Atom
2.5.1. Definisi Spektrofotometri Serapan Atom
Spektrofotometri Serapan Atom adalah suatu metode pengukuran kuantitatif suatu unsur yang terdapat dalam suatu cuplikan berdasarkan penyerapan cahaya pada panjang gelombang tertentu oleh atom-atom bentuk gas dalam keadaan dasar.
2.5.2. Prinsip dan Dasar Teori
Jika cahaya dengan panjang gelombang tertentu dilewatkan pada nyala yang mengandung atom-atom bersangkutan, maka sebagian cahaya itu akan diserap, dan jauhnya
penyerapan akan berbanding lurus dengan banyaknya atom dalam keadaan dasar yang berada dalam nyala. Hal ini merupakan dasar penentuan kuantitatif logam-logam dengan menggunakan SSA (Walsh,A., 1955).
2.5.3. Peralatan Spektrofotometri Serapan Atom (SSA)
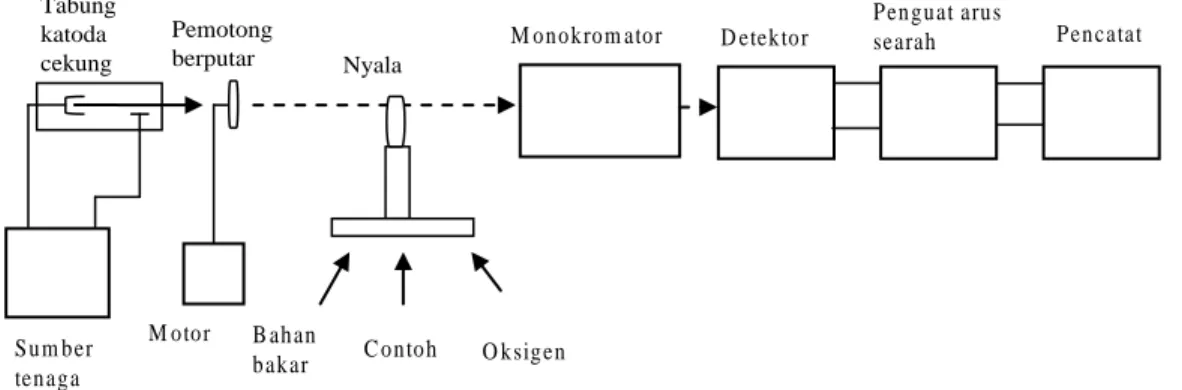
Komponen penting yang membentuk spektrofotometer serapan atom dapat diperlihatkan secara skematis pada gambar berikut:
Gambar 2.3. Komponen-komponen spektrofotometer serapan atom (Day, R.A.Jr.,Underwood A.L. 1988).
1. Sumber Tenaga
Suatu sumber radiasi yang digunakan harus memancarkan spektrum atom dari unsur yang ditentukan. Spektrum atom yang dipancarkan harus terdiri dari garis tajam yang mempunyai setengah lebar yang sama dengan garis serapan yang dibutuhkan oleh atom-atom dalam contoh. Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hallow chatode lamp) (Bassett dkk, 1994).
2. Nyala dan Sistem Pembakar- Pengabut
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Untuk spektroskopi nyala suatu
Tabung katoda cekung
Pemotong
berputar Nyala
M onokrom ator D etektor
Penguat arus
searah P encatat
Sum ber tenaga
B ahan
bakar C ontoh O ksigen
persyaratan yang penting adalah bahwa nyala yang dipakai hendaknya menghasilkan temperature lebih dari 2000oK. Untuk memenuhi persyaratan ini digunakan suatu gas pembakar bersama-sama dengan suatu gas pengoksidasi / oksidator, seperti udara ataupun gas dinitrogen oksida (N2O) (Haswell,S.J, 1991). Tujuan sistem pembakar – pengabut
adalah untuk mengubah larutan uji menjadi atom-atom dalam bentuk gas. Fungsi pengabut adalah menghasilkan kabut atau aerosol larutan uji. Larutan yang akan dikabutkan ditarik kedalam pipa kapiler oleh aksi semprotan udara yang ditiupkan melalui ujung kapiler, diperlukan aliran gas bertekanan tinggi untuk menghasilkan aerosol yang halus (Basset dkk, 1994).
3. Monokromator
Dalam spektroskopi serapan atom fungsi monokromator adalah untuk memisahkan garis resonansi dari semua garis yang tak diserap yang dipancarkan oleh sumber radiasi. ( Braun, R.D, 1982).
4. Detektor
Detektor pada spektrofotometer serapan atom berfungsi mengunggah intensitas radiasi yang datang menjadi arus listrik. Pada spektrofotometer serapan atom yang umum dipakai sebagai detektor adalah tabung penggandaan foton (PMT = Photo Multiplier Tube Detector). (Mulja, 1997).
5. Pencatat
Pencatat merupakan sistem pencatatan hasil. Hasil pembacaan dapat berupa angka atau berupa kurva dari suatu recorder yang menggambarkan absorbansi atau intensitas emisi (Braun, R.D, 1982).
2.5.4. Optimasi peralatan Spektrofotometri Serapan Atom
Pada peralatan optimasi Spektrofotometri Serapan Atom agar memberikan wacana dan sejauh mana sensitivitas dan batas deteksi alat terhadap sampel yang akan dianalisis, optimasi pada peralatan SSA meliputi:
• Pemilihan persen (%) pada transmisi • Lebar celah (slith width)
• Kedudukan lampu terhadap focus slit • Kemampuan arus lampu Hallow Cathode • Kedudukan panjang gelombang (λ)
• Set monokromator untuk memberikan sinyal maksimum • Pemilihan nyala udara tekanan asetilen
• Kedudukan burner agar memberikan absorbansi maksimum • Kedudukan atas kecepatan udara tekan
• Kedudukan atas kecepatan asetilen
2.5.5. Gangguan-gangguan pada Spektrofotometri Serapan Atom
Yang dimaksud dengan gangguan pada Spektrofotometri Serapan Atom adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel. Gangguan-gangguan yang terjadi adalah sebagai berikut:
1. Gangguan yang berasal dari sampel yang mana dapat mempengaruhi banyaknya sampel yang mencapai nyala. Hal tersebut dapat berpengaruh terhadap laju aliran bahan bakar / gas pengoksidasi. Sifat-sifat tersebut meliputi viskositas, tegangan permukaan, berat jenis, dan tekanan uap. Gangguan yang lain adalah pengendapan unsur yang dianalisis sehingga jumlah atom yang mencapai nyala menjadi lebih sedikit dari konsentrasi yang seharusnya terdapat dalam sampel.
2. Gangguan kimia yang dapat mempengaruhi jumlah / banyaknya atom yag terjadi didalam nyala. Meliputi disosiasi senyawa yang tidak sempurna dan ionisasi atom-atom dalam nyala. Disosiasi tidak sempurna disebabkan oleh terbentuknya senyawa yang bersifat refraktorik ( sukar diuraikan didalam nyala api ), misal oksida garam-garam fosfat, silikat, aluminat dari logam alkali tanah. Ionisasi ion dalam nyala dapat terjadi jika suhu yang digunakan untuk atomisasi tinggi. Jika suhu yang digunakan terlalu tinggi maka akan mengganggu pengukuran absorbansi karena spektrum atom tersebut mengalami ionisasi yang tidak sama dengan spektrum atom dalam keadaan netral.
3. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang dianalisis, yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi dalam nyala. Hal ini juga dapat terjadi karena suhu atomisasi terlalu tinggi, penambahan senyawa penyangga, dan pengektraksian unsur yang akan dianalisis
4. Gangguan oleh penyerapan non-atomik ( non atomic absorption )
Gangguan jenis ini berarti terjadinya penyerapan cahaya dari sumber sinar yang bukan berasal dari atom-atom yang akan dianalisis. Penyerapan tersebut terjadi karena penyerapan cahaya oleh partikel-partikel padat yang berada didalam nyala ( Rohman, 2007).