REAKTIFITAS BERBAGAI JENIS PELARUT
DARI RESIDU KILANG MINYAK PLAJU PADA
PENCAIRAN BATUBARA BANKO TENGAH
HartiniatiPusat Teknologi Pengembangan Sumberdaya Energi BPPT Gedung II lantai 22, Jl. MH Thamrin No. 8 10340
E-mail: hartiniati@bppt.go.id; hartiniati@yahoo.com
Abstract
An effect of two different residue for liquefaction of Central Banko coal is disccused. The residue was obtained from side-stream of refinery plant, which so-called long residue and short residue solvents. The liquefaction test was carried out under the reference conditions that have been developed in BPPT coal liquefaction laboratory, at temperature of 450oC and initial H2 pressure of
12MPa for 1 hour. The result shows that the distillate yield, Bottom (BTM) yield, and hydrogen consumption were dependent on the nature of solvent. Short residue solvent shown higher reactivity than the long residue. Reaction between Central Banko and Short Residue gave distillate yield higher than the long residue. Moreover, its BTM yield was also lower than that of long residue solvent. This result confirmed the lower hydrogen consumption for reaction short residue and Central Banko coal compared to that for reaction long residue and Central Banko. In this study, it also confirmed that the yield of H2O and CO+CO2 were
dependent on the material input condition. However, the yield of hydrocarbon gases (C1~C4) was mainly affected by de-alkylation in the solvent and coal during
the reaction
Kata kunci: residu minyak bumi, proses pencairan batubara, central Banko
1. PENDAHULUAN 1.1. Latar Belakang
Untuk meningkatkan efisiensi proses pencairan batubara pada skala komersial, salah satu alternatif yang dapat dilakukan adalah dengan memanfaatkan residu kilang minyak bumi.
Studi untuk pemanfaatan fraksi berat sebagai produk samping dari pengilangan minyak yang terutama merupakan jenis residu rantai panjang dan pendek, dimungkinkan, karena faktor keberadaan beberapa kilang minyak di Indonesia. Residu rantai panjang sendiri merupakan produk fraksi berat kolom distilasi atmosferik. Produk residu ini umumnya diumpankan ke kolom distilasi vakum dan menghasilkan turunannya berupa residu rantai pendek. Secara fisis, dibandingkan dengan residu rantai panjang, residu yang rantai pendek memiliki titik didih lebih tinggi. Hal tersebut mengindikasikan bahwa residu rantai pendek adalah fraksi yang lebih berat dari yang rantai panjang.
Fraksi berat minyak baik residu rantai panjang maupun rantai pendek mempunyai struktur kimia polisiklis dan struktur rantai panjang ataupun pendek alifatis yang relatif sangat sedikit. Konsentrasi hidrogen keduanya relatif lebih tinggi dibandingkan dengan pelarut berat (heavy oil) dan creosote oil yang diperoleh dari pirolisa batubara. Tingginya kandungan hidrogen dalam pelarut akan membantu proses pencairan batubara. Hal ini karena sangat besar kemungkinannya bahwa dalam proses depolimerisasi struktur batubara, pelarut tersebut dapat mensuplai molekular hydrogen (Shinn, et.al., 1984; Yamada, et.al., 1976; Yusnitati dan Artanto, 2000). Dengan pertimbangan demikian, pengkajian lebih lanjut terhadap pemanfaatan kedua jenis residu ini sebagai pelarut donor sangat dianjurkan.
1.2. Permasalahan
Sampai sejauh ini, produk samping kilang minyak baik residu rantai panjang maupun rantai pendek belum banyak dimanfaatkan di Indonesia untuk menghasilkan produk yang bernilai tinggi.
Seiringan dengan kondisi tersebut, belum diperolah perbandingan yang pasti antara keunggulan karakteristik dari keduanya memproduksi minyak sintetis.
1.3. Tujuan Riset
Tujuan dari riset ini adalah untuk mengetahui pelarut mana yang lebih menguntungkan. Reaktifitas pelarut kedua jenis residu sebagai pelarut organik akan diuji kemampuannya dalam proses pencairan batubara. Tingkat perolehan produk proses tersebut akan dibandingkan antara pelarut residu rantai panjang dan rantai pendek.
2. Bahan Baku
2.1. Batubara dan pelarut
Dalam riset ini digunakan lignit Banko Tengah (SB), diperoleh dari daerah Muara Enim, Sumatera Selatan, yang mula-mula digerus menggunakan ball mill sampai lolos saringan ukuran 200 mesh (75m). Setelah itu, untuk memperoleh hasil sampel yang representatif, dilakukan sampling. Batubara sampling kemudian disimpan di dalam botol dan ditempatkan di dalam desikator agar oksidasi dan kontak dengan uap air dari udara dapat dicegah.
Sekitar 50 gram sampel kemudian dianalisa ultimat dan proksimat. Sedangkan sampel lainnya disiapkan untuk pengujian pencairan dan pengujian lainnya.
Pelarut jenis residu rantai panjang dan rantai pendek keduanya diperoleh dari Pertamina UP III Plaju (dari crude distillation unit II dan vacuum
distillation unit II). Sampel disimpan di dalam
drum. Pelarut residu rantai panjang mempunyai titik didih sekitar 340oC dan relatif cair pada kondisi kamar. Sedangkan pelarut residu rantai pendek mempunyai rentang titik didih (TBP) >+520oC dan pour point sekitar 58oC.
Tabel 1. Analisa proksimat batubara Banko Tengah (SB), residu rantai panjang
Lg dan rantai pendek Sh
% bkta Abu %bk C H N S O SB 72,9 5,3 1,2 0,7 19,9 2,3 Lg 86,9 12,9 <0,01 0,1 0,1 0,01 Sh 86,4 13,3 <0,01 0,1 0.2 0,01
%bkta : % berat kering tanpa abu
Adapun sebelum dipergunakan dalam reaksi pencairan, kedua jenis residu tersebut sebagai bahan kaku harus didistilasi terlebih dulu untuk mengetahui komposisi fraksi distilat di dalamnya. Metode distilasi yang dipergunakan adalah ASTM-D1160.
Tabel 2. Komposisi fraksi hasil distilasi Lg dan Sh
(% berat) Fraksi distilasi H2O LO MO HO BTM* Lg 5,2 17,5 23,2 23,2 25,1 Sh 0,0 0,5 0,5 5,9 93,0 2.2. Umpan gas
Dalam reaksi pencairan, dipergunakan gas hidrogen dan gas nitrogen. Penggunaan gas hidrogen adalah sebagai gas reaktan dalam reaksi. Sementara itu, gas nitrogen diperlukan untuk membersihkan ruangan udara di dalam
autoclave dan menurunkan konsentrasi oksigen
di dalam udara. Hal tersebut perlu dilakukan agar konsentrasi oksigen yang ada di dalam autoclave tidak menyebabkan ledakan jika terjadi kontak dengan gas hidrogen.
Seluruh gas dialirkan langsung dari tanki gas yang tekanannya dijaga agar tetap pada 150MPa (suplai gas dibantu oleh kompresor gas hidrogen yang mengalirkan gas dari tabung silinder ke tanki gas). Aliran gas dikontrol dengan pengatup otomatis.
2.3. Katalis
Dalam studi ini, dipergunakan katalis limonit yang diambil dari daerah Soroako, Sulawesi Selatan. Katalis tersebut dipersiapkan dalam bentuk pasta (slurry), yaitu dengan melarutkan katalis menggunakan pelarut heavy oil solvent
(td.300-420oC) yang didapat dari unit pencairan batubara
skala BSU (Bench Scale Unit) yang terdapat di TCLC (Takasago Coal Liquefaction Centre), Jepang. Rasio pelarut dengan katalis dibuat 70:30. Apabila slurry telah terbentuk, katalis dan pelarut digiling di dalam tower mill selama 4 jam dengan kecepatan putraran 1000 rpm untuk membantu pendispersian bijih katalis ke dalam pelarut. Ukuran katalis yang diperoleh bisa mencapai 0,5m.
Katalis dianalisa dengan AAS (Atomic
Adsorbtion Spectroscopy) untuk mengukur konsentrasi Fe di dalam padatan. Adapun komponen logam yang terdapat di dalam katalis adalah sebagai berikut:
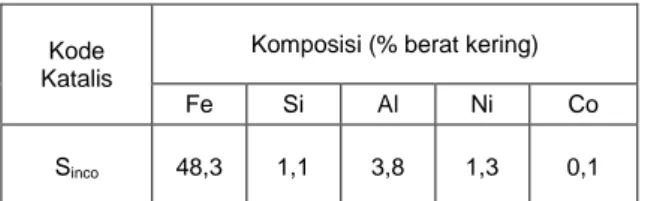
Tabel 3. Hasil analisa komposisi logam di dalam katalis limonit Soroako*
* konsentrasi katalis padat di dalam pelarut : 25,58% Kode
Katalis
Komposisi (% berat kering)
Fe Si Al Ni Co
Menurut analisa XRD, Fe di dalam katalis limonit sebagian besar berupa -FeOOH. Dalam reaksi pencairan batubara, konsentrasi nikel (Ni) dan Co (kobalt) sebagaimana tertera pada tabel di atas tidak signifikan untuk meningkatkan kecepatan reaksi (Artanto, 2002).
Tabel 4. Fraksi distilat dari pelarut minyak berat
Berdasarkan informasi yang diberikan pada Tabel 5, terutama mengenai kandungan hidrogen, mengindikasikan bahwa pelarut heavy
oil tidak bersifat donor hidrogen dibandingkan
dengan pelarut residu rantai pendek (lihat juga Tabel 1). Oleh karena itu, pengaruh jenis residu ini terhadap perolehan minyak atau distilat dapat dikatakan lebih dominan.
Tabel 5. Analisa ultimat dari pelarut minyak berat
Pelarut minyak berat yang digunakan sebagai campuran katalis dalam reaksi pencairan, selama reaksi mengalami degradasi sangat kecil untuk membentuk fraksi-fraksi produk minyak atau distilat.
2.4. Eksperimen reaksi pencairan
Sampel batubara dari dalam desikator ditimbang sebanyak 80 gram, kemudian dimasukkan ke dalam autoclave. Selanjutnya pelarut masing-masing residu rantai panjang maupun rantai pendek, dengan berat dua kali berat batubara (rasio pelarut/BT 2:1 dengan basis bkta) dimasukkan ke dalam autoclave. Setelah itu katalis larutan limonit (1% berat BT-bkta dengan basis Fe) yang sudah ditambah dengan sulfur (rasio atom sulfur/Fe 3:1) dimasukkan juga ke dalam autoclave.
Autoclave lalu ditutup dan dilakukan tes
untuk mendeteksi ada tidaknya kebocoran gas, mengingat reaksi berlangsung pada suhu dan tekanan tinggi. Oleh karena itu, sebelumnya konsentrasi oksigen di dalam autoclave dikurangi dengan mengalirkan dan mengeluarkan gas nitrogen pada tekanan 3MPa sebanyak tiga kali. Kemudian tes deteksi dilakukan menggunakan gas hidrogen yang tekanannya dijaga pada 25MPa selama kurang lebih 4 jam untuk melihat apakah terjadi kebocoran atau tidak (dideteksi dengan alat monitor gas hidrogen). Jika tidak terjadi kebocoran, maka tekanan tersebut
diturunkan hingga tekanan awal yang sudah ditetapkan. Di dalam studi ini, tekanan awal hidrogen yang digunakan adalah 12 MPa.
Setelah itu, pemanas autoclave dioperasikan. Suhu reaksi yang diinginkan di dalam studi ini adalah 450oC (Yusnitati, 2003). Adapun kecepatan pemanasan autoclave 1 liter dari suhu kamar ke 450oC adalah 123oC/jam. Setelah tercapai suhu 450oC, waktu reaksi mulai dihitung selama 1 jam.
Setelah reaksi selesai, pengaduk dibiarkan berputar dan segera alirkan udara melalui blower udara ke pemanas autoclave. Bersamaan dengan proses tersebut, pemanas autoclave dimatikan. Kecepatan pendinginan autoclave adalah 150o/jam. Apabila suhu cairan telah menjadi 100oC, maka pengaduk dan blower udara dimatikan. Pengambilan produk dapat dilakukan ketika suhu cairan mencapai 50oC.
2.5. Analisa produk (gas dan cairan)
Pengambilan gas baru dilakukan bila suhu cairan produk mencapai suhu 50oC. Agar konsentrasi gas di dalam autoclave menjadi homogen, sebelum pengambilan gas dilakukan, pengaduk dibiarkan menyala.
Aliran gas yang keluar dari autoclave dilewatkan meter gas (mengukur volume gas produk di dalam autoclave). Pengambilan gas dilakukan pada tiga tekanan yang berbeda dan kemudian konsentrasi gas dihitung rata-rata dari tiga tekanan berbeda tersebut di atas.
Untuk menganalisa konsentrasi gas, digunakan gas kromatografi. Konsentrasi gas hidrokarbon (C1-C4) dideteksi dengan
menggunakan GC-FID (gas
chromatography-Flame Ionized Detector). Sedangankan komposisi gas CO, CO2, H2 dan CH4 dianalisa
memakai GC-TCD (gas chromatography-Thermal
Conductivity Detector). Konsentrasi gas H2S
diukur dengan menggunakan alat dragger, alat ini berupa tabung kecil yang berisi zeolit penyerap gas H2S.
Setelah pengambilan sampel gas selesai, produk cair diambil dari autoclave. Produk cair tersebut kemudian dipisahkan fraksi-fraksinya dengan alat distilasi vakum 10 mmHg. Metode distilasi yang dipergunakan merujuk pada ASTM-D1160.
Produk distilasi dibagi dalam tiga bagian titik didih. Titik didih dari suhu kamar sampai 180oC adalah minyak ringan (light oil, LO). Fraksi titik didih 180-420oC dinamakan minyak resirkulasi atau daur ulang (recycle solvent, RS) dan fraksi titik didih >420oC dinamakan residu (coal liquid
bottom, CLB).
Analisa ultimat (% bkta)
C H S N Odiff.
88,4 8,5 1,0 0,1 2,0
Fraksi distilasi (% berat)
H2O LO MO HO BTM
3. HASIL DAN DISKUSI
3.1. Perbandingan Perolehan Distilat dan
Bottom Residue (BTM) dan Konsumsi
Hidrogen antara Residu Rantai Panjang dan Pendek
Perbandingan perolehan produk dan konsumsi gas hidrogen dalam reaksi pencairan batubara dengan pelarut jenis rantai panjang dan rantai pendek ditampilkan di dalam Tabel 6 berikut.
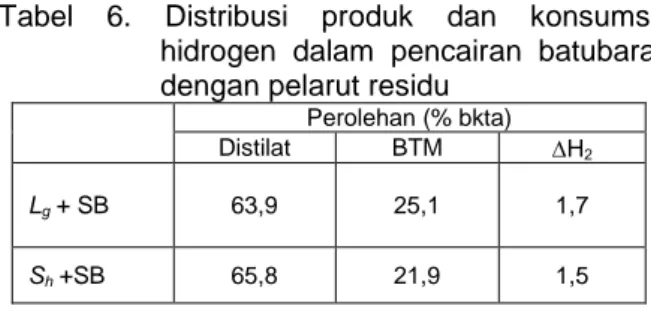
Pada Tabel 6 terlihat dimana distilat yang dihasilkan dari reaksi antara batubara dengan pelarut residu rantai pendek relatif lebih besar dibandingkan dengan pelarut residu rantai panjang (65,8% vs 63,9%). Untuk menjelaskan bagaimana hasil sedemikian dapat tercapai adalah kompleks, mengingat residu rantai panjang mempunyai fraksi ringan LO, fraksi menengah MO dan fraksi berat HO relatif lebih besar dibanding rantai pendek sementara fraksi BTM-nya relatif lebih kecil. Adapun perbedaan konsentrasi hidrogen antara residu rantai panjang dan rantai pendek tidak berbeda besar, dimana yang rantainya panjang lebih rendah hanya sekitar 0,4% konsentrasi hidrogennya dibandingkan dengan residu rantai pendek. Tabel 6. Distribusi produk dan konsumsi
hidrogen dalam pencairan batubara dengan pelarut residu
Perolehan (% bkta)
Distilat BTM H2
Lg + SB 63,9 25,1 1,7
Sh +SB 65,8 21,9 1,5
Diperkirakan bahwa yang menyebabkan distilat hasil reaksi pencairan (Sh +SB) lebih besar
dibandingkan dengan (Lg + SB) adalah karena
sebagian besar dari fraksi BTM yang terdegradasi di dalam fraksi residu rantai pendek membentuk fragmen-fragmen bebas yang berfungsi sebagai donor hidrogen dan pencegah reaksi re-polimerisasi. Fragmen-fragmen ini sangat membantu dalam memfraktur struktur batubara baik struktur mikro maupun makro sehingga fraksi-fraksi distilat seperti fraksi ringan LO, fraksi menengah MO dan fraksi berat HO menjadi semakin banyak dan stabil. Keberadaan bantuan donor hidrogen sedemikian dapat dikonfirmasi dari relatif kecilnya konsumsi gas hidrogen dalam reaksi (Sh +SB) yaitu 0,2% lebih rendah dibanding reaksi (Lg + SB). Kondisi ini
memperlihatkan bahwa semakin reaktif suatu pelarut, konsumsi gas hidrogen yang disuplai dari aliran gas atau fase gas semakin berkurang.
Perolehan berbagai jenis fraksi di dalam distilat juga mengindikasikan perbedaan antara reaksi (Sh +SB) dan (Lg+SB). Di dalam Tabel 7
tertera bahwa dibandingkan dengan hasil reaksi (Sh +SB), perolehan LO dan MO hasil reaksi (Lg
+ SB). relatif lebih rendah. Hal ini menunjukkan bahwa mekanisme reaksi yang diawali dengan degradasi fraksi BTM di dalam pelarut, serta hasil degradasi tersebut, yakni fragmen-fragmen bebas, memicu perengkahan ikatan di dalam struktur batubara mikro dan makro yang kemudian membentuk fraksi-fraksi LO, MO dan HO. Adapun fraksi LO, MO dan HO yang sudah ada di dalam pelarut hanya mengalami sedikit perengkahan. Keberadaan fraksi-fraksi ini berfungsi untuk membantu molekul hidrogen bebas mencegah reaksi kondensasi (re-polimerisasi).
Tabel 7. Distribusi fraksi-fraksi di dalam distilat
Perolehan (% bkta)
LO MO HO
Lg + SB 17,5 23,2 23,2
Sh +SB
24,6 25,9 15,3
Perolehan HO untuk reaksi (Lg + SB) di atas menunjukkan jumlah yang sama dengan jumlah fraksi di dalam pelarut LR sebelum reaksi. Hasil ini mengkonfirmasi penjelasan sebelumnya bahwa fraksi HO di dalam pelarut residu rantai panjang diperkirakan tidak mengalami degradasi membentuk fraksi yang lebih ringan dan akibatnya cenderung untuk membantu dalam stabilisasi gugus radikal bebas dari struktur batubara yang terengkah. Sementara itu, pelarut residu rantai pendek, terlepas dari hasil yang diberikan, memiliki peranan yang serupa dengan pelarut residu rantai panjang.
Perbedaan reaktifitas pelarut dari kedua jenis residu juga ditunjukkan oleh perolehan BTM. Perolehan BTM dari reaksi (Lg + SB) relatif lebih
besar 3,2% dibandingkan dengan perolehan BTM dari reaksi (Sh+SB). Ini merupakan
konfirmasi lebih lanjut bahwa untuk reaksi pencairan batubara banko Tengah reaktivitas residu rantai pendek lebih baik dibandingkan dengan residu rantai panjang. Reaktivitas pelarut tersebut diperkirakan dipengaruhi oleh jumlah fraksi BTM di dalam pelarut. Semakin besar jumlah fraksi BTM maka kemungkinan terbentuknya fragmen-fragmen bebas yang berfungsi sebagai donor hidrogen semakin meningkat. Akibatnya, kemampuan struktur ikatan mikro dan makro batubara untuk merengkah menjadi lebih besar.
3.2. Perbandingan Perolehan H2O, CO+CO2 dan C1~C4 antara Residu Rantai Panjang dan Rantai Pendek
Distribusi produk H2O, CO+CO2 dan C1~C4
dalam reaksi pencairan batubara dengan pelarut residu rantai panjang dan residu rantai pendek ditabulasikan dalam Tabel 8 di bawah ini.
Tabel 8 menunjukkan bahwa perbedaan perolehan H2O antara reaksi dengan pelarut
residu rantai panjang dan rantai pendek tidak terlalu besar. Perbedaan tersebut disebabkan oleh kandungan air pelarut residu rantai panjang relatif besar dibandingkan dengan pelarut residu rantai pendek (lihat Tabel 2). Hal ini dimungkinkan karena produk H2O di dalam reaksi
pencairan batubara lebih banyak dipengaruhi oleh kandungan air di dalam material umpan.
Perolehan CO+CO2 untuk kedua system
reaksi juga tak mempunyai perbedaan. Seperti tertulis di dalam Tabel 1, kandungan oksigen kedua pelarut sangat rendah dan relatif sama. Perolehan CO+CO2 lebih banyak dipengaruhi
oleh kandungan oksigen material umpan, sebagaimana perolehan H2O.
Tabel 8. Distribusi produk H2O, CO+CO2 dan
C1~C4 dalam pencairan batubara
dengan pelarut residu (Lg dan Sh ) Perolehan (% bkta)
H2O CO+CO2 C1~C4
Lg + SB 5,2 3,2 4,3
Sh +SB 4,5 3,6 5,7
Gas hidrokarbon yang diproduksi dari reaksi batubara Banko Tengah dan residu rantai panjang (Lg + SB) lebih rendah dibandingkan dengan reaksi batubara Banko Tengah dengan residun rantai pendek (Sh+SB). Beberapa
kemungkinan yang mengakibatkan hasil penelitian sedemikian dapat dijelaskan secara teknis sebagai berikut.
Dibandingkan dengan residu rantai panjang, gugus alkil (rantai panjang) di dalam struktur residu rantai pendek lebih besar. Gugus alkil di dalam residu rantai pendek lebih banyak terikat dengan struktur polisiklis dan relatif lebih mudah terlepas membentuk gas hidrokarbon.
Fragmen-fragmen radikal bebas dari struktur pelarut residu rantai pendek sangat membantu pelepasan ikatan gugus alkil di dalam batubara. Akibatnya, lebih banyak gas hidrokarbon yang terbentuk bila dibandingkan reaksi batubara dengan pelarut residu rantai panjang.
Kontribusi gugus alkil yang terbentuk dari dua mekanisme di atas menghasilkan total gas hidrokarbon.
4. KESIMPULAN
Berdasarkan studi ini dapat disimpulkan bahwa pelarut residu rantai panjang dan rantai pendek yang diperoleh dari unit kilang minyak bumi Pertamina UP III Plaju, ternyata terbukti secara signifikan dapat dipergunakan sebagai pelarut dalam reaksi pencairan batubara Banko Tengah. Keduanya berpotensi menjadi pelarut alternatif karena menghasilkan perolehan distilat yang relatif tinggi serta berhasil menekan pembentukan perolehan residu pencairan batubara (bottom residue, BTM).
Pelarut residu rantai pendek ditemukan lebih reaktif dibandingkan dengan pelarut residu rantai panjang. Ini karena pelarut residu rantai pendek ini mempunyai kandungan hidrogen dan BTM yang relatif tinggi yang mengakibatkan kemampuannya menjadi donor hidrogen menjadi lebih besar. Akibatnya, kebutuhan molekul hidrogen berkurang karena telah disokong oleh pelarut residu rantai pendek. Fragmentasi struktur pelarut residu rantai pendek ini dalam membentuk gugus radikal bebas juga memiliki peran besar dalam degradasi struktur mikro dan makro batubara.
Daftar Pustaka
Artanto, Y., 2002. Pengaruh Penambahan Nickel Ferrite Terhadap Aktivitas Katalis Limonit Pada Proses Pencairan Lignit, Prosiding Seminar Nasional Kimia. UNDIP.
Artanto, Y., 1996. Conversion of Indonesian
Banko Coal into Oil: The Influence of Temperature on the Hydrogenation of Banko Coal, Intern Technical Report, June 15,
Agency for the Assessment and Application of Technology
Artanto, Y., Jackson, W.R., Redlich, P.J. and Marshall, M., 2000. Liquefaction of Some
Indonesian Low-rank Coals, Fuel, vol.79, hal
1333-1340
Shinn, J.H., Dahlberg, A.J., Kuehler, C.W. and Rosenthal, J.W.,”The Chevron Co-Refining
Process”, Proceedings of the Ninth Annual EPRI Contractors’ Conference on Coal
Liquefaction, Palo Alto, California, May 1984. Yamada, Y., Honda, H. and Kakiyama, H., 1976.
Liquefaction of Coal with Petroleum System Heavy Oil Solvent, Japanese Patent 53502,