SINTESIS HIDROKSIAPATIT BERPORI DARI CANGKANG KEONG
SAWAH (Bellamya javanica) DENGAN PENAMBAHAN PATI
SINGKONG SEBAGAI POROGEN
ALDHI ATHAWI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2013
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Sintesis Hidroksiapatit dari Cangkang Keong Sawah (Bellamya javanica) dengan Penambahan Pati Singkong sebagai Porogen adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Oktober 2013 Aldhi Athawi NIM G44090016
ABSTRAK
ALDHI ATHAWI. Sintesis Hidroksiapatit Berpori dari Cangkang Keong Sawah (Bellamya javanica) dengan Penambahan Pati Singkong sebagai Porogen. Dibimbing oleh CHARLENA dan TETTY KEMALA.
Hidroksiapatit (HAp) disintesis dengan cara mencampurkan Ca(OH)2 dan
(NH4)2·HPO4 serta tambahan pati singkong sebagai porogen. Metode yang
digunakan adalah metode basah (presipitasi) yaitu mereaksikan Ca(OH)2 yang
berasal dari cangkang keong sawah dengan (NH4)2·HPO4 teknis. Pencirian dengan
difraksi sinar X menunjukkan bahwa perlakuan sonikasi 2, 4, dan 6 jam menghasilkan kemurnian HAp yang beragam. HAp dengan waktu sonikasi 6 jam memiliki kemurnian tertinggi sehingga digunakan untuk sintesis HAp berpori. HAp berpori dibentuk dengan menambahkan pati singkong sebagai porogen dengan konsentrasi 20 dan 30%. Pati menghilang saat proses kalsinasi dan membentuk pori pada HAp. Pengamatan di bawah mikroskop payaran elektron Identifikasi SEM menunjukkan HAp dengan tambahan porogen pati singkong 30% memiliki pori yang lebih besar yaitu 13.2-46.79 µm. Analisis spektrum inframerah transformasi fourier menunjukkan HAp berporogen pati singkong 30% memiliki pita gugus fungsi yang berbeda dengan pita gugus fungsi dari HAp tanpa porogen. Pertumbuhan kristal apatit pada uji in vitro menunjukkan HAp berporogen bersifat bioaktif.
Kata kunci: cangkang keong sawah, hidroksiapatit, pati singkong.
ABSTRACT
ALDHI ATHAWI. Synthesis of Pored Hydroxyapatite from Snail’s Shell (Bellamya javanica) with Added Cassava Starch as Porogen. Supervised by CHARLENA and TETTY KEMALA.
Hydroxyapatite (HAp) was synthesized by mixing Ca(OH)2 with
(NH4)2·HPO4 and adding cassava starch as porogen. The method used was wet
method (presipitation), by reactioning Ca(OH)2 from snail’s shell with technical
(NH4)2·HPO4. Characterizing using X-ray diffractogram (XRD) showed that the
sonication treatment of 2, 4, and 6 hours produced various Hap purities. HAp with sonication time of 6 hours gave the highest in purity level, so it was used for synthezing the pored HAp. Pored HAp was formed by adding cassava starch as porogen with concentration at 20 and 30%. Cassava starch was lost in calcination process and it created the pores in HAp. Characterization by XRD showed that the samples formed HAp but still contained some wastes. Identification by scanning electron microscope described the porogened Hap by 30% cassava starch had larger pore, between 13.2 and 46.79 µm. Analisis of infrared spectrum on porogened HAp by 30% cassava starch showed band that the functional groups had patterns. The growth of apatite crystal in in vitro test showed bioactivity of the porogenated HAp.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
SINTESIS HIDROKSIAPATIT BERPORI DARI CANGKANG KEONG
SAWAH (Bellamya javanica) DENGAN PENAMBAHAN PATI
SINGKONG SEBAGAI POROGEN
ALDHI ATHAWI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2013
Judul Skripsi : Sintesis Hidroksiapatit Berpori dari Cangkang Keong Sawah (Bellamya javanica) dengan Penambahan Pati Singkong sebagai Porogen
Nama : Aldhi Athawi
NIM : G44090016
Disetujui oleh
Dr Charlena, MSi Pembimbing I
Dr Tetty Kemala, MSi Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas rahmat dan karunia-Nya, sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2013 sampai Agustus 2013 ini adalah hidroksiapatit, dengan judul Sintesis Hidroksiapatit Berpori dari Cangkang Keong Sawah (Bellamya javanica) dengan Penambahan Pati Singkong sebagai Porogen.
Terima kasih penulis ucapkan kepada Ibu Dr Charlena, MSi dan Ibu Dr Tetty Kemala, MSi selaku pembimbing. Di samping itu, perhargaan penulis sampaikan kepada Bapak Syawal, Bapak Caca, Bapak Mulyadi, dan Bapak Wawan yang telah membantu penulis dalam pemakaian alat dan bahan di Laboratorium Kimia Anorganik dan Laboratorium Bersama Departemen Kimia FMIPA IPB. Ungkapan terima kasih juga disampaikan kepada ayah dan ibu tercinta, serta seluruh keluarga, atas doa dan kasih sayangnya. Ucapan terima kasih kepada Agung, Desy, Muga, Trias dan teman-teman seperjuangan black and white chemist 46 serta teman-teman terdekat Adil, Azis, Habibie, Arman, Novita, Sahri, Yeni, Dedi, Mahdan, Putra, dan Rinaldy yang telah memberikan semangat, motivasi, dan rasa peduli kebersamaan.
Semoga karya ilmiah ini bermanfaat.
Bogor, Oktober 2013
DAFTAR ISI
DAFTAR GAMBAR vi DAFTAR LAMPIRAN vi PENDAHULUAN 1 METODE PENELITIAN 2 Bahan 2 Alat 2 Tahapan Penelitian 2HASIL DAN PEMBAHASAN 5
Preparasi Cangkang Keong sawah 5
Sintesis dan Pencirian Hidroksiapatit 7
Sintesis dan Pencirian Hidroksiapatit Berporogen 9
Morfologi Hidroksiapatit 10
Identifikasi Hidroksiapatit dengan FTIR 12
Uji In Vitro 13
SIMPULAN DAN SARAN 14
Simpulan 14 Saran 15 DAFTAR PUSTAKA 15 LAMPIRAN 17 RIWAYAT HIDUP 31
DAFTAR GAMBAR
1 Difraktogram sinar-X cangkang keong sawah sebelum kalsinasi 6 2 Difraktogram sinar-X cangkang keong sawah setelah kalsinasi 7 3 Difraktogram sinar-X HAp tanpa porogen dengan variasi waktu
sonikasi 8
4 Difraktogram sinar-X HAp dengan penambahan porogen pati singkong 10
5 Morfologi HAp tanpa porogen 11
6 Morfologi HAp berporogen pati singkong 11
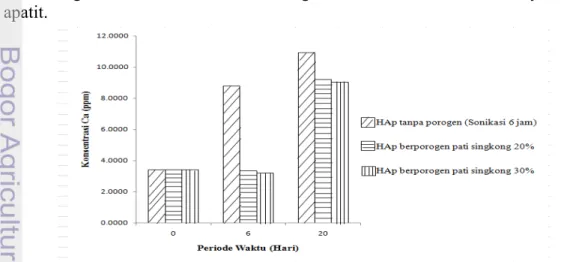
7 Perbandingan spektogram inframerah HAp 12 8 Konsentrasi kalsium larutan SBF terhadap periode waktu perendaman 13
DAFTAR LAMPIRAN
1 Bagan alir penelitian 17
2 Data perhitungan konsentrasi kalsium cangkang keong sawah 18
3 Data pencirian XRD 19
4 Data komposisi bahan yang digunakan untuk menghasilkan HAp 24 5 Data JCPDS (Joint Commitee on Powder Diffraction Standards) 25 6 Contoh perhitungan ukuran pori hasil foto SEM 28 7 Perhitungan ukuran kristal dan parameter kisi 29
8 Data perhitungan konsentrasi kalsium hasil analisis uji in vitro 30
PENDAHULUAN
Hidroksiapatit merupakan senyawa mineral apatit dengan rumus Ca10(PO4)6(OH)2 yang memiliki kesamaan komposisi kimia dengan jaringan
tulang asli. Kesamaan karakter HAp dengan jaringan tulang mendorong beberapa peneliti untuk mengembangkannya sebagai material dalam implantasi biomedis untuk jaringan tulang. Syarat medis yang harus dipenuhi oleh senyawa mineral yang akan diimplankan ke tulang adalah bioaktif, biokompatibel, dan tidak beracun (Dahlan et al. 2009). Menurut Maachou et al. (2008) HAp memiliki sifat bioaktif, biokompatibel, dapat berikatan kuat dengan tulang, membentuk lapisan pada permukaan jaringan tulang, dan mempercepat pembentukan tulang pada permukaan yang diimplantasi.
Bahan dasar yang digunakan untuk mensintesis HAp pada penelitian ini adalah cangkang keong sawah (B. javanica) yang didapatkan di daerah pulau Jawa. Cangkang keong sawah merupakan limbah dari konsumsi daging keong sawah dan saat ini belum memiliki pemanfaatan komersial yang signifikan. Menurut Baby et al. (2010) cangkang keong sawah (B. bengalensis) yang berasal dari daerah Asia Selatan mengandung kalsium (24%), fosfor (57.4%), besi (10.25%), natrium (6.86%), dan kalium (1.39%). Kalsium yang terkandung dalam cangkang moluska umumnya berupa kalsium karbonat (CaCO3) yang tergabung
dalam struktur cangkang sebagai kristal kalsit dan aragonit (Soido et al. 2009). Keberadaan kalsium ini mendorong penggunaan cangkang keong sawah sebagai bahan dasar dalam pembentukan HAp.
Media pertumbuhan jaringan tulang terjadi pada pori-pori HAp. Jaringan sel tulang baru akan tumbuh dalam pori-pori, sehingga dapat meningkatkan regenerasi tulang dengan baik (Pane 2004). HAp berpori memiliki banyak kegunaan dalam aplikasi biomedis, yaitu untuk regenerasi jaringan tulang, sebagai bahan pengisi untuk cacat tulang dan augmentasi, dan materi graft tulang buatan, serta melapisi logam pen (Dahlan et al. 2009).
Pembentukan HAp berpori dapat dilakukan menggunakan bahan porogen yang akan menghilang selama proses kalsinasi. Bahan-bahan yang dapat digunakan antara lain: parafin, naftalena, pati atau beberapa polimer seperti poli(asam laktat), gelatin, alginat, dan kitosan (Sopyan et al. 2007). Porogen yang digunakan pada penelitian ini berasal dari pati singkong. Pati tersusun dari dua macam karbohidrat yaitu amilosa dan amilopektin dalam komposisi yang berbeda-beda. Amilosa merupakan pati dengan struktur tidak bercabang dan memberikan sifat keras sedangkan amilopektin merupakan pati dengan struktur bercabang dan menyebabkan sifat lengket. Pemilihan pati singkong sebagai porogen karena memiliki sifat biodegradabel, biokompatibel, dapat larut dalam air, dan harganya murah (Sadjadi et al. 2010). Al-Sokanee et al (2009) telah berhasil menggunakan pati sebagai porogen dengan menggunakan HAp yang berasal dari tulang sapi untuk pembuatan pori steger pada aplikasi biomedis.
Penelitian mengenai HAp berpori juga telah dilakukan Hidayat (2012) menggunakan tulang ikan alu-alu dengan porogen pati singkong. Akan tetapi, pori yang dihasilkan masih terlalu kecil, yaitu sekitar 2.38 – 3.28 µm. Ukuran tersebut nyatanya dapat menghambat pertumbuhan jaringan tulang pada tubuh karena pori minimum yang dibutuhkan untuk pertumbuhan pada jaringan tulang sekitar 100 –
2
150 µm pada makropori (Sopyan et al. 2007). Namun, osteokonduksi masih bisa terjadi pada pori yang lebih kecil, yaitu 50 µm (Chang et al. 2000).
Beberapa metode pembentukan HAp pernah dilakukan seperti metode kering dan basah (Muntamah 2011) serta metode sol gel (Romawarni 2011). Metode yang digunakan ialah metode basah yaitu mereaksikan larutan cair menjadi padatan. Metode ini dipilih karena memiliki kelebihan, seperti produk HAp yang dihasilkan relatif lebih banyak dan pelarut yang digunakan tidak terlalu mahal. Hasil samping berupa air memungkinkan kontaminasi zat-zat lain selama proses pengerjaan sangat rendah. Selain itu, reaksi ini merupakan reaksi sederhana, murah, dan tidak menimbulkan polusi lingkungan dan memiliki kemurnian yang tinggi (Kehoe 2008).
Penelitian ini bertujuan mensintesis hidroksiapatit berpori dari cangkang keong sawah dengan variasi sonikasi 2, 4, dan 6 jam serta penambahan konsentrasi pati singkong 20 dan 30% sebagai porogen sehingga didapatkan HAp dengan morfologi yang diharapkan. Hasil penggunaan cangkang keong sawah sebagai bahan dasar biomaterial HAp diharapkan dapat memberi manfaat tambahan untuk bidang biomedis.
METODE PENELITIAN
Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah cangkang keong sawah (B. javanica), pati singkong komersil, HCl 37%, HNO3 pekat, (NH4)2HPO4,
larutan SBF (Simulated Body Fluid), air bebas ion, dan akuades.
Alat
Alat-alat yang digunakan adalah peralatan kaca, plat penangas, pengaduk, mortar, indikator pH universal, sonikator 8893 Lok-Parmer, sentrifugasi Hermle Labnet Z206A, oven Memmert Wisconsia, oven Sanyo MOV-212, tanur Nabertherm, spektroskopi serapan atom (SSA) Shimadzu AA-7000, difraksi sinar-X (sinar-XRD) Maxima Shimadzu 7000, mikroskop elektron payaran (SEM) ZEISS, spektroskopi infra merah transformasi fourier (FTIR) One Merk Perkin Elmer.
Tahapan Penelitian
Sintesis HAp pada penelitian ini dilakukan dengan metode basah (presipitasi). Penelitian ini terdiri dari enam tahapan. Tahap pertama melakukan preparasi, karakterisasi, dan uji kadar abu cangkang keong sawah.. Tahap kedua dilanjtukan dengan kalsinasi, hidrasi, dan uji kadar kalsium cangkang. Tahap ketiga adalah pembuatan suspensi Ca(OH)2, larutan (NH4)2.HPO4, dan larutan pati
3 adalah sintesis HAp berporogen. Tahap keenam pencirian dengan XRD, SEM, FTIR dan uji in vitro menggunakan larutan SBF (Lampiran 1).
Preparasi, Pencirian, dan Uji Kadar Abu Cangkang Keong Sawah
Preparasi awal dilakukan dengan membilas keong sawah dengan air bersih. Keong sawah direbus selama 60 menit, kemudian daging keong dipisahkan dari cangkang. Cangkang dipanaskan dibawah sinar matahari sampai kering. Cangkang digiling hingga menjadi serbuk dengan ukuran 100 mesh. Serbuk cangkang dicirikan dengan menggunakan XRD. Pencirian dengan XRD dilakukan untuk mengidentifikasi fase CaCO3 yang terkandung dalam cangkang
keong sawah yang digunakan. Uji kadar abu dilakukan dengan memanaskan sebanyak dua gram serbuk cangkang didalam tanur pada suhu 700 °C selama enam jam. Kemudian serbuk didinginkan dan ditimbang.
Kalsinasi, Hidrasi, dan Uji Kadar Kalsium
Kalsinasi serbuk cangkang dilakukan dengan modifikasi metode Soido et al. (2009). Serbuk cangkang dimasukkan ke dalam cawan porselen yang sebelumnya sudah dibilas dengan HNO3 pekat kemudian dikalsinasi didalam tanur pada suhu
1000 °C selama dua jam. Kalsinasi dilakukan untuk mengubah fase CaCO3
menjadi fase CaO.
Hasil kalsinasi berupa serbuk CaO kemudian dibiarkan kontak dengan udara (yang mengandung uap air) selama satu minggu pada suhu ruang laboratorium anorganik departemen kimia IPB. Selanjutnya, dilakukan pencirian XRD untuk memastikan bahwa serbuk yang terbentuk adalah serbuk Ca(OH)2. Serbuk CaO
dapat ditransformasi menjadi Ca(OH)2 melalui suatu reaksi eksotermik dengan air.
Uji kadar kalsium dilakukan untuk mengetahui besarnya kalsium yang terkandung didalam cangkang. Uji kadar kalsium ditentukan dengan menggunakan SSA. Sebanyak 0.1 g sampel serbuk cangkang hasil kalsinasi 1000 ºC dilarutkan dengan 5 mL HCl 37% lalu dimasukkan ke dalam labu takar 100 mL dan ditera dengan air bebas ion. Sebanyak 1 mL larutan sampel dimasukkan ke dalam labu takar 100 mL dan ditera dengan air bebas ion. Blanko dibuat dari 5 mL HCl 37% yang ditera dengan air bebas ion di dalam labu takar 100 mL. Sebanyak 1 mL larutan blanko dimasukkan ke dalam labu takar 100 mL dan ditera dengan air bebas ion. Panjang gelombang (λ) yang digunakan adalah 422.7 nm.
Pembuatan Suspensi Ca(OH)2, Larutan (NH4)2.HPO4, dan Larutan Pati
Suspensi Ca(OH)2 0.5 M dibuat dengan cara ditimbang sebanyak 18.5 g
serbuk Ca(OH)2 dan ditambahkan dengan 500 mL air bebas ion. Larutan
(NH4)2.HPO4 0.3 M dibuat dengan cara ditimbang sebanyak 19.7 g serbuk
(NH4)2.HPO4 dan dilarutkan dengan 500 mL air bebas ion, diaduk hingga
4
dan 30 gram pati singkong dilarutkan masing-masing dengan 100 mL air bebas ion dan diaduk homogen.
Sintesis Hidroksiapatit (Santos et al. 2004)
Sebanyak 500 mL larutan (NH4)2.HPO4 0.3 M di dalam buret diteteskan
dengan kecepatan 6 mL/menit ke dalam gelas piala berisi 500 mL suspensi Ca(OH)2 0.5 M pada suhu 40±2 °C sambil diaduk konstan, pH dimonitor namun
tidak dikoreksi. Campuran yang terbentuk didiamkan selama 1 malam dan dihomogenkan dengan menggunakan sonikator dengan variasi waktu yaitu 2, 4, dan 6 jam. Kemudian diendapkan dengan sentrifuse dua kali dengan kecepatan 4500 rpm selama 15 menit. Endapan yang diperoleh dicuci dengan air bebas ion. Endapan yang diperoleh lalu dikeringkan dalam oven suhu 105 °C selama 3 jam, dimasukkan ke dalam tanur suhu 900 °C selama 2 jam. Sampel digerus hingga berbentuk serbuk halus dan dimasukkan ke dalam eksikator. Proses selanjutnya dilakukan pencirian dengan XRD. Waktu sonikasi yang menghasilkan HAp paling sedikit pengotor digunakan selanjutnya untuk sintesis hidroksiapatit berporogen. HAp terbaik atau HAp dengan sedikit pengotor diidentifikasi dengan SEM dan FTIR.
Sintesis Hidroksiapatit Berporogen
Sebanyak 200 mL larutan (NH4)2.HPO4 0,3 M di dalam buret diteteskan
dengan kecepatan 6 mL/menit ke dalam gelas piala berisi 200 mL suspensi Ca(OH)2 0.5 M pada suhu 40±2 °C sambil diaduk konstan, pH dimonitor namun
tidak dikoreksi. Campuran dipisahkan menjadi dua bagian. Campuran 1 ditambahkan 40 mL larutan pati 20% dan campuran 2 ditambahkan 60 mL larutan pati 30%, diaduk homogen dan didiamkan selama 1 malam pada suhu ruang. Setelah itu, dihomogenkan dengan menggunakan sonikator selama 6 jam dan diendapkan dengan sentrifuse dua kali dengan kecepatan 4500 rpm selama 15 menit. Endapan yang diperoleh dicuci dengan air bebas ion. Endapan yang diperoleh lalu dikeringkan dalam oven suhu 105 °C selama 3 jam, dimasukkan ke dalam tanur suhu 900 °C selama 2 jam. Sampel digerus hingga berbentuk serbuk halus dan dimasukkan ke dalam eksikator. Proses selanjutnya dilakukan pencirian dengan SEM untuk mengetahui ukuran pori yang terbentuk. HAp yang memiliki pori lebih besar dicirikan dengan XRD dan FTIR.
Analisis XRD, SEM, dan FTIR, serta Uji In vitro dengan Larutan SBF
Analisis difraksi sinar-X (XRD) dilakukan untuk melihat fasa yang terbentuk pada sampel HAp. Sampel yang sudah kering digerus dengan menggunakan lumpang sampai halus. Setelah itu, sampel dimasukkan ke dalam kompartemen. Kompartemen berisi sampel dikaitkan pada diffraktometer. Selanjutnya, pada komputer dilakukan pengatur nama sampel, sudut awal, sudut akhir, dan kecepatan analisis. Sudut awal pada 10º dan sudut akhir pada 80º
5 dengan kecepatan baca 0.60 detik, panjang gelombang 1.54060 Å , dan sebagai target adalah tembaga (Cu). Sampel hasil sintesis ditempatkan pada suatu spesimen kompartemen kemudian diletakkan pada difraktometer. Analisis ini dilakukan untuk mengetahui fasa yang terkandung di dalam sampel.
Morfologi dan pori dari HAp dikarakterisasi dengan menggunakan SEM. Sampel diletakkan pada plat alumunium kemudian dilapisi dengan pelapis emas setebal 48 nm. Proses selanjutnya, sampel yang telah dilapisi emas diamati menggunakan SEM dengan tegangan 20 kV. Sedangkan penentuan sampel dengan FTIR bertujuan untuk mengetahui gugus fungsi yang terbentuk dalam HAp. Satu miligram sampel dicampur dengan 100 mg KBr dan kemudian dibuat pelet. Pelet dianalisis dengan sinar infra merah dengan jangkauan bilangan gelombang 4000-400 cm-1.
Uji in vitro dengan larutan SBF digunakan untuk mengetahui sifat bioaktif HAp terhadap tubuh. Pengujian secara in vitro dilakukan dengan metode Sharma et al. (2009). Larutan SBF dibuat dengan mencampurkan bahan-bahan berikut ini : NaCl 99.5%, NaHCO3 99.5%, KCl 99.0%, Na2HPO4·2H2O 99.5%,
MgCl2·6H2O 98%, CaCl2·2H2O 99%, Na2SO4, (CH2OH)3CNH2 99.2%, dan HCl
1M. Sebanyak 2 g sampel dibuat pelet kemudian dimasukkan pada larutan SBF 100 mL. Proses perendaman dilakukan dengan rentang waktu yang telah ditentukan, yaitu selama 6 dan 20 hari. Hasil perendaman larutan SBF diambil 20 mL kemudian dilakukan penyaringan larutan dengan kertas saring Whatman No 40. Pencirian dilakukan dengan menggunakan SSA.
HASIL DAN PEMBAHASAN
Preparasi Cangkang Keong sawah
Keong sawah (marga Bellamya) termasuk dalam kelompok Operculata yang hidup di perairan dangkal berdasar lumpur dengan aliran air yang lamban dan ditumbuhi rerumputan air, misalnya sawah, rawa, pinggir danau, dan pinggir sungai kecil. Umumnya, keong sawah memiliki tinggi cangkang hingga 4 cm dengan diameter 15–25 mm dan bentuknya seperti kerucut, membulat dengan warna hijau kecoklatan atau kuning kehijauan. Cangkang keong sawah pada penelitian ini dibeli dari Pasar Anyar Bogor. Cangkang keong sawah pada digunakan sebagai sumber kalsium untuk sintesis HAp. Kalsium diperoleh dari hasil kalsinasi dan hidrasi CaCO3 yang terkandung dalam cangkang. Kandungan
kalsium yang diperoleh dari cangkang keong sawah setelah proses kalsinasi dan hidrasi adalah sebesar 88.54% (b/v) (Lampiran 2). Kadar kalsium yang dikandung cangkang keong sawah ini masih lebih tinggi daripada cangkang kerang (Trianita 2012) sebesar 44.39% dan cangkang telur (Prihantoko 2011) sebesar 40.48%.
Proses kalsinasi bertujuan mengubah kalsium karbonat menjadi kalsium oksida. Menurut Bahrololoom et al. (2009) kalsium karbonat yang telah dikalsinasi selama dua jam pada suhu 1000 ⁰C akan berubah menjadi kalsium oksida. Proses hidrasi melibatkan senyawa CaO dengan uap air (H2O). Senyawa
6
CaO yang terbentuk dibiarkan kontak dengan uap air pada suhu ruang selama satu minggu. Adapun reaksi yang terjadi sebagai berikut:
CaCO3(s) CaO(s) + CO2(g) (proses kalsinasi)
2CaO(s) + 2H2O(g) 2Ca(OH)2(s) (ΔHr = −63.7 kJ/mol CaO) (proses hidrasi)
Kandungan CaCO3 cangkang keong sawah dapat diidentifikasi dengan
pencirian XRD. Hasil pencirian XRD cangkang keong sawah sebelum kalsinasi dapat dilihat pada Gambar 1.
Gambar 1 Difraktogram sinar-X cangkang keong sawah sebelum kalsinasi 1000 ºC selama dua jam
Selain fasa kalsium karbonat (CaCO3), di dalam cangkang keong sawah
sebelum kalsinasi juga terdapat fasa kalsium fosfat [Ca3(PO4)2]. Fasa CaCO3 yang
terbentuk begitu dominan menempati seluruh puncak dengan intensitas rendah maupun tinggi yang ditunjukkan oleh puncak sudut 2θ sebesar 26.25⁰, 33.16⁰, 45.18⁰, dan 52.49⁰ (Lampiran 3). Hal ini tidak lepas dari pendapat Soido et al.( 2009) yang menyebutkan bahwa kalsium yang terkandung dalam cangkang moluska umumnya berupa kalsium karbonat yang tergabung dalam struktur cangkang sebagai kristal kalsit dan aragonit. Keberadaan fasa Ca3(PO4)2
ditunjukkan pada sudut 2θ sebesar 42.94⁰. Fasa Ca3(PO4)2 terbentuk diduga
karena adanya kandungan fosfor dalam cangkang keong sawah yang terikat dalam bentuk trikalsium fosfat. Cangkang keong sawah yang belum diberi perlakuan kalsinasi masih mengandung beberapa mineral. Menurut Baby et al. (2010) cangkang keong sawah (Bellamya bengalensis) mengandung kalsium (24%), fosfor (57.4%), besi (10.25%), natrium (6.86%), dan kalium (1.39%).
Keberadaan kalsium karbonat adalah salah satu indikator yang menunjukkan bahwa cangkang keong sawah dapat digunakan sebagai bahan dasar HAp. Namun CaCO3 harus diubah terlebih dahulu ke bentuk CaO dengan proses kalsinasi
kemudian dilanjutkan dengan proses hidrasi sehingga menghasilkan Ca(OH)2.
Jika keberadaan ion karbonat tidak dihilangkan maka dapat mengganggu proses pembentukan kristal HAp (Dahlan et al. 2009). Gambar 2 merupakan hasil pencirian XRD cangkang keong sawah setelah kalsinasi 1000 ºC selama dua jam dan hidrasi satu minggu.
7
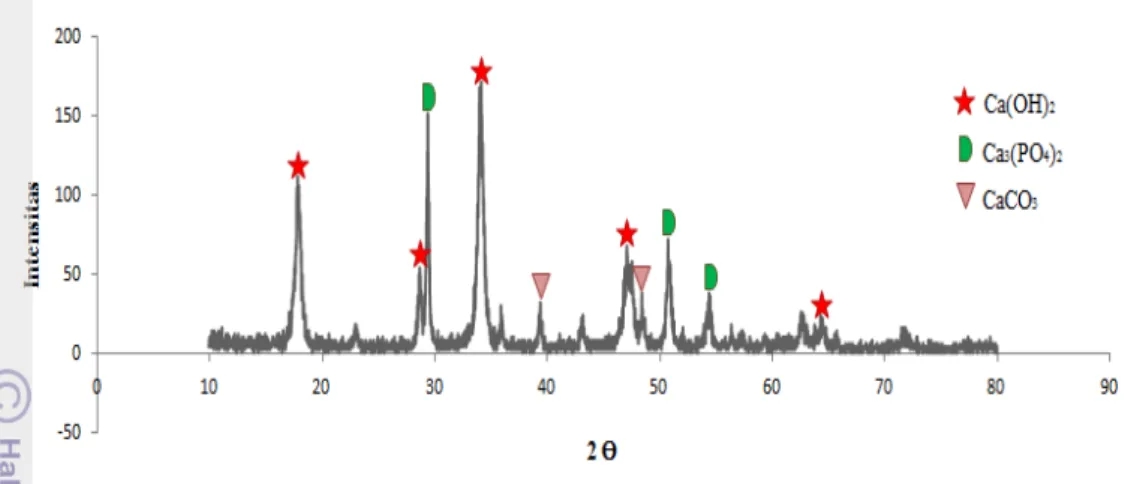
Gambar 2 Difraktogram sinar-X cangkang keong sawah setelah kalsinasi 1000 ⁰C selama dua jam dan hidrasi satu minggu
Cangkang keong sawah yang sudah dikalsinasi dan dihidrasi mengandung fasa Ca(OH)2, Ca3(PO4)2, dan CaCO3. Fasa yang diharapkan terbentuk adalah fasa
Ca(OH)2 sedangkan fasa Ca3(PO4)2 dan CaCO3 dianggap sebagai fasa pengotor.
Keberadaan Ca(OH)2 ditunjukkan pada puncak tertinggi sudut 2θ sebesar 17.9⁰
dan 34.1⁰ (Lampiran 3). Fasa Ca(OH)2 terbentuk dari senyawa CaO yang
merupakan hasil kalsinasi CaCO3, dan kemudian bereaksi dengan uap air (H2O)
pada proses hidrasi. Pencirian XRD menunjukkan fasa Ca3(PO4)2 memiliki
puncak yang cukup tinggi yaitu pada sudut 2θ sebesar 29.36⁰. Keberadaan fasa [Ca3(PO4)2] muncul karena sebelumnya sudah terbentuk pada cangkang sebelum
kalsinasi, kemudian setelah dipanaskan terjadi peningkatan densitas fasa. Hal ini sesuai dengan pendapat German (1984) yang mengatakan suhu berpengaruh terhadap perubahan densitas yaitu semakin tinggi suhu maka menyebabkan pengurangan besar volume yang berakibat meningkatnya densitas. Sedangkan fasa CaCO3 terbentuk diduga karena adanya proses karbonasi oleh CO2 terhadap
Ca(OH)2. Fasa CaCO3 berada pada sudut 2θ sebesar 48.40⁰.
Sintesis dan Pencirian Hidroksiapatit
Sintesis hidroksiapatit [Ca10(PO4)6(OH)2] membutuhkan sumber kalsium
dan fosfor. Sebelumnya sudah disebutkan sumber kalsium yang digunakan pada penelitian ini berasal dari Ca(OH)2 hasil kalsinasi dan hidrasi cangkang keong
sawah. Sumber fosfor yang digunakan bersal dari larutan (NH4)2·HPO4. Jumlah
komposisi Ca(OH)2 dan (NH4)2·HPO4 ditentukan berdasarkan hasil perhitungan
stokiometri sehingga menghasilkan rasio konsentrasi Ca/P sebesar 1.67 (Lampiran 4). Adapun reaksi pembentukan HAp yang terjadi pada penelitian ini sebagai berikut:
10Ca(OH)2(susp) + 6(NH4)2.HPO4(aq) Ca10(PO4)6(OH)2(s) + 6H2O(aq)+ 12NH4OH(aq) Metode yang digunakan untuk mensintesis hidroksiapatit adalah metode presipitasi (basah) yaitu mereaksikan cairan (dari larutan menjadi padatan). Kelebihan metode ini adalah mudah mengontrol komposisi dan karakteristik fisik dari hidroksiapatit, murah, dan mudah penggunaannya (Pankaew et al. 2010).
8
Sedangkan kelemahan metode ini ialah sulit mengatur nilai pH diatas 9 untuk mencegah pembentukan kalsium hidroksiapatit yang tidak sempurna sehingga dapat membentuk trikalsium fosfat saat proses sintering (Balamurugan et al. 2006).
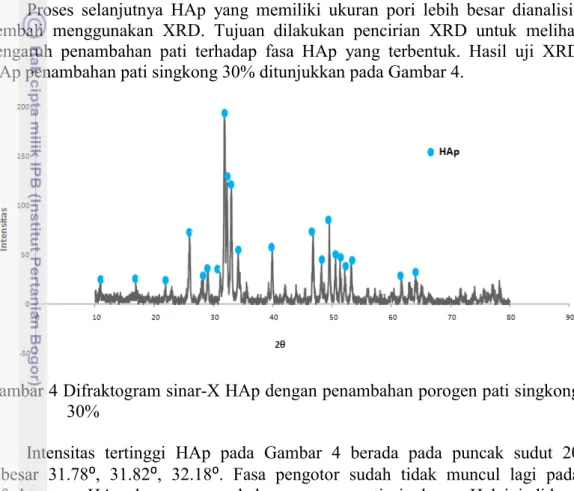
Sintesis HAp yang dilakukan pada penelitian ini adalah sintesis HAp tanpa porogen serta sintesis HAp dengan penambahan porogen pati singkong. Sintesis HAp tanpa porogen dilakukan dengan variasi waktu sonikasi 2, 4, dan 6 jam. Gambar 3 merupakan hasil pencirian XRD sintesis HAp tanpa penambahan porogen dengan waktu sonikasi 2, 4, dan 6 jam.
(a)
(b)
(c)
Gambar 3 Difraktogram sinar- X HAp tanpa porogen waktu sonikasi (a) 2 jam (b) 4 jam (c) 6 jam
Gambar 3(a) merupakan hasil pencirian XRD sintesis HAp tanpa porogen dengan waktu sonikasi 2 jam. Fasa yang muncul yaitu HAp, apatit tipe-A (AKA) [Ca10(PO4)6CO3], apatit tipe-B (AKB) [Ca10(PO4)3(CO3)3(OH)2 ], CaCO3, dan
9 Ca(OH)2. Fasa yang diharapkan terbentuk adalah fasa HAp. Fasa HAp sonikasi 2
jam memiliki puncak tertinggi pada sudut 2θ sebesar 31.84°. Keberadaan beberapa pengotor seperti AKA dan AKB diduga diakibatkan oleh CaCO3 yang
sebelumnya sudah ada pada cangkang keong hasil kalsinasi dan hidrasi, sehingga mengganggu proses pembentukan kristal apatit. Ion karbonat dapat menempati dua posisi pada struktur hidroksiapatit, yaitu pada posisi pertama menggantikan OH¯ membentuk apatit karbonat tipe A Ca10(PO4)6CO3 (AKA) pada suhu tinggi
dan posisi kedua menggantikan PO43- membentuk apatit karbonat tipe B
Ca10(PO4)3(CO3)3(OH)2 (AKB) pada suhu rendah (Aoki 1991). Fasa Ca(OH)2
muncul akibat kurang bereaksi sempurna dengan larutan amonium hidrogen fosfat. Fasa yang terbentuk pada HAp tanpa porogen dengan waktu sonikasi 4 jam ditunjukkan oleh Gambar 3(b). Hasil pencirian XRD memunculkan pengotor yang lebih sedikit daripada HAp sonikasi 2 jam, namun masih terdapat AKA dan AKB dengan intensitas dan puncak yang berbeda. Keberadaan AKA dan AKB tersebut tidak mengganggu fungsi dari HAp karena senyawa paduan Ca/P yang telah mengalami pemanasan di atas 900 ⁰C memiliki struktur yang stabil dan tidak berbahaya jika dimplankan ke dalam tubuh makhluk hidup (Aoki 1991). Intensitas tertinggi HAp dengan waktu sonikasi 4 jam berada pada puncak sudut 2θ sebesar 31.76°, 32.14°, dan 33.88°.
Hasil pencirian XRD HAp tanpa porogen dengan waktu sonikasi 6 jam pada Gambar 3(c) menunjukkan fasa yang terbentuk dominan HAp. Fasa yang terbentuk dibandingkan dengan data JCPDS (Joint Commitee on Powder Diffraction Standards) (Lampiran 5). Fasa HAp terlihat pada puncak sudut intensitas tinggi maupun rendah. Intensitas tertinggi HAp ditunjukkan oleh puncak sudut 2θ sebesar 31.72º, 31.80º, dan 32.96º. FasA pengotor tidak terdeteksi lagi keberadaannya oleh XRD. Hal ini diduga karena pengaruh perlakuan waktu sonikasi yang lebih lama. Tujuan sonikasi adalah untuk homogenisasi antara senyawa kalsium dan senyawa fosfat serta menghomogenisasikan antara senyawa kalsium fosfat yang telah terbentuk dengan porogen pati. Hal ini menunjukkan semakin lama waktu sonikasi maka proses reaksi antara Ca(OH)2 dan (NH4)2·HPO4 semakin homogen dan sempurna. Selain
itu, kemampuan sonikasi dalam menghomogenkan senyawa memudahkan proses penghilangan pengotor saat kalsinasi.
Berdasarkan tiga variasi sonikasi yaitu 2, 4, dan 6 jam, HAp yang memilki kemurnian paling tinggi ditunjukkan oleh HAp sonikasi 6 jam karena lebih sedikit fasa pengotor. Secara umum dari ketiga perlakuan tersebut telah terbentuk HAp. Berdasarkan hasil pencirian difraksi sinar-X menunjukkan semakin lama waktu sonikasi, HAp yang dihasilkan semakin murni. Tingkat kemurnian inilah yang mendorong dilakukannya penggunaan HAp waktu sonikasi 6 jam untuk perlakuan sintesis hidroksiapatit berpori.
Sintesis dan Pencirian Hidroksiapatit Berporogen
Hidroksiapatit berpori adalah komponen anorganik yang utama terdapat pada tulang dan merupakan salah satu kandidat terbaik untuk memperbaiki tulang dan meregenerasinya karena sifat bioaktif dan osteokonduktivitasnya. Oleh karena itu, untuk lebih meningkatkan fungsi HAp dalam mempercepat pertumbuhan
10
jaringan tulang ditambahkan dengan larutan pati singkong. Pati merupakan salah satu bahan yang dapat memperbesar pori pada HAp yang akan menghilang selama proses kalsinasi (Sopyan et al. 2007). Pati yang ditambahkan pada HAp dilakukan dengan variasi konsentrasi 20 dan 30%. Penambahan pati ke dalam Ca(OH)2 dilakukan terlebih dahulu sebelum proses pencampuran dengan
(NH4)2·HPO4. Hasil dari kedua penambahan variasi konsentrasi pati ini,
selanjutnya dikarakterisasi dengan menggunakan SEM untuk melihat ukuran pori yang terbentuk.
Proses selanjutnya HAp yang memiliki ukuran pori lebih besar dianalisis kembali menggunakan XRD. Tujuan dilakukan pencirian XRD untuk melihat pengaruh penambahan pati terhadap fasa HAp yang terbentuk. Hasil uji XRD HAp penambahan pati singkong 30% ditunjukkan pada Gambar 4.
Gambar 4 Difraktogram sinar-X HAp dengan penambahan porogen pati singkong 30%
Intensitas tertinggi HAp pada Gambar 4 berada pada puncak sudut 2θ sebesar 31.78⁰, 31.82⁰, 32.18⁰. Fasa pengotor sudah tidak muncul lagi pada difraktogram HAp dengan penambahan porogen pati singkong. Hal ini diduga karena adanya interaksi antara pati dengan senyawa-senyawa organik, sehingga pati dan senyawa-senyawa lainnya bersamaan menghilang saat proses kalsinasi. Dengan penambahan porogen, selain dapat memperbesar pori juga dapat memurnikan HAp yang terbentuk.
Morfologi Hidroksiapatit
Karakterisasi SEM dilakukan untuk mengetahui morfologi hidroksiapatit dengan atau tanpa adanya porogen pati. Karakterisasi fisik dari HAp berpori yang meliputi ukuran pori, morfologi pori, dan keseragaman pori akan mempengaruhi pertumbuhan tulang ke dalam implan (Sopyan et al. 2007). Morfologi pori yang diidentifikasi pada penelitian ini adalah hidroksiapatit tanpa porogen dengan perlakuan waktu sonikasi 6 jam dan HAp dengan penambahan porogen pati singkong dengan konsentrasi masing-masing 20 dan 30%.
11 Gambar 5 merupakan bentuk partikel HAp tanpa penambahan porogen pati singkong dengan perbesaran 1230×. Morfologi permukaan HAp tanpa penambahan pati singkong menunjukkan telah terbentuknya pori dengan ukuran antara 0.09-0.40µ. Morfologi HAp terdiri dari granula-granula yang membentuk suatu agregat dengan ukuran yang tidak merata.
Gambar 5 Morfologi HAp tanpa porogen dengan waktu sonikasi 6 jam pada perbesaran 1230×
Morfologi HAp dengan penambahan pati singkong 20 dan 30% dapat ditunjukkan pada gambar 6. Morfologi HAp dengan penambahan pati singkong 20% memiliki bentuk pertikel seperti granula-granula dengan permukaan kasar serta terbentuknya pori yang cukup banyak dengan ukuran pori yang bervariasi yaitu sekitar 4.54 – 19.69 µm dan HAp dengan penambahan pati 30% menghasilkan ukuran pori sebesar 13.2 - 46.79 µm. Pori HAp yang terbentuk pada penelitian ini sudah lebih besar daripada pori yang dihasilkan oleh Romawarni (2011) sebesar 1 µm dan Hidayat (2012) sebesar 2.38 – 3.28 µm.
Gambar 6 Morfologi HAp berporogen pati singkong (a) 20% perbesaran 1170× (b) 30% perbesaran 1300×
Berdasarkan hasil perhitungan ukuran pori (Lampiran 6) menunjukkan ukuran pori HAp dengan penambahan porogen pati singkong 30% lebih besar daripada HAp dengan penambahan porogen pati singkong 20% dan HAp tanpa porogen. Hal ini disebabkan adanya kandungan amilopektin pati yang berperan penting dalam memperbesar granula. Menurut Murphy (2000) ukuran granula pati
12
singkong adalah sekitar 4-35 µm. Besarnya ukuran granula pati menyebabkan ukuran pori yang dibentuk juga semakin besar. Selain itu, konsentrasi pati yang besar menyebabkan adanya akumulasi pati yang besar yang terjebak dalam HAp, sehingga pada saat proses kalsinasi menghasilkan jejak pori yang besar. Pori terbentuk karena porogen pati terjebak diantara partikel-partikel HAp. Pati akan menghilang pada saat proses pemanasan suhu tinggi dan terlepas dari partikel HAp sehingga meninggalkan jejak berupa pori (Trianita 2012).
HAp yang dihasilkan dalam penelitian ini belum dapat diaplikasikan secara implan ke dalam tubuh karena pori yang terbentuk masih sangat kecil dan ukuran tidak seragam. Pori minimum yang dibutuhkan untuk pertumbuhan pada jaringan tulang sekitar 100–150 µm pada makropori (Sopyan et al. 2007). Namun, HAp ini masih bisa diaplikasikan untuk osteokonduksi. Menurut Chang et al. (2000) osteokonduksi bisa terjadi pada pori yang lebih kecil, yaitu 50 µm.
Struktur kristal HAp dapat ditentukan dengan menghitung parameter kisi kristal yang terbentuk. Struktur kristal HAp adalah heksagonal dengan parameter kisi a=b≠c. Nilai parameter kisi a dan c untuk HAp berturut-turut adalah 9.418 Å dan 6.884 Å sesuai dengan JCPDS (Lampiran 5). Pada penelitian ini, HAp tanpa porogen dan HAp berporogen pati singkong 30% memiliki parameter kisi yang mirip dengan HAp standar JCPDS. HAp tanpa porogen (sonikasi 6 jam) memiliki parameter kisi a = 9.413 Å dan c = 6.883 Å, sedangkan HAp berporogen pati singkong 30% memilki a = 9.487 Å dan c = 6.927 Å. Hal ini menunujukkan bahwa HAp yang telah disintesis berbentuk heksagonal.
Identifikasi Hidroksiapatit dengan FTIR
Spektroskopi inframerah Fourier Transform Infrared (FTIR) dapat mengidentifikasi kandungan gugus kompleks dalam senyawa HAp, tetapi tidak dapat digunakan untuk menentukan unsur-unsur penyusunnya. Spektroskopi inframerah memanfaatkan energi vibrasi gugus penyusun senyawa HAp, yaitu gugus PO43-, gugus CO32-, dan gugus OH-.
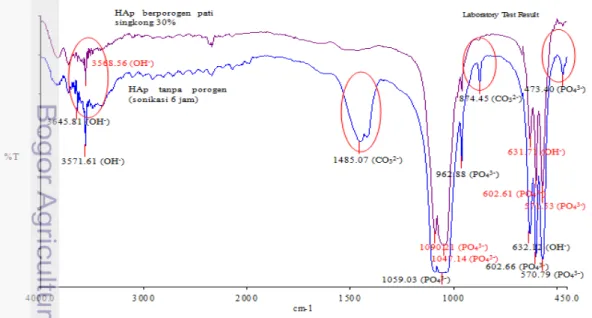
Gambar 7 Perbandingan spektogram inframerah HAp murni dengan HAp-pati singkong 30%
13 Spektrum FTIR antara HAp tanpa porogen dengan HAp berporogen pati singkong 30% terdapat beberapa perbedaan puncak pita serapan. Pada HAp tanpa porogen menghasilkan pita serapan OH- yang lebih banyak yaitu pada pita serapan 3645.81 cm-1, 3571.61 cm-1, dan 632.12 cm-1, sedangkan pita serapan OH -pada HAp berporogen berada -pada bilangan gelombang 3568.56 cm-1 dan 631.71 cm-1. Pita serapan 3645.81 cm-1 menunjukkan adanya air yang terikat dengan HAp. Keberadaan air ini dapat dihilangkan dengan pemanasan diatas 200 ⁰C (Soejoko dan Wahyuni 2002). Keberadaan OH- menunjukkan bahwa HAp yang disintesis mengandung gugus penyusun HAp. Namun proses menghilangnya air pada HAp berporogen disebabkan oleh adanya ikatan antara ikatan α-(1,4) amilosa pati dengan air. Amilosa memiliki sifat fisik mudah larut dalam air sehingga pada saat pemanasan terjadi penghilangan pati dan air.
Pita serapan karbonat CO32- pada HAp tanpa porogen dapat diamati pada
bilangan gelombang 1545 cm-1, 1450 cm-1, dan 890 cm-1, sedangkan pada HAp berporogen ion karbonat tidak terdeteksi. Keberadaan CO32- pada HAp tanpa
porogen diduga karena saat proses pencampuran antara kalsium dan fosfat terdapat CO2 dari udara yang masuk dan bereaksi dengan CaO membentuk ion
karbonat. Adanya kemapuan ion karbonat dalam menggantikan posisi PO43- pada
HAp, menyebabkan terjadinya pergeseran puncak serapan ion fosfat ke daerah bilangan gelombang 473.40 cm-1 seperti yang ditunjukkan pada spektrum HAp tanpa porogen, namun munya ikatan gugus fosfat dengan intensitas yang paling tinggi terdapat pada bilangan gelombang 1000-1100 cm-1. Artinya, pergantian posisi PO43- dengan ion karbonat menyebabkan penurunan intensitas serapan
fosfat.
Uji In Vitro
Sifat bioaktif adalah sifat yang dimiliki HAp karena kemampuannya bereaksi dengan jaringan dan menghasilkan ikatan kimia yang baik. Untuk menentukan kemampuan bioaktif HAp di dalam tubuh dilakukan uji in vitro dengan menggunakan larutan SBF. Larutan simulated body fluid (SBF) merupakan larutan yang mengandung ion-ion yang komposisinya kurang lebih sama dengan cairan tubuh. Cairan ini digunakan untuk media tumbuhnya kristal apatit.
14
Perendaman sampel HAp dilakukan selama 6 dan 20 hari. Gambar 8 menunjukkan konsentrasi kalsium dalam larutan SBF awal sebesar 3.4267 ppm. Pada periode waktu 6 hari telah terjadi peningkatan jumlah kalsium pada HAp tanpa porogen yaitu sebesar 8.7844 ppm, sedangkan kalsium pada HAp berporogen pati singkong 20 dan 30% terjadi penurunan konsentrasi menjadi sebesar 3.3467 dan 3.1978 ppm (Lampiran 7). Kenaikan jumlah kalsium pada larutan SBF pada HAp tanpa porogen terjadi karena adanya pertukaran ion antara permukaan sampel dan larutan akibat perbedaan potensial kimia sehingga terjadi pelepasan ion Ca2+ dari sampel ke larutan SBF yang mengakibatkan kandungan Ca2+ dalam larutan SBF meningkat. Pada penelitian ini, HAp tanpa porogen memiliki komposisi HAp yang lebih besar sehingga kalsium yang terkandung juga lebih banyak dibandingkan dengan HAp berporogen. Oleh karena itu, peningkatan kalsium larutan SBF pada HAp tanpa porogen lebih tinggi daripada HAp berporogen. Penurunan kalsium pada HAp berporogen diduga karena potensial kimia yang dimiliki oleh larutan SBF lebih besar daripada sampel HAp sehingga terjadi pelepasan ion Ca2+ dari larutan SBF ke sampel HAp yang mengakibatkan kandungan Ca2+ dalam SBF mengalami penurunan.
Perubahan konsentrasi kalsium HAp terjadi setelah perendaman 20 hari. Kalsium HAp tanpa porogen mengalami kenaikan menjadi 10.9378 ppm. Sedangkan HAp berporogen pati singkong 20 dan 30% yang sebelumnya mengalami penurunan konsentrasi kalsium, setelah perendaman 20 hari terjadi kenaikan konsentrasi kalsium yaitu sebesar 9.1933 dan 9.0467 ppm. Proses kenaikan ini disebabkan karena kalsium yang dikeluarkan terus menerus oleh sampel HAp mengalami pengendapan. Kenaikan konsentrasi ini akan terus berlanjut seiring bertambahnya waktu perendaman. Sharma et al. (2009) menyatakan bahwa setelah 7 hari perendaman akan terjadi pengedapan ion Ca2+ yang merupakan langkah awal dalam pertumbuhan kristal. Pertumbuhan kristal apatit membutuhkan ion kalsium dan fosfat (Oudadesse et al. 2011). Dalam hal ini ion Ca2+ yang dikeluarkan sampel HAp akan berikatan dengan ion fosfat dari larutan SBF membentuk kristal apatit. Adanya kenaikan kalsium pada HAp berporogen setelah perendaman 6 hari menandakan telah terbentuknya kristal apatit sehingga dapat dikatakan bahwa material HAp yang disintesis dengan menggunakan pati singkong bersifat bioaktif.
SIMPULAN DAN SARAN
Simpulan
Sintesis hidroksiapatit berporogen pati singkong berhasil dilakukan dengan metode basah (presipitasi) seperti yang dicirikan XRD. Sintesis dengan perlakuan sonikasi 6 jam menghasilkan HAp yang lebih murni daripada perlakuan sonikasi 2 dan 4 jam. Semakin lama waktu sonikasi, maka kemurnian HAp semakin tinggi. HAp penambahan pati singkong 30% memiliki ukuran pori yang lebih besar daripada HAp tanpa dan penambahan pati singkong 20%. Analisis FTIR menggambarkan pita HAp berporogen tidak mengandung pita karbonat sedangkan HAp tanpa porogen terdapat pola pita karbonat. Uji in vitro menunjukkan
15 pertumbuhan kristal apatit terjadi setelah 6 hari perendaman dengan larutan SBF. HAp berpori bersifat bioaktif dan memilki kapasitas yang sangat baik untuk pertumbuhan apatit, namun belum bisa diaplikasikan untuk implan tulang manusia.
Saran
Penelitian ini masih memerlukan beberapa perlakuan tambahan seperti pengukuran ukuran granula pati. Perlu pencampuran bahan dengan menggunakan ballmill (metode kering) agar HAp yang dihasilkan lebih homogen, bebas pengotor, dan ukuran pori yang seragam. Pemotongan kristal HAp secara melintang untuk melihat pori-pori yang terbentuk di bagian dalam HAp. Selain itu, dilakukan pengukuran konsentrasi kalsium HAp yang digunakan pada uji in vitro SBF untuk membandingkan potensial kimia antara sampel HAp dan larutan SBF.
DAFTAR PUSTAKA
Al-Sokanee ZN, Toabi AAH, Al-Assadi MJ, Al-Assadi EA. 2009. The drug release study of ceftriaxone from porous hydroxyapatite scaffolds. AAPS Pharmacy Science Technology. 10(5):772-779.
Aoki H. 1991. Science Medical Applications of Hydroxyapatite. Tokyo (JP): JAAS.
Baby RL, Hasan I, Kabir KA, Naser MN. 2010. Nutrient Analysis of Some Commercially Important Molluscs of Bangladesh. J Sci Res. 2(2):390–396. Balamurugan A, Kannan S, Rajeswari S. 2002. Bioactive sol-gel hydroxyapatite
surface for biomedical applications-in vitro study. Trends Biomater Artif Org. 16(1):18-20.
Chang BS, Lee CK, Hong KS, Youn HJ, Ryu HS, Chung SS, Park KW. 2000. Osteoconduction at porous hydroxyapatite with various pore configurations. J Biomater. 21:1291.
Dahlan K, Prasetyanti F, Sari YW. 2009. Sintesis hidroksiapatit dari cangkang telur menggunakan dry method. J Biofis. 5(2):71-78.
German RM. 1984. Powder Metalurgi Science. New Jersey (US): Metal Powder Industries Federation.
Hidayat MW. 2012. Modifikasi pori Hidroksiapatit dari Tulang Ikan Alu-alu (Sphyraena barracuda) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Kehoe S. 2008. Optimisation of Hydroksiapatite (HAp) for Orthopaedic Application via the Chemical Precipitaion Technique [thesis]. Dublin (IE): Dublin City University.
Maachou H et al. 2008. Characterization and in vitro bioactivity of chitosan/ hydroxyapatite composite membrane prepared by freeze-gelation method. Trend s Biomater Artif Org. 22(1):16-27.
Oudadesse H, Mostafa A, Bui X V, Foad E, Kamal G, Legal Y, Cathelineau G. 2011. Physico-chemical assessment of biomimetic nano-hydroxyapatite polymer matrix for use in bony surgery. Int J B Biomed Eng. 5:3.
16
Pane MS. 2004. Penggunaan hidroksiapatit sebagai bahan dental implan [skripsi]. Medan (ID): Universitas Sumatra Utara.
Pankaew P, Hoonnivathana E, Limsuwan P, Naemchanthara K. 2010. Temperature effect on calcium phosphate synthesized from chicken eggshells and ammonium phosphate. J Appl Sci. 10(24): 3337-3342.
Prihantoko DA. 2011. Karakterisasi paduan CoCrMo dengan pelapisan titanium nitrida dan hidroksiapatit-kitosan [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Romawarni A. 2011. Sintesis dan uji in vitro hidroksiapatit berporogen kitosan dengan metode sol gel [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Sadjadi MS, Meskinfam M, Jazdarreh H. 2010. Hydroxyapatite-starch nano biocomposites synthesis and characterization. Int Nano Dimens. 1(1):57-63. Santos MH, de Oliveira M, SouzaL PF,Mansur HS, Vasconcelos WL. 2004.
Synthesis Control and Characterization of Hydroxyapatite Prepared by Wet Precipitation Process. Mater Res. 7(4): 625-630.
Sharma S, Son vp, Bellare JR. 2009. Chitosan reinforced apatite-wollastonite coating by electrophoretic deposition on tittanium implants. J Mater Sci. 20:1427-1436.
Soejoko DS, Wahyuni S. 2002. Spektroskopi inframerah senyawa kalsium fosfat hasil presipitasi. Makara Sains. 6(3): 117-122.
Soido C, Vasconcellos MC, Diniz AG, PinheiroJ. 2009. An Improvement of Calcium Determination Technique in the Shell of Molluscs. Brazilian Archiv Bio Tech. 52(1):93-98.
Sopyan I, Mel M, Ramesh S, Khalid KA. 2007. Porous hydroxyapatite for artificial bone applications. Sci Tech Adv Mater. 8:116–123.
Trianita VN. 2012. Sintesis hidroksiapatit berpori dengan porogen polivinil alkohol dan pati [skripsi]. Bogor (ID): Institut Pertanian Bogor.
17
LAMPIRAN
Lampiran 1 Bagan alir penelitian
Dipanasakan 700 ºC 6 jam
Penentuan
Kadar Abu (Kandungan Ca) Analisis AAS Kalsinasi 1000 ºC (2 jam) CaCO3 Æ CaO Analisis XRD [Ca(OH)2] Analisis XRD (HAp Terbaik)
Uji In vitro (SBF) Uji FTIR Analisis SEM
Analisis XRD (CaCO3)
Hidrasi (suhu ruang) CaO Æ Ca(OH)2
Preparasi Cangkang Keong
Sintesis Hidroksiapatit Ca(OH)2 + (NH4)2HPO4
(sonikasi 2, 4, dan 6 jam)
Sintesis Hidroksiapatit Ca(OH)2 + (NH4)2HPO4
18 y = 0.031x ‐ 0.002 R² = 0.999 ‐0.1 0 0.1 0.2 0.3 0.4 0.5 0.6 0 5 10 15 20 Ab so rb an Konsentrasi (ppm)
Lampiran 2 Data perhitungan konsentrasi kalsium cangkang keong sawah a. Absorban standar kalsium
b. Absorban dan konsentrasi kalsium cangkang keong sawah
Sampel Absorban Konsentrasi (ppm) Bobot sampel (g) DF VF Konsentrasi sebenarnya (ppm) Blanko sampel 0.0076 0.3594 1 1 1 Cangkang keong 1 0.2788 9.0305 0.1022 100 100 848444.2 Cangkang keong 2 0.2941 9.5197 0.1011 100 100 906063.3 Cangkang keong 3 0.2958 9.5741 0.1022 100 100 901634.1 Rerata 885381.5
Contoh perhitungan ulangan 1 (cangkang keong 1)
Konsentrasi Ca = K – K DF VF WF = . – . . = 848444.2 ppm Konsentrasi rerata Ca = = . . . = 885380,5 ppm = 88.54%
Konsentrasi standar (ppm) Absorban
2.0000 0.0594 4.0000 0.1201 8.0000 0.2487 12.0000 0.3698 16.0000 0.4974
19
Lampiran 3 Data pencirian XRD
a. Serbuk cangkang keong sawah sebelum kalsinasi
2 Ө Intensitas Fasa 26.25 80 CaCO3 27.21 26 CaCO3 31.16 38 CaCO3 33.16 143 CaCO3 36.14 29 CaCO3 37.93 49 CaCO3 38.43 23 CaCO3 42.94 56 Ca3(PO4)2 45.88 93 CaCO3 48.45 22 CaCO3 50.23 22 CaCO3 52.49 70 CaCO3 53.03 35 CaCO3
b. Serbuk cangkang keong sawah setelah kalsinasi 1000 ºC dan hidrasi selama 1 minggu 2 Ө Intensitas Fasa 17.90 112 Ca(OH)2 28.64 54 Ca(OH)2 29.36 152 Ca3(PO4)2 34.10 172 Ca(OH)2 39.36 32 CaCO3 47.06 68 Ca(OH)2 48.40 38 CaCO3 50.74 72 Ca3(PO4)2 54.38 38 Ca3(PO4)2 64.30 24 Ca(OH)2
20
Lanjutan Lampiran 3
c. HAp tanpa porogen (sonikasi 2 jam)
2 Ө Intensitas Fasa 21.84 24 HAp 22.90 22 HAp 25.94 102 AKA 28.18 34 AKB 29.10 46 HAp 31.84 230 HAp 32.24 130 AKA 33.02 170 CaCO3 34.12 54 Ca(OH)2 35.50 20 AKA 37.46 20 CaO 39.22 22 AKA 39.86 68 HAp 42.08 20 HAp 43.92 20 HAp 45.46 22 HAp 46.74 84 HAp 48.14 38 HAp 49.54 102 AKB 50.58 46 HAp 50.66 44 Ca(OH)2 52.18 42 AKB 53.22 44 HAp 61.70 22 HAp
21 Lanjutan Lampiran 3
d. HAp tanpa porogen (sonikasi 4 jam)
2 Ө Intensitas Fasa 17.90 26 Ca(OH)2 25.80 76 AKB 28.04 22 HAp 28.90 52 HAp 31.76 230 HAp 32.14 136 HAp 32.88 142 HAp 34.08 94 Ca(OH)2 35.46 22 HAp 39.18 28 HAp 39.76 58 AKA 42.04 20 HAp 46.70 76 HAp 48.10 50 HAp 49.48 84 HAp 50.50 48 HAp 51.32 26 HAp 52.12 36 HAp 53.18 40 HAp 61.64 24 HAp 17.90 26 HAp 25.80 76 HAp 28.04 22 HAp 28.90 52 HAp
22
Lanjutan Lampiran 3
e. HAp tanpa porogen (sonikasi 6 jam)
2 Ө Intensitas Fasa 22.82 24 HAp 25.90 100 HAp 27.82 20 HAp 27.86 24 HAp 28.94 40 HAp 31.76 206 HAp 31.80 216 HAp 32.20 126 HAp 32.88 126 HAp 34.04 60 HAp 39.76 58 HAp 41.98 20 HAp 46.68 70 HAp 48.10 34 HAp 48.02 20 HAp 49.48 92 HAp 50.44 34 HAp 51.36 32 HAp 52.06 34 HAp 53.20 44 HAp 61.66 22 HAp 65.06 20 HAp 22.82 24 HAp 25.90 100 Hap
23 Lanjutan Lampiran 3
f. HAp berporogen pati singkong 30%
2θ Intensitas Fasa 10.80 22 HAp 16.84 22 HAp 21.82 22 HAp 25.90 68 HAp 28.96 36 HAp 31.78 188 HAp 31.82 190 HAp 32.18 124 HAp 34.12 54 HAp 35.54 22 HAp 39.22 22 HAp 39.90 58 HAp 42.04 20 HAp 43.80 20 HAp 46.80 72 HAp 48.11 44 HAp 49.48 82 HAp 50.60 48 HAp 51.36 46 HAp 52.11 38 HAp 53.26 42 HAp 61.72 26 HAp 62.96 22 HAp 64.10 30 HAp 77.02 20 HAp 78.26 24 HAp
24
Lampiran 4 Data komposisi bahan yang digunakan untuk menghasilkan HAp Pereaksi Ca(OH)2 (NH4)2.HPO4
Bobot molekul (g/mol) 74.0780 131.9880 Bobot teoritis (g) 3.7039 3.9596 Konsentrasi (M) 0.5 0.3 Volume (mL) 100 100 a. Larutan (NH4)2.HPO4 0,3 M M = M x 0.3 = . x g = 3. 9596 gram b. Suspensi Ca(OH)2 0.5 M M = M x 0.5 = . x g = 3.7039 gram c. Rasio konsentrasi Ca/P
Ca/P = 1.67 Ca = 0.5 M P = 0.3 M
25 Lampiran 5 Data JCPDS (Joint Commitee on Powder Diffraction Standards) a. Data JCPDS HidroksiapatitCa10(PO4)6(OH)2
26
Lanjutan Lampiran 5
c. Data JCPDS Apatit Karbonat Tipe A Ca10(PO4)6(CO3)2
27 Lanjutan Lampiran 5
e. Data JCPDS Kalsium Oksida (CaO)
28
Lanjutan Lampiran 5
g. Kalsium hidroksida: Ca(OH)2
Lampiran 6 Contoh perhitungan ukuran pori hasil foto SEM
Keterangan :
A= diameter pori dalam cm / diameter pori pada foto (cm) B= diameter pori sesungguhnya (µm)
C= diameter skala dalam cm / panjang skala pada foto (cm)
D= diameter skala sesungguhnya (µm) / panjang skala pada foto (µm) Perhitungan: A B C D . B . µ B = 1.02 µm
29 Lampiran 7 Perhitungan ukuran kristal dan parameter kisi
a. Ukuran kristal
Sampel 2θ (°) β (°) (rad)2θ θ (rad) cos θ (rad) β (rad) D (nm) rata-rataD HAp tanpa porogen (sonikasi 6 jam) 31.7200 0.2074 0.5536 0.2768 0.9619 0.0036 41.5898 41.9586 31.8000 0.2074 0.5550 0.2775 0.9617 0.0036 41.5981 32.9600 0.2027 0.5753 0.2876 0.9589 0.0035 42.6879 HAp berporogen pati singkong 30% 31.7800 0.2685 0.5547 0.2773 0.9618 0.0047 32.1304 33.9013 31.8200 0.2685 0.5554 0.2777 0.9617 0.0047 32.1336 32.1800 0.2307 0.5630 0.2815 0.9606 0.0040 37.4399 Contoh perhitungan (HAp berporogen pati singkong):
D = . D
=
. . . .D = 32.1304 nm Keterangan: D = ukuran kristal (nm) 0.9 = konstanta kristal
λ = panjang gelombang sinar X (nm)
β = Full Weight Hall Modulation (FWHM) (rad)
θ = sudut difraksi (rad) b. Parameter kisi HAp
Sampel a (Å) c (Å)
HAp standar (JCPDS) 9.418 6.884
HAp (sonikasi 2 jam) 9.463 6.913
HAp (sonikasi 4 jam) 9.417 6.893
HAp (sonikasi 6 jam) 9.413 6.883
30
Lampiran 8 Data perhitungan konsentrasi kalsium hasil analisis uji in vitro a. Absorban standar kalsium
Konsentrasi standar (ppm) Absorban
2.0000 0.1000
4.0000 0.1933
8.0000 0.3677
12.0000 0.5654
16.0000 0.7318
b. Absorban dan konsentrasi kalsium
Sampel Konsentrasi Ca (ppm) Absorban
Instrumen Perhitungan
Blanko larutan SBF 3.1677 3.4267 0.1592
HAp tanpa porogen (6 hari) 8.5027 8.7844 0.4003
HAp+pati singkong 20% (6 hari) 3.1084 3.3467 0.1556 HAp+pati singkong 30% (6 hari) 2.9607 3.1978 0.1489 HAp tanpa porogen (20 hari) 10.6389 10.9378 0.4972 HAp+pati singkong 20% (20 hari) 8.9084 9.1933 0.4187 HAp+pati singkong 30% (20 hari) 8.7629 9.0467 0.4121 Contoh perhitungan HAp penambahan pati singkong 30% (20 hari):
Persamaan garis: y = 0.045x + 0.005 Konsentrasi Ca = A . . = . . . = 9.0467 ppm y = 0.045x + 0.005 R² = 0.999 0 0.2 0.4 0.6 0.8 0 2 4 6 8 10 12 14 16 18 Ab sorb an Konsentrasi (ppm)
31
RIWAYAT HIDUP
Penulis dilahirkan di Padangsidimpuan, Sumatera Utara pada tanggal 8 Januari 1991 dari ayah Baginda Harahap dan ibu Yusrah Erliana. Penulis adalah anak ketiga dari tiga bersaudara. Tahun 2009 penulis lulus dari SMA Negeri 2 Padangsidimpuan dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB dan diterima di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis menjadi asisten praktikum Kimia TPB tahun ajaran 2012/2013, asisten praktikum Kimia Anorganik dan Layanan pada tahun ajaran yang sama. Penulis juga aktif sebagai staf Departemen Eksternal Ikatan Mahasiswa Kimia (IMASIKA) IPB tahun 2010/2011 dan staf Departemen Pendidikan Ikatan Mahasiswa Tapanuli Selatan (IMATAPSEL) Bogor tahun 2010-2012. Bulan Juli-Agustus 2012 penulis melaksanakan Praktik Lapangan di Balai Penelitian Ternak (BALITNAK) Ciawi, Bogor dengan judul Pengaruh Enzim BS4 dalam Meningkatkan Fermentasi Tongkol Jagung secara In vitro.