J. Sains MIPA, Edisi Khusus Tahun 2007, Vol. 13, No. 2, Hal.: 100 - 106 ISSN 1978-1873
ISOLASI, PEMURNIAN DAN KARAKTERISASI ENZIM PROTEASE TERMOSTABIL
DARI BAKTERI ISOLAT LOKAL Bacillus subtilis ITBCCB148
Yandri A.S, Dian Herasari, Tati Suhartati
Jurusan Kimia FMIPA, Universitas Lampung, Jl. Soemantri Brojonegoro No. 1, Bandar Lampung 35145
Diterima 28 Agustus 2007, perbaikan 10 Desember 2007, disetujui untuk diterbitkan 27 Desember 2007
ABSTRACT
Protease catalyzes the hydrolysis of peptide bond to produce amino acid and peptide. This enzyme was used in many industrial processes, especially in the detergent industry. The aims of this research are to isolate, purify and characterize the extracellular protease from a local bacteria Bacillus subtilis ITBCCB148To achieve these aims, the determination of an optimum condition to produce protease with high activity, production, isolation, and purification of enzyme. Determination of optimum condition was carried out by various pH and temperatures of fermentation. The purification of the enzyme was conducted by few steps which fractionation with ammonium sulphate, CM- Sephadex C-50 cation exchange column chromatography, and molecular sieves column chromatography using Sephadex G-100. The purified enzyme was characterized by determining the temperature, pH, and kinetic data. The results showed that the protease which was produced by Bacillus subtilis ITBCCB148 has the optimum activity at the fermentation temperature of 35 C, the fermentation media at pH 7.0; and the duration time of fermentation was 60 hours with unit activity of 0.24 U/mL. The specific activity of the purified enzyme was 65.8 U/mg; increasing by 263 times than that of the crude enzyme extract with specific activity of only 0.25 U/mg. The optimum pH value of the purified enzyme was 7.5, however this enzyme was active at a pH range of 6.0-8.0. The optimum temperature value of the pure enzyme was 60 C, while the Km and Vmax
value were 6.48 mg mL-1 and 3.26 mol mL-1 min-1, respectively.
Keywords: protease, Bacillus subtilis ITBCCB148, isolation and purification
1. PENDAHULUAN
Pada akhir-akhir ini, penelitian tentang kestabilan enzim sangat menarik perhatian karena kaitannya dengan pengembangan industri, khususnya industri deterjen, sirup gula cair dari pati, sintesis senyawa organik, pulp dan kertas, pakan ternak, dan pada penanganan buangan industri1. Hingga saat ini sebagian besar enzim yang digunakan dalam
industri di Indonesia masih diimpor. Keadaan ini tentunya sangat merugikan jika ditinjau secara ekonomi, padahal Indonesia merupakan negara tropis yang kaya akan sumber alam hayati, terutama mikroba penghasil enzim, termasuk protease. Melihat kondisi ini sangatlah penting untuk mengembangkan teknik produksi, pemurnian dan teknik untuk meningkatkan kestabilan enzim, sehingga dapat memenuhi tuntutan industri agar tidak selalu tergantung pada sumber dari luar negeri.
Umumnya enzim tidak stabil pada kondisi suhu yang tinggi dan pH yang ekstrim2, padahal kondisi tersebut diperlukan
dalam proses industri. Untuk mendapatkan enzim yang sesuai dengan kebutuhan industri, dapat dilakukan dengan mengisolasi langsung dari organisme yang ada di alam dan hidup pada kondisi tersebut atau dengan modifikasi kimia terhadap enzim yang berasal dari organisme yang hidup pada kondisi tidak ekstrim3. Menurut Mozhaev dan Martinek4)
stabilisasi enzim yang berasal dari mikroba mesofilik merupakan cara yang lebih disukai untuk memperoleh enzim yang stabil. Sedangkan Mozaev et al.5) menyarankan penggunaan modifikasi kimia untuk meningkatkan kestabilan enzim.
Beberapa penelitian yang telah dilakukan dengan modifikasi kimia menunjukkan enzim hasil modifikasi meningkat kestabilannya terhadap pH dan suhu dibandingkan dengan enzim tanpa dimodifikasi6-9).
Berdasarkan hasil-hasil yang telah dilaporkan tersebut, maka pada penelitian ini dipilih memproduksi, mengisolasi dan memurnikan enzim protease dari bakteri isolat lokal Bacillus subtilis ITBCCB148 yang bersifat mesofilik. Dengan dikuasainya teknik produksi, isolasi dan pemurnian, maka tujuan utama penelitian ini untuk mendapatkan enzim yang stabil terhadap suhu dan pH dapat dilakukan, sehingga enzim hasil isolasi dan pemurnian dapat digunakan dalam industri yang dapat menunjang kemajuan pembangunan dan institusi. Enzim hasil pemurnian dapat dimodifikasi untuk meningkatkan kestabilannya. Selanjutnya enzim hasil pemurnian dengan aktivitas dan tingkat kemurnian yang tinggi
J. Sains MIPA, Edisi Khusus Tahun 2007, Vol. 13, No. 2
juga dapat digunakan untuk mempelajari struktur enzim terutama struktur primernya untuk menunjang kemajuan ilmu pengetahuan dan teknologi.
2. METODE PENELITIAN
2.1. Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium Mikrobiologi Universitas Lampung (mulai bulan Maret 2007 Juli 2007).
2. Prosedur Penelitian
Tahapan penelitian yang akan dilakukan adalah sebagai berikut : produksi, isolasi, pemurnian, karakterisasi.
2.2.1 Produksi enzim protease
Tahap produksi protease meliputi : penentuan lama waktu inkubasi untuk mendapatkan enzim dengan aktivitas tertinggi, penentuan suhu optimum, dan penentuan pH optimum media fermentasi. Media fermentasi yang digunakan adalah media yang mengandung pepton 0,5%, ekstrak ragi 0,15%, glukosa 0,036%, dan NaCl 0,25%.
2.2.2. Isolasi dan pemurnian enzim protease
Isolasi dan pemurnian dilakukan beberapa tahap, yaitu : pemisahan cairan enzim dari sel dengan sentrifuga dingin sehingga diperoleh ekstrak kasar enzim, pengendapan dengan garam amonium sulfat dengan berbagai tingkat kejenuhan, kromatografi kolom penukar ion, dan kromatografi kolom penyaringan molekul10).
2.2.3. Uji aktivitas protease dan penentuan kadar protein
Pengujian aktivitas protease dilakukan dengan metode Kunitz modifikasi11). Kadar protein ditentukan dengan metode
Lowry12).
2.3. Karakterisasi enzim hasil pemurnian
Karakterisasi enzim hasil pemurnian meliputi: penentuan pH dan suhu optimum, dan penentuan data kinetika.
2.3.1. Penentuan pH dan suhu optimum enzim hasil pemurnian
Untuk mencari pH optimum enzim sebelum dan sesudah modifikasi digunakan bufer fosfat 0,1 M dengan pH bervariasi, yaitu 5,0; 5,5; 6,0; 6,5; 7,0; 7,5; 8,0; 8,5; dan 9,0. Suhu dijaga tetap pada suhu optimum yang telah ditentukan. Sedangkan untuk mencari suhu optimum, digunakan suhu yang bervariasi, yaitu 40, 45; 50; 55; 60; 65; 70 dan 75 C.
2.3.2. Penentuan data kinetika enzim hasil pemurnian
Konstanta Michaelis-Menten (Km) dan laju reaksi maksimum (Vmaks) enzim sebelum dan sesudah modifikasi ditentukan
dari persamaan Lineweaver-Burk.
3. HASIL DAN PEMBAHASAN
3.1. Produksi Enzim Protease
3.1.1. Penentuan suhu, dan waktu panen
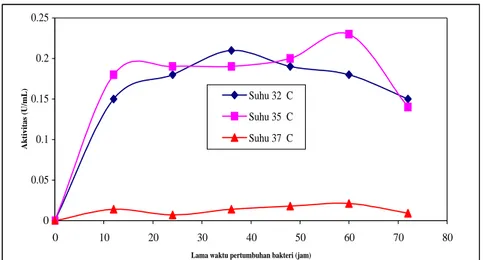
Gambar 1 menunjukkan hubungan antara lama waktu pertumbuhan bakteri terhadap aktivitas enzim protease yang dihasilkan. Grafik tersebut menunjukkan bahwa suhu optimum pertumbuhan bakteri untuk mendapatkan enzim protease dengan aktivitas maksimum adalah pada suhu 35 C. Sedangkan lama waktu pertumbuhan bakteri untuk mendapatkan enzim dengan aktivitas optimum adalah jam ke-60. Aktivitas enzim pada jam ke-60 adalah 0,23 U/mL. Aktivitas enzim pada suhu 32 C tidak berbeda jauh dengan aktifitas enzim pada suhu 35 0C. Sedangkan aktivitas enzim pada suhu 37
Yandri A.S. dkk... Isolasi, Pemurnian dan Karakterisasi Enzim Protease Termostabil
C sangat kecil sekali dibandingkan kedua suhu tersebut, ini menunjukkan pertumbuhan bakteri sudah tidak berlangsung dengan baik sehingga enzim protease tidak dapat dihasilkan secara optimal.
Gambar 1. Kurva hubungan antara lama waktu pertumbuhan bakteri terhadap aktivitas enzim protease yang diproduksi
pada berbagai suhu
3.1.2. Penentuan pH optimum
Penentuan pH optimum media, untuk menghasilkan enzim protease dengan aktivitas optimum dilakukan dengan memvariasikan pH media fermentasi yaitu: 5,0; 6,0; 7,0; dan 8,0. Suhu fermentasi yang digunakan 35oC. Grafik pada
Gambar 2 menunjukkan hubungan antara lama waktu pertumbuhan bakteri dengan aktivitas enzim protease yang dihasilkan pada berbagai pH media fermentasi. Grafik tersebut menunjukkan enzim protease dengan aktivitas optimum dihasilkan pada media fermentasi dengan pH 7,0. Aktivitas enzim pada pH tersebut dengan lama waktu inkubasi 60 jam
adalah 0,304 U/mL.
Gambar 2. Kurva hubungan antara lama waktu pertumbuhan bakteri terhadap aktivitas enzim protease yang diproduksi
pada berbagai pH
3.2. Isolasi dan Pemurnian Enzim Protease 3.2.1. Fraksinasi dengan garam amonium sulfat
Gambar 3 menunjukkan hubungan antara kejenuhan amonium sulfat dengan aktivitas spesifik enzim yang menunjukkan enzim protease mempunyai aktivitas tertinggi pada fraksi 50-65% dengan aktivitas spesifik 0,55 U/mg.
0 0.05 0.1 0.15 0.2 0.25 0 10 20 30 40 50 60 70 80
Lama waktu pertumbuhan bakteri (jam)
A k ti v it a s (U /m L ) Suhu 32 C Suhu 35 C Suhu 37 C 0 0.1 0.2 0.3 0.4 0.5 0 6 12 18 24 30 36 42 48 54 60 66 72 78
Lama waktu pertumbuhan bakteri (jam)
A k ti v it a s (U /m L ) Aktivitas (pH 5.0) Aktivitas (pH 6.0) Aktivitas (pH 7.0) Aktivitas (pH 8.0)
J. Sains MIPA, Edisi Khusus Tahun 2007, Vol. 13, No. 2
Gambar 3. Hubungan antara kejenuhan amonium sulfat dengan aktivitas spesifik enzim protease 3.2.2. Kromatografi penukar kation CM-Sephadex C-50
Pola protein (A280 ) dan aktivitas (U/mL) enzim protease hasil kromatografi kolom CM-Sephadex C-50 dapat dilihat pada
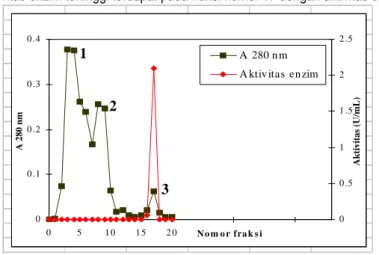
Gambar 4. Gambar 4 menunjukkan aktivitas enzim protease terletak pada puncak protein nomor 3 yaitu pada fraksi ke 16 dan 17 . Aktivitas enzim tertinggi terdapat pada fraksi nomor 17 dengan aktivitas unit sebesar 2,10 U/mL.
Gambar 4. Kromatogram enzim protease dari Bacillus subtilis ITBCCB148 pada kolom CM-Sephadex C-50 3.2.3. Kromatografi kolom penyaringan molekul Sephadex G-100
Pemurnian enzim dengan kromatografi kolom penyaringan molekul Sephadex G-100 menggunakan bufer fosfat 0,05 M, pH 7,0 sebagai bufer elusi. Pola protein (A280) dan aktivitas enzim protease hasil kromatografi kolom Sephadex G-100
dapat dilihat pada Gambar 5. Gambar 5 menunjukkan dari 4 puncak protein yang diperoleh hanya satu puncak protein nomor 3 yang beraktivitas enzim protease, yaitu fraksi 13 sampai fraksi ke-18 dengan aktivitas tertinggi pada fraksi ke 16 dengan aktivitas 0,25 U/mL
0 0.1 0.2 0.3 0.4 0.5 0.6 0 - 20 20 - 35 35 - 50 50 - 65 65 - 80 85 - 100
Fraksi am. sulfat (%)
A k t. S p es if ik ( u /m g ) 0 0.05 0.1 0.15 0.2 0 5 10 15 20 25 30 Nomor fraksi A 2 8 0 n m 0 0.05 0.1 0.15 0.2 0.25 0.3 A k ti v it a s (U /m L ) A 280 nm Aktivita s e nzim 1 4 3 2 0 0 .1 0 .2 0 .3 0 .4 0 5 1 0 1 5 2 0 N o m o r fra k s i A 2 8 0 n m 0 0 .5 1 1 .5 2 2 .5 A k ti v it a s (U /m L ) A 280 n m A ktiv itas en zim
3 1
Yandri A.S. dkk... Isolasi, Pemurnian dan Karakterisasi Enzim Protease Termostabil
Tabel tahapan pemurnian enzim protease dari Bacillus subtilis ITBCCB148 dapat dilihat pada Tabel 1. Data pada Tabel 1 menunjukkan terjadi peningkatan aktivitas spesifik enzim yang tinggi untuk masing-masing tahap pemurnian, terutama hasil kromatografi kolom Sephadex G-100. Peningkatan aktivitas spesifik enzim pada tahap pemurnian dengan fraksinasi amonium sulfat adalah 19 x ; 245 x pada pemurnian dengan kromatografi kolom CM-Sephadex C-5; dan 263 x pada pemurnian dengan kromatografi kolom Sephadex G-100. Hasil ini menunjukkan pemurnian yang dilakukan telah berhasil mendapatkan enzim protease hasil pemurnian dengan tingkat kemurnian yang tinggi.
Tabel 1. Skema pemurnian enzim protease dari Bacillus subtilis ITBCCB148
Tahap Vol. (mL) Aktivi-tas total (U) Protein (mg/mL) Total protein (mg) Akt.spe-sifik (u/mg) Hasil (%) Kemur-nian (X) Eks.kasar Am S. 35-85 % CM-Sephadex Sephadex G-100 3450 475 332,5 1163,8 828 726,75 698,25 291 0,96 0,32 0,034 0,0038 3312 152 11,37 4,42 0,25 4,78 61,4 65,8 100 87,8 84,3 35,1 1 19 245 263
3.3. Karakterisasi Enzim Protease Hasil Pemurnian
3.3.1. Penentuan pH optimum enzim protease hasil pemurnian
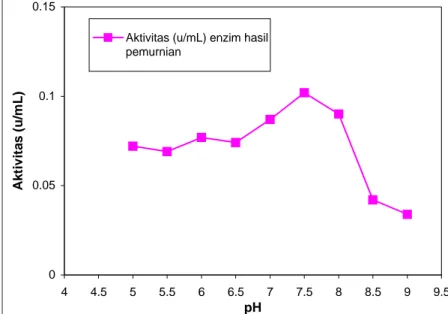
Aktivitas enzim protease hasil pemurnian Bacillus subtilis ITBCCB148 pada berbagai pH dapat dilihat pada Gambar 6 yang menunjukkan pH optimum enzim protease hasil pemurnian 7,5 dengan aktivitas 0,102 (U/mL). Enzim protease ini termasuk enzim protease netral. Data pada gambar juga menunjukkan enzim protease mengalami penurunan aktivitas pada pH 8 dan mengalami penurunan aktivitas yang tinggi pada pH 8,5.
0 0.05 0.1 0.15 4 4.5 5 5.5 6 6.5 7 7.5 8 8.5 9 9.5 pH A k ti v it a s ( u /m L )
Aktivitas (u/mL) enzim hasil pemurnian
Gambar 6. Kurva hubungan antara pH dengan aktivitas enzim protease hasil pemurnian 3.3.2. Penentuan suhu optimum enzim protease hasil pemurnian
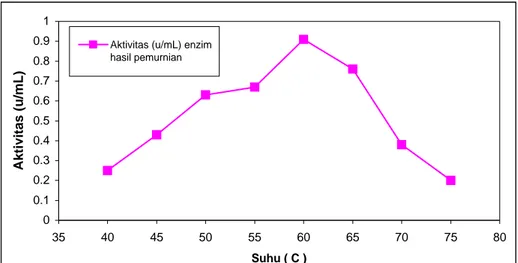
Aktivitas enzim protease hasil pemurnian dari Bacillus subtilis ITBCCB148 pada berbagai suhu dapat dilihat pada Gambar 7. Suhu optimum enzim protease hasil pemurnian berdasarkan gambar tersebut 60 C, dengan aktivitas 0,91 U/mL. Enzim protease ini termasuk enzim yang bersifat termostabil.
J. Sains MIPA, Edisi Khusus Tahun 2007, Vol. 13, No. 2 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1 35 40 45 50 55 60 65 70 75 80 Suhu ( C ) A k ti v it a s ( u /m L )
Aktivitas (u/mL) enzim hasil pemurnian
Gambar 7. Kurva hubungan antara suhu dengn aktivitas enzim protease hasil pemurnian 3.3.3. Penentuan data kinetika enzim protease hasil pemurnian
Kurva penentuan harga Km dan Vmaks enzim protease hasil pemurnian Bacillus subtilis ITBCCB148 dapat dilihat pada
Gambar 8. Dari persamaan Lineweaver-Burk diperoleh harga Vmaks enzim hasil pemurnian 3,26 U/mL, sedangkan Km
enzim hasil pemurnian 6,48 mg/mL substrat.
y = 1.9882x + 0.3069 R2 = 0.9902 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 -0.5 -0.4 -0.3 -0.2 -0.1 0 0.1 0.2 0.3 0.4 0.5 1/S 1 /V
Gambar 8. Kurva Lineweaver-Burk enzim protease hasil pemurnian
4. KESIMPULAN DAN SARAN
4.1. Kesimpulan
Aktivitas spesifik enzim protease hasil pemurnian 65,8 U/mg protein, meningkat 263 kali dibandingkan dengan ekstrak kasar enzim yang mempunyai aktivitas spesifik 0,25 U/mg protein. Pemurnian enzim telah berhasil mendapatkan enzim dengan aktivitas dan tingkat kemurnian yang tinggi. Enzim protease hasil pemurnian mempunyai pH optimum 7,5 dan stabil pada rentang pH 5,0 8,0. Enzim ini termasuk enzim yang dapat bekerja pada rentang pH yang cukup lebar dan memenuhi syarat untuk penggunaan dalam industri. Suhu optimum eanzim protease hasil pemurnian adalah 60 C; termasuk enzim yang bersifat termostabil dan dapat digunakan dalam proses industri. Nilai Km enzim hasil pemurnian
adalah 6,48 mg /mL substrat, dan Vmaks 3,26 U/ mL/ menit, enzim ini mempunyai afinitas yang tinggi terhadap substrat. 4.2. Saran
Untuk meningkatkan kestabilan enzim terhadap suhu dan pH perlu dilakukan penelitian lebih lanjut yaitu dengan
-1/Km
Yandri A.S. dkk... Isolasi, Pemurnian dan Karakterisasi Enzim Protease Termostabil
DAFTAR PUSTAKA
1. Vieille, C. and Zeikus, J. G. 1996. Thermozymes: Identifying molecular determinant of protein structural and functional stability, Tibtech., 14 (6): 183-189.
2. Goddettee, D.W., Terri, C., Beth, F.L., Maria, L., Jonathan, R.M., Christian, P., Robert, B.R., Shiow, S.Y. and Wilson, C.R. 1993. Strategy and implementation of a system for protein engineering, J. Biotechnol., 28: 41-54. 3. Wagen, E.S. 1984. Strategies for increasing the stability of enzymes, in Enzyme Engineering 7, The New York
Academy of Sciences, New York, 1-19.
4. Mozhaev, V. V., Martinek, K. 1984. Structure-stability relationship in proteins: New approaches to stabilizing enzymes, Enzyme Microb. Technol., 6: 50-59.
5. Mozhaev, V. V., Melik-Nubarov, N.S., Siksnis, V. and Martinek, K. 1990. Strategy for stabilizing enzymes. Part two: Increasing enzyme stability by selective chemical modification, Biocatalysis, 3: 189-196.
6. Yandri, A.S. , Cynthia, R., Muliawati, S, Soetijoso, S. 2005. Pengaruh modifikasi kimia terhadap stabilitas termal enzim -amilase dari bakteri isolat lokal Bacillus subtilis ITBCCB148, J. Sains Tek.i, 9 (1): 9-16.
7. Morand, P., and Biellmann, J. F. 1991. Modification of -amylase from Bacillus licheniformis by the polyaldehyde derived from -cyclodextrine and -amylase thermostability, Fed. Eur. Biochem. Soc., 2: 148-150.
8. Kobayashi, M. and Takatsu, K. 1994. Cross-linked stabilization of trypsin with dextran-dialdehyde, Biosci. Biotech. Biochem., 58(2): 275-278.
9. Yang, Z., Michael, D., Robert, A., Fang, X.Y. and Alan, J.R. 1996. Polyethylene glycol-induced stabilization of subtilisin, Enzyme Microb. Technol., 18: 82-89.
10. Yandri, A.S. , Kosasih, P., Soetijoso, S., Muliawati, S. 2000. Isolasi, pemurnian dan karakterisasi enzim -amilase termostabil dari bakteri lokal Bacillus sp. B. 148, Prosiding Kimia Bersama ITB-UKM Keempat, Bandung, 294-302. 11. Yamaguchi, T., Yamashita, Y., Takeda, I. and Kiso, H. 1982. Proteolytic enzymes in green asparagus, kiwi fruit and
miut: occurence and partial characterization, Agric. Biol. Chem., 46: 1983-1986.
12. Lowry, O.H., Rosebrough, N.J., Farr, A.L., Randall, R.J. 1951 Protein measurment with the Folin phenol reagent, J. Biol. Chem., 193-265.