BAB II
TINJAUAN PUSTAKA
2.1 Penyakit Kusta (Morbus Hansen, Lepra)
Penyakit kusta adalah penyakit kronis yang disebabkan oleh infeksi
Mycobacterium leprae (M. leprae) yang pertama menyerang saraf tepi, selanjutnya dapat menyerang kulit, mukosa mulut, saluran napas bagian
atas, sistem retikuloendotelial, mata, otot, tulang dan testis kecuali susunan
saraf pusat. Pada kebanyakan orang yang terinfeksi dapat asimtomatik,
namun sebagian kecil memperlihatkan gejala dan mempunyai
kecenderungan untuk menjadi cacat, khususnya pada tangan dan kaki.
2.2 Epidemiologi
1-4
Sampai saat ini epidemiologi penyakit kusta belum sepenuhnya
diketahui secara pasti. Penyakit kusta tersebar di seluruh dunia terutama di
daerah tropis dan subtropis. Dapat menyerang semua umur, frekwensi
tertinggi pada kelompok umur antara 30-50 tahun dan lebih sering mengenai
laki-laki daripada wanita.
Menurut WHO (2002), diantara 122 negara yang endemik pada
tahun 1985 dijumpai 107 negara telah mencapai target eliminasi kusta
dibawah 1 per 10.000 penduduk pada tahun 2000. Pada tahun 2006 WHO
mencatat masih ada 15 negara yang melaporkan 1000 atau lebih penderita
baru selama tahun 2006. Lima belas negara ini mempunyai kontribusi 94%
dari seluruh penderita baru didunia. Indonesia menempati urutan prevalensi
ketiga setelah India, dan Brazil.
Di Indonesia penderita kusta terdapat hampir pada seluruh propinsi
dengan pola penyebaran yang tidak merata. Meskipun pada pertengahan
tahun 2000 Indonesia secara nasional sudah mencapai eliminasi kusta
namun pada tahun tahun 2002 sampai dengan tahun 2006 terjadi
peningkatan penderita kusta baru. Pada tahun 2006 jumlah penderita kusta
baru di Indonesia sebanyak 17.921 orang. Propinsi terbanyak melaporkan
penderita kusta baru adalah Maluku, Papua, Sulawesi Utara dan Sulawesi
Selatan dengan prevalensi lebih besar dari 20 per 100.000 penduduk.
2,7
2
Pada
tahun 2010, tercatat 17.012 kasus baru kusta di Indonesia dengan angka
prevalensi 7,22 per 100.000 penduduk sedangkan pada tahun 2011, tercatat
19.371 kasus baru kusta di Indonesia dengan angka prevalensi 8,03 per
100.000 penduduk.
2.3 Etiologi
6,16
Kuman penyebab penyakit kusta adalah M. leprae yang ditemukan
oleh GH Armauer Hansen, seorang sarjana dari Norwegia pada tahun 1873.
Kuman ini bersifat tahan asam, berbentuk batang dengan ukuran 1-8 mikron
dan lebar 0,2 - 0,5 mikron, biasanya berkelompok dan ada yang tersebar
satu-satu, hidup dalam sel terutama jaringan yang bersuhu dingin dan tidak
dapat dikultur dalam media buatan. Kuman ini juga dapat menyebabkan
Secara skematik struktur M. leprae terdiri dari :
A. Kapsul
1,17
Di sekeliling organisme terdapat suatu zona transparan elektron
dari bahan berbusa atau vesikular, yang diproduksi dan secara struktur
khas bentuk M. leprae . Zona transparan ini terdiri dari dua lipid,
phthioceroldimycoserosate, yang dianggap memegang peranan
protektif pasif, dan suatu phenolic glycolipid, yang terdiri dari tiga
molekul gula hasil metilasi yang dihubungkan melalui molekul fenol
pada lemak (phthiocerol). Trisakarida memberikan sifat kimia yang
unik dan sifat antigenik yang spesifik terhadap M. leprae
B. Dinding sel
Dinding sel terdiri dari dua lapis, yaitu:
a. Lapisan luar bersifat transparan elektron dan mengandung
lipopolisakarida yang terdiri dari rantai cabang arabinogalactan
yang diesterifikasi dengan rantai panjang asam mikolat , mirip
dengan yang ditemukan pada Mycobacteria lainnya.
b. Dinding dalam terdiri dari peptidoglycan: karbohidrat yang
dihubungkan melalui peptida-peptida yang memiliki rangkaian
asam-amino yang mungkin spesifik untuk M. leprae walaupun
peptida ini terlalu sedikit untuk digunakan sebagai antigen
C. Membran
Tepat di bawah dinding sel, dan melekat padanya, adalah suatu
membran yang khusus untuk transport molekul-molekul kedalam dan
keluar organisme. Membran terdiri dari lipid dan protein. Protein
sebagian besar berupa enzim dan secara teori merupakan target yang
baik untuk kemoterapi. Protein ini juga dapat membentuk ‘antigen
protein permukaan’ yang diekstraksi dari dinding sel M. leprae yang
sudah terganggu dan dianalisa secara luas.
D. Sitoplasma
Bagian dalam sel mengandung granul-granul penyimpanan,
material genetik asam deoksiribonukleat (DNA), dan ribosom yang
merupakan protein yang penting dalam translasi dan multiplikasi.
Analisis DNA berguna dalam mengkonfirmasi identitas sebagai
M. leprae dari mycobacteria yang diisolasi dari armadillo liar, dan
menunjukkan bahwa M. leprae, walaupun berbeda secara genetik,
terkait erat dengan M. tuberculosis dan M. scrofulaceum.
2.4 Diagnosis
Untuk menetapkan diagnosis penyakit kusta perlu dicari tanda-tanda
utama atau tanda kardinal, yaitu:
1,2,7,18,19
A. Lesi (kelainan) kulit yang mati rasa.
Kelainan kulit/lesi yang dapat berbentuk bercak keputihan
(hypopigmentasi) atau kemerahan (erithematous) yang mati rasa
B. Penebalan saraf tepi yang disertai dengan gangguan fungsi saraf.
Gangguan fungsi saraf tepi ini biasanya akibat dari peradangan
kronis pada saraf tepi (neuritis perifer). Adapun gangguan-gangguan
fungsi saraf tepi berupa:
a. Gangguan fungsi sensoris: mati rasa.
b. Gangguan fungsi motoris: kelemahan otot (parese) atau kelumpuhan
(paralise).
c. Gangguan fungsi otonom: kulit kering.
C. Ditemukannya M. leprae pada pemeriksaan bakteriologis.
2.5 Klasifikasi
Setelah seseorang didiagnosis menderita kusta, maka untuk tahap
selanjutnya harus ditetapkan tipe atau klasifikasinya. Penyakit kusta dapat
diklasifikasikan berdasarkan manifestasi klinis (jumlah lesi, jumlah saraf
yang terganggu), hasil pemeriksaan bakteriologi, pemeriksaan histopatologi
dan pemeriksaan imunologi.
Klasifikasi bertujuan untuk:
2,4,19,20
A. Menentukan rejimen pengobatan, prognosis dan komplikasi.
4
B. Perencanaan operasional, seperti menemukan pasien-pasien yang
menularkan dan memiliki nilai epidemiologi yang tinggi sebagai target
utama pengobatan.
Terdapat banyak jenis klasifikasi penyakit kusta diantaranya adalah
klasifikasi Madrid, klasifikasi Ridley-Jopling, klasifikasi India dan
klasifikasi menurut WHO.
A. Klasifikasi Internasional: klasifikasi Madrid (1953)
1,2,7,19,21
Pada klasifikasi ini penyakit kusta dibagi atas
Indeterminate (I), Tuberculoid (T), Borderline-Dimorphous (B),
Lepromatous (L). Klasifikasi ini merupakan klasifikasi paling
sederhana berdasarkan manifestasi klinis, pemeriksaan bakteriologis,
dan pemeriksaan histopatologi, sesuai rekomendasi dari International
Leprosy Association di Madrid tahun 1953.1,2,7,19
B. Klasifikasi Ridley-Jopling (1966)
Pada klasifikasi ini penyakit kusta adalah suatu spektrum klinis
mulai dari daya kekebalan tubuhnya rendah pada suatu sisi sampai
mereka yang memiliki kekebalan yang tinggi terhadap M.leprae di sisi
yang lainnya. Kekebalan seluler (cell mediated imunity = CMI)
seseorang yang akan menentukan apakah dia akan menderita kusta
apabila individu tersebut mendapat infeksi M.leprae dan tipe kusta yang
akan dideritanya pada spektrum penyakit kusta. Sistem klasifikasi ini
banyak digunakan pada penelitian penyakit kusta, karena bisa
menjelaskan hubungan antara interaksi kuman dengan respon
imunologi seseorang, terutama respon imun seluler spesifik.
Kelima tipe kusta menurut Ridley-Jopling adalah tipe
Lepromatous (LL), tipe Borderline Lepromatous (BL), tipe Mid
Borderline (BB), tipe Borderline Tuberculoid (BT), dan tipe
Tuberculoid (T).
C. Klasfikasi menurut WHO
1,2,7,19,22-24
Pada tahun 1982, WHO mengembangkan klasifikasi untuk
memudahkan pengobatan di lapangan. Dalam klasifikasi ini seluruh
penderita kusta hanya dibagi menjadi 2 tipe yaitu tipe Pausibasiler (PB)
dan tipe Multibasiler (MB). Sampai saat ini Departemen Kesehatan
Indonesia menerapkan klasifikasi menurut WHO sebagai pedoman
pengobatan penderita kusta. Dasar dari klasifikasi ini berdasarkan
manifestasi klinis dan hasil pemeriksaan bakteriologi.
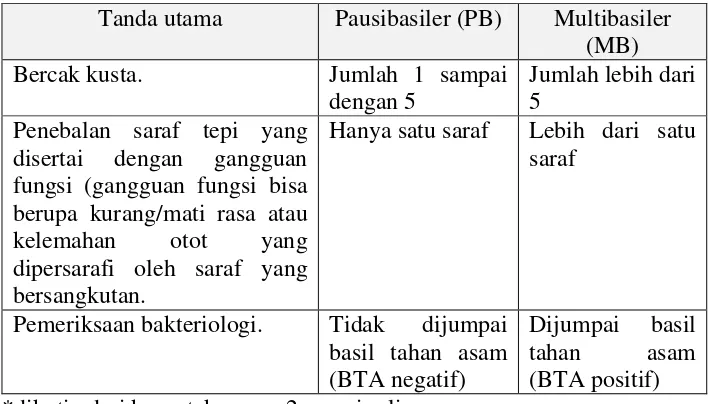
Tabel 1. Pedoman utama dalam menentukan klasifikasi / tipe penyakit kusta menurut WHO (1982)*
2,24-26
Tanda utama Pausibasiler (PB) Multibasiler (MB)
Bercak kusta. Jumlah 1 sampai
dengan 5
Jumlah lebih dari 5
Penebalan saraf tepi yang disertai dengan gangguan fungsi (gangguan fungsi bisa berupa kurang/mati rasa atau kelemahan otot yang dipersarafi oleh saraf yang bersangkutan.
Hanya satu saraf Lebih dari satu saraf
Pemeriksaan bakteriologi. Tidak dijumpai basil tahan asam (BTA negatif)
Dijumpai basil tahan asam (BTA positif)
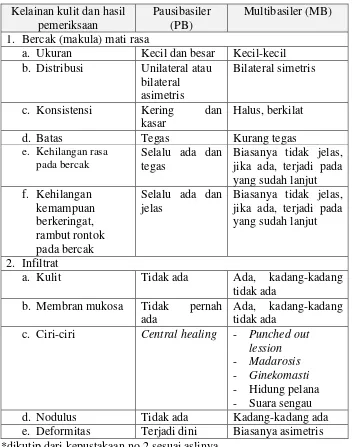
Tabel 2. Tanda lain yang dapat dipertimbangkan dalam penentuan klasifikasi menurut WHO (1982) pada penderita kusta*
Kelainan kulit dan hasil pemeriksaan
Pausibasiler (PB)
Multibasiler (MB)
1. Bercak (makula) mati rasa
a. Ukuran Kecil dan besar Kecil-kecil b. Distribusi Unilateral atau
bilateral asimetris
Bilateral simetris
c. Konsistensi Kering dan
kasar
Halus, berkilat
d. Batas Tegas Kurang tegas
e. Kehilangan rasa pada bercak
Selalu ada dan tegas
Biasanya tidak jelas, jika ada, terjadi pada yang sudah lanjut f. Kehilangan
kemampuan berkeringat, rambut rontok pada bercak
Selalu ada dan jelas
Biasanya tidak jelas, jika ada, terjadi pada yang sudah lanjut
2. Infiltrat
a. Kulit Tidak ada Ada, kadang-kadang
tidak ada b. Membran mukosa Tidak pernah
ada
Ada, kadang-kadang tidak ada
c. Ciri-ciri Centralhealing - Punched out lession - Madarosis - Ginekomasti - Hidung pelana - Suara sengau d. Nodulus Tidak ada Kadang-kadang ada e. Deformitas Terjadi dini Biasanya asimetris *dikutip dari kepustakaan no.2 sesuai aslinya
2.6 Antigen M. leprae
Unsur kimia utama dari M. leprae bersifat antigenik, tetapi M. leprae
mengandung antigen yang relatif sedikit (sekitar 20) yang dikenali antibodi
di dalam serum pasien penderita lepra dibandingkan dengan BCG (sekitar
1981, saat Brennan melaporkan phenolic glikolipid dan menunjukkan
bahwa phenolic glikolipid bersifat spesifik pada M. leprae, semua antigen
yang diidentifikasi sampai sejauh ini umumnya bereaksi-silang dengan
Mycobacteria lainnya, walaupun ada sebagian kecil molekul, suatu epitope,
yang spesifik pada M. leprae. Spesifisitas epitope memungkinkan tes
antibodi spesifik bisa ditetapkan dengan menggunakan serum yang telah
diabsorbsi dengan spesies Mycobacteria lainnya.
Antigenisitas dari M. leprae didominasi oleh antigen yang
mengandung karbohidrat, yang stabil secara fisik-kimia.
1,16
A. Phenolic Glicolipid (PGL)
1
Terdapat varian-varian kecil pada struktur ditandai dengan I, II
dan III. PGL-1 mengandung suatu kelompok glikosilasi fenol dengan
karakteristik trisakarida yang hanya dijumpai pada M.leprae. PGL-1
berbeda dengan PGL-2 dan PGL-3 dalam pola residu gula. Trisakarida
terminal pada PGL-1 memberikan spesifisitas antigenik pada M.leprae.
Trisakarida ini telah berhasil disintesis dan dapat berikatan dengan
sample carrier protein yang digunakan pada seroepidemiologik pada
beberapa penelitian.
Antigen PGL-1 dapat menstimulasi produksi antibodi IgM.
Antigen ini ditemukan pada semua jaringan yang terinfeksi dengan
M. leprae dan tetap bertahan dalam waktu yang lama bahkan setelah
organisme mati. Individu dengan indeks bakteri yang tinggi umumnya
menunjukkan titer antibodi IgM anti PGL-1 yang tinggi.
Kecenderungan kadar antibodi IgM anti PGL-1 yang rendah untuk tetap
positif mungkin berhubungan dengan persistensi basiler. Antigen
PGL-1 itu sendiri tidak larut dalam air dan dapat menetap di jaringan
dalam jangka waktu yang lama, menstimulasi respon antibodi yang
rendah tanpa adanya basil yang hidup. Respon antibodi anti PGL-1
terutama pada kelas IgM mengindikasikan bahwa sifat IgM tidak
tergantung oleh respon sel T terhadap antigen glikolipid ini, berbeda
dengan respon IgG yang predominan terhadap antigen karbohidrat
utama lipoarabinomannan (LAM).1,16,28-31
B. Lipoarabinomannan (LAM)
Ini merupakan komponen utama dari dinding sel M. leprae;
komponen ini stabil dan tidak bisa dicerna. Komponen ini
bereaksi-silang dengan Mycobacteria lainnya, tetapi mengandung epitope
spesifik yang dikenali oleh serum yang terabsorbsi, dan memicu
antibodi IgG.
C. Antigen protein
1,16
Ada banyak antigen protein pada M. leprae, di mana lima di
antaranya sangat menarik perhatian karena antibodi monoklonal tikus
menunjukkan bahwa antigen protein ini mengandung epitope spesifik
M. leprae. Protein yang bisa larut yang diekstraksi dari M. leprae
terbukti berguna meskipun bukan merupakan antigen yang sangat
dan diekspresikan pada E. coli, yang sangat membantu dalam analisa
antigen tersebut.
2.7 Imunologi Kusta 1,16
Respon imun pada penyakit kusta sangat kompleks, dimana
melibatkan respon imun seluler dan humoral. Sebagian besar gejala dan
komplikasi penyakit ini disebabkan oleh reaksi imunologi terhadap antigen
yang dimiliki oleh M. leprae. Jika respon imun yang terjadi setelah infeksi
cukup baik, maka multiplikasi bakteri dapat dihambat pada stadium awal
sehingga dapat mencegah perkembangan tanda dan gejala klinis
selanjutnya.
M. leprae merupakan bakteri obligat intraseluler, maka respon imun
yang berperan penting dalam ketahanan tubuh terhadap infeksi adalah
respon imun seluler. Respon imun seluler merupakan hasil dari aktivasi
makrofag dengan meningkatkan kemampuannya dalam menekan
multiplikasi atau menghancurkan bakteri.
1,32
Respon imun humoral terhadap M. leprae merupakan aktivitas sel
limfosit B yang berada dalam jaringan limfosit dan aliran darah.
Rangsangan dari komponen antigen basil tersebut akan mengubah sel
limfosit B menjadi sel plasma yang akan menghasilkan antibodi yang akan
membantu proses opsonisasi. Namun pada penyakit kusta, fungsi respon
imun humoral ini tidak efektif, bahkan dapat menyebabkan timbulnya
beberapa reaksi kusta karena diproduksi secara berlebihan yang tampak
pada kusta lepromatosa.
1,32
2.8 Pemeriksaan Serologi
Tes serologi merupakan tes diagnostik penunjang yang paling
banyak dilakukan saat ini. Selain untuk penunjang diagnostik klinis
penyakit kusta, tes serologi juga dipergunakan untuk diagnosis infeksi
M. leprae sebelum timbul manifestasi klinis. Uji laboratorium ini diperlukan
untuk menentukan adanya antibodi spesifik terhadap M. leprae di dalam
darah. Dengan diagnosis yang tepat, apalagi jika dilakukan sebelum timbul
manifestasi klinis lepra diharapkan dapat mencegah penularan penyakit
sedini mungkin.
Pemeriksaan serologis kusta yang kini banyak dilakukan cukup
banyak manfaatnya, khususnya dalam segi seroepidemiologi kusta di daerah
endemik. Selain itu pemeriksaan ini dapat membantu diagnosis kusta pada
keadaan yang meragukan karena tanda-tanda klinis dan bakteriologis tidak
jelas. Karena yang diperiksa adalah antibodi spesifik terhadap basil kusta
maka bila ditemukan antibodi dalam titer yang cukup tinggi pada seseorang
maka patutlah dicurigai orang tersebut telah terinfeksi oleh M.leprae. Pada
kusta subklinis seseorang tampak sehat tanpa adanya penyakit kusta namun
di dalam darahnya ditemukan antibodi spesifik terhadap basil kusta dalam
kadar yang cukup tinggi.
33
Beberapa jenis pemeriksaan serologi kusta yang banyak digunakan,
antara lain:
A. Uji FLA-ABS (Fluorescent leprosy Antibodi-Absorption test)
Uji ini menggunakan antigen bakteri M. leprae secara utuh yang
telah dilabel dengan zat fluoresensi. Hasil uji ini memberikan
sensitivitas yang tinggi namun spesivisitasnya agak kurang karena
adanya reaksi silang dengan antigen dari mikrobakteri lain.
B. Radio Immunoassay (RIA)
34
Uji ini menggunakan antigen dari M. leprae yang dibiakkan
dalam tubuh Armadillo yang diberi label radio aktif.
C. Uji MLPA (Mycobacterium leprae particle agglutination)
34
Uji ini berdasarkan reaksi aglutinasi antara antigen sintetik
PGL-1 dengan antibodi dalam serum. Uji MLPA merupakan uji yang
praktis untuk dilakukan di lapangan, terutama untuk keperluan skrining
kasus seropositif.
D. Antibodi monoklonal (Mab) epitop MLO4 dari protein 35-kDa
M.leprae menggunakan M. leprae sonicate (MLS) yang spesifik dan
sensitif untuk serodiagnosis kusta. Protein 35-kDa M. leprae adalah
suatu target spesifik dan yang utama dari respon imun seluler terhadap
M. leprae, merangsang proliferasi sel T dan sekresi interferon gamma
pada pasien kusta dan kontak.
34
E. Uji ELISA (Enzyme Linked Immuno-Assay)
Uji ELISA pertama kali digunakan dalam bidang imunologi
untuk menganalisis interaksi antara antigen dan antibodi di dalam suatu
sampel, dimana interaksi tersebut ditandai dengan menggunakan suatu
enzim yang berfungsi sebagai penanda.35
Dalam perkembangan selanjutnya, selain digunakan sebagai uji
kualitatif untuk mengetahui keberadaan suatu antibodi atau antigen
dengan menggunakan antibodi atau antigen spesifik, teknik ELISA juga
dapat diaplikasikan dalam uji kuantitatif untuk mengukur kadar
antibodi atau antigen yang diuji dengan menggunakan alat bantu berupa
spektrofotometer.
Prinsip uji ELISA adalah mengukur banyaknya ikatan antigen
antibodi yang terbentuk dengan diberi label (biasanya berupa enzim)
pada ikatan tersebut, selanjutnya terjadi perubahan warna yang dapat
diukur dengan spektrofotometer dengan panjang gelombang tertentu.
Pemeriksaan ini umumnya menggunakan plat mikro untuk tempat
terjadinya reaksi.
35
Terdapat tiga metode ELISA, antara lain:
34-36
35
A. Direct ELISA
Pada direct ELISA, antigen melekat pada fase solid dan
bereaksi dengan antibodi sekunder yang dilabel enzim, kemudian
ditambahkan substrat sehingga terjadi perubahan warna yang dapat
B. Indirect ELISA
Pada indirect ELISA, antigen melekat pada fase solid dan
bereaksi dengan antibodi primer, kemudian dilakukan penambahan
antibodi sekunder yang dilabel enzim dan terjadi reaksi antara
antibodi primer dengan antibodi sekunder yang dilabel enzim,
kemudian ditambahkan substrat sehingga terjadi perubahan warna
yang dapat diukur dengan spektrofotometer.
C. Sandwich ELISA.
Pada sandwich ELISA, prinsip kerjanya hampir sama dengan
direct ELISA, hanya saja pada sandwich ELISA, larutan antigen
yang diinginkan tidak perlu dipurifikasi.
Dalam bidang penyakit kusta, uji ELISA dapat dipakai untuk
mengukur kadar antibodi terhadap basil kusta, misalnya antibodi anti
PGL-1, antibodi anti protein 35kD, dan lain-lain. Kelas antibodi yang
diperiksa juga ditentukan, misalnya IgM anti PGL-1, IgG anti PGL-1
dan sebagainya. Untuk antibodi anti PGL-1 biasanya IgM lebih
dominan dibandingkan IgG. Pemeriksaan ELISA dikembangkan
menggunakan reagen poliklonal atau monoklonal yang telah terbukti
sangat spesifisik terhadap residu gula dari PGL-1 dan memungkinkan
deteksi titer anti PGL-1 pada pasien kusta atau kontak serumah. Untuk
menentukan nilai ambang (cut off) dari hasil uji ELISA ini, biasanya
yang tidak sakit kusta. Di daerah Jawa Timur, nilai ambang untuk
antibodi IgM anti PGL-1 telah diketahui sekitar 605 μ/ml.
Pada penelitian ini akan menggunakan metode indirect ELISA
untuk mengukur kadar antibodi IgM anti PGL-1 pada penderita kusta.
Salah satu keuntungan dari uji ELISA adalah sensitif karena dapat
mendeteksi dari level 0,01 μg/ml.
34,35
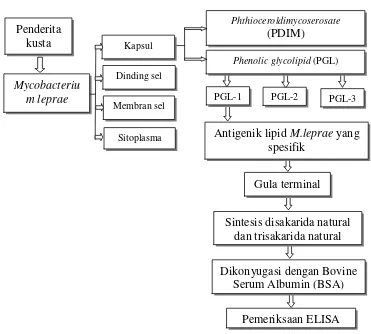
2.9 Kerangka Teori
35
Gambar 1. Diagram kerangka teori penelitian Penderita
kusta
Mycobacteriu m leprae
Kapsul
Dinding sel
Membran sel
Sitoplasma
Phthioceroldimycoserosate
(PDIM)
Phenolic glycolipid (PGL)
PGL-1
Antigenik lipid M.leprae yang spesifik
Gula terminal
Sintesis disakarida natural dan trisakarida natural
Pemeriksaan ELISA Dikonyugasi dengan Bovine
Serum Albumin (BSA)
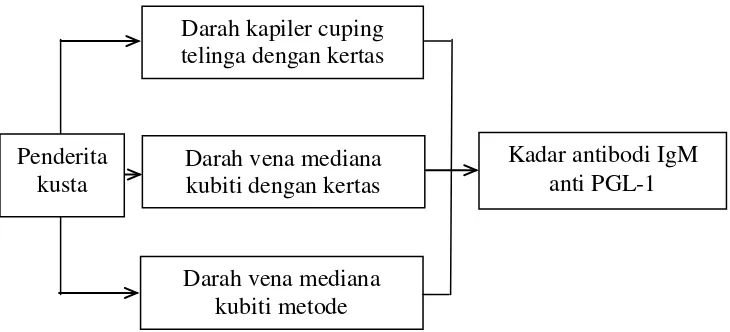
2.10 Kerangka Konsep
Gambar 2. Diagram kerangka konsep penelitian Darah kapiler cuping
telinga dengan kertas
Darah vena mediana kubiti dengan kertas
Darah vena mediana kubiti metode
Kadar antibodi IgM anti PGL-1 Penderita