RESIDU ANTIBIOTIKA SPIRAMISIN PADA HATI DAN
DAGING AYAM PEDAGING YANG DICEKOK
ANTIBIOTIKA SPIRAMISIN
(Spiramycin Residue in Muscle and Liver of Chicken
Received Spiramycin Antibiotic Administered Orally)
RAPHAELLA WIDIASTUTI danT.B.MURDIATI
Balai Besar Penelitian Veteriner, Jl. R.E. Martadinata 30, Bogor 16114
ABSTRACT
Spiramycin, one of macrolides antibiotic is widely used in veterinary medicine to treat respiratory diseases or as feed additives to promote growth. However uncontrolled usage and/or slaughtered the animal before the recommended withdrawal period may cause the presence of residue in animal products. The aim of this research was to study the distribution of spiramycin residue in meat and liver of 6 weeks chicks that were orally treated with 1 g/l spiramycin for 7 consecutive days. The spiramycin residue in meat and liver samples were extracted chemically and analysed by a high performance liquid chromatography (HPLC). Spiramycin residue in meat disappeared rapidly and remained only for one day post withdrawn. On the other hand the occurrence of spiramycin residue in liver tissue was higher than in meat and remained more than 7 days post withdrawn.
Key Words: Spiramycin, Residue, Broiler Chicken, Meat, Liver
ABSTRAK
Spiramisin adalah salah satu antibiotika golongan makrolida yang banyak digunakan di bidang peternakan untuk pengobatan penyakit saluran pernafasan atau sebagai imbuhan untuk pemacu pertumbuhan. Namun penggunaan obat hewan yang melebihi dosis yang ditentukan dan/atau saat pemotongan yang tidak memperhatikan waktu hentinya akan menimbulkan residu pada produk ternak. Tujuan dari penelitian ini adalah untuk mengetahui distribusi terbentuknya residu spiramisin pada organ hati dan daging (otot) dari ayam pedaging usia 6 minggu yang dicekok dengan 1 g/l spiramisin selama 7 hari berturut-turut. Residu spiramisin dari sampel organ hati dan daging yang telah diekstraksi kemudian dianalisis dengan kromatografi cair kinerja tinggi (KCKT). Residu spiramisin yang terbentuk dalam daging (otot) sangat cepat menghilang dan sehari pascapenghentian pencekokan residu sudah tidak terdeteksi lagi. Sebaliknya, konsentrasi residu pada organ hati terdeteksi lebih tinggi dan mampu bertahan lebih dari 7 hari pascapenghentian dibandingkan dengan residu pada daging ayam.
Kata Kunci: Spiramisin, Residu, Ayam Pedaging, Daging, Hati
PENDAHULUAN
Spiramisin merupakan salah satu antibiotika dari golongan makrolida yang diisolasi dari bakteri Streptomyces. Spiramisin banyak digunakan di bidang veteriner untuk tujuan pengobatan penyakit pernafasan maupun sebagai imbuhan pakan untuk pemacu pertumbuhan. Spiramisin terserap secara baik setelah pemberian secara oral dan terdistribusi ke paru-paru, jaringan, serta organ hati dan ginjal (DUBOIS et al., 2001). Mekanisme kerja
antimikroba sebagai imbuhan pakan dalam tubuh ternak masih belum diketahui secara tepat, namun pada umumnya melawan bakteri Gram positif dalam usus (BARTON, 2000) dengan cara menghambat sintesa protein (ANADON dan MARTINEZ-LARRANAGA, 1999).
Dampak negatif dari pemakaian antibiotik secara luas yang tidak terkontrol dalam dunia peternakan adalah timbulnya residu yang dapat menyebabkan penurunan populasi mikroflora yang diperlukan oleh manusia dan resistensi terhadap antibiotika (BARTON, 2000). Sebab
itu negara-negara yang tergabung pada Uni Eropa (European Union) sejak tahun 1999 melarang penggunaaan spiramisin di samping tiga antiobitika lainnya (zink basitrasin, tilosin, virginiamisin) sebagai imbuhan pakan (CASEWELL et al., 2003).
FAO/WHO (2010) menetapkan batas maksimum residu (BMR) spiramisin pada produk ternak asal ayam sebesar 0,6 ppm (600 µg/kg) (hati), 0,3 ppm (300 µg/kg) (lemak) dan 0,2 ppm (200 µg/kg) (daging). Nilai BMR tersebut diperhitungkan sebagai penjumlahan konsentrasi spiramisin dan neospiramisin untuk residu dalam daging sapi dan ayam. Adapun BMR yang diizinkan di Indonesia adalah 0,2 ppm (200 µg/kg) (DEWAN STANDARISASI NASIONAL, 2000).
Hasil penelitian di Indonesia mengenai keberadaan residu spiramisin telah dilaporkan YUNINGSIH dan MURDIATI (2003) pada penelitian terhadap 36 sampel daging ayam pedaging yang berasal dari pasar tradisional di Kabupaten Sukabumi, Bogor dan Tangerang. Hasil penelitian tersebut memperlihatkan bahwa spiramisin hingga saat itu masih digunakan di Indonesia, yaitu 36 sampel (97%) diantaranya positif terdeteksi residu spiramisin dengan kisaran 31 hingga 610 µg/kg, bahkan 5 di antaranya sudah melebihi batas maksimum residu (BMR) yang diizinkan di Indonesia.
Penelitian ini bertujuan untuk mempelajari distribusi terbentuknya residu spiramisin pada daging dan hati ayam pedaging akibat penggunaan spiramisin dengan dosis yang berlebihan dan waktu yang lama. Penggunaan dosis 1 g/l (1000 ppm) berdasarkan hasil penelitian awal dengan dosis rekomendasi 0,4 g/l memperlihatkan tidak adanya residu yang terdeteksi baik pada hati maupun daging, sehingga pengamatan terhadap distribusi residu sebagaimana yang diharapkan tidak dapat diamati, sedangkan metode analisis residu spiramisin diadopsi dari metode yang dikembangkan NAGATA dan SAEKI (1986) dan dideteksi secara kromatografi cair kinerja tinggi (KCKT).
MATERI DAN METODE Pembuatan larutan cekokan spiramisin
Larutan cekok spiramisin dengan konsentrasi 1 g/l (1000 ppm) spiramisin dibuat
dengan melarutkan 5 g Suanovil (PT Rhône Poulenc, Indonesia) yang mengandung 20% spiramisin dengan 1 l akuades.
Penyiapan sampel
Pada penelitian ini digunakan 50 ekor ayam pedaging (galur Shaver Starbro, PT Cargill) berumur 6 minggu dengan berat badan sekitar 1 – 1,2 kg yang dipelihara secara liter dan dibagi dalam 2 kelompok yaitu kelompok A (perlakuan) yang terdiri atas 36 ekor (3 ekor diantaranya untuk cadangan) yang dicekok dengan 1 ml larutan spiramisin dengan dosis 1 g/l selama 7 hari berturut-turut dan kelompok B (kontrol negatif) sebanyak 15 ekor (4 ekor diantaranya untuk cadangan) yang tidak diberi cekokan. Ayam yang telah dicekok dengan spiramisin selama 7 hari berturut-turut kemudian diterminasi sesaat setelah pencekokan terakhir (0 jam), dan selanjutnya pada jam ke-12, 24, 36, 48, 60, 72, 96, 120, 144 dan 168 setelah pemberian terakhir spiramisin untuk dilakukan koleksi terhadap daging (otot) dan organ hati dan disimpan pada suhu -45°C sampai waktu analisis.
Setiap kali pemotongan diambil sebanyak masing-masing 3 ekor ayam perlakuan untuk dikoleksi daging (otot) paha dan dada serta hati. Pada saat yang bersamaan juga dilakukan pemotongan terhadap 1 ekor ayam hewan kontrol (cukup digunakan 1 ekor saja untuk penghematan bahan kimia dengan asumsi bahwa semua hewan kontrol tidak mengandung residu spiramisin karena pakan yang digunakan tidak mengandung antibiotika spiramisin).
Analisis residu spiramisin dalam daging dan hati
Analisis residu spiramisin dilakukan dengan mengeskstraksi terlebih dulu 10 g sampel hati maupun daging (otot) yang telah dihomogenkan dan dimasukkan ke dalam erlenmeyer 250 ml dan ditambahkan sebanyak 60 ml asetonitril ke dalamnya dan kemudian dikocok dengan shaker selama 1 jam. Ekstrak asetonitil disaring dan dikeringkan pada suhu 45C, kemudian ditambah dengan 20 ml bufer fosfat (pH 6), dan selanjutnya dicuci dengan 20 ml heksana sebanyak 3 kali dan fasa heksana
dibuang. Fasa bufer fosfat yang tertinggal diulangi untuk diekstraksi sebanyak 3 kali dengan 20 ml kloroform yang akhirnya dikeringkan dengan rotavapor pada suhu 45°C. Kemudian ekstrak kering dilarutkan dengan 200 µl campuran asetonitril dan 0,1 M natrium dihidrogen fosfat (23 : 77) dan selanjutnya diidentifikasi dan dianalisis terhadap residu spiramisin dengan menyuntikkan 20 µl sampel ke dalam alat KCKT Waters 501 HPLC Pump (Waters, Milford, USA) dengan kolom µ-Bondapak C18 (Waters, Milford, USA) dan fasa gerak yang terdiri atas campuran asetonitril dan 0,1 M natrium dihidrogen fosfat (23 : 77) dengan kecepatan alir 1,0 ml/menit dan detektor UV pada panjang gelombang 231 nm.
Sampel diidentifikasi dengan
membandingkan luas puncak sampel terhadap luas puncak dari standar yang digunakan pada waktu retensi yang sama. Standar spiramisin disiapkan dengan membuat larutan standar 1000 ppm spiramisin dengan cara melarutkan 10 mg spiramisin (Sigma Aldrich, USA) ke dalam 10 ml metanol HPLC grade, dan selanjutnya dijadikan larutan standar kerja dengan konsentrasi 10 dan 20 ppm spiramisin.
HASIL DAN PEMBAHASAN
Sebelum dilakukan analisis residu terhadap sampel daging dan hati, tahap awal dari penelitian ini adalah melakukan pengembangan metode terhadap analisis residu spiramisin. Perubahan yang dilakukan dibandingkan dengan metode asli yang digunakan adalah perubahan fasa gerak dari campuran metanol dan 0,04% asam fosfat (v/v 70 : 30) menjadi campuran asetonitril dan 0,1 M natrium dihidrogen fosfat (v/v 23 : 77) dengan pertimbangan bahwa kelarutan spiramisin lebih baik dalam asetonitril dibandingkan dengan metanol dan perubahan keasaman menjadi lebih lemah (pH 4) dengan mengganti asam fosfat menjadi natrium dihidrogen fosfat karena sifat spiramisin yang tidak stabil terhadap asam dan basa.
Hasil validasi metode di atas yang diperlihatkan dari hasil uji perolehan kembali untuk pengembangan metode ini dengan cara penambahan 0,5 ppm dan 2 ppm spiramisin pada sampel blanko adalah 83,4% (penambahan 0,5 ppm spiramisin) dan 90,3% (penambahan 2
ppm spiramisin). Hasil uji perolehan kembali mengartikan bahwa metode ini cukup baik untuk diaplikasikan pada sampel yang akan dianalisis, Sedangkan deteksi limit terhadap spiramisin pada metode ini adalah 0,1 ppm, sehingga kadar residu lebih kecil dari 0,1 ppm akan dinyatakan sebagai tidak terdeteksi (tt).
Residu dalam tubuh ternak terbentuk akibat pemberian dengan dosis berlebihan atau ternak diterminasi sebelum melewati masa henti (withdrawal time). Spiramisin yang diberikan pada unggas akan terdeteksi sebagai residu spiramisin dan neospiramisin (FAO, 1991) yang merupakan hasil hidrolisisnya pada daging, hati maupun ginjal. Namun pada penelitian ini residu yang dideteksi hanya spiriamisin disebabkan tidak tersedianya standar neospiramisin.
Hasil analisis residu spiramisin pada organ hati dan daging dari ayam kelompok A yang dicekok 1g/l (1000 ppm) selama 7 hari berturut- turut dapat dilihat pada Tabel 1. Sedangkan residu pada hewan kelompok B tidak terdeteksi adanya spiramisin (data tidak ditampilkan).
Residu spiramisin yang berada dalam daging sangat cepat menghilang. Konsentrasi sesaat (0 jam) setelah pemberian dosis terakhir yaitu sebesar 0,41 ppm, selanjutnya 12 jam kemudian meningkat menjadi 1,17 ppm. Namun sehari pascapenghentian pencekokan residu spiramisin sudah tidak terdeteksi lagi, sedangkan residu pada organ hati memperlihatkan bahwa konsentrasi 24 jam pasca penghentian besarnya residu masih cukup rendah, yaitu 0,30 ppm, selanjutnya meningkat dan mencapai puncaknya hingga 134,36 ppm pada jam ke-60 setelah penghentian pemberian spiramisin, kemudian turun menjadi 2,27 ppm pada 168 jam (hari ke-7) setelah pemberian terakhir, namun konsentrasi pada saat itu belum berada di bawah BMR yang ditetapkan FAO/WHO (2010) yaitu sebesar 0,60 ppm. Residu yang ditemukan pada organ hati lebih tinggi dan bertahan lebih lama melebihi 7 hari pascapenghentian dibandingkan keberadaannya pada daging. Penelitian sejenis yang dilakukan oleh BOSC et al. (1993) dengan dosis 0,8 g/l (800 ppm) selama 3 hari dan dilakukan pengamatan konsentrasi residu pada 5 hari pascapemberian juga menunjukkan bahwa residu spiramisin tidak terdeteksi pada daging maupun kulit, namun terlihat lebih tinggi pada hati dibandingkan dengan ginjal.
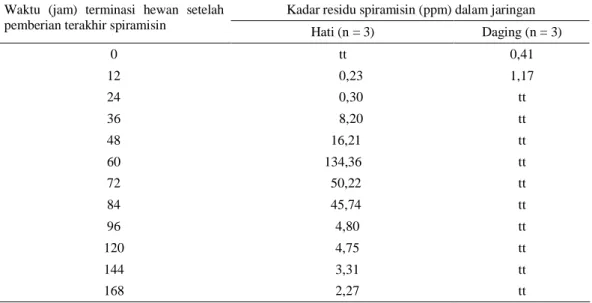
Tabel 1. Kadar residu spiramisin dalam daging ayam dan hati yang mendapat cekokan 1 g/l (1000 ppm) spiramisin (kelompok A) selama 7 hari berturut-turut
Kadar residu spiramisin (ppm) dalam jaringan Waktu (jam) terminasi hewan setelah
pemberian terakhir spiramisin
Hati (n = 3) Daging (n = 3) 0 tt 0,41 12 0,23 1,17 24 0,30 tt 36 8,20 tt 48 16,21 tt 60 134,36 tt 72 50,22 tt 84 45,74 tt 96 4,80 tt 120 4,75 tt 144 3,31 tt 168 2,27 tt
nilai rata-rata diperoleh dari rata-rata 3 sampel per waktu koleksi; tt: tidak terdeteksi Konsentrasi residu yang tinggi pada hati
berkaitan dengan fungsi hati sebagai alat biotransformasi.
Hasil penelitan di atas dapat diartikan bahwa untuk mengkonsumsi organ hati hendaknya harus berhati-hati karena eliminasi residu spiramsin hingga tercapai di bawah BMR yang diizinkan (0,60 ppm) membutuhkan waktu yang cukup panjang dan penelitian mengenai waktu henti (withdrawal time) ini seharusnya menggunakan minimal 6 ekor ayam per terminasi sebagaimana yang disarankan oleh Commission of the European Communities pada tahun 1991 (ANADON dan MARTINEZ-LARRANAGA, 1999) dengan dosis pemberian yang tepat. Dosis 1 g/l (1000 ppm) spiramisin yang digunakan dalam penelitian ini serta pemberian selama 7 hari berturut-turut merupakan dosis yang berlebihan jika dibandingkan dengan dosis rekomendasi Suanovil yaitu 2 g/l (mengandung 20% spiramisin) yang setara dengan 0,4 g/l (400 ppm) selama 3 hari berturut-turut.
KESIMPULAN
Residu spiramisin yang terbentuk pada daging (otot) dan hati ayam pedaging yang dicekok dengan 1 g/l (1000 ppm) spiramisin selama 7 hari berturut-turut memperlihatkan
pola yang berbeda. Residu spiramisin dalam daging (otot) sangat cepat menghilang dan sehari pascapenghentian pencekokan residu spiramisin sudah tidak terdeteksi lagi. Residu pada organ hati pada 24 jam pascapenghentian besarnya masih cukup rendah dan meningkat hingga mencapai puncaknya pada jam ke-60 jam setelah penghentian pemberian spiramisin, kemudian konsentrasi pada jam ke-72 mulai menunjukkan penurunan. Namun pada akhir penelitian (168 jam) pascapenghentian pencekokan belum tercapai konsentrasi di bawah BMR, sehingga sebaiknya penelitian ini dilanjutkan hingga tercapai konsentrasi yang aman untuk dikonsumsi dengan menggunakan jumlah hewan coba yang tepat. Selain residu spiramisin yang terbentuk, perlu juga diketahui residu neospiramisin yang terbentuk untuk mengetahui total residu spiramisin yang sesungguhnya.
DAFTAR PUSTAKA
ANADON, A. and M.R. MARTINEZ-LARRANAGA, 1999. Residual of microbial drugs and feed additives in animal products: regulatory aspects. Livestock Prod. Sci. 59: 183 – 198. BARTON,M.D. 2000. Antibiotic Use in Animal Feed
and its Impact on Human Health. Nutr. Res. Rev. 13: 279 – 299.
BOSC,F.,J.F.CAMPAGNA,A.M.HUET and A. WEIL. 1993. Determination of Spiramycin and Neospiramycin in Plasma and Tissue Samples of Chickens Following Administration of Suanovil 50 in the Drinking Water at a Dose of 0,8 g/l for 3 Days. Rhône Mérieux (Protocol MET233P). Rhône Mérieux Report No. MET233, June 1993.
CASEWELL,M.,C.FRIIS,E.MARCO,P.MCMULLIN
and PHILLIPS. 2003. The European ban on growth-promoting antibiotics and emerging consenquenses for human and animal health. J. Antimicrob. Chemother. 52: 159 – 161. DEWAN STANDARISASI NASIONAL. 2000. Batas
maksimum cemaran mikroba dan batas maksimum residu dalam bahan makanan asal hewan. No: 01-6366-2000.
DUBOIS, M., D. FLUCHARD, E. SIOR and PH. DELAHAUT. 2001. Identification and quantification of five macrolide antibiotics in several tissues, eggs and milk by liquid chromatography-electrospray tandem mass spectrometry. J. Chromatogr. B. 753: 189 – 202.
FAO. 1991. Residues of some veterinary drugs in animals and foods. FAO, Food and Nutrition Paper. 41/4. Monographs prepared by the Thirty-eighth Meeting of the Joint FAO/WHO Expert Committee on Food Additives, Rome, 22 – 31 January 1991. p. 97 – 107.
FAO/WHO, 2010. Maximum residue limits for spiramycin. Updated up to 32nd session of the Codex Allimentarius Commision 2009. NAGATA,T and M.SAEKI. 1986. LC determination
of spiramycin residues in chicken tissues. J. Assoc. Off. Anal. Chem. 69: 644 – 646. YUNINGSIH dan T.B. MURDIATI. 2003. Analisis
residu antibiotika spiramisin dalam daging ayam secara khromatografi cair kinerja tinggi (KCKT). Prosiding Seminar Nasional Teknologi Peternakan dan Veteriner, Bogor. 29 – 30. September 2003. Puslitbangnak. hlm. 462 – 465.
DISKUSI
Pertanyaan:
1. Waktu apa ada pengaruh dengan distribusi terbentuknya residu?
2. Berapa batas toleransi, di daging bisa membantu pertumbuhan, tapi tidak ada residu di hati?
Jawaban:
1. Antibiotik mungkin bukan dari golongan makrolida, sehingga tidak tahu sifat-sifat antibiotik-antibiotik pengurainya. Spiramisin: antibiotik-antibiotik untuk imbuhan pakan untuk pemacu pertumbuhan dan pengobatan saluran napas. Jika terjadi residu akan menimbulkan masalah bagi manusia yang menggunakan antibiotik yang sama. Residu di hati bertahan lebih lama, namun di daging residu cepat menghilang.
2. Interval waktu: untuk praktis 0, 12, dst. Lebih dari hari ke-3 baru ke-4, 5, 6, dst. Cara pemberian lewat minum/cekok lewat selang.